Proteínas Fibrosas
Noções básicas - Proteínas
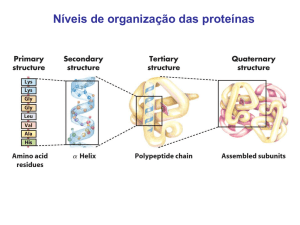
Existem várias estruturas diferentes de proteínas:
o Estrutura primária (num único plano)
o Estrutura Secundária (2 planos), sendo que os tipos
principais são a -hélice e a conformação
o Estrutura terciária, que corresponde ao enrolamento
tridimensional das estruturas primária e secundárias
o Estrutura quaternária, que corresponde ao arranjo
tridimensional de duas ou mais cadeias polipeptidicas, iguais ou diferentes entre
si.
Hélice
a) O esqueleto da cadeia polipeptidica forma uma estrutura helicoidal
com 3 a 6 resíduos em cada volta.
b) É estabilizada por ligações de hidrogénio entre cada 4 resíduos
(devido aos grupos CO e NH).
c) As cadeias laterais – R – possuem grupos funcionais que difere no
tamanho, forma, carga, etc e encontram-se viradas para fora.
d) Pode imaginar-se a cadeia como uma escada em caracol, na qual os
grupos R formam os degraus, sendo uma estrutura rígida em virtude da
planaridade das ligações.
Folha
a) Diferentes segmentos do esqueleto de uma cadeia polipeptidica, ou
de cadeias diferentes, encontram-se ligados por ligações de Hidrogénio, em que
participam todos os resíduos.
b) Forma-se uma estrutura planar onde as cadeias laterais se encontram
viradas para cima e para baixo, e nunca interagem umas com as outras.
c) Os segmentos podem estar orientados na mesma direcção (paralela)
ou em direcções opostas (anti-paralelas).
Dentro das estruturas mais complexas podem-se, ainda, apontar dois tipos
proteicos diferentes:
o Proteínas Globulares – cadeias polipeptidicas organizadas
de forma esférica ou globular.
o Proteínas Fibrosas – cadeias polipeptidicas organizadas
segundo longas lâminas.
Estes dois tipos proteicos
funcionalmente:
Nível Estrutural
Nível funcional
diferem
tanto estruturalmente
Proteínas fibrosas
Consistem num único
tipo
de
estrutura
secundária
Responsáveis
pelo
suporte, pela forma e
pela protecção externa
dos vertebrados.
como
Proteínas Globulares
Apresentam,
muitas
vezes, vários tipos de
estruturas secundárias
Várias
enzimas
e
proteínas reguladoras são
proteínas globulares
Proteínas Fibrosas
Funções gerais – As proteínas fibrosas desempenham um papel
importante no conhecimento da estrutura das proteínas assim como fornecem
exemplos claros da relação existente entre a sua estrutura e função.
- Estas proteínas apresentam propriedades responsáveis
pela força e flexibilidade das estruturas onde ocorrem.
Características gerais:
a) Todas as proteínas fibrosas são insolúveis em água,
característica esta devida à alta concentração de aminoácidos hidrofóbicas
existentes no interior e à superfície das proteínas.
b) Têm cadeias polipeptidicas organizadas segundo longas
lâminas.
c) A unidade estrutural fundamental consiste na repetição de um
elemento de estrutura secundária, podendo também apresentar estrutura terceária
ou quaternária.
d) A força conseguida pelas proteinas fibrosas deve-se à
existência de “cross-links” entre cadeias polipeptidicas e entre cadeias adjacentes
nos complexos supramoleculares.
Tipos Principais - -Queratina , colagénio e “silk fibroin”.
-Queratina
Função: são responsáveis pela força.
Onde de encontram: podem-se encontrar nos mamíferos, e constituem
grande parte do peso seco do cabelo, unhas, pêlos e grande parte das superfícies
externas.
Características gerais:
o -hélice da Queratina:
a) É semelhante à -hélice que se pode encontrar em
muitas outras proteínas, composta por cade polipeptidicas arranjados lado a lado.
b) Consiste na repetição de 7 resíduos (a,b,c,d,e,f,g),
sendo que a e d são não polares.
c) Duas cadeias de -hélice da Queratina, orientadas em
paralelo – isto é, com as terminações amino do mesmo lado – encontram-se
enroladas entre si formando uma estrutura serpenteada. Este enrolamento
amplifica a força de toda a estrutura.
d) Na superficie onde as hélices se tocam existem
aminoácidos hidrofóbicos: Valina, Metionina, Leucina, entre outros. Estes
aminoacidos permitem uma forte união das cadeias polipeptidicas.
e) O enrolar de 2 polipéptidos em -hélice é um exemplo
de estrutura quaternária. Hélices deste tipo são elementos estruturais comuns nas
proteinas filamentosas e na miosina (proteína moscular).
f) A -hélice da Queratina, quando em grande número,
organiza-se em grandes complexos supramoleculares, como é o exemplo dos
filamentos intermédios dos cabelos.
g) A existência de “cross-links” estabilizam a sua
estrutura quaternária.
Colagénio
Função: são responsáveis pela força.
Onde de encontram: Encontram-se nas junções tecidulares, como
cartilagem, tendões e a matriz orgânica dos ossos.
Características gerais:
o Hélice de colagénio:
a) Única estrutura secundária significativamente diferente
da -hélice
b) O colagénio é também uma estrutura helicoidal, que
consiste em 3 cadeias polipeptidicas (cadeias ), entrelaçadas entre si em tripla
hélice. A possibilidade de se entrelaçar as cadeias de várias formas distintas,
justifica os diversos graus de força e de resistência.
c) As moléculas de colagénio em tripla hélice são,
também, denominadas de moléculas Tropocolagénicas.
Sequência de aminoácidos:
a) A sequência de aminoácidos no colagénio consiste na
repetição das seguintes unidades tripeptidicas: Gly-X-Y
Gly corresponde ao aminoácido glicina;
X corresponde, muitas das vezes, ao aminoácido
Prolina, que permite o enlace da hélice;
Y corresponde, na sua maioria ao aminoácido 4
Hyp.
b) A sequência de aminoácidos e a estrutura entrelaçada
permite que as 3 cadeias se apresentem intimamente ligadas.
Valor proteico:
a) O colagénio tem um baixo valor proteico, uma vez
que apresenta baixos valores em aminoácidos essenciais à dieta humana.
Rigidez das junções tecidulares:
a) A enorme rigidez das junções tecidulares advêm do
acumular de “croos-links” covalentes nas fibras de colagénio (aglomerados
supramoleculares de moléculas de colagénio em tripla hélice).
“Silk fibroin” (fibras sedosas)
Origem: Produzida por insectos e aranhas
Características gerais:
o Conformação :
a) As
suas
cadeias
polipeptidicas
estão
predominantemente na conformação .
Aminoácidos:
a) É rica em Alanina e glicina, que permite que as folhas
e os grupos R estejam muito próximos.
Estrutura:
a) A sua estrutura é establilizada pelas extensas ligações
Hidogenóides entre os péptidos que unem as cadeias polipeptidcas de cada
lâmina e pelas interacções de Van Der Walls entre as lâminas.
b) Não estica, uma vez que a conformação já está
estendida ao máximo.
c) Apresenta flexibilidade pois as várias camadas estão
unidas por numerosas interacções de fraca intensidade.
Trabalho realizado por:
Grupo 8:
Lígia Figueiredo
Liliana Valente
Teresa Cardoso