Disciplina de Bioquímica ( DB-105 )
Aula Teórica
05/04/2002
Tópico 6 - Proteínas
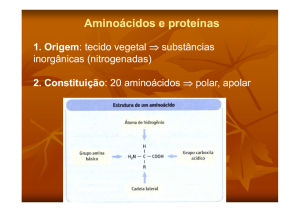
I -Definição: São substâncias orgânicas constituídas por unidades fundamentais denominadas
de aminoácidos.
II - Classificação:
a) Constituição: simples e conjugadas.
b) Forma: fibrosas e globulares.
c) Função: enzimas, reserva, transporte, contráteis, proteção, toxinas, hormônios,
estrutural.
d) Solubilidade:
III - Aminoácidos:
a) Comuns
b) Especiais: 4-hidroxiprolina
c) Comportamento ácido-base: os a.a. em solução aquosa estão ionizados e podem agir
como ácidos ou bases.
d) Classificação segundo a polaridade de seus grupos R:
Grupos R não polares: alanina, prolina, valina, etc.
Grupos R polares não-carregados: asparagina, glicina, serina.
Grupos R carregados negativamente: ácido aspártico, ácido glutâmico.
Grupos R carregados positivamente: arginina, histidina, lisina.
e) Aminoácidos de proteínas oticamente ativas são L-estereoisômeros.
IV - Peptídeos:
a) Ligação peptídica: ligação amida substituída, isto é, há remoção de uma molécula de
água do grupo carboxila de um a.a. e do grupo amino do outro.
b) Peptídeos naturais: encefalinas, bradicinina, gramicidina.
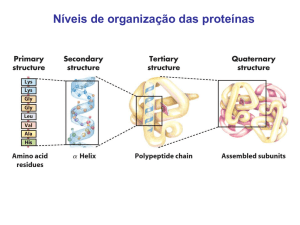
V - Estrutura Primária: É representada pela seqüência dos a.a. nas cadeias polipeptídicas e
pelas suas ligações peptídicas.
VI - Estrutura Secundária: Refere-se aos arranjos no espaço de resíduos de aminoácidos
adjacentes numa cadeia polipeptídica. Exemplos: -hélice e
conformação .
VII - Estrutura Terciária: É a estrutura tridimensional completa do polipeptídio. Apresenta os
grupos R polares no exterior e os grupos R hidrofóbicos no interior.
VIII - Estrutura Quaternária: Designa o arranjo mútuo de várias cadeias subunitárias de
estruturas terciárias. É o caso das proteínas oligoméricas,
apresentando duas ou mais cadeias polipeptídicas.
-1-