Proteínas
“As proteínas são o centro da acção em
todos os processos biológicos.”
Voet & Voet “Biochemistry”
• As proteínas são os compostos
orgânicos mais abundantes dos
organismos vivos (~50% do peso sêco)
•As proteínas desempenham uma
multiplicidade de papeis estruturais e
funcionais, tais como: enzimas, transporte,
armazenamento, reconhecimento, defesa,
estrutura, locomoção, produção de luz,
etc...
• As proteínas são polímeros lineares dos
20 aminoácidos, cuja sequência resulta da
tradução do gene correspondente
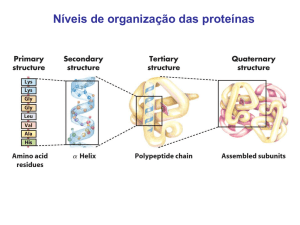
• Cada proteína apresenta geralmente
uma estrutura tridimensional bem definida,
determinada pela sequência dos seus
aminoácidos
Funções das proteínas
Transporte de oxigénio
Produção de luz
Função estrutural
Proteínas
• Elementos constitutivos das proteínas: C
(50%), O(23%), N(16%), H(7%), S (0-3%).
• As proteínas são polímeros lineares dos
20 aminoácidos, ligados entre si por
ligações peptídicas
• As proteínas são sintetizadas nos
ribossomas
• Os 20 aminoácidos podem sofrer
modificações após a síntese ribossomal
das proteínas
• À cadeia de aminoácidos podem
encontrar-se ligados, covalentemente ou
não, um ou mais grupos prostéticos, que
não são formados por aminoácidos.
• A proteína funcional pode ser constituida
por uma associação de várias cadeias
polipetídicas
Diversidade de funções das proteínas
Classe funcional
Exemplo
Enzimas
Proteínas estruturais
Lisozima, catalase,
tripsina
Colagénio, queratina
Proteínas de
transporte
Hemoglobina,
lipoproteínas
Proteínas de reserva
Albumina, caseína
Proteínas de
protecção
Anticorpos,
complemento
Proteínas de
motilidade
Actina, miosina,
dineína
Hormonas
Insulina, hormona do
crescimento
Citocromos,
ferredoxina
Toxina da difteria,
venenos de cobra
Proteínas redox
Toxinas
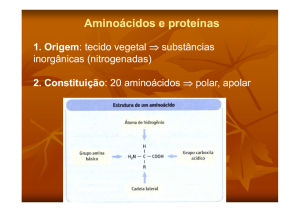
Aminoácidos
As proteínas são polímeros lineares de aminoácidos,
em que cada aminoácido está ligado ao próxima por
um tipo especial de ligação covalente (ligação
peptídica).
20 aminoácidos são geralmente encontrados nas
proteínas.
O primieiro aminoácido a ser descoberto foi a
asparagina (do espargo, asparagus), em 1806. O
último a ser descoberto foi a treonina, 1938.
Grupo
carbóxilo
Grupo
amina
Carbono α
Cadeia lateral
Fórmula geral de um α-aminoácido
Lisina
Nomenclatura dos carbonos da cadeia lateral
Quiralidade dos aminoácidos
O carbon α dos α-aminoácidos é um centro
quiral, porque se encontra ligado a 4 grupos
diferentes. Isto significa que a imagem no
espelho de um α-aminoácido é distinta do
original. Moléculas com esta propriedade
denominam-se enantiómeros:
L-α-aminoácido
Formas de representação de enantiómeros
Espelho
A nomenclature L, D é baseada
na estrutura do gliceraldeído
As proteínas são constituídas por L-aminoácidos!
Propriedades dos aminoácidos
Os aminoácidos podem ser classificados
de acordo com o seu grupo lateral R
Classificação dos aminoácidos
• Grupos R não-polares (alifáticos): os aminoácidos
alanina, valina, leucina e isoleucina estabilizam a
estruturas das proteínas através do efeito hidrofóbico. O
aminoácido glicina é o aminoácido mais pequeno. A
metionina é um dos dois únicos aminoácidos contendo
enxofre. A prolina é, de facto, um iminoácido.
• Grupos R aromáticos: a fenilalanina, tirosina e
triptofano têm cadeias laterais aromáticas e são
relativamente hidrofóbicos. A tirosina e o triptofano são
relativamente mais polares que a fenilalanina, pois
possuem átomos polares. A absorvância característica
das proteínas a 280 nm (ultravioleta) é resultado das
cadeias laterais do triptofano e tirosina e, em menor
grau, da fenilalanina.
• Grupos R polares, não carregados: estes grupos
são mais solúveis em água (hidrofílicos), devido à
presença de grupos polares capazes de formar ligações
de hidrogénio com a água. Incluem a serina, a treonina,
a asparagina, glutamina e cisteína. A cadeia lateral da
cisteína pode formar pontes de dissulfureto com outra
cadeia do mesmo aminoácido.
• Grupos R carregados positivamente: os resíduos
mais hidrofílicos são aqueles que se encontram
ionizados a pH 7. Os aminoácidos lisina e arginina são
básicos (pKa > 7) e carregados positivamente a pH 7. O
aminoácido histidina tem um pKa próxima de 7, podendo
perder ou ganhar facilmente um protão a pH fisiológico.
• Grupos R carregados negativamente: os
aminoácidos aspartato e glutamato são ácidos (pKa <7)
e carregados negativamente a pH 7.0
Mecanismo de formação de
pontes de dissulfureto
Absorvância dos resíduos
aromáticos no ultravioleta
As proteínas podem conter aminoácidos
modificados
Prototrombina
Colagénio
Colagénio
Elastina
Miosina
Este aminoácidos resultam de modificações dos 20
aminoácidos após a síntese proteíca, e
desempenham papeis muito importantes em
diferentes proteínas.
A selenocisteína é um caso especial, porque é
codificada geneticamente e inserida durante a síntese
proteíca em alguns microorganismos.
Os aminoácidos podem funcionar
como ácidos e bases
Forma
não-iónica
Forma
zwitteriónica
Zwitterião - molécula neutra mas que
contém cargas positivas e negativas
Curva de titulação da glicina
As curvas de titulação permitem
prever a carga dos aminoácidos
A curva de titulação dos aminoácidos está relacionado
com a sua carga total. No ponto de inflexão entre os
dois patamares da curva de titulação (pH=5.97), a
glicina encontra-se na predominantemente na forma
totalmente ionizada, mas a sua carga total é zero. O
pH a que a carga total é zero tem o nome de ponto
isoeléctrico (pI). Para um aminoácido diprótico, o pI
pode ser calculado como:
pI = (pK1+pK2)/2 = (2.34+9.60)/2 = 5.97
A glicina tem carga total positiva a qualquer ponto
abaixo do seu pI, e carga total negativa a qualquer
ponto acima do seu pI.
pI = (pK1+pK2)/2
O ambiente químico dos aminoácidos
afecta os valores de pKa
Os aminoácidos têm diferentes
propriedades ácido-base
pI = 3.22
pI = 7.59
Péptidos e proteínas
Os péptidos e proteínas são polímeros de
aminoácidos. O seu tamanho pode variar desde dois
até milhares de resíduos de aminoácido.
Ligação entre os grupos amina e carbóxilo de dois
aminoácidos, com eliminação de uma molécula de
água:
Ligação peptídica
Normalmente usa-se o termo oligopéptido para
péptidos com poucos aminoácidos, polipéptido para
polímeros até ~100 resíduos, e proteína para
sequências mais longas. No entanto não há uma
definição rigorosa destes termos!
Ligação peptídica
A polimerização dos aminoácidos dá-se através
da formação de ligações peptídicas, por
eliminação de uma molécula de água entre os
terminais amino e carboxilo de cada par de
aminoácidos.
Formação de um dipéptido
Ligação peptídica
Cadeia principal
Resíduos de aminoácido
Estrutura de uma cadeia polipeptídica
As cadeias polipeptídicas leêm-se de N para C !
Pentapéptido serilgliciltirosilalanilleucina:
Terminal carbóxilo
(C-terminal)
Terminal amina
(N-terminal)
Ser-Gly-Tyr-Ala-Leu
Alanilglutamilglicillisina
Os péptidos biologicamente activos
apresentam uma grande variedade
de dimensões
Exemplo de dipéptido biologicamente activo:
Os polipéptidos tem uma composição
característica
A mistura de aminoácidos que se obtém após
hidrólise de uma proteína tem uma composição
bem definida e constante para cada tipo de
proteína:
As proteínas podem conter grupos
químicos não-aminoacídicos
Enquanto muitas proteínas, como a lisozima ou a
ribonuclease, contêm apenas resíduos de aminoácidos
na sua composição (proteínas simples), existem outras
que estão permanentement associados a outros grupos
químicos (grupos prostéticos), normalmente essenciais
para a sua função.
A mioglobina, por exemplo, encontra-se associada a um
grupo hémico, essencial para o tranposrte de oxigénio.
A ligação ao grupo prostético pode ser ou não covalente.
A este último tipo de proteínas dá-se o nome de
proteínas conjugadas.