Aminoácidos e Peptídeos
Universidade Federal do Ceará
Centro de Ciências
Departamento de Bioquímica e Biologia Molecular
Disciplina de Introdução a Bioquímica
Aminoácidos e Peptídeos
1. Introdução
2. Aminoácidos
2.1. Definição e Características dos Aminoácidos
2.2. Classificação dos Aminoácidos
2.3. Característica de Ácidos e Bases dos aminoácidos
2.4. Curvas de Titulação de Aminoácidos
2.5. Ponto Isoelétrico (pI)
3. Peptídeos
Aminoácidos e Peptídeos
AMINOÁCIDOS E PEPTÍDEOS
1. Introdução
• Proteínas:
o Macromoléculas mais abundantes nas células vivas;
o Grande variabilidade de estrutura;
o Grande diversidade de funções biológicas;
o Papel central no Metabolismo Celular.
• Subunidade Monomérica: Aminoácidos
o Todas as proteínas, desde as formas mais antigas de bactérias
até as formas mais complexas de vida, são compostas pelo
mesmo grupo de 20 aminoácidos;
o Esses aminoácidos são ligados entre si para formar as proteínas
por ligações covalentes;
• Proteínas com propriedades extremamente diferentes são formadas pelos
mesmos 20 aminoácidos em muitas combinações e seqüências diferentes;
• É a partir destes 20 compostos que organismos diferentes produzem uma
grande diversidade de proteínas, com inúmeras e distintas propriedades.
2. Aminoácidos
• Primeiro Aminoácido a ser identificado: Asparagina (1806);
• O último dos 20 a ser identificado foi o aminoácido Treonina (1938);
• Para serem classificados dentro de um grupo químico, eles possuem
características estruturais em comum.
2.1. Definição e Características dos Aminoácidos
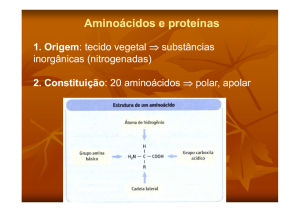
• Todos os aminoácidos possuem:
Aminoácidos e Peptídeos
o Um grupo carboxílico (−COOH), um grupo amino (−+NH3) e um
átomo de H ligados ao mesmo átomo de carbono;
o Além dos grupos acima, está ligado neste mesmo carbono um
grupo radical R que é variável em tamanho e característica
química entre os diferentes aminoácidos;
o O átomo de carbono central é chamado de Cα e é um centro
assimétrico da molécula;
• Aminoácidos Padrões e suas Abreviações
• Cα e Estereoisomeria dos Aminoácidos:
o Forma tetraédrica dos orbitais de ligação;
o Forma D e forma L, baseada na configuração absoluta do L e do
D-Gliceraldeído;
o Todos
os
aminoácidos
que
ocorrem
nas
proteínas
são
estereoisômeros do tipo L;
o Estereoisômeros L e D → Significado para os sistemas vivos
• Os aminoácidos estão ionizados em soluções aquosas
o Forma Zwitteriônica.
• Nomenclatura Abreviada dos Aminoácidos
o 3 Letras (Ser, Gly, Trp, Try, Phe, Ala, etc.);
o 1 Letra (A, T, G, W, Q, N, M, D, E, K, R, etc.).
2.2. Classificação dos Aminoácidos
• Os aminoácidos podem ser classificados de acordo com as propriedades
químicas do grupo R;
• Esta classificação não é completamente fixa e pode apresentar variações;
• A polaridade do grupo R é um dos fatores mais importantes na
classificação dos aminoácidos;
• Principais Grupos:
Aminoácidos e Peptídeos
o Aminoácidos Não-polares, com grupos R alifáticos
• Particularidades
o Aminoácidos com grupos R aromáticos
• Particularidades:
• Absorção de Luz na região do Ultravioleta
o Aminoácidos Polares, com grupos R não carregados
• Particularidades
o Aminoácidos com grupos R carregados positivamente
o Aminoácidos com grupos R carregados negativamente
Outros aminoácidos que podem ocorrer nas proteínas
2.3. Característica de Ácidos e Bases dos aminoácidos
• Os aminoácidos podem funcionar como doadores e aceptores de prótons
H+;
• Substâncias com esta característica são chamadas de anfotéricas;
• Exemplos.
2.4. Curvas de Titulação de Aminoácidos
• Constantes de Equilíbrio de reações de ionização → Constante de
Dissociação, Ka;
pK a = − log K a
• pKa do grupo −COOH (pK1);
• pKa do grupo −+NH3 (pK2);
• Pontos importantes da curva de titulação de aminoácidos
• Pontos de capacidade tamponante de soluções de aminoácidos
Aminoácidos e Peptídeos
2.5. Ponto Isoelétrico (pI)
• Valor de pH onde a carga líquida dos aminoácidos é igual a zero;
• Neste pH, se um determinado aminoácido for submetido a um campo
elétrico, ele não apresentará movimento;
• Quando o aminoácido não tiver um grupo R ionizável, o seu pI pode ser
calculado pela média dos pKa dos grupos amina e carboxila:
1
pI = ( pK1 + pK 2 )
2
• Aplicação Prática
Curvas de Titulação de Aminoácidos com grupo R ionizável:
• pI → Média dos pKa mais próximos
3. Peptídeos
• Cadeias de aminoácidos ligados entre si por uma ligação covalente,
chamada ligação peptídica;
• Ligação Peptídica;
o Estrutura
o Características
• Oligopeptídeo → poucos aminoácidos
• Polipeptídeo → vários aminoácidos (Peso molecular < 10,000)
• Aminoácidos ligados por ligação peptídica → Resíduos de Aminoácidos
• Polaridade da Cadeia Polipeptídica
o Amino-terminal ou N-terminal;
o Carboxi-terminal ou C-terminal.
• Pequenos Polipeptídeos e Peptídeos com atividade biológica
o Insulina → 2 cadeias de polipeptídeos (30 e 21);
o Glucagon → 29 aminoácidos
o Dipeptídeos: Aspartame (Adoçantes) e Aspartato de Arginina.