Texto retirado na íntegra: http://www.sobiologia.com.br/conteudos/quimica_vida/quimica3.php
Como são os lipídios?
Os lipídios são compostos orgânicos insolúveis em água. Dissolvem-se
bem em solventes orgânicos como o éter e o álcool. A estrutura química
molecular dos lipídios é muito variável. Vamos dar a você uma noção da
composição química de óleos e gorduras e alguns dos principais componentes
desse grupo.
Óleos e gorduras – pertencem à categoria dos ésteres e são formados por meio da reação de
umálcool, chamado glicerol, com ácidos orgânicos de cadeia longa, conhecidos como ácidos graxos. A
exemplo do que ocorre com os carboidratos, a reação do glicerol com os ácidos graxos é de condensação, havendo
liberação de moléculas de água.
Como o glicerol é um triálcool (possui três terminações OH na molécula), três ácidos graxos a ele se ligam,
formando-se o chamado triglicerídeos. Nos seres vivos, existem diversos tipos de triglicerídeos, uma vez que são
muitos os tipos de ácidos graxos deles participantes.
Com relação aos ácidos graxos que participam de um triglicerídeos, lembre-se que são substâncias de cadeia
longa. Em uma das extremidades de cada ácido graxo há uma porção ácida (a “cabeça”), seguida de uma longa
“cauda” formada por uma seqüência de átomos de carbono ligados a átomos de hidrogênio.
Nos chamados ácidos graxos saturados, todas as ligações disponíveis dos átomos de carbono são ocupados por
átomos de hidrogênio. Já nos ácidos graxos insaturados, nem todas as ligações do carbono são ocupadas por
hidrogênios; em conseqüência, forma-se o que em química é conhecido como duplas ligação entre um átomo de
carbono e o seguinte (motivo pelo qual o ácido graxo recebe a denominação de insaturado). Nos ácidos graxos
poliinsaturados há mais de uma dupla ligação.
Fosfolipídios – as membranas biológicas são constituídas por fosfolipídios. Nos fosfolipídios há apenas duas
moléculas de ácidos graxos – de natureza apolar – ligadas ao glicerol. O terceiro componente que se liga ao
glicerol é um grupo fosfato (daí a denominação fosfolipídio) que, por sua vez, pode estar ligado a outras moléculas
orgânicas. Assim, cada fosfolipídio contém uma porção hidrofóbica – representada pelos ácidos graxos – e uma
porção hidrofílica – corresponde ao grupo fosfato e às moléculas a ele associadas. Um fato notável é que, ao
serem colocadas em água, as moléculas de fosfolipídios podem assumir o formato de um esfera, conhecida como
micela: as porções polares, hidrofílicas, distribuem-se na periferia , enquanto as caudas hidrofóbicas ficam no
interior da micelas afastadas da água.
Nas células, os fosfolipídios das membranas biológicas (membrana plasmática e de muitas organelas)
dispõem-se formando bicamadas. As porções hidrofílicas ficam em contato com a água dos meios interno e
externo celular, enquanto as hidrofóbicas situam-se internamente na membrana, afastadas da água, o que faz
lembrar um sanduíche de pão-de-forma.
Prostaglandinas – essas substâncias atuam como mensageiras químicas em muitos tecidos humanos. Seu nome
deriva do fato de terem sido descobertas em componentes do sêmen humano produzidos na glândula próstata.
Terpenos – lipídios de cadeia longa, componentes de pigmentos biologicamente importantes como a clorofila
(pigmento vegetal participante da fotossíntese). Uma importante categoria de terpenos é a dos carotenóides
(pigmentos amarelados), dos quais o mais importante é o B-caroteno (encontrado em muitos alimentos de origem
vegetal, como a cenoura, por exemplo), que é precursor da vitamina A (retinol).
Esteróides – alguns esteróides são hormônios (por exemplo, a testosterona, o hormônio sexual masculino) e
outros são vitaminas (por exemplo, a vitamina D). O colesterol, que para os químicos é um álcool complexo, é
outro exemplo de esteróide: é importante componente de membranas celulares, embora hoje seja temido como
causador de obstrução (entupimento) em artérias do coração.
O colesterol não “anda” sozinho no sangue. Ele se liga a uma proteína e, dessa forma, é transportado. Há dois
tipos principais de combinações: o HDL, que é o bom colesterol e o LDL que é o mau colesterol. Essas siglas
derivam do inglês e significam lipoproteína de alta densidade (HDL – High Density Lipoprotein) e lipoproteína de
baixa densidade (LDL – Low Density Lipoprotein).
O LDL transporta colesterol para diversos tecidos e também para as artérias, onde é depositado, formando placas
que dificultam a circulação do sangue, daí a denominação mau colesterol. Já o HDL faz exatamente o contrário,
isto é, transporta colesterol das artérias principalmente para o fígado, onde ele é inativado e excretado como sais
biliares, justificando o termo bom colesterol.
O colesterol não existe em vegetais, o que não significa que devemos abusar dos óleos vegetais,
porque afinal, a partir deles (ácidos graxos), nosso organismo produz colesterol.
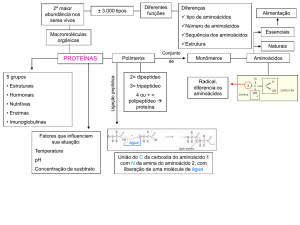
Proteínas: A construção dos seres vivos
Você já deve ter ouvido falar de proteínas, certo? As proteínas são compostos orgânicos relacionados ao
metabolismo de construção. Durante as fases de crescimento e desenvolvimento do indivíduo, há um aumento
extraordinário do número de suas células que passam a exercer funções especializadas, gerando tecidos e órgãos.
As proteínas possuem um papel fundamental no crescimento, já que muitas delas desempenham papel estrutural
nas células, isto é, são componentes da membrana plasmática, das organelas dotadas de membrana, do
citoesqueleto dos cromossomos etc. E para produzir mais células é preciso mais proteína. Sem elas não há
crescimento normal. A diferenciação e a realização de diversas reações químicas componentes do metabolismo
celular dependem da paralisação de diversas reações químicas componentes do metabolismo celular, dependem
da participação de enzimas. Há também uma categoria de proteínas de defesa, chamadas anticorpos, sem eles
nosso organismo fica extremamente vulnerável.
Certos
hormônios,
substâncias
reguladoras
das
atividades do nosso organismo, também são protéicos. É
o caso da insulina, que controla a taxa de glicose
sangüínea.
As proteínas são macromoléculas formadas por
uma sucessão de moléculas menores conhecidas
como aminoácidos. A maioria dos seres vivos,
incluindo o homem, utiliza somente cerca de vinte tipos
diferentes de aminoácidos, para a construção de suas
proteínas. Com eles, cada ser vivo é capaz de produzir
centenas de proteínas diferentes e de tamanho variável.
Como é isso possível, a partir de um pequeno número de aminoácidos?
Imagine um brinquedo formado por peças de plástico, encaixáveis umas nas outras, sendo as cores em número de
vinte, diferentes entre si. Havendo muitas peças de cada cor, como você procederia para montar várias
sequencias de peças de maneira que cada sequencia fosse diferente da anterior? Provavelmente , você repetiria as
cores, alternaria muitas delas, enfim, certamente inúmeras seriam as sequencias e todas diferentes entre si. O
mesmo raciocínio é valido para a formação das diferentes proteínas de um ser vivo, a partir de um conjunto de
vinte aminoácidos.
Cada aminoácido é diferente de outro. No entanto, todos possuem alguns componentes comuns. Todo
aminoácido possui um átomo de carbono, ao qual estão ligados uma carboxila, uma amina e um
hidrogênio. A quarta ligação é a porção variável, representada por R, e pode ser ocupada por um hidrogênio,
ou por um metil ou por outro radical.
Aminoácidos mais conhecidos
Ligação peptídica: unindo aminoácidos
Do mesmo modo que em um trem cada vagão está
engatado ao seguinte, em uma proteína cada
aminoácido está ligado a outro por uma ligação
peptídica. Por meio dessa ligação, o grupo amina de
um aminoácido une-se ao grupo carboxila do outro,
havendo a liberação de uma molécula de água. Os
dois aminoácidos unidos formam um dipeptídio.
A ligação de um terceiro aminoácido ao dipeptídeo
origina um tripeptídeo que então, contém duas
ligações peptídicas. Se um quarto aminoácido se ligar
aos três anteriores, teremos um tetrapeptídeo, com
três ligações peptídicas. Com o aumento do número
de aminoácidos na cadeia, forma-se um polipetídio,
denominação utilizada até o número de 70
aminoácidos. A partir desse número considera-se que
o composto formado é uma proteína.
Aminoácidos essenciais e naturais
Todos os seres vivos produzem proteínas. No entanto, nem todos produzem os vinte tipos de aminoácidos
necessários para a construção das proteínas. O homem, por exemplo, é capaz de sintetizar no fígado
apenas onze dos vinte tipos de aminoácidos. Esses onze aminoácidos são considerados naturais para a nossa
espécie. São eles:alanina, asparagina,cisteína, glicina, glutamina, histidina, prolina, tiroxina, ácido aspártico, ácido
glutâmico.
Os outros nove tipos, os que não sintetizamos, são os essenciais e devem ser obtidos de quem os produz (plantas
ou animais). São eles: arginina, fenilalanina, isoleucina, leucina, lisina, metionina, serina, treonina, triptofano e
valina.
É preciso lembrar que um determinado aminoácido pode ser essencial para uma espécie e ser natural para outra.
Uma visão espacial da proteína
Uma molécula de proteína tem, a grosso modo, formato de um colar de contas. O fio fundamental da proteína,
formado como uma sequencia de aminoácidos (cuja sequencia é determinada geneticamente), constitui a
chamada estrutura primária da proteína.
Ocorre, porém, que o papel biológico da maioria das
proteínas depende de uma forma espacial muito mais
elaborada. Assim, o fio fundamental é capaz de se
enrolar sobre si mesmo, resultando um filamento
espiralado que conduz à estrutura secundária,
mantida estável por ligações que surgem entre os
aminoácidos.
Novos dobramentos da espiral conduzem a uma nova
forma, globosa, mantida estável graças a novas
ligações que ocorrem entre os aminoácidos. Essa
forma globosa representa a estrutura terciária.
Em certas proteínas, cadeias polipeptídicas em
estruturas terciárias globosa unem-se, originando
uma forma espacial muito complexa, determinante
do papel bioquímico da proteína. Essa nova forma
constitui a estrutura quaternária dessas proteínas.
A figura abaixo mostra as quatro estruturas da
hemoglobina juntas. A hemoglobina esta presente
dentro os glóbulos vermelhos do sangue e seu papel
biológico é ligar-se a moléculas de oxigênio,
transportando-as a nossos tecidos.
O fio do telefone pode ilustrar bem a idéia das estruturas protéicas:
Forma e função: um binômio inseparável
Logo mais você compreenderá de que modo a
estrutura espacial de uma proteína está relacionado
à função biológica que ela exerce. Por enquanto,
lembre-se que, a manutenção das estruturas
secundárias e terciárias deve-se a ligações que
ocorrem entre os aminoácidos no interior da
molécula protéica, determinando os diferentes
aspectos espaciais observados.
O aquecimento de uma proteína a determinadas temperaturas promove a ruptura das ligações internas
entre os aminoácidos, responsáveis pela manutenção das estruturas secundária e terciária. Os aminoácidos não
se separam, não se rompem as ligações peptídicas, porém a proteína fica “desmantelada”, perde a sua estrutura
original. Dizemos que ocorreu uma desnaturação proteica, com perda da sua forma origina. Dessa maneira a
função biológica da proteína é prejudicada.
Nem sempre, porém, é a temperatura ou a alteração da acidez do meio que provoca a mudança da forma da
proteína. Muitas vezes, a substituição de um simples aminoácido pode provocar alteração da forma da
proteína.
Um exemplo importante é a substituição, na
molécula de hemoglobina, do aminoácido ácido
glutâmico pelo aminoácido valina. Essa simples
troca provoca uma profunda alteração na forma da
molécula inteira de hemoglobina, interferindo
diretamente na sua capacidade de transportar
oxigênio.
Hemácias
contendo
a
hemoglobina
alterada
adquirem o formato de foice, quando submetidas a
certas condições, o que deu nome a essa
anomalia: anemia falciforme.
Enzimas
A vida depende da realização de inúmeras reações químicas que ocorrem no interior das células e também fora
delas (em cavidades de órgãos, por exemplo). Por outro lado, todas essas reações dependem, para a sua
realização , da existência de uma determinada enzima. As enzimas são substâncias do grupo das proteínas e
atuam como catalisadores de reações químicas.
Catalisador é uma substância que acelera a velocidade de ocorrência de uma certa reação química.
Muitas enzimas possuem, além da porção proteica propriamente dita, constituída por uma sequencia de
aminoácidos, uma porção não proteica.
A parte proteica é a apoenzima e a não proteica é o cofator. Quando o cofator é uma molécula orgânica, é
chamado de coenzima. O mecanismo de atuação da enzima se inicia quando ela se liga ao reagente, mais
propriamente conhecido como substrato. É formado um complexo enzima-substrato, instável, que logo se desfaz,
liberando os produtos da reação a enzima, que permanece intacta embora tenha participado da reação.
Mas para que ocorra uma reação química entre duas substâncias orgânicas que estão na mesma solução é preciso
fornecer uma certa quantidade de energia, geralmente, na forma de calor, que favoreça o encontro e a colisão
entre elas. A energia também é necessária para romper ligações químicas existentes entre os átomos de cada
substância, favorecendo, assim a ocorrência de outras ligações químicas e a síntese de uma nova substância a
partir das duas iniciais.
Essa energia de partida, que dá um “empurrão” para que uma reação química aconteça, é chamada de energia de
ativação e possui um determinado valor.
A enzima provoca uma diminuição da energia de ativação necessária para que uma reação química aconteça e isso
facilita a ocorrência da reação.
O mecanismo “chave-fechadura”
Na catálise de uma reação química, as enzimas interagem com os substratos, formando com eles,
temporariamente, o chamado complexo enzima-substrato. Na formação das estruturas secundária e terciária de
uma enzima (não esqueça que as enzimas são proteínas), acabam surgindo certos locais na molécula que servirão
de encaixe para o alojamento de um ou mais substratos, do mesmo modo que uma chave se aloja na fechadura.
Esses locais de encaixe são chamados de sítio ativos e ficam na superfície da enzima. Ao se encaixarem nos sítios
ativos, os substratos ficam próximos um do outro e podem reagir mais facilmente.
Assim que ocorre a reação química com os substratos, desfaz-se o complexo enzima-substrato. Liberam-se os
produtos e a enzima volta a atrair novos substratos para a formação de outros complexos.
Lembre-se!! Uma enzima não é consumida durante a reação química que ela catalisa.´