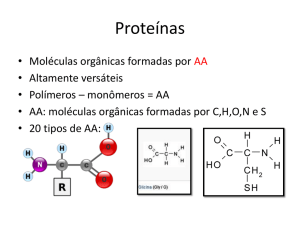
O que são enzimas?
Catalizadores biológicos
- Aceleram reações químicas específicas sem
a formação de produtos colaterais
Reagentes = substratos
Local onde a reação ocorre = sitio ou centro
ativo
S + E ES EP P + E
Características das enzimas
1 - Grande maioria das enzimas são proteínas
(algumas moléculas de RNA tem atividade catalítica – ribozimas)
2 - Funcionam em soluções aquosas diluídas,
em condições muito suaves de temperatura e
pH (mM, pH neutro, 25 a 37oC)
Pepsina estômago – pH 2
Enzimas de organismos hipertermófilos
ambientes quentes) atuam a 95oC
(crescem
em
3 - Apresentam alto grau de especificidade por
seus reagentes (substratos)
4 - Peso molecular: varia de 12.000 à 1 milhão
daltons (Da),
são portanto muito grandes
quando comparadas ao substrato.
Molécula que se
liga ao sítio
ativo e que vai
sofrer a ação da
enzima =
substrato
Região da enzima
onde ocorre a
reação = sítio ativo
5 - A atividade catalítica das Enzimas depende
da integridade de sua conformação protéica
nativa – local de atividade catalítica (sitio
ativo)
glicose
catalase
Tetrâmero – 60KDa ~
500aa
hexoquinas
e
98000 Da 920aa
Sítio ativo e toda a molécula proporciona um
ambiente adequado para ocorrer a reação
química desejada sobre o substrato
Nomes comuns de enzimas
Normalmente se adiciona o sufixo ase ao
nome do substrato ou à atividade
realizada:
Amilase – hidrolisa o amido
Amido sintetase – síntese do amido
DNA-polimerase – polimeriza DNA
Transaminase ou aminotransferase
Hidrolase
Classificação das enzimas – 6 Classes de acordo
com o tipo de reação/função
classe
grupo
Reação catalisada
EC 1
Oxidorredutase
Transferência de elétrons (íons
hidreto ou átomos de H)
EC 2
Transferase
Transferência de grupos
EC 3
Hidrolase
Hidrólise (transferência de grupos
funcionais envolvendo água)
EC 4
Liase
Adição de grupos funcionais a
dupla ligação ou formação de
dupla ligação pela remoção de
grupos
EC 5
Isomerase
Transferência de grupos dentro da
mesma molécula formando
isômeros
EC 6
Ligase
Formação de ligações C-C, C-S, CO e C-N por meio de ligações de
condensação e quebra de ATP
Comitê de Nomenclatura da União Internacional de Bioquímica e
Biologia Molecular http://www.chem.qmul.ac.uk/iubmb/enzyme/
Como as enzimas agem?
Enzimas fornecem um
ambiente específico para
tornar uma reação biológica
termodinamicamente mais
favorável.
As enzimas aumentam a velocidade das
reações químicas
A velocidade da reação está
relacionada à energia de ativação
O que é a energia de ativação?
Velocidade
Equilíbrio
Energia de ativação é dada pela diferença energética
entre o estado fundamental e o de transição
As enzimas aumentam a velocidade das
reações diminuindo a energia de ativação
das reações
Como as enzimas diminuem a energia de ativação?
Várias ligações e interações entre os resíduos de aa
do centro ativo e o substrato proporcionam a
ocorrência da reação química necessária –
aumentando a velocidade da reação química
Direcionam o
substrato para a
posição adequada
dos grupos reativos
Proporciona a
associação e a aquisição
de cargas elétricas
importantes para a
reação
Substrato posicionado no sítio ativo da enzima: grupos
catalíticos funcionais auxiliam a quebra e a formação de
ligações por meio de uma variedade e mecanismos
Quais são os grupos catalíticos e
como a catálise ocorre?
Três tipos de mecanismos catalíticos:
Catálise ácido-base geral (transferência de prótons
de um substrato ou de um intermediário)
Catálise covalente (formação de ligação covalente
transitória entre o substrato e a enzima)
Catálise por íons metálicos (íons metálicos
ligados às enzimas auxiliam a reação)
Aminoácidos que recebem ou doam prótons
nos centro ativos das enzimas
Isso explica a
dependência
do pH na
atividade das
enzimas
Esse tipo de catálise ocorre na maioria das enzimas
Catálise covalente
Nesse tipo de catálise ocorre a formação de uma
ligação covalente entre a enzima e o substrato
(ex: hidrólise)
A B
H2O
A +B
Na presença de uma enzima com um grupo
nucleofílico essa reação acontece em dois passos
A B + X:
A X +B
H2O
A + B + X:
Aminoácidos mostrados anteriormente e alguns grupos
funcionais de coenzimas agem como nucleófilos
Catálise por íons metálicos
Nesse tipo de catálise o íon (zinco, magnésio ou
cálcio) estão ligados a aminoácidos do centro ativo
e participam da catálise como nas catálises ácidobase orientando o substrato ou estabilizando o
complexo ES eletricamente.
Atividade enzimática é afetada pelo pH
O pH pode influenciar a atividade de uma enzima através de maneiras
distintas. Primeiramente, o pH pode levar à desnaturação proteica.
O pH também pode interferir na atividade de uma enzima alterando o
padrão de cargas de um determinado sítio ativo ou catalítico, ou alterando
a conformação geral da proteína.
Atividade enzimática é afetada pela temperatura
O aumento de temperatura aumenta a taxa de reação enzimática devido
ao aumento de energia cinética das moléculas participantes da reação.
A temperatura pode interferir nas interações que mantém as estruturas
secundárias e terciárias (pontes de hidrogênio e interações hidrofóbicas),
podendo levar à desnaturação protéica.
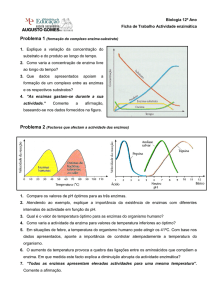
Curva que relaciona [S] e V0 é uma hipérbole, concentrações
mais baixas aumento linear da velocidade, concentrações mais
altas velocidade atinge um valor máximo
Concentrações
baixas de
substrato ocorre
aumento linear
entre
Velocidade(V0) e o
Substrato [S]
[S] V0
aumenta cada vez
menos até atingir
um patamar (Vmax)
Curva relacionando [S] e V0 pode ser expressa algebricamente
Equação de Michaelis-Menten
Constante de Michaelis
O que é Km ?
É a concentração do substrato
onde se obtém metade da
velocidade máxima da reação
Equação de Michaelis-Menten
Transformações da equação de Michaelis-Menten
Equação de Lineweaver-Burk ou duplo-recíproco
Inversão dos dois lados da equação de Michaelis-Menten
Separação dos componentes do lado direito.
Equação de Lineweaver-Burk ou duplo-recíproco
inverter
Separar
componentes e
resolver
y
=
Km
a
1
x
+
b
Com essa transformação matemática
passa-se a trabalhar com uma reta e
não com uma hipérbole, mais fácil.
a = coeficiente angular
y=0
b = coeficiente linear
x=0
A atividade de todas as enzimas pode ser
inibida por determinadas moléculas
Inibidores enzimáticos
São moléculas que interferem com a
catálise diminuindo ou interrompendo a
reação enzimática
Como são classificados os inibidores de
acordo com seu mecanismo de ação?
Reversíveis
Irreversíveis
Inibição competitiva
Inibição incompetitiva
Inibição mista ou não competitiva
Como eles atuam?
Reversíveis - Inibição competitiva
Inibidor compete com o substrato pelo sitio ativa da enzima
Inibidor tem estrutura molecular semelhante à do substrato
[S] deslocar inibidor do
sítio ativo e manter Vmax
V max é constante na presença do inibidor devido à
grande quantidade de substrato
Reversíveis - Inibição incompetitiva
Inibidor se liga em um
sítio diferente do centro
ativo, impede a reação do
complexo ES.
Independente da concentração do substrato o Km e a
Vmax estão alterados
Reversíveis - Inibição mista ou não competitiva
Inibidor se liga tanto ao
complexo ES como à
enzima, em um sítio
diferente do centro ativo
Independente da concentração do substrato o
Km e a Vmax estão alterados
Inibição irreversível
Inibidor se liga de maneira estável ou covalente
com um grupo funcional importante para a
atividade enzimática
Utilizados experimentalmente para definir os
aminoácidos essenciais do centro ativo das
enzimas
Inativar determinadas enzimas em situações
biológicas importantes
Este é o mecanismos de ação dos inseticidas
organofosforados, como o malathion e o parathion.
Absorção via pele, inalação e ingestão alimentos contaminados.
Metabolismo hepático lento - intoxicação
Reagem com o resíduo de serina no sitio ativo das serinoenzimas, formando um complexo irreversível.
Uma das enzimas altamente sensível a esses compostos é
a acetilcolinesterase, responsável pela metabolização do
neurotransmissor acetilcolina em neurônios centrais e
periféricos (envenenamento por organofosforados)
Sintomas – depressão respiratória, letargia, convulsões, coma
•Regulam a velocidade das reações metabólicas
•São reguladas por determinados sinais
•Tipos:
Enzimas alostéricas
Enzimas reguladas por modificações
covalentes reversíveis
Enzimas reguladas por proteólise
Enzimas alostéricas
•Possui sítios reguladores
para a ligação do
modulador especifico
•Maiores e mais
complexas que as não
alostéricas (mais que uma
cadeia polipeptídica)
Sofrem modificações
conformacionais em
resposta à ligação do
modulador (positivo ou
negativo)
Enzimas reguladas por modificações
covalentes reversíveis
•Diferentes grupos
podem se ligar á
molécula
enzimática e
regular sua
atividade
•Grupos ligados
covalentemente e
removidos pela
ação de outras
enzimas
Menos ativa
Mais ativa
Enzimas reguladas por proteólise
Enzimas proteolíticas – mecanismo de
proteção/regulação
Enzima inativa
Fatores externos
(autólise ou ação
de outra protease)
Parte da cadeia é
retirada e a enzima
muda sua
conformação
expondo o sítio ativo