ESTRUTURA
DAS
PROTEÍNAS
Aminoácidos ligam-se por ligações
peptídicas = reação de condensação entre:
–OH do grupo carboxila de um aminoácido
–H do grupo amina do outro aminoácido
( liberação de uma molécula de água)
Esqueleto polipeptídico
Interações
hidrofóbicas e
hidrofílicas
As cadeias laterais (radicais) dos
aminoácidos polimerizados livres
interagem entre si e com a água
Ligações
de
hidrogênio
Ligações dissulfeto
Forças usadas para a manutenção
da estrutura tridimensional das
proteínas - conformação
Interações
iônicas
A conformação de uma proteína é fundamental para a
função que ela exerce
• Perda da conformação ou da
estrutura tridimensional da
proteína = perda da função e das
características naturais da molécula
Como é a estrutura das proteínas???
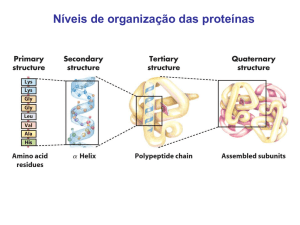
4 níveis estruturais
Estrutura primária, secundária, terciária e quaternária
Mantidas por:
•ligações covalentes (ligação peptídica e ligação dissulfeto
•forças fracas ( ligações de hidrogênio, interações
hidrofóbicas / hidrofílicas e iônicas
Estrutura primária
sequência linear
dos aminoácidos
unidos por ligações
peptídicas
Estrutura terciária
arranjo
tridimensional da
cadeia polipeptídica,
interações entre
aminoácidos mais
distantes
Estrutura secundária
conformação local de
alguns regiões da
cadeia polipeptídica
(-hélice, -pregueada
e dobras β)
Estrutura quaternária
arranjo tridimensional
de diferentes cadeias
polipeptídicas
Estrutura primária das proteínas
Seqüência de aminoácidos unidos por ligações peptídicas
Terminal amino e carboxila
Número variável de resíduos de aminoácidos
Tamanho diferentes das moléculas – número de resíduos
Composição
diferente de
aminoácidos
Sequencia de aminoácidos determinada pelo material genético do
organismo – comparação entre organismos
Através da análise da sequencia
dos aminoácidos de um proteína
pode-se avaliar a relação
evolutiva entre as espécies ou
comparar espécies similares
Estrutura secundária das proteínas
Mantida por ligações de hidrogênio
entre aminoácidos próximos
conformação em - hélice
conformação -pregueada
dobra
Conformação em -hélice
Arranjo tridimensional
que a cadeia polipeptídica
assume conformação
helicoidal ao redor de um
eixo imaginário
Mantida por ligações de
hidrogênio entre os grupos C=O
e o N-H da ligação peptídica
quatro resíduos subsequentes.
Cada volta da hélice inclui 3,6
resíduos de aminoácidos
O hidrogênio do carbono
fica para dentro da hélice
enquanto as cadeia laterais
ficam para o lado de fora
A presença de grupos grandes,
eletricamente carregados ou polares
ou de Pro e Gli desestabilizam a
estrutura da -hélice
Conformação -pregueada
Cadeia polipeptídica estende-se em zigzag e
podem estar arrumadas lado a lado formando um
estrutura chamada folhas pregueada
Folhas pregueada
Ligações de H são formadas entre as cadeias
adjacentes (C=O e o N-H da ligação peptídica)
Existem dois tipos de folhas pregueada
Paralelas – mesma orientação
das cadeias (terminal amino e
carboxílico)
Anti-Paralelas –orientação
oposta das cadeias (terminal
amino e carboxílico)
Proteínas globulares podem apresentar essas duas
estruturas, entretanto para ficar compacta a cadeia
deve apresentar dobras (representações)
Conformação
-hélice +
Conformação
-hélice
Dobras
Elemento de conexão entre as regiões com
estrutura secundária diferentes ou não
Dobras compreende uma estrutura que causa uma volta
de 180º
Envolve 4 aminoácidos
Forma ligação de Hidrogênio entre oxigênio da carboxila do
primeiro resíduo com o H do grupo amina do quarto resíduo
Resíduos 2 e 3 não
participam de nenhuma
interação
Dobras são encontradas
normalmente na superfície
das proteínas – ligações de
H dos resíduos 2 e 3
(cadeia lateral) com a água
Estrutura terciária e
quaternária das proteínas
Grupo
Heme
Estrutura terciária - arranjo tridimensional da
cadeia peptídica estabilizado por interações entre
grupos de aminoácidos distantes
Estrutura quaternária - arranjo entre cadeias
polipeptídicas (subunidades) que constituem um
proteína ativa
Mantida por
interações fracas
(ligações de H,
ligações iônicas e
interações
hidrofóbicas) e /ou
ligações dissulfeto
entre resíduos
distantes na
própria molécula
ou das
subunidades.
Tanto as proteínas fibrosas como as globulares
podem se associar para desempenhar uma função
biológica (estrutura quaternária)
Quanto ao número de subunidades as proteínas podem ser:
Monomérica – uma unidade
Oligomérica – poucas subunidades (dímero, trímero,
tetrâmero...)
Multímero – proteína ou complexo proteico formado
por muitas subunidades polipeptídicas
Unidades de repetição - protômeros
Hemoglobina – tetrâmero
(quatro unidades) duas
cadeias e duas cadeias
Pode ser considerada
um dímero de dois
protômeros
(unidade repetitiva)
RUBISCO
8 cadeias pequenas
8 cadeias grandes
Oligômero (16 cadeias
ou 8 protômeros)
Virus do mosaico do
Tabaco - cápsula de
proteínas - Multímero
Com relação à estrutura e sua função biológica
as proteínas podem ainda ser classificadas em
Fibrosas e Globulares
Proteínas Fibrosas
Função – estrutural, suporte e proteção
Cadeias longas e folhas
Tipo simples de estrutura secundária
Caracterizadas por proporcionar resistência e
flexibilidades às estruturas onde ocorrem
São insolúveis em água
Estruturas principais:
• α – Queratinas
• Colageno
• Fibroina
α – Queratinas
Cabelo, unhas,
cascos, chifres, lã,
penas e camada
externa pele.
Estrutura secundária – hélice
orientada para a direita
Monômero
Dímero enovelado
Protofibrila
Rica em resíduos
hidrofóbicos
(Ala, Val, Leu, Ile, Met e Phe)
Fibrila
Arranjo similar - formam
estruturas superenoveladas
que se agrupam formando
filamentos
Interações hidrofóbicas entre
cadeias laterais dos
aminoácidos e ligações
dissulfeto mantem a estrutura
Filamento
Um fio de cabelo é
formado por
muitos filamentos
Colágeno
Tendões, cartilagens,
córnea, matriz orgânica
ossos
3 resíduos de aminoácidos que se
repetem Gly-X-Pro ou Gly-X-HyPro
(X qualquer aminoácido)
Estrutura secundaria em hélice
voltada para a esquerda
Estrutura quaternária 3 cadeias
enroladas
Formam fibrilas - estrutura mantidas
por algumas ligações covalentes não
habituais (Lys – HyLis ou His)
Gelatina – derivada do colágeno –
baixo valor nutricional humano pelos
aminoácidos que a constituem
Fibroína
Fios de seda e teia de aranha
Estrutura secundária - β - pregueada
Rica em Ala e Gly - cadeias lateais pequenas e empacotamento
dos grupos R
Fibras são
camadas de folhas
β antiparalelas
arranjadas
densamente
Estrutura mantida
por ligações de
hidrogênio
Proteínas Globulares
Função – enzimas, reguladoras, transporte e de defesa
Cadeias esféricas ou globulares
Diversos tipos de estrutura secundária
Cadeia polipeptídica se dobra formando uma estrutura
compacta - diversas estruturas e funções
Grupos hidrofóbicos interior e hidrofílicos exterior –
pontes H com a água - solúveis
Diversidade estrutural
Mioglobina
Imunoglobulina
RUBISCO
Amilase salivar
Estrutura proteína esta relacionada com sua conformação
Conformação é em grande parte determinada pelas
interações fracas entre as cadeias laterais (R) dos
aminoácidos
Forças que possam influenciar forças mantem estrutura
das proteínas podendo mudar sua conformação
•
•
•
•
•
•
Aumento de temperatura;
Extremos de pH;
Solventes orgânicos miscíveis com a água (etanol e acetona);
Solutos (uréia); Sais (sulfato de amônio);
Exposição da proteína a detergentes;
Agitação mecânica vigorosa da solução proteica até formação
abundante de espuma.
Perda da estrutura tridimensional = desnaturação
Perda da conformação de uma proteína = perda função
e características (solubilidade)