Capítulo 7
NEUROFARMACOLOGIA
1- Anatomia e Organização do Sistema Nervoso Central
O SNC recebe, analisa e integra informações. É o local onde ocorre a tomada de decisões e o envio de
ordens. O SNP carrega informações dos órgãos sensoriais para o sistema nervoso central e do sistema nervoso
central para os órgãos efetores (músculos e glândulas).
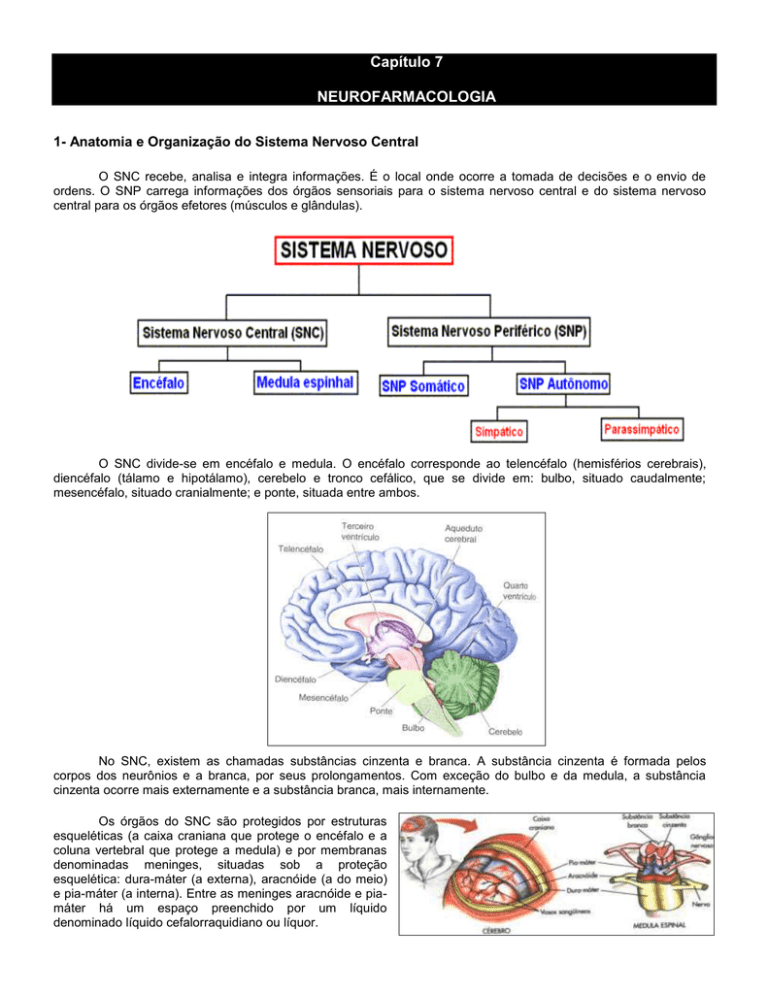
O SNC divide-se em encéfalo e medula. O encéfalo corresponde ao telencéfalo (hemisférios cerebrais),
diencéfalo (tálamo e hipotálamo), cerebelo e tronco cefálico, que se divide em: bulbo, situado caudalmente;
mesencéfalo, situado cranialmente; e ponte, situada entre ambos.
No SNC, existem as chamadas substâncias cinzenta e branca. A substância cinzenta é formada pelos
corpos dos neurônios e a branca, por seus prolongamentos. Com exceção do bulbo e da medula, a substância
cinzenta ocorre mais externamente e a substância branca, mais internamente.
Os órgãos do SNC são protegidos por estruturas
esqueléticas (a caixa craniana que protege o encéfalo e a
coluna vertebral que protege a medula) e por membranas
denominadas meninges, situadas sob a proteção
esquelética: dura-máter (a externa), aracnóide (a do meio)
e pia-máter (a interna). Entre as meninges aracnóide e piamáter há um espaço preenchido por um líquido
denominado líquido cefalorraquidiano ou líquor.
1.1- Telencéfalo
O encéfalo humano contém cerca de 35 bilhões de neurônios e pesa aproximadamente 1,4 kg. O telencéfalo
ou cérebro é dividido em dois hemisférios cerebrais bastante desenvolvidos. Nestes, situam-se as sedes da memória
e dos nervos sensitivos e motores. Entre os hemisférios, estão os ventrículos cerebrais (ventrículos laterais e terceiro
ventrículo); contamos ainda com um quarto ventrículo, localizado mais abaixo, ao nível do tronco encefálico. São
reservatórios do líquido céfalo-raquidiano, (líqüor), participando na nutrição, proteção e excreção do sistema
nervoso.
O córtex cerebral está dividido em mais de quarenta áreas funcionalmente distintas, sendo a maioria
pertencente ao chamado neocórtex. Cada uma das áreas do córtex cerebral controla uma atividade específica.
A região superficial do telencéfalo, que acomoda bilhões de corpos celulares de neurônios (substância
cinzenta), constitui o córtex cerebral. O córtex recobre um grande centro medular branco, formado por fibras axonais
(substância branca). Em meio a este centro branco (nas profundezas do telencéfalo), há agrupamentos de corpos
celulares neuronais que formam os núcleos (gânglios) da base, envolvidos em conjunto, no controle do movimento.
Parece que os gânglios da base participam também de um grande número de circuitos paralelos, sendo apenas
alguns poucos de função motora. Outros circuitos estão envolvidos em certos aspectos da memória e da função
cognitiva.
1.2- Diencéfalo (tálamo e hipotálamo)
Todas as mensagens sensoriais, com exceção das provenientes dos receptores do olfato, passam pelo
tálamo antes de atingir o córtex cerebral. Esta é uma região de substância cinzenta localizada entre o tronco
encefálico e o cérebro.
O tálamo atua como estação retransmissora de impulsos nervosos para o córtex cerebral. Ele é responsável
pela condução dos impulsos às regiões apropriadas do cérebro onde eles devem ser processados. O tálamo
também está relacionado com alterações no comportamento emocional; que decorre, não só da própria atividade,
mas também de conexões com outras estruturas do sistema límbico (que regula as emoções).
O hipotálamo, também constituído por substância cinzenta, é o principal centro integrador das atividades dos
órgãos viscerais, sendo um dos principais responsáveis pela homeostase corporal. Ele faz ligação entre o sistema
nervoso e o sistema endócrino, atuando na ativação de diversas glândulas endócrinas. É o hipotálamo que controla
a temperatura corporal, regula o apetite e o balanço de água no corpo, o sono e está envolvido na emoção e no
comportamento sexual.
1.3- Tronco Encefálico
O tronco encefálico interpõe-se entre a medula e o diencéfalo, situando-se ventralmente ao cerebelo. Possui
três funções gerais:
- Recebe informações sensitivas de estruturas cranianas e controla os músculos da cabeça;
- Contém circuitos nervosos que transmitem informações da medula espinhal até outras regiões encefálicas
e, em direção contrária, do encéfalo para a medula espinhal (lado esquerdo do cérebro controla os movimentos do
lado direito do corpo; lado direito de cérebro controla os movimentos do lado esquerdo do corpo);
- Regula a atenção, função esta que é mediada pela formação reticular (agregação mais ou menos difusa de
neurônios de tamanhos e tipos diferentes, separados por uma rede de fibras nervosas que ocupa a parte central do
tronco encefálico).
Na constituição do tronco encefálico entram corpos de neurônios que se agrupam em núcleos e fibras
nervosas, que, por sua vez, se agrupam em feixes denominados tratos, fascículos ou lemniscos. Estes elementos da
estrutura interna do tronco encefálico podem estar relacionados com relevos ou depressões de sua superfície.
Muitos dos núcleos do tronco encefálico recebem ou emitem fibras nervosas que entram na constituição dos nervos
cranianos. Dos 12 pares de nervos cranianos, 10 fazem conexão no tronco encefálico.
1.4- Cerebelo
O cerebelo está situado atrás do cérebro e é primariamente um centro para o controle dos movimentos
iniciados pelo córtex motor (possui extensivas conexões com o cérebro e a medula espinhal). Como o cérebro,
também está dividido em dois hemisférios. Porém, ao contrário dos hemisférios cerebrais, o lado esquerdo do
cerebelo está relacionado com os movimentos do lado esquerdo do corpo, enquanto o lado direito, com os
movimentos do lado direito do corpo.
O cerebelo recebe informações do córtex motor e dos gânglios basais de todos os estímulos enviados aos
músculos. A partir das informações do córtex motor sobre os movimentos musculares que pretende executar e de
informações proprioceptivas que recebe diretamente do corpo (articulações, músculos, áreas de pressão do corpo,
aparelho vestibular e olhos), avalia o movimento realmente executado. Após a comparação entre desempenho e
aquilo que se teve em vista realizar, estímulos corretivos são enviados de volta ao córtex para que o desempenho
real seja igual ao pretendido. Dessa forma, o cerebelo relaciona-se com os ajustes dos movimentos, equilíbrio,
postura e tônus muscular.
1.5- Neurônios
Nosso cérebro é composto por aproximadamente 100 bilhões de células nervosas, chamadas de neurônios.
Os neurônios têm a incrível habilidade de juntar e transmitir sinais eletroquímicos, como se fossem entradas, saídas e
fios de um computador. Os neurônios compartilham as mesmas características e têm as mesmas partes que as outras
células, mas o aspecto eletroquímico os deixa transmitir sinais por longas distâncias e passar mensagens de um para
o outro. Os neurônios possuem três partes básicas: corpo celular, axônio e dendritos.
Corpo celular: essa parte principal contém todos os componentes necessários da célula, como o núcleo (que
contém DNA), retículo endoplasmático e ribossomos (para construir proteínas) e mitocôndria (para produzir energia).
Se o corpo celular morrer, o neurônio morre.
Axônio: essa projeção da célula, longa e semelhante a um cabo, transporta a mensagem eletroquímica
(impulso nervoso ou potencial de ação) pela extensão da célula; dependendo do tipo do neurônio, os axônios podem
ser cobertos por uma fina camada de mielina, como um fio elétrico com isolamento. A mielina é feita de gordura e
ajuda a acelerar a transmissão de um impulso nervoso através de um axônio longo. Os neurônios com mielina
costumam ser encontrados nos nervos periféricos (neurônios sensoriais e motores), ao passo que os neurônios sem
mielina são encontrados no cérebro e na medula espinhal.
Dendritos ou terminações nervosas: essas projeções pequenas e semelhantes a galhos realizam as conexões
com outras células e permitem que o neurônio se comunique com outras células ou perceba o ambiente a seu redor.
Os dendritos podem se localizar em uma ou nas duas terminações da célula.
2- Ação dos Fármacos no SNC
No sistema nervoso central, assim como no periférico, o controle é exercido por meio de neurotransmissores.
Os neurotransmissores são substâncias liberadas pelo neurônio capaz de realizar a neurotransmissão, ou seja, a
transmissão do impulso de um neurônio a outro, resultando na sua excitação ou inibição.
Vários tipos de mediadores químicos podem operar no SNC, sendo os convencionais o glutamato, o GABA, a
noradrenalina, a dopamina, a 5-hidroxitriptamina e a acetilcolina.
Alguns fatores importantes na farmacologia do SNC devem ser considerados, tais como:
Os efeitos dos fármacos psicotrópicos levam semanas para ocorrer, o que sugere que sejam mais uma
resposta adaptativa do que os efeitos farmacodinâmicos imediatos do fármaco. É o que ocorre, por exemplo, com os
antidepressivos.
O desenvolvimento de dependência ocorre de forma gradual como ocorre, por exemplo, com o uso de
analgésicos opióides.
A existência da barreira hematoencefálica que permite a passagem apenas das pequenas moléculas apolares
através de difusão passiva ou facilitada. É o caso de alguns anti-histamínicos que tem efeitos centrais como a
sonolência.
3- Classificação dos Fármacos Psicotrópicos
A OMS, em 1967, determinou a seguinte classificação para os fármacos psicotrópicos:
Agentes anestésicos: fármacos usados para produzir anestesia cirúrgica como o propofol e o halotano.
Ansiolíticos e Sedativos: fármacos que causam sono e reduzem a ansiedade como os barbitúricos (Ex:
fenobarbital) e os benzodiazepínicos (Ex: diazepam).
Fármacos antipsicóticos: fármacos eficazes no alívio da esquizofrenia como a clorpromazina e o haloperidol.
Fármacos antidepressivos: fármacos usados para o tratamento da depressão como a amitriptilina e a
fluoxetina.
Fármacos analgésicos: fármacos usados para o controle da dor como os opióides (Ex: morfina) e a
carbamazepina.
Fármacos estimulantes psicomotores: fármacos que causam estado de alerta e euforia como as anfetaminas,
a cocaína e a cafeína.
Fármacos psicotomiméticos: fármacos que causam distúrbios da percepção (alucinações) e do
comportamento como a dietilamida do ácido lisérgico (LSD).
4- Neurotransmissores do SNC
Os principais neurotransmissores do SNC são o glutamato, o GABA, a noradrenalina, a dopamina, a 5hidroxitriptamina e a acetilcolina.
4.1- Glutamato
O Glutamato é amplamente distribuído no SNC de maneira uniforme. É derivado da glicose ou da glutamina
sintetizada pelas células gliais e armazenado em vesículas sinápticas, sendo, então, liberado por exocitose
dependente de Ca2+. O glutamato liberado é captado pelas células em troca com o Na +. Sua ação é encerrada pela
recaptação para os terminais nervosos e sua consequente conversão em glutamina.
Existem 4 tipos de receptores de glutamato:
Receptor NMDA: relacionado à potencialização e à depressão por longo prazo, alterações adaptativas e
patológicas de longo prazo no cérebro. Alguns fármacos como anestésicos e agentes psicotomiméticos agem
bloqueando seletivamente os canais operados pelos receptores NMDA.
Receptor AMPA: ocorre nos astrócitos e nos neurônios e são responsáveis pela transmissão excitatória rápida
e o seu bloqueio pode cessar a função cerebral.
Receptor de cainato: tem a mesma função dos receptores AMPA.
Receptor Metabotrópico: apresenta função na excitotoxicidade mediada pelo Glutamato.
O uso de antagonistas de Glutamato está relacionado à redução da lesão cerebral após um acidente vascular
ou trauma craniano e ao tratamento da epilepsia, da doença de Alzheimer e da esquizofrenia.
Hoje em dia, estão em uso clínico dois antagonistas de receptores NMDA: a Cetamina, usada para analgesia
e anestesia, e a Memantina, usada no tratamento da doença de Alzheimer.
4.2- Ácido -aminobutírico (GABA)
O GABA é o principal neurotransmissor inibitório no cérebro, onde está distribuído uniformemente. É formado
a partir do glutamato pela ação da descarboxilase de ácido glutâmico, uma enzima encontrada apenas nos neurônios
sintetizadores de GABA no cérebro. É destruído por uma reação catalisada pela enzima GABA-transaminase.
Os neurônios GABAérgicos captam o GABA através de transportadores específicos, sendo estes os
responsáveis por sua remoção após a liberação.
O GABA funciona como um neurotransmissor inibitório em muitas vias diferentes do SNC. Cerca de 20% dos
neurônios do SNC são GABAérgicos.
O GABA age em dois tipos de receptores distintos: GABAA e GABAB.
Os receptores GABAA são responsáveis pelos efeitos inibitórios lentos produzidos pelo GABA que se difunde
além do local de liberação. Esses receptores estão acoplados a canais de Cl -. A sua abertura leva ao aumento da
permeabilidade ao Cl-, o que hiperpolariza a célula, reduzindo, dessa forma, sua excitabilidade. Esses receptores são
o alvo para a ação de fármacos como os Benzodiazepínicos, os Barbitúrico e os Anestésicos Gerais. Nesses
receptores também atua o muscimol, um derivado de um cogumelo alucinógeno. Os benzodiazepínicos, por exemplo,
potencializam os efeitos do GABA nos receptores GABAA, promovendo as ações sedativas e ansiolíticas.
Os receptores GABAB exercem sua ação inibindo os canais de cálcio operados por voltagem e abrindo os
canais de potássio, reduzindo, assim a excitabilidade pós-sináptica. Alguns fármacos com atividade antagonista sobre
estes receptores tem demonstrado ação antiepiléptica, mas apenas em modelos animais. Já os agonistas como o
Baclofeno é usado nos casos de espasticidade.
4.3- Noradrenalina
A noradrenalina produz ações principalmente inibitórias sobe o SNC através de receptores , porém algumas
podem ser excitatórias. Acredita-se que ela desempenhe papel importante no estado de alerta e no de humor e
também na regulação central da pressão sanguínea. Segundo a hipótese das catecolaminas, a depressão resulta de
uma deficiência funcional da noradrenalina em certas partes do cérebro, enquanto a mania resulta do excesso desse
neurotransmissor. Entretanto, isso ainda permanece incerto, uma vez que achados subsequentes sugerem que a 5hidrotriptamina pode ser mais importante que a Noradrenalina em relação ao humor.
Como já foi visto, fármacos como a Clonidina e a Metildopa podem reduzir a descarga dos nervos simpáticos
do SNC, resultando em queda da pressão arterial.
Os fármacos psicotrópicos que agem na transmissão noradrenérgica no SNC incluem antidepressivos, a
cocaína e anfetaminas.
4.4- Dopamina
A dopamina constitui um dos mais importantes neurotransmissores do SNC, uma vez que está envolvida em
diversos distúrbios tais como a doença de Parkinson, a esquizofrenia, o déficit de atenção e até mesmo na
dependência aos fármacos.
A dopamina está presente no corpo estriado, no sistema motor extrapiramidal, no sistema límbico e no
hipotálamo. A sua síntese segue o mesmo caminho da síntese de noradrenalina, com a conversão de tirosina em
dopa e, em seguida, a conversão em dopamina. Após sua liberação na sinapse, a dopamina é recaptada por um
transportador específico e é metabolizada pela MAO e pela COMT.
Existem cinco tipos de receptores para a dopamina, designados por D1 a D5. Os receptores D1 são os mais
abundantes e estão presentes no corpo estriado, no sistema límbico e no hipotálamo. Os receptores D 2 estão
presentes na hipófise. Os receptores D3 ocorrem no sistema límbico apenas. Os receptores D4 tem fraca expressão
no córtex cerebral e no sistema límbico.
As funções das vias dopaminérgicas podem estar relacionadas ao controle motor, a efeitos comportamentais
e ao controle endócrino..
Controle motor: A atuação da dopamina no controle motor tem sido útil no tratamento de doenças como a de
Parkinson e como antipsicóticos. A doença de Parkinson é um distúrbio do controle motor associado à deficiência de
dopamina no SNC. Muitos fármacos antipsicóticos são antagonistas do receptor D 2, cujo maior efeito colateral é
causar distúrbios no movimento, provavelmente devido ao bloqueio desses receptores.
Efeitos comportamentais: O principal receptor dopaminérgico envolvido com os efeitos comportamentais é o
receptor D1. As anfetaminas, por exemplo, podem ativar esses receptores.
Controle endócrino: A via dopaminérgica presente na hipófise é também responsável pelo controle da
secreção de prolactina. Isso explica porque alguns fármacos antipsicóticos que bloqueiam receptores dopaminérgicos
pode aumentar a secreção de prolactina e levar ao desenvolvimento das mamas e a lactação, até mesmo no sexo
masculino. A dopamina também pode aumentar a produção do hormônio do crescimento.
Vômitos: A dopamina age na zona de gatilho quimiorreceptora, causando náuseas e vômitos. Por isso, a
metoclopramida que é um antagonista de dopamina é usada como antiemético.
4.5- Hidroxitriptamina ou Serotonina
A serotonina é sintetizada a partir do aminoácido essencial triptofano. Após a sua liberação na fenda sináptica,
pode ser recaptada e armazenada ou rapidamente inativada pela enzima monoamino-oxidase (MAO). Na glândula
pineal, a serotonina serve como precursor para a melatonina, um hormônio estimulador dos melanócitos.
A maior parte da serotonina é encontrada nas células enterocromafins do trato gastrointestinal. No sangue, é
encontrada nas plaquetas. E no Sistema Nervoso Central está presente nos neurônios serotonérgicos que participam
de várias funções como sono, regulação da temperatura, percepção dolorosa, humor, agressividade e regulação da
pressão sanguínea.
Os neurônios serotoninérgicos estão concentrados na ponte e no bulbo e projetam-se para o córtex cerebral,
o sistema límbico, o hipotálamo e medula espinhal.
Acredita-se que a serotonina está envolvida em condições como a depressão, ansiedade e enxaqueca. A
depressão, por exemplo, tem sido associada a um déficit de serotonina no sistema nervoso central. Por isso, muitos
antidepressivos atuam aumentando a sua concentração quer através da inibição de sua recaptação, quer através da
inibição de sua degradação pela MAO.
A serotonina não apresenta nenhuma aplicação clínica como medicamento.
A serotonina exerce várias ações e apresenta várias diferenças entre as espécies.
No sistema cardiovascular produz vasoconstrição, exceto nos músculos esquelético e cardíaco;
No trato gastrointestinal provoca aumento do peristaltismo;
No sistema nervoso central é um potente estimulante das terminações nervosas da dor e do prurido, sendo
responsável por alguns dos sintomas causados por lesões provocadas por insetos e plantas. Provoca comportamento
alucinatório, alterações de humor e das emoções, controle do sono, da temperatura corporal e da êmese.
4.6- Acetilcolina
A acetilcolina está amplamente distribuída no SNC. Certas doenças neurodegenerativas como a doença de
Parkinson e a demência estão associadas a anormalidades nas vias colinérgicas.
Os receptores nicotínicos medeiam os efeitos centrais da nicotina e os muscarínicos medeiam efeitos
comportamentais associados ao estado de alerta, ao aprendizado e à memória de curto prazo.
Exercícios de revisão de conteúdo:
1- Associe:
(A)- Telencéfalo
(B)- Diencéfalo
(C)- Cerebelo
(D)- Substância cinzenta
(E)- Substância branca
(F)- Hipotálamo
(
(
(
(
(
(
)- Fazem parte o tálamo e o hipotálamo.
)- Formada pelos prolongamentos dos neurônios.
)- Faz ligação entre o sistema nervoso e o sistema endócrino.
)- Formada pelos corpos dos neurônios.
)- Centro para o controle dos movimentos iniciados pelo córtex motor.
)- Corresponde aos hemisférios cerebrais.
2- Observe a figura abaixo:
a)- Que célula está representada na figura acima?
b)- Que partes da célula estão representadas pelas letras 2, 4 e 6?
c)- Qual dessas partes é considerada a mais importante por conter
a maioria das organelas celulares?
d)- Qual dessas partes é responsável pela condução do impulso
nervoso?
e)- Qual dessas partes é responsável pela síntese e liberação dos
neurotransmissores?
f)- O que representa o número 1 da figura acima?
g)- As estruturas representadas pelo número 3 são as mesmas
representadas por qual outro número na figura?
3- Por que dentre os psicotrópicos existe a hipótese de que seus efeitos sejam mais relacionados a uma resposta
adaptativa do que aos efeitos farmacodinâmicos imediatos do fármaco?
4- O que são fármacos antipsicóticos? Dê um exemplo:
5- Quais são os principais neurotransmissores do SNC?
6- Qual a utilidade clínica dos antagonistas de Glutamato?
7- Qual é o principal neurotransmissor inibitório do cérebro?
8- Qual são os tipos de receptores GABAérgicos?
9- Como age o GABA ao se ligar aos recepotores GABAérgicos do tipo A?
10- Que fármacos atuam sobre os receptores GABAA?
11- Como é a ação da Noradrenalina ao atuar sobre os receptores presentes no SNC?
12- O que diz a hipótese das catecolaminas em relação à etiopatogênese da depressão? Que teoria contrapõe-se a
essa hipótese?
13- A quais funções orgânicas as vias dopaminérgicas podem estar relacionadas?
14- Por que a dopamina pode ser útil no tratamento da doença de Parkinson?
15- Como age a metoclopramida no controle do vômito?
16- Descreva a síntese, a liberação e a inativação da serotonina:
17- Em que partes do organismo a serotonina pode ser encontrada?
18- Qual a relação entre a serotonina e a depressão?
Texto complementar:
Os Receptores de Glutamato
Capítulo 8
FÁRMACOS ANSIOLÍTICOS E HIPNÓTICOS
1- Ansiedade
A ansiedade refere-se à antecipação de reações como comportamentos defensivos, reflexos autonômicos,
despertar e alerta, secreção de corticosteróides e emoções negativas. Entretanto, é muito difícil distinguir a ansiedade
patológica da ansiedade normal. Tal distinção não é completamente nítida, mas está relacionada ao ponto em que os
sintomas interferem nas atividades normais do indivíduo, prejudicando-o.
O uso de fármacos ansiolíticos tem se tornado cada vez menos freqüente devido ao seu benefício incerto e a
existência de riscos definidos.
Clinicamente, a ansiedade pode se manifestar através de transtornos, dentre os quais, os mais importantes
são:
Transtorno de ansiedade generalizada: caracterizado por uma ansiedade excessiva sem razão ou foco.
Transtorno do pânico: caracterizado por crises súbitas de medo incontrolável associadas a sintomas como
sudorese, taquicardia, dor no peito, tremores e sensação de asfixia.
Fobias: caracterizadas por medos intensos de objetos ou situações específicas.
Transtorno do estresse pós-traumático: caracterizado por uma ansiedade desencadeada por lembranças de
experiências estressantes passadas.
Transtorno obsessivo-compulsivo: caracterizado por comportamento com rituais compulsivos dominado por
ansiedade irracional.
O tratamento da ansiedade é feito com a associação de abordagens psicológicas e medicamentos, dentre os
quais podem ser utilizados ansiolíticos, antidepressivos e antipsicóticos.
Os fármacos ansiolíticos estão classificados em diversos grupos de acordo com o seu mecanismo de ação.
Assim, temos a seguinte classificação:
1- Benzodiazepínicos: é o grupo mais importante.
2- Antagonistas de receptores 5-HT: o fármaco desse grupo é a buspirona.
3- Antagonistas de receptores -adrenérgicos: o melhor exemplo é o propranolol.
4- Barbitúricos: hoje não mais utilizados como ansiolíticos, mas apenas como anestésicos e anticonvulsivantes.
5- Fármacos variados: grupo que inclui o zolpidem, os anti-histamínicos sedativos, etc.
Neste capítulo, apenas os Benzodiazepínicos serão abordados em virtude de sua importância como fármacos
mais utilizados como ansiolíticos e hipnóticos.
2- Benzodiazepínicos
O primeiro benzodiazepínico surgiu em 1961 através de uma síntese acidental que gerou o Clordiazepóxido.
Esses fármacos são agrupados num só grupo por terem uma estrutura química comum, composta por um anel de
sete elementos fundido com um anel aromático com 4 grupos substituintes principais.
Entre os fármacos do grupo, pode-se estabelecer uma subdivisão baseada na duração total da ação
farmacológica, da seguinte forma:
- Benzodiazepínicos de ação ultracurta: a duração da ação é menor que 6 horas.
- Benzodiazepínicos de ação curta: a duração da ação varia de 12 a 18 horas.
- Benzodiazepínicos de ação média: com duração de ação em torno de 24 horas.
- Benzodiazepínicos de ação longa: com duração de ação entre 24 e 48 horas.
2.1- Fármacos Benzodiazepínicos
Os principais fármacos desse grupo são:
Midazolam: hipnótico usado como anestésico IV de ação ultracurta.
Lorazepam: ansiolítico e hipnótico de ação curta.
Alprazolam: ansiolítico e antidepressivo de ação média.
Nitrazepam: ansiolítico e hipnótico de ação média.
Diazepam: ansiolítico, relaxante muscular e anticonvulsivante (por via IV) de ação longa.
Clordiazepóxido: ansiolítico e relaxante muscular de ação longa.
Flurazepam: ansiolítico de ação longa.
Clonazepam: anticonvulsivante e ansiolítico de ação longa. Tem pouco efeito sedativo.
2.2- Mecanismo de Ação
Os benzodiazepínicos se ligam seletivamente a receptores GABA A que medeiam a transmissão sináptica
inibitória no SNC. Assim, esses fármacos intensificam a resposta ao GABA, promovendo a abertura dos canais de
cloreto ativados pelo GABA.
O receptor GABA corresponde a um canal iônico que consiste em uma montagem pentamérica de diferentes
subunidades, dentre as quais as mais importantes são a , a e a , cada uma das quais ocorrendo em três
isoformas (1, 2 e 3). As várias combinações das subunidades constituintes do receptor GABA ocorrem em diferentes
partes do cérebro.
Os estudos mais recentes correlacionam a atividade desempenhada pelo fármaco benzodiazepínico à
subunidade ligante no receptor GABA. Assim, os receptores GABAA contendo a subunidade 1 são os responsáveis
pelos efeitos sedativos, amnésicos e anticonvulsivantes dos Benzodiazepínicos. Os receptores contendo a
subunidade 2 respondem pelos efeitos ansiolíticos e de relaxante muscular dos Benzodiazepínicos. Isso sugere que
a seletividade para uma ou outra subunidade dos receptores GABAA pode resultar em fármacos com menores efeitos
adversos.
2.3- Efeitos e Usos Clínicos dos Benzodiazepínicos
Os principais efeitos farmacológicos dos Benzodiazepínicos são:
2.3.1- Redução da ansiedade e da agressividade
A utilização de benzodiazepínicos tem sido cada vez mais substituída pelos barbitúricos para reduzir a estado
de ansiedade.
2.3.2- Sedação e indução do sono
Os benzodiazepínicos podem reduzir o tempo em que se leva para dormir e aumentar a duração total do
sono, embora esse efeito só ocorra em indivíduos que normalmente dormem menos de 6 horas por noite. Esses
efeitos, entretanto, tendem a declinar quando os benzodiazepínicos são administrados regularmente por 1 a 2
semanas.
2.3.3- Redução do tônus muscular e da coordenação
Os benzodiazepínicos reduzem o tônus muscular por sua ação no sistema nervoso central, podendo reduzir o
desempenho em atividades físicas. Entretanto, esse efeito relaxante sobre os músculos pode ser clinicamente útil em
estados de ansiedade que ocasionam dores musculares e cefaléia.
2.3.4- Efeito anticonvulsivante
Todos os benzodiazepínicos apresentam em diferentes níveis atividade anticonvulsivante em testes com
animais. Por isso, o clonazepam é usado para tratamento da epilepsia e o diazepam pode ser usado por via IV para
controlar crises convulsivas que coloquem a vida em risco no estado do mal epiléptico.
2.3.5- Amnésia anterógrada
Os benzodiazepínicos podem comprometer a memória de eventos ocorrentes enquanto sob sua influência.
Esse efeito tem sido utilizado em casos de procedimentos cirúrgicos menores para não deixar lembranças
desagradáveis.
2.4- Farmacocinética
Os benzodiazepínicos, em geral, são bem absorvidos pela via oral, exceto o Lorazepam que apresenta
absorção lenta. Ligam-se fortemente às proteínas plasmáticas. Apresentam alta lipossolubilidade, o que pode acarreta
acúmulo gradual com o uso frequente no tecido adiposo.
Por via Intravenosa, o Diazepam pode ser útil nas crises convulsivas do mal epiléptico e o Midazolam em
anestesia.
A eliminação dos benzodiazepínicos é principalmente através da urina.
2.5- Efeitos Adversos
Os efeitos adversos relacionados aos benzodiazepínicos estão relacionados a efeitos tóxicos decorrentes da
superdosagem, a efeitos adversos durante o uso terapêutico normal, à tolerância e à dependência.
2.5.1- Efeitos tóxicos decorrentes da superdosagem aguda:
Dentre os fármacos ansiolíticos e hipnóticos, os benzodiazepínicos são os menos perigosos em casos de
superdosagem. Nesses casos, causam sono prolongado sem depressão grave da respiração ou da função
cardiovascular. Entretanto, na presença de outros depressores do sistema nervoso central como o álcool, por
exemplo, os benzodiazepínicos podem causar depressão respiratória grave ou morte.
Para os casos de superdosagem, o antídoto é o Flumazenil, um antagonista dos receptores GABA.
2.5.2- Efeitos adversos durante o uso terapêutico normal
Os principais efeitos adversos relacionados ao uso de benzodiazepínicos incluem sonolência, confusão,
amnésia e comprometimento da coordenação. Os benzodiazepínicos intensificam os efeitos depressores do álcool e
de outros fármacos.
2.5.3- Tolerância
A tolerância a um determinado fármaco refere-se à necessidade de doses progressivas necessárias para
produzir o efeito procurado e pode ocorrer com todos os benzodiazepínicos. Entretanto, a tolerância com
benzodiazepínicos é menor do que a observada com os barbitúricos.
Essa tolerância parece estar relacionada à mudança nos receptores GABA, mas o mecanismo não está
totalmente esclarecido.
2.5.4- Dependência
A suspensão do tratamento depois de meses de uso de benzodiazepínicos pode causar aumento dos
sintomas da ansiedade como tremores e tonturas (síndrome de abstinência).
Exercícios de revisão de conteúdo
1- Defina ansiedade? Como ela pode ser distinta entre o estado patológico e o normal?
2- Através de que transtornos a ansiedade pode se manifestar?
3-Quais são os 3 principais grupos de fármacos ansiolíticos? Dê um exemplo de cada:
4- Associe o fármaco a uma de suas características farmacológicas:
(A)- Midazolam
( )- Ansiolítico e hipnótico de ação curta.
(B)- Alprazolam
( )- Anticonvulsivante (por via IV) de ação longa.
(C)- Diazepam
( )- Tem pouco efeito sedativo.
(D)- Lorazepam
( )- Hipnótico usado como anestésico IV de ação ultracurta.
(E)- Clonazepam
( )- Antidepressivo de ação média.
5- Baseado no mecanismo de ação, explique como os benzodiazepínicos podem exercer efeitos depressores como a
sonolência e o efeito ansiolítico sobre o SNC:
6- Quais são os principais efeitos dos benzodiazepínicos que podem ser aplicados na clínica médica?
7- Por que o uso frequente de benziazepínicos pode acarretar o seu acúmulo gradual no tecido adiposo?
8- Qual é o principal efeito tóxico relacionado à superdosagem com benzodiazepínicos?
9- Por que a interação entre benzodiazepínicos e álcool pode ser perigosa?
10- Quais são os principais efeitos adversos durante o uso terapêutico normal de benzodiazepínicos?
11- O que é a tolerância?
12- O que é a dependência? Como ela se manifesta em relação aos benzodiazepínicos?
Capítulo 9
ANTIDEPRESSIVOS
1- Depressão
A depressão é uma afecção caracterizada por distúrbios do humor podendo variar de leve a grave (psicótica).
É um dos distúrbios afetivos mais comuns.
Os sintomas da depressão incluem componentes emocionais e biológicos, dentre eles infelicidade, apatia,
pessimismo, baixa auto-estima, sentimentos de culpa, inadequação, sentimento de inferioridade, indecisão, perda da
motivação, retardo do pensamento e da ação, perda de libido, distúrbio do sono e perda de apetite.
A depressão pode ser distinta em dois tipos:
A depressão unipolar com oscilações de humor sempre na mesma direção, geralmente associada ao
estresse, ansiedade e agitação, e a bipolar com alternância entre a depressão e a mania. A mania é caracterizada por
entusiasmo, autoconfiança excessivas, reações impulsivas, irritabilidade, impaciência, agressividade e delírios de
grandeza. Aparece no início da vida adulta e tem forte tendência genética.
O advento de medicamentos antidepressivos tornou a depressão um problema médico, passível de
tratamento. Nas últimas cinco décadas, a psicofarmacologia da depressão evoluiu muito e rapidamente. Os
primeiros antidepressivos, os antidepressivos tricíclicos (ADTs) e os inibidores da monaminooxidase (IMAOs), foram
descobertos através da observação clínica. Os ADTs apresentavam boa eficácia devido à sua ação, aumentando a
disponibilidade de norepinefrina e serotonina. Seu uso foi limitado em função do bloqueio de receptores de
histamina, colinérgicos e alfa-adrenérgicos que acarretavam efeitos colaterais levando à baixa tolerabilidade e risco
de toxicidade. Da mesma forma, o uso dos IMAOs ficou comprometido em função do risco de crises hipertensivas
potencialmente fatais. A nova geração de antidepressivos é constituída por medicamentos que agem em um único
neurotransmissor (como os inibidores seletivos de recaptação de serotonina ou de noradrenalina) ou em múltiplos
neurotransmissores/receptores, como venlafaxina, bupropion, trazodona, nefazodona e mirtazapina, sem ter como
alvo outros sítios receptores cerebrais não relacionados com a depressão (tais como histamina e acetilcolina).
2- Teoria Bioquímica da Depressão
A depressão é causada por um déficit funcional de neurotransmissores monoaminas em certas áreas
cerebrais. Evidências farmacológicas sugerem que a principal monoamina relacionada à depressão seja a 5Hidroxitriptamina (5-HT) ou Serotonina. Outras sugerem ser a noradrenalina o principal neurotransmissor envolvido.
As evidências farmacológicas não possibilitam uma distinção clara a ser feita entre as teorias da noradrenalina
e da 5-HT para a depressão. Clinicamente parece que os inibidores da recaptura da noradrenalina e da recaptura da
5-HT são igualmente eficazes como antidepressivos, embora pacientes individuais possam responder melhor.
As principais evidências farmacológicas que respaldem a hipótese das monoaminas são:
Antidepressivos que bloqueiam a captação de 5-HT e Noradrenalina melhoram o humor;
Antidepressivos que inibem a MAO aumentam os depósitos de NA e 5-HT, melhorando o humor;
Aminoácidos como o triptofano levam ao aumento na síntese de 5-HT e melhoram o humor;
Metildopa inibe a síntese de NA e pioram o humor;
A eletroconvulsoterapia aumenta as respostas do SNC à NA e à 5-HT, melhorando o humor.
3- Antidepressivos
O antidepressivo é uma substância considerada eficaz na remissão de sintomas característicos da síndrome
depressiva, em pelo menos um grupo de pacientes com transtorno depressivo. Algumas substâncias com atividade
antidepressiva podem ser eficazes também em transtornos psicóticos.
Os antidepressivos podem ser classificados de acordo com a estrutura química ou as propriedades
farmacológicas. Atualmente os antidepressivos, preferencialmente, são classificados em função da ação
farmacológica, mais útil na prática clínica porque os antidepressivos de nova geração não compartilham estruturas
comuns.
4- Classificação dos Antidepressivos
A)- Inibidores da captação de monoaminas:
Nesta classe encontra-se uma subdivisão de acordo com a seletividade para o neurotransmissor:
Antidepressivos Tricíclicos: a maioria dos antidepressivos tricíclicos são inibidores não seletivos da captação
de aminas. Inibem a captação de Noradrenalina e 5-Hidrotriptamina. Ex: Imipramina, Amitriptilina e Clomipramina (não
seletivos); Desipramina (seletivo para Noradrenalina) e Nortriptilina (levemente seletivo para Noradrenalina).
Outros Inibidores não seletivos da captação de Noradrenalina/5-hidroxitriptamina. Ex: Venlafaxina e
Duloxetina e Bupropiona.
Inibidores seletivos da captação de Noradrenalina. Ex: Maprotilina, Reboxetina e Fenelzina.
Inibidores seletivos da Captação de 5-Hidroxitriptamina. Ex: fármacos altamente seletivos como Fluoxetina,
Paroxetina, Fluvoxamina, Citalopram e Sertralina.
B)- Inibidores da Monoaminaoxidase (IMAO):
→ Não seletivos para a enzima (MAO-A e MAO-B): Fenelzina, Tranilcipromina (inibidor irreversível) e
Isocarboxazida.
→ Seletivos para MAO-A: Moclobemida (inibidor reversível).
C)- Antidepressivos atípicos:
→ Trazodona: inibe fracamente a captação de 5-HT, bloqueia receptores 5HT 2 e H1 e aumenta a liberação de
Noradrenalina e 5-HT.
→ Mirtazapina: bloqueia receptores α2, 5-HT2 e 5-HT3.
Todos os antidepressivos levam pelo menos duas semanas para produzir efeitos benéficos, embora seus
efeitos farmacológicos sejam produzidos imediatamente, o que mostra a importância das alterações adaptativas
secundárias.
5- Antidepressivos Tricíclicos
Os principais fármacos representantes da classe dos antidepressivos tricíclicos são Imipramina,
Clomipramina, Amitriptilina, Desipramina e Nortriptilina.
Esses fármacos são utilizados para tratar a depressão endógena moderada a grave com insônia por terem
efeito sedativo (amitriptilina, por exemplo) e para os transtornos de pânico, obsessivos e de fobia (Clomipramina, por
exemplo).
5.1- Mecanismo de Ação
O mecanismo de ação comum aos antidepressivos tricíclicos em nível pré-sináptico é o bloqueio de recaptura
de monoaminas, principalmente noradrenalina (NA) e 5-hidroxitriptamina (5-HT), em menor proporção dopamina (DA),
por competição pelo sítio de ligação do transportador de aminas.
Outras ações dos antidepressivos tricíclicos incluem efeito anticolinérgico periférico e central devido à
potente e elevada afinidade de ligação por receptores muscarínicos, bloqueando-os; efeito sedativo pela forte
afinidade de ligação por receptores histamina H1 e hipotensão ortostática devida a bloqueio 2-adrenérgico. Essas
ações não se correlacionam necessariamente com efeito antidepressivo, mas com efeitos colaterais. O bloqueio do
receptor 5-HT1 contribui para o efeito terapêutico.
5.2- Farmacocinética
Os antidepressivos tricíclicos tem rápida e ampla absorção por via oral. Liga-se 90 a 95% às proteínas
plasmáticas. Sofre metabolismo hepático através de conjugação com o ácido glicurônico. É eliminado através da urina
e tem meia-vidas que variam de 10 a 80 horas.
O início da ação desses fármacos é lenta, de forma que o tratamento deve ser pelo menos 4 a 6 semanas
antes de se concluir que um fármaco não tem efeito. O tratamento deve também continuar por pelo menos 4 meses
após a remissão dos sintomas da depressão . E a sua retirada deve ser gradual durante várias semanas.
5.3- Efeitos Adversos
Nos primeiros dias de tratamento podem ocorrer sedação devido ao bloqueio de receptores H1, confusão
mental e falta de coordenação motora. A fraqueza e a fadiga são atribuíveis aos efeitos centrais dos antidepressivos
tricíclicos, que produzem efeitos anti-histamínicos centrais potentes. Outro efeito no SNC é o risco variável de
desenvolver confusão ou delírio.
Os antidepressivos tricíclicos frequentemente causam respostas autônomas adversas, em parte relacionadas
com seus efeitos antimuscarínicos relativamente potentes. Isso inclui boca seca e gosto metálico ou ácido,
desconforto apigástrico, constipação, tontura, taquicardia, palpitações, visão embaçada e retenção urinária.
E ainda hipotensão postural por bloqueio de receptores -adrenérgicos, além de aumentar o risco de morte
súbita cardíaca.
Em casos de superdosagem, os antidepressivos tricíclicos podem provocar cardiotoxicidade manifestada por
arritmias ventriculares, excitação, delírio, sonolência grave, alucinações, inquietação ou agitação, convulsões, coma e
depressão respiratória.
5.4- Interações Medicamentosas
As principais interações medicamentosas estão relacionadas à potencialização os efeitos do álcool e de
anestésicos, podendo levar à depressão respiratória grave e morte. Além disso, interferem na ação dos antihipertensivos.
A ligação dos antidepressivos tricíclicos a albumina plasmática pode ser reduzida pela competição com alguns
fármacos, inclusive a fenitoina, AAS, aminopirina, escopolamina e fenotiazinas.
Os barbitúricos e alguns agentes anticonvulsivantes (principalmente carbamazepina), assim com o tabagismo,
podem acelerar o metabolismo hepático dos antidepressivos por meio da indução das CYP.
Os antidepressivos potencializam os efeitos do álcool e provavelmente dos outros sedativos. A atividade
anticolinérgica dos antidepressivos tricíclicos pode somar-se aos efeitos dos agentes usados para tratar doença de
Parkinson, dos agentes antipsicóticos de baixa potência, ou de outros compostos que tem atividade antimuscarinica e
produz efeitos tóxicos. Os antidepressivos tricíclicos têm interações importantes e potencialmente perigosas com as
aminas biogênicas como a norepinefrina, que normalmente é removida do seu local de ação pela recaptação
neuronial.
6- Outros inibidores não seletivos da Captação de monoaminas
Esses fármacos inibem a captação de 5-hidroxitriptamina e noradrenalina. Os principais representantes são
Venlafaxina e Duloxetina.
A venlafaxina não apresenta afinidade por receptores adrenérgicos 1, receptores muscarínicos ou
histamínicos e também não inibe a monoamino-oxidase. Sua potência na inibição da recaptação de serotonina é
superior à da recaptação de noradrenalina. É rapidamente absorvida, sua biodisponibinidade é de 45%, e a ingestão
com alimentos retarda, porém não compromete sua absorção.
Os efeitos colaterais mais freqüentemente relatados com o uso da venlafaxina são: náuseas, tonturas,
sonolência, hipertensão, sudorese abundante e tremores. Podem ser relatados diminuição da libido, anorgasmia,
retardo ejaculatório e impotência.
Tais fármacos apresentam menor risco de efeitos cardíacos, sendo mais seguros em superdosagem que os
antidepressivos tricíclicos.
7- Inibidores Seletivos da Captação de 5-Hidroxitriptamina (ISRS)
Os principais fármacos desse grupo são Fluoxetina, Paroxetina, Fluvoxamina, Citalopram e Sertralina.
Esses fármacos são atualmente os mais prescritos no tratamento.
Suas vantagens em relação aos demais antidepressivos são:
São mais seletivos em relação à captação da 5-Hidroxitriptamina do que em relação à Noradrenalina;
Oferecem menor probabilidade de causar efeitos colaterais anticolinérgicos em comparação com os
antidepressivos tricíclicos;
São menos perigosos em superdosagem em comparação com os tricíclicos;
Não causam “reação ao queijo”, diferentemente dos inibidores da MAO;
Na depressão moderada, têm a mesma eficácia que os antidepressivos tricíclicos e os Inibidores da MAO;
São úteis no tratamento do transtorno obsessivo-compulsivo.
Sua desvantagem está relacionada ao fato de serem menos eficazes que os tricíclicos para tratar depressão
intensa.
7.1- Mecanismo de Ação
Os ISRSs inibem de forma potente e seletiva a recaptação de serotonina, resultando em potencialização da
neurotransmissão serotonérgica. A potência da inibição de recaptação da serotonina é variada, assim como a
seletividade por noradrenalina e dopamina. Sertralina e paroxetina são os mais potentes inibidores de recaptação.
7.2- Usos Clínicos
Esses fármacos são utilizados no tratamento de depressão, transtornos de ansiedade, crises de pânico e
transtorno obsessivo-compulsivo.
7.3- Farmacocinética
Os inibidores seletivos da captação de 5-HT apresentam boa absorção por via oral. Todos os ISRSs
apresentam alta ligação protéica. Suas meias-vidas plasmáticas ocorrem entre 15 e 24 horas, exceto a Fluoxetina que
tem meia-vida de 24 a 96 horas. O efeito terapêutico ocorre após 2 a 4 semanas de início do tratamento.
Metabolizados primariamente pelo fígado, todos os ISRSs afetam as enzimas metabolizadoras do citocromo
P-450 (em menor proporção sertralina) e podem comprometer o metabolismo de outras drogas metabolizadas por
este sistema. Assim, a paroxetina e a fluoxetina são inibidores enzimáticos e podem, por isso, inibir o metabolismo
hepático dos antidepressivos tricíclicos, levando ao risco de aumentar a sua toxicidade. Portanto, tal associação não
deve ser usada no tratamento da depressão.
7.4- Efeitos Adversos
Em função de sua ação seletiva, apresentam perfil mais tolerável de efeitos colaterais. Os efeitos mais
comuns desses fármacos são náuseas, vômitos, dor abdominal, diarréia, anorexia, insônia, agitação, ansiedade,
insônia, mania, nervosismo, tremores, perda ou ganho de peso, perda da libido e incapacidade de ter orgasmo.
Em combinação com os Inibidores da MAO, podem ocasionar a síndrome da serotonina, caracterizada por
tremor, hipertermia, diarréia, febre, confusão, hipomania, agitação, colapso cardiovascular e morte.
Outros efeitos incluem o aumento da agressividade e de idéias suicidas, sobretudo na faixa etária até 18 anos.
8- Inibidor Seletivo de Recaptação de Norepinefrina
A reboxetina é o primeiro composto comercializado de uma nova classe de antidepressivos, os inibidores da
recaptação de noradrenalina. Apresenta atividade seletiva sobre a recaptação de noradrenalina, com atividade
antagonista 2. Não possui efeitos significativos sobre receptores colinérgicos, histamínicos, 1-adrenérgicos, ou na
inibição da monoaminoxidase.
A reboxetina é absorvida pelo trato gastrintestinal, apresenta alta ligação às proteínas plasmáticas. Atinge
pico plasmático em 1,5 a 2,5 horas. Sofre metabolização hepática, entretanto, não interage com isoenzimas do
sistema citocromo P450. Sua meia-vida é de cerca de 12 a 13 horas e a eliminação se dá pela urina (76% na forma
inalterada e metabólitos) e fezes (7% a 16%).
Os efeitos colaterais mais significativos da reboxetina são: taquicardia, impotência, retenção urinária, insônia,
sudorese excessiva, constipação intestinal e boca seca.
9- Inibidores da Monoaminooxidade (IMAO)
Nesse grupo, encontram-se fármacos sem seletividade, atuando igualmente sobre a MAO-A e MAO-B e os
seletivos para a MAO-A. Fenelzina, Tranilcipromina e Iproniazida são fármacos não seletivos que se ligam de forma
irreversível às MAOs A e B. A moclobemida é um antidepressivo inibidor seletivo da MAO-A e reversível, ao passo
que inibidores seletivos da MAO-B, como a selegilina, não possuem ação antidepressiva significativa.
9.1- Mecanismo de Ação
Os IMAOs promovem inibição prolongada e indistinta da Monoaminooxidase, ou seja, inibição das duas
principais isoenzimas.
A MAO é uma enzima encontrada em quase todos os tecidos do corpo sob duas formas moleculares
semelhantes (isoenzimas), a MAO-A e a MAO-B.
A MAO-A tem como principal substrato a 5-Hidroxitriptamina sendo, portanto, o principal alvo dos
antidepressivos IMAOs, mas pode agir também sobre a Noradrenalina e a Dopamina. A MAO-B tem como principal
substrato a feniletilamina, mas pode agir também sobre a Noradrenalina e a Dopamina. É inibida seletivamente pela
Selegilina, usada no tratamento do mal de Parkinson.
É importante ressaltar que a MAO atua dentro das terminações nervosas, regulando a concentração
intraneuronal livre de Noradrenalina e 5-Hidroxitriptamina e, portanto, os depósitos reguláveis desses
neurotransmissores. Não está envolvida com a inativação do neurotransmissor liberado.
Os IMAOs ligam-se covalentemente à enzima, inativando-a por tempo prolongado. A enzima tem sua
atividade recuperada somente após várias semanas. A redução na atividade da MAO resulta em aumento na
concentração desses neurotransmissores nos locais de armazenamento no sistema nervoso central (SNC) e no
sistema nervoso simpático. O incremento na disponibilidade de um ou mais neurotransmissores tem sido relacionado
à ação antidepressiva dos IMAOs.
9.2- Farmacocinética
Os IMAOs são bem absorvidos pelo trato gastrintestinal, sofrem biotransformação hepática rápida por
oxidação e possivelmente têm metabólitos ativos. O início de ação se dá entre 7 a 10 dias com doses apropriadas em
alguns pacientes, mas pode levar de 4 a 8 semanas para atingir o efeito terapêutico pleno.
Em média são necessários 10 dias para que a atividade da MAO se recupere, já que em 5 a 10 dias os IMAOs
irreversíveis inibem as MAOs A e B de forma permanente. Elas voltam a ser produzidas em uma a duas semanas,
mas nesta fase o paciente continua vulnerável ao desencadeamento de crises hipertensivas pelo aumento da
concentração de aminas provenientes da dieta ou de medicamentos aminérgicos.
9.3- Efeitos Farmacológicos
Os efeitos primários dos IMAOs estão relacionados ao rápido aumento dos níveis de 5-Hidroxitriptamina,
Noradrenalina e Dopamina, sendo a 5-HT mais afetada e a Dopamina, menos. Entretanto, os IMAOs não aumentam a
resposta dos órgãos à estimulação nervosa simpática como ocorre com os antidepressivos Tricíclicos.
Os IMAOs causam aumento imediato da atividade motora e desenvolvem euforia e excitação durante alguns
dias.
9.4- Efeitos Adversos
Os principais efeitos adversos dos IMAOs são:
Por bloqueio no sistema nervoso simpático causam hipotensão postural grave (vertigens e tonturas,
especialmente ao levantar; podem ocorrer quedas);
Estimulação central excessiva com tremores, excitação e insônia;
Aumento do apetite, levando ao ganho de peso;
Efeitos antimuscarínicos menores que os Tricíclicos: boca seca, visão embaçada, retenção urinária,
constipação, etc;
Neurotoxicidade;
Fenelzina e Iproniazida causam hepatotoxicidade.
Em casos de superdosagem podem causar convulsões.
Alguns estudos têm sugerido que os antidepressivos podem aumentar o risco de suicídio em pacientes
depressivos, sobretudo nas primeiras semanas de tratamento.
Os IMAOs são muito menos usados que outros antidepressivos devido aos efeitos adversos que produzem e
às graves interações que ocorrem com seu uso.
9.5- Interações com Alimentos
Em relação aos IMAOs é bastante comum a “reação ao queijo”. A tiramina presente em alimentos como
queijos, cerveja, vinhos, soja, etc. é normalmente metabolizada pela MAO na parede do intestino e no fígado, de
forma que apenas uma pequena quantidade chega à corrente sanguínea. A inibição da MAO promovida por esses
antidepressivos resulta em absorção maior de tiramina que, nas terminações nervosas, podem favorecer o
deslocamento de Noradrenalina, acarretando efeitos nervosos simpáticos. O resultado é uma hipertensão aguda com
cefaléia latejante intensa e, ocasionalmente, hemorragia intracraniana.
10- Antidepressivos Atípicos
10.1- Trazodona
O mecanismo de ação da trazodona envolve a inibição da recaptação de serotonina e noradrenalina.
Apresenta atividade antagonista de receptores 1-adrenérgicos e anti-histamínicos, mais relacionadas aos seus
efeitos colaterais.
A trazodona é bem absorvida pelo trato gastrintestinal e se ingerida às refeições, ou imediatamente após,
pode haver aumento na quantidade absorvida. Em geral os picos plasmáticos são atingidos em duas horas.
Apresenta alta ligação proteica (cerca de 90%) e sofre hidroxilação hepática. Sua meia-vida é de 6 a 11 horas. A
eliminação é renal (75%) e biliar (20%).
Os efeitos colaterais mais freqüentes da trazodona são: sedação, hipotensão ortostática, tonturas, cefaléia,
náuseas, boca seca. Reações alérgicas e irritação gástrica podem aparecer.
10.2- Mirtazapina
A ação da mirtazapina se dá através do aumento da atividade noradrenérgica e serotonérgica central. A
mirtazapina é um antagonista de receptores 2-adrenérgicos e antagonista 5-HT pós-sináptico. Sua afinidade pelos
receptores histamínicos H1 explica o efeito sedativo. Apresenta fraca atividade por receptores muscarínicos e
dopaminérgicos.
A mirtazapina é bem absorvida pelo trato gastrintestinal, porém devido ao metabolismo de primeira
passagem sua biodisponibilidade é de 50%. Apresenta alta ligação a proteínas plasmáticas (85%). Os picos
plasmáticos são atingidos em cerca de duas horas e o estado de equilíbrio em cinco dias. Sofre metabolização
hepática e seus metabólitos são ativos e eliminados na urina (75%) e nas fezes (15%).
Os efeitos colaterais mais freqüentemente relatados são: sedação excessiva, ganho de peso, boca seca,
edema, constipação intestinal, dispnéia.
11- Estabilizadores de Humor
A ação dos estabilizadores de humor consiste em controlar as oscilações de humor características da doença
maníaco depressiva, também conhecida como transtorno bipolar.
Os principais fármacos utilizados nesse sentido são o Lítio e os antiepilépticos como Carbamazepina,
Valproato e Gabapentina, bloqueadores dos canais de sódio.
O tratamento com tais fármacos é longo e seus efeitos benéficos leva de 3 a 4 semanas para desenvolver-se.
11.1- Lítio
O Lítio é clinicamente eficaz em concentrações plasmáticas de 0,5 a 1,0 mmol/L; acima de 1,5 mmol/L
ocorrem seus efeitos tóxicos, e uma dose de 3 a 5 mmol/L é capaz de levar o paciente à morte. Isso mostra que o
fármaco tem uma estreita janela terapêutica, necessitando, com o seu uso, de um monitoramento frequente.
O lítio, por ser um cátion monovalente, pode simular o papel do Na + em tecidos excitáveis, por ser capaz de
permear os canais de Na+ controlados por voltagem e responsáveis pela geração do potencial de ação. Entretanto, a
Na+K+ATPase não tem afinidade pelo lítio, de forma que ele não é bombeado para fora da célula, podendo se
acumular dentro da mesma. Consequentemente há uma perda parcial de K+ intracelular e uma despolarização da
célula.
O Lítio é usado na forma de sal carbonato por via oral e eliminado na urina. Tem longa duração de
permanência no organismo, podendo se acumular até que seja alcançado o steady state.
O lítio é indicado para a profilaxia e o tratamento da mania e para a profilaxia do transtorno bipolar ou unipolar.
Os principais efeitos tóxicos do lítio são:
Inibição da ação do hormônio antidiurético (ADH), acarretando em diabetes insípido e poliúria;
Aumento na secreção de aldosterona com conseqüente aumento na retenção de sódio;
Náuseas, vômitos e diarréia;
Tremor;
Dano tubular renal grave acarretando em Insuficiência renal;
Hipertrofia da tireóide;
Ganho de peso.
Na toxicidade aguda ocasionada pelo lítio podem ocorrer efeitos neurológicos como confusão,
comprometimento motor, coma, convulsões e morte, se a concentração plasmática chegar entre 3 e 5 mmol/L.
Exercícios de revisão de conteúdo
1- Como é sintetizada a serotonina? E como ela é inativada?
2- Em que partes do corpo encontramos a serotonina?
3- No sistema nervoso, em que funções atua a serotonina?
4- Quais são os fármacos inibidores seletivos da captação de 5-hidroxitriptamina?
5- Cite três vantagens oferecidas pelos Inibidores Seletivos da Captação de 5-Hidroxitriptamina em relação aos
demais antidepressivos:
6- Qual é a sua desvantagem em relação aos Tricíclicos?
7- Por que não está correto o uso associado de inibidores seletivos da captação de 5-HT como a fluoxetina e os
antidepressivos tricíclicos?
8- Cite os efeitos adversos dos inibidores seletivos da captação de 5-Hidroxitriptamina:
9- Quais são os fármacos inibidores da MAO?
10- Quais são as isoenzimas da MAO? Quais os seus substratos?
11- Onde e como atua a Monoaminooxidase nas terminações nervosas?
12- Por que os IMAOs podem provocar boca seca, visão embaçada, retenção urinária e constipação?
13- Por que os IMAOs são muito menos usados que outros antidepressivos?
14- Explique o que é a “reação do queijo” observada com o uso de IMAOs:
15- O que são os estabilizadores de humor? Dê exemplos de fármacos com esta ação:
16- Como o lítio pode causar a despolarização de uma célula?
17- Por que o uso de lítio pode causar poliúria?
18- Por que o lítio tem uma estreita janela terapêutica?
Texto Complementar
De acordo com o texto “Depressão maior: da descoberta à solução”, responda às questões que seguem:
1- O que é a depressão maior? O que a caracteriza?
2- Qual é o objetivo do tratamento antidepressivo?
3- Que fitoterápico tem sido utilizado no tratamento da depressão, porém sem eficácia confirmada?
4- Que medida não farmacológica é aplicada em casos graves não-responsivos à farmacoterapia?
5- Em que se baseia a escolha dos antidepressivos?
6- O que explica as diferentes respostas terapêuticas e de padrão de efeitos adversos entre os antidepressivos?
7- Que efeitos adversos são mais pronunciados entre os antidepressivos tricíclicos quando comparados aos inibidores
seletivos da recaptação de serotonina (ISRS)?
8- E que efeitos adversos são mais pronunciados entre os ISRS?
9- Por que o abandono do tratamento é mais comum com os antidepressivos tricíclicos em comparação com os
ISRS?
10- Qual é o tempo necessário para se avaliar a resposta farmacológica de um antidepressivo?
11- De acordo com que característica é definido o melhor horário para se administrar um antidepressivo?
12- Por que a retirada de antidepressivos tricíclicos deve ser feita lenta e gradualmente?
13- Sendo os ensaios clínicos, qual é o antidepressivo mais favorável para uso em crianças?
14- Que fármacos antidepressivos são primeira escolha para o tratamento da depressão pós-parto?












