Universidade Castelo Branco.
Curso: Ciências Biológicas.
Profª: Celeste.
Aluno: Gilberto Fortes Lopes.
Matricula: 2007040082.
Turma: REAL - EAD – 3º período.
TRABALHO DE QUIMICA
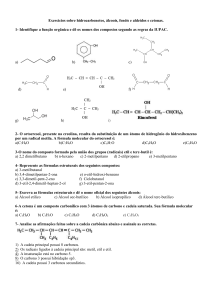
FUNÇÕES DA QUIMICA ORGÂNICA
ÁLCOOIS
Formalmente, os álcoois monohidroxilados, ROH, são derivados orgânicos que se formam
substituindo um hidrogénio da água por um grupo alquilo. Os nome dos álcoois formam-se
como do grupo alquilo, precedido da palavra álcool. Assim, por exemplo, o composto CH3 CH2OH, chama-se etanol.
Ao numerar a cadeia há que designar o número mais baixo
possível na posição do grupo funcional hidroxilo (OH-). Assim, o composto CH3 - CH2 - CH2OH
chama-se 1-propanol e não 3-propanol.
Os álcoois classificam-se em primários, secundários e terciários, dependendo de levarem
um, dois ou três carbonos unidos ao carbono que se liga ao grupo hidroxilo, respectivamente.
Denominam-se álcoois polihidroxílicos aos que contêm mais de um grupo hidroxilo. Os álcoois
com dois grupos hidroxilo denominam-se glicóis ou «dióis» e os que têm três grupos hidroxilo
chamam-se trióis.
O metanol, etanol, 1-propanol, 2-propanol, 1-butanol e muitos álcoois polihidroxílicos são
completamente miscíveis em água. Outros álcoois com muito maior número de átomos de
carbono são ligeiramente solúveis ou mesmo insolúveis em água.
ÉTERES
Formalmente, os éteres (ROR') derivam da substituição dos dois hidrogénios da água por
grupos alquilo ou arilo.
Os éteres numeram-se indicando em primeiro lugar os dois grupos hidrocarbonados
unidos ao oxigénio e acrescenta-se a palavra éter. Assim, o composto CH3 - CH2 - O - CH2 CH3 denomina-se dietiléter ou éter dietílico.
Os pontos de fusão e de ebulição dos éteres são comparáveis aos dos hidrocarbonetos de
peso molecular semelhante.
A maioria dos éteres são imiscíveis na água. Pelo contrário, os éteres são bons solventes
da maioria dos compostos orgânicos. Não apresentam ligações de hidrogénio
intermoleculares tal como pode observa-se nos seus espectros IV, onde não aparece nenhuma
banda a 3.330 cm -1, embora se observe uma intensa banda a 1125 cm -1 característica da
vibração de tensão da ligação C-O.
O termo mais importante da série é o éter etílico, que se obtem desidratando o etanol com
ácido sulfúrico. É um líquido incolor, muito volátil e inflamável. Os seus vapores ardem com
violência explosiva. Utiliza-se como solvente e anestésico.
FENÓIS
Formalmente, os fenóis são álcoois do tipo ROH, onde R é um grupo benzénico (arílico).
O composto mais simples da família é o fenol ou hidrobenzeno. Os monometilfenóis recebem o
nome de cresóis:
Derivados importantes do fenol são o 2, 4, 6 - trinitrofenol, que recebe o nome vulgar de
ácido pícrico e se utiliza como anti-séptico no tratamento das queimaduras, e o ácido ohidroxibenzóico, conhecido com o nome de ácido salicílico, a partir do qual se obtem o ácido
acetilsalicílico, que é o analgésico denominado aspirina:
ALDEÍDOS
Os aldeídos e as cetonas são compostos carbonílicos uma vez que contêm o grupo
funcional carbonilo,
, motivo pelo qual têm muitas propriedades comuns
determinadas pela reactividade do referido grupo funcional.
São compostos carbonílicos do tipo R-COH, onde R é um grupo alquilo ou arilo.
Nomeiam-se substituindo por -al a terminação do hidrocarboneto do mesmo número de
átomos de carbono. Assim, por exemplo, o composto CH 3 - COH chama-se etanal. Ao numerar
a cadeia deve-se designar sempre o número 1 ao carbono aldeídico. Para os aldeídos até
cinco átomos de carbono costumam empregar-se os nomes vulgares formaldeído, acetaldeído,
propionaldeído, butiraldeído e valeraldeído. Quando se usam nomes vulgares, a posição dos
substituintes deve-se indicar somente através das letras gregas, começando por a no carbono
contíguo ao grupo funcional principal. Às vezes emprega-se a letra w para indicar o último
átomo de carbono da cadeia.
CETONAS
As cetonas são compostos carbonílicos do tipo
alquilo ou arilo.
, onde R e R' são grupos
Os nomes das cetonas derivam do nome do hidrocarboneto correspondente, acrescentando
o sufixo -ona ao nome da cadeia hidrocarbonada mais comprida que contenha o grupo
carbonilo. A cadeia hidrocarbonada começa a numerar-se pelo extremo que origina o menor
número possível ao grupo carbonilo. Assim, por exemplo, o composto CH3 - CO - CH2 - CH2 CH3 chama-se 2-pentanona e não 4-pentanona.
Usualmente as cetonas costumam numerar-se indicando os grupos hidrocarbonados unidos
ao grupo carbonilo, acrescentando no final a palavra cetona. Assim, o composto anterior
chamar-se-ia metilpropilcetona.
As cetonas alifáticas com menos de dez átomos de carbono são líquidos solúveis em
água, ainda que a solubilidade diminua ao aumentar o número de átomos de carbono.
Os pontos de ebulição são análogos aos dos aldeídos de peso molecular semelhante.
As cetonas encontram-se amplamente distribuídas na Natureza e com frequência têm
odores muito agradáveis, pelo que se empregam para fabricar perfumes. A propanona ou
acetona é a mais importante de todas as cetonas e emprega-se em grandes quantidades
como solvente de compostos orgânicos.
A redução das cetonas produz álcoois secundários. A diferença em relação aos aldeídos
reside no facto das cetonas não experimentarem facilmente reacções de oxidação. De modo
idêntico aos aldeídos, as acetonas reagem com os álcoois formando hemicetais e cetais.
ÁCIDOS CARBOXÍLICOS
São compostos que contêm o grupo funcional carboxilo (-COOH), assim chamado por ser
formalmente a combinação de um grupo carbonilo e um grupo hidroxilo. Como resultado da
combinação de ambos os grupos funcionais, o grupo hidroxilo experimenta um acentuado
aumento de acidez. Os ácidos carboxílicos formam ligações de hidrogénio mais fortes que as
dos álcoois uma vez que as suas ligações O-H estão mais polarizadas e o átomo de hidrogénio
que serve de ponte pode-se unir a um oxigénio carbonílico, que está carregado muito mais
negativamente que o oxigénio do outro grupo hidroxilo, como no caso dos álcoois. Por este
motivo, os ácidos carboxílicos existem na forma de dímeros cíclicos no estado sólido e
líquido:
Para numerar de modo sistemático os ácidos carboxílicos, substitui-se a terminação do
nome do hidrocarboneto que contém o grupo carboxilo pelo sufixo -oico. Assim, por exemplo, o
composto CH3 - (CH2)5 - COOH chamar-se-á ácido heptanóico. Ao numerar a cadeia de um
ácido carboxílico deve-se considerar sempre número 1 o carbono carboxílico.
Os compostos com menos de seis átomos de carbono recebem nomes vulgares muito
usuais: fórmico, acético, propiónico, butírico e valeriânico. Também são muito empregados os
nomes vulgares dos ácidos dicarboxílicos até sete átomos de carbono: oxálico, malónico,
succínico, glutárico, adípico e pimélico.
ÉSTERES
Os ésteres são compostos que se obtêm da reacção de um ácido carboxílico com um
álcool:
Este tipo de reacção recebe o nome de esterificação.
Os ésteres designam-se como se fossem sais de alquilo ou de arilo dos sais ácidos
carboxílicos. Assim, por exemplo, o éster CH3 - COO - CH3 chamar-se-á acetato de metilo.
Os ésteres são geralmente insolúveis em água e têm pontos de ebulição um pouco mais
altos que os hidrocarbonetos de análogo peso molecular.
Muitos ésteres desprendem odores característicos a fruta e usam-se como
aromatizantes. Os acetatos de etilo e de butilo empregam-se como solventes na fabricação de
vernizes. As gorduras e os óleos são ésteres formados por ácidos de 12 a 22 átomos de
carbono e gricerol, CH2OH - CHOH - CH2OH.
AMINAS
As aminas são derivados orgânicos do amoníaco obtidas formalmente por substituição de
um, dois ou três hidrogénios por grupos alquilo ou arilo.
As aminas classificam-se em primárias, secundárias e terciárias, dependendo de se terem
substituído
um,
dois
ou
três
átomos
de
hidrogénio.
Se todos os substituintes são grupos alquilo, as aminas denominam-se alifáticas. Se algum
substituinte é um grupo arilo, as aminas chamam-se aromáticas.
Para designar as aminas especificam-se os grupos substituintes e acrescenta-se o sufixo amina. Assim, por exemplo, as aminas CH3NH2, (CH3)2NH e (CH3)3N designam-se
respectivamente, metilamina, dimetilamina e trimetilamina.
As aminas até cinco átomos
de carbono são muito solúveis em água e as suas soluções são básicas. As aminas
alifáticas dissolvem-se em ácidos diluídos devido à formação de sais amoniacais solúveis.
As aminas aromáticas obtêm-se geralmente por redução dos correspondentes nitroderivados.
As aminas alifáticas podem obter-se por acção do amoníaco sobre os halagenetos de alquilo
ou também tratando as amidas com bromo e uma base forte, método conhecido como
degradação de Hofmann.
As aminas mais importantes são as aromáticas e entre elas destaca-se a fenilamina ou
anilina, C6H5NH2. A anilina é um líquido incolor, pouco solúvel em água que se emprega como
matéria-prima na fabricação de corantes.
AMIDAS
As amidas são os compostos orgânicos que se formam por reacção de um ácido
carboxílico com o amoníaco ou uma amina.
As amidas classificam-se em primárias, secundárias e terciárias, dependendo do número
de substituintes do átomo de azoto.
As amidas primárias designam-se substituindo o sufixo -oico do nome do ácido carboxílico
pela terminação -amida. As amidas substituídas designam-se antepondo um N ao nome dos
substituintes. Assim, por exemplo, as amidas CH3 - CO - NH2, CH3 - CO - NHCH3 e CH3 - CO N(CH3)2 chamam-se, respectivamente, acetamida, N-metilacetamida e N, Ndimetilacetamida.
Em geral as amidas primárias são sóldas e apresentam fortes ligações de hidrogénio
intermoleculares. As amidas simples são neutras ou debilmente básicas. As ureias são
diamidas que derivam formalmente do ácido carbónico e que recebem o nome do composto
mais simples da família, a ureia, NH2 - CO - NH2. A síntese da ureia a partir do isocianato de
amónio, efectuada em 1828 pelo químico alemão Wohler (1800-1882) foi um golpe de
misericórdia à teoria vitalista que limitava o desenvolvimento na química orgânica:
As poliamidas empregam-se em grandes quantidades na fabricação de fibras artificiais.