Proteínas
São compostos orgânicos de
alto peso molecular, são
formadas
pelo
encadeamento
de
aminoácidos.
Representam cerca do 50 a
80% do peso seco da célula
sendo,
portanto,
o
composto orgânico mais
abundante de matéria viva.
PROTEÍNAS
MÚSCULO
80%
SANGUE
70%
PELE
90%
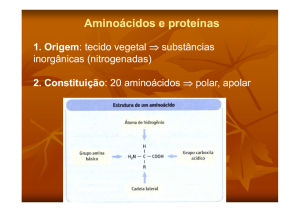
Aminoácidos
CARACTERÍSTICAS GERAIS:
• São as unidades fundamentais das proteínas.
• Todas as proteínas são formadas a partir da ligação em
sequência de aminoácidos.
• Existem, além destes 20 aminoácidos principais, alguns
aminoácidos especiais, que só aparecem em alguns tipos de
proteínas.
AMINOÁCIDOS
• Também conhecidos como peptídeos, pois são formadas por
aminoácidos ligados entre si por ligações peptídicas. Uma
ligação peptídica é a união do grupo amino (-NH 2 ) de um
aminoácido com o grupo carboxila (-COOH) de outro
aminoácido, através da formação de uma amida.
CÓDIGO GENÉTICO - AMINOÁCIDOS
As células animais não sintetizam todos os aminoácidos
necessários, sendo que alguns devem ser ingeridos com o
alimento.
Assim, os aminoácidos podem ser classificados em dois
tipos:
• ESSENCIAIS - NÃO SINTETIZADOS pelos animais.
Ex: HUMANOS Fenilalanina; Valina; Triptofano; Treonina;
Lisina; Leucina; Isolucina; Metionina.
• NÃO ESSENCIAIS (Naturais) – SINTETIZADOS pelos
animais.
Ex: Glicina; Alanina; Serina; Cisteína; Tirosina; Arginina;
Ácido aspártico; Ácido glutâmico; Histidina; Asparagina;
Glutamina; Prolina.
• Vegetais produzem os 20 aminoácidos
necessários para a produção de suas
proteínas.
• Para os vegetais, todos os aminoácidos são
NÃO ESSENCIAIS ou NATURAIS.
• Classificar um aminoácido em não essencial
ou essencial depende da espécie estudada!!!
O QUE DIFERE AS PROTEÍNAS:
•
Quantidade de AA do polipeptídio
•
Tipos de AA
•
Seqüência dos AA
Classificação
• Proteínas simples
– Somente aminoácidos
• Proteínas conjugadas (proteínas
ligadas a outras substâncias)
–
–
–
–
Nucleoproteínas (Ác. Nucleicos)
Glicoproteínas (Glicídios)
Metaloproteínas (Metais)
Lipoproteínas (Lipídios)
Níveis de Organização:
Estrutura Primária (sequência linear de AA)
• Dada pela sequência de aminoácidos e ligações
peptídicas da molécula.
• É o nível estrutural mais simples e mais importante,
pois dele deriva todo o arranjo espacial da molécula.
• "colar de contas", com uma extremidade "amino
terminal" (-NH2)e uma extremidade "carboxi terminal“
(-COOH).
Estrutura Secundária (enrolamento helicoidal )
• É o arranjo espacial de aminoácidos
próximos entre si na sequência primária da
proteína.
• Alfa-hélice
• Ocorre graças à possibilidade de rotação das
ligações entre os carbonos a dos
aminoácidos e seus grupamentos amina e
carboxila.
Estrutura Terciária (dobramento sobre si
mesma)
• Dada pelo arranjo espacial de
aminoácidos distantes entre si na
sequência polipeptídica.
• É a forma tridimensional como a
proteína se "enrola".
Estrutura Quaternária (união de cadeias polipeptídicas)
• Surge apenas nas proteínas oligoméricas ( mais de uma cadeia
polipeptídica).
• Estrutura TRIDIMENSIONAL, pela distribuição espacial de mais de uma
cadeia polipeptídica no espaço, as subunidades da molécula.
• As subunidades podem atuar de forma independente ou
cooperativamente no desempenho da função bioquímica da proteína.
• Proteínas GLOBULARES (Albumina) e FIBROSAS (Queratina)
PROTEÍNAS
Organização Estrutural
• v
Classificação Quanto à Forma
Fibrosas
• São formadas
geralmente por longas
moléculas “retilíneas” e
paralelas ao eixo da
fibra.
• Proteínas de estruturacolágeno do conjuntivo,
as queratinas dos
cabelos, a fibrina do soro
sanguíneo ou a miosina
dos músculos.
Globulares
• Estrutura espacial mais
complexa, são
“esféricas”.
• Enzimas,
transportadores como a
hemoglobina, etc.
Funções:
• Função estrutural - participam da estrutura dos tecidos.
–
–
–
–
Tendões
Cartilagens
Membranas
Músculos
- Resistência aos tecidos : Colágeno: proteína de alta
resistência, encontrada na pele, nas cartilagens, nos
ossos e tendões.
- Contração muscular : Actina o Miosina: proteínas
contráteis, abundantes nos músculos, onde
participam do mecanismo da contração muscular.
- Revestimento e impermeabilização: Queratina:
proteína impermeabilizante encontrada na pele, no
cabelo e nas unhas. Evita a dessecação, a que
contribui para a adaptação do animal à vida
terrestre.
• Função hormonal
– muitos hormônios de nosso organismo são de
natureza proteica.
– Podemos caracterizar os hormônios como
substancias elaboradas pelas glândulas endócrinas
e que, uma vez lançadas no sangue, vão estimular
ou inibir a atividade de certos órgãos.
– Exemplo: insulina, hormônio produzido no pâncreas
e que se relaciona com e manutenção da glicemia
(taxa de glicose no sangue).
• Função de defesa
– Células capazes de "reconhecer"
proteínas "estranhas" que são
chamadas de antígenos. Na presença
dos antígenos o organismo produz
proteínas de defesa, denominados
anticorpos.
– A reação antígeno-anticorpo é
altamente específica, o que significa
que um determinado anticorpo liga-se
apenas ao antígeno responsável pela
sua formação.
Os anticorpos são produzidos por
certas células de corpo (como os
linfócitos, um dos tipos de glóbulo
branco do sangue).
• Função nutritiva ou energética
– As proteínas servem como
fontes de aminoácidos,
incluindo os essenciais
requeridos pelo homem e
outros animais. Esses
aminoácidos podem, ainda, ser
oxidados como fonte de energia
no mecanismo respiratório.
– Nos ovos de muitos animais
(como os das aves) o vitelo,
material que se presta à
nutrição do embrião, é
particularmente rico em
proteínas.
• Coagulação sangüínea
– Vários são os fatores da coagulação que possuem
natureza protéica, como por exemplo:
fibrinogênio, globulina anti-hemofílica, etc...
• Transporte
– Pode-se citar como exemplo a hemoglobina,
proteína responsável pelo transporte de oxigênio
no sangue.
• Função enzimática
– TODA enzima é uma proteína.
– As enzimas são fundamentais como
moléculas reguladoras das reações
biológicas.
– Exemplos: lipases (lipídios ácidos graxos
e glicerol), Amilase, proteínase.
Enzimas
• Promovem a catálise de reações biológicas
(BIOCATALIZADORAS)
• Reduzem a energia de ativação das reações químicas
aumentam a velocidade de reação.
• NÃO são produtos ou reagentes das reações.
• Praticamente todas as reações que caracterizam o
metabolismo celular são catalisadas por enzimas.
• Possuem especificidade com o substrato
Modelo de Chave-Fechadura
As enzimas são classificadas segundo os compostos
nos quais elas agem:
• lipases atuam nas gorduras decompondo-as em glicerol e
ácidos graxos;
• catalases decompõem a água oxigenada;
• amilases decompõem os amidos em açúcares mais simples;
• proteases decompõem as proteínas;
• celulases decompõem a celulose;
• pectinases decompõem a pectina;
• xilanases decompõem a xilana;
• isomerases catalizam a conversão da glicose em frutose;
• outras.
Classificação pelo local de ação
• Endocelulares
• Atuam no interior das células onde foram
produzidas, para agir em reações da própria
célula.
• Ectocelulares
• São produzidas no interior de determinadas
células, mas atuam fora das mesmas. Como
ocorre com as enzimas digestivas.
Classificação pela composição
• SIMPLES
– Enzimas formadas por apenas aminoácidos,
unidos por ligações peptídicas.
• CONJUGADAS
– Composta pela APOENZIMA (parte proteica) e
pela COENZIMA (porção não proteica, por
exemplo hormônios ou vitaminas).
– A enzima só estará ativada e funcional na
presença da COENZIMA, formando um complexo
denominado HOLOENZIMA.
ENZIMA CONJUGADA
• Algumas enzimas podem exigir
um componente adicional para
sua ativação. Este componente
químico é chamado de
COFATOR.
• COFATOR: Íons inorgânicos.
Ferro, Magnésio, Manganês,
Níquel, Cobre...
• COENZIMA: Hormônios e
vitaminas, principalmente.
Concentração do Substrato
• Quanto maior a concentração do substrato, maior a velocidade da reação,
até o momento em que todas as enzimas estejam ocupadas. Não adianta
aumentar a concentração do substrato porque a velocidade da reação
aumentará.
FATORES QUE AFETAM A ATIVIDADE DAS ENZIMAS:
• TEMPERATURA:
• temperatura atividade enzimática / até certo limite.
• agitação moléculas possibilidades de choques , pode ocorrer
rompimento de ligações (perda da conformação), ou seja, ocorre
desnaturação e inativação da enzima.
• Temperatura Ótima / HOMEM ~ 35 E 40 ºC
pH
• Cada enzima tem uma ação ótima de acordo com um determinado pH.
Grandes mudança no pH podem provocar desnaturação de proteínas, e
consequentemente, sua inativação.
DESNATURAÇÃO DAS PROTEÍNAS;
• TEMPERATURA / agitação das
moléculas rompimento de
ligações / Ex: ovo cozido
• GRAU DE ACIDEZ / meios
ácidos ou básicos
rompimento de atrações
elétricas que ajudam manter a
configuração espacial /
fabricação de queijos e
coalhadas
Inibição enzimática
• INIBIDORES IRREVERSÍVEIS
– Ligam-se as enzimas inativando-as de maneira
definitiva. Ocorrem modificações covalentes e
definitiva no sítio de ligação ou no sítio catalítico
da enzima.
• INIBIDORES REVERSÍVEIS
– Podem ser classificados como COMPETITIVOS ou
NÃO COMPETITIVOS. Essa divisão é baseada na
presença ou não de competição entre o inibidor e
o substrato pelo centro ativo da ENZIMA.
Inibição Enzimática
• COMPETITIVA
– Substrato compete, pelo sítio ativo da enzima,
com outra moléculas semelhante à sua estrutura.
– Quando a molécula semelhante se liga à enzima,
está ficará , temporariamente, indisponível para o
substrato. Ocorre então a redução da velocidade
da reação.
Inibição Ezimática
• NÃO COMPETITIVA
– O inibidor NÃO possui estrutura semelhante ao
substrato.
– Este inibidor liga-se à enzima em outro local,
formando um complexo enzima-inibidor. Este
complexo inativa a enzima através de uma
modificação na configuração do seu sítio ativo,
impedindo a ligação do substrato.
– NÃO OCORRE COMPETIÇÃO ENTRE INIBIDOR E
SUBSTRATO!!!