UNIVERSIDADE DO ESTADO DE SANTA CATARINA
CENTRO DE CIÊNCIAS TECNOLÓGICAS
DEPARTAMENTO DE QUÍMICA – DQMC
BIOQUÍMICA – BIO0001
Biomoléculas e a Base
Molecular da Vida
Prof Karine P. Naidek
Agosto/2016
A BIOLOGIA NO SEC. XIX
Vitalismo, élan vital: característica particular e única
existente apenas em organismos vivos – pensamento
místico em círculos acadêmicos
Desenvolvimento da bioquímica e da genética
Tentativa de explicar a vida em bases físicas
Trazer o rigor das ciências exatas para as ciências biológicas
Objetivo alcançado com a biologia molecular
Estudos do fim do sec. XIX e início do sec. XX mostram que
apenas as forças químicas das moléculas inanimadas é capaz
de explicar a constituição dos organismos vivos
SACO DE MOLÉCULAS?
Organismos vivos são compostos de moléculas
sem-vida
O que distingue, então, um organismo vivo de
um saco de moléculas?
Complexidade e Organização
Capacidade de extrair, transformar e utilizar a energia
do ambiente
Capacidade de replicação
DIVERSIDADE DOS ORGANISMOS
OLHANDO MAIS DE PERTO
ORGANISMO
Sistemas
Órgãos
Por trás da diversidade
anatômica existe uma
incrível similaridade em
nível celular e químico
A LÓGICA MOLECULAR DA
VIDA
Poucas generalizações
podem ser feitas para
todos os organismos
Tecidos
Células
Proteínas
Organelas
Moléculas
Aminoácidos
Polissacarídeos
Acidos Nucléicos
Açúcares simples
A, T, C e G
ALFABETO QUÍMICO
Todos os organismos vivos
são constituídos a partir das
mesmas
unidades
monoméricas
A
estrutura
macromoléculas é
determina a sua
biológica
das
o que
função
Cada espécie apresenta um
conjunto
distinto
de
macromoléculas
VIDA E ABUNDÂNCIA DE ÁTOMOS
99%
C, H, O, N
Seres Vivos
1%
99%
Outros elementos
Crosta Terrestre
1%
C, H, N
Outros elementos
VIDA E ABUNDÂNCIA DE ÁTOMOS
A maioria dos constituintes moleculares dos
seres vivos são compostos de átomos de C
ligados a outros átomos de C, H, O, N, P e S
Se encontrássemos vida fora da Terra...
Massa celular -- 99% CHON
BIOELEMENTOS
Principais bioelementos
CHONPS
Elementos presentes como íons
Na K Mg Ca Cl
Microelementos
Fe Cu Zn Mn Co
I Mo V Ni Cr F
Se Si Sn B As
UM POUCO
DE QUÍMICA
Hidrogênio
Água
Número de
elétrons não
emparelhados
Átomo
Camada
Completa
Amônia
1
8
7
Metano
6
16
15
Sulfeto de
Hidrogênio
Ácido Fosfórico
TRÊS VIVAS
PARA O CARBONO
Corresponde a mais de 50%
do peso seco das células
Versatilidade na formação de
ligações químicas
Formação de cadeias lineares,
cadeias
ramificadas
e
estruturas cíclicas
Compostos
orgânicos
–
moléculas que apresentam
esqueletos
de
carbono
covalentemente ligados
GRUPOS FUNCIONAIS EM MOLÉCULAS
VIVAS
EXEMPLOS DE BIOMOLÉCULAS
BIOMOLÉCULAS
Ácidos Nucleicos
Armazenamento da
informação genética
Proteínas
Enzimática
Estrutural
Transporte
Hormônios
Polissacarídeos
Armazenamento
Estrutura
Lipídeos
Armazenamento
Estrutura
Hormônios
Características em comum:
ALTO PESO MOLECULAR
ÁCIDOS
NUCLEICOS
DNA, RNA
Armazenamento
da informação
genética
Polímeros de
nucleotídeos
DNA E RNA
Polímeros de
nucleotídeos
Esqueleto de
ribose-fosfato ligado
às bases nitrogenadas
REPLICAÇÃO
DO DNA
O DNA é composto por uma
dupla-hélice
Replicação
semi-conservativa:
as bases presentes em uma das
fitas contém toda a informação
necessária para a síntese da
nova fita
A complementaridade das bases
A = T, G = C
As duas fitas do DNA são
antiparalelas
EVOLUÇÃO POR MUTAÇÕES
A modificação
das moléculas de
DNA ao longo do
tempo (mutação)
é um dos
principais fatores
evolutivos
DOGMA CENTRAL E TRADUÇÃO
PROTEÍNAS
Moléculas mais
importantes?
Polímeros de
aminoácidos
Apenas 20
diferentes
aminoácidos
estão presentes
nas moléculas
biológicas
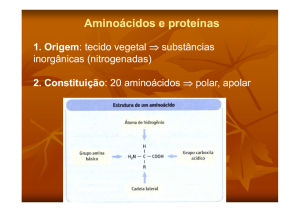
Carboxil
Amino
AMINOÁCIDOS
LIGANDO AMINOÁCIDOS
ESTRUTURA DAS PROTEÍNAS
COMPOSTOS PRECURSORES
Aminoácidos
Proteínas
Hormônios peptídeos
Neurotransmissores
Alcalóides
Adenina
Ácidos nucléicos
ATP
Coenzimas
Ácido úrico
HIERARQUIA ESTRUTURAL
HIERARQUIA ESTRUTURAL
Células
Organelas
Núcleo
Mitocôndria
Complexo de Golgi
Retículo endoplasmático
Complexos supramoleculares
Macromoléculas
Proteínas
DNA/RNA
Polissacarídeos
Unidades Fundamentais
Membrana
Ribossomos
Cromatina
Microtúbulos
Aminoácidos
Glicose
Adenina e outras bases
Ácidos palmítico
AMINOÁCIDOS, PEPTÍDEOS E
PROTEÍNAS
FUNÇÕES DAS PROTEÍNAS
• Vagalume
– Enzima luciferase quebra a proteína luciferina na
presença de ATP
Os aminoácidos
• Os aminoácidos
presentes nas
proteínas são
isômeros L
– A biologia é canhota
• Glicina não
tem isomeria
óptica
Carbono
alfa
Grupo R apolar e alifáticos
• Aminoácidos apolares e hidrofóbicos
• Ligações de Van der Waals
• Ala, Val, Leu, Iso
– Interações hidrofóbicas
• Gly; menor aminoácido
• Met
– Possui átomo de enxofre
• Pro
– Iminoácido, menor flexibilidade estrutural
Grupo R aromáticos
• Aminoácidos hidrofóbicos
• Tirosina pode formar pontes de hidrogênio
com a água
• Modificações póstraducionais
– Fosforilação do OH
da tirosina
• Fenilalanina
– Mais apolar
Grupos R polares, não carregados
• Solubilidade intermediária em água
• Serina e treonina
– Grupos hidroxil
• Asparagina e glutamina
– Grupo amida
• Cisteína
– Grupo sulfidril
– Ligações dissulfeto
Grupos R carregados
• Aminoácidos básicos
–
–
–
–
Carga positiva
Lisina, segundo grupo amino
Arginina, grupo guanidina
Histidina, grupo aromático
imidazol
• Aminoácidos ácidos
– Carga negativa
– Possuem segundo grupo
ácido carboxílico
Aminoácidos
incomuns
• Modificações pós-traducionais
–
–
–
–
–
4-hidroxiprolina
5-hidroxilisina
6-N-metil-lisina
Gama-carboxiglutamato
Fosforilação de resíduos
• Selenocisteína
– Selênio ao invés de enxofre na Cys
– É adicionado durante a tradução por
mecanismo específico e regulado
pH e pKa
• Constantes de dissociação dependem do pH
do meio e são diferentes para diferentes
moléculas
• Ionização
• < pH; > [H]+
estado não-ionizado
Aminoácidos são ionizáveis
• Substâncias
anfóteras: possuem
natureza dual
• Podem funcionar
assim como ácidos ou
bases
– Doam ou recebem
prótons
Titulação de um aminoácidos
• pKa: tendência de um
grupo fornecer um próton
ao meio
• Aminoácidos podem
perder até 2 prótons para
o meio
• Conclusão: a função das
proteínas depende do pH
ao qual estão submetidas
Curvas de titulação predizem a
carga elétrica dos aminoácidos
• Alguns aminoácidos podem ter átomos ionizáveis
também em sua cadeia lateral
Polipeptídeo
>Insulina [Homo sapiens]
MALWMRLLPLLALLALWGPDPAAAFVN
QHLCGSHLVEALYLVCGERGFFYTPKT
RREAEDLQVGQVELGGGPGAGSLQPLA
LEGSLQKRGIVEQCCTSICSLYQLENY
CN
Peptídeos tbm são ionizáveis
• Ou seja, possuem
curva de titulação
característica
• Funcionam em
faixas de pH ótimas
Número de resíduos por proteína
Uso de
aminoácidos
• Varia bastante entre as
proteínas
• Não permite predizer
com precisão o
comportamento
molecular da molécula
Proteínas com outros grupos
químicos
• Adicionados pós-traducionalmente
Proteínas podem ser separadas e
purificadas
• Sabendo que a célula possui milhares
de proteínas, como purificar uma única
delas?
– Basta selecionar por propriedade
• Tamanho, carga e propriedades de ligação
• Obter o extrato bruto
– “correr” em cromatografia de coluna
• Fase estável (matriz)
• Fase móvel (solução com tampão)
– Coluna maior permite maior resolução
na separação
Cromatografia por troca iônica
• Polímero carregado
negativamente
– Proteínas positivas ligam ao
polímero e demoram mais
a ser eluídas da coluna
• Afinidade da proteína é
definido também pelo pH
Cromatografia por exclusão de
tamanho
• Grânulos porosos na
matriz seguram as
moléculas menores
• Moléculas grandes
não entram nos
poros e são eluídas
primeiro
Cromatografia de afinidade
• Adiciona-se à matriz da
coluna algum tipo de
molécula
ligante
da
molécula de interesse
• Molécula ligadora de ATP;
adiciona-se ATP à matriz
• Elui-se com solução de ATP
Eletroforese -- Histórico
•
1952, Markham and Smith
–
•
1955, Smithies
–
•
Géis de acrilamida com maior resolução e permitem
separar ainda moléculas grandes de DNA
1980, Schwartz and Cantor
–
•
Géis de amido funcionam bem para separar
proteínas do soro humano
1967, Loening
–
•
Ao estudarem hidrólise de RNA percebem que
moléculas de diferentes estruturas têm sua
mobilidade diferenciada quando aplicadas num
papel e submetidas a um campo elétrico
Eletroforese em campo pulsado separa fragmentos
enormes
É hoje impossível imaginar um laboratório de
biomol sem eletroforese acontecendo a todo
instante...
Vou ali correr
um gelzinho e
já volto
Tenho que ir senão
vou perder meu gel
Eletroforese
•
Movimento de partículas dispersas
num fluído sob influência de um campo
elétrico uniforme
•
DNA, carga negativa
– Tem tendência a se dirigir ao polo
positivo quando sujeito a um campo
elétrico
•
Serve para separar moléculas por
tamanho/carga elétrica
– Proteína deve ser desnaturada com
detergente (SDS)
•
Técnica utilizada à exaustão em
trabalhos de biologia molecular
Eletroforese, etapas
1.Preparação do gel
2.Aplicação das amostras
3.Eletroforese
4.Coloração
5. Análise dos resultados
Aplicação das amostras
Definição do mapa das
amostras por canaleta
Corrida do gel
• Aplicação do campo elétrico
• Fonte elétrica gera fluxo de
íons através da solução
tampão
• Terminais positivo e
negativo
• Tempo adequado, senão o
DNA sai do gel
Coloração das moléculas
• Prata
– Gel SDS-PAGE
• PoliAcrilamide Gel Electrophoresis
– Melhor resolução
• Coomassie blue, etc
• Brometo de etídio
– Agente intercalante do DNA
• Cancerígeno!
– Composto fluorescente à luz UV
– Gel de agarose
Eletroforese de um resultado de
cromatografia
O marcador de peso molecular
• Comprado de uma empresa
– Possui proteínas de peso molecular bem conhecido
• Permite saber o peso molecular da(s) proteína(s) presente(s)
numa amostra