Exercíciosde Funções Orgânicas
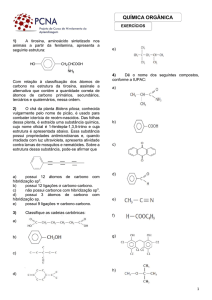
1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um
círculo e dê o nome da função.
REVISÃO DE ISOMERIA PLANA E GEOMETRICA
1) Indique o tipo de isomeria existente entre os compostos listados a seguir:
2) Observe as fórmulas estruturais a seguir de quatro compostos diferentes:
a) Dê o nome de cada substância.
b) Quais são isômeros? Determine o tipo de isomeria.
c) Qual composto apresenta maior e a menor temperatura de ebulição? Justifique.
3) Considere três substâncias X, Y e Z, de mesma fórmula molecular C 3H8O. A substância X é
isômera de posição de Y e possui apenas 1 hidrogênio ligado a um carbono secundário. Z é
isômero de função de X e Y. Agora responda:
a) Quais os nomes dessas substâncias?
b) É possível a substância Z apresentar algum metâmero? Justifique.
4) Sabe-se que a ingestão freqüente de lipídios contendo ácidos graxos (ácidos
monocarboxílicos alifáticos) de cadeia carbônica insaturada com isomeria trans apresenta maior
risco para o desenvolvimento de doenças cardiovasculares, sendo que isso não se observa com
os isômeros cis. Dentre os critérios seguintes, o mais adequado à escolha de um produto
alimentar saudável contendo lipídios é:
a) Se contiver bases nitrogenadas, estas devem estar ligadas a uma ribose e a um aminoácido.
b) Se contiver sais, estes devem ser de bromo ou de flúor, pois são essas as formas mais
freqüentes nos lipídios cis.
c) Se estiverem presentes compostos com ligações peptídicas entre os aminoácidos, os grupos
amino devem ser esterificados.
d) Se contiver lipídios com duplas ligações entre os carbonos, os ligantes de maior massa devem
estar do mesmo lado da cadeia.
e) Se contiver poli-hidroxialdeídos ligados covalentemente entre si, por ligações simples, esses
compostos devem apresentar estrutura linera.
5) A largata-rosada (Pectinophora gossypiella) é considerada uma das pragas mais importantes
do algodoeiro. Armadilhas de feromônio sexual à base de gossyplure permitem o
monitoramento da infestação e a conseqüente redução das aplicações de inseticidas. Observe a
estrutura da molécula de gossuplure.
Considere as seguintes afirmações a respeito dessa molécula
I – ela apresenta 18 átomos de carbono
II – ela apresenta duas ligações duplas C = C com configuração geométrica cis.
III – trata-se de um éster cujo grupamento ligado ao oxigênio é uma cadeia alifática insaturada.
Quais estão corretas?
a) Apenas I
b) Apenas II c) Apenas III d) Apenas I e II
e) Apenas I e III
6) Considere os compostos e as afirmações apresentadas sobre eles:
I) 1 e 2 são isômeros geométricos;
II) 3 e 4 apresentam a mesma fórmula molecular (C 3H6O2), isto é, correspondem à mesma
substância; portanto não se trata de isomeria;
III) 5 e 6 mostram um exemplo de isomeria de posição;
IV) 1, 2, 5 e 6 são hidrocarbonetos.
Dessas afirmações, apenas
a) I é correta.
b) IV é correta.
c) I e II são corretas.
d) I e IV são corretas.
e) I, II e IV são corretas.
ISOMERIA OPTICA
Determinação da Isomeria Óptica
A condição necessária para a ocorrência de isomeria óptica é que a molécula da substância seja
assimetrica, quando existir na estrutura molecular pelo menos um carbono assimétrico ou
quiral ou ainda centro quiral.
E no comportamento diante de uma luz polarizada (luz polarizada é aquela que vibra em um
único sentido).
Algumas definições:
Carbono assimétrico ou quiral: está ligado a quatro radicais diferentes entre si (a, b, c, d)
comumente representado por C*. carbono com ligação dupla ou tripla nunca pode ser
assimétrico.
Isômeros opticamente ativo (IOA): é aquela que desvia o plano de luz polarizada, se o desvio
for para a direita dizemos que é dextrógiro (d ou pelo sinal + na frente do nome) e se o desvio
for para a esquerda dizemos que é levógiro (l ou pelo sinal – na frente do nome).
Isômeros opticamente inativo (IOI): é aquela que não desvia o plano de luz polarizada. (dl)
Mistura racêmica: é opticamente inativa por compensação externa, ou seja quando isômeros d
e l estão presentes na mesma quantidade. Nessa mistura o isômero d desvia a luz polarizada em
um certo ângulo para a direita e o isômero l desvia a luz polarizada no mesmo ângulo para a
esquerda. Como ambos estão presentes na mesma concentração, o somatório dos desvios é nulo
e a luz polarizada acaba não sendo desviada.
Exercícios
Observe a estrutura:
1. Quais funções orgânicas estão presentes na molécula?
2. Escreva sua fórmula estrutural e indique o carbono quiral.
3. Quais dos compostos seguintes apresentam carbono assimétrico?
4) A respeito da estrutura apresentada a seguir, responda:
a) Quais funções estão presentes na molécula?
b) Escreva sua fórmula molecular.
c) Indique o número de carbonos assimétricos (quirais).
d) Qual o número de isômeros opticamente ativos?
e) Qual o número de isômeros opticamente inativos (racêmicos)?
REVISÃO SOBRE REAÇÕES
Reações de Substituição em alcanos. (Reação de Substituição de Aromática)
Halogenação – substituição de um hidrogênio por halogênio (Br, Cl, I, F).
Nitração – envolve ácido nítrico, substitui um hidrogênio por NO2 e forma água.
Sulfonação – envolve ácido sulfúrico, substitui um hidrogênio por SO3H e forma água.
EXERCÍCIOS
1) Os produtos principais das reações são:
Reação de Adição (característico de compostos insaturados, que podem sofrer quebra
parcial dessas ligações).
Hidrogenação – ocorre adição de H2, na presença de catalisadores metálicos, como níquel (Ni),
paládio (Pd) ou platina (Pt).
Halogenação – ocorre adição de halogênio (F2, Cl2, Br2, I2) às insaturações.
Hidro-halogenação – ocorre adição de haletos de hidrogênio, como HCl, Hbr ou HI.
Hidratação – ocorre na presença de água formando um enol (composto orgânico que possui
uma hidroxila ligada a carbono com dupla ligação), enóis são instáveis e sofrem um rearranjo
originando uma cetona ou um aldeído.
2) Complete as reações a seguir, indicando a fórmula estrutural e o nome dos compostos
formados.
3) Observe as representações a seguir e escreva o produto predominante das reações:
Oxidação de Alcenos
Oxidação Branda – ocorre adição de hidroxila em cada carbono da ligação dupla, produzindo
diálcool. No processo usa-se solução aquosa de permanganato de potássio (KmnO 4 – Teste de
Baeyer).
Ozonólise – ocorre quebra do alceno pelo ozônio (O3) originando aldeídos ou cetonas e H2O2.
Oxidação enérgica – ocorre formação de ácido carboxílico e cetona. Quando a dupla ligação
encontra-se na extremidade da cadeia ocorre formação de ácido carboxílico e liberação de CO 2 e
H2O.
EXERCÍCIOS
4) Dois hidrocarbonetos têm fórmula molecular C3H6.
a) Dê as fórmulas estruturais e os nomes desses hidrocarbonetos.
b) Em temperatura ambiente, esses compostos são gasosos. É possível identificá-los com o teste
de Baeyer?
5) Equacione as reações:
a) 3H2C = CH2 + 2KMnO4 + 2H2O
b) H3C – CH = C – C2H5
CH3
→
O3
c) H2C = CH – CH = C – CH3
CH3
d) HC ≡ C – CH2 – CH3
[O]
→
enérgica
[O]
→
enérgica
Reações envolvendo Álcoois
Desidratação – consiste na perda de água. Intermolecular produz éter, e Intramolecular produz
alceno.
Esterificação – reação entre ácido carboxílico e um álcool, formando éster e água.
Oxidação – em carbono primário produz aldeído e no final da reação ácido carboxílico; em
carbono secundário produz cetona; em carbono terciário não sofre reação.
EXERCÍCIOS
6) Dê nome e complete as reações na formação do produto final.
a) 2H3C – CH2 – OH
b) H3C – CH2– OH →
c) H3C – C = O + HO – CH2 – CH3 →
OH
d) H3C – C – H2 [O] →
água
OH
e)
OH
H3C – C – CH3
H
[O]
água
→