Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
DESENVOLVIMENTO E ANÁLISES DE
QUALIDADE DE COMPRIMIDOS DE
AMOXICILINA PRODUZIDOS POR MÉTODO DE
GRANULAÇÃO VIA SECA
DEVELOPMENT AND QUALITY ANALYSIS OF AMOXICILLIN TABLETS PRODUCED BY DRY
GRANULATION METHOD
Angelaine Caroline RIBEIRO1; Gabriela de Fátima PELISSARI1; Cristina Maria FRANZINI1.
1
Curso de Farmácia (Disciplina: Farmacotécnica Industrial) no Centro Universitário Hermínio
Ometto – FHO|Uniararas
Autora responsável: Cristina Maria Franzini. Endereço: Rua Nunes Machado, n. 279, apto 72,
Centro, Araras – SP. CEP: 13600-020, fone: (19) 9-9709-0944, e-mail:
<[email protected]>.
RESUMO
A amoxicilina é um fármaco antimicrobiano de amplo
espectro empregado na prática clínica destinada ao
tratamento de infecções, sobretudo daquelas
acometedoras do trato respiratório. As propriedades
físico-químicas e biofarmacêuticas da amoxacilina
tornam o desenvolvimento de uma preparação
farmacêutica com este princípio ativo um grande
desafio. Neste sentido, para esta substância, é necessário
considerar como barreiras no processo de
desenvolvimento de um novo produto sua restrita
solubilidade em meio aquoso, assim como sua
susceptibilidade ao processo de hidrólise. Diante dessas
considerações, a produção de comprimidos por via seca
demonstra ser uma alternativa interessante para o
preparo de comprimidos constituídos de amoxicilina.
Além disso, esta via de preparação apresenta inúmeras
vantagens sobre o processo produtivo industrial.
Portanto, este trabalho teve como objetivo desenvolver
comprimidos constituídos de amoxicilina por via seca
de compactação e promover ensaios de controle de
qualidade destes comprimidos. Para isso, foi proposta
uma fórmula farmacêutica empregando-se a
amoxicilina em uma dose terapêutica de 500mg, tendo
como adjuvantes farmacotécnicos a celulose
microcristalina, o estearato de magnésio, a lactose
anidra e a croscarmelose sódica. A preparação foi
submetida posteriormente a ensaios de controle de
qualidade representados por: avaliação de aspecto, peso
médio, friabilidade, tempo de desintegração e perfil de
dissolução. Foi possível garantir a obtenção de
comprimidos constituídos de amoxicilina com perfil de
dissolução condizentes com preparações de liberação
imediata, bem como a adequabilidade desta diante dos
demais ensaios de controle de qualidade.
Palavras-chave: Compactação Via Seca. Perfil de
Dissolução. Controle de Qualidade. Beta-lactâmicos.
ABSTRACT
Amoxicillin is a broad-spectrum antimicrobial drug
used in clinical practice for the treatment of infections,
especially those of the respiratory tract. The physicochemical and pharmaceutical properties of amoxicillin
make the development of a pharmaceutical preparation
with this active principle a great challenge. In this sense,
for this substance, it is necessary to consider as barriers
in the process of developing a new product its restricted
solubility in aqueous medium, as well as its
susceptibility to the hydrolysis process. In view of these
considerations, dry tablet production proves to be an
interesting alternative for the preparation of tablets
consisting of amoxicillin. In addition, this route of
preparation presents numerous advantages over the
industrial production process. Therefore, the objective
of this study was to develop compressed dry tablets of
amoxicillin and to promote quality control of these
tablets. For this, a pharmaceutical formula was
proposed using amoxicillin in a therapeutic dose of
500mg, having microcrystalline cellulose, magnesium
stearate, anhydrous lactose and croscarmellose sodium
as pharmacotechnical adjuvants. The preparation was
subsequently subjected to quality control tests
27
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
represented by: appearance evaluation, average weight,
friability, desintegration time and dissolution profile. It
was possible to obtain tablets containing amoxicillin
with a dissolution profile compatible with immediate
release preparations, as well as the suitability of this in
the face of other quality control tests.
Keywords: Dry Compression. Dissolution Profile.
Quality Control. Beta-lactams.
INTRODUÇÃO
A amoxicilina é uma aminopenicilina semisintética, com amplo espectro de atividade
bactericida, usada em sua forma tri-hidratada em
produtos de uso oral. Este fármaco ainda se
caracteriza por ser ácido-resistente e constituído de
amplo espectro de ação, atuando contra bactérias
Gram positivas e Gram negativas, sendo
amplamente empregado no tratamento de infecções
do trato respiratório (WHITE et al., 2004;
GRESSER, 2001; GOMES; SOUZA, 2010;
BELMAR-LIBERATO et al., 2011). Quimicamente,
seu aspecto é de um pó branco, levemente aromático
e com gosto amargo, sendo pouco solúvel em água
(1:400) e em álcool (1:1000), dissolvendo-se em
soluções de ácidos ou hidróxidos (US
PHARMACOPEIA, 1989; BIRD, 1994).
A amoxicilina tri-hidratada normalmente é
branca (ou quase branca), cristalina, e é bem
absorvida quando administrada via oral, com uma
bioatividade que parece ser bem maior que o
esperado diante de suas propriedades físicomecânicas e biofarmacêuticas diante da concepção
da teoria da partição (GUJRAL; HAQUE, 2010;
HILTON; DEASY, 1993).
A amoxicilina tri-hidratada é caracterizada
por sua solubilidade, já que é ligeiramente solúvel
em água; sua estabilidade pode estar relacionada à
quantidade de água agregada e ao seu comportamento de higroscopicidade. Por ser pouco solúvel,
a amoxicilina tri-hidratada pode ser considerada
uma droga cuja velocidade de otimização deve ser
otimizada (BRITISH PHARMACOPEIA, 2011;
MARTINDALE, 1996; AULTON, 2005; PATIL,
PATHADE; BAIRAGI, 2011).
Após administradas via oral, preparações
farmacêuticas constituídas de 500mg apresentam
cerca de 90% de absorção, havendo um pico sérico
de 3µg/mL após 45 minutos. Sua meia-vida
corresponde a um intervalo de 1-1,5 h, e a presença
de alimentos no trato gastrointestinal não interfere
em sua absorção (KOROLKOVAS, 1995;
CAIAFFA et al., 2002; HARDMAN; LIMBIRD,
2004; ORTOFARMA, s/d).
A amoxicilina pode formar vários
complexos com íons metálicos, tais como Fe(II),
Ni(II), Zn(II) etc., os quais atuam como
catalisadores, degradando a amoxicilina por meio
do processo de solvólise. Da mesma forma, a
amoxicilina também é rapidamente degradada sob
condições ácidas em função de o anel β-lactâmico
ser sucessível à degradação hidrolítica quando o pH
desvia significativamente do ponto isoelétrico (pH
4,8) (BARICCATTI et al., 2008).
A técnica de compactação direta, além de
ser economicamente viável (relação tempo, custo e
energia) se comparada à técnica tradicional de
granulação, é um processo restrito a fármacos
sensíveis à água e termolábeis como a amoxicilina.
Outra vantagem da compressão direta é quanto ao
tempo de desintegração do comprimido que é
otimizado, ou seja, as partículas primárias do
comprimido são rapidamente liberadas, permitindo,
posteriormente, sua dissolução (WANCZINSKI et
al., 2002; FU et al., 2004; AULTON, 2005;
BOLHUIS et al., 1979; PRISTA et al., 1995;
PALACIOS, 2000).
Agentes agregantes-diluentes (multifuncionais) devem ser cuidadosamente escolhidos para o
sucesso de uma formulação desenvolvida por
compressão direta, principalmente quando o
fármaco apresenta elevada dosagem, podendo
haver dificuldades de compactação e fluxo.
Nesse sentido, a celulose microcristalina
mostra um fluxo relativamente bom, além de boa
compressibilidade e alto potencial de diluição,
sendo fisiologicamente inerte e não tóxica (REIER;
SHANGRA, 2006; HANDBOOK, 2009). Ela é
multifuncional, com capacidade agregante,
desintegrante e diluente, mas, certamente, pela sua
propriedade intrínseca de desintegração, permite a
dissolução do fármaco de maneira otimizada
(ANSEL; POPOVICH; ALLEN JR., 2000;
ISHIKAWA et al., 2001; HANDBOOK, 2009).
A lactose anidra pode ser utilizada em
associação com a celulose microcristalina para
reduzir custos. De acordo com as especificações, o
tempo de desintegração da massa compacta de
28
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
lactose depende da sua concentração, sendo necessária, às vezes, a adição de agentes desintegrantes
específicos (HANDBOOK, 2009).
A croscarmelose é um superdesintegrante
que aumenta o tempo de desintegração de
comprimidos, o que pode ser considerado um
aspecto positivo quando a liberação do medicamento
deve ser imediata (HANDBOOK, 2009).
Diante dessas premissas, este trabalho visou
desenvolver comprimidos de amoxicilina pelo
método de compactação via seca e realizar análises
de controle de qualidade destes comprimidos.
MATERIAIS E MÉTODOS
Foi proposto o desenvolvimento de uma
preparação farmacêutica na forma de comprimidos
constituídos por amoxicilina tri-hidratada, celulose
microcristalina, lactose anidra, estearato de
magnésio e croscarmelose sódica.
A quantidade (para cada unidade) dos
constituintes da preparação sólida proposta em
escala piloto foi determinada conforme apresenta a
Tabela 1 a seguir.
Tabela 1 Composição do comprimido constituído de amoxicilina.
Componentes
Amoxicilina Tri-hidratada
Microcrystalline cellulose
Quantidade (mg/unidade)
500
125,25
Lactose Anidra
175,25
Magnesium Stearate
18,50
Croscarmellose sodium
16,00
Após a pesagem, os pós foram devidamente
misturados em escala geométrica volumétrica
conforme rigor farmacotécnico descrito por Ansel,
Popovich e Allen Jr. (2000), visando à obtenção de
uma mistura homogênea de pós. O estearato de
magnésio foi reservado para ser adicionado à
mistura de pós nos períodos pré-compactação.
A mistura foi conduzida à máquina de
compactação rotacional (Neuberger NM – 40), com
punções circulares bicôncavas de tamanho
referentes a 12 mm. Os comprimidos primários
foram submetidos à máquina de granulação
(GRANULADOR OSCILANTE – LEMAQ – LM300). Os grânulos recém-preparados foram
compactados nas mesmas condições determinadas
para a mistura de pós.
Foram obtidos, aproximadamente, 1000
comprimidos neste ensaio piloto. O lote piloto
resultante foi submetido às análises de controle de
qualidade destinadas às preparações na forma de
comprimidos, considerando-se o aspecto, o peso
médio, a friabilidade, o tempo de desintegração e o
teste de dissolução.
Testes de Controle de Qualidade: análise
macroscópica
Assim como descrito por Wanczinski et al.
(2002), foram observados os caracteres visuais da
forma farmacêutica obtida em relação à forma
geométrica, à uniformidade de conteúdo, à
coloração e à presença de partículas estranhas à
formulação.
Peso médio
Neste ensaio, aplicou-se a metodologia
prevista na Farmacopeia Brasileira (1988), usando
faixa de tolerância de 5% para comprimidos com
peso médio acima de 250,0g. Foram pesados 20
comprimidos, aleatória e individualmente, em
balança analítica, determinando-se a média e os
desvios de cada comprimido (SOUZA; SPANIOL;
PETROVICK, 2005). Como limite aceitável, foi
considerada a faixa correspondente a 793,25 –
876,75.
Determinação da friabilidade
A friabilidade foi determinada a partir de 20
comprimidos, por meio do cálculo do percentual de
perda de material por queda e erosão, utilizando-se
29
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
friabilômetro (ÉTICA – MOD. 300) numa velocidade de 25 rotações por minuto durante 15 minutos.
Considerou-se aceitável a perda friável inferior a
1,5% (FARMACOPEIA BRASILEIRA, 1988;
REIS; MOREIRA; PIANETTI, 2003).
Determinação do tempo de desintegração
O tempo de desintegração foi determinado
em meio constituído de água destilada a 37 °C ± 1
°C de acordo com os procedimentos destinados a
comprimidos com amoxicilina devidamente
reconhecidos pela USP (1995). Os resultados
expressam a média de três determinações
individuais.
Determinação da dissolução
Consideradas as recomendações da
Farmacopeia Americana (1989), o experimento foi
realizado nas seguintes condições:
• meio de dissolução: 900 mL de água
destilada à temperatura de 37 ºC ± 0,5 ºC;
• velocidade de agitação: 100 rpm;
• sistema de agitação: cesta (aparato 1);
• tempo de ensaio: 90 minutos.
Para se conhecerem os perfis de dissolução
das preparações, foram coletadas alíquotas (n=3)
de 10 mL com igual volume de reposição do meio
de dissolução nos seguintes intervalos de tempo: 5,
10, 20, 40, 60, 75 e 90 minutos. As preparações
foram filtradas em papel de filtro quantitativo,
prosseguindo-se com a quantificação do fármaco
por meio de espectrofotometria no ultravioleta em
274 nm.
RESULTADOS E DISCUSSÃO
Quando se pensa no desenvolvimento de
uma forma farmacêutica, é possível identificar que
esse processo engloba várias etapas, como estudos
de pré-formulação e de formulação propriamente
ditos, os quais consistem na caracterização física,
química, físico-química e biológica de todas as
matérias-primas, incluindo o fármaco utilizado na
elaboração do produto, assim como das
características e da qualidade do produto final a ser
obtido (LE HIR, 1997; ANSEL; POPOVICH;
ALLEN JR., 2000).
A compressão direta (CD) e a compressão
por via úmida são processos otimizados para a
produção de medicamentos em escala industrial.
São adequados para aquelas substâncias que
possuem fluxo livre, propriedades de coesão e que
podem ser compactadas diretamente, sem o
processo de granulação por via úmida (PRISTA et
al., 1995). Entretanto, por meio de tais métodos de
compactação, fica limitado o número de fármacos
que pode ser produzido em forma de comprimido
sem granulação com umidificação prévia (PRISTA
et al., 1995; ANSEL; POPOVICH; ALLEN JR.,
2000; WU et al., 2001). Nesse sentido, excipientes
especiais com otimizada propriedade de fluidez e
compressibilidade têm proporcionado garantia de
sucesso dos processos de compactação por via seca
de algumas formulações (PALACIOS, 2000).
Inúmeras vantagens podem ser citadas
decorrentes dos processos de compactação direta ou
por via seca, tais como: rapidez, facilidade de
obtenção e redução de perdas de princípio ativo.
Além disso, esses processos podem ser utilizados no
caso de substâncias instáveis frente à umidade e à
temperatura elevada, o que diminui os riscos de
contaminação e aumenta a capacidade produtiva,
gerando, assim, economia (PRISTA et al., 1995;
ANSEL; POPOVICH; ALLEN JR., 2000;
PALACIOS, 2000). Além disso, por meio dos
alimentadores forçados, ocorre a deaeração sobre os
pós volumosos e leves, tornando-os mais densos, o
que permite que fluam uniforme e completamente
para as cavidades da matriz. A deaeração também
elimina o aprisionamento de ar no interior da matriz,
reduzindo, assim, a formação de capping ou rachaduras nos comprimidos (ANSEL; POPOVICH;
ALLEN JR., 2000).
Associada às diversas vantagens expostas
anteriormente, quanto às vias secas de compactação,
vale ressaltar que formulações envolvendo fármacos
extremamente vulneráveis à hidrólise e/ou à
oxidação devem usar o processo da dupla
compressão e/ou compressão por via úmida
utilizando solventes orgânicos, a fim de reduzir
possíveis prejuízos farmacoterapêuticos aos
pacientes submetidos a terapias específicas que
envolvem tais fármacos.
Diante do processo de desenvolvimento
deste trabalho, foi possível constatar a obtenção de
comprimidos com aspecto caracterizados em:
coloração branca, circulares, planos e isentos de
estrias e de material estranho.
Considerando-se que a Farmacopeia
Brasileira (1988) permite uma variação de ± 5% no
peso dos comprimidos com massa superior a 250
mg, é possível constatar por meio da Tabela 2 a
seguir que o peso médio dos comprimidos de 835
30
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
mg foi satisfatório, levando-se em consideração
que todos estavam dentro da faixa de tolerância de
± 5% preconizado.
Tabela 2 Peso médio ± DP dos comprimidos de amoxicilina produzidos.
Número de amostras
Massas (mg ± DP)
Desvio padrão do peso médio
em relação ao peso teórico
20
0,8411 ± 0,014592
0,731
Quanto à friabilidade, a qual pode ser
conceituada como a falta de resistência dos
comprimidos à abrasão/atrito quando submetidos à
ação mecânica de aparelhagem específica, a
formulação proposta apresentou valor de perda
friável equivalente a 1,34%. Este resultado indica
que a preparação proposta demonstrou que a
característica de resistência ao atrito e que a força
de compactação empregada foi adequada, uma vez
que o limite aceitável para este parâmetro é
correspondente à perda friável de até 1,5% (ZADE
et al., 2009). O resultado apresentado diante da
friabilidade de preparação também contribui
concebendo valor desta grandeza para a relação
estabelecida no trabalho de Zade et al. (2009), que
relaciona valores de friabilidade com o método de
preparo empregado no processo de compactação.
Pasquoloto et al. (2005) exploram a relação
entre o uso de diferentes adjuvantes e a influência
destes diante das propriedades mecânicas de
comprimidos e reconhecem que o tamanho
reduzido da partícula de celulose microcristalina
pode promover redução da resistência mecânica de
comprimidos.
Este
último
processo
é
plausivelmente explicado se for considerado que
partículas de maior dimensão apresentam menor
área de contato, o que reduz interações
interpartículas da massa compactada (redução das
forças de coesão e adesão) (GORDON et al., 1990).
A consideração desse parâmetro também é
extremamente importante, uma vez que o atrito das
unidades farmacotécnicas (entre si ou com os
diferentes tipos de embalagens) ocorre durante o
transporte e a manipulação da preparação
farmacêutica (AULTON, 2005).
Sabe-se que uma preparação na forma de
comprimidos, ao ser administrada, alcança os
fluídos biológicos iniciando os processos que
concederão a possibilidade de tornar o princípio
ativo biodisponível. Assim, a massa compacta
percorrerá ao longo do trato gastrointestinal
sofrendo um processo desintegração, com a
desagregação do material compacto e a formação de
agregados de partículas de tamanhos menores
(secundárias) e de partículas sólidas individuais
(partículas primárias), que estarão aptas a se
dissolver num processo gradual. Logo, reconhecese que tanto o processo de desintegração como o de
dissolução são etapas importantes para se garantir o
perfil de biodisponilidade dos compostos ativos
administrados em forma de comprimido. Nesse
sentido, o tempo médio de processo de
desintegração da formulação proposta foi menor
que 5 minutos (4’32’’), evidenciando adequação
diante deste ensaio, uma vez que o resultado
encontrado compreende-se dentro do limite
estabelecido (30min) para comprimidos de
liberação
convencional
(FARMACOPEIA
BRASILEIRA, 1988).
É importante salientar que a desintegração
imediata e rápida condiz com o perfil de ação
esperada para cada apresentação farmacêutica
constituída por um ou mais compostos ativos.
Nesse contexto, ao considerar o efeito antibiótico
da amoxicilina, é possível reconhecer que o menor
tempo de desintegração e, consequentemente, o
início otimizado de fenômeno de dissolução
possibilitam a obtenção de concentrações do
fármaco na circulação sanguínea em um menor
período de tempo, o que pode ser considerado um
aspecto positivo para o combate de agentes
patogênicos infecciosos (RAVAL; PATEL;
PATEL, 2010).
Em concordância com estudos conduzidos
por Pasqualoto et al. (2005), o uso de determinados
adjuvantes farmacotécnicos pode resultar em variações nos parâmetros de desintegração e dissolução
de comprimidos constituídos por amoxicilina, de
31
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
Como mencionado anteriormente, a
absorção de fármacos em comprimido depende da
dissociação da substância ativa a partir da forma de
apresentação, do processo concebido como
desintegração e da dissolução em condições
fisiológicas. Em razão da natureza crítica dos
primeiros dois passos, a dissolução in vitro
constitui uma relevante predição do desempenho in
vivo de medicamentos (AULTON, 2005).
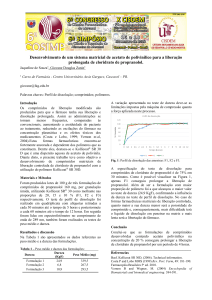
Considerando-se todos os testes de controle
empregados nesse tipo de apresentação, o ensaio de
dissolução mostra-se como um dos mais
importantes (Figura 1), pois possibilita agregar em
seus resultados interpretações diversas.
% do Fármaco Liberado
tal forma que a presença de croscarmelose sódica
(superdesintegrante) e do constituinte multifuncional descrito como celulose microcristalina
propiciou um processo de desintegração em um
curto período de tempo. A lactose empregada
também confere à preparação menor força coesiva
entre as partículas compactadas, facilitando o
processo de fragmentação (desintegração) e, consequentemente, dissolução. A força de compactação
empregada também pode ser mencionada como
possível variável que refletiu na constatação de
resultados do parâmetro descrito como tempo de
desintegração da preparação proposta.
Tempos de Análises (minutos)
Figura 1 Perfil de dissolução do comprimido de amoxicilina desenvolvido.
De acordo com a metodologia empregada
para a avaliação do perfil de dissolução, a
quantidade de fármaco dissolvida durante o
período de 90 minutos deve corresponder à
percentagem não inferior a 80% da quantidade
teórica equivalente a cada unidade farmacotécnica
(500 mg). Logo, o resultado apresentado pela
representação gráfica demonstra que mais de 80%
da amoxicilina foi dissolvida em período inferior a
30 minutos, demonstrando que o processo de
compactação por via seca é viável considerando-se
esse aspecto biofarmacêutico.
É interessante mencionar que o perfil de
dissolução, com base nos estudos conduzido por
Hassan, Najib e Suleiman et al. (1991), pode ser
influenciado pelo tamanho da partícula do agente
multifuncional
concebido
como
celulose
microcristalina, de tal forma que maiores
dimensões dessas partículas podem resultar em um
processo de dissolução com menor tempo no meio
de dissolução. Além disso, a partir desses estudos
também concluiu-se que a presença da lactose pode
exercer um efeito de competição no fenômeno de
dissolução do fármaco, aumentando o tempo do
processo em questão.
Logo, pode-se identificar que a natureza e
as características físico-químicas dos adjuvantes
contribuíram para o processo de compreensão dos
resultados expostos anteriormente, referentes às
propriedades físico-químicas e mecânicas do
comprimido de amoxicilina desenvolvido por via
seca de compactação.
CONCLUSÃO
Conclui-se que foi possível obter comprimidos de liberação imediata de amoxicilina por via
seca de compactação (dupla compactação), além de
caracterizar tal preparação como adequada diante
dos ensaios de controle de qualidade de preparações sólidas representados pelas análises de
aspecto, peso médio, friabilidade, tempo de
desintegração e perfil de dissolução.
32
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
REFERÊNCIAS
ANSEL, H. C.; POPOVICH, N. G.; ALLEN JR.,
L. V. Farmacotécnica: formas farmacêuticas e
sistemas de liberação de fármacos. 7. ed.
São Paulo: Editora Premier, 2000.
AULTON, M. E. Delineamento de formas
farmacêuticas. Porto Alegre: Artmed, 2005.
BARICCATTI, R. A. et al. Degradação hidrolítica
e fotoquímica da amoxicilina na presença de βciclodextrina. Eclética Química. v. 33,
p. 79-83, 2008.
dissolution and friability. J. Pharm. Sci., v. 79,
p. 43-47, 1990.
GRESSER, U. Amoxicillin-clavulanic acid
therapy may be associated with severe side effects
– review of the literature. European Journal of
Medical Research, v. 6, p. 139-149, 2001.
GUJRAL, R. S.; HAQUE, S. M. Simultaneous
Determination of Potassium Clavulanate and
Amoxicillin Trihydrate in Bulk, Pharmaceutical
Formulations and in Human Urine Samples by
UV Spectrophotometry. International Journal of
Biomedical Science, v. 6, p. 335-343, 2010.
BELMAR-LIBERATO, R. et al. Amoxicillin and
amoxicillin-clavulanic acid resistance in veterinary
medicine – the situation in Europe: a review.
Veterinarni Medicina, v. 56, p. 473-485, 2011.
HANDBOOK OF PHARMACEUTICAL
EXCIPIENTS. 6. ed. Pharmaceutical Press:
London, 2009.
BIRD, A. E. Analytical profiles of drug
substances and excipients. v. 23, p. 1-52, 1994.
HARDMAN, J. G.; LIMBIRD, L. E. As bases
farmacológicas da Terapêutica. 10. ed. Rio de
Janeiro: Editora McGrow-Hill, 2004.
BOLHUIS, G. K. et al. Comparative evaluation of
excipients for direct compression. Pharmaceutisch
Weekblad Scientifi, v. 1, p. 203-215, 1979.
HASSAN, M. A. J.; NAJIB, N. M.; SULEIMAN,
M. S. Characterization of glibenclamide glassy
state. Int. J. Pharm. v. 67, p. 131-137, 1991.
BRITISH PHARMACOPOEIA. Londres, 2011.
v. 1 e 2.
HILTON, A. K.; DEASY, P. B. In vitro and in
vivo evaluation of an oral sustained-release
floating dosage form of amoxycillin trihidrate.
Int. J. Pharm., v. 86, p. 79-88, 1993.
CAIAFFA, M. C. et al. Estudo biofarmacotécnico
de cápsulas de amoxicilina. Análise comparativa
de produtos industrializados e magistrais. Cinética
de dissolução. Revista Lecta, v. 20, n. 1,
p. 77-90, 2002.
FARMACOPEIA Brasileira. 4. ed. São Paulo:
Atheneu, 1988. v. 3 e 4.
FU, Y. et al. Orally fast disintegrating tablets:
developments, technologies, taste-masking and
Clinical Studies. Therapeutic Drug Carrier
Systems, v. 21, p. 433-475, 2004.
GOMES, M. L. P. C; SOUZA, S. V. C. Validação
de método para determinação de resíduos de
amoxicilina aplicado à validação de limpeza em
indústria farmacêutica de penicilânicos.
Quim. Nova, v. 33, p. 972-977, 2010.
GORDON, M. S. et al. Effect of the mode of
croscarmellose sodium incorporation on tablet
ISHIKAWA, T. et al. Preparation of Rapidly
Disintegrating Tablet Using New Types of
Microcrystalline Cellulose (PH-M Series) and Low
Substituted- hydroxypropylcellulose or Spherical
Sugar Granules by Direct Compression Method.
Chem. Pharm. Bull., v. 49, p. 134-139, 2001.
KOROLKOVAS, A. Dicionário Terapêutico
Guanabara. Rio de Janeiro: Guanabara
Koogan, 1995.
LE HIR, A. Noções de Farmácia Galênica. 6. ed.
São Paulo: Andrei, 1997.
MARTINDALE: The Extra Pharmacopoeia.
London, The Royal Pharmaceutical Society, 1996.
ORTOFARMA: ESTUDO DE PERFIL DE
DISSOLUÇÃO. Cápsulas de Amoxicilina (como
tri-hidratada) 500mg. Disponível em:
33
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
<http://www.ortofarma.com.br/INTRANET/Web
%20Forms/arquivos>. Acesso em: 20 nov. 2011.
PALACIOS, A. Realidade em granulação e
compresssão direta. A Fórmula, n. 1,
p. 12-13, 2000.
PASQUALOTO, K. F. M. et al. Development and
Evaluation of Amoxicillin Formulations by Direct
Compression: Influence of the Adjuvants on
Physicomechanical and Biopharmaceutical
Properties of the Tablets. Acta Farm.
Bonaerense, v. 24, p. 39-47, 2005.
SOUZA, T. P.; SPANIOL, B.; PETROVICK, P.
R. Avaliação de comprimidos revestidos por
película contendo alta concentração de produto
seco por aspersão de Phyllanthus niruri. Acta
Farm. Bonaerense, v. 24, p. 61-67, 2005.
UNITED STATES PHARMACOPEIA. 22. ed.
Rockville: United States Pharmacopeial
Convention, 1989.
UNITED STATES PHAMACOEIA. 23. ed.
Rockville: United States Pharmacopoeial
Convention, 1995.
PATIL, D. M.; PATHADE, B. A; BAIRAGI, V.
A. Design and Evaluation of bilayer floating
tablets of amoxicillin tryhydrate. Int. J. Res.
Pharm. Sci., v. 2, p. 366-372, 2011.
WANCZINSKI, B. J. et al. Desenvolvimento de
comprimidos de AAS 500 mg: influência do
Amido 1500® na compressão direta. Acta
Scientiarum, v. 24, p. 649-655, 2002.
PRISTA, L. N. et al. Tecnologia Farmacêutica. 5.
ed. Lisboa: Fundação Calouste Gulbenkian, 1995.
WHITE, A. R. et al. Augmentin®
(amoxicillin/clavulanate) in the treatment of
community-acquired respiratory tract infection: a
review of the continuing development of an
innovative antimicrobial agent. Journal of
Antimicrobial Chemotherapy., v. 53, p. 3-20, 2004.
RAVAL, J.; PATEL, J.; PATEL, M. Formulation
and in vitro characterization of spray dried
microspheres of amoxicillin. Acta Pharm., v. 60,
p. 455-465, 2010.
REIER, G. E.; SHANGRA, W. Use of
hydroxypropyl methylcellulose acetate succinate in
an enteric polymer matrix to design controlledrelease tablets of amoxicillin trihydrate. Journal of
Pharmaceutical Science, v. 55, p. 510-514, 2006.
REIS, A. M. M.; MOREIRA, L. M. M.;
PIANETTI, G. A. Estudo da Biodisponibilidade
de comprimidos de carbonato de cálcio. Rev.
Bras. Farm., v. 84, p. 75-79, 2003.
WU, Y. et al. Properties of application of
impinging streams. Chem. Indus. Eng.
Progress., v. 20, n. 11, p. 8-13, 2001.
ZADE, P. S. et al. Formulation, Evaluation and
Optimization of Fast dissolving tablet containing
Tizanidine Hydrochloride. International Journal
of PharmTech Research., v. 1, p. 34-42, 2009.
34
http://www.uniararas.br/revistacientifica
Revista Científica da FHO|UNIARARAS v. 4, n. 1/2016
35
http://www.uniararas.br/revistacientifica