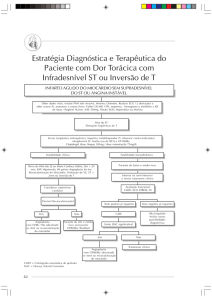
Qual a eficácia e a segurança dos inibidores das glicoproteínas plaquetárias
IIb/IIIa no sindrome coronário agudo? - Metanálise
Bento M., Borges M., Brandão M., Figueiredo L., Jácome J., Neves J., Oliveira M., Sousa L.,
Sousa M., Vilaça M.
Serviço de Bioestatística e Informática Médica da Faculdade de Medicina da Universidade
do Porto
Abstract
Contexto: Vários estudos têm vindo a fortalecer o papel benéfico dos inibidores das
glicoproteínas plaquetárias IIb/IIIa (GPIIb/IIIa) na prevenção da agregação de plaquetas
característica dos síndromes coronários agudos (SCAs). Todavia, muitas questões se colocam
ainda relativamente à segurança e eficácia destes fármacos face às terapêuticas
convencionais. Objectivo: Estudar a eficácia e segurança dos inibidores GPIIb/IIIa nos
SCAs. Métodos: Os estudos seleccionados correspondem a ensaios clínicos randomizados
com mais de 500 pacientes com SCAs sem supradesnivelamento do segmento ST e que
comparam os inibidores das glicoproteínas IIb/IIIa com placebo ou terapêutica de controlo.
Foram excluídos os estudos cujos pacientes estavam recomendados para revascularização
precoce. Resultados: Para um total de 49316 pacientes, o uso destes fármacos em estratégias
de tratamento conservadoras reflectiu-se numa redução de 3% do OR da taxa de morte ou
enfarte de miocárdio a 30 dias (IC 95% 0.91 a 1.03), sem significado estatístico e sem
diferenças
significativas
entre
a
heterogeneidade
dos
estudos.
Existe
evidência
estatisticamente significativa do aumento do risco associado a hemorragia major (OR 1.32
[IC95% 1.19 a 1.46]) e hemorragia minor (OR 1.89 [IC95% 1.75 a 2.05]). A análise das
categorias quanto ao risco de morte e enfarte do miocárdio a 30 dias favorece
significativamente os inibidores de administração intravenosa (OR 0.92 [IC95% 0.86 a
0.99]). Os inibidores orais não só aumentam esta incidência (OR 1.12 [IC95% 0.98 a 1.27]),
como também a de hemorragias major (OR 1.51 [IC95% 1.27 a 1.81]) e minor (OR 1.92
[1.75 a 2.12]). Em diabéticos, a taxa de morte e enfarte do miocárdio a 30 dias sofreu um
decréscimo significativo de 26% (OR 0.74 [IC95% 0.59 a 0.92]). Conclusão: Embora os
1
inibidores GPIIb/IIIa de administração intravenosa sejam mais vantajosos no combate aos
SCAs, estes fármacos são, globalmente, menos seguros e aparentemente menos eficazes que
a terapêutica convencional.
Introdução
Os SCAs, como o enfarte agudo do miocárdio (MI) resultante da rotura das placas
ateroscleróticas, promovem a formação de trombos por agregação plaquetária [1]. A
activação plaquetária conduz a uma alteração conformacional dos receptores das
glicoproteínas plaquetárias IIb/IIIa (GPIIb/IIIa) existentes na superfície das plaquetas. Por
conseguinte, dá-se o aumento da afinidade dos receptores ao fibrinogénio e a outros ligandos,
induzindo a agregação plaquetária que, em situações patológicas, pode levar à formação de
trombos. Não obstante, a activação dos receptores das GPIIb/IIIa é a via final comum a mais
de 100 vias de agregação de plaquetas [2]. Existem dois locais de união das GPIIb/IIIa, sendo
um deles a sequência de aminoácidos Arginina-Glicina-Aspartato, designada de sequência
RGD. Deste modo, os inibidores das GPIIb/IIIa são fármacos cuja acção passa pela ocupação
dos receptores, de forma a inibir a agregação das plaquetas. Estes têm assim, um efeito
protector contra o enfarte de miocárdio e morte ao impedir a formação de trombos em
pacientes propostos para intervenção coronária percutânea (PCI) [3].
Estes fármacos podem dividir-se em quatro grupos distintos, consoante o seu mecanismo
de acção. O primeiro engloba o abciximab que é um anticorpo monoclonal quimérico que
actua de forma irreversível. Os inibidores peptídicos ou integrilinas correspondem ao
eptifibatide que é um heptapéptido cíclico que contem uma sequência KGD (Lisina-GlicinaAsparagina) que interage selectivamente com a sequência RGD já referida. A terceira família
dos inibidores em estudo são fármacos não peptídicos, nomeadamente o tirofiban e o
lamifiban [4]. Os inibidores GPIIb/IIIa orais são “pré-fármacos” uma vez que são activados
quando administrados aos pacientes (orbofiban, xemilofiban, sibrafiban, roxifiban,
ledrafiban...) [5]. De um modo geral, podem-se distinguir estes fármacos em intravenosos e
2
orais, dependendo do modo de administração [6]. A eficácia destes fármacos é avaliada por
comparação com placebos usualmente utilizados como a aspirina ou famílias de
anticoagulantes. Nestas incluem-se os anticoagulantes que necessitam de cofactor e os que
actuam directamente no trombo Os primeiros dividem-se em duas classes: as heparinas não
fraccionadas (são administradas intravenosamente e reduzem significativamente a incidência
de morte, enfarte e angina refractária aguda, patenteando-se tal benefício apenas entre 30 e 90
dias – heparina) e as heparinas de baixo peso molecular (dalteparina e enoxaparina) com uma
vida mais prolongada e uma maior biodisponibilidade. Os inibidores directos de trombos são
um grupo de fármacos que actuam directamente contra os trombos quer livremente, quer
ligados a estes sem necessitarem de um cofactor para actuar, embora muitos destes fármacos
(por exemplo, a hirudina) possuírem um peso molecular mais elevado que a heparina [7] .
Ensaios clínicos anteriores demonstraram que os inibidores das GP IIb/IIIa, em
comparação com placebo e/ou terapêutica de controlo, reduziram a frequência da morte ou
enfarte em 38% [8].
Portanto, propusemo-nos a realizar uma revisão sistemática que apresentava como
objectivo primário a análise do efeito dos inibidores das glicoproteínas plaquetárias IIb/IIIa,
tendo como base ensaios clínicos randomizados.
Métodos
I. Selecção e descrição dos estudos
1. Pesquisa bibliográfica
Procedeu-se a uma pesquisa cuja população alvo correspondia a publicações indexadas na
MEDLINE de ensaios clínicos randomizados. Foi utilizada a query ("Platelet Aggregation
Inhibitors"[MeSH] AND "Platelet Glycoprotein GPIIb-IIIa Complex"[MeSH]) AND
(("Angina, Unstable"[MeSH] OR "Myocardial Infarction"[MeSH] OR "Myocardial
Ischemia"[MeSH]) OR "acute coronary syndromes"), considerando como limites
“Randomized Controlled Trials” e “Humans” de modo a obter artigos que explorassem o
3
papel dos inibidores de agregação plaquetária relacionados com as GP IIb/IIIa nos síndromes
coronários agudos. Refira-se que o termo “síndrome coronário agudo” é relativamente
recente, daí a utilização da disjunção desta palavra-chave com as suas especificações.
Obteve-se um total de 162 artigos.
2. Revisão sistemática dos estudos
Foram definidas antecipadamente uma série de critérios de exclusão e inclusão. Com a
aplicação destes critérios, 8 artigos foram considerados válidos. Os artigos obtidos foram
divididos por 2 grupos de revisores, ambos de 3 elementos, ficando o primeiro com os 80
artigos iniciais e o segundo com os restantes.
a) Critérios de exclusão
Foram rejeitados os estudos que não avaliavam a eficácia dos inibidores das
glicoproteínas plaquetárias IIb/IIIa, já que a sua aceitação estaria a violar o objectivo
primário inerente a esta revisão sistemática. Também foram ignorados os estudos cujos
pacientes estavam recomendados para cirurgia de revascularização precoce, assim como
aqueles que comparavam estratégias conservadoras com estratégias interventivas de
revascularização. Nestes casos, o uso dos inibidores está totalmente dependente de uma
intervenção cirúrgica de revascularização, a qual nunca poderia, pelas razões apontadas, ser
considerada um endpoint primário nesta revisão sistemática. Os estudos com menos de 500
doentes foram também rejeitados, de modo a garantir uma maior fiabilidade e validade na
aferição de generalizações.
b) Critérios de inclusão
A selecção de estudos processou-se através da escolha de casos clínicos randomizados
de pacientes com síndromes coronários agudos cujo electrocardiograma (ECM) não
apresentava supradesnivelamento do segmento ST. Quando tal acontece, o paciente é
imediatamente recomendado para revascularização dada a situação de gravidade que
patenteia o ECM. Interessava também a comparação dos inibidores GPIIb/IIIa com placebo
4
ou com a terapêutica de controlo, pois somente tal possibilitava a aferição de vantagens ou
desvantagens destes fármacos em relação a outras terapias.
c) Avaliação da qualidade dos estudos
Para avaliar a qualidade dos estudos foi utilizado um sistema de classificação para
estudos experimentais [10]. Esta avaliação de qualidade teve em conta vários critérios,
designadamente a selecção de participantes associada à ocultação da randomização, as
diferenças de bases de dados e seu ajustamento, a unidade e os desenhos de estudo e a taxa de
seguimento dos doentes, isto é, o seu follow-up completo. Dos 8 artigos seleccionados, todos
comportavam os requisitos indispensáveis para proceder à sua integração numa metanálise.
d) Concordância
Recorreu-se a um teste de avaliação de concordância Kappa de Cohen (1960) para
avaliar esta mesma propriedade entre as escolhas dos diferentes revisores. Como se formaram
dois grupos de revisores de artigos, esta análise foi feita separadamente para os 2 grupos. Os
resultados obtidos foram: 0,74 para o primeiro grupo e 0,46 para o segundo. Perante as
conclusões de Landis e Koch (1977) podemos classificar estas concordâncias,
respectivamente, como substancial e moderada.
II. Gestão da informação
1. Definição das variáveis
Consideraram-se variáveis relativas ao indivíduo potencialmente determinantes na
avaliação de outcomes [3], como idade, sexo, peso, pressão arterial, nível de colesterol,
história cardíaca e medicação cardíaca. Foram também definidas variáveis relacionadas com
os ensaios clínicos como o fármaco e sua categoria, o número de pacientes e os endpoints
primários respectivos.
2. Definição dos endpoints de eficácia (primários) e de segurança (secundários)
Os endpoints (variáveis que permitem avaliar a eficácia da terapêutica) podem ser
classificados como endpoints de eficácia (a administração do fármaco é interrompida devido
5
a desvantagens irrefutáveis em relação ao placebo) ou de segurança (impossibilidade de
continuar a prática da terapia ou porque a sua administração seria irrelevante para o estudo,
devido à alteração das condições do estudo). É considerado como endpoint de eficácia
(primário) “morte e enfarte do miocárdio a 30 dias”. Por outro lado, os endpoints de
segurança correspondem a complicações de vários tipos, destacando-se as hemorrágicas.
Tanto a hemorragia major como a hemorragia minor encontram-se definidas de acordo com
os critérios TIMI [9]. Foram também definidos como endpoints de segurança a transfusão
sanguínea (realizada sempre que necessária) e situações em que a contagem de plaquetas
fosse inferior a 50000 por mm3 de sangue.
3. Criação de uma base de dados
Os dados relativos aos estudos seleccionados foram compilados numa base de dados
electrónica, através do software “SPSS 12.0 for Windows”.
III. Análise estatística
1. Metanálise
Os estudos incluídos eram semelhantes, ou seja, a amostra, a intervenção e os desfechos
clínicos eram homogéneos, o que possibilitou a metanálise. Desta forma, recorrendo ao
software Review Manager 4.2.3 (RevMan 4.2), foram calculadas estatísticas apropriadas ao
estudo em causa, através do cálculo dos odds ratio (OR) e intervalos de confiança a 95% de
uma série de variáveis consideradas relevantes para a análise, assim como através da
aplicação de testes de heterogeneidade, de modo a avaliar a validade das generalizações.
Para efeitos de análise, foi sempre tomado como nível significância o valor 0,05.
Resultados
1. Características dos pacientes
Os oito estudos seleccionados incluíram, no total, 49316 doentes (29744 no grupo
experimental e 19572 no grupo de controlo). A média de idade da população foi de 64,5 anos,
68% eram homens e 21% eram diabéticos (Tabela 1)
6
2. Endpoints de eficácia
Ao fim de 30 dias, o número de doentes que morreram ou tiveram um enfarte de
miocárdio no grupo experimental foi 2545 (8,6%) e no grupo de controlo 1894 (9,7%). No
entanto, esta diferença não é estatisticamente significativa (p=0,31). Para verificarmos se
haveria, neste resultado, a interferência de um ou mais estudos que fossem muito discrepantes
dos restantes, aplicámos um teste de heterogeneidade, cujo p=0,12, ou seja, não existe uma
heterogeneidade significativa entre os estudos seleccionados (Fig. 1).
Procedeu-se a uma comparação entre os diferentes grupos e classes de inibidores quanto a
esta mesma variável. A única categoria de inibidores GPIIb/IIIa que apresenta uma diferença
entre inibidores e placebo estatisticamente significativa é a dos peptídicos, cujo p=0.04. A
heterogeneidade (Fig. 2) calculada entre as categorias de inibidores (p=0.03) proporcionou a
identificação dos grupos entre os quais se encontravam diferenças, tendo-se somente aferido
uma única diferença estatisticamente significativa entre os inibidores não peptídicos e os
orais (p=0.03), sendo que é no caso dos não peptídicos que o tratamento com inibidor é mais
benéfico que o com a terapêutica de controlo.
Foi efectuada a comparação entre os inibidores GPIIb/IIIa intravenosos e orais (p=0.002).
Além disso, a administração do inibidor intravenoso é significativamente mais vantajosa
do que a terapêutica de controlo (p=0.03 para OR 0.92 [IC95% 0.86 a 0.99]) contrariamente
aos orais que, apesar de não existirem diferenças estatisticamente significativas na
comparação placebo vs. inibidor (p=0,09), parecem ser clinicamente menos eficazes.
3. Endpoints de segurança
O uso de inibidores das glicoproteínas IIb/IIIa está associado a um risco acrescido de
hemorragia major e minor, em comparação com o grupo de controlo (p<0,0001 em ambos os
casos) (Fig 3). Quer na hemorragia major como na minor, os grupos são homogéneos.
Na Tabela 2 podem observar-se os Odds Ratios e Intervalos de Confiança a 95% para
todos os endpoints de segurança considerados. As hemorragias são menos frequentes com o
7
placebo do que com o inibidor aparentemente em todos os casos (OR>1), mas apenas
significativamente nos orais e nos peptídicos.
Relativamente ao placebo, os inibidores intravenosos aumentam significativamente a
incidência de hemorragia major (OR 1.21 [1.07 a 1.38]) e de hemorragia minor (OR 1.78
[1.56 a 2.03]).
Quando comparados, verificaram-se diferenças significativas entre os inibidores orais
e os peptídicos quanto à hemorragia major (p=0.02) apresentando, respectivamente, OR e IC
95% de 1.52 [1.27;1.82] e 1.19 [1.03;1.36].
Quanto à hemorragia minor, verificaram-se apenas diferenças significativas entre
orais e não peptídicos (p=0.02) e peptídicos e não peptídicos (p=0.03).
Verificou-se também que existe uma diferença estatisticamente significativa entre os
efeitos dos inibidores comparativamente a placebo, quanto à concentração de plaquetas <
50000 mm3, nos inibidores orais (p=0.03; OR 1.83 [IC95% 1.07 a 3.13])
Os pacientes submetidos a placebo necessitam de menos transfusão sanguínea
(p<0,001; OR 1.44 [IC95% 1.22 a 1.70]), comparativamente aos que recorreram a inibidores.
4. Efeitos do tratamento em subgrupos
Verificou-se uma diferença estatisticamente significativa na análise de pacientes
diabéticos (p=0,007; OR 0,74 [IC95% 0,59 a 0,92]) (Fig 4). Esta não era verificada nos
pacientes não diabéticos (p=0.99). Isto foi confirmado pela diferença significativa entre os
efeitos dos inibidores nos pacientes diabéticos e nos não diabéticos (p=0.03). Aparentemente,
os inibidores são vantajosos nos pacientes diabéticos mas não o são nos não diabéticos.
Discussão
Face ao objectivo primário do estudo, verificou-se que os inibidores GPIIb/IIIa não
apresentam, globalmente, vantagens significativas face à terapia convencional, apesar de
existir um ligeiro favorecimento destes (Fig. 1) quanto à incidência de morte ou enfarte do
8
miocárdio a 30 dias. O uso destes fármacos leva, porém, a um aumento significativo de
hemorragia major (1,32 vezes) e de hemorragia minor (1,89 vezes).
No entanto, a análise dos inibidores intravenosos permite concluir que estes são mais
eficazes que a terapêutica convencional (p=0,03), havendo uma significativa redução do OR
em 8%. Apesar desta vantagem implicam uma taxa hemorrágica maior que o placebo, ou
seja, aumento da hemorragia major em 21% e da minor em 78%. Refira-se, no entanto, que o
cálculo do OR dos endpoints de segurança para os inibidores intravenosos não comporta os
anticorpos monoclonais.
Outros estudos revelam que a utilização de inibidores GPIIb/IIIa intravenosos após PCI
(Percutaneous Coronary Intervention) reduz o risco de morte entre 20 e 30%. Este efeito é,
todavia, mais significativo a curto prazo (30 dias) do que a 6 meses ou períodos superiores
[18].
A comparação das famílias de inibidores permitiu a obtenção de conclusões mais
relevantes: primeiramente, o uso dos inibidores peptídicos é realmente mais eficaz que a
terapêutica convencional, uma vez que há uma redução da incidência de morte ou MI a 30
dias de 11%; contudo, os pacientes tratados com estes fármacos apresentam uma incidência
significativamente maior de hemorragia que os respectivos controlos (aumento de 19% para
hemorragia major e 85% para hemorragia minor). Em contrapartida, é de realçar que os
anticorpos monoclonais apresentam desvantagens aparentes (p=0.36) no combate aos
síndromes coronários agudos, pois verifica-se uma maior incidência, repetindo, não
significativa, de morte ou enfarte de miocárdio a 30 dias nos pacientes.
O abciximab foi o primeiro inibidor a ser usado. Os primeiros ensaios clínicos efectuados
sobre os efeitos deste no homem demonstraram que este fármaco seria de grande importância
para o tramtamento dos SCA. Com o GUSTO-IV ACS, primeiro estudo de grandes
dimensões com seguimento póstumo dos intervenientes, surge a ideia de que talvez este
fármaco não apresente tantas vantagens no tratamento de SCA como seria de esperar (Fig 5).
9
Os inibidores orais demonstraram ser aqueles que apresentam mais desvantagens
relativamente ao controlo: embora não aumentem significativamente a incidência de morte ou
enfarte a 30 dias (p=0,09) parece haver um aumento considerável do endpoint primário no
grupo sujeito a esta classe de fármacos (1,12 [0,98; 1,28]). Promovem também uma maior
incidência de hemorragia major (51%) e hemorragia minor (92%). Efectivamente, a
comparação entre estes e os inibidores intravenosos favorece significativamente os últimos,
quanto a eficácia (p=0,002), como segurança (hemorragia major – p=0,009). É de focar o
facto de os pacientes que foram tratados com inibidores orais apresentarem uma contagem de
plaquetas inferior a 50.000 mm3 significativamente inferior ao grupo de controlo, o que se
deve provavelmente a efeitos colaterais que este método de administração terá em dadas vias
metabólicas. No entanto, outros estudos demonstraram que a utilização de inibidores orais
promove a redução de intervenções de revascularização precoce, ao mesmo tempo que
provoca um aumento da incidência de morte [19]. Assim se compreende o desuso clínico
desta categoria de fármacos, relativamente, por exemplo, aos inibidores intravenosos.
Curiosamente os estudos que testam inibidores não peptídicos (destacando-se o
PRISM), apresentam resultados bastante diferentes de todos os outros ensaios – os seus
resultados destacam-se positivamente em termos de eficácia e de segurança. Os inibidores
não peptídicos adivinham-se os mais seguros pois a comparação entre os dois grupos sujeitos
ao ensaio traduz-se em resultados não significativos.
Pelos resultados obtidos (Fig 4) observa-se que os inibidores são vantajosos nos pacientes
com diabetes, não o sendo nos que estão na situação inversa, ainda que para esta análise
tenham sido incluídos somente pacientes cujos fármacos usados eram de administração
intravenosa. A utilização de inibidores nestes pacientes leva a um decréscimo de 26% na
incidência de morte ou enfarte do miocárdio a 30 dias, perante o controlo. Compreende-se
assim que, embora sejam um grupo de risco, os diabéticos são actualmente recomendados
para administração destes fármacos em detrimentos de terapêuticas convencionais. Certos
10
estudos que se debruçaram sobre esta vantagem relativa dos inibidores concluiram que,
efectivamente, a presença de inibidores GPIIb/IIIa reduz significativamente a activação
plaquetária que despoleta os SCAs em pacientes diabéticos (p=0,02), propondo,
inclusivamente, que a menor taxa de ligação do fibrinogénio às plaquetas se deve à glicação
das proteínas das membranas plaquetárias que, deste modo, ocorre em maior escala em
pacientes diabéticos do que em pacientes sem esta patologia [21].
Limitações
Este trabalho sujeitou-se a inúmeras limitações metodológicas, estatísticas e relativas à
obtenção de resultados. Por um lado, as limitações inerentes à pesquisa bibliográfica dizem
respeito à problemática de definição da query e à possível não catalogação de todos os
ensaios relevantes na Medline. Quanto aos problemas estatísticos, note-se, por exemplo que
no PRISM, o enpoint primário foi obtido a 48 horas e no PRISM-PLUS a 7 dias (embora
todos os eventos a 30 dias sejam referidos), além de que determinados endpoints não vinham
referidos em todos os ensaios clínicos. Portanto, os resultados obtidos para cada estudo são,
de certo modo, muito rígidos, já que o facto de somente ter sido considerado como endpoint
de eficácia “morte ou MI a 30 dias” condicionou possíveis aferências temporais que advêm
da administração dos inibidores, designadamente no efeito destes a curto e a longo prazo. De
facto, certos estudos [20], ao considerarem os diferentes endpoints em diferentes alturas,
conseguem prever qual o efeito dinâmico dos inibidores GPIIb/IIIa: por exemplo, repare-se
que a 30 dias o tirofiban (inibidor não peptídico, alvo do estudo PRISM) favorece o
tratamento, não o favorecendo entre as 48 e 96 horas após randomização. Embora de forma
menos clara, passa-se o contrário com o lamifiban utilizado no PARAGON e o eptifibatide
utilizado no PURSUIT (Fig 6).
Estatisticamente, a heterogeneidade entre os protocolos, agentes terapêuticos, regimes e
população limitou a capacidade inferencial da revisão sistemática, tal como foi confirmado
em determinadas situações pelos testes de heterogeneidade aplicados. Em tais situações,
11
procedeu-se a outra análise. Na análise de subgrupos, os estudos não estavam desenhados
para a análise dos efeitos em pacientes diabéticos, embora tenha sido adquirida informação
para análise deste efeito.
Os resultados obtidos possibilitam aferir que a aplicação clínica dos inibidores GPIIb/IIIa
é, de um modo geral, incerta quando comparada com as terapêuticas tradicionais. No entanto,
esta realidade é condicionada pela inclusão de um grande número de pacientes submetidos a
inibidores orais, visto que estudos anteriores que não incluíam inibidores orais mostraram
que, globalmente, os inibidores GPIIb/IIIa são estatisticamente favorecidos, reduzindo a
morte ou MI a 30 dias em 9% [3]. A utilização de determinadas categorias destes fármacos
como os peptídicos e não peptídicos e especificamente a utilização de inibidores intravenosos
em pacientes diabéticos revela-se promissora no combate à rotura das placas ateroscleróticas
que desencadeia os SCAs. Perante isto, pode-se concluir que o objectivo primário do estudo
foi cumprido.
Referências
1 The PURSUIT Trial Investigators. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute
coronary syndromes. The New England Journal of Medicine. 1998 Ago 13; 339(7): 436-43
2 Chanu B. Inhibitors of GP IIb/IIIa platelet receptors. Arch Mal Couer Vaiss. 1999; 92(7):893-902
3 Boersman E et al. Platelet glycoprotein IIb/IIIa inhibitors in acute coronary syndromes: a meta-analysis of all major
randomised clinical trials. Lancet. 2002 Jan 19; 359:189-98
4 Sebastian M, Makkar R . Glycoprotein IIb/IIIa receptor antagonists: clinical pharmacology in cardiovascular diseases of
aging. Drugs Aging. 1999; 15(3):207-18
5 Reimann JD et al. Pharmacokinets and Pharmacodynamics of Sibrafiban, an Orally Administered GP IIb/IIIa Antagonist,
following Coadministration of Aspirin and Heparin. J Clin Pharmacol. 2000; 40:488-495
6 Roe MT, Moliterno JD. Emerging Tratment of Acute Coronary Syndromes with Platelet Glycoprotein IIb/IIIa Inhibitors.
Journal of Thrombosis and Thrombolysis. 1999; 7:247-57
7 Cohen M. New therapies for unstable angina and non-Q-wave myocardial infarction: recent clinical trials. Am Heart J.
1998 Jun; 135:343-52
8 Kang DF, Calliff, RM et al. Clinical outcomes of therapeutic agents that block the platelet glycoproteins IIb/IIIa integrin in
ischemic heart disease. Circulation. 1998:2829-35
9 Chesebro JH et al. Thrombolysis in Myocardial Infarction (TIMI) Trial, phase I: a comparison between intravenous tissue
plasminogen activator and intravenous streptokinase: clinical findings through hospital discharge. Circulation. 1987; 76:14254
10 Mitchell E, Sullivan F. A descriptive feast but an evaluative famine: systematic review of published articles on primary
care computing during 1980-97. Information in practise. 2001;322: 279-282
11 The PRISM Study Investigators. A comparison of aspirin plus tirofiban with aspirin plus heparin for unstable angina.
Platelet Receptor Inhibition in Ischemic Syndrome Management. N Engl J Med. 1998 Mai 21; 338:1498-505
12 The PRISM-PLUS Study Investigators. Inhibition of the platelet glycoprotein IIb/IIIa receptor with tirofiban in Unstable
Angina and non Q-wave Miocardial Infarction. Platelet Receptor Inhibition In Ischemic Syndrome Management in Patients
Limited by Unstable Signs and Symptoms. N Engl J Med. 1998 Mai 21; 338:1488-97
13 The PARAGON Investigators. International, Randomized, Controlled Trial of Lamifiban (a Platelet Glycoprotein IIb/IIIa
Inhibitor), Heparin, or Both in Unstable Angina. Circulation. 1998; 97:2386-95
14 The OPUS-TIMI 16 Trial Investigators. Oral Glycoprotein IIb/IIIa Inhibition With Orbofiban in Pacients With Unstable
Coronary Syndromes. Circulation. 2000 Jul 11; 102:149-56
15 The SYMPHONY Investigators. Comparison of sibrafiban with aspirin for prevention of cardiovascular events after
acute coronary syndromes: a randomised trial. Lancet. 2000 Jan 29; 355:337–345.
16 The GUSTO-IV ACS Investigators. Effect of glycoprotein IIb/IIIa receptor blocker abciximab on outcome in pacients
with acute coronary syndromes without early coronary revascularization. Lancet. 2001 Jun 16; 357:1915-24
12
17 The PARAGON-B Investigators. Randomized, placebo controlled trial of titrated intravenous lamifiban for acute
coronary syndromes. The Platelet IIb/IIIa Antagonist for the Reduction of Acute coronary syndrome in a Global
Organization Network. Circulation. 2002 Jan 22; 105:316-21
18 Karvouni E et al. Intravenous Glycoprotein IIb/IIIa Receptor Antagonists Reduce Mortality After Percutaneous Coronary
Interventions. Journal of the American College of Cardiology. 2003 Jan 1; 41(1):26-32
19 Chew D et al. Increased Mortality With Oral Platelet Glycoprotein IIb/IIIa Antagonists – A Meta-analysis of Phase III
Multicenter Randomized Trials. Circulation. 2001 Jan 16; 103:201-206
20 Kong D et al. Clinical Outcomes of Therapeutic Agents That Block the Platelet Glycoprotein IIb/IIIa Integrin in Ischemic
Heart Disease. Circulation. 1998 Dez 22/29; 98: 2829-35
21 Keating FK et al. Augmentation of inhibitory effects of glycoprotein IIb/IIIa antagonists in patients with diabetes.
Thromb Res. 2004; 113(1):27-34
13
Figura 1 – Morte ou enfarte de miocárdio a 30 dias.
Figura 2 – Morte ou enfarte de miocárdio a 30 dias para cada categoria de inibidor GPIIb/IIIa.
Figura 3 – Hemorragias major (em baixo) e minor para cada ensaio clínico.
Figura 4: Morte e enfarte do miocárdio a 30 dias para pacientes diabéticos.
14
Figura 5 – Morte e MI a 30 dias para ensaios que
utilizam o anticorpo monoclonal abciximab (in 16).
Figura 6 – OR e IC95% para o risco de morte entre as 48 e 96 horas após randomização de inibidores GPIIb/IIIa vs
placebo (à esquerda) e a 30 dias (in 20).
Não
peptídicos
Peptídicos
Orais
OR [IC 95%]
(hemorragia major)
1.47 [0.99, 2.17]
OR [IC 95%]
(hemorragia minor)
1.03 [0.63, 1.70]
1.19 [1.03, 1.36]
1.85 [1.61, 2.13]
1.52 [1.27, 1.82]
1.95 [1.77, 2.15]
OR [IC 95%]
(plaquetas)
2.54 [0.80, 8.12]
OR [IC 95%]
(transfusão)
1.57 [1.19, 2.07]
------------- ------------------------- ------------1.84 [1.07, 3.14] 1.37 [1.11, 1.69]
Tabela 2 – OR para enspoints secundários nas várias classes (inibidor vs controlo)
15
PRISM [11]
1994-1996
Período de estudo
3232
Nº de pacientes
Nº de pacientes do 2199 (68,1%)
sexo masculino
Grupo de inibidor Intravenoso
Família de inibidor Não peptídico
62.5
Idade média da
amostra (anos)
79.0
Peso médio da
amostra (kg)
Último episódio de ≤24h
angina de peito
Medicação em estudo
Inibidor
Tirofiban
Regime
a) 0,6 μg/kg + infusão
de 0,15 μg/kg/min +
heparina placebo
b) placebo + heparina
PRISM-PLUS [12]
1994-1996
1915
1291 (67.4%)
PARAGON [13]
1995-1996
2282
1495 (65.5%)
PURSUIT [1]
1995-1997
9461
6102 (64.5%)
OPUS-TIMI 16 [14]
1997-1998
10288
7625 (74.1%)
SYMPHONY [14]
1997-1998
9233
6692 (72.5%)
GUSTO-IV ACS [16]
1998-2000
7800
4870 (62.4%)
Intravenoso
Não peptídico
63.0
Intravenoso
Não peptídico
66.0
Intravenoso
Peptídico
64.0
Oral
Oral
60.5
Oral
Oral
60.0
Intravenoso
Intravenoso
Anticorpo monoclonal Não peptídico
77.4
63.0
Sem informação
disponível
≤12h
76.2
80.0
80.0
65.2
77.0
≤12h
≤24h
Sem informação
disponível
≤72h
≤7dias
≤24h
≤12h
Tirofiban
a) 0,6 μg/kg/min
durante 30 min +
infusão 0.15
μg/kg/min + heparina
placebo
b) 0.4 μg/kg/min
durante 30 min +
infusão 0.1 μg/kg/min
+ heparina
c) Placebo + heparina
Lamifiban
a) 300 μg + infusão de
1 μg/min + heparina
ou heparina placebo
b) 750 μg + infusão de
5 μg/min + heparina
ou heparina placebo
c) Placebo + heparina
Eptifibatide
a) 180 μg/kg/min +
infusão 1.3-2
μg/kg/min
b) Placebo
Orbofiban
a) 50 mg 2 vezes por
dia (grupo 50/50)
b) 50 mg 2 vezes por
dia durante 30 dias
seguido de 30 mg 2
vezes por dias (grupo
50/30)
c) Placebo
Abciximab
a) 250 μg/kg + infusão
0.125 μg/kg/min
(máximo 10 μg/min)
durante 24h
b) 250 μg/kg + infusão
0.125 μg/kg/min
(máximo 10 μg/min)
durante 48h
c) Placebo
Lamifiban
a) 500 μg + infusão de
1.0-2.0 μg/min
b) placebo
Tratamento
Aspirina/dia
48-96 h
325 mg
72-120h
75-325 mg
72-96 h
80-325 mg
2-4 semanas
150-162 mg
Sibrafiban
a) Baixa dose
(permite 25% de
inibição da
agregação
plaquetária)
b) Alta dose (permite
50% de inibição da
agregação
plaquetária)
c) Aspirina (2 vezes
80 mg)
2-4 semanas
80 mg (só ao grupo
de controle)
24 ou 48 h
150-325 mg
72-120 h
150-325 mg
Endpoints
Primários
Secundários
48 h
300-325 mg
Morte, EM, Isquemia Morte, EM, Isquemia
refractória a 48 horas. refractória a 7 dias
Hemorragia
intracraniana,
sangramento que leva
à diminuição da
concentração de
hemoglobina a 50g/L
Hemorragia
intracraniana;
sangramento levando à
diminuição da
concentração de
hemoglobina para
valores inferiores a 40
g/L
Morte ou EM a 30
dias
Morte ou EM a 30
dias
Morte, EM,
Isquemia, Paragem
cardíaca a 6 meses
Hemorragia
Hemorragia
Frequência de
intracraniana,
intracraniana;
hemorragia major ou
sangramento
sangramento
minor a 90 dias
comprometedor de
comprometedor de
(determinado por um
intervenção cirúrgica intervenção cirúrgica algoritmo
informático)
PARAGON-B [17]
1998-1999
5225
3448 (66.0%)
Morte, EM, Isquemia Morte ou EM a 30
refractória a 90 dias dias
Morte, EM, ou Isquemia
refractória a 30 dias
Hemorragias major e Hemorragia
minor
intracraniana;
diminuição da
concentração de
hemoglobina para
valores inferiores a 50
g/L
Hemorragia intracraniana;
sangramento
comprometedor de
intervenção cirúrgica
Tabela 1 – Características dos ensaios clínicos seleccionados, respectivo desenho de estudo e endpoints primários e secundários
16