Orbitais e Números Quânticos
Até ao modelo de Bohr
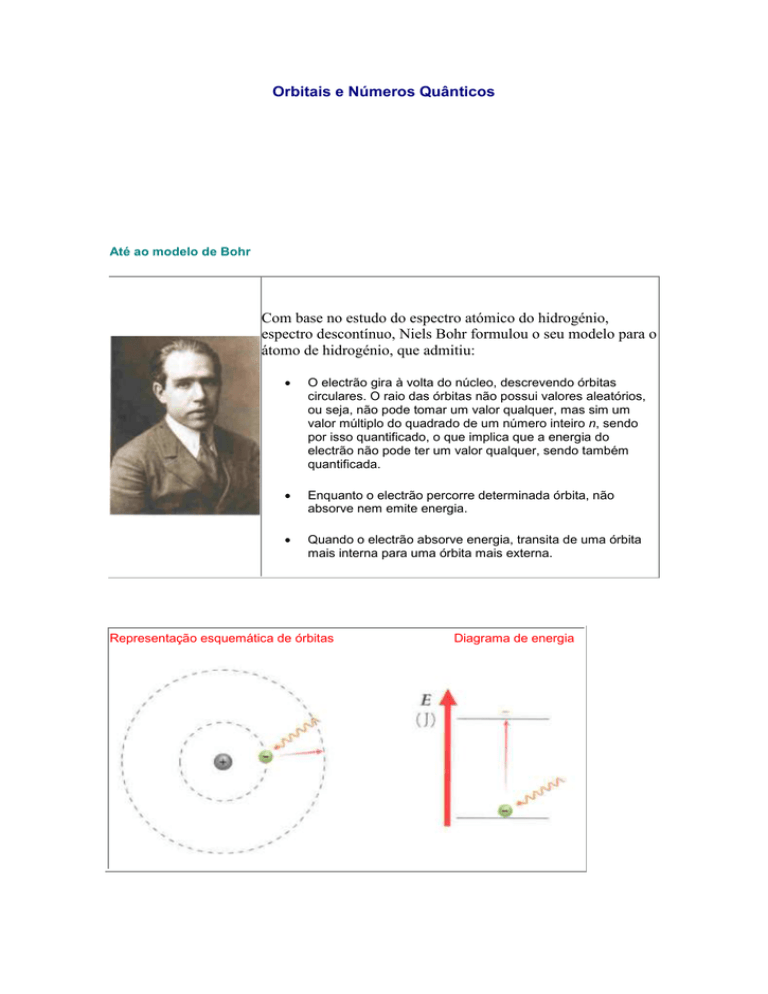
Com base no estudo do espectro atómico do hidrogénio,
espectro descontínuo, Niels Bohr formulou o seu modelo para o
átomo de hidrogénio, que admitiu:
O electrão gira à volta do núcleo, descrevendo órbitas
circulares. O raio das órbitas não possui valores aleatórios,
ou seja, não pode tomar um valor qualquer, mas sim um
valor múltiplo do quadrado de um número inteiro n, sendo
por isso quantificado, o que implica que a energia do
electrão não pode ter um valor qualquer, sendo também
quantificada.
Enquanto o electrão percorre determinada órbita, não
absorve nem emite energia.
Quando o electrão absorve energia, transita de uma órbita
mais interna para uma órbita mais externa.
Representação esquemática de órbitas
Diagrama de energia
Quando o electrão transita de uma órbita mais externa para uma órbita mais interna,
emite energia.
Representação esquemática de órbitas
Diagrama de energia
O electrão do átomo de hidrogénio pode ser excitado, o que implica um aumento da sua
energia, por elevação de temperatura, da amostra de hidrogénio atómico, colisão com um
electrão de elevada energia cinética, acção de uma descarga eléctrica ou acção de uma
radiação electromagnética.
Pode depois desexcitar-se, perdendo energia, através de emissão de radiação
electromagnética, isto é, emitindo um fotão.
O modelo de Bohr foi depois estendido a átomos polielectrónicos.
o número máximo de electrões por nível de energia, ou camada electrónica, é
calculado a partir da relação 2n2, sendo n o número quântico principal, o número que
determina o nível de energia considerado.
O estado fundamental corresponde a n = 1.
o último nível de energia, ou camada electrónica, só pode conter o máximo de 8
electrões, à excepção do caso em que o último nível de energia é simultaneamente o
primeiro, e aí só pode conter 2 electrões.
a energia dos electrões é quantizada.
No modelo de Bohr eram admitidas órbitas circulares para os electrões, isto é, implica o
conhecimento em simultâneo da posição e velocidade do electrão, ou seja, da sua energia,
num dado instante.
O físico alemão Werner Heisenberg (1901-1976) demonstrou que
é impossível conhecer simultaneamente a posição e a energia do
electrão no átomo, Princípio da Incerteza de Heisenberg, o que
levou à criação de outro modelo para o átomo, um modelo
baseado na Mecânica Quântica, o modelo da nuvem electrónica.
Este modelo descreve o comportamento do electrão no átomo a partir da resolução da
equação de Schrodinger.
A energia do electrão vem quantizada,
mas quanto à posição do mesmo, deixou
de ser considerada uma certeza, e
portanto deixou de se falar em órbita,
mas passou a considerar-se a
probabilidade de um electrão com uma
determinada energia se localizar no
espaço em torno do núcleo, passando a
falar-se em orbital.
Assim, uma orbital é definida como uma
região do espaço onde, sob a acção do
núcleo, o electrão com uma dada
energia tem probabilidade de se
encontrar.
Os electrões movem-se com elevada velocidade em torno dos respectivos núcleos e sem
trajectórias definidas.
O esquema abaixo mostra a representação dos modelos de Bohr e da nuvem electrónica,
para o átomo de berílio,
.
Podemos considerar a orbital como a região que envolve 90% de probabilidades de se
encontrar o electrão.
No modelo atómico de Bohr No modelo atómico actual
O electrão descreve uma órbita O electrão ocupa uma orbital
Linha onde existe a certeza de encontrar o
electrão, com uma dada energia.
Região do espaço onde há probabilidade de
se encontrar um electrão com uma dada
energia.
Números quânticos e caracterização da orbital
Para caracterizar as orbitais atómicas são necessários três parâmetros, designados por
números quânticos, que resultam da equação de Schrodinger:
número quântico principal
número quântico de momento angular
número quântico magnético
Cada um deles relaciona-se com uma característica da orbital. Assim:
o número quântico principal está relacionado com o tamanho da orbital
(distância média do electrão ao núcleo) e pode assumir os valores inteiros
1,2,3,...
o número quântico de momento angular está relacionado com a forma da orbital
(tipo de orbital)
Os valores de
dependem dos valores de
O número quântico
entre e
.
.
, só pode assumir os valores inteiros compreendidos
o número quântico magnético está relacionado com a orientação da orbital no
espaço
Os valores de
dependem do valor de
.
Estes valores são os números inteiros de
a
.
orbital
1
2
0
0
1s (1, 0, 0)
0
0
2s (2, 0, 0)
-1
2p (2, 1, -1)
0
2p (2, 1, 0)
+1
2p (2, 1, 1)
0
3s (3, 0, 0)
-1
3p (3, 1, -1)
0
3p (3, 1, 0)
+1
3p (3, 1, 1)
-2
3d (3, 2, -2)
-1
3d (3, 2, -1)
0
3d (3, 2, 0)
+1
3d (3, 2, 1)
+2
3d (3, 2, 2)
1
0
1
3
2
nº de orbitais
1
1
3
4
1
3
9
5
Um conjunto de orbitais com o mesmo valor do número quântico principal é designado
por nível de energia ou camada.
Para cada
há
Para cada
há
orbitais.
orbitais.
Tamanho, forma e orientação das orbitais
As orbitais s apresentam simetria esférica, verificando-se que o tamanho da orbital
aumenta com o número quântico .
As orbitais p apresentam dois lóbulos simétricos, tendo o núcleo como centro. Estes
lóbulos estão orientados segundo cada um dos eixos cartesianos.
Tal como nas orbitais s, o tamanho das orbitais p aumenta com o número quântico
principal.
As orbitais d apresentam uma forma mais complexa.
Energia das orbitais
Quanto maior for o número quântico principal
, maior é a energia.
E3s E2s
Em átomos monoelectrónicos a energia da orbital
só depende de .
E2s = E2p
Em átomos polielectrónicos, para um único valor
de , quanto maior o número quântico de momento
angular
, maior é a energia.
E2p E2s
Orbitais com igual número quântico de momento
angular têm a mesma energia.
E2px = E2py = E2pz
Para átomos diferentes, a energia e o tamanho
de um dado tipo de orbital são diferentes.
Discute a orbital 1s para
e
. Discussão
Caracterização do electrão: número quântico de spin
Experiências realizadas com um feixe de átomos de hidrogénio submetido a um campo
magnético, revelaram que o feixe de electrões se dividia em dois desviando-se em
sentidos opostos.
Tal comportamento resultaria de um movimento de rotação do electrão sobre si próprio
(spin).
Dado que existiam dois movimentos de rotação possíveis para o electrão, um no sentido
retrógrado, outro no sentido directo, existiriam dois estados de spin.
Criou-se, então, um quarto número quântico, o número quântico de spin
pode assumir os valores:
, que apenas
Conclusão:
Para caracterizar uma orbital são necessários três números quânticos
Para caracterizar um electrão no átomo são necessários quatro números
quânticos
.
.