Digestão e absorção de proteínas; Rui Fontes
Digestão e absorção de proteínas e aminoácidos
1-
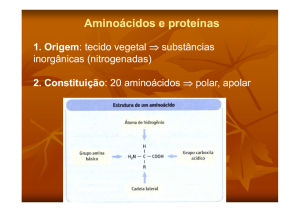
As proteínas são formadas por resíduos de aminoácidos ligados entre si (numa cadeia linear) por
ligações covalentes que os químicos designam por ligações amida. No caso particular das proteínas (e
na maioria das ligações entre os resíduos aminoacídicos dos peptídeos), essas ligações também se
costumam designar por ligações peptídicas. As ligações peptídicas são ligações amida que envolvem o
grupo α-amina de um aminoácido e o grupo carboxilo (que contém o carbono 1) do aminoácido que o
precede na cadeia (ver Fig. 1). A hidrólise destas ligações leva à separação de grupos carboxilo e αamina de dois resíduos de aminoácidos contíguos; consequentemente, a hidrólise completa de uma
proteína leva à separação dos resíduos dos aminoácidos componentes dessa proteína (ver Equação 1). A
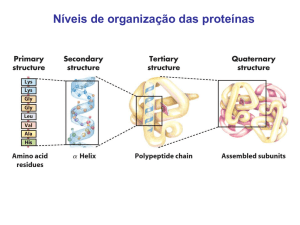
sequência de aminoácidos de uma proteína designa-se por estrutura primária e escreve-se pela mesma
ordem com que são incorporados durante a sua síntese nos ribossomas: do aminoácido que contém o
grupo α-amina livre (o terminal amina) até ao aminoácido que está no outro extremo da cadeia e contém
o grupo carboxilo do carbono 1 livre (o terminal carboxilo).
Equação 1
proteína ou peptídeo com n resíduos aminoacídicos + n-1 H2O → n aminoácidos livres
2-
O aminoácido mais simples é a glicina (CH2NH2COOH; com 2 átomos de carbono e 1 de azoto:
2C,1N). A cadeia lateral da glicina é constituída apenas por um átomo de hidrogénio e, porque nenhum
dos carbonos da glicina é assimétrico, não existem enantiómeros da glicina. Com exceção do caso da
glicina, o carbono 2 dos aminoácidos é um carbono assimétrico; ou seja, os quatro substituintes ligados
ao carbono 2 (ou α) são todos distintos: (1) o grupo amina, (2) o carbono carboxílico, (3) um átomo de
hidrogénio e (4) uma “cadeia lateral” que distingue os diferentes aminoácidos entre si. Os aminoácidos
que fazem parte das proteínas são todos α-aminoácidos e, com exceção da glicina, são todos de tipo L1.
Isto significa que, quando os aminoácidos são orientados de acordo com a convenção de Fischer, o
grupo α-amina fica voltado para a esquerda. Ou seja, quando os carbonos 1, 2 e 3 estão alinhados na
vertical, o carbono 2 está no plano do papel e os carbonos 1 e 3 estão atrás do plano do papel, o grupo
NH2 ligado no carbono 2 fica para cá do plano do papel e voltado para a esquerda. Na Fig. 2 está
representada a alanina L estando a sua molécula orientada de acordo com a convenção de Fischer.
3-
Os aminoácidos podem ser classificados tendo em conta características químicas estruturais da cadeia
lateral. Na glicina [2C,1N] e na alanina [3C,1N] a cadeia lateral é muito simples: no primeiro caso é
um átomo de hidrogénio e no segundo um grupo metilo (-CH3). Nos “aminoácidos ramificados” (o
que inclui a valina [5C,1N], a isoleucina [6C,1N] e a leucina [6C,1N]) a cadeia lateral é uma cadeia
alifática ramificada que tem 3 carbonos no caso da valina e 4 nos casos da leucina e da isoleucina.
Nalguns aminoácidos a cadeia lateral contém grupos hidroxilo e, assim, a expressão “aminoácidos
hidroxilados” refere-se à serina [3C,1N,1OH], à treonina [4C,1N,1OH] e à tirosina [9C,1N,1OH].
Dois aminoácidos que fazem parte das proteínas contêm átomos de enxofre e, assim, a expressão
“aminoácidos sulfurados” refere-se à cisteína [3C,1N,1S] e à metionina [5C,1N,1S]. Dois
aminoácidos contêm grupos carboxilo no último carbono (o aspartato [4C,1N] e o glutamato
[5C,1N]). Nos valores de pH do meio interno os grupos carboxilo das cadeias laterais dos ácidos
glutâmico e aspártico (pKa de cerca de 4) sofrem protólise e são, de facto, grupos carboxilato tendo
carga negativa. Porque os grupos carboxilo são dadores de protões, o glutamato e o aspartato são
chamados de aminoácidos acídicos. Há dois aminoácidos que contêm grupos amida (sem carga
elétrica) no último carbono: a asparagina [4C,2N] e a glutamina [5C,2N]. A asparagina distingue-se
do aspartato por conter um grupo amida em vez de um carboxilato no último carbono (o 4); o caso da
glutamina em relação ao glutamato é semelhante mas o carbono em questão é, neste caso, o 5.
Frequentemente os aminoácidos lisina [6C,2N], arginina [6C,4N] e também a histidina [6C,3N] são
associados à expressão “aminoácidos básicos”. A lisina contém um grupo amina no último carbono (o
carbono 6) em que o pKa é 12,5; ou seja, nos valores de pH existentes no meio interno, este grupo
amina está sempre protonado. Uma situação semelhante acontece no caso da arginina: a arginina
contém um grupo guanidina [1C,3N] ligado ao carbono 5. O pKa do grupo guanidina é de 10,8 e, por
1
Alguns polipeptídeos bacterianos (incluindo bactérias existentes no lúmen do colon dos seres humanos) contêm
aminoácidos D, mas não existem aminoácidos D nas proteínas bacterianas. Na tradução proteica todos os aminoácidos
incorporados são L (com exceção da glicina que não tem enantiómeros).
Página 1 de 5
Digestão e absorção de proteínas; Rui Fontes
isso, nos valores de pH existentes no meio interno, este grupo químico está sempre protonado2 . A
expressão “aminoácidos aromáticos” refere-se aos aminoácidos que têm um anel aromático na cadeia
lateral. É o caso da fenilalanina [9C,1N] que tem um anel benzénico [6C], do seu derivado hidroxilado
tirosina [9C,1N,1OH], do triptofano [11C,2N] que tem um anel indol [8C,1N] e da histidina [6C,3N]
que tem um anel imidazol [3C,2N] 3 . Assim, a tirosina tanto pode ser incluída nos aminoácidos
aromáticos como nos hidroxilados e a histidina tanto pode ser incluída nos aminoácidos aromáticos
como nos básicos. A prolina [5C,1N] é o único aminoácido presente nas proteínas em que o grupo αamina é uma amina secundária: ou seja, o azoto do grupo α-amina liga-se simultaneamente ao carbono
α e ao carbono 5 formando um anel heterocíclico com 4 carbonos e 1 azoto4.
4-
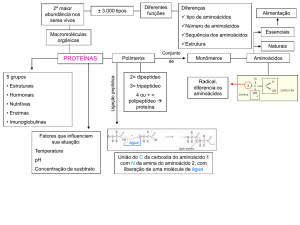
Para além de serem importantes constituintes das células e do espaço extracelular, as proteínas são
também importantes componentes da dieta constituindo na dieta ocidental típica cerca de 15% do valor
calórico total (cerca de 100 g/dia). Tal como os glicídeos, também as proteínas da dieta são hidrolisadas
durante o processo digestivo por ação catalítica de enzimas. O ambiente em que as enzimas digestivas
atuam também é importante e, neste contexto, tem importância a secreção de ácido clorídrico pelas
células parietais do estômago e a neutralização deste ácido pelo bicarbonato (HCO3-) presente no suco
pancreático e na bílis.
5-
O ácido clorídrico é segregado nas células parietais do estômago podendo o pH do estômago ser da
ordem de 1-2. O processo envolve a conversão do CO2 em ácido carbónico por ação catalítica da
anídrase carbónica (ver Equação 2) e a subsequente dissociação do ácido carbónico (protólise) em
bicarbonato + protão no citoplasma das células parietais (ver Equação 3). No polo apical (luminal)
destas células a ATPase do H+/K+ catalisa a troca de H+ que sai (contra gradiente) por K+ que entra
(também contra gradiente); a componente exergónica do processo é a hidrólise do ATP. No transporte
de Cl- do sangue para o lúmen estão envolvidos transportadores: no polo basal (contraluminal) existe
um antiporter que troca Cl- (que entra para a célula) por HCO3- (que sai para o sangue); no polo apical
existe um canal iónico que permite a saída do Cl- para o lúmen. Assim, quando as células parietais são
estimuladas a segregar ácido clorídrico, o bicarbonato que resultou da dissociação do ácido carbónico
vai alcalinizar o plasma sanguíneo. As células que forram o estômago não são normalmente agredidas
pelo ácido porque estão protegidas pelo muco (que é rico em mucina, uma glicoproteína muito
resistente à ação hidrolítica das protéases). O pH ácido do estômago tem importância na digestão
gástrica porque é o pH adequado para a ação das enzimas que aqui atuam (lípase gástrica e pepsina) e
provoca desnaturação das proteínas da dieta facilitando o acesso das enzimas à cadeia aminoacídica
destas proteínas. A estimulação da secreção ácida resulta de estímulos nervosos (via nervo vago), da
ação parácrina da histamina (sintetizada por células, designadas por enterocromafins, localizadas por
debaixo da mucosa gástrica) e da hormona gastrina. A gastrina é sintetizada por células endócrinas
localizadas na mucosa gástrica e, para além de estimular a secreção de ácido, também estimula a
secreção das enzimas digestivas gástricas por células que são designadas por células principais.
Equação 2
Equação 3
6-
CO2 + H2O ↔ H2CO3
H2CO3 ↔ H+ + HCO3-
Ao contrário da lípase gástrica e da pepsina, as enzimas que atuam no lúmen do duodeno e do intestino
têm pHs ótimos próximos da neutralidade. No lúmen do duodeno o ácido do estômago é neutralizado
pelo HCO3- dos sucos pancreático e biliar produzindo-se ácido carbónico que rapidamente (mesmo na
2
Na histidina a cadeia lateral contém um anel heterocíclico com 3 carbonos e 2 azotos designado por imidazol. Apesar de
ser costume classificar a histidina como um aminoácido básico, a verdade é que o pKa da forma livre do anel imidazol é
6,0 e não será muito diferente de 6 quando a histidina é um resíduo de uma proteína. Assim, é de prever que, ao contrário
do que acontece nos casos da arginina e da lisina, a cadeia lateral da maioria das moléculas livres e dos resíduos de
histidina estejam na forma desprotonada. Apesar de, na histidina, a forma protonada só predominar sobre a forma
desprotonada quando o pH do meio é inferir a 6, é frequente agrupar-se a histidina com os outros dois aminoácidos
básicos.
3
Enquanto nos anéis benzénicos (presentes na fenilalanina e na tirosina) os átomos que formam o anel são todos átomos
de carbono, os anéis indol e imidazol dizem-se heterocíclicos porque contêm átomos de carbono e de azoto. O anel indol
(presente no triptofano) pode ser descrito como um anel benzénico ligado a um anel pirrol [4C,1N].
4
Nalguns livros de texto a prolina é classificada como sendo um iminoácido. Na opinião do autor deste texto, a expressão
não é adequada porque num grupo imina existe um átomo de azoto ligado a um átomo de carbono através de uma ligação
dupla e não é isto que acontece na prolina.
Página 2 de 5
Digestão e absorção de proteínas; Rui Fontes
ausência de anídrase carbónico) se converte em CO2 e H2O (ver Equação 3 e Equação 2). O CO2 é um
gaz que passa por difusão simples (não mediada) para o sangue e acaba por sair do organismo nos
pulmões. O pH 7-8 do lúmen intestinal é adequado para a ação das enzimas digestivas
pancreáticas e intestinais. O bicarbonato é sintetizado e segregado num processo em que também
participa a anídrase carbónica (ver Equação 2 e Equação 3) e que ocorre nas células dos canalículos
pancreáticos. Tal como nas células parietais do estômago, através da ação da anídrase carbónica e a
subsequente protólise formam-se protões e iões bicarbonato no citoplasma das células (ver Equação 2 e
Equação 3). No entanto, ao contrário do que acontece nas células parietais, o bicarbonato sai no polo
luminal (via trocador Cl-/HCO3-) sendo um componente do suco pancreático, enquanto o protão sai para
o sangue no polo basal via transporte ativo primário ou secundário. O estímulo para a secreção de
bicarbonato tem origem na secretina, uma hormona sintetizada por células endócrinas situadas no
epitélio intestinal. A secretina também tem ação estimuladora na secreção exócrina pancreática de
enzimas digestivas mas, neste papel, tem maior relevância a colecistocinina. A colecistocinina é uma
outra hormona sintetizada por outras células endócrinas situadas no mesmo epitélio intestinal e, para
além de estimular a secreção de enzimas digestivas pancreáticas (pelas células acinares do pâncreas),
também estimula a contração da vesícula biliar e a consequente descarga de bílis no lúmen duodenal. A
síntese destas duas hormonas é estimulada pela presença de oligopeptídeos no lúmen duodenal; estes
oligopeptídeos resultaram da ação da pepsina nas proteínas da dieta.
7-
Na digestão das proteínas que, num dado momento, estão presentes no lúmen do tubo digestivo
participam protéases (hidrólases de proteínas) com origem nas células principais do estômago
(pepsina), nas células acinares pancreáticas (tripsina, quimotripsina, elástase e carboxipeptídase A e
B) e nos enterócitos (aminopeptídases e dipeptídases). Por ação destas enzimas ocorre rotura das
ligações peptídicas das proteínas gerando-se peptídeos com tamanho cada vez menor e, no final do
processo, aminoácidos. A pepsina, a tripsina, a quimotripsina, a elástase e a enteropeptídase (ver
abaixo) dizem-se endopeptídases porque catalisam a rotura de ligações peptídicas situadas no
“interior” da estrutura primária dos seus substratos. Pelo contrário, as carboxipeptídases (libertam o
aminoácido da extremidade carboxílica), as aminopeptídases (libertam o aminoácido da extremidade
amina) e as dipeptídases dizem-se exopeptídases porque atuam em ligações peptídicas das
extremidades e da sua ação catalítica resulta a libertação de aminoácidos. Embora sejam muito
inespecíficas no que se refere aos seus substratos, cada uma das enzimas proteolíticas atua
preferencialmente em ligações peptídicas que envolvam determinados aminoácidos e estas
“preferências” são diferentes de enzima para enzima5. As protéases e peptídases digestivas são capazes
de catalisar a hidrólise das proteínas da dieta, das proteínas que fazem parte das células da mucosa que
“descamam” (em constante renovação), assim como das próprias enzimas digestivas (que também são
proteínas6). De facto, se admitirmos uma ingestão diária de cerca 60-80 g de proteínas na dieta, uma
massa semelhante de proteínas endógenas é diariamente vertida no lúmen digestivo e apenas uma
fração menor (o equivalente a cerca de 10 g de proteínas/dia) de produtos de origem proteica aparece
nas fezes [1]. A maior parte do azoto das fezes é constituinte das proteínas das bactérias que povoam o
intestino grosso. Estas bactérias usam os produtos nitrogenados que escaparam à absorção no intestino
delgado como substratos do seu metabolismo aminoacídico e para a sua síntese proteica [2].
8-
A pepsina é segregada no estômago como um zimogénio inativo (pepsinogénio) que, em contacto com
o pH ácido do estômago, se hidrolisa gerando a enzima ativa (pepsina) e um polipeptídeo inativo (ver
Equação 4). A separação do polipeptídeo torna o centro ativo da enzima acessível aos seus substratos. A
ativação do pepsinogénio também ocorre por autocatálise: a própria pepsina tem atividade hidrolítica
sobre o pepsinogénio promovendo a ativação deste a pepsina.
Equação 4
zimogénio + H2O → enzima ativa + polipeptídeo inativo
5
A pepsina atua preferencialmente em ligações peptídicas em que o aminoácido que participa com o grupo carboxilo é
um aminoácido aromática e hidrofóbico (concretamente o triptofano, tirosina, fenilalanina ou leucina); ou seja, se
representarmos a proteína alvo pela sequência AA(1-N terminal)-…-AA(x-1)-AA(x)-…-AA(carboxilo terminal), a pepsina tem
preferência por ligações peptídicas AA(x-1)-AA(x) em que o aminoácido AA(x-1) é um dos aminoácidos listados acima. No
caso da quimotripsina a preferência é semelhante. No caso da tripsina o aminoácido AA(x-1) é a arginina ou a lisina e no
caso da elástase é a glicina, a alanina ou a serina.
6
As enzimas digestivas são extensamente glicosiladas e isto faz com que sejam relativamente maus substratos da ação
digestiva; por isso, a sua hidrólise ocorre de forma relativamente lenta e a sua inativação é tardia.
Página 3 de 5
Digestão e absorção de proteínas; Rui Fontes
9-
As protéases de origem pancreática também são segregadas como zimogénios inativos; são o
tripsinogénio, o quimotripsinogénio, a pró-elástase e as pró-carboxipeptídases A e B. No duodeno
e jejuno proximal, a enteropeptídase (às vezes impropriamente designada por enteroquínase) catalisa a
hidrólise do tripsinogénio levando à formação de tripsina (ver Equação 4). (A enteropeptídase é uma
endopeptídase e, por isso, na sua ação sobre o tripsinogénio, resulta a tripsina e um polipeptídeo
inativo.) A tripsina formada vai, por sua vez, catalisar a hidrólise do quimotripsinogénio, da próelástase e das pró-carboxipeptídases A e B levando à formação de enzimas ativas, que se designam,
respetivamente, por quimotripsina, elástase e carboxipeptídases A e B (ver Equação 4). Até há pouco
tempo pensava-se que, à semelhança do que acontece no caso do pepsinogénio/pepsina, a tripsina podia
hidrolisar a ligação peptídica que leva à conversão de tripsinogénio em tripsina, mas não é essa a
convicção atual; esta conversão é estritamente dependente da ação da enteropeptídase [2]. A
enteropeptídase é uma ectohidrólase que está “ancorada” na membrana apical dos enterócitos do
intestino delgado proximal com o centro ativo voltado para o lúmen. Esta localização faz com que a
ativação do tripsinogénio e a consequente ativação dos outros zimogénios apenas ocorra no lúmen do
tubo digestivo prevenindo a autodigestão do pâncreas.
10-
Da ação combinada das enzimas proteolíticas pancreáticas e da pepsina resultam alguns aminoácidos
livres e polipeptídeos, mas a digestão destes últimos continua por ação de outras ectohidrólases
(aminopeptídases e outras peptídases) que, tal como a enteropeptídase, estão ancoradas na membrana
apical dos enterócitos. (A fosfátase alcalina é também uma ectohidrólase da membrana dos enterócitos
que catalisa a desfosforilação hidrolítica de fosfoproteínas.) Estes processos podem levar à formação de
aminoácidos livres no lúmen intestinal, mas a absorção pode ocorrer em fases menos avançadas da
digestão das proteínas [3].
11-
A absorção ocorre nos enterócitos, cuja membrana apical tem múltiplas projeções em forma de
“dedo” que se designam de microvilosidades: ao conjunto dá-se o nome de bordadura em escova. Por
sua vez, os enterócitos e outras células do epitélio intestinal formam uma camada epitelial contínua que
limita projeções digitiformes que se designam de vilosidades intestinais. Quer as microvilosidades quer
as vilosidades intestinais contribuem para aumentar enormemente a área de absorção. A absorção das
proteínas é um processo complexo podendo fazer-se na forma de aminoácidos, de dipeptídeos, de
tripeptídeos ou mesmo de proteínas inteiras.
12-
No polo apical dos enterócitos, o transporte dos aminoácidos envolve vários simportes em que, na
maioria dos casos, o Na+ é cotransportado com os aminoácidos (transporte ativo secundário em que o
componente exergónico é o transporte de Na+)7. No caso dos di- e tripeptídeos o único transportador
conhecido é um simporte peptídeo/H+ (PEPT1; da expressão inglesa “peptide transporter 1”)
altamente inespecífico relativamente aos aminoácidos constituintes do peptídeo transportado [3]. A
energia envolvida neste transporte é, pelo menos em parte, a que resulta do gradiente eletroquímico do
protão. Os protões têm tendência a entrar nas células devido ao potencial elétrico ser negativo no
interior, acoplando (via PEPT1) a entrada de di- e tripeptídeos. Os protões presentes no lado luminal da
membrana apical dos enterócitos resultaram da ação de um trocador Na+/H+ que catalisa a troca de um
protão que sai para o lúmen por um ião Na+ que entra a favor do gradiente eletroquímico.
13-
Os di- e tripeptídeos e outros peptídeos incompletamente digeridos que foram absorvidos são
maioritariamente hidrolisados por diversas peptídases do citoplasma dos enterócitos. No polo basal
dos enterócitos os múltiplos sistemas transportadores de aminoácidos são distintos dos que existem no
polo apical e, na maioria dos casos, são uniportes, não envolvendo cotransporte de iões inorgânicos. Na
maioria dos casos, os aminoácidos que entraram para os enterócitos ou foram aí libertados via hidrólise
de peptídeos entram na corrente sanguínea através do sistema porta hepático. No entanto, alguns
aminoácidos (com particular destaque para a glutamina) são, em grande parte, oxidados nos enterócitos
sendo aqui importantes nutrientes do ponto de vista energético [3]. O transporte catalisado pelos
uniportes da membrana basal é passivo, ou seja, o sentido em que ocorre depende do gradiente de
concentrações: participam na absorção de aminoácidos dos enterócitos para o sangue mas, em
7
No caso de aminoácidos com carga global positiva (como a arginina e a lisina) o transporte pode não depender do Na+,
mas depende também da ação da ATPase do Na+/K+: a energia envolvida no processo é o potencial elétrico negativo no
interior das células (criado pela ATPase do Na+/K+) que atrai os aminoácidos com carga global positiva.
Página 4 de 5
Digestão e absorção de proteínas; Rui Fontes
condições metabólicas em que os enterócitos estão a consumir aminoácidos presentes no plasma
sanguíneo, catalisam o transporte de aminoácidos em sentido inverso.
14-
Apesar de existirem enzimas capazes de hidrolisar completamente as proteínas da dieta, algumas
moléculas escapam ao processo e podem aparecer intactas no plasma sanguíneo. A absorção de
proteínas inteiras pode ocorrer por dois mecanismos. Um deles, designado por transcitose e envolve a
endocitose no polo luminal dos enterócitos e a subsequente exocitose no polo basal. O outro, designado
por transporte paracelular, envolve a passagem das moléculas proteicas através dos espaços entre os
enterócitos; isto pode ocorrer quando há lesão das junções impermeáveis (tight junctions) que
normalmente impedem esta passagem. A entrada de moléculas proteicas do lúmen intestinal para o
sangue é mais frequente nos bebés que nos adultos e permite que os anticorpos presentes no leite
materno desempenhem um papel na proteção do bebé. No entanto, uma outra consequência é a maior
propensão para a ocorrência de alergias alimentares nos bebés.
1. Matthews, D. E. (2006) Proteins and aminoacids in Modern Nutrition in Health and Disease (Shils, M. E., ed) pp. 23-61,
Lippincott, Phyladelphia.
2. Moughan, P. & Stevens, B. (2013) Digestion and absorption of proteins in Biochemical, physiological and molecular aspects of
human nutrition (Stipanuk, M. H. & Caudill, M. A., eds) pp. 162-178, Elsevier, St. Louis.
3. Daniel, H. (2004) Molecular and integrative physiology of intestinal peptide transport, Annu Rev Physiol. 66, 361-84.
Fig. 1. O tetrapeptídeo seril-valil-alanil-glicina.
Fig. 2: Estrutura da alanina que existe nos seres vivos (alanina L).
Página 5 de 5