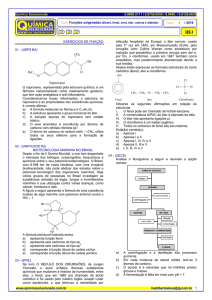
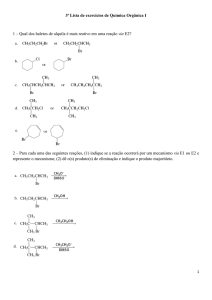
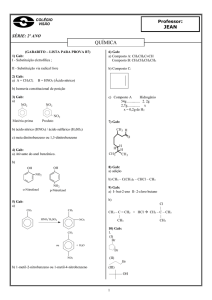
Dicas de Química ‐ Arilson Questão 01)
A acidez e a basicidade são importantes propriedades relacionadas às substâncias orgânicas. Essas propriedades
possuem relação direta com a reatividade e a purificação dos compostos orgânicos.
NO 2
CH3
OH
OH
OH
A
B
C
Considerando essas informações e as estruturas apresentadas ao lado, faça o que se pede.
a)
Dê o nome oficial (IUPAC) das substâncias A, B e C.
b)
Coloque em ordem crescente de acidez as substâncias A, B e C.
c)
Explique a diferença de acidez entre as substâncias A, B e C.
d)
Escreva a equação balanceada da reação de B e C com quantidade estequiométrica de NaOH.
Gab:
a)
A 4-metilfenol ou para-metilfenol ou 4-metilbenzenol
B fenol ou benzenol
C 4-nitrofenol ou 4-nitrobenzenol ou para-nitrofenol
b)
A<B<C
c)
O NO2 presente na substância C apresenta efeito indutivo retirador de elétrons, o que provoca um aumento
da acidez da substancia. Já na substância A o CH3 presente apresenta efeito indutivo doador de elétrons, o
que provoca efeito contrário, ou seja, diminuição da acidez. No caso da substância B, esta presente o
átomo de hidrogênio, ficando com valor de acidez entre o da substância A e C.
d)
+ H2O
+ NaOH
ONa
OH
B
NO 2
NO2
+ H2O
+ NaOH
OH
ONa
C
Questão 02)
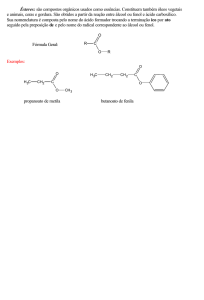
Tendo em vista a figura abaixo, que representa a fórmula estrutural de um composto orgânico:
M eO
a)
mencione as funções orgânicas encontradas na estrutura da substância;
b)
mencione quantos centros quirais (carbonos assimétricos) existem na estrutura da molécula;
c)
desenhe as fórmulas estruturais dos produtos orgânicos formados na reação entre a substância apresentada
com excesso de NaOH, sob aquecimento.
Gab:
a)
Éter, éster
b)
Três centros quirais
c)
CO 2Et
M eO
CO2Et
aquecimento
NaOH
CO2-Na+
M eO
+ EtOH
Produtos
Questão 03)
O resveratrol é uma substância orgânica encontrada em casca de uva vermelha, e é associada à redução da
incidência de doenças cardiovasculares entre os habitantes de países nos quais ocorre consumo moderado de
vinho tinto. Mais recentemente, foi encontrada outra substância com propriedades semelhantes, na fruta
“blueberry” (conhecida no Brasil como mirtilo), substância esta denominada pterostilbeno.
As fórmulas estruturais do resveratrol e do pterostilbeno são fornecidas a seguir.
OH
H
HO
C
OH
H
C
H3CO
C
C
H
OH
OCH 3
Pterostilbeno
a)
Escreva o nome de todas as funções químicas oxigenadas presentes no resveratrol e pterostilbeno.
b)
Identifique o tipo de isomeria e escreva as fórmulas estruturais dos isômeros que o pterostilbeno pode
formar, considerando-se que as posições dos substituintes em seus anéis aromáticos não se alteram e que
esses anéis não estejam ligados a um mesmo átomo de carbono.
Gab:
a)
Resveratrol
H
OH
H
HO
Fenol
OH
H
C
C
H 3CO
C
C
H
H
OH
Fenol
Resveratrol
OCH3
Éter
Pterostilbeno
b)
Isomeria geométrica ou cis-trans:
OH
H3CO
H
H
H
C
C
H3CO
C
C
H
OH
OCH3
isômero cis
OCH3
isômero trans
Questão 04)
Os fogos de artifício propiciam espetáculos em diferentes eventos. Para que esses dispositivos funcionem,
precisam ter em sua composição uma fonte de oxigênio, como o clorato de potássio (KClO3), combustíveis,
como o enxofre (S8) e o carbono (C), além de agentes de cor como o SrCl2 (cor vermelha), o CuCl2 (cor verde
esmeralda) e outros. Podem conter também metais pirofóricos como Mg que, durante a combustão, emite intensa
luz branca, como a do flash de máquinas fotográficas.
a)
Escreva as equações químicas, balanceadas, que representam:
— a decomposição do clorato de potássio, produzindo cloreto de potássio e oxigênio diatômico;
— a combustão do enxofre;
— a combustão do magnésio.
b)
Considerando o modelo atômico de Rutherford-Bohr, como se explica a emissão de luz colorida pela
detonação de fogos de artifício?
Gab:
a)
Decomposição do clorato de potássio, produzindo cloreto de potássio e oxigênio diatômico;
2KClO3(s) 2KCl(s) + 3O2(g)
A combustão do enxofre;
2S(s) + 3O2(g) 2SO3(g)
A combustão do magnésio;
2Mg(s) + O2(g) 2MgO(s)
b)
Durante o processo de queima, ocorre a excitação dos elétrons para níveis mais externos que, de acordo
com o modelo de Rutherford-Bohr, possuem maior energia. Quando esses elétrons retornarem para níveis
mais internos, de menor energia, ocorrerá liberação de luz de cores diferentes para elementos diferentes.
Questão 05)
O eixo y da figura abaixo representa as temperaturas de ebulição de compostos dos elementos das famílias 14 e
16 da tabela periódica. No eixo x tem-se os valores das massas molares. Levando-se em consideração o gráfico a
seguir, responda aos itens abaixo:
a)
Explique o comportamento observado para os pontos de ebulição nos compostos da família do carbono.
b)
Explique por que a água apresenta ponto de ebulição superior ao dos demais compostos do grupo do
oxigênio e por que essa discrepância não ocorre com os compostos da família do carbono.
Gab:
a)
Com o aumento da massa molar ocorre aumento da temperatura de ebulição.
b)
Por que a água estabelece ligações de hidrogênio, na família do carbono isso não ocorre.
Questão 06)
O gráfico a seguir representa o estudo cinético de uma reação R → P.
Sabendo-se que o consumo do reagente se dá conforme a equação [R] = 1/t, e a formação do produto pela
equação [P] = 1 – 1/t, com t, o tempo, em segundos,
a)
determine o instante, em segundos, em que a concentração dos reagentes é igual à dos produtos;
b)
represente o gráfico do estudo cinético após a adição de um catalisador.
a)
t = 2s
b)
Com a adição do catalisador, o instante em que as concentrações dos reagentes e produtos se igualam é
menor do que 2s, ou seja menor do que t2.
Gab:
Questão 07)
O potássio metálico, quando exposto ao ar, reage com o oxigênio, produzindo o K2O(s). Considerando essa
espécie química,
a)
calcule o calor de formação desse composto, sabendo que:
(I)
K(s) + H2O(l) KOH(aq) + ½H2(g)
H = –314kJ
(II)
K2O(s) + H2O(l) 2KOH(aq)
H = –335kJ
(III)
H2(g) + ½O2(g) H2O(l)
H = –286
b)
Mostre a equação química balanceada representativa de sua reação com a água.
a)
Hf = –579kJ
b)
K(s) + H2O(l) KOH(aq) + ½H2(g)
Gab:
Questão 08)
A proporção do isótopo radioativo do carbono (14C), com meia-vida de, aproximadamente, 5.700 anos, é
constante na atmosfera. Todos os organismos vivos absorvem tal isótopo por meio de fotossíntese e alimentação.
Após a morte desses organismos, a quantidade incorporada do 14C começa a diminuir exponencialmente, por não
haver mais absorção.
a)
Balanceie a equação química da fotossíntese, reproduzida na folha de respostas, e destaque nela o composto
em que o 14C foi incorporado ao organismo.
Luz solar
CO2 + H2O C6H12O6 + H2O +
O2
b)
Por que um pedaço de carvão que contenha 25% da quantidade original de 14C não pode ser proveniente de
uma árvore do início da era cristã?
c)
Por que não é possível fazer a datação de objetos de bronze a partir da avaliação da quantidade de 14C?
Gab:
a)
Luz solar
6 CO2 + 12 H2O C6H12O6 + 6H2O + 6O2
Quimicamente, a reação de fotossíntese pode ser representada pela equação balanceada:
Luz solar
6CO2 + 6H2O C6H12O6 + 6O2
b)
Porque o tempo total do processo seria de 11.400 anos
Um pedaço de carvão com essas características só poderia provir de uma árvore morta antes do início da era
cristã, ou seja, há mais de 2010 anos.
c)
Porque o bronze é fundamentalmente uma liga entre cobre e estanho. Não há carbono-14 para se efetuar a
datação.
Questão 09)
O cumeno é uma substância química de grande interesse industrial, pois quando submetido a uma reação de
oxidação é possível obter fenol e acetona. Uma variedade de métodos pode ser empregada na produção de
cumeno; o esquema a seguir é um exemplo:
Cl
+ CH3
CH
CH3
catalisador
CH3
CH
CH3
Fenol
catalisador
oxidação
Acetona
a)
Identifique o tipo de reação envolvida na produção do cumeno a partir do benzeno e do 2-cloropropano, em
presença de catalisador.
b)
Forneça as fórmulas estruturais do fenol e da acetona.
c)
Dê o nome, segundo a IUPAC, do cumeno.
Gab:
a)
Substituição
b)
OH
O
H3C
C
CH 3
Acetona
fenol
c)
Isopropilbenzeno
Questão 10)
O fluxograma ao abaixo representa um processo para a produção de magnésio metálico a partir dos íons Mg2+
dissolvidos na água do mar.
a)
Preencha a tabela abaixo com as fórmulas químicas das substâncias que foram representadas, no
fluxograma, pelas letras A, B, C e D.
Substância
A
B
C
D
Fórmula química
b)
Escreva as duas semirreações que representam a eletrólise ígnea do MgCl2, identificando qual é a de
oxidação e qual é a de redução.
c)
Escreva a equação química que representa um método, economicamente viável, de produzir a substância A.
Gab:
a)
Substância
A
B
C
Fórmula química CaO Mg(OH)2 Cl2
D
HCl
b)
(ânodo) 2Cl-
Cl2 + 2e-, oxidação do Cl-
(cátodo) Mg2+ + 2e-
Mg, redução do Mg2+
c)
A substância A (CaO) é produzida por pirólise do calcário (CaCO3), de acordo com a equação:
CaCO3 CaO + CO2