Artigo
Citomegalovírus: Revisão dos Aspectos
Epidemiológicos, Clínicos, Diagnósticos e de
Tratamento
Jader Joel Machado Junqueira1, Talita Marçal Sancho1 e Vera Aparecida dos Santos2
1. Acadêmico(a) do Curso de Medicina da Faculdade de Medicina da Universidade de São Paulo (FMUSP)
2. MD, PhD, Patologista Clínica, Diretora do Serviço de Imunologia da Divisão de Laboratório Central do Hospital das Clínicas da FMUSP (DLC-HCFMUSP)
Serviço de Imunologia da Divisão de Laboratório Central do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
Resumo
Summary
O citomegalovírus (CMV) é um herpesvírus humano
que ocorre em todas as regiões do mundo, variando com
as condições socioeconômicas locais. Possui como característica peculiar sua capacidade de latência, podendo
ser reativado em diferentes circunstâncias. É considerado
um dos mais importantes patógenos oportunistas do paciente imunocomprometido
A contaminação ocorre por meio de contato com
secreções corpóreas contaminadas, por transmissão
horizontal ou vertical, tanto por vias naturais como por
via iatrogênica.
A doença clínica é rara em indivíduos imunocompetentes. No entanto, em imunocomprometidos, a infecção
se torna sintomática e pode resultar em sérias complicações, com o possível envolvimento de órgãos. No caso
de indivíduos com AIDS, a imunossupressão aumenta a
atividade do CMV, levando a um efeito deletério.
Esta revisão visa a apresentar os principais aspectos
epidemiológicos, clínicos, diagnósticos e tratamentos de
infecções por CMV em suas várias formas de transmissão.
São discutidos também a etiologia e o ciclo viral.
Cytomegalovirus: Review of epidemiologics,
clinics, diagnostics and treatments aspects
Cytomegalovirus (CMV) is a human herpesvirus that occurs in all regions of the world, variating with local socioeconomics conditions. It has as peculiar characteristic its capacity
of latency and can be reactivated in different circumstances.
It is considerated one of de most importants opportunists
pathogens of the immunodepressed patient.
The contamination happens through contact with contaminated body secretions, by horizontal or vertical transmission,
both in natural and iatrogenic ways.
The clinic disease is rare in immunocompetents individuals. But in immunodepresseds, the infection becomes
symptomatic and can result in important disorders, with
possible organs involvement. In individuals with AIDS, the
immunossupression increases the activity of the CMV, leading
to a deletery effect.
This review has as objective to present the main epidemiological, clinics aspects, diagnoses and treatment in infection
by CMV in its many forms of transmission. The etiology and
cycle of the virus are also discussed.
Palavras-chave: Citomegalovírus, epidemiologia,
diagnóstico, sintomas e sinais
Keywords: Cytomegalovirus, epidemiology, diagnoses,
clinics aspects
Etiologia
O citomegalovírus (CMV), também conhecido como HHV-5, é um
herpesvírus humano (HHV) e pertencente à família Herpesviridae,
assim como o vírus varicela-zoster,
o vírus Epstein-Barr o HHV-8 (vírus
associado ao Sarcoma de Kaposi),
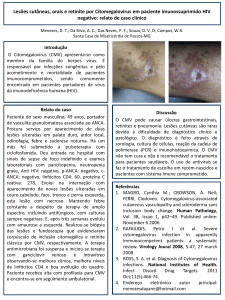
e subfamília β-Herpesvirida. Seu
88
genoma é constituído de DNA que
se encontra na interior de um capsídeo protéico icosaédrico, o qual é
rodeado por uma camada amorfa
de proteínas, chamada tegumento e
envolvido por uma bicamada lipídica,
onde se encontram as glicoproteínas
virais (1-7) (Figura 1).
O capsídeo é montado inicialmen-
te com a formação de um cadafalso
interno de proteínas, seguido pela
clivagem proteolítica, remoção do
cadafalso e empacotamento do genoma viral no núcleo (8).
Uma característica peculiar desse
vírus é a sua capacidade de latência.
Assim, após uma infecção primária,
geralmente assintomática, o vírus
NewsLab - edição 86 - 2008
Figura 1
não é eliminado do organismo e,
como os outros herpesvírus, permanece ali de forma latente, e sua
viremia se mantém em níveis reduzidos. Em diferentes circunstâncias,
ele pode ser reativado como, por
exemplo, em casos de gestação,
uso de drogas imunossupressoras,
AIDS ou qualquer outro fator que
altere o sistema imunitário, causando
diversas doenças como pneumonia,
esofagite, encefalite, hepatite, pancreatite, gastrite, enterite, colite e
retinite (1, 4-7, 9-11).
Apesar de possuir replicação inteiramente intracelular, o que impede
a ação de anticorpos neutralizantes,
o CMV pode ser facilmente inativado
por fatores físico-químicos. Sua vida
média a 37ºC é de 45min. O único
reservatório para a transmissão dos
CMV em humanos é o próprio homem.
Para haver contaminação é necessário o contato íntimo já que secreções
biológicas como sêmen, secreções
vaginais, saliva e urina atuam como
vetores. Além disso, pode haver contaminação horizontal por transfusão
de órgãos e sangue. Uma última forma
de contaminação ocorre por transmissão vertical durante a gestação
(via transplacentária), no momento
do parto ou no período pós-natal (via
leite materno) (3-5, 12, 13).
A infecção primária em recém-
90
nascidos e a reativação do vírus em
pacientes imunocomprometidos podem levar a severas patologias (14).
CICLO VIRAL
A aquisição ou infecção primária
por CMV é resultado da introdução de
vírus em um hospedeiro humano. O
DNA do CMV, após atacar a superfície
celular da célula hospedeira, entra no
seu núcleo e começa um processo de
replicação, tendo como conseqüência
a liberação de novos vírus no sangue
e em outros fluidos corporais (Figura
2). A infecção por CMV provoca um
impacto dramático na célula, que
começa imediatamente após a infecção e continua mais tardiamente. A
replicação do CMV depende dos produtos genéticos da célula hospedeira
trabalhando em conjunto com as
funções virais e leva a uma dramática
desregulação da expressão do ciclo
genético da célula. O ciclo replicatório
segue uma cascata de eventos que
depende das funções tanto da célula
viral quanto da célula do hospedeiro.
A replicação do DNA viral começa
entre 14 e 24 h após a infecção. Esse
processo causa mudanças na forma
da célula hospedeira, metabolismo e
transcrição genética, componentes
essenciais para uma replicação eficiente (14).
O ciclo replicatório dura aproxi-
madamente 24h e consiste de três
fases:
• 1ª Fase (4h) – Há a produção
de proteínas regulatórias
• 2ª Fase (8h) – Há a produção
da DNA polimerase viral
• 3ª Fase (12h) – Há produção de
proteínas estruturais e montagem de
novos vírus
Em um paciente imunocompetente, a maior parte do vírus é destruída
(por células T citotóxicas específicas
para CMV) e a infecção procede de
forma assintomática. A presença desta
infecção assintomática é baseada na
detecção de CMV nos fluidos corporais.
O período de incubação, após a infecção, é de quatro a 12 semanas, quando o antígeno já pode ser detectado.
Nesse período, há o aparecimento de
IgM-CMV ou, mais tarde, aumento de
cerca de 400% no nível de IgG-CMV.
No entanto, em pacientes imunocomprometidos que não receberam
os tratamentos adequados contra
CMV, a infecção se torna sintomática
(CMVD – CMV Disease) e com possível
envolvimento de órgãos (5), como é
mostrado na Figura 2.
Figura 2
NewsLab - edição 86 - 2008
Os CMV podem permanecer latentes no interior de vários órgãos
e ser reativados em decorrência de
depressão da imunidade celular, em
situações como a gravidez e doenças
como a AIDS, ou quando do uso de
drogas imunossupressoras (1, 4-6,
9-11, 15).
O CMV pode infectar a retina, trato gastrointestinal, fígado, pulmões
e sistema nervoso. A manifestação
mais comum é a retinite, responsável
por 85% de todos os casos de sintomas clínicos do CMV. Doenças gastrintestinais são a segunda mais comum
e incluem esofagite, colite, gastrite e
hepatite. Acometimento do sistema
nervoso central ocorre em menos
de 1% dos casos. Infecções recorrentes por CMV podem ser causadas
por reativação do vírus causador da
infecção primária ou por reinfecção.
A reinfecção tem sido observada em
casos de exposição a cepas diferentes
de CMV (1, 3-6, 9-11, 16).
EPIDEMIOLOGIA
As infecções por CMV são muito
freqüentes, porém observa-se que
a doença clínica é rara em crianças
e adultos imunocompetentes. Entre
30% e 90% dos adultos imunocompetentes apresentam anticorpos
IgG-CMV presentes no organismo,
sendo descritos como soropositivos
para CMV (5, 15-17).
Estudos de soroprevalência de
anticorpos anti-CMV na população
mundial demonstraram que o CMV
ocorre em todas as regiões do mundo
(18), sendo inversamente proporcional ao status socioeconômico do
local. Isso permite que dentro de
uma mesma região haja grandes variações de prevalência. Nos EUA, por
exemplo, foi mostrado que, enquanto
em áreas socioeconomicamente su-
92
periores 60% das gestantes tinham
anticorpos anti-CMV, em áreas socioeconomicamente inferiores 85% das
gestantes os tinham (19).
A explicação para essa variação
de acordo com as áreas pode ser
dada pelo fato de a transmissão
viral depender, em grande parte,
da higiene, moradia e hábitos da
população, já que, como já foi dito,
o CMV é encontrado em praticamente todos os líquidos corporais.
É importante ressaltar ainda que os
fatores paridade e idade também
influenciam de forma crescente
na prevalência da doença. Além
disso, pelo fato de a mulher estar,
cada vez mais, trabalhando fora de
casa, um número maior de crianças
passou a habitar, por mais tempo,
creches e escolas, facilitando a
transmissão. Quando um indivíduo
introduz o vírus em casa, aproximadamente 50% dos moradores
apresentarão soroconversão num
prazo de seis meses em média (1,
5, 20, 21).
Acima de 20% das crianças nos
Estados Unidos contrairão o CMV
antes da puberdade. Essas crianças
podem, por sua vez, ser reinfectadas por diferentes linhagens do
vírus. A infecção é também comum
na adolescência e corresponde
diretamente ao início da atividade
sexual (17).
A infecção primária pelo CMV
pode ocorrer no período pré-natal,
perinatal ou pós-natal, tanto por
vias naturais quanto por via iatrogênica (3).
Infecção Congênita
A prevalência de infecção congênita por CMV é variável em diversas
partes do mundo, atingindo taxas
de 0,2% a 2,6% de todos os nasci-
mentos. Para mulheres gestantes,
a fonte mais provável de infecção
é o contato com urina ou saliva de
crianças jovens, principalmente
seus próprios filhos (20, 22, 23).
O CMV pode infectar o feto tanto
durante a infecção primária materna, quanto durante a reativação da
infecção materna presente antes da
concepção. As infecções primárias
ocorrem em 1%-4% das mulheres
gestantes soronegativas e levam à
infecção do feto em 40%-50% dessas gestações. A reativação do CMV
materno ou reinfecção com uma
linhagem diferente leva à infecção
fetal em cerca de 1% das mulheres
gestantes soropositivas. Portanto,
a infecção primária é muito mais
danosa ao feto que sua reativação
e a presença, no feto, de anticorpos
maternos não lhe confere proteção
contra a infecção congênita. As
manifestações clínicas são quase
exclusivas de recém-nascidos de
mães com infecção primária durante principalmente a primeira metade da gestação (15, 20, 24).
Aproximadamente 10% das
crianças infectadas por via congênita são sintomáticas ao nascimento, apresentando a doença
congênita por CMV que inclui as
seguintes manifestações: retardo
do crescimento intra-uterino, prematuridade, icterícia colestática,
hepato-esplenomegalia, púrpura,
plaquetopenia, pneumonite intersticial e as manifestações neurológicas: microcefalia, calcificações
intracranianas, crises convulsivas
no período neonatal, coriorretinite
e deficiência de acuidade visual e
auditiva. Das 90% assintomáticas,
10%-15% desenvolverão sintomas
dentro de alguns meses ou mesmo
anos (15, 25, 26).
NewsLab - edição 86 - 2008
A infecção congênita pode ocorrer em qualquer época da gestação,
não estando ainda estabelecido, no
homem, uma relação entre época
da infecção materna e risco de
infecção ou sintomas no recémnascido, mesmo porque a maioria
das infecções por CMV durante a
gestação são subclínicas. Porém,
sabe-se que se a infecção ocorrer
no primeiro trimestre o risco de
conseqüências clínicas para o feto
é maior (35 a 45%) do que se a
infecção ocorrer nos dois últimos
trimestres (0 a 25%). Como poucos recém-nascidos são rastreados
para CMV, o verdadeiro impacto
da infecção congênita por CMV é
subestimado (1,20).
Acredita-se que o vírus seja
transmitido quando leucócitos
infectados atravessam a placenta
(transmissão vertical), via cordão
umbilical, instalando-se no epitélio
tubular renal, onde ocorre a replicação (27).
O CMV congênito é um objetivo
primário de prevenção não só devido ao substancial fardo de sua doença, mas também porque a biologia
e a epidemiologia do CMV sugerem
que há caminhos para reduzir a
transmissão viral. Devido ao fato
de a exposição à saliva ou urina de
crianças jovens ser a principal causa
de infecção por CMV entre mulheres
grávidas, é provável que a higiene
pessoal, especialmente o hábito de
lavar as mãos, possa reduzir o risco
de aquisição de CMV (20). Infecção Perinatal
As infecções adquiridas no período peri-parto e até três semanas
pós-natais são denominadas infecções perinatais (15). A transmissão
pode se dar durante o trabalho de
94
parto, por transfusão maternofetal; pela ascensão de microorganismos na cavidade amniótica
e acometimento das membranas
amnióticas, do cordão umbilical e
da placenta; ou devido à aspiração
de líquido amniótico contaminado;
ou, ainda, pelo contato da pele
e mucosas gástrica e ocular do
recém-nascido com sangue e secreções genitais ou fezes maternas
que contenham microorganismos
que estejam se replicando. A principal fonte de infecções pós-natais
do recém-nascido é a mãe. Embora
os tratos respiratório e gastrintestinal maternos sejam os sítios mais
comuns a partir dos quais ocorre a
transmissão de microorganismos
da mãe para o recém-nascido no
período pósnatal, o aleitamento
materno também pode ser a fonte
da infecção. A infecção perinatal por
CMV resulta da exposição da criança à secreção cervical ou ao leite
materno nas primeiras semanas de
vida ou da transmissão iatrogênica
pós-transfusional (3,4).
Na transmissão que ocorre por
exposição às secreções maternas,
após a ingestão do material contaminado, o vírus iniciaria replicação
na superfície das mucosas bucal,
faríngea, esofágica ou glândulas
salivares, tecidos pelos quais o CMV
tem tropismo. A infecção perinatal
pode ser resultado de infecção
primária materna, mas freqüentemente é causada por infecção
recorrente. O período de incubação varia de quatro a 12 semanas.
Assim, na ausência de virúria ao
nascimento, a detecção viral após
a quarta semana de vida define a
infecção perinatal por CMV.
A gravidade da infecção perinatal que ocorre nos recém-nascidos
prematuros submetidos a transfusões sangüíneas de doadores
infectados por CMV é proporcional
à quantidade de sangue transfundido (15).
Está associada à contaminação
do recém-nascido com secreções do
cérvix uterino no momento do parto
e com leite materno contendo CMV,
nas primeiras semanas de vida.
Assim, o CMV no cérvix uterino não
é somente uma fonte potencial de
transmissão por via sexual.
A alta excreção cervical durante
o terceiro semestre de gestação
sugere uma maior probabilidade de
infecção no momento do parto (26
a 57%), mas esta forma de contaminação ainda fica aquém daquela
que ocorre através do leite materno
(63%) (3).
Programas de rastreamento sorológico ou virológico para detectar
CMV em mulheres com potencial
para engravidar não são práticas
ou custo-efetivas. Restrições ao
aleitamento materno também não
são feitas, pois os benefícios do
leite materno se sobrepõem ao
risco da criança adquirir CMV da
mãe (20).
Infecção Adquirida
Esta transmissão se dá de forma
horizontal, no período pós-natal
através do contato de secreções
corpóreas contaminadas.
Pode ser dividida em dois períodos:
• Na infância a transmissão
ocorre basicamente por contato de
urina e saliva de outras crianças,
sendo assim, ambientes com muitas pessoas e creches acabam predispondo a uma maior infecção.
• Na idade adulta além das duas
formas já citadas, há ainda a trans-
NewsLab - edição 86 - 2008
missão por contato sexual via sêmen e secreções do
cérvix. A freqüência de infecção de CMV no cervix
varia com a idade, classe socioeconômica, promiscuidade sexual e paridade (3). Aproximadamente
1 a 2% das mulheres que passam por exame médico de rotina carrega o vírus. Em Seatle/EUA, um
estudo feito em 347 mulheres atendidas em uma
clinica de DST’s constatou-se presença de CMV no
cérvix de 34% destas mulheres (4). O CMV pode ser
encontrado em altos títulos no sêmen de homens
hetero e homosexuais, HIV-positivo ou não. Além
disso, algumas característica como baixa idade (≤
24 anos), promiscuidade sexual e passividade no
sexo anal têm sido correlacionadas com a presença
do vírus.
Transmissão Iatrogênica
Este tipo de transmissão ocorre através de
transfusões sanguíneas e transplantes de órgãos
e só é possível devido à capacidade do vírus de
permanecer latente, podendo ser reativado posteriormente (28).
Sugere-se que a transmissão por transfusão
sanguínea seja proporcional ao número de unidades
transfundidas e é estimado como 5 a 12% por unidade. Pelo fato do CMV estar associado a leucócitos,
e ainda, pelo fato de sendo o doador soropositivo
a chance de haver infecção no receptor aumentar
muito, na década de 1970 recomendou-se a usar
sangue destituído de leucócitos como forma de
prevenção (29).
Existem casos de pacientes soropositivos que,
após uma transfusão múltipla, tiveram aumento do
título de anticorpos anti-CMV, o que indica reinfecção com cepas distintas do CMV ou ainda reativação
do vírus latente no receptor. Assim, o melhor meio
de se evitar infecções deste tipo seria através da
utilização de doadores soronegativos (30).
A infecção por CMV é, certamente, a mais
comum infecção em órgãos transplantados. No
Serviço de Imunologia da Divisão de Laboratório
Central do HC FMUSP, a análise sorológica dos 110
doadores de órgão, no período de outubro de 2005
a junho de 2006, revelou a incidência de 78,2%
de positividade na pesquisa de IgG-CMV (D+).
Dados do Banco de Tecidos do HC FMUSP mostram
que, entre o período de maio de 2001 a maio de
NewsLab - edição 86 - 2008
95
2006, dos 112 doadores recebidos
que possuíam sorologia para CMV,
91,1% eram positivos na pesquisa
de IgG-CMV (D+).
O risco de desenvolvimento de
CMVD em pacientes transplantados varia de acordo com inúmeros
fatores:
• O tipo de órgão transplantado:
Pulmão e coração-pulmão têm alta
freqüência de infecção, seguido de
fígado, pâncreas e rim.
• A sorologia do doador (D)
e receptor (R). Assim há quatro
combinações, como é mostrado na
Figura 3.
Na combinação D+/R-, que corresponde a 20% de todos os órgãos
transplantados, há um grande risco
(50 a 70%) de desenvolvimento de
CMVD. Já as combinações D+/R+
e D-/R+, juntas somam aproximadamente 70% de todos os rins e
fígados transplantados, tendo 10 a
20% de chance de desenvolvimento
de CMVD (5).
Inúmeros estudos epidemiológicos têm sugerido uma relação entre
o risco de infecção pelo citomegalovírus (CMV) em pacientes queimados e a utilização de aloenxertos
com sorologia positiva para CMV,
além de que esta infecção contribui para o aumento da morbidade
e mortalidade destes pacientes.
Estes estudos mostram uma taxa
de soroconversão de pacientes
anteriormente soronegativos que
receberam aloenxertos de pele de
cadáver soropositivos variando entre 17 e 22,7% (30-32). Esta incidência é similar à de soroconversão
em pacientes submetidos a transplante de órgãos sólidos, em que a
importância da análise sorológica
dos doadores já é bem aceita atualmente (33-35). Alguns estudos
96
Figura 3
sugerem que a imunossupressão
pós-queimadura (36), a transfusão
de sangue (28) e o transplante de
pele de doadores sorologicamente
positivos para CMV (37) podem ser
considerados fatores de risco para
o desenvolvimento de infecção por
CMV (38).
Embora em indivíduos imunocompetentes a infecção pelo CMV
não seja capaz de expressar nenhum efeito patogênico, procedendo-se de forma assintomática, em
indivíduos imunocomprometidos
pode resultar em sérias complicações, devido à sua disseminação
pelo organismo, com possível
envolvimento de órgãos, gerando
distúrbios do trato gastrointestinal,
do sistema nervoso central, corioretinites, pneumonites, adrenalite,
além de tornar o paciente mais
suscetível a outras infecções, como
aspergilose, criptococose, candidíase e pneumocistose (5). Além disso,
pacientes com sorologia positiva
para infecção por CMV apresentam
um maior tempo de estadia hospitalar, quando comparados aqueles
sem evidência sorológica (31), o
que acaba por aumentar os gastos
com o tratamento e, principalmente, gerar uma maior exposição destes pacientes a outras infecções.
QUADROS CLÍNICOSaros Clínicos
Infecção Congênita
De 10 a 25% dos recém-nascidos
infectados congenitamente apresentam inúmeros sintomas, tais como,
prematuridade, icterícia (70% dos
casos), hepatoesplenomegalia (60%
dos casos), petéquias, púrpuras e
alterações neurológicas (desabilidade
motora, calcificação cerebral, microcefalia, convulsões e diminuição do
reflexo de sucção) (3, 39).
Cerca de 30% das crianças sintomáticas ao nascimento poderão
evoluir para óbito no período neonatal
e 95% das que sobrevivem terão
seqüelas neurológicas como microcefalia, retardo do desenvolvimento
neuromotor, coriorretinite e calcificações cerebrais. Das crianças assintomáticas, 10% a 15% terão alterações
tardias, como a surdez, graus variáveis de lesões neurológicas; porém,
crianças assintomáticas com evolução
neurológica normal até um ano de
vida não apresentam maior risco de
desenvolver anormalidades tardias
quando comparadas às crianças não
infectadas (1, 9, 15).
A avaliação do recém-nascido visa
determinar a extensão da doença,
principalmente no sistema nervoso
central. É importante a investigação
por meio de ultra-sonografia e tomografia computadorizada de crânio,
mesmo em crianças aparentemente
assintomáticas, pois o exame radiológico simples de crânio tem baixa
sensibilidade para visualização de
calcificações intracranianas e outras
alterações. Deve-se realizar exame
oftalmológico e audiológico, incluindo-se fundoscopia ocular, quando do
diagnóstico e periodicamente para
detecção de anormalidades tardias.
Outros exames complementares
NewsLab - edição 86 - 2008
incluem hemograma completo com
contagem de plaquetas e avaliação
da função hepática (9).
Infecção Perinatal
Pelo fato do período de incubação
do CMV ser de quatro a 12 semanas,
a grande maioria dos recém-nascidos
é assintomática. Porém, podem estar
associadas a quadros de pneumonia
intersticial de gravidade variável e
hepatoesplenomegalia (2).
Infecção Adquirida
A infecção freqüentemente assintomática, porém, quando sintomática
proporciona grande risco a adultos e
crianças que se submetem a grandes transfusões após acidentes ou
cirurgias invasivas. Isso ocorre após
transfusão de granulócitos, assim
o risco seria menor se fosse usado
sangue com poucos leucócitos, criopreservação do sangue ou doador
soronegativo (30).
A febre, que aparece no decorrer da doença, normalmente é a
manifestação mais proeminente. É
prolongada e geralmente com mais
de 10 dias de duração. Além disso,
aumento de linfonodos, fígado, pâncreas e amídalas não são comuns,
mas podem ocorrer, principalmente
em crianças. Podem ocorrer ainda
raras complicações tais como: pneumonia intersticial, hepatite, síndrome
de Guillain-Barre, meningoencefalite,
miocardite, trombocitopenia e anemia
hemolítica (3, 4).
Infecção Iatrogênica
Os processos da doença relacionada ao CMV manifestam-se de maneira
diferente, dependendo de qual é o
órgão transplantado. Em receptores
de medula óssea, a infecção por CMV
ocorre como uma pneumonia inters-
98
ticial, com alta taxa de mortalidade.
Em receptores de fígado, a hepatite
pode ser problemática e difícil de ser
diferenciada de uma rejeição do órgão. Ao contrário do que se observa
nos pacientes com AIDS, nos receptores de transplantes a renitine tem
baixa incidência. A apresentação da
“síndrome do CMV”, que consiste em
febre, leucopenia, linfócitos atípicos,
hepatomegalia, mialgia e artralgia, é
a manifestação mais comum da infecção primária por CMV em pacientes
que receberam transplante de rim.
CMV pode ser responsabilizado por
30% dos episódios de febre, 35%
de toda leucopenia e 20% de toda
chance de falha do transplante do
órgão (3, 40, 17).
CMV EM PACIENTES COM AIDS
O CMV é considerado um dos mais
importantes patógenos oportunistas
do paciente imunocomprometido. O
impacto causado pelo CMV em cada
um dos tipos de imunosupressão varia de acordo com as características
de cada uma delas. No caso da AIDS,
o CMV tem um efeito deletério em
sua progressão, pois há uma grande
relação entre o CMV e o HIV (41).
A progressiva imunosupressão
resultante da infecção do HIV aumenta a atividade do CMV. A retinite
responde por aproximadamente 85%
das manifestações da doença no
paciente, tanto que entre o período
de 1981 e 1989 a retinite era usada
como diagnostico definidor de AIDS,
e é provável que essa tendência continue conforme os pacientes infectados pelo HIV vivam mais tempo com
imunodeficiência profunda (2).
A retinite por CMV (CMV–R)
desenvolve-se em cerca de 28-35%
de todos os pacientes com AIDS
em estádios avançados da doença
e, freqüentemente, leva à cegueira
(42). Pacientes com HIV podem
apresentar diversas variedades de
complicações visuais secundárias à
retinite, incluindo visão embaçada,
flashes de luz, escotoma, ou perda
da visão central, dependendo da
localização e extensão da lesão na
retina. A retinitie causada por CMV
é um tipo focal necrotizante, com ou
sem hemorragias. A destruição da
retina, que causa cegueira irreversível, pode ser detida e suprimida por
agentes anti-CMV. Esses medicamentos interrompem a replicação de CMV,
mas não eliminam o vírus. O curso
natural da retinite não tratada resulta
na progressão da doença dentro de
aproximadamente duas semanas.
Pacientes que possuem infecção por
HIV deveriam ser questionados por
seus médicos sobre seus sintomas
visuais a cada visita (17).
Há ainda a possibilidade de surgimento de esofagites e colite (cerca
de 20%), pneumonite, hepatite,
adrenalite, entre outras (15). As manifestações neurológicas são menos
freqüentes, mas podem se apresentar
como uma encefalite micronodular
difusa, ou como ventrículo-encefalite,
clinicamente indistinguíveis (3).
DIAGNÓSTICO LABORATORIAL
O diagnóstico, que antigamente
era apenas baseado em dados clínicos, atualmente, devido à sofisticação
das técnicas laboratoriais, baseia-se
em resultados clínicos e imunológicos.
Há vários métodos para a detecção do
CMV. O isolamento viral em cultura
de fibroblastos humanos é o método
convencional. O vírus geralmente
está presente na urina com elevados
títulos, principalmente na infecção
congênita sintomática por CMV, e as
culturas são comumente positivas
NewsLab - edição 86 - 2008
após três a cinco dias. Essa técnica
requer assepsia rigorosa na coleta de
urina e processamento até 12 horas
da amostra a 4oC (15).
Para saber se a infecção é congênita ou perinatal, faz-se um isolamento do vírus de um tecido de biópsia ou
fluido corporal, principalmente urina.
Se este isolamento somente puder
ser feito em quatro a oito semanas
após o nascimento tem-se uma infecção perinatal. Caso o isolamento
for feito antes, tem-se uma infecção
congênita. Após o isolamento, o CMV
pode ser replicado in vitro, incubado
com fibroblastos a 36ºC por um a
três semanas, e posteriormente,
analisado com o objetivo de se identificar possíveis inclusões do CMV no
tecido analisado. Este é considerado
o padrão-ouro para o diagnóstico de
CMVD. Essa técnica, não e tão viável,
pois a necessidade de um longo período de incubação dificulta o rápido
diagnóstico (3, 5).
Já na técnica do shell-vial, muito
parecida com a de cima, o tempo de
revelação (feito por imunofluorescência indireta - IFI) cai para 24, 48 ou
72h, pois utilizam-se anticorpos monoclonais contra diferentes antígenos
do CMV e uma centrífuga que facilita
o processo de penetração do vírus no
fibroblasto (3, 43).
A PCR (Polymerase Chain Reaction) é uma técnica rápida (~6h)
e de alta sensibilidade baseada na
amplificação seletiva de seqüências
específicas de acido nucléico. Permite a detecção do DNA viral e é um
método alternativo para urina ou
outra amostra clínica, apresentando
sensibilidade e especificidade semelhante ao isolamento viral e possuindo
vantagens sobre o isolamento, tais
como a rapidez do resultado e a
possibilidade de as amostras serem
100
Figura 4
congeladas e armazenadas. É muito
utilizada apesar do seu alto custo e de
sua difícil execução. Pode ser utilizada
tanto qualitativamente (diagnóstico
por PCR), quanto quantitativamente na medição da carga viral, que
é proporcional ao nível de DNA do
CMV (44).
As detecções de IgM e IgG através
dos diversos métodos sorológicos
(imunofluorescência indireta, ELISA,
raioimunoensaio), são rotineiramente solicitadas para o diagnóstico da
infecção congênita por CMV, porém
têm papel limitado, não permitindo
afastar ou confirmar esta infecção na
ausência de detecção viral (4).
O método de ELISA (EnzimeLinked Immunosorbent Assay), que
apresenta sensibilidade de 100% e
especificidade de 86%, detecta anticorpos no sangue. Existe a possibilidade de resultados falsos-positivos
devido a reações cruzadas com alguns vírus da família Herpesviridae,
fatores reumatóides e anticorpos
antinucleares (45).
O esquema de interações que
ocorre numa placa de ELISA é demonstrado na Figura 4.
Pelo fato dos anticorpos IgG,
diferentemente dos IgM, conseguirem passar passivamente através
da placenta, sua pesquisa se torna
sem aplicação para o diagnóstico de
infecção congênita. Assim, no método
de ELISA, deve-se haver uma prévia
separação das frações de IgM e IgG
do soro do paciente para diminuir a
possibilidade de resultados falsosnegativos, já que há competição
entre IgG maternos e IgM dos recémnascido (46). Apenas 30% a 89%
das crianças sabidamente infectadas
intra-útero apresentarão anticorpos
IgM anti-CMV ao nascimento. Os anticorpos IgG anti-CMV são geralmente
adquiridos da mãe e a sorologia seriada para avaliar elevação dos títulos
não permite diferenciar a infecção
congênita da perinatal (15).
Para o diagnóstico da infecção
materna ainda pode ser utilizado
o Western Blotting que permite a
mensuração da afinidade ou avidez
do anticorpo IgG-CMV pelo antígeno
viral e a detecção da reatividade de
anticorpos IgM-CMV para diferentes
proteínas do antígeno viral (47).
Este método, apesar de detectar a
primoinfecção materna mais precocemente que o método ELISA, ainda
apresenta uma viabilidade comercialmente questionável.
Histologicamente, a detecção
de corpos de inclusão “owl’s eye”
na amostra de tecido pode ser um
método altamente específico para
determinar o envolvimento do CMV
no órgão (17).
TRATAMENTO
O tratamento é baseado na administração de drogas antivirais.
NewsLab - edição 86 - 2008
Atualmente, apenas o ganciclovir e
o foscarnet são aprovados pelo FDA.
Ambas as drogas possuem pouca
biodisponibilidade oral e elevada toxicidade. Agem de forma virustática,
ou seja, inibindo a replicação viral
enquanto são administradas. Além
de sua ação anti-CMV, o foscarnet
tem atividade in vitro anti-HIV. Como
efeito da toxicidade pode-se citar
a mielossupressão (neutropenia,
trombocitopenia), insuficiência renal,
hepática, coma, convulsão, além de
distúrbios eletrolíticos (hipocalcemia,
hipomagnesemia, hipofosfatemia e
hipocalemia) (3, 48).
A importância dada no sentido de
não interromper o tratamento é freqüente. Sabe-se que intensificações
dos sintomas iniciais podem ocorrer
neste caso, o que sugere um rigoroso
controle da medicação.
Sabendo das lesões irreversíveis
às quais os fetos estão sujeitos
antes do nascimento, um grupo
de vacinas começou a ser desenvolvida - dois a quatro meses após
a inoculação do vírus atenuado
tem-se quantidades máximas de
anticorpos anti-CMV (12).
A introdução da terapia com
antiretrovirais altamente ativos
(HAART - highly active antiretroviral
therapy), uma combinação de três
ou mais drogas antiretrovirais de
pelo menos duas classes diferentes, tem conseguido resultados na
reconstituição do sistema imune de
pacientes com HIV, de tal modo a
permitir que a infecção por CMV seja
controlada. Assim, a HAART tem feito
muito no sentido de reduzir a taxa
de mortalidade associada com CMV
em tais pacientes. Apesar disso, a
resposta ao tratamento nesses pacientes ainda permanece abaixo do
nível ideal e muitos não têm acesso
a tal terapia. Então, os esforços para
melhorar o tratamento do CMV tem
sido uma prioridade (16).
Correspondências para:
Jader Joel Machado Junqueira
[email protected]
Referências Bibliográficas
1. Couto CFC, Rodrigues MV, Melo GEBA, Menezes GA, Leite JM. Citomegalovírus e Gestação: Um Antigo Problema sem Novas Soluções. Femina
Jul. 2003 Nº. 06 Vol. 31; 509-516.
2. Libman H,Witzburg RA. Infecção pelo HIV – Um Manual Clínico. Medsi Editora Médica e Científica Ltda, 2ª Edição 1995; Capítulo 22 –
Infecção por Citomegalovírus.
3.Veronesi R, Focaccia R.Tratado de Infectologia – Livro 1. Editora Ateneu, 2ª Edição. 190- 196; 150-155.
4. Mandell GL, Douglas RG, Bennett JE. Principles and Practice of Infectious Diseases. Editora Churchill Livingstone, 3ª Edição. 1159-1169.
5. Anaizy N, PhD. Citomegalovírus in solid organ transplantation. Disponível em: <http://www.thedrugmonitor.com/cmv-1.html>
6. Coordenação Nacional de DST/AIDS. Manual de Controle das Doenças Sexualmente Transmissíveis DST. Infecção pelo Citomegalovírus
(CMV). 3ª Edição 1999. Disponível em: <http://www.aids.gov.br/assistencia/manualdst/item14.htm>
7.Trabulsi LR, Alterthum F. Microbiologia. Editora Atheneu, 4ª Edição. 603-05.
8.Yu X,Trang P, Shah S, Atanasov I, Kim YH, Bai Y, Zhou ZH, Liu F. Dissecting human cytomegalovirus gene function and capsid maturation by
ribozyme targeting and electron cryomicroscopy. Proc Natl Acad Sci U S A. 2005;102(20): 7103-8. Epub 2005 May 9.
9. Vinha C. Citomegalovírus relacionado a área de fonoaudiologia. Disponível em: <http://www.geocities.com/hotsprings/falls/3233/
citomega.html
10. Alford CA, Stagno S, Pass RF, Britt WJ. Congenital and perinatal cytomegalovirus infections. Rev Infect Dis, 1990;12 Suppl 7:S745-S753.
11. Brown HL, Albernathy MP. Cytomegalovirus infection. Semin Perinatal 1998;22:260-266.
12. Brandão RS, Guerzet EA, Souza E, Camano L. Citomegalovirus: Diagnóstico e conduta na infecção fetal. Femina Jul. 2003 Nº 06 Vol. 31;
551-553.
13. Stagno S. Cytomegalovirus. Infectious disease of the fetus and newborn infant. Philadelphia,WB Saunders Company 2001: 389-424.
14. Hertel L, Mocarski ES. Global analysis of host cell gene expression late during cytomegalovirus infection reveals extensive dysregulation of
cell cycle gene expression and induction of Pseudomitosis independent of US28 function. J Virol. 2004; 78(21): 11988-2011
15. Mussi-Pinhata MM,Yamamoto AY. [Congenital and perinatal infections] J Pediatr (Rio J). 1999; 75(Suppl 1):S15-30. Portuguese.
16. Griffiths P. Cytomegalovirus infection of the central nervous system. Herpes. 2004;11 Suppl 2:95A-104A. Review.
17.Taylor GH. Cytomegalovirus. Am Fam Physician. 2003; 67(3):519-24. Review.
18. Gold E, Nankervis GA. Cytomegalovirus.Viral infections of human: epidemiology and control. Plenum Press, New York, 3ª Ed. Capítulo 8. 169.
1991.
19. Hunter K, Stagno S, Capps E, Smith RJ. Prenatal screening of pregnant women for infections caused by cytomegalovirus, Epstein-Barr virus,
102
NewsLab - edição 86 - 2008
herpesvirus, rubella, and Toxoplasma gondii. Am J Obstet Gynecol 1983; 145(3): 269-273.
20. Cannon MJ, Davis KF:Washing our hands of the congenital cytomegalovirus disease epidemic. BMC Public Health. 2005; 5:70.
21. Larson E. A causal link between handwashing and risk of infection? Examination of the evidence. Infect Control 1988; 9:28-36.
22. Pass RF, Hutto C, Ricks R, Cloud GA. Increase rate of cytomegalovirus infection among parents of children attending daycare centers. N Engl
J Med 1986; 314:1414-1418.
23. Adler SP. Cytomegalovirus and child day care: risk factors for maternal infection. Pediatr Infect Dis J 1991;10: 590-594.
24. Hemmings DG, Kilani R, Nykifourk C, Preiksaitis J, Guilbert LJ. Permissive cytomegalovirus infection of primary villous term and first trimester
trophoblasts. J Virol 1998; 72:4970-4979.
25. Stagno S,WhitleyRJ. Herpesvirus infection of pregnancy. N. Engl. J Med 1985; 313:1270-1274.
26. Flower KB, Stagno S, Pass RF, BrittWJ, BpllTJ,Alford CA.The outcome of congenital cytomegalovirus infection in relation in to maternal antibody
status. N Engl J Med 1992; 326:663-667.
27. Negishi H, Yamada H, Hirayama E, Okuyama K, Sagawa T, Matsumoto Y, Fujimoto S. Intraperitoneal administration of cytomegalovirus
hyperimmunoglobulin to the cytomegalovirus-infected fetus. J Perinatol. 1998; 18(6 Pt 1):466-9.
28. Preiksaitis JK, Brown L e McKenzie M.The risk of cytomegalovirus infection in seronegative transfusion recipients not receiving exogenous
immunosuppression. J Infect Dis 1988; 156:523.
29. Adler SP.Transfusion-associated cytomegalovirus infection. Rev Infect Dis. 1983; 5:977.
30. Kealey GP, Aguiar J, Lewis RW 2nd, e cols. Cadaver skin allografts and transmission of human cytomegalovirus to burn patients. J Am Coll
Surg 1996; 182(3):201-205.
31. Bale JF, Kealey P, Massanari RM, e cols. The Epidemiology of Citomegalovirus Infection Among Patients with Burns. Infect Control Hosp
Epidemiol 1990; 11(1): 17-22.
32. Kagan RJ, Naraqui S, Matsuda T, e cols. Herpes simplex vírus ans cytomegalovirus infections in burned patients. J Trauma 1985; 24: 40-45.
33. Breinig MK, Zitelli B, Starzl TE, e cols. Epstein-Barr virus, cytomegalovirus and other viral infections in children after liver transplantation. J
Infect Dis 1987; 156: 273-279.
34. Merigan TC, Renlund DG, Keay S, e cols. A controlled trial of ganciclovir to prevent cytomegalovirus disease after heart transplantation. N
Engl J Med 1992; 326: 1182-1186.
35. Goodrich JM, Mori M, Gleaves CA, e cols. Early treatment with ganciclovir to prevent cytomegalovirus disease after allogeneic bone marrow
transplantation. N Engl J Med 1991; 325: 1601-1607.
36. Polk HC, Wellhausen SR, Regan MP, e cols. A systematic study of host defense processes in badly injured patients. Ann Surg 1986;
204:282.
37. Shelby J, Shanley J.Transfer of murine cytomegalovirus by syngeneic skin grafts.Transplantation 1987; 44:318.
38. Bale JF Jr, Kealey GP, Ebelhack CL, e cols. Cytomegalovirus infection in a cyclosporine-treated burn patient: case report. J Trauma 1992; 32(2):
263-267.
39. Boppana SB, Pass RF, Britt WJ, Stagno S, Alford CA. Symptomatic congenital cytomegalovirus infection: neonatal morbidity and mortality.
Pediatr Infect Dis J. 1992 Feb; 11(2): 93-9.
40. Betts RF, Freeman RB, Douglas RG Jr,Talley TE. Clinical manifestations of renal allograft derived primary cytomegalovirus infection. Am J Dis
Child. 1977l; 131(7): 759-63.
41. Northfield JW, Harcourt G, Lucas M, Klenerman P. Immunology of viral co-infections with HIV.Arch Immunol Ther Exp (Warsz). 2005; 53(1):
3-12. Review.
42. Fernandes AP, Goncalves MA, Zavanella RB, Figueiredo JF, Donadi EA, Rodrigues ML. HLA markers associated with progression to AIDS are
also associated with susceptibility to cytomegalovirus retinitis. AIDS. 2003;17(14):2133-6.
43. Gleaves CA, Smith TF, Shuster EA, Pearson GR. Comparison of standard tube and shell vial cell culture techniques for the detection of cytomegalovirus in clinical specimens. J Clin Microbiol 1985; 21(2): 217-21.
44. Demmler GJ, Buffone GJ, Schimbor CM, May RA. Detection of cytomegalovirus in urine from newborns by using polymerase chain reaction
DNA amplification. J Infect Dis 1988; 158(6): 1177-84.
45. Daiminger A, Bader U, Eggers M. Evaluation of two novel enzyme immunoassays using recombinant antigens to detect cytomegalovirus
specific immunoglobulins M in sera from pregnant women. J Clin Virol 1999; 13: 161-171.
46. Hodinka RL, Friedman HD. Human cytomegalovirus. Manual of Clinical Microbiology. 5ª Ed.Washington.American Society for Microbiology.
829. 1991.
47. Landini MP, Lazzarotto T. Prenatal diagnosis of congenital cytomegalovirus infection: light and shade Herpes. J Virol 1999; 6: 645-649.
48.Whitley RJ, Cloud G, Gruber W, Storch GA, Demmler GJ, Jacobs RF, Dankner W, Spector SA, Starr S, Pass RF, Stagno S, Britt WJ, Alford C Jr,
Soong S, Zhou XJ, Sherrill L, FitzGerald JM, Sommadossi JP. Ganciclovir treatment of symptomatic congenital cytomegalovirus infection: results of a
phase II study. National Institute of Allergy and Infectious Diseases Collaborative Antiviral Study Group. J Infect Dis. 1997 May; 175(5):1080-6.
104
NewsLab - edição 86 - 2008