PRODUÇÃO DE ANTICORPO POLICLONAL ANTI-EIF2 BETA HUMANO A PARTIR DA
CLONAGEM, EXPRESSÃO, PURIFICAÇÃO DA PROTEÍNA RECOMBINANTE EIF2 BETA EM
ESCHERICHIA COLI
Mauricio Schiavo (PROBIC/FAPERGS), Ana Paula Longaray Delamare, Sérgio Echeverrigaray,
Jomar Pereira Laurino (Orientador(a))
Aproximadamente trezentas macromoléculas diferentes cooperaram para a síntese polipeptídica. A síntese
proteica começa com a formação do complexo ternário, a qual ocorre pela ligação do heterotrímero de
eIF2 (a, b e g), Met-tRNAi e GTP, este é o mais importante passo regulador de toda síntese proteica. A
caracterização de formas mutantes da proteína eIF2b, não funcionais no processo de tradução, pode
representar uma ferramenta molecular com a finalidade de diminuir a proliferação celular. Uma limitação
para mostrar o trânsito destas moléculas na célula reside no fato de que os anticorpos monoclonais
comerciais existentes não possuem uma boa sensibilidade aos epítopos in natura de eIF2b. O objetivo
deste trabalho é produzir anticorpo policlonal que possa ser utilizado para a detecção da expressão das
formas selvagem e demais mutações de eIF2b. Este anticorpo poderá ser usado para analisar eIF2b em
células de mamíferos por "immunoblotting" e por imunoflorescência. Neste sentido, a região codificadora
do gene de eIF2b humano foi clonada em plasmídio de expressão pET-23a(+) em Escherichia coli
BL21DE3 Codon Plus-RIL. Um clone foi selecionado com ampicilina e induzido com IPTG para realizar a
super-expressão da proteína eIF2b humana recombinante. O extrato de proteínas totais bacteriana passou
por processo de purificação cromatográfica de afinidade em coluna de Níquel NTA. A proteína de fusão
eIF2b humana recombinante foi eluída com imidazol. As amostras obtidas das eluições cromatográficas
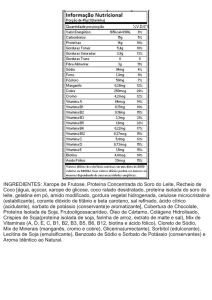
foram dialisadas e concentradas. Os eluatos foram mensurados pelo método de Bradford. Alíquotas destas
purificações foram aplicadas em gel de poliacrilamida SDS para analise de pureza. Apenas uma proteína
com peso molecular de aproximadamente 58kDa, correspondente a eIF2b humana foi observada. A
proteína purificada humana foi utilizada na imunização de coelho da raça Agouti. Foram realizadas quatro
imunizações em intervalos de duas semanas. Após a última imunização foi respeitado um período de
quatro semanas até a obtenção da amostra final de soro. Foram coletadas amostras de soro
imediatamente antes de cada imunização. Nestas amostras foram realizados testes de "immunoblotting"
contendo extratos de células humanas HEK 293 super-expressando a proteína eIF2b. Houve
reconhecimento específico no soro da primeira semana de imunização. Assim, o soro produzido referente
a primeira semana de imunização poderá ser utilizado para estudos de expressão gênica da proteína eIF2.
Palavras-chave: eIF2 beta, anticorpos policlonais, inicio de tradução em eucariotos
Apoio: UCS, FAPERGS
1