Contaminação Química
Prevenção de Risco na Terapia de Infusão
Contaminação Química
Estratégias
Causas
Definição
O termo contaminação química é definido
como a exposição não intencionada de um
profissional de saúde a fármacos
perigosos.=
O American National Institute for Occupational Safety and
Health (Instituto Americano para Segurança e Saúde
Ocupacional (NIOSH)) define um fármaco perigoso como
qualquer fármaco identificado por, no mínimo, um dos
seguintes critérios: carcinogenicidade, teratogenicidade ou
toxicidade de desenvolvimento, toxicidade na reprodução
em humanos, toxicidade de órgão em doses baixas em
humanos ou animais, genotoxicidade ou novos fármacos
que mimetizam os fármacos perigosos existentes em
estrutura ou toxicidade [NIOSH 2004]. Estão listados 136
fármacos perigosos, que incluem:
Agentes quimioterápicos / citotóxicos
Antibióticos / Antivirais
Fármacos derivados da bioengenharia
Anticorpos monoclonais
Agentes genéticos e hormonais
Outros fármacos diversos
Causas
Esta brochura apresentará um esboço sobre as
causas da contaminação química.
Kromhout e outros observaram que a causa ou via
exata desta exposição não está definida [Kromhout
et al. 2000], porém podem ser encontradas duas
vias primárias na literatura: uma via dérmica
[Valanis et al. 1993a, b] e por aerossol [Kromhout
et al. 2000].
Contaminação dérmica
A contaminação foi encontrada em diversas áreas,
sendo identificada como contaminação dérmica, ou
‘por toque’. Eles incluem:
a superfície de frascos [ Mason et al. 2003].
a superfície das caixas de fármacos [Schmaus et
al. 2002]
preparação de fármacos, como ciclofosfamida
[Fransman et al. 2004]
e manipulação de fluidos corporais de pacientes
que se submetem ao tratamento citostático
[Fransman et al. 2004, Kromhout et al. 2000].
A presença de contaminação nessas áreas sugere
que a preparação de agentes citostáticos, assim
como de frascos de manipulação, caixas e fluidos
corporais é uma causa de contaminação.
Outras causas de contaminação, discutidas pelas
agências regulatórias, como a NIOSH, são
derramamentos inadequadamente
descontaminados, priming de equipos IV,
manipulação fora da farmácia e escolha
inadequada do produto [NIOSH 2004].
Fig. 1: Contaminação causada por priming de equipos IV
2
“Os resultados mostram que os técnicos de farmácia e
enfermeiros do setor de oncologia foram expostos
dermicamente à ciclofosfamida”.
[Fransman et al. 2004]
Riscos
Contato com a pele durante:
Contato com as superfícies do frasco
Contato com as superfícies da embalagem
Manipulação de fluidos corporais de pacientes
Contaminação por Aerossol
A contaminação por aerossol durante a preparação e
administração de um fármaco é um tipo de
contaminação aceito por agências, como a NIOSH,
podendo ser encontrado na literatura [Neal et al.
1983, NIOSH 2004, Sessink 1994]. No entanto,
alguns estudos não encontraram evidência para a
contaminação por aerossol, porém sugeriram que
esta é decorrente de inadequados limites de detecção
[Larson et al. 2003].
Fig. 2: Contaminação causada durante a preparação
3
Derramamentos
Priming de equipos IV
Contato com aerossol durante:
Preparação de fármacos
Administração de fármacos
Contaminação Química
Consequências
As consequências da contaminação química
dependem do fármaco em questão. Por este motivo,
parece ser apropriada uma diferenciação entre
contaminação tóxica e não tóxica.
Contaminação Não Tóxica
A exposição a medicações não tóxicas, como
determinados antibióticos, apresenta consequências
e tem demonstrado levar à dermatite [Gielen e
Goossens 2001] e hipersensibilidade [AFS 2005], que
podem reduzir a eficiência do trabalho.
Contaminação Tóxica
1. Sintomas agudos
Os Resumos de Características do Produto (SPCs)
do fármaco são a principal fonte de informação em
relação aos efeitos indesejáveis, devendo ser
consultados regularmente.
Considera-se, por exemplo, que paclitaxel leva a
sintomas agudos, como náusea, alopecia (perda de
cabelo) e bradicardia [Paclitaxel SmPC 2010]. Os
estudos mostram um aumento significativo em
sintomas agudos similares entre casos controle e
casos expostos aos agentes antineoplásicos (por
exemplo, diarreia, irritação na garganta, erupções
cutâneas) [McDiarmid et al. 1988, Valanis et al.
1993a]. No entanto, o principal sintoma agudo é a
mutagenicidade. Os estudos demonstraram diversos
indicadores de mutagenicidade, como trocas de
cromátides irmãs ou aberrações [Falck et al. 1979,
Sarto et al. 1990]. Como a mutagenicidade
cromossômica após exposição é de natureza
estocástica [Health Counsel 1994[, uma única
molécula mínima pode causar uma mutação. Por este
motivo, as agências regulatórias não mencionam os
níveis limítrofes sob os quais a exposição é aceitável.
“Os resultados mostraram que enfermeiros expostos
aos agentes antineoplásicos no trabalho foram
significativamente mais propensos a apresentar uma
mutagenicidade urinária, em comparação aos
enfermeiros não expostos... Uma proporção
significativamente maior de resultados indesejáveis
na gravidez ocorreu em gestações com exposição a
agentes antineoplásicos.” [Rogers e Emmett 1987].
4
2. Sintomas crônicos
Carcinogenicidade
A mutagenicidade, embora seja um sintoma agudo em si,
pode levar à doença crônica do câncer. Também foi
demonstrada a ligação entre a exposição a elevadas
doses de medicação citotóxica e neoplasia maligna
secundária, o que levou à Agência Internacional para
Pesquisa no Câncer (International Agency for Research
on Cancer (IARC)) a classificar muitos fármacos
antineoplásicos como compostos do grupo 1
(carcinogênico para seres humanos) [IARC]. A natureza
estocástica da carcinogenicidade faz com que até mesmo
as doses baixas, como aquelas encontradas durante uma
contaminação, representem um risco. Os estudos que
demonstraram essa ligação estão sujeitos a certos
desafios estatísticos em decorrência da baixa ocorrência
de câncer na população e aos limitados tamanhos de
amostra. No entanto, Sessink calculou que o risco teórico
no tempo de vida que um profissional de saúde sofre com
a leucemia foi de 95-475 por milhão [Sessink et al. 1995].
Skov demonstrou um risco elevado de leucemia e linfoma
não Hodgkin em profissionais que trabalham em hospitais
[Skov et al. 1992].
Efeitos na reprodução
Os estudos demonstram uma elevada ocorrência de
perda fetal [Selevan et al. 1985, Stücker et al, 1990,
Valanis et al. 1999], assim como de teratogenicidade
[Hemminki et al. 1985].
Outros efeitos crônicos
Como possíveis consequências adicionais, Sotaniemi
mostrou dano hepático crônico e fibrose [Sotaniemi et al.
1983] resultante da exposição aos fármacos tóxicos.
“Foi observada uma associação estatisticamente
significativa entre perda fetal e exposição ocupacional
aos fármacos antioneoplásicos durante o primeiro
trimestre de gestação”. [Selevan et al., 1985].
Caixa
de transporte
Reconstituição
de pó
ou diluição
de fluidos
Derramamentos
inadequadamente
descontaminados
Priming
do equipo IV
Fluidos corporais
do paciente
Aerossol formado
durante
a administração
Causas
Superfície
do frasco
Exposição na enfermaria
Aguda
Outras agudas,
por exemplo, diarreia
Mutagenicidade /
genotoxicidade
Crônica
Carcinogenicidade
Fig. 3: Causas da contaminação química e suas potenciais consequências.
5
Outras crônicas,
por exemplo
dano hepático
Reprodutivo
Consequências
Exposição na farmácia
Contaminação Química
Consequências
Os fatores de custo serão divididos aqui no custo para a
sociedade e no custo para as instituições de saúde que
serão discutidos abaixo (ver Fig. 4).
Custo para o hospital
Os procedimentos operacionais padrão (POPs) comuns
em hospitais, assim como nas diretrizes publicadas, ditam
que os profissionais de saúde expostos à contaminação
devem lavar completamente a área exposta com água por
dez minutos. Se os olhos forem contaminados, um
oftalmologista deve ser consultado [QuapoS 2003].
Adicionado a esta perda em produtividade, existem alguns
custos com equipamentos para lavagem, pomadas,
bandagens e medicação para aliviar os sintomas de
qualquer consequência aguda, como diarreia.
A dermatite e a hipersensibilidade causadas pela
exposição repetida à medicação não foram investigadas
com respeito ao custo, porém Mälkönen demonstrou que
os profissionais de saúde com uma doença cutânea
ocupacional tiveram que tirar licença médica (21%) ou
foram forçados a mudar de ocupação (21%) [Mälkönen
2009]. A redução da eficiência no trabalho da equipe que
permanece, e o treinamento de novo pessoal para
substituir aqueles que deixam a ocupação são dois fatores
de custo que não devem ser esquecidos.
Outro caso em que uma complicação leva à perda de
produtividade é o câncer: por exemplo, no Reino Unido, os
pacientes recebem uma licença média estatutária de 28
semanas com um auxílio doença de 79,15 ₤ (90 €) por dia
[Macmillan cancer support 2010].
De modo similar, os custos hospitalares associados com
as complicações reprodutoras, como perda fetal, ocorrem
quando é concedida a licença médica compassiva ao
profissional de saúde. Embora isto certamente possa
variar significativamente, para muitas indústrias na
Alemanha, a licença legal mínima para a perda de parente
em primeiro grau é de 2 dias [IGBCE 2000].
Dependendo do país, é possível imaginar que, se algum
desses problemas de saúde estiver relacionado com
procedimentos de segurança inadequados, pode haver
consequências legais custosas para uma instituição de
saúde.
6
Fig 4: Estimativa dos possíveis custos adicionais em consequência de complicações causadas por contaminação
química.
7
Contaminação Química
Estratégias
de Prevenção
Fig. 5: Preparação
centralizada na farmácia
Fig. 6: Dispositivos de
segurança
Fig. 7: Roupa de
proteção em uso em
uma cabine de fluxo
laminar
8
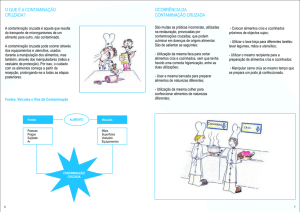
Estratégias de prevenção
As estratégias de prevenção são geralmente
recomendadas por agências nacionais (ver a caixa) e
focam na redução da exposição. As figuras (à
esquerda) ilustram os principais cuidados, isto é:
Prevenir a contaminação causada por erros de
manipulação centralizando a preparação [QuapoS
2003]. Isto permite que a medicação seja
manipulada por uma equipe especialmente treinada
(Fig. 5).
Prevenir a contaminação tóxica (liberação de
substâncias tóxicas) utilizando dispositivos de
“segurança” [NIOSH 2004]. Eles têm por objetivo
reduzir a contaminação por aerossol (por exemplo,
filtros de aerossol), assim como a contaminação
por respingos (por exemplo, dispositivos livres de
agulha) (Fig. 6).
Agências Regulatórias
Alguns focos de contaminação, como a superfície do
frasco, no entanto, são difíceis de prevenir e,
portanto, devem ser contidos (Fig. 7):
Qualquer contaminação com aerossol formado é
contida utilizando fluxo laminar (LAF) ou cabines de
isolamento [Nguyen et al. 1982, Crauste-Manciet et
al. 2005].
Qualquer contaminação por respingo formado pode
ser prevenida, evitando a sua absorção com o uso
de capas de proteção, como aventais, máscaras e
luvas [ASTM 2005].
Sociedade Alemão para Farmácia em Oncologia
Além disso, são recomendados controles regulares,
como exames de sangue, a fim de monitorar os
níveis de exposição [QuapoS 2003]. Se forem
colocadas em prática medidas protetoras
sistemáticas, a exposição pode ser reduzida
[Ündeger et al. 1999, Skov et al. 1992].
9
As seguintes agências (entre outras) publicaram
recomendações para a prevenção
da contaminação química:
National Institute for Occupational Safety and Health
(NIOSH – Instituto Nacional para a Segurança e Saúde
Ocupacional), EUA
Os Centros de Controle e Prevenção da Doença
(CDC), EUA
International Society of Pharmacovigilance (ISOP,
Sociedade Internacional de Farmacovigilância)
(DGOP), Alemanha
Autoridade Sueca de Ambiente no Trabalho (AFS),
Suécia
Contaminação Química
Prevenção do
Risco
Mini-Spike® Chemo V
Pino de dispensação com orifício para transferência
segura e conveniente de fluido com seringas.
Orifício de ventilação inclui filtro embutido para
impedir o escape de aerossóis tóxicos.
A valva de duas vias previne respingos e
vazamentos.
Cyto-Set® Mix
A solução completa do sistema para preparações
seguras e fáceis com substâncias tóxicas.
Permite a mistura sem agulha no recipiente de
infusão.
Compatibilidade ideal do sistema com Cytoset.
Ecoflac® plus
O inovador recipiente de solução IV que oferece
aplicação segura e conveniente de todos os
procedimentos IV da mistura até a administração do
fármaco.
As propriedades superiores da membrana com
porta resselável impedem respingos.
O design inovador da tampa permite um processo
de mistura fácil e segura do fármaco e adição
segura.
Safeflow / Ultrasite®
Válvulas para acesso seguro e conveniente à linha
de infusão.
A válvula garante que o sistema permaneça fechado.
Os sistemas de infusão livre de agulha da B. Braun
reduzem o risco de contaminação de respingos e
reduz o uso de agulhas.
10
Ecoflac® Connect
Sistema de transferência fechado com tampa para
mistura de fármaco de dose única.
O sistema fechado do Ecoflac® Connect garante
que não haja contato com o ambiente externo.
Este sistema fechado reduz a exposição do
profissional de saúde à medicação.
Intrafix® SafeSet
Equipo IV para infusões seguras e convenientes.
Priming automático, livre de respingos através da
inovadora membrana Prime Stop embutida na
extremidade da tampa.
Cyto-Set®
A solução completa do sistema para infusões
seguras e fáceis de substâncias tóxicas.
Previne os respingos tóxicos permitindo o simples
pré- e pós-preenchimento da linha com solução
neutra.
O seu design dispensa a necessidade para novas
preparações (adições/injeções).
Discofix® C
A exclusiva torneira para segurança melhorada.
Um material especial impede que respingos tóxicos
sejam lançados para fora do sistema eliminando as
rachaduras por estresse.
11
Contaminação Química
Literatura
Literatura
AFS Cytostatics and other medications with permanent
toxic effects [translation] Swedish Work Environment
Agency 2005: 5
ASTM. D6978-05: Standard Practice for Assessment
of Resistance of Medical Gloves to Permeation by
Chemotherapy Drugs, American Society for Testing
and Materials 2005
Crauste-Manciet S, Sessink PMJ, Ferrari S, Jomier JY,
Brossard D. Environmental Contamination with
Cytotoxic Drugs in Healthcare Using Positive Air
Pressure Isolators. Ann Occup Hyg 2005; 49(7): 619–
628
Falck K, Gröhn P, Sorsa M, Vainio H, Heinonen E,
Holsti LR. Mutagenicity in urine of nurses handling
cytostatic drugs. Lancet 1979; 1(8128): 1250–1251
Flintoff JP. Thalidomide: the battle for compensation
goes on. The Sunday Times. March 23, 2008
Fransman W, Vermeulen R, Kromhout H. Occupational
dermal exposure to cyclophosphamide in Dutch
hospitals: a pilot study. Ann Occup Hyg 2004; 48(3):
237–244
Prevalence Counts, Invasive Cancers Only, January 1,
2006, Using Different Tumor Inclusion Criteria. Accessed
at
http://seer.cancer.gov/csr/1975_2006/results_single/sect_
01_table.21_2pgs.pdf on September 3, 2009
IARC Monographs on the Evaluation of Carcinogenic
Risks to Humans - Overall Evaluations of Carcinogenicity:
An Updating of IARC Monographs 1987. Supplement 7;
Volumes 1-42
IGBCE. Manteltarifvertrag 2000
Kromhout H, Hoek F, Uitterhoeve R, Huijbers R,
Overmars RF, Anzion R, Vermeulen R. Postulating a
dermal pathway for exposure to antineoplastic drugs
among hospital workers. Applying a conceptual model to
the results of three workplace surveys.
Ann Occup Hyg 2000; 44(7): 551–560
Larson RR, Khazaeli MB, Dillon HK. A New Monitoring
Method Using Solid Sorbent Media for Evaluation of
Airborne Cyclophosphamide and Other Antineoplastic
Agents. Appl Occup Environ Hyg 2003; 18(2): 120-131
Gielen K, Goossens A. Occupational allergic contact
dermatitis from drugs in healthcare workers. Contact
Dermatitis 2001; 45: 273–279
Macmillan cancer support website. A guide to benefits and
financial help for people affected by cancer.
http://www.cancer.gov/
aboutnci/servingpeople/CostOfCancer. Accessed Feb.
2010
Health Counsel of the Neatherlands. Risk assessment
of carcinogenic chemicals in the Neatherlands. Regul
Toxicol Pharmacol
1994; 19: 14-30
Mälkönen T, Jolanki R, Alanko K, Luukkonen R, AaltoKorte K, Lauerma A, Susitaival P. A 6-month follow-up
study of 1048 patients diagnosed with an occupational
skin disease. Contact Dermatitis 2009; 61(5): 261-8
Hemminki K, Kyyrönen P, Lindbohm M-L.
Spontaneous abortions and malformation in the
offspring of nurses exposed to anaesthetic gases,
cytostatic drugs, and other potential hazards in
hospitals, based on registered information of outcome.
J Epidemiol Community Health 1985; 39: 141-147
Mason HJ, Morton J, Garfitt SJ, Iqbal S, Jones K.
Cytotoxic drug contamination on the outside of vials
delivered to a hospital pharmacy. Ann Occup Hyg 2003;
47(8): 681–685
Horner MJ, Ries LAG, Krapcho M, et al (eds). SEER
Cancer Statistics Review, 1975-2006, National Cancer
Institute. Bethesda, Md, based on November 2008
SEER data submission, posted to the SEER web site,
2009. Table I-21, US
12
McDiarmid MA, Egan T. Acute occupational exposure to
antineoplastic agents. J Occup Med 1988; 30(12): 984–
987
National Cancer Institute website (USA).
http://www.cancer.gov/aboutnci/servingpeople/CostOfCan
cer. Accessed Feb. 2010
Neal AdW, Wadden RA, Chiou WL. Exposure of
hospital workers to airborne antineoplastic agents. Am
J Hosp Pharm 1983; 40(4): 597-601
Nguyen TV, Theiss JC, Matney TS. Exposure of
pharmacy personnel to muta genic antineoplastic
drugs. Cancer Res 1982; 42: 4792–4796
NHS Careers website. www.nhscareers.nhs.uk.
Accessed Feb. 2010
NIOSH Alert: Preventing occupational exposures to
antineoplastic and other hazardous drugs in health
care settings. U.S. Department of Health and Human
Services, Public Health Service, Centers for Disease
Control and Prevention, National Institute for
Occupational Safety and Health, DHHS (NIOSH) 2004.
Publication No. 2004-165
Paclitaxel SmPC. BMS 2010
QuapoS 3 Quality Standard for the Oncology
Pharmacy Service with Commentary. Institute for
Applied Healthcare Sciences (IFAHS e.V.) for the
German Society of Oncology Pharmacy (DGOP e.V.).
2003
Rogers B, Emmett EA. Handling anti-neoplastic
agents: urine mutagenicity in nurses. J Nurs Scholarsh
1987; 19: 108–113
Sarto F, Trevisan A, Tomanin R, Canova A, Fiorentino
M. Chromosomal Aberrations, Sister Chromatid
Exchanges, and Urinary
Thioethers in Nurses Handling Antineoplastic Drugs.
Am J Ind Med 1990; 18: 689495
Sessink PJM, Van De Kerkhof MCA, Anzion RBM,
Noordhoek J, Bos RP. Environmental contamination and
assessment of exposure to antineoplastic agents by
determination of cyclophosphamide in urine of exposed
pharmacy technicians: is skin absorption an important
exposure route? Arch Environ Health 1994; 49(3): 165–
169
Sessink PJM, Kroese ED, van Kranen HJ, Bos RP.
Cancer risk assessment for health care workers
occupationally exposed to cyclophosphamide. Int Arch
Occup Environ Health 1995; 67: 317-323
Skov T, Maarup B, Olsen J, Rørth M, Winthereik H, Lynge
E. Leukaemia and reproductive outcome among nurses
handling antineoplastic drugs. Br J Ind Med 1992; 49:
855–861
Sotaniemi EA, Sutinen S, Arranto AJ, Sutinen S,
Sotaniemi KA, Lehtola J, Pelkonen RO. Liver Damage in
Nurses Handling Cytostatic Agents. Acta Med Scand
1983; 214: 181-9
Stücker I, Caillard J-F, Collin R, Gout M, Poyen D, Hémon
D. Risk of spontaneous abortion among nurses handling
antineoplastic drugs. Scand J Work Environ Health 1990;
16: 102–107
Ündeger Ü, Baþaran N, Kars A, Güç D. Assessment of
DNA damage in nurses handling antineoplastic drugs by
the alkaline COMET assay. Mutat Res 1999; 439: 277–
285
Valanis BG, Vollmer WM, Labuhn KT, Glass AG. Acute
symptoms associated with antineoplastic drug handling
among nurses. Cancer Nurs 1993a; 16(4): 288–295
Schmaus G, Schierl R, Funck S. Monitoring surface
contamination by anti-neoplastic drugs using gas
chromatography-mass spectrometry and voltammetry.
Am J Health Syst Pharm 2002; 59: 956–961
Valanis BG, Vollmer WM, Labuhn KT, Glass AG.
Association of antineoplastic drug handling with acute
adverse eff ects in pharmacy personnel. Am J Hosp
Pharm 1993b; 50: 455–462
Selevan SG, Lindbohm M-L, Hornung RW, Hemminki
K. A study of occupational exposure to antineoplastic
drugs and fetal loss in nurses. N Engl J Med 1985;
313(19): 1173–1178
Valanis B, Vollmer WM, Steele P. Occupational exposure
to antineoplastic agents: self-reported miscarriages and
stillbirths among nurses and pharmacists. J Occup
Environ Med 1999; 41(8): 632–638
13
Contaminação Química
Observações
14
15
C
m ont a
i cr m
ob i n
i o aç
l ó ão
gi
ca
Embolia
aérea
Contaminação
química
o s
sã t o
Le obj e dos
u
m g
co nt i a
po
Erro
de medicação
de
a
d
i l i t osa
b
ti n
pa me
om i ca
c
In ed
m
ão
aç s
i n ul a
am t íc
nt ar
Co or p
p
Riscos
da terapia
de infusão
As informações científicas resumidas apresentadas neste documento foram preparadas para profissionais da área
da saúde. Elas se baseiam em uma análise da literatura publicada e em diretrizes. A intenção é fornecer uma
introdução dos riscos comumente associados à terapia de infusão e aumentar a conscientização dos profissionais
de saúde sobre esses tipos de problemas. Devido à sua natureza resumida, este texto se limita a uma visão geral
e não leva em consideração todos os tipos de condições locais. A B. Braun não se responsabiliza por quaisquer
consequências que possam resultar das intervenções terapêuticas baseadas nestes aspectos gerais.
B. Braun Melsungen AG | Cuidado Hospitalar | 34209 Melsungen |
Alemanha
Tel. +49 5661 71-0 | www.bbraun.com | www.safeinfusiontherapy.com
16
Nr. 6069097 Edição: 03/2011