XI Encontro da SBQ-Rio de Janeiro
Universidade Federal Fluminense, 29 a 31 de outubro de 2007
XI ENCONTRO DA SBQ-RIO
P103
Comparação de Métodos Farmacopeicos e Interferência da
Formulação na Dissolução de Comprimidos de Hidroclorotiazida
Wagner Wollinger (PG), Denise Santos de Vasconcelos (PQ), Érico Daemon de
Oliveira (PQ), Glaucia Barbosa Cândido Alves Slana (PQ), Laís Bastos da
Fonseca (PQ)
Farmanguinhos - Fundação Oswaldo Cruz - Rua Sizenando Nabuco, 100 - CEP 21041-250 - Rio
de Janeiro (RJ)
[email protected]
Introdução e Objetivo
A hidroclorotiazida (Figura 1) é um
diurético tiazídico amplamente utilizado no
tratamento de edemas, doenças cardíacas e
diversas formas de disfunção renal e
hepática. É praticamente insolúvel em água a
25 °C e apresenta solubilidade limitada em
HCl 0,1 M (250 mg/L). Em função da baixa
solubilidade, o estudo de dissolução torna-se
fundamental, pois problemas tecnológicos ou
relacionados
à
formulação
podem
comprometer a biodisponibilidade do produto.
Figura 1. Hidroclorotiazida
O objetivo do trabalho foi comparar
diferentes metodologias para o teste de
dissolução e verificar a influência da
formulação na dissolução de comprimidos de
hidroclorotiazida.
Resultados e Discussão
Para o estudo da dissolução foram
empregados os meios HCl 0,1 M e água; no
primeiro caso, foi utilizado o aparato 1 com
velocidade de agitação de 100 (conforme
USP 29, 2006) a 150 rpm (conforme F. Bras.
IV, 1996); no segundo, aparato 2 a 50 rpm
(Rosa, 2005). Foi analisada uma formulação
de 25 mg comprimida com durezas de 5,0 e
10,0 kgf, bem como uma formulação de 75
mg (dureza 10 kgf) que utiliza excipientes
distintos, ambas fabricadas em triplicata por
Farmanguinhos. Além disso, os resultados
foram confrontados com os obtidos no estudo
de perfil de dissolução do produto de
referência Clorana® 25 mg (Sanofi-Aventis),
submetido às mesmas condições.
Todos as amostras de 25 mg cumpriram o
critério de aceitação para o teste de
dissolução pontual descrito nos métodos
empregados (Q = 65 % em 60 minutos). Em
contrapartida, nenhuma das amostras de
dosagem 75 mg alcançou o percentual
especificado para o teste.
A dureza do comprimido de 25 mg não
exerceu influência significativa na velocidade
de dissolução nos níveis avaliados (5 e 10
kgf).
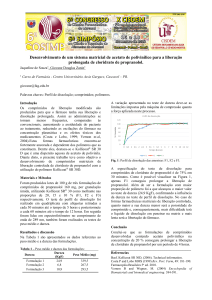
A liberação do fármaco na apresentação
de 25 mg desenvolvida por Farmanguinhos
foi mais rápida em água nos primeiros
tempos do perfil, ao contrário do que ocorreu
com as amostras de 75 mg, que
principalmente em meio ácido apresentaram
um processo de estagnação da dissolução
próxima a 30 minutos. No teste conduzido
com água como meio de dissolução e pás a
50 rpm, as amostras da apresentação de 25
mg apresentaram perfis semelhantes ao do
referência. Este grupo inclui produtos de
dureza baixa (5 kgf) e alta (10 kgf). Nenhuma
das amostras de 75 mg atingiu semelhança
com o produto de referência.
Para a formulação de 75 mg, a alta
proporção de carbonato de cálcio na
formulação – insolúvel em água e solúvel em
ácidos diluídos – facilitou a liberação da
HCTZ no início do teste em meio ácido,
embora ao final do perfil os testes em água
tenham apresentado resultados superiores
XI Encontro da SBQ-Rio de Janeiro
Universidade Federal Fluminense, 29 a 31 de outubro de 2007
de dissolução. A principal diferença desta
formulação para a de 25 mg é que a última
apresenta como principal componente a
celulose microcristalina.
Conclusão
O
meio
de
dissolução
água
demonstrou o melhor perfil de dissolução,
uma vez que os demais apresentaram uma
cinética de liberação muito lenta, não
atingindo o platô de dissolução mesmo após
2 horas de teste. No entanto, os métodos que
utilizam meio ácido não devem ser de todo
descartados
uma
vez
que
também
apresentaram certo potencial discriminativo.
Assim, o ideal seria construir uma correlação
in vivo-in vitro para uma avaliação mais
detalhada.
Referências bibliográficas
1
1
Farmacopéia Brasileira. 4.ed. São Paulo:
Atheneu, 1988.
Guidance for Industry: dissolution testing of
immediate release solid oral dosage forms.
FDA: Center for Drug Evaluation and
Research (CDER), 1997.
Resolução RE 310, de 1° de setembro de
2004. Agência Nacional de Vigilância
Sanitária.
Rosa, T.C.C. Dissertação de Mestrado.
Faculdade de Farmácia – UFRJ. Rio de
Janeiro, Brasil, 2005.
The United States Pharmacopeia USP 29.
Rockville: The United States Pharmacopeial
Convention, INC., 2006.