ESTUDO COMPARATIVO DOS PERFIS DE DISSOLUÇÃO DE COMPRIMIDOS DE
LORATADINA 10 MG
ALEXANDRE MACHADO RUBIM ([email protected]) / Centro Universitário Franciscano, Santa Maria RS
LUCIANE VARINI LAPORTA ([email protected]) / Centro Universitário Franciscano, Santa Maria
- RS
MARIANNE KELLERMANN ([email protected]) / Externo, Santa Maria - RS
MARCOS ROBERTO DOS SANTOS ([email protected]) / Centro Universitário Franciscano, Santa
Maria - RS
Palavras-Chave:
PERFIL DE DISSOLUÇÃO; LORATADINA; EFICIÊNCIA DE DISSOLUÇÃO.
A loratadina é um anti-histamínico tricíclico potente, de ação prolongada, pertencente à segunda geração,
com atividade seletiva antagônica nos receptores H1 periféricos, denominada quimicamente de 1-ácido
piperidinico, 4-(8-cloro-5,6-diidro-11H-benzol [5,6] ciclohepta [1,2-b] piridin-11-ilideno). É utilizada no
tratamento de doenças alérgicas como rinite alérgica, urticária crônica e asma (GENNARO, 2000). O fármaco
está disponível na forma de comprimidos, na concentração de 10 mg, ou comprimidos revestidos na mesma
concentração. No mercado nacional, existem cerca de 40 produtos contendo loratadina, excluindo-se os
medicamentos que contém esse ativo em associação. Destes, 25 são medicamentos genéricos e 7 deles
encontram-se na forma farmacêutica de comprimidos. A absorção de fármacos na forma de comprimidos
depende da capacidade do princípio ativo liberar-se da formulação em condições fisiológicas. Os
comprimidos possuem características que podem alterar a dissolução e comprometendo a bioequivalência.
Esta capacidade pode ser determinada através do estudo de perfil de dissolução, o que permite avaliar como
ocorre a dissolução de um fármaco em determinado tempo conhecido. Existem vários métodos propostos na
literatura para a realização da comparação de perfis de dissolução, divididos em modelos dependentes e
independentes. Acredita-se que entre todos os métodos possíveis os fatores de diferença (f1), e o fator de
semelhança (f2), são os mais utilizados devido a facilidade de aplicação e interpretação, o que leva vários
órgãos regulatórios, como FDA e ANVISA a adotá-los, especialmente f2, como indicativo da semelhança
entre perfis de dissolução (BRASIL, 2010; COSTA e LOBO, 2001).
O presente trabalho teve como objetivo principal avaliar a qualidade e comparar, através do estudo de perfil
de dissolução in vitro, de nove medicamentos contendo loratadina (quatro genéricos e cinco similares), com o
medicamento referência. As análises foram realizadas em conformidade com a monografia de loratadina
comprimidos, descrita na The United States Pharmacopeia (2011), que emprega as seguintes condições: 900
ml de ácido clorídrico 0,1 M, como meio de dissolução, aparto pás e velocidade de agitação de 50 rpm.
Alíquotas do meio foram coletadas nos tempos de 5; 10; 15; 20; 30; 60 e 90 minutos e o volume retirado foi
reposto, empregando-se o mesmo meio, na mesma temperatura. As amostras foram filtradas e diluídas até a
concentração adequada. Para a quantificação do produto, construiu-se curva analítica na faixa de
concentração de 5 µg/ml a 17 µg/ml utilizando-se loratadina SQR. Mediram-se as absorbâncias das soluções
em 280 nm, utilizando-se ácido clorídrico 0,1 M, para ajuste do zero. Calculou-se a quantidade de loratadina
dissolvida no meio, através da equação da reta, obtida da curva analítica. Os perfis de dissolução obtidos
foram comparados através do cálculo do fator de semelhança (f2), utilizando a porcentagem média dos
valores liberados na dissolução de cada produto, e através da eficiência de dissolução (ED), que foi
calculada a partir das curvas de porcentagem de fármaco dissolvido versus tempo (perfil de dissolução),
obtendo-se a área sob a curva (AUC) e a área total do gráfico (KHAN, 1975).
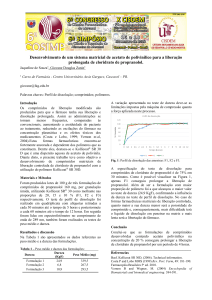
Os resultados referentes ao perfil de dissolução do medicamento referência, dos genéricos e similares de
loratadina 10 mg, foram interpolados na curva analítica (0,024x+0,0072), previamente construída, garantindo
linearidade na faixa de 5 a 17 µg/ml (r2 0,9999), não apresentando desvio de linearidade (p=0,05), quando
avaliada pela Análise de Variância (ANOVA). O medicamento referência, os quatro genéricos e quatros
similares apresentaram perfis de liberação imediata, ou seja, 85% do fármaco dissolvido em 15 minutos,
dispensando o cálculo do f2. Quando avaliamos a eficiência de dissolução, percebemos que somente G4,
S2, S3 e S4 possuem a mesma eficiência de dissolução que o medicamento Referência (R). Pela legislação
vigente, todos os medicamentos analisados apresentaram perfil de dissolução semelhante ao medicamento
de referência, o que é um bom indicativo para a possivel intercambialidade entre eles.
REFERÊNCIAS:
COSTA, Paulo.; LOBO. José Manuel Sousa; Modeling and comparison of dissolution profiles; European
Journal Pharmaceutical Sciences; 13; 123-133; 2001.
BRASIL; Agência Nacional de Vigilância Sanitária; RDC nº 31 de 11 de agosto de 2010; 08-2010.
GENNARO, Alfonso Remington.; Remington: the science and practice of pharmacy; Philadelphia;
Philadelphia; 2000.
KHAN, K. A.; The concept of dissolution efficiency.; J. Pharm. Pharmacol.; 28; 48-49; 1975.
THE UNITED STATES PHARMACOPEIA.; THE UNITED STATES PHARMACOPEIA.; Maryland; Rockville;
2008.