
Eletroquímica
Questão 01 - (PUC RS/2015)
Analise as informações a seguir.
A revista Nature publicou, em 6 de abril de 2015, o artigo “Uma bateria recarregável de íons
de alumínio ultrarrápida”, no qual apresenta uma bateria flexível recarregável que usa uma
placa de alumínio como ânodo e um cátodo de grafite-espuma tridimensional. A bateria
opera por deposição eletroquímica e dissolução de alumínio no ânodo, com formação de
ânions cloroaluminato no grafite, usando como eletrólito um líquido iônico não inflamável.
Cada pilha produz tensão aproximada de 2 volts, e a estrutura da bateria possibilita a
recarga em aproximadamente um minuto, podendo resistir a mais de 7.500 ciclos de
recarga.
As equações propostas para a pilha pelos autores são:
Al + 7AlCl4–
Cn[AlCl4] + e–
4Al2Cl7– + 3e–
Cn + AlCl4–
Sobre o tema e o texto, é correto afirmar que
a)
o alumínio se oxida e seu estado de oxidação se eleva de zero a +3.
b)
o ânodo de alumínio é o eletrodo onde ocorre a redução.
c)
há formação de cátions AlCl no cátodo.
d)
uma pilha eletroquímica funciona quando o potencial da reação global é negativo.
e)
ocorre a oxidação do metal alumínio na recarga da bateria.
4
–
TEXTO: 1 - Comum à questão: 2
FISCHETTI, Mark. Energia expolosiva. Scientific American Brasil – Aula Aberta, ano II, n. 15,
2013.
Grandes recalls de fabricantes de baterias de íons de lítio para notebooks suscitaram
questões sobre como essas fontes de energia podem aquecer a ponto de pegar fogo.
Igualmente válida é a dúvida sobre por que os acidentes não são mais frequentes: são
poucos proporcionalmente às centenas de milhões de baterias vendidas anualmente.
As células eletroquímicas de íons de lítio empregam vários materiais, mas quase todas são
recarregáveis, como as usadas em câmeras fotográficas e telefones celulares, que utilizam
óxido de lítio-cobalto no cátodo e grafite no ânodo. Embora essa formulação seja “de certo
modo inerentemente insegura”, a fabricação cuidadosa e os dispositivos de segurança
embutidos limitaram os acidentes a poucas ocorrências. Mesmo assim, os fabricantes de
baterias têm aumentado a capacidade de carga em determinada célula devido à demanda
dos fabricantes de eletrônicos por maior durabilidade. Portanto, agora a margem de erros
é ainda menor. Aumentando o número de íons na célula, os fabricantes quadruplicaram a
capacidade energética desde seu lançamento comercial em 1991. (FISCHETTI. 2013. p. 1011).
Questão 02 - (UNEB BA/2014)
O cátodo da célula eletroquímica é formado por óxido de lítio e de cobalto, LiCoO 2(s), e o
ânodo, por grafite, quando a bateria está descarregada. Durante a recarga, a corrente
elétrica é invertida, e os íons de lítio são reduzidos no eletrodo do grafite. Na descarga, os
íons de lítio, Li+, deixam o grafite, após reação e voltam a formar óxido de lítio e de cobalto.
Com base nas informações do texto, das figuras e considerando-se o funcionamento de
célula eletroquímica e a força eletromotriz de célula igual a 3,7V, é correto afirmar:
01. O eletrólito é uma solução aquosa de sal de lítio.
02. O óxido de LiCoO2 é oxidado a CoO2, na recarga da pilha.
03. A oxidação e a redução ocorrem, respectivamente, no cátodo e no ânodo, durante a
descarga da pilha.
04. A voltagem de bateria, formada a partir da ligação em paralelo de quatro células
eletroquímicas de óxido de lítio-cobalto, é, aproximadamente, 15V.
05. A ligação entre o cátodo e o ânodo através do separador, por meio de partículas
metálicas, desvia o fluxo de corrente elétrica e causa resfriamento da célula
eletroquímica.
Questão 03 - (UECE/2015)
A primeira bateria a gás do mundo, conhecida hoje como célula a combustível, foi inventada
por sir Wiliam Robert Grove (1811-1896) que àquela época já se preocupava com as
emissões de gases poluentes causadas pelo uso de combustíveis fósseis. O combustível
básico da maioria das células a combustível é o hidrogênio, que reage com o oxigênio e
produz água e eletricidade e calor, de acordo com as reações simplificadas abaixo
representadas.
Reação 1: 2 H2(g) 4 H+(aq) + 4e–
Reação 2: O2(g) + 4 H+aq) + 4e– 2 H2O(l)
Sobre células a combustível, marque a afirmação verdadeira.
a)
A reação 1 é uma oxidação e ocorre no cátodo da célula.
b)
A reação líquida da célula é o oposto da eletrólise.
c)
A célula a combustível produz somente corrente alternada.
d)
A célula a combustível é um conversor de energia termoiônica.
Questão 04 - (UFAM/2015)
As células a combustíveis (CaC) são sistemas eficientes de conversão de energia química em
energia elétrica. Dentre os vários tipos de células a combustível, as células conhecidas como
PEMFC (Polymer Electrolyte Membrane Fuel Cell) têm se destacado, pois operam em baixas
temperaturas e podem ter aplicações móveis e estacionárias. Normalmente, a eficiência da
célula é máxima quando utiliza H2 e O2 como reagentes, onde um é reduzido e outro é
oxidado. As seguintes informações foram dadas acerca destas células:
I.
Uma CaC funciona de forma geral como se fosse uma pilha comum comprada num
supermercado.
II.
Uma CaC tem dois polos, um positivo (cátodo) e um negativo (ânodo).
III. O H2 é reduzido e o O2 é oxidado em uma CaC.
IV. No lugar de H2 poderia ser utilizado outro reagente, por exemplo, metanol, etanol ou
ar.
Assinale a alternativa correta:
a)
Somente a informação I está correta
b)
Somente as informações I e II estão corretas
c)
Somente as informações II, III e IV estão corretas
d)
Somente a informação IV está correta
e)
Todas as informações estão corretas
Questão 05 - (UNICAMP SP/2015)
Uma proposta para obter energia limpa é a utilização de dispositivos eletroquímicos que
não gerem produtos poluentes, e que utilizem materiais disponíveis em grande quantidade
ou renováveis. O esquema abaixo mostra, parcialmente, um dispositivo que pode ser
utilizado com essa finalidade.
Nesse esquema, os círculos podem representar átomos, moléculas ou íons. De acordo com
essas informações e o conhecimento de eletroquímica, pode-se afirmar que nesse
dispositivo a corrente elétrica flui de
a)
A para B e o círculo representa o íon O2–.
b)
B para A e o círculo representa o íon O2+.
c)
B para A e o círculo representa o íon O2–.
d)
A para B e o círculo representa o íon O2+.
Questão 06 - (FGV SP/2015)
Fontes alternativas de energia têm sido foco de interesse global como a solução viável para
crescentes problemas do uso de combustíveis fósseis. Um exemplo é a célula a combustível
microbiológica que emprega como combustível a urina. Em seu interior, compostos
contidos na urina, como ureia e resíduos de proteínas, são transformados por microorganismos que constituem um biofilme no anodo de uma célula eletroquímica que produz
corrente elétrica.
(http://www.rsc.org/chemistryworld/News/2011/October/31101103.asp. Adaptado)
Sobre essa célula eletroquímica, é correto afirmar que, quando ela entra em operação com
a geração de energia elétrica, o biofilme promove a
a)
oxidação, os elétrons transitam do anodo para o catodo, e o catodo é o polo positivo
da célula.
b)
oxidação, os elétrons transitam do catodo para o anodo, e o catodo é o polo positivo
da célula.
c)
oxidação, os elétrons transitam do anodo para o catodo, e o catodo é o polo negativo
da célula.
d)
redução, os elétrons transitam do anodo para o catodo, e o catodo é o polo positivo
da célula.
e)
redução, os elétrons transitam do catodo para o anodo, e o catodo é o polo negativo
da célula.
Questão 07 - (UFRGS RS/2015)
Célula a combustível é uma alternativa para a produção de energia limpa. As semirreações
da célula são
H2
2H+ + 2e–
½ O2 + 2H+ + 2e–
H2O
Sobre essa célula, pode-se afirmar que
a)
H2 é o gás combustível e oxida-se no cátodo.
b)
eletrólise da água ocorre durante o funcionamento da célula.
c)
H2O e CO2 são produzidos durante a descarga da célula.
d)
célula a combustível é um exemplo de célula galvânica.
e)
O2 é o gás comburente e reduz-se no ânodo.
Questão 08 - (FGV SP/2016)
Em um experimento em laboratório de química, montou-se uma célula eletrolítica de
acordo com o esquema:
Usaram-se como eletrodo dois bastões de grafite, uma solução aquosa 1,0 mol.L–1 de
CuSO4 em meio ácido a 20 ºC e uma pilha.
Alguns minutos, após iniciado o experimento, observaram-se a formação de um sólido
de coloração amarronzada sobre a superfície do eletrodo de polo negativo e a formação de
bolhas na superfície do eletrodo de polo positivo.
Com base nos potenciais de redução a 20 ºC,
Cu2+ (aq) +2e–
Cu (s)
+ 0,34 V
2H+ (aq) + 2e–
H2 (g)
0,00 V
O2 (g) + 4H+ (aq) + 4e–
É correto afirmar que se forma cobre no
H2O (l)
+ 1,23 V
a)
catodo; no anodo, forma-se O2.
b)
catodo; no anodo, forma-se H2O.
c)
anodo; no catodo, forma-se H2.
d)
anodo; no catodo, forma-se O2.
e)
anodo; no catodo, forma-se H2O.
TEXTO: 2 - Comum à questão: 9
A galvanostegia é um processo usado na metalurgia para produzir revestimentos metálicos
em qualquer objeto como niquelagem, cromagem, prateação e douradura.
Para pratear um objeto de zinco, foi preparada uma solução através da dissolução de 2,0 g
de nitrato de prata, AgNO3, em água destilada até completar o volume de 50 mL e,
posteriormente, adicionada a uma cuba eletrolítica.
Questão 09 - (FM Petrópolis RJ/2015)
O objeto a ser prateado teve um papel fundamental como
a)
catodo, polo negativo.
b)
catodo, polo positivo.
c)
anodo, polo positivo.
d)
ponte salina.
e)
elemento que sofreu redução.
Questão 10 - (IFSC/2015)
O veículo elétrico é aquele que utiliza, pelo menos, um motor elétrico como forma de tração
para o transporte de pessoas, objetos e cargas. Compreendem os trólebus que recebem
energia de uma rede aérea, veículos elétricos a bateria que se abastecem na rede elétrica
quando estacionados e veículos elétricos híbridos que possuem mais de uma fonte de
energia para proporcionar tração. Nestes, a energia é gerada a bordo a partir de
combustíveis convencionais ou de células a combustível que utilizam hidrogênio.
Embora a venda e utilização de carros elétricos e híbridos ainda seja pequena, mesmo em
países mais desenvolvidos, existe uma grande oportunidade para a penetração desses
veículos no mercado de automóveis.
Fonte: http://www.mma.gov.br/clima/energia/veiculos-eletricos.
Acesso em: 2 out. 2014.
Alguns desses carros elétricos utilizam as baterias de lítio, que possuem ânodos de lítio
metálico. Por essa e outras razões, a produção de lítio mundial está em alta. Uma das etapas
de obtenção de lítio metálico é a eletrólise de cloreto de lítio.
Sobre a obtenção de lítio metálico, a partir da eletrólise de cloreto de lítio, assinale no
cartão-resposta a soma da(s) proposição(ões) CORRETA(S).
01. Na eletrólise de uma solução de cloreto de lítio, há formação de lítio metálico e gás
cloro.
02. O lítio metálico é obtido a partir da eletrólise ígnea do cloreto de lítio.
04. Tanto na eletrólise ígnea quanto na eletrólise aquosa do cloreto de lítio, há formação
de gás cloro.
08. O lítio metálico é produzido no cátodo da célula eletrolítica.
16. No ânodo da célula eletrolítica ocorre a reação de redução do lítio, produzindo, assim,
o lítio metálico.
Questão 11 - (UEPG PR/2015)
A figura abaixo apresenta uma cela eletrolítica, contendo uma solução aquosa 0,10 mol/L
de NaCl e uma fonte externa. Sobre o sistema apresentado, assinale o que for correto.
01. O cátodo é o eletrodo de grafite e o ânodo é o eletrodo de ferro.
02. Uma semirreação catódica possível é:
2H2O(l) + 2e–
H2(g) + 2OH–(aq).
04. O pH do meio reacional vai diminuir devido à formação de HCl.
08. No eletrodo de grafite ocorre um processo de redução.
16. No eletrodo de ferro pode-se observar a reação: Fe(s)
Fe2+(aq) + 2e–.
Questão 12 - (UNISA/2014)
A galvanoplastia é uma técnica utilizada em aplicações diversas, como a confecção de
bijuterias folheadas com metais nobres (ouro e prata) e o recobrimento de utensílios
ferrosos com metais, como o crômio, conferindo proteção e beleza a esses materiais. Na
confecção de bijuterias banhadas a ouro, ocorre a eletrodeposição desse metal sobre uma
peça de latão (liga de cobre e zinco). Todos os banhos de ouro são baseados nos sais
complexos de cianeto, ouro e potássio [KAu(CN)2], dissolvidos em água. A figura mostra
esquematicamente uma cuba eletrolítica, por onde passa uma corrente elétrica de 10 A
durante 193 s, em que o eletrodo que sofre oxidação deve ser constituído por uma peça de
ouro puro:
(http://chemistryh2t13.blogspot.com.br. Adaptado.)
Considere as possíveis reações com os íons Au+ e K+:
Au+ + e– Auº (massa molar = 197 gmol–1)
K+ + e– Kº (massa molar = 39 gmol–1)
Com base nas informações, e sabendo que o potássio continua dissolvido após o processo,
é correto afirmar que:
a)
durante o processo, a concentração de íons Au+ na solução deverá diminuir.
b)
o número de elétrons doados é igual ao número de elétrons recebidos, não sendo
assim um processo de oxirredução.
c)
a massa de ouro depositada sobre a peça de bijuteria é igual a 0,394 g.
d)
como só ocorre deposição de ouro sobre a peça, o íon Au+ apresenta maior potencial
de redução do que o íon K+.
e)
a peça de bijuteria a ser revestida deve ser conectada ao ânodo do sistema.
TEXTO: 3 - Comum à questão: 13
A vida em grandes metrópoles apresenta atributos que consideramos sinônimos de
progresso, como facilidades de acesso aos bens de consumo, oportunidades de trabalho,
lazer, serviços, educação, saúde etc. Por outro lado, em algumas delas, devido à
grandiosidade dessas cidades e aos milhões de cidadãos que ali moram, existem muito mais
problemas do que benefícios. Seus habitantes sabem como são complicados o trânsito, a
segurança pública, a poluição, os problemas ambientais, a habitação etc. Sem dúvida, são
desafios que exigem muito esforço não só dos governantes, mas também de todas as
pessoas que vivem nesses lugares. Essas cidades convivem ao mesmo tempo com a ordem
e o caos, com a pobreza e a riqueza, com a beleza e a feiura. A tendência das coisas de se
desordenarem espontaneamente é uma característica fundamental da natureza. Para que
ocorra a organização, é necessária alguma ação que restabeleça a ordem. É o que acontece
nas grandes cidades: despoluir um rio, melhorar a condição de vida dos seus habitantes e
diminuir a violência, por exemplo, são tarefas que exigem muito trabalho e não acontecem
espontaneamente. Se não houver qualquer ação nesse sentido, a tendência é que prevaleça
a desorganização. Em nosso cotidiano, percebemos que é mais fácil deixarmos as coisas
desorganizadas do que em ordem. A ordem tem seu preço. Portanto, percebemos que há
um embate constante na manutenção da vida e do universo contra a desordem. A luta
contra a desorganização é travada a cada momento por nós. Por exemplo, desde o
momento da nossa concepção, a partir da fecundação do óvulo pelo espermatozoide, nosso
organismo vai se desenvolvendo e ficando mais complexo. Partimos de uma única célula e
chegamos à fase adulta com trilhões delas, especializadas para determinadas funções.
Entretanto, com o passar dos anos, envelhecemos e nosso corpo não consegue mais
funcionar adequadamente, ocorre uma falha fatal e morremos. O que se observa na
natureza é que a manutenção da ordem é fruto da ação das forças fundamentais, que, ao
interagirem com a matéria, permitem que esta se organize. Desde a formação do nosso
planeta, há cerca de 5 bilhões de anos, a vida somente conseguiu se desenvolver às custas
de transformar a energia recebida pelo Sol em uma forma útil, ou seja, capaz de manter a
organização. Para tal, pagamos um preço alto: grande parte dessa energia é perdida,
principalmente na forma de calor. Dessa forma, para que existamos, pagamos o preço de
aumentar a desorganização do nosso planeta. Quando o Sol não puder mais fornecer essa
energia, dentro de mais 5 bilhões de anos, não existirá mais vida na Terra. Com certeza a
espécie humana já terá sido extinta muito antes disso. (Adaptado de: OLIVEIRA, A. O Caos e a
Ordem.
Ciência
Hoje.
Disponível
<http://cienciahoje.uol.com.br/colunas/fisica-sem-misterio/o-caos-e-a-ordem>.
Acesso em: 10 abr. 2015.)
em:
Questão 13 - (UEL PR/2016)
Em sintonia com o que é mencionado no texto I, também sob a perspectiva da
termodinâmica, deve-se realizar trabalho não espontâneo para combater a desordem.
Sistemas químicos que exploram reações químicas de oxidação e redução podem realizar
trabalhos espontâneos ou não espontâneos.
Sobre reações químicas em pilhas e em processos de eletrólise de soluções aquosas e de
compostos fundidos, assinale a alternativa correta.
a)
Em um processo de eletrólise, os elétrons fluem do cátodo para o ânodo em um
processo espontâneo.
b)
Em um processo de eletrólise, a energia elétrica é convertida em energia química
através de um processo não espontâneo.
c)
Em uma pilha galvânica, a energia elétrica é convertida em energia química através de
um processo não espontâneo.
d)
Em uma pilha galvânica, a reação espontânea apresenta um valor negativo de E◦, com
geração de energia sob a forma de trabalho.
e)
Em uma pilha galvânica, há um processo não espontâneo, na qual o cátodo é o polo
negativo e o ânodo é o polo positivo.
Questão 14 - (UCS RS/2015)
Halogênios são muito reativos e por esse motivo não são encontrados na natureza na
forma de substâncias simples. Entretanto, os mesmos podem ser obtidos industrialmente
a partir de um processo conhecido como eletrólise ígnea. No caso do cloro, esse processo
é realizado em uma cuba eletrolítica com o cloreto de sódio fundido. Aproximadamente 12
milhões de toneladas de Cl2 são produzidas anualmente nos Estados Unidos. Cerca de
metade desse cloro é utilizada na fabricação de compostos orgânicos halogenados,
enquanto o restante é empregado como alvejante na indústria do papel e de tecidos.
O volume de Cl2, medido nas CNPT, quando uma corrente elétrica de intensidade igual
a 10 ampères atravessa uma cuba eletrolítica contendo cloreto de sódio fundido durante
965 segundos é de
Dado: F = 96.500 C/mol
a)
0,71 L
b)
1,12 L
c)
2,24 L
d)
3,55 L
e)
4,48 L
Questão 15 - (UFJF MG/2015)
O alumínio metálico pode ser produzido a partir do mineral bauxita (mistura de óxidos de
alumínio, ferro e silício). Trata-se de um processo de produção caro, pois exige muita
energia elétrica. A última etapa do processo envolve a eletrólise de uma mistura de alumina
(Al2O3) e criolita (Na3AlF6) na temperatura de 1000 ºC. As paredes do recipiente que ficam
em contato com a mistura funcionam como cátodo, e os cilindros constituídos de grafite,
mergulhados na mistura, funcionam como ânodo.
Dados:
Al3+(l) + 3e–
Al(l)
0
= – 1,66 V
O2 (g) + 4e–
2 O2–(l)
0
= + 1,23 V
Responda ao que se pede.
a)
Explicite qual semirreação ocorre no ânodo e qual ocorre no cátodo.
Reação do ânodo:
Reação do cátodo:
b)
Escreva a equação equilibrada que representa a reação global e calcule a variação de
potencial do processo.
c)
O processo é espontâneo? Justifique a sua resposta.
Questão 16 - (UNIFOR CE/2016)
Para galvanizar uma chapa metálica com níquel, deve-se partir de um cloreto de niquel II
(por exemplo) por eletrólise em água. Para que seja depositada uma massa de níquel
equivalente a 1,96 g de níquel metálico sobre a chapa, o valor da corrente elétrica a ser
usada, supondo que o processo dure aproximadamente 100s, é de:
DADOS: CONSTANTE DE FARADAY = 96500 C; MASSA MOLAR: Ni = 58,7 g/mol.
a)
64,4 A.
b)
64,4 V.
c)
6,44 A.
d)
7,44 V.
e)
640 A.
Questão 17 - (UEPA/2015)
Um artesão de joias utiliza resíduos de peças de ouro para fazer novos modelos. O
procedimento empregado pelo artesão é um processo eletrolítico para recuperação desse
tipo de metal. Supondo que este artesão, trabalhando com resíduos de peças de ouro,
solubilizados em solventes adequados, formando uma solução contendo íons Au3+, utilizou
uma cuba eletrolítica na qual aplicou uma corrente elétrica de 10 A por 482,5 minutos,
obtendo como resultado ouro purificado.
Dados: Au=197 g/mol; constante de Faraday = 96.500C/mol.
O resultado obtido foi:
a)
0,197 gramas de Au
b)
1,97 gramas de Au
c)
3,28 gramas de Au
d)
197 gramas de Au
e)
591 gramas de Au
Questão 18 - (UERN/2015)
Para cromar uma chave, foi necessário montar uma célula eletrolítica contendo uma
solução aquosa de íon de cromo (Cr+2) e passar pela célula uma corrente elétrica de 15,2 A.
Para que seja depositada na chave uma camada de cromo de massa igual a 0,52 grama, o
tempo, em minutos, gasto foi de, aproximadamente:
(Considere a massa atômica do Cr = 52 g/mol.)
a)
1.
b)
2.
c)
63.
d)
127.
Questão 19 - (Unimontes MG/2015)
Determinadas peças de um antiquário foram submetidas a um banho de prata. Para cada
grama de prata processada foram gastos R$2,10 (dois reais e dez centavos). Nesse
processo, a quantidade de carga envolvida foi de 100 F.
O valor gasto no processo, em reais, é de
a)
R$22680.
b)
R$10800.
c)
R$5142.
d)
R$210.
Questão 20 - (UERN/2015)
As latas de conserva de alimento são feitas de aço. Para não enferrujar em contato com o
ar e não estragar os alimentos, o aço nelas contido é revestido por uma fina camada de
estanho. Não se deve comprar latas amassadas, pois com o impacto, a proteção de estanho
pode romper-se, o que leva à formação de uma pilha, de modo que a conserva acaba sendo
contaminada. De acordo com esse fenômeno, é correto afirmar que
a)
o ferro serve como metal de sacrifício.
b)
o polo positivo da pilha formada é o estanho.
c)
ao amassar a lata, o estanho passa a perder elétrons.
d)
quando a lata é amassada, o ferro torna-se o cátodo da reação.
Questão 21 - (Unimontes MG/2015)
O estudo dos valores de potenciais é essencial para o controle de operações industriais e
escolha de materiais que evitem problemas de corrosão de ferro. A corrosão pode ser
minimizada ou evitada por associação do ferro com outros metais. São dados os seguintes
potenciais das semirreações:
Em relação à oxidação do ferro, é INCORRETO o que se afirma em
a)
A utilização de magnésio pode impedir a corrosão do ferro.
b)
O oxigênio, entre as espécies apresentadas, é o oxidante mais efetivo.
c)
Em meio aquoso, a associação do ferro com o oxigênio constitui uma pilha.
d)
A associação com materiais de cobre retarda a corrosão do ferro.
Questão 22 - (UFU MG/2015)
A estocagem de solução de sulfato de zinco em recipientes metálicos exige
conhecimentos sobre possíveis processos de oxidação do zinco com o metal do recipiente,
de modo a não danificá-lo. A semirreação de redução do zinco pode ser descrita como
segue:
Zn2+(aq) + 2e–
Zn(s)
Eored = –0,76 V
Para auxiliar na decisão por diferentes recipientes que pudessem armazenar a referida
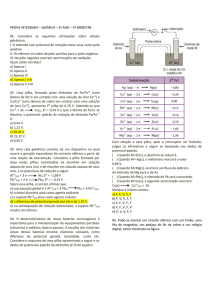
solução, um químico utilizou os dados da tabela a seguir.
Assim, o químico concluiu que, para a armazenagem do sulfato de zinco, deverá utilizar
um recipiente formado por
a)
material que não sofra oxidação.
b)
níquel que sofrerá oxidação na presença de Zn2+.
c)
ferro cuja reação com o Zn2+ possui potencial negativo.
d)
metais que se oxidam enquanto o íon zinco sofrer redução.
Questão 23 - (UNITAU SP/2015)
Para evitar a oxidação de estruturas metálicas que contêm ferro (Fe), é comum o uso de
blocos metálicos de sacrifício, os quais são colocados em contato com essas estruturas de
ferro. Os blocos de sacrifício doam elétrons para o ferro e assim evitam a sua oxidação.
Dentre os metais abaixo, qual ou quais se prestariam como metais de sacrifício?
Zn2+ + 2e–
Zn
Eº = –0,76 volts
Fe2+ + 2e–
Fe
Eº = –0,44 volts
Cu2+ + 2e–
Cu
Eº = +0,15 volts
Ni2+ + 2e–
Ni
Eº = –0,25 volts
a)
Apenas o Zn
b)
Apenas o Cu
c)
Apenas o Ni
d)
Zn e Cu
e)
Cu e Ni
Questão 24 - (ENEM/2015)
Alimentos em conserva são frequentemente armazenados em latas metálicas seladas,
fabricadas com um material chamado folha de flandres, que consiste de uma chapa de aço
revestida com uma fina camada de estanho, metal brilhante e de difícil oxidação. É comum
que a superfície interna seja ainda revestida por uma camada de verniz à base de epóxi,
embora também existam latas sem esse revestimento, apresentando uma camada de
estanho mais espessa.
SANTANA, V. M. S. A leitura e a química das substâncias. Cadernos PDE. Ivaiporã:
Secretaria de Estado da Educação do Paraná (SEED);
Universidade Estadual de Londrina, 2010 (adaptado).
Comprar uma lata de conserva amassada no supermercado é desaconselhável porque o
amassado pode
a)
alterar a pressão no interior da lata, promovendo a degradação acelerada do alimento.
b)
romper a camada de estanho, permitindo a corrosão do ferro e alterações do alimento.
c)
prejudicar o apelo visual da embalagem, apesar de não afetar as propriedades do
alimento.
d)
romper a camada de verniz, fazendo com que o metal tóxico estanho contamine o
alimento.
e)
desprender camadas de verniz, que se dissolverão no meio aquoso, contaminando o
alimento.
Questão 25 - (ITA SP/2016)
Considere uma célula eletrolítica na forma de um tubo em H, preenchido com solução
aquosa de NaNO3 e tendo eletrodos inertes mergulhados em cada ramo vertical do tubo e
conectados a uma fonte externa. Num determinado instante, injeta-se uma solução aquosa
de CuCrO4 verde na parte central do ramo horizontal do tubo. Após algum tempo de
eletrólise, observa-se uma mancha azul e uma amarela, separadas (em escala) de acordo
com o esquema da figura.
Com base nas informações do enunciado e da figura, assinale a opção ERRADA.
a)
O eletrodo Ee corresponde ao anodo.
b)
Há liberação de gás no Ed.
c)
Há liberação de H2 no Ee.
d)
O íon cromato tem velocidade de migração maior que o íon cobre.
e)
O pH da solução em torno do Ed diminui.
Questão 26 - (FAMERP SP/2015)
A figura representa o esquema de uma pilha formada com placas de níquel e zinco
mergulhadas em soluções contendo seus respectivos íons.
O catodo e a diferença de potencial da pilha são, respectivamente,
a)
a placa de níquel e + 0,53 V.
b)
a placa de níquel e – 0,53 V.
c)
a placa de zinco e – 0,53 V.
d)
a placa de zinco e + 0,53 V.
e)
a placa de níquel e – 0,99 V.
TEXTO: 4 - Comum à questão: 27
Um estudante de química montou três sistemas constituídos de tubos de ensaio com
amostras de metais imersos em soluções aquosas salinas para observar a ocorrência de
reações químicas, conforme a ilustração a seguir:
Tubo 1: Prata metálica (Ag) em solução de sulfato de magnésio (MgSO4)
Tubo 2: Zinco metálico (Zn) em solução de nitrato de prata (AgNO3)
Tubo 3: Alumínio metálico (Al) em solução de sulfato de cobre (CuSO4)
Questão 27 - (IFGO/2015)
Considerando os metais presentes na tabela, assinale qual a maior diferença de potencial
que é possível conseguir ao montar uma pilha escolhendo dois desses metais.
a)
Eº = + 4,03 V
b)
Eº = + 2,71 V
c)
Eº = + 2,46 V
d)
Eº = + 2,00 V
e)
Eº = +3,17 V
Questão 28 - (Fac. Direito de São Bernardo do Campo SP/2016)
A bateria de chumbo/ácido é um exemplo de bateria recarregável bastante empregada em
automóveis. A bateria consiste em várias pilhas em paralelo para aumentar a corrente
elétrica e seis conjuntos em série, fornecendo uma ddp de 12 V.
Cada pilha é formada por um eletrodo poroso de chumbo onde ocorre a semirreação:
Pb (s) + HSO4– (aq)
PbSO4 (s) + H+ (aq) + 2 e–
E = 0,30 V
O outro eletrodo é revestido por óxido de chumbo(IV). A reação que ocorre nesse eletrodo
pode ser representada pela semirreação:
PbO2 (s) + 3 H+ (aq) + HSO4– (aq) + 2 e–
PbSO4 (s) + 2H2O (l)
E = 1,70 V
Os dois eletrodos estão submersos em uma solução aquosa de ácido sulfúrico de densidade
aproximadamente 1,3 g.cm–3.
Sobre a bateria chumbo/ácido é INCORRETO afirmar que
a)
a solução aquosa de ácido sulfúrico age como eletrólito da pilha.
b)
durante a descarga, o eletrodo de chumbo é o polo negativo, enquanto que o eletrodo
de óxido de chumbo(IV) é o polo positivo.
c)
durante a descarga, a oxidação ocorre no eletrodo de chumbo poroso, enquanto a
redução ocorre no eletrodo de óxido de chumbo (IV).
d)
durante a descarga, o eletrodo de chumbo é o cátodo, enquanto que o eletrodo de
óxido de chumbo(IV) é o ânodo.
Atualmente há um número cada vez maior de equipamentos elétricos portáteis e isto tem
levado a grandes esforços no desenvolvimento de baterias com maior capacidade de carga,
menor volume, menor peso, maior quantidade de ciclos e menor tempo de recarga, entre outras
qualidades.
Questão 29 - (UNICAMP SP/2012)
Desenvolveu-se, recentemente, uma bateria com uma grande capacidade de carga e
número de ciclos, além de rapidez de recarga. Simplificadamente, no funcionamento dessa
bateria ocorre uma deposição de lítio metálico num eletrodo de estanho e carbono (Sn/C),
enquanto num eletrodo de carbono e sulfeto de lítio (Li2S/C) liberam-se o íon lítio e o
enxofre elementar. Considerando essas informações, pode-se afirmar que no
funcionamento da bateria ocorre
a)
uma reação de redução no eletrodo de Sn/C e uma reação de oxidação no eletrodo
Li2S/C, e essas reações não se invertem no seu processo de recarga.
b)
uma reação de oxidação no eletrodo de Sn/C e uma reação de redução no eletrodo
Li2S/C, e essas reações se invertem no seu processo de recarga.
c)
uma reação de oxidação no eletrodo de Sn/C e uma reação de redução no eletrodo
Li2S/C, e essas reações não se invertem no seu processo de recarga.
d)
uma reação de redução no eletrodo de Sn/C e uma reação de oxidação no eletrodo
Li2S/C, e essas reações se invertem no seu processo de recarga.
Questão 30- (UNIFOR CE/2014)
A pilha seca ácida foi desenvolvida em 1866, pelo químico francês George Leclanché (18391882). Trata-se de uma pilha comum hoje em dia, pois é a mais barata sendo usada em
lanternas, rádios, equipamentos portáteis e aparelhos elétricos como gravadores, flashes e
brinquedos. Essa pilha na verdade não é seca, pois dentro dela há uma pasta aquosa, úmida.
(Fonte: http://www.mundoeducacao.com/quimica/pilha-seca-leclanche.htm)
A reação global de funcionamento da pilha seca ácida é apresentada abaixo:
Zn (s) + 2MnO2(aq) + 2NH4+ (aq)
Zn2+ (aq) + Mn2O3 (s) + 2NH3(g)
Sobre a referida reação é possível afirmar que
a)
No anodo, ocorre a oxidação do zinco metálico que fica no envoltório da pilha segundo
a reação: Zn (s) Zn2+ (aq) + 2 e–. Os 2 elétrons do Zn metálico oxidado são
transferidos para o dióxido de manganês que assim é convertido a trióxido de
manganês.
b)
O dióxido de manganês sofre oxidação sendo convertido a trióxido de manganês e
portanto age como agente redutor no processo.
c)
Zinco metálico sofre oxidação no catodo e geram a corrente de 1,5 V típica destas
pilhas.
d)
Dióxido de manganês sofrem redução no anodo e geram a corrente de 1,5 V típica
destas pilhas.
e)
No catodo, ocorre a oxidação do zinco metálico que fica no envoltório da pilha segundo
a reação: Zn (s) Zn2+ (aq) + 2 e–. Os 2 elétrons do Zn metálico reduzido são
transferidos para o dióxido de manganês que assim é convertido a trióxido de
manganês.
GABARITO:
1) Gab: A
2) Gab: 02
3) Gab: B
4) Gab: B
5) Gab: A
6) Gab: A
7) Gab: D
8) Gab: A
9) Gab: A
10) Gab: 14
11) Gab: 27
12) Gab: D
13) Gab: B
14) Gab: B
15) Gab:
a) Reação do ânodo: 2 O2–(l) O2 (g) + 4e–
Reação do cátodo: Al3+(l) + 3e– Al(l)
b) 4 Al3+(l) + 6 O2–(l) 3 O2 (g) + Al(l)
0 1,6 1,23V
0 2,89V
c)
Não. Pois se trata de uma eletrólise que é um processo com variação de potencial
negativa.
16) Gab: A
17) Gab: D
18) Gab: B
19) Gab: A
20) Gab: B
21) Gab: D
22) Gab: C
23) Gab: A
24) Gab: B
25) Gab: A
26) Gab: A
27) Gab: E
28) Gab: D


![a) MnBr2 b) Na2S2O3 c) O3 d) [NO3]-](http://s1.studylibpt.com/store/data/004824294_1-e6644befe23aef65a5e854b9876a94db-300x300.png)








