CURSO DE LICENCIATURA EM QUÍMICA
ENCONTRO DE VIVÊNCIA 2015 – LICENCIATURA QUÍMICA
REVISÃO FÍSICO-QUIMICA - ARÉA 3
Prof. Osmir Fabiano Lopes
QUESTÃO 01 1- A corrosão eletroquímica opera como uma pilha. Ocorre uma transferência de elétrons quando
dois metais de diferentes potenciais são colocados em contato. O zinco ligado à tubulação de ferro, estando a
tubulação enterrada – pode-se, de acordo com os potenciais de eletrodo –, verificar que o anodo é o zinco, que
logo sofre corrosão, enquanto o ferro, que funciona como cátodo, fica protegido.
Dados: potenciais-padrão de redução em solução aquosa:
Temperatura = 25ºC; pressão = 1 atm; concentração da solução no eletrodo = 1,0 M
Semi reação Δ Eº (volt)
Zn2+ + 2e → Zn(s) – 0,763 V
Fe2+ + 2e → Fe(s) – 0,440 V
Assinale a equação global da pilha com a respectiva ddp da mesma:
a) Fe2+ + 2e → Zn2+ + 2e ΔE = + 0,232V
b) Zn + Fe2+ → Zn2+ + Fe ΔE = + 0,323V
c) Fe2+ + Zn → Zn + Fe2+ ΔE = – 0,323V
d) Fe + Zn → Zn2+ + Fe2+ ΔE = + 0,323V
QUESTÃO 02 2- Os halogênios são agentes oxidantes de variadas aplicações. Por exemplo, o flúor, como fluoreto,
é adicionado à água de beber para redução da cárie dentária; o Cloro é utilizado no tratamento de água para o
consumo humano, e como branqueador na indústria têxtil e de celulose; o Bromo é usado na síntese do
dibromoetileno, um poderoso inseticida; e o Iodo encontra aplicação na dieta alimentar para prevenção de
doenças da tireóide.
O poder oxidante dos halogênios F2, Cl2, Br2 e I2, pode ser avaliado pelos potenciais de redução das semireações:
F2 (g, 1 atm) + 2e– → 2F– (aq, 1M) E0 = 2,87 V
Cl2 (g, 1 atm) + 2e– → 2Cl– (aq, 1M) E0 = 1,36 V
Br2 (l) + 2e– → 2Br– (aq, 1M) E0 = 1,07 V
I2 (s) + 2e– → 2I– (aq, 1M) E° = 0,53 V
Dessa forma, pode-se afirmar que a adição de Cl2(g) a uma solução aquosa de NaF, NaBr e NaI, a 25ºC causará:
a) oxidação de Cl2 e I–
b) redução de F– e oxidação de Br–.
c) oxidação de Br e I–.
d) redução de Cl2 e I–.
e) oxidação de F–, Br e I–.
QUESTÃO 03 As células primárias são células galvânicas (pilhas) com os reagentes selados
dentro de um invólucro. Elas não podem ser recarregadas e quando descarregam-se são
descartadas, tornando-se um problema ao meio ambiente. Uma célula seca é um tipo de célula primária mais
popular, conhecida simplesmente por pilha. Nesta pilha, a região cilíndrica de zinco serve como ânodo, e no
centro fica o cátodo, um bastão de carbono. O interior da pilha é forrado com papel que serve como barreira
porosa. O eletrólito é uma mistura pastosa e úmida de cloreto de amônio, NH4Cl, óxido de manganês (IV),
MnO2,carbono finamente pulverizado e um suporte inerte, usualmente goma. A amônia, NH3,proveniente dos
íons amônio, forma o complexo Zn(NH3)42+ com os íons Zn2+, e impede seu aumento e conseqüentemente
CURSO DE LICENCIATURA EM QUÍMICA - ENADE 2015
redução do potencial. Essas células secas são largamente utilizadas em diversos aparelhos, tais como lanternas,
brinquedos e relógios. Quanto à pilha citada, é correto afirmar que
a) produz energia através de um processo espontâneo.
b) o zinco metálico é reduzido a Zn2+.
c) o fluxo de elétrons parte do cátodo para o ânodo.
d) a diferença de potencial dessa pilha é um valor negativo.
e) no ânodo ocorre a oxidação do Zn2+.
QUESTÃO 04 4- Um estudante resolveu folhear sua chave com prata, utilizando a seguinte montagem:
Nessa célula, a chave corresponde ao:
A) anodo, que é o pólo positivo.
B) anodo, que é o pólo negativo.
C) catodo, que é o pólo positivo.
D) catodo, que é o pólo negativo.
E) cátodo, onde ocorre a oxidação.
QUESTÃO 05 “A eletrólise é um processo que separa os elementos químicos de um composto através do uso da
eletricidade. Resumindo, procede-se primeiro à decomposição (ionização ou dissociação) do composto em íons e,
posteriormente, com a passagem de uma corrente contínua através destes íons, são obtidos os elementos
químicos. Em muitos casos, dependendo da substância a ser eletrolisada e do meio em que ela ocorre, além de
formar elementos ocorre também a formação de novos compostos. O processo da eletrólise é uma reação de
oxirredução oposta àquela que ocorre numa célula galvânica, sendo, portanto, um fenômeno físico-químico não
espontâneo.” Assinale a alternativa incorreta:
a) Eletrólise ígnea é a reação química provocada pela passagem de corrente elétrica através de um composto
iônico fundido.
b) Eletrólise aquosa é a reação química provocada pela passagem de corrente elétrica por meio de uma solução
aquosa de um eletrólito.
c) Com a eletrólise podemos produzir substâncias na indústria química como a soda cáustica e hipocloritos.
d) A ddp negativa indica que a reação é espontânea e que poderá ser usada para gerar corrente elétrica.
e) Na eletrólise de uma solução aquosa de KI, o íon iodeto, quando volta a ser átomo, perde um elétron.
QUESTÃO 06 “O alumínio é um elemento químico de símbolo Al de número atômico 13 ( 13 prótons e 13
elétrons) com massa atómica 27 u. Na temperatura ambiente é sólido, sendo o elemento metálico mais
abundante da crosta terrestre. Sua leveza, condutividade elétrica, resistência à corrosão e baixo ponto de fusão
lhe conferem uma multiplicidade de aplicações, especialmente nas soluções de engenharia aeronáutica.
Entretanto, mesmo com o baixo custo para a sua reciclagem, o que aumenta sua vida útil e a estabilidade do seu
valor, a elevada quantidade de energia necessária para a sua obtenção reduzem sobremaneira o seu campo de
aplicação, além das implicações ecológicas negativas no rejeito dos subprodutos do processo de reciclagem, ou
mesmo de produção do alumínio primário.”
CURSO DE LICENCIATURA EM QUÍMICA - ENADE 2015
O alumínio é obtido industrialmente pela eletrólise ígnea da alumina (Al2O3). Indique a alternativa falsa:
a) O íon alumínio sofre redução.
b) O alumínio possui carga +3
c) O alumínio é produzido no cátodo.
d) O metal alumínio é agente redutor.
e) O íon O2- sofre oxidação.
QUESTÃO 07 A eletrólise é muito empregada na indústria com o objetivo de reaproveitar parte dos metais
sucateados. O cobre, por exemplo, é um dos metais com maior rendimento no processo de eletrólise, com uma
recuperação de aproximadamente 99,9%. Por ser um metal de alto valor comercial e de múltiplas aplicações, sua
recuperação torna-se viável economicamente. Suponha que, em um processo de recuperação de cobre puro,
tenha-se eletrolisado uma solução de sulfato de cobre (II) (CuSO4 ) durante 3h, empregando-se uma corrente
elétrica de intensidade igual a 10A. A massa de cobre puro recuperada é de aproximadamente Dados: Constante
de Faraday F = 96500C/mol; Massa molar em g/mol: Cu = 63,5.
A)0,02 g.
B) 0,04 g.
C) 2,40 g.
D)35,5 g.
E) 71,0 g.
QUESTÃO 08 Para que apresente condutividade elétrica adequada a muitas aplicações, o cobre bruto obtido por
métodos térmicos é purificado eletroliticamente. Nesse processo, o cobre bruto impuro constitui o ânodo da
célula, que está imerso em uma solução de CuSO4. À medida que o cobre impuro é oxidado no ânodo, íons Cu2+
da solução são depositados na forma pura no cátodo. Quanto às impurezas metálicas, algumas são oxidadas,
passando à solução, enquanto outras simplesmente se desprendem do ânodo e se sedimentam abaixo dele. As
impurezas sedimentadas são posteriormente processadas, e sua comercialização gera receita que ajuda a cobrir
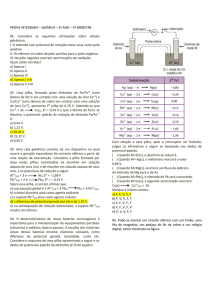
os custos do processo. A série eletroquímica a seguir lista o cobre e alguns metais presentes como impurezas no
cobre bruto de acordo com suas forças redutoras relativas.
Entre as impurezas metálicas que constam na série apresentada, as que se sedimentam abaixo do ânodo de cobre
são
a) Au, Pt, Ag, Zn, Ni e Pb.
b) Au, Pt e Ag.
c) Zn, Ni e Pb.
d) Au e Zn.
e) Ag e Pb.
QUESTÃO 09 O alumínio metálico pode ser obtido por processo eletroquímico, no qual o íon Al3+ é convertido a
alumínio metálico. Se uma unidade montada com esta finalidade opera a 100.000 A e 4 V, qual será a massa do
metal obtida após 50 minutos de operação? (Dados: constante de Faraday: 96.500 C mol–1 , Al = 27 g mol–1 ).
a) 3,0 x 108 g
b) 2,8 x 104 g
c) 27,0 g
d) 8.100 g
e) 8,1 x 106 g
CURSO DE LICENCIATURA EM QUÍMICA - ENADE 2015
QUESTÃO 10 Dário Belo, um torcedor fanático e vibrador, no ano em que seu time foi campeão, ouviu seguidas
vezes a narração do gol da vitória, narrado pelo saudoso e inigualável “Gandulão de Ouro”. Admita que o
desgaste sofrido pela cápsula de zinco da pilha, apenas para Dário Belo ouvir as várias repetições da narração do
gol, foi de 0,327g. Sabendo-se que a corrente elétrica fornecida pela pilha é constante e igual a 0,2 ampère, e que
a narração do gol levou exatos 25s, qual o número de vezes que o fanático Dário ouviu a narração do gol ? (Dado:
Zn = 65,4 u)
a) 100;
b) 193;
c) 1.000;
d) 10.000;
e) 300.
GABARITO:
01
B
02
C
03
A
04
D
05
D
06
D
07
D
08
B
CURSO DE LICENCIATURA EM QUÍMICA - ENADE 2015
09
B
10
B


![a) MnBr2 b) Na2S2O3 c) O3 d) [NO3]-](http://s1.studylibpt.com/store/data/004824294_1-e6644befe23aef65a5e854b9876a94db-300x300.png)