ESTUDO DA INFLUÊNCIA DA SINVASTATINA ENCAPSULADA
EM MICROESFERAS DE PLDLA NA REGENERAÇÃO ÓSSEA
Marlon Moda1, Cíntia C. Santos1, Diego D. Leonato1, Andrea R. Esposito1,2, Bruna A.
Mas1,2, Silvia M. M. Cattani1, Kelly F. Martins1, Maria L. P. Barbo1, Eliana A. R.
Duek1,2
2
1
Laboratório de Biomateriais, Pontifícia Universidade Católica de São Paulo, Sorocaba (SP), Brasil
Departamento de Engenharia de Materiais, Universidade Estadual de Campinas, Campinas (SP), Brasil
E-mail: [email protected]
Resumo. Estudos recentes demonstram que o uso de polímeros biorreabsorvíveis como
microcarregadores de fármacos oferece flexibilidade na dosagem e na cinética de liberação, melhorando
a eficácia no tratamento e fornecendo melhores condições para os pacientes. A sinvastatina tem como
efeito pleiotrópico a melhora da regeneração óssea mostrando-se adequada para associação a
microesferas no tratamento do tecido ósseo. O objetivo deste estudo consistiu em obter microesferas do
copolímero biorreabsorvível e biocompatível poli(L-co-DL ácido láctico) (PLDLA) contendo sinvastatina
e investigar sua ação na regeneração óssea em estudo in vivo. Para tanto, microesferas com e sem o
fármaco foram obtidas pelo processo de simples emulsão e caracterizadas por microscopia eletrônica de
varredura. No estudo in vivo, defeitos ósseos foram realizados na região proximal da tíbia de 45 ratos
Wistar, nos quais as microesferas com e sem o fármaco foram implantadas, além do grupo controle que
permaneceu sem tratamento. As microesferas obtidas apresentaram morfologia esférica, superfície lisa,
tamanho em escala micrométrica e grande distribuição de diâmetros. Após os períodos de 15, 30 e 60
dias os resultados histológicos evidenciaram diferenças entre o crescimento ósseo dos grupos,
principalmente no período de 15 dias pós-operatório. Todos os grupos apresentaram preenchimento do
defeito com trabéculas jovens e irregulares, porém no grupo com microesferas contendo sinvastatina o
fechamento foi total, sugerindo o efeito osteogênico do fármaco. Portanto, os resultados obtidos
mostraram que as microesferas de PLDLA são dispositivos promissores para emprego na liberação
controlada de fármacos na engenharia tecidual e medicina regenerativa, demonstrando a
biocompatibilidade do dispositivo no tecido ósseo.
Palavras-chave: PLDLA, Microesferas, Sinvastatina, Liberação controlada de
fármacos
INTRODUÇÃO
Atualmente, grande parte dos medicamentos é administrada por via parenteral e
para assegurar a eficácia do tratamento, concentrações elevadas do fármaco ou alta
frequência de dosagem devem ser administradas. Com isso, efeitos colaterais
exacerbados e resposta imune intensa pode ser desencadeados levando o paciente a um
grande desconforto e em alguns casos a desistência do tratamento (LANGER &
TIRELL, 2004; HAMMAN et al., 2005; BRANCO & SCHNEIDER, 2009;
AYUKAWA et al., 2010).
Para aumentar a eficácia da liberação parental de fármacos, tratamentos
localizados têm sido pesquisados. Eles envolvem carreadores que possibilitam a
liberação do fármaco no local a ser tratado, de forma controlada e otimizada em um
determinado período de tempo, reduzindo a toxicidade, pois o fármaco é mantido a um
nível terapeuticamente desejável no plasma e com isso diminuem os efeitos colaterais
(PAWAR et al., 2004; SHI & LI, 2005; GOLDBERG et al., 2007; LEE & YUK, 2007;
JABR-MILANE et al., 2008; KIM et al., 2010; ROMEO & FANOVICH, 2010; ZOU et
al., 2012 ).
Há vários meios de se promover a liberação controlada de fármacos, mas duas
formas vêm se destacando pelas suas propriedades diferenciadas: as nano e as
microesferas (PINTO et al., 2010).
As microesferas são partículas esféricas com diâmetro entre 1 e 250 µm
desenvolvidas visando inúmeras aplicações terapêuticas já que muitos dos novos
fármacos de estruturas complexas, como peptídeos, são frequentemente difíceis de
serem administrados de maneira conveniente por outros meios e no caso dos
antiinflamatórios não-esteroidais (AINES) pode-se evitar a irritação da mucosa gástrica
causada pelo medicamento (PEPPAS, 1997). Nestes vetores é possível encapsular o
fármaco e controlar sua liberação obtendo, assim, além da redução de gastos, maior
eficácia no tratamento parenteral (KUMAR, 2000).
A matriz ideal para liberação de fármacos deve ser inerte, biocompatível,
confortável para o paciente, capaz de carregar altas cargas de fármacos, simples para
administração e remoção, fácil de fabricar e esterilizar e de baixo custo. O modelo e
material adequados para a seleção da matriz em cada aplicação específica dependem de
diversas variáveis, incluindo propriedades físicas (mecânica, degradação, formação do
gel), propriedades do transporte (difusão) e propriedades biológicas (adesão celular e
sinalização) (DRURY & MOONEY, 2003).
Polímeros biorreabsorvíveis têm sido muito usados na área médica em
decorrência das inúmeras vantagens apresentadas por essa classe de polímeros
(BARBANTI et al., 2005; LIU et al., 2006; ESPOSITO et al., 2009; LEONATO et al,
2009; MODA et al., 2009; ESPOSITO et al., 2010; LIU et al, 2010; RAJPUT &
AGRAWAL, 2010; CATTANI et al., 2011; ESPOSITO et al., 2011), sendo a principal
delas o fato de degradarem por hidrólise de suas ligações ésteres, em contato com os
fluidos corpóreos, originando produtos na forma de oligômeros solúveis e não tóxicos
que, após sofrerem a ação metabólica do organismo, são transformados em CO2 e H2O
(AMBROSE & CLANTON, 2004).
Neste sentido, microesferas poliméricas têm-se mostrado ideais, pois apresentam
as características adequadas para a aplicação em questão e oferecem flexibilidade na
dosagem, cinética de liberação e marcação de receptores para liberação de fármacos ou
genes (YUN et al, 2004).
O poli(L-co-D,L acido lático), PLDLA, é um copolímero formado por dois
enantiômeros do acido lático que tem como característica diminuir a cristalinidade,
conferir boas propriedades mecânicas ao material, com tempo de degradação mais
adequado ao requerido pelas fraturas ósseas e liberação controlada de fármacos
(MOTTA & DUEK, 2008).
Apesar de a composição óssea possuir alta resistência, fraturas representam uma
realidade absoluta dentro da área médica e com grandes repercussões na saúde pública.
Mesmo com uma capacidade de regeneração extremamente eficaz, muitas fraturas
determinam uma perda de massa óssea incompatível com o processo de regeneração
humana e é nesse contexto que a intervenção cirúrgica ganha destaque, sendo que,
atualmente, duas estratégias são utilizadas: os transplantes e os implantes, isto é,
obtenção de substitutos de origem sintética ou natural que sejam inertes e capazes de
restabelecer a biomecânica da região envolvida (TREJO et al., 2000).
Neste contexto, microesferas contendo fatores de crescimento ósseo ou fármacos
podem estimular a regeneração. Estudos recentes mostraram que as estatinas (dentre
elas, a sinvastatina), um grupo de drogas usadas para a diminuição do colesterol,
possuem entre os vários efeitos pleiotrópicos, a melhora da regeneração do tecido ósseo
uma vez que podem alterar os mecanismos de formação e reabsorção óssea (MUNDY et
al, 1999; GARRETT & MUNDY, 2002; THYLIN et al., 2002; JADHAV & JAIN,
2006).
O efeito benéfico da sinvastatina no tecido ósseo foi verificado em um modelo
de ratas ovarioctomizadas, demonstrado que o fármaco preveniu parcialmente a perda
de osso esponjoso enquanto aumentou a formação do osso cortical (OXLUND &
ANDREASSEN, 2004). O aumento da expressão de BMP-2 também foi verificado em
trabalhos de cultura de células indiferenciadas tratadas com sinvastatina (SUGIYAMA
et al., 2000; MAEDA et al., 2001; PHILLIPS et al., 2001; SONG et al., 2003).
Recentemente, Nyan e colaboradores (2010) mostraram que a sinvastatina
libertada a partir de α-tricálcio fosfato por mais de 2 semanas melhorou a cicatrização
de defeitos realizados em calvárias de ratos, aparentemente através de um aumento
expressão de BMP-2 e TGF-β1.
Griffiths & Cartmell (2007), fizeram cultura de osteoblastos em uma solução
contendo sinvastatina e subsequentemente semearam as células em um arcabouço de
poli(L-ácido lático) (PLLA). A análise da matriz mostrou um aumento da mineralizacão
e da expressão da proteína óssea morfogenética do tipo 2 e da proteína não colágena
ostepontina. Esses achados sugerem que as estatinas além de aumentarem a
mineralizacão da matriz, têm o potencial de aumentar a diferenciação e crescimento de
osteoblastos, podendo contribuir assim, em cirurgias ortopédicas de reconstrução.
O estudo de caracterização das microesferas de PLDLA/sinvastatina realizado
por Santos (2011) evidenciou que o método de simples emulsão possibilitou a obtenção
de microesferas de PLDLA com morfologia e diâmetro variável entre 4 a 60 µm,
portanto compatível para a aplicação como dispositivo para liberação controlada de
fármacos, com eficiência na encapsularão da sinvastatina, mantendo a integridade das
estruturas do polímero e do fármaco. Além disso, a análise de HPLC demonstrou que
houve maior liberação inicial de fármaco, característica de sistemas compostos por
microesferas de diâmetros variados.
Sabe-se que para a obtenção de microesferas para liberação de fármaco por um
longo período de tempo é desejável que as partículas tenham distribuição de tamanho
variando de 20 a 100 µm (JEFFERY et al., 1991; JOHANSON et al., 2000; O’HAGAN
& SINGH, 2004).
Diante deste cenário, o presente estudo tem como objetivos obter microesferas
de PLDLA e estudar a eficiência desse novo dispositivo polimérico com encapsulação
da sinvastatina, visando aplicações terapêuticas no processo de regeneração de tecidos
ósseos.
MATERIAIS E MÉTODOS
1. Obtenção das Microesferas
As microesferas de PLDLA com e sem o fármaco foram obtidas pelo processo
extração/remoção do solvente onde a técnica por simples emulsão (O/W) foi escolhida
em função do fármaco hidrofóbico utilizado.
1.1. Microesferas sem o medicamento
O PLDLA foi sintetizado no laboratório de Biomateriais da PUC-SP, conforme
descrito por Motta (2007).
Inicialmente 1,0 g de PLDLA granulado foi dissolvido em 10,0 mL de clorofórmio
(Merck) sob agitação em agitador magnético (Ika) para sua total dissolução. A solução
resultante foi adicionada a 100 mL de solução aquosa de PVAl a 1% (Vetec) sob
agitação constante em emulsificador a 24 rpm por 6 minutos formando-se a assim a
simples emulsão.
Para que ocorresse a evaporação do solvente, a solução final permaneceu em
agitação por 3 horas. O conteúdo do béquer foi, então, vertido em tubos de ensaio e
estes submetidos à centrifugação por 5 minutos a 3500 rpm. As microesferas foram
retiradas do tubo e secas por 24 horas em estufa à vácuo e, ao final foram congeladas
em nitrogênio líquido e liofilizadas para estocagem. O processo descrito foi adaptado de
Garret e colaboradores (2007).
1.2. Microesferas com o fármaco Sinvastatina
O procedimento para a obtenção das microesferas de PLDLA com o fármaco
seguiu a mesma metodologia da obtenção das microesferas sem o fármaco. A diferença,
entretanto foi a adição 0,2g de sinvastatina dissolvida em 4mL de acetona à solução de
PLDLA. Posteriormente a solução polímero/fármaco foi submetida à emulsificação com
PVAl 1% seguindo a metodologia descrita anteriormente.
2. Morfologia das microesferas (MEV)
Para a análise morfológica das microesferas de PLDLA com e sem o fármaco foi
utilizado um microscópio eletrônico de varredura modelo JEOL JXA 840A com tensão
de 10kV. Para metalização das amostras foi utilizado um metalizador SPUTER
COATER BALTEC SCD 050 com corrente de 40mA por 200s.
3. Estudo in vivo
3.1. Animais experimentais
Foram utilizados quarenta e cinco (45) ratos Wistar de ambos os sexos com
idade aproximada de três meses e pesando entre 250 e 300 g, provenientes do Biotério
da Faculdade de Ciências Médicas e da Saúde da Pontifícia Universidade Católica de
São Paulo (FCMS/PUC-SP). Os animais foram mantidos em gaiolas coletivas
recebendo ração comercial e água “ad libitum” e em regime de claro-escuro
correspondente a 12 horas e temperatura controlada de cerca de 23 ºC 2 ºC.
Eles foram divididos em três (3) grupos equivalentes aos tempos de implantes
das microesferas: quinze (15), trinta (30) e sessenta (60) dias, sendo quinze (15) ratos
para cada tempo, onde cinco (n=5) receberam implantes de microesfera de PLDLA
pura, cinco receberam implantes de microesferas de PLDLA com sinvastatina, e os
outros cinco não receberam nenhum tratamento (controle negativo), a fim de evitar a
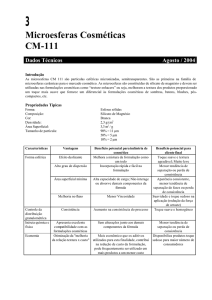
influência sistêmica do medicamento. A figura 1 representa, esquematicamente, através
de uma radiografia simples, o local onde foi realizado o defeito na tíbia do animal e os
tratamentos utilizados.
Molécula de Sinvastatina
Figura 1: Esquema representativo do local de implante na tíbia de ratos Wistar visto através de
uma radiografia simples e dos tratamentos utilizados (microesferas de PLDLA, microesferas de
PLDLA encapsuladas com sinvastatina e controle negativo, onde foi realizado apenas o defeito,
sem implante de nenhum material).
3.2. Procedimento cirúrgico
Os ratos foram pesados e submetidos à anestesia geral administrada via
intramuscular com uma solução de cloridrato de cetamina 10% (40 mg/kg) mais
cloridrato de xilazina 2% (5 mg/kg) por peso corporal.
Para o implante das microesferas de PLDLA (Fig. 2-A), depois de anestesiados,
os animais foram posicionados em decúbito dorsal e submetidos à tricotomia da região
medial da pata traseira direita (Fig. 2-B). Foi realizada uma incisão longitudinal na pele
de aproximadamente 2cm ao longo da borda anterior da tíbia. Com auxilio do bisturi, o
tecido muscular foi seccionado e afastado até a exposição do periósteo e do tecido ósseo
(Fig. 2-C). Com o uso de um mini-motor odontológico elétrico de baixa rotação (Beltec)
e uma broca Carbide de 2mm de diâmetro, foi produzido um defeito no terço superior
da tíbia (Fig. 2-D) sob irrigação constante com solução fisiológica estéril a fim de evitar
superaquecimento das bordas do defeito (ALMEIDA PRADO et al., 2006; ANBINDER
et al., 2006). A cavidade foi produzida na camada cortical atingindo o canal medular,
permitindo a introdução de 1,6 mg de microesferas contendo ou não sinvastatina, de
acordo com o grupo de tratamento (Fig. 2-E). Este procedimento foi realizado em uma
das patas de todos os animais para evitar um maior trauma e a influência da droga. A
sutura da musculatura e da pele foi realizada com Mononylon 4.0 com pontos simples
(Fig. 2-F), seguida de anti-sepsia com solução de iodo-polvedine na região do
ferimento.
Para o grupo controle, o defeito crítico de 2 mm ocasionado na tíbia do animal
permaneceu vazio.
A
B
C
D
E
F
Figura 2: Procedimento cirúrgico utilizado para o implante das microesferas de PLDLA. (A)
microesferas; (B) tricotomia da região medial da pata traseira direita; (C) incisão longitudinal na
pele ao longo da borda anterior da tíbia com exposição do periósteo e do tecido ósseo; (D)
defeito crítico no terço superior da tíbia; (E) implante das microesferas com ou sem sinvastatina,
de acordo com o grupo tratamento; (F) sutura simples da pele.
Finalizados os períodos pós-cirúrgicos, os animais foram sacrificados por
overdose de Halotano, um anestésico inalante. Em seguida, as tíbias de cada animal
foram cuidadosamente removidas e colocadas em solução fixadora de líquido de Bouin
por um período de 8 horas.
4. Processamento do material
As tíbias foram transferidas para uma solução de EDTA a 4,13% por
aproximadamente 30 dias, para a descalcificação.
A região do defeito foi marcada com tinta nanquim e os segmentos contendo os
defeitos foram preparados para análise histológica convencional de acordo com as
técnicas utilizadas para microscopia de luz, utilizando-se parafina como meio de
inclusão. A marcação com corante nanquim possibilitou o rápido reconhecimento das
áreas de osso neoformado após o trauma, isto também facilitou a inclusão do material e
a realização dos cortes.
Três cortes semi-seriados de cada bloco, com aproximadamente 3µm de
espessura e 15µm entre cada nível foram realizados a fim de analisar toda a região do
defeito realizado. As lâminas foram coradas com hematoxilina e eosina (HE) e
analisadas e fotografadas em microscópio óptico com luz polarizada (Eclipse E800 –
Nikon).
RESULTADOS E DISCUSSÃO
1. Morfologia das microesferas
As imagens obtidas pela microscopia eletrônica de varredura demonstraram que
as microesferas de PLDLA com e sem o fármaco apresentaram morfologia esférica,
superfície lisa, tamanho em escala micrométrica, grande distribuição de diâmetros, e
ausência de agregação ou adesão como pode ser observado na Fig. 3.
A
B
C
Figura 3: Eletromicrografias de varredura das microesferas de PLDLA com o fármaco (A e B) e
sem o fármaco (C).
Segundo Martin e colaboradores (2000) microesferas preparadas com polímeros
amorfos como o PLGA, poliestireno e resinas acrílicas tem levado a formação de
esferas com superfície lisa enquanto que as preparadas com polímeros cristalinos como
o poli(hidroxi butirato), PHB, e o poli(hidroxi butirato-co-valerato), PHBV, tem
apresentado superfície rugosa e porosa, sugerindo que as porções cristalinas do PHB e
do PHBV determinam o comportamento das cadeias poliméricas.
A porosidade das microesferas depende, em parte, do fluxo de água entre as
partículas poliméricas que vão originar as microesferas. Microesferas porosas permitem
maior facilidade de difusão do meio pelo interior da mesma, liberando assim o fármaco
de forma mais acelerada quando comparadas às microesferas maciças (WISCHKE &
SCHWENDEMAN, 2008), contudo, apresentam degradação mais rápida.
2. Estudo In vivo
Todos os animais sobreviveram ao procedimento cirúrgico até o tempo da
eutanásia. Durante o pós-operatório observou-se satisfatória recuperação clínica dos
ratos, os quais não apresentaram qualquer imobilização e mantiveram suas funções e
atividades semelhantes aos ratos não operados. Na execução do procedimento cirúrgico
foram encontradas algumas dificuldades relacionadas à retenção das microesferas no
interior do defeito, devido ao fluxo de sangue proveniente da medula óssea. Embora
durante o período de implantação das microesferas o fluxo sanguíneo tenha cessado ou
diminuído, não se pode afirmar o mesmo após o fechamento da incisão. Esta dificuldade
também foi relatada por outros autores (AYUKAWA et al., 2010; MASUZAKI et al.,
2010).
2.1. Análise macroscópica
A avaliação macroscópica da pele demonstrou que todos os animais
apresentaram completa cicatrização da incisão. Nenhuma diferença clínica pôde ser
detectada entre os grupos estudados.
Em relação à morfologia externa das tíbias retiradas no tempo de 15 dias pósoperatório pode-se observar no grupo controle (Fig. 4-A) a presença do defeito crítico
parcialmente fechado, sem evidencia de fibrose externa. Já no grupo com microesferas
puras (Fig. 4-B) e com microesferas contendo sinvastatina (Fig. 4-C) observou-se a
presença de um tecido fibroso envolvendo todo o defeito, resultado semelhante ao
encontrado no tempo de 30 dias pós-operátório com a diferença de que neste tempo
houve aparente fechamento total do defeito no grupo controle (Fig. 4-D).
A
B
C
D
Figura 4: Imagens macroscópicas das tíbias. (A) 15 dias - Grupo controle mostrando defeito;
(B) 15 dias - Grupo com microesferas apresentando tecido fibroso ao redor do defeito; (C) 15
dias - Grupo com microesferas contendo sinvastatina notando-se fibrose ao redor do defeito; (D)
30 dias - Grupo controle com aparente fechamento total do defeito. As setas indicam os
defeitos.
No tempo de 60 dias pós-operatório nota-se que no grupo controle houve
fechamento total do defeito semelhante ao período anterior. No grupo contendo
microesferas puras e com sinvastatina evidencio-se que em 4 ratos houve fechamento
total com escassa presença de fibrose enquanto que em um deles foi possível notar um
tecido fibrótico ao redor do defeito, semelhante ao tempo anterior.
2.2. Análise histológica
Grupo controle
A análise histológica após 15 dias pós-operatórios (Fig. 5-A e B) revela que
houve preenchimento das feridas em padrão irregular com formação de delicadas
trabéculas ósseas de aspecto imaturo, porém sem formação de osso cortical
propriamente dito, o que resultou em aspecto esponjoso. As trabéculas estão rodeadas
por células osteoblásticas hiperplásicas (indicativas de intensa atividade) e, entre elas,
evidenciam-se capilares e células fusiformes, sem presença de elementos das linhagens
hematopoiéticas, isto é, sem medula propriamente dita. No periósteo há fibrose evidente
e o osso neoformado é de padrão membranoso com pequenos focos de ossificação
endocondral, localizados nas bordas da lesão. Na medula observam-se macrófagos com
hemossiderina.
Após 30 dias pós-operatório (Fig. 5-C e D) houve fechamento quase total, porém
ainda irregular, com focos de fibrose e trabéculas mais espessas e agora anastomosadas,
com presença de medula entre elas e sem hiperplasia das células osteoblásticas. Nota-se
a presença de osso de aspecto mais maduro.
No tempo de 60 dias pós-operatório (Fig. 5-E), evidencia-se fechamento total
ainda sem osso totalmente maduro e em algumas lâminas observam-se falhas com
delicada fibrose. Um animal apresentou osteomielite e fechamento total do defeito,
porém com sequestros de osso necrótico, fibrose e abundante tecido de granulação com
polimorfonucleares neutrófilos (Fig. 5-F).
Implante de microesfera de PLDLA sem fármaco
Observou-se que no tempo de 15 dias pós-operatório (Fig. 6-A e B), houve
fechamento praticamente total, porém irregular, com trabéculas delicadas rodeadas por
acentuada hiperplasia das células osteoblásticas. Diferentemente do grupo controle,
entre as trabéculas observam-se elementos medulares com células da linhagem
hematopoiética. Houve degradação do polímero caracterizada por macrófagos
espumosos, sem presença de células gigantes e a fibrose é escassa. Além disso, ocorreu
neoformação óssea ao redor, tendendo a invadir a área representada pelo polímero. O
calo ósseo é evidente e há acentuada presença de osso jovem de aspecto esponjoso.
Após 30 dias pós-operatório (Fig. 6-C e D) é possível observar o fechamento
total, porém também irregular, com trabéculas mais espessas do que as observadas no
período anterior. Há crescimento ósseo ao redor do polímero, porém sem invasão das
porções internas do dispositivo. Este mostra, além de células espumosas, presença de
escassas células gigantes multinucleadas. As células osteoblásticas, ao redor das
trabéculas ósseas, são de volume e número menor do que no tempo anterior.
O tempo de 60 dias pós-operatório (Fig. 6-E e F) demonstrou fechamento total
com osso praticamente maduro com trabéculas espessas. Em alguns cortes identificamse restos do polímero com delicada fibrose ao redor. Em um animal há calo ósseo
maduro rodeando toda a espessura da haste óssea e presença de macrófagos com
hemossiderina.
Implante de microesfera de PLDLA com Sinvastatina
O tempo de 15 dias pós operatório (Fig. 7-A e B) apresentou fechamento
irregular com trabéculas jovens e não há exuberante hiperplasia das células
osteoblásticas como observado no grupo sem sinvastatina. Nota-se maior crescimento
ósseo nas áreas não lesadas, apresentando-se mais espesso na cortical ao redor de toda a
haste óssea, para fora do periósteo.
Após 30 dias pós-operatório (Fig. 7-C e D) houve fechamento total sem aspecto
uniforme, o que resulta em aspecto semelhante ao observado no grupo controle. Em
alguns animais é possível identificar o polímero. Nota-se hiperplasia das células
osteoblásticas no osso cortical maduro contralateral.
No tempo de 60 dias pós-operatório (Fig. 7-E e F) ocorreu fechamento total com
osso praticamente maduro e de aspecto semelhante ao anterior. Também não se
encontra o polímero em todos os animais e quando observado, o aspecto é semelhante
ao descrito anteriormente. A sinvastatina aparentemente não modificou o aspecto do
polímero e este continua a apresentar macrófagos espumosos e escassas células
gigantes.
Os resultados histológicos estão de acordo com a avaliação macroscópica.
A
B
C
D
E
F
Figura 5: Fotomicrografias do grupo controle: (A) 15 dias - Preenchimento da lesão em padrão
irregular com neocrescimento ósseo, HE, 20x; (B) 15 dias - Fibrose evidente e o osso
neoformado, HE, 100x; (C) 30 dias - Fechamento total, porém ainda irregular, HE, 20x; (D) 30
dias - Tecido ósseo neoformado na área da lesão e fibrose evidente, HE, 100x; (E) 60 dias Fechamento total com tecido maduro e trabéculas ósseas espessas, HE, 20x; (F) 60 dias Osteomielite, HE, 20x.
A
B
C
D
E
F
Figura 6: Fotomicrografias do grupo contendo microesferas de PLDLA sem fármaco: (A) 15
dias - Fechamento total e irregular da lesão com presença de micoresferas no interior, HE, 20x;
(B) 15 dias - Osso neoformado na área lesionada, HE, 100x; (C) 30 dias - Fechamento total sem
a presença de microesferas, HE, 20x; (D) 30 dias - Tecido ósseo neoformado com trabéculas
espessas, HE, 100x; (E) 60 dias - Fechamento total com presença das microesferas, HE, 20x; (F)
60 dias - Tecido ósseo neoformado com trabéculas e medula, HE, 100x.
A
B
C
D
E
F
Figura 7: Fotomicrografias do grupo contendo microesferas de PLDLA com sinvastatina: (A)
15 dias - Fechamento irregular da lesão com presença de microesferas com sinvastatina no
interior do defeito, HE, 100x; (B) 15 dias - Neoformação óssea com trabéculas finas. HE, 200x;
(C) 30 dias - Fechamento total sem a presença de microesferas, HE, 20x; (D) 30 dias - Tecido
ósseo neoformado em direção as microesferas com trabéculas espessas, HE, 100x; (E) 60 dias Fechamento total sem a presença de microesferas, HE, 20x; (F) 60 dias - Crescimento
neotecidual ósseo na região em que o defeito foi realizado, HE, 100x.
Um estímulo para a osteogênese local é um fator importante na
reparação de defeitos ósseos em geral. Nos últimos anos várias substâncias
têm sido utilizadas com este objetivo, incluindo proteínas morfogenéticas ósseas,
fatores de crescimento, drogas e hormônios. No entanto, tais substâncias ainda não são
empregadas clinicamente devido a problemas como custo, eficácia e segurança.
(MERAW et al., 1999; SCHMIDMAIER et al., 2002; FRANKE et al., 2003;
STENPORT et al., 2003; TRESGUERRES et al., 2003; SYKARAS et al., 2004; DE
RANIERI et al., 2005; CARTMELL, 2008; MORIYAMA et al., 2008; AKAGAWA et
al., 2009; AYUKAWA et al., 2010; MASUZAKI et al., 2010; MORIYAMA et al.,
2010; BROWN, et al., 2011; ZOU et al., 2012 ).
No presente estudo empregou-se uma estatina no intuito de verificar sua
influência na regeneração óssea. Além de atuar na redução dos níveis de LDL-colesterol
as estatinas exercem efeitos pleiotrópicos, tais como anti-inflamatório, antioxidante,
imunomoduladores, antitrombóticos e angiogênicos (HORIUNCHI & MAEDA, 2006).
Em relação à osteogênese seus efeitos estão associados ao aumento da biossíntese do
BMP-2 por inibir a prenilação de pequenas GTPases (MUNDY et al, 1999;
SUGIYAMA et al., 2000; GARRETT et al., 2001; OHNAK et al., 2001; SKOGLUND
et al., 2002; PARK, 2009; MASUZAKI et al., 2010; MORIYAMA et al., 2010; NYAN
et al., 2010; ZOU et al., 2012).
Vários estudos têm indicado que o uso de estatinas em seres humanos pode estar
associado ao aumento da densidade mineral óssea e uma diminuição do risco de fraturas
(EDWARD et al., 2000; CHAN et al., 2000; MEIER et al., 2000; MORIYAMA et al.,
2010).
Na formação óssea, os efeitos benéficos estão mais associados ao aumento da
expressão de BMP-2, que estimula a proliferação e diferenciação dos osteoblastos.
Embora o exato mecanismo pelo qual as estatinas influenciam a formação óssea ainda
não esteja claro, existe a possibilidade de que pequenas enzimas GTPases, preniladas
pelos produtos da síntese do colesterol, regulem negativamente a expressão de BMP-2
(MUNDY et al, 1999; GARRETT & MUNDY, 2002; ANBINDER et al., 2006;
HORIUCHI & MAEDA, 2006; WU et al., 2008; PARK, 2009; MASUZAKI et al.,
2010; NYAN et al., 2010; ZOU et al., 2012).
Por outro lado, as estatinas também podem ter efeito na diminuição da
reabsorção óssea. Os osteoclastos usam moléculas intermediárias da biosíntese do
colesterol, o farnesil e geranilgeranil, para modificar e ativar proteínas chaves
intracelulares. Assim, a ausência desses subprodutos pode causar efeitos que diminuem
a formação e função dos osteoclastos (CRUZ & GRUBER, 2002; GRASSER et al.,
2003).
Estudos demonstram que tanto a administração sistêmica/oral quanto a local
possuem efeitos positivos no osso. Porém, o primeiro apresenta uma maior dificuldade
para se conseguir a osteogênese, pois, uma vez que a droga sofre metabolização
hepática (reduzindo a concentração que chega ao osso), exige administração diária e em
maiores doses, exacerbando os efeitos colaterais e trazendo desconforto ao paciente. Por
outro lado, a administração local não sofre o metabolismo de primeira passagem no
fígado, mas exige o estabelecimento de um sistema de liberação controlada da droga.
Por esse motivo, neste estudo utilizou-se a aplicação local (CORSINI et al., 1999;
AYUKAWA et al., 2004; GUTIERREZ et al., 2006; MORIYAMA et al., 2008;
AYUKAWA et al., 2010; MASUZAKI et al., 2010; ROMEO & FANOVICH, 2010;
ZOU et al., 2012).
Vários tipos de carreadores foram empregados nos estudo citados acima, tais
como géis de metilcelulose, esponjas de colágeno, sulfato de cálcio e micro e
nanoesferas de polímeros biodegradáveis (THYLIN et al., 2002; WONG & RABIE,
2003; GARRETT et al., 2007; NYAN et al., 2007; LEE et al., 2008; JIANG et al.,
2010; MORIYAMA et al., 2010).
Sistemas poliméricos de liberação de fármacos são largamente utilizados e não
só permitem uma liberação lenta e gradual do ingrediente ativo, como também podem
possibilitar o direcionamento a alvos específicos do organismo a ser tratado, como um
sítio de inflamação e tumor (MOTTA & DUEK, 2008).
A partir da análise histológica dos resultados pode-se perceber diferenças entres
os grupos, principalmente no tempo de 15 dias pós operatório. A melhor resposta foi
obtida no grupo utilizando microesferas encapsuladas com sinvastatina conforme
relatado, também, por outros autores (MORIYAMA et al., 2008; MASUZAKI et al.,
2010; MORIYAMA et al., 2010).
Todos os grupos apresentaram preenchimento do defeito com trabéculas jovens,
irregulares e delicadas, porém no grupo contendo apenas microesferas esse fechamento
ocorreu quase totalmente enquanto que no grupo com microesferas contendo
sinvastatina o fechamento foi total. Além disso, esse último grupo apresentou células da
linhagem hematopoiética entre as trabéculas e menor quantidade de osteoblastos
hiperplásicos o que indica uma menor atividade óssea devido à maior maturação do
osso, ou seja, as trabéculas desse grupo encontravam-se em um estado de maior
maturação que as dos grupos anteriores.
A presença de tecido conjuntivo entre as trabéculas é inversamente proporcional
à maturidade óssea (em oposição à presença de células hematopoiéticas, que é
proporcional), uma vez que a regeneração de defeitos ósseos ocorre à partir da
diferenciação de células do tecido conjuntivo em osteoblastos que secretam a matriz
orgânica a ser mineralizada (OLIVEIRA, 2006).
Outra característica encontrada apenas no grupo de microesferas contendo
sinvastatina é a hiperplasia das células osteoblásticas no osso cortical maduro
contralateral, o que contraria os resultados encontrados por AYUKAWA e
colaboradores (2010) que não evidenciaram os efeitos da sinvastatina nessa região. Tal
resultado pode indicar que a sinvastatina teve ação não só na área do defeito, mas
também em regiões próximas, propagando-se através dos vasos sanguíneos da região.
A presença de macrófagos e células gigantes incluindo o desenvolvimento de
algum tecido de granulação já era considerada uma resposta esperada. Para os materiais
degradáveis a ação dessas células é necessária, caso contrário haveria a formação de
uma espessa cápsula fibrosa em torno do material, gerando diversas consequências
negativas (KATJA & RECHENBERG, 2008).
Analisando apenas os animais do grupo controle, apesar de em todos os tempos
analisados ter ocorrido o fechamento linear do defeito experimental, em todos os
espécimes o defeito foi identificado, diferindo do tecido ósseo antigo, sem haver
completa remodelação espontânea conforme descrito anteriormente por Almeida Prado
e colaboradores (2006).
No presente estudo, o defeito crítico realizado com 2mm de diâmetro está de
acordo com a literatura que utiliza roedores como modelo animal, encorajando sua
utilização para a avaliação da ação de medicamentos e materiais em estudos de
regeneração óssea (ALMEIDA PRADO et al., 2006). Além de defeitos maiores como,
por exemplo, de 3,5 cm e 4,0 cm, serem desencorajados por outros pesquisadores
devido ao elevado risco de fraturas e por isso não foram realizados (ALMEIDA
PRADO et al., 2006).
Diante do exposto, o presente estudo encontrou-se maior diferença histológica
entre o grupo controle e o de microesferas com sinvastatina no tempo de 15 e 30 dias
pós operatório do que no período de 60 dias, sendo mais evidente no tempo de 15 dias.
Tal achado corrobora os resultados de Masuzaki e colaboradores (2010) que avaliaram a
influência de microesferas de PLGA encapsuladas com sinvastatina no processo de
regeneração óssea ao redor de implantes realizados em tíbias de ratos. Esses autores
observaram que o efeito da droga no local do implante foi maior até a segunda semana e
manteve-se até a quarta semana, mas as diferenças entre os grupos de estatina e nãoestatina foram menores em 4 semanas do que às em 2 semanas. Esses resultados podem
implicar que a formação de osso atingiu um patamar em menos de 4 semanas. Neste
contexto, estatinas podem atuar numa fase precoce da formação do osso.
CONCLUSÕES
Os resultados evidenciaram que a obtenção de microesferas de PLDLA é uma
técnica eficaz para aplicação na liberação controlada de fármacos além de demonstrar a
biocompatibilidade desse material polimérico no tecido ósseo.
A sinvastatina mostrou ter propriedade osteoindutora, uma vez que ocorreu um
aumento na formação de tecido ósseo no defeito quando analisado histologicamente.
Os resultados sugerem o potencial para uso do material na engenharia tecidual e
medicina regenerativa.
AGRADECIMENTOS
Os autores agradecem a Fundação de Amparo à Pesquisa do Estado de São
Paulo – FAPESP pela bolsa concedida (Processo 10/20421-2).
REFERÊNCIAS
Akagawa, Y.; Kubo, T.; Koretake, K.; Hayashi, K.; Doi, K.; Matsuura, A.; Morita, K.; Takeshita, R.;
Yuan, Q.; Tabata Y. Initial bone regeneration around fenestrated implants in Beagle dogs using basic
fibroblast growth factor-gelatin hydrogel complex with varying biodegradation rates. Journal of
Prosthodontology Research, v. 53, p. 41-47, 2009.
Almeida Prado, F.; Anbinder, A. L.; Jaime, A. P. G.; Lima, A. P.; Balducci, I.; Rocha, R. F. Defeitos
ósseos em tíbias de ratos: padronização do modelo experimental. Revista de Odontologia da
Universidade Cidade de São Paulo, v. 18, n. 1, p. 7-13, 2006
Ambrose, C. G. & Clanton, T. O. Bioabsorbable implants: Review of clinical experience in orthopedic
surgery. Annals of Biomedical Engineering, v. 32, n.1, p. 171-177, 2004.
Anbinder, A. L.; Junqueira, J. C.; Mancini, M. N. G.; Balducci, I.; Rocha, R. F.; Carvalho, Y. R.
Influence os simvastatin on bone regeneration of tibial defects and blood cholesterol level in rats.
Brazilian Dental Journal, v. 17, n. 4, p. 267-273, 2006.
Ayukawa, Y.; Okamura, A.; Koyano, K. Simvastatin promotes osteogenesis around titanium implants.
Clinical Oral Implants Research, v. 15, p. 346-350, 2004.
Ayukawa, Y.; Ogino, Y.; Moriyama, Y.; Atsuta, I.; Jinno, Y.; Kihara, M.; Tsukiyama, Y.; Koyano, K.
Simvastatin enhances bone formation around titanium implants in rat tibiae. Journal of Oral
Rehabilitation, v. 37, p. 123-130, 2010.
Barbanti, S. H.; Zavaglia, C. A. C.; Duek, E. A. R. Polímeros bioreabsorvíveis na engenharia de
tecidos. Polímeros, v. 15, n. 1, p. 13-21, 2005.
Branco, M. C. & Schneider, J. P. Self-assembling materials for therapeutic delivery. Acta
Biomaterialia, v. 5, p. 817-831, 2009.
Brown, K. V.; Li. B.; Guda, T.; Perrien, D. S.; Guelcher, S. A.; Wenke, J. C. Improving bone
formation in a rat femur segmental defect by controlling bone morphogenetic protein-2 release. Tissue
Engineering Part A, v. 17, n. 13-14, p. 1735-1746, 2011.
CARTMELL, S. Controlled Release Scaffolds for Bone Tissue Engineering. Journal of
Pharmaceutical Sciences, v. 98, n. 2, p. 430-441, 2009.
Cattani, S. M. M.; Esposito, A. R.; Moda, M.; Cardoso, T. P.; Barbo, M. L. P.; Duek, E. A. R. Análise
histológica de arcabouços de PLDLA/PCT-T previamente cultivados com fibrocondrócitos após
implantes como prótese de menisco. In: Jornada Nacional de Iniciação Científica/63ª Reunião Anual da
SBPC, 2011.
Chan, K. A.; Andrade, S. E.; Boles, M.; Buist, D. S.; Chase, G. A.; Donahue, J. G.; Goodman, M. J.;
Gurwitz, J. H.; Lacroix, A. Z.; Platt, R. Inhibitors of hydroxymethylglutaryl-coenzyme A reductase and
risk of fractures among older women. Lancet, v. 355, p. 2185–2188, 2000.
Corsini, A.; Bellosta, S.; Baetta, R.; Fumagalli, R.; Paoletti, R.; Bernini, F. New insights into the
pharmacodynamic and pharmacokinetic proprieties of statins. Pharmacology Therapies, v. 84, p. 413428, 1999.
Cruz, A. C. & Gruber, B. L. Statins and osteoporosis: Can these lipid-lowering drugs also bolster
bones? Cleveland Clinic Journal of Medicine, v. 69, n.4, p. 277-288, 2002.
Dash, A. K. & Cutworth Ii, G. C. Therapeutic, Application Of Implantable Drug Delivery Systems.
Journal of Pharmacological and Toxicological Methods, v. 40, n. 1, p. 1-12, 1998.
De Ranieri, A.; Virdi, A. S.; Kuroda, S.; Shott, S.; Leven, R. M.; Hallab, N. J.; Sumner, E. R. Local
application of rhTGF-β2 enhances peri-implant bone volume and bone–implant contact in a rat model.
Bone, v. 37, p. 55-62, 2005.
Drury, J. L. & Mooney, D. J. Hydrogels for tissue engineering: scaffold design variables and
applications. Biomaterials, v. 24, p. 4337-4354, 2003.
Edward, C. J.; Hart, D. J.; Sector, T. D. Oral statins and increased bone-mineral density in
postmenopausal women. Lancet, v. 355, p. 2218-2219, 2000.
Esposito, A. R.; Silva, D. R.; Moda, M.; Alberto-Rincon, M. C.; Aragones, A.; Cardoso, T. P.; Duek,
E. A. R. Cell-based therapy on PLGA scaffolds for knee meniscal repair. In vivo study. In: Internacional
Conference on Tissue Engineering (ICTE), 2009, Leiria. Anais Leiria: Proceedings of Internacional
Conference on Tissue Engineering. Lisboa: IST Press, v. 1. p. 147-154, 2009.
Esposito, A. R; Duek, E. A. R; Cardoso, T. P.; Barbo, M. L. P.; Santana, G.; Moda, M.; Cattani, S. M.
M.; Barbieri, J. A.; Munhoz, M. M. Prótese meniscal de polímero biorreabsorvível pré-cultivada com
fibrocondrócitos. In: 43º Congresso Brasileiro de Ortopedia e Traumatologia, 2011.
Esposito, A. R; Cattani, S. M. M; Moda, M.; Barbieri, J. A.; Munhoz, M. M.; Cardoso, T. P.; Barbo,
M. L. P.; Duek, E. A. R. Regeneração completa do menisco utilizando pré-cultivo de fibrocondrócitos
sobre arcabouços de PLDLA/PCL-T. In: 6th Latin American Congress of Artificial Organs and
Biomaterials, 2010.
Franke Stenport, V.; Johansson, C. B.; Sawase, T.; Yamasaki, Y.; Oida, S. Fgf-4 and titanium
implants: a pilot study in rabbit bone. Clinical Oral Implants Research, v. 14, p. 363-368, 2003.
Garrett, I. R.; Gutierrez, G.; Mundy, G. R. Statins and bone formation. Current Pharmaceutical
Design, v. 7, p. 15-36, 2001.
Garrett, I. R. & Mundy, G. R. The role os statins as potential target for bone formation. Arthritis
Research, v. 4, n. 4, p. 237-240, 2002.
Garrett, I. R.; Gutierrez, G. E.; Rossini, G.; Nyman, J.; Mccluskey, B.; Flores, A.; Mundy, G. R.
Locally delivered lovastatin nanoparticles enhance fracture healing in rats. Journal of Orthopaedic
Research, v. 25, n. 10. p. 1351-1357, 2007.
Grasser, W. A.; Baumann, A. P.; Petras, S. F.; Harwood, H. J. Jr.; Devalaraja, R.; Renkiewicz, R.;
Baragi, V.; Thompson, D. D.; Paraklar, V. M. Regulation of osteoclast differentiation by statins. Journal
of Musculoskeletal and Neuronal Interactions, v. 3, n.1, p. 53-62, 2003.
Griffiths, S. L. & Cartmell, S. H. Use of statins for enhancing bone-tissue-engineered grafts.
European Journal of Plastic Surgery, 2007.
Goldberg, M.; Langer, R.; Jia, X. Nanostructured materials for applications in drug delivery and tissue
engineering. Journal of Biomaterials Science, Polymer Edition, v.18, n. 3, p.241-68, 2007.
Gutierrez, G. E.; Lalka, D.; Garrett, I. R.; Rossini, G.; Mundy, G. R. Transdermal application of
lovastatin to rats causes profound increases in bone formation and plasma concentrations. Osteoporosis
International, v. 17, p. 1033-1042, 2006.
Hamman, J. H.; Enslin, G. M.; Kotzé, A. F. Oral delivery of peptide drugs: barriers and developments.
BioDrugs, v. 19, n. 3, p. 165-177, 2005.
Horiuchi, N. & Maeda, T. Statins and bone metabolism. Oral Diseases, v. 12, p. 85-101, 2006.
Jabr-Milane, L. S.; Van Vlerken, L. E.; Yadav, S.; Amiji, M. M. Multi-functional nanocarriers to
overcome tumor drug resistance. Cancer Treatment Reviews, v. 34, p. 592-602, 2008.
Jadhav, S. B. & Jain, G. K. Statins and osteoporosis: new role for old drugs. Journal of Pharmacy and
Pharmacology, v. 58, n. 1, p. 3-18, 2006.
Jeffery, H.; Davis, S. S.; O’hagan, D. T. The preparation and characterisation of poly(lactide-coglycolide) microparticles: I: oil-in-water emulsion solvent evaporation. International Journal of
Pharmaceutics. v. 77, n. 2-3, p. 169–175, 1991.
Jiang, T.; Nukavarapu, S. P.; Deng, M.; Jabbarzadeh, E.; Kofron, M. D.; Doty, S. B.; Abdel-Fattah,
W. I.; Laurencin, C. T. Chitosan-poly(lactide-co-glycolide) microsphere-based scaffolds for bone tissue
engineering: in vitro degradation and in vivo bone regeneration studies. Acta Biomaterialia, v. 6, n. 9, p.
3457-3470, 2010.
Johanson, P.; Men, Y.; Merkle, H. P.; Gander, B. Revisiting PLA/PLGA microspheres: an analysis of
their potential in parenteral vaccination. European Journal of Pharmaceutics and Biopharmaceutics. v.
50, n. 1, p. 129-146, 2000.
Katja, M. R. N. & Rechenberg, B. V. Biocompatibility Issues with Modern Implants in Bone - A
Review for Clinical Orthopedics. The Open Orthopaedics Journal, v. 2, p. 66-78, 2008.
Kim, H.; Park, H.; Lee, J.; Kim, T. H.; Lee, E. S.; Oh, K. T.; Lee, K. C.; Youn, Y. S. Highly porous
large poly(lactic-co-glycolic acid) microspheres adsorbed with palmityl-acylated exendin-4 as a longacting inhalation system for treating diabetes. Biomaterials, 2010.
Ko, E. K.; Jeong, S. I.; Rim, N. G.; Lee, Y. M.; Shin, H.; Lee, B. K. In Vitro Osteogenic
Differentiation of Human Mesenchymal Stem Cells and In Vivo Bone Formation. Tissue Engineering
Part A, v. 14, n. 12, p. 2105-2119, 2008.
Kumar, M. N. V. R. Nano and Microparticles as Controlled Drug Delivery Devices. Journal of
Pharmacy and Pharmaceutical Sciences, v. 3, n. 2, p. 234-258, 2000.
Kumar, D. A.; Sujan, D. P.; Vijayasree, V.; Rao, L. N. Simultaneous determination of simvastatin and
ezetimibe in tablets by HPLC. E-Journal of Chemistry, v. 6, n. 2, p. 541-544, 2009.
Langer, R. & Tirrell, D. Designing materials for biology and medicine. Nature, v. 428, n. 6982, p.
487-492, 2004.
Lee, K. Y. & Yuk, S. H. Polymeric protein delivery systems. Progress in Polymer Science, v. 32, p.
669-97, 2007.
Lee, Y.; Schmid, M. J.; Marx, D. B.; Beatty, M. W.; Cullen, D. M.; Collins, M. E.; Reinhardt, R. A.
The effect of local simvastatin delivery strategies on mandibular bone formation in vivo. Biomaterial, v.
29, p. 1940-1949, 2008.
Leonato, D. D.; Duek, E. A. R.; Barbo, M. L. P. Estudo in vivo de membranas de PLDLA na pele de
ratos Wistar. In: 18º Encontro de Iniciação Cientifica da PUC-SP, 2009.
Liu, R.; Huang, S. S.; Wan, Y. H.; Ma, G. H.; Su, Z. G. Preparation of insulin-loaded PLA/PLGA
microcapsules by a novel membrane emulsification method and its release in vitro. Colloids and Surface
B: Biointerfaces, v. 51, n. 1, p. 30-38, 2006.
Liu, B.; Dong, Q.; Wang, M.; Shi, L.; Wu, Y.; Yu, X.; Shi, Y.; Shan, Y.; Jiang, C.; Zhang, X.; Gu, T.;
Chen, Y.; Kong, W. Preparation, characterization, and pharmacodynamics of exenatide-loaded poly(DLlactic-co-glycolic acid) microspheres. Chemical & Pharmaceutical Bulletin, v. 58, n. 11, p. 1474-1479,
2010.
Maeda, T.; Matsunuma, A.; Kawane, T.; Horiuchi, N. Simvastatin promotes osteoblast differentiation
and mineralization in MC3T3-E1 cells. Biochemical and Biophysical Research Communications, v. 280,
n. 3, p.874-877, 2001.
Martin, M. A.; Miguens, F. C.; Rieumont, J.; Sanchez, R. Tailoring of the external and internal
morphology of poly 3-hydroxy butyrate microparticles. Colloids and Surfaces B: Biointerfaces, v. 17, n.
2, p. 111-116, 2000.
Masuzaki, T., Ayukawa, Y.; Moriyama, Y.; Jinno, Y.; Atsuta, I.; Ogino, Y.; Koyano, K. The effect of
a single remote injection of statin-impregnated poly(lactic-co-glycolic acid) microspheres on osteogenesis
around titanium implants in rat tibia. Biomaterials, v. 31, p. 3327-3334, 2010.
Meier, C. R.; Schlienger, R. G.; Kraenzlin, M. E.; Schlegel, B.; Jick, H. HMG-CoA reductase
inhibitors and the risk of fractures. Journal of the American Medical Association, v. 283, p. 3205-3210,
2000.
Meraw, S. J.; Reeve, C. M.; Wollan, P. C. Use of alendronate in peri-implant defect regeneration.
Journal Periodontology, v. 70, p. 151-158, 1999.
Moda, M.; Esposito, A. R.; Barbo, M. L. P.; Duek, E. A. R. Estudo in vivo de arcabouços de PLGA
cultivados com fibrocondrócitos para aplicação como prótese de menisco. In: 18º Encontro de Iniciação
Cientifica da PUC-SP, 2009.
Moriyama, Y.; Ayukawa, Y.; Ogino, Y.; Atsuta, I.; Koyano, K. Topical application of statin affects
bone healing around implants. Clinical Oral Implants Research, v. 19, p. 600-605, 2008.
Moriyama, Y.; Ayukawa, Y.; Ogino, Y.; Atsuta, I.; Todo, M.; Takao, Y.; Koyano, K. Local
application of fluvastatin improves peri-implant bone quantity and mechanical properties: A rodent study.
Acta Biomaterialia, v. 10, p. 1610-1618, 2010.
Motta, Adriana Cristina. Síntese, Caracterização de dispositivos de poli (L-co D, L ácido lático).
Estudo da degradação in vitro e in vivo. Faculdade de Engenharia Mecânica, Universidade Estadual de
Campinas. 124 p., 2007. Tese de Doutorado.
Motta, A. C. & Duek, E. A. R. Estudo inicial da degradação “in vitro” de poli(L-co-D,L ácido lático)
sintetizado em laboratório. Revista Matéria, v.13, n.3, p. 429-438, 2008.
Mundy, G.; Garret, R.; Harris, S.; Chan, J.; Chen, D.; Rossini, G.; Boyce, B.; Zhao, M.; Gutierrez, G.
Stimulation of bone formation in vitro and in rodents by statins. Science, v. 286, n. 5446, p. 1946-1949,
1999.
Nyan, M.; Sato, D.; Oda, M.; Machida, T.; Kobayashi, H.; Nakamura, T.; Kasugai, S. Bone formation
with the combination of simvastatin and calcium sulfate in criticalsized rat calvarial defect. Journal of
Pharmacological Sciences, v. 104, p. 384-386, 2007.
Nyan, M.; Miyahara, T.; Noritake, K.; Hao, J.; Rodriguez, R.; Kuroda, S.; Kasugai, S. Molecular and
tissue responses in the healing of rat calvarial defects after local application of simvastatin combined with
alpha tricalcium phosphate. Journal of Biomedical Materials Research Part B: Applied Biomaterials, v.
93, n. 1, p. 65-73, 2010.
Ohnaka, K.; Shimoda, S.; Nawata, H.; Shimokawa, H.; Kaibuchi, K.; Iwamoto, Y. Pitavastatin
enhanced BMP-2 and osteocalcin expression by inhibition of Rho-associated kinase in human osteoblasts.
Biochemical Biophysical Research Communications, v. 287, p. 377-342, 2001.
O’hagan, D. T., Singh, M. Microparticles as vaccine adjuvants and delivery systems, 2004. In:
Kaufmann, S.H.E. (Ed.), Novel Vaccination Strategies. Wiley, Weinheim, p. 147-172.
Oliveira, N. M. Ultra-estrutura e imunocitoquímica da regeneração do processo alveolar de ratos após
aplicação local de sinvastatina. Instituto de Ciências Biomédicas, Universidade de São Paulo, 2006. Tese
de doutorado.
Oxlund, H. & Andreassen, T. Simvastatin treatment partially prevents ovariectomy-induced bone loss
while increasing bone formation. Bone, v. 34, n. 4, p. 609-618, 2004.
Park, J. B. The use of simvastatin in bone regeneration. Medicina Oral, Patología Oral y Cirugía
Bucal, v. 14, n. 9, p. 485-8, 2009.
Pawar, R.; Ben-Ari, A.; Domb, A. J. Protein and peptide parenteral controlled delivery. Expert
Opinion on Biological Therapy, v. 4, n. 8, p. 1203-1212, 2004.
Peppas, L. B. Polymers in Controlled Drug Delivery. Medical Plastics and Biomaterials, p. 1, 1997.
Phillips, B. W.; Belmonte, N.; Vernochet, C.; Ailhaud, G.; Dani, C. Compactin enhances osteogenesis
in murine embryonic stem cells. Biochemical and Biophysical Research Communications, v. 284, n. 2, p.
478-484, 2001.
Pinto, E.; Zhang, B.; Song, S.; Bodor, N.; Buchwald, P.; Hochhaus, G. Feasibility of localized
immunosuppression: 2. PLA microspheres for the sustained local delivery of a soft immunosuppressant.
Pharmazie, v. 65, n. 6, p. 429-435, 2010.
Rajput, M. S. & Agrawal, P. Microspheres in cancer therapy. Indian Journal of Cancer, v. 47, n. 4, p.
458-468, 2010.
Romeo, H. E. & Fanovich, M. A. Functionalized bridged silsesquioxane-based nanostructured
microspheres: performance as novel drug-delivery devices in bone tissue-related applications. Journal of
Biomaterials Applications, 2010.
Santos, Cíntia Cristina. Obtenção e caracterização de microesferas de pldla carregadas com
sinvastatina. São Paulo, Universidade Estadual de Campinas, Faculdade de Engenharia Mecânica. 81 p.
Dissertação de Mestrado, 2011
Sawyer, A. A; Song, S. J.; Susanto, E.; Chuan, P.; Lam, C. X. F.; Woodruff, M. A.; Hutmacher, D.
W.; Cool, S. M. The stimulation of healing within a rat calvarial defect by mPCL-TCP/collagen scaffolds
loaded with rhBMP-2. Biomaterials, v. 30, p. 2479-2488, 2009.
Schmidmaier, G.; Wildemann, B.; Cromme, F.; Kandziora, F.; Haas, N. P.; Raschke, M. Bone
morphogenetic protein-2 coating of titanium implants increases biomechanical strength and accelerates
bone remodeling in fracture treatment: a biomechanical and histological study in rats. Bone, v. 30, p. 816822, 2002.
Shi, Y. & Li, L. Current advances in sustained-release systems for parenteral drug delivery. Expert
Opinion on Drug Delivery, v. 2, n. 6, p. 1039-1058, 2005.
Skoglund, B.; Forslund, C.; Aspenberg, P. Simvastatin improves fracture healing in mice. Journal of
Bone Mineral Research, v. 17, p. 2004-2008, 2002.
Song, C.; Guo, Z.; Ma, Q.; Chen, Z.; Liu, Z.; Jia, H.; Dang, G. Simvastatin induces osteoblastic
differentiation and inhibits adipocytic differentiation in mouse bone marrow stromal cells. Biochemical
and Biophysical Research Communications, v. 308, p. 458-462, 2003.
Stenport, V. F.; Johansson, C. B.; Sawase, T.; Yamasaki, Y.; Oida, S. FGF-4 and titanium implants: a
pilot study in rabbit bone. Clinical Oral Implants Research, v. 14, p. 363-368, 2003.
Sugiyama, M.; Kodama, T.; Konishi, K.; Abe, K.; Asami S.; Oikawa, S. Compactin and Simvastatin,
but not pravastatin, induce bone morphogenetic protein-2 in human osteosarcoma cells. Biochemical and
Biophysical Research Communications, v. 271, p. 688-692, 2000.
Sykaras, N.; Iacopino, A. M.; Triplett, R. G.; Marker, V. A. Effect of recombinant human bone
morphogenetic protein-2 on the osseointegration of dental implants: a biomechanics study. Clinical Oral
Investigation, v. 8, p. 196-205, 2004.
Thylin, M. R.; Mcconnell, J. C.; Schmid, M. J.; Reckling, R. R.; Ojha, J.; Bhattacharyya, I.; Marx, D.
B.; Reinhardt, R. A. Effects of simvastatin gels on morine calvarial bone. Journal of Periodontology, v.
73, n. 10, p. 1141-1148, 2002.
Trejo, P. M.; Weltman, R.; Caffesse, R. Treatment of intraosseous defects with bioabsorsbable
barriers alone or in combination with decalcified freeze-dried bone allograft: a randomized clinical trial.
Journal of Periodontology, v. 71, n. 12, p. 1852-1861, 2000.
Tresguerres, I. F.; Blanco, L.; Clemente, C.; Tresguerres, J. A. F. Effects of local administration of
growth hormone in peri-implant bone: an experimental study with implants in rabbit tibiae. International
Journal of Oral and Maxillofacial Implants, v. 18, p. 807-811, 2003.
Wischke, C.; Schwendeman, S. P. Principles of encapsulating hydrophobic drugs in PLA/PLGA
microparticles. International Journal of Pharmaceutics, v. 364, n. 2, p. 298-327, 2008.
Wong, R. W. & Rabie, A. B. Statin collagen grafts used to repair defects in the parietal bone of
rabbits. British Journal of Oral and Maxillofacial Surgery, v. 41, p. 244-248, 2003.
Wu, Z.; Liu, C.; Zang, G.; Sun,H. The effect of simvastatin on remodeling of the alveolar bone
following tooth extraction. International Journal of Oral Maxillofacial Surgery, v. 37, p. 170-176, 2008.
Yun, Y. H.; Goetz, D. J.; Yellen, P.; Chen, W. Hyaluronan microspheres for sustained gene delivery
and site-specific targeting. Biomaterials, v. 25, n. 1, p. 147-157, 2004.
Zou, Y.; Brooks, J. L.; Talwalkar, V.; Milbrand, T. A.; Puleo, D. A. Development of an injectable
two-phase drug delivery system for sequential release of antiresorptive and osteogenic drugs. Journal of
Biomedical Materials Research Part B: Applied Biomaterials, v. 100, n. 1, p. 155-162; 2012.
INFLUENCE OF SIMVASTATIN LOADED PLDLA MICROSPHERES
IN BONE REGENERATION
Marlon Moda1, Cíntia C. Santos1, Diego D. Leonato1, Andrea R. Esposito1,2, Bruna A.
Mas1,2, Silvia M. M. Cattani1, Kelly F. Martins1, Maria L. P. Barbo1, Eliana A. R.
Duek1,2
1
Laboratory of Biomaterials, Pontifical Catholic University of São Paulo, Sorocaba (SP), Brazil
2
Departament of Materials Engineering, State University of Campinas, Campinas (SP), Brazil
E-mail: [email protected]
Abstract. Recent studies have shown that the use of bioresorbable polymers as drug microcarriers
provides flexibility in dosage and in the kinetics of release, improving the effectiveness in treating and
providing better conditions for the patients. Simvastatin has like a pleiotropic effect the improvement of
bone regeneration proved to be suitable for combination with microspheres in the treatment of bone
tissue. The aim of this study was to obtain microspheres of the bioresorbable and biocompatible
copolymer poly(DL-co-L lactic acid) (PLDLA) loaded with simvastatin and investigate its effect on bone
regeneration. For this purpose, microspheres with and without the drug were obtained by the process of
simple emulsion and subjected to in vitro characterization using scanning electron microscopy. Bone
defects were made in the proximal tibia of 45 Wistar rats in which the microspheres with and without
drug were implanted, in addition to the control group remained untreated. After periods of 15, 30 and 60
days the histological results showed differences of bone growth between the groups, especially after 15
days postoperatively. All groups showed a filling defect with irregular and young trabecular, but in the
group with microspheres containing simvastatin closure was complete, suggesting the osteogenic effect of
the drug. Therefore, the results showed that the PLDLA microspheres are promising devices for use in
controlled drug delivery in tissue engineering and regenerative medicine, demonstrating the
biocompatibility of the device in the bone tissue.
Keywords: Microspheres, PLDLA, Simvastatin, Controlled drug delivery system