UNIVERSIDADE FEDERAL FLUMINENSE
CENTRO DE ESTUDOS GERAIS
INSTITUTO DE QUÍMICA
PROGRAMA DE PÓS-GRADUAÇÃO EM GEOCIÊNCIAS – GEOQUÍMICA
ALINE SOARES FREIRE
AVALIAÇÃO DA RESINA QUELANTE CHELEX-100® NA
PRÉ-CONCENTRAÇÃO E DA ESPECTROMETRIA DE ABSORÇÃO
ATÔMICA DE ALTA RESOLUÇÃO COM FONTE CONTÍNUA E FORNO DE
GRAFITE PARA A DETERMINAÇÃO DE METAIS-TRAÇO EM ÁGUA
PRODUZIDA DE ALTA SALINIDADE
NITERÓI
2011
ALINE SOARES FREIRE
AVALIAÇÃO DA RESINA QUELANTE CHELEX-100® NA
PRÉ-CONCENTRAÇÃO E DA ESPECTROMETRIA DE ABSORÇÃO
ATÔMICA DE ALTA RESOLUÇÃO COM FONTE CONTÍNUA E FORNO DE
GRAFITE PARA A DETERMINAÇÃO DE METAIS-TRAÇO EM ÁGUA
PRODUZIDA DE ALTA SALINIDADE
Dissertação apresentada ao Curso de PósGraduação em Geociências da Universidade
Federal Fluminense, como requisito parcial
para a obtenção do Grau de Mestre. Área de
Concentração: Geoquímica Ambiental
Orientador: Prof. Dr. RICARDO ERTHAL SANTELLI
NITERÓI
2011
F866 Freire, Aline Soares.
Avaliação da resina quelante chelex-100® na pré-concentração e
da espectrometria de absorção atômica de alta resolução com fonte
contínua e forno de grafite para a determinação de metais-traço em
água produzida de alta salinidade / Aline Soares Freire. – Niterói :
[s.n.], 2011.
189 f. : il. color. ; 30 cm.
Dissertação (Mestrado em Geociências - Geoquímica
Ambiental) - Universidade Federal Fluminense, 2011. Orientador:
Prof. Dr. Ricardo Erthal Santelli.
1.
Química analítica. 2. Espectrometria de absorção atômica.
3. Água produzida. 4. Metal-traço. 5. Chelex-100. 6. Produção
intelectual. I. Título.
CDD 543.0858
"No fim, tudo dá certo. E se não
deu certo, é porque ainda não
chegou ao fim"
Fernando Sabino
“Yo no creo en brujas... Pero que
las hay, las hay!”
Miguel de Cervantes
(Don Quijote de la Mancha)
Aos meus pais, por tudo.
Ao meu cachorro Jack, única
companhia nas madrugadas...
Ao maior e mais intenso amor da
minha vida...
AGRADECIMENTOS
Primeiramente, ao meu querido equipamento de HR-CS AAS. Se nem mesmo ele
funcionasse, esse texto não exirtiria!!!
Ao Prof. Dr. Ricardo Erthal Santelli, pela presença ao longo de todo o trabalho. Por
ter estado sempre presente nos momentos em precisei de "orientação"... Por nunca
ter me abandonado. Obrigada também pela amizade, parceria no trabalho (seja ele
qual for...) e principalmente pela confiança que sempre depositou em mim e pelo
exemplo de pessoa e de profissional. Tenho muito orgulho de ter estado sob sua
orientação, que espero que seja mantida...
Ao Professor Bernhard Welz, da UFSC, pela disponibilidade em avaliar a
Dissertação. É uma imensa honra contar com sua presença e com seu valiosíssimo
conhecimento, do qual eu sou grande admiradora.
A Professora Maria Goreti Rodrigues do Vale, da UFRGS, por toda a atenção
sempre dispensada cada vez a encontro, seja em Congressos ou em cursos de
sobre o HR. É realmente uma pena que só possa haver um membro externo...
Aos Professores do Departamento de Geoquímica, Renato Campello Cordeiro e
Wilson Thadeu Valle Machado, por aceitarem o convite para a participação da PréBanca. Especialmente ao Wilson pela presença na Banca Avaliadora, apesar de sua
agenda lotada e de todos os contratempos...
A cada um dos meus "filhotes", por todo conhecimento que me propuseram não
apenas nos 2 anos de Mestrado, mas em todos os 5 anos de GPEAA.
Especialmente ao Hitachi (o primeiro) e ao HR (o último, ao menos até o presente
momento...). E com um carinho todo especial ao HJY, que, apesar de ser a última
coisa envolvida na minha Dissertação, foi o maior e mais importante dos (muitos)
maravilhosos acontecimentos.
À minha madrinha Marly, meus tios Eneida e Salvador (in memoriam) e minha prima
Renata, por todo incentivo, apoio e ajuda desde que eu era bem pequenina...
A minha amiga Lívia, pela paciência, por aguentar minhas (frequentes) flutuações de
humor e pela companhia durante o 3⁰ turno... Mas principalmente por nunca falar
comigo quando estou fazendo soluções-padrão!!! Por fim, pelos 8 longos anos de
amizade. Acho que você é a única que resiste!!!
Ao meu "primo" Ricardo Soares, por todos os cafés responsáveis pela "atualização
das informações"...!
Aos todos os colegas da minha turma de Mestrado e da turma do Doutorado (2009)
especialmente Nafisa, Raffaela D’Ângelo (“Miss Jacuecanga”) e Marcelo Maciel pela
companhia, trabalhos em conjunto e por toda a diversão durante as aulas!!! Ao
amigo Thiago Dias por sempre achar que sou uma química exemplar com análises
perfeitas... Como se isso realmente existisse!
A todos os colegas do GPEAA (laboratórios 108 e 403), por todos esses longos anos
de trabalho e boa convivência... Especialmente ao Leonardo Frazão (Leozinho),
Carolina Dallarosa e Rodrigo Derossi, pelo apoio e incentivo sempre.
Aos funcionários do Departamento de Geoquímica, especialmente a Hildete,
Anselmo e a bibliotecária Rosa. Ao bibliotecário Luís, que sempre com muita
paciência me ajudou com as benditas formatações da Dissertação. E obviamente ao
ilustríssimo secretário da coordenação, Nivaldo Camacho, por estar sempre me
"salvando" de tudo quanto é encrenca... Você é 1000!!!!!!!
A Rede Temática de Geoquímica da PETROBRAS pelo suporte financeiro e pela
concessão das amostras.
Aos orgãos de fomento CNPq, CAPES e FAPERJ por todo o suporte financeiro.
Especialmente a CAPES pela Bolsa de Mestrado durante o 1⁰ ano e a FAPERJ pela
Bolsa de Mestrado Nota 10 durante o 2⁰ ano de curso.
E por fim, a todos que de alguma forma contribuíram direta ou indiretamente para
este trabalho.
LISTA DE FIGURAS
Figura 1: Distribuição (em %) da matriz energética de 2004 no Brasil e no mundo. . 29
Figura 2: Notícia do jornal Estado da Bahia em 21 de janeiro de 1939, registrando o
início da exploração de petróleo no Brasil ................................................................. 32
Figura 3: Esquema de alguns tipos de água na exploração petrolífera offshore ....... 34
Figura 4: Produção offshore com injeção de água .................................................... 36
Figura 5: Perfis típicos de produção de óleo e água para um campo produtor no
nordeste do Atlântico ................................................................................................. 44
Figura 6: Expectativa de injeção de água e produção de óleo e água na Bacia de
Campos ..................................................................................................................... 45
Figura 7: Possíveis destinos para a água produzida ................................................. 45
Figura 8: Histórico e projeção da produção e do descarte de água produzida na
plataforma continental da Noruega. .......................................................................... 46
Figura 9: Aparato para a Extração em Fase Sólida ................................................... 51
Figura 10: Grupo funcional quelante das resinas funcionalizadas com IDA.............. 55
Figura 11: Aquisição de diferentes cátions divalentes pela resina quelante Dowex A1, em função do pH ................................................................................................... 55
Figura 12: Formas zwitteriônicas da Chelex-100® em função do pH ....................... 56
Figura 13: Demarcações aproximadas em análise quantitativa comumente usados 75
Figura 14: Faixa analítica para análise de traços de algumas técnicas
espectrométricas ....................................................................................................... 76
Figura 15: Projeção feita por Hieftje para a AAS por volta dos anos 2000 ................ 80
Figura 16: Representação esquemática de um espectrômetro de absorção atômica
de alta resolução com fonte contínua ........................................................................ 88
Figura 17: Foto de uma lâmpada de arco curto de xenônio operando em (A) modo
hot-spot e (B) em modo difuso .................................................................................. 90
Figura 18: Lâmpada de arco curto de xenônio (A) isolada e com detalhe nos
eletrodos e (B) dentro de seu compartimento no equipamento de HR-CS AAS ....... 90
Figura 19: Vista superior do monocromador DEMON ............................................... 92
Figura 20: Representação esquemática do detector de arranjo linear de dispositivos
de carga acoplada ..................................................................................................... 93
Figura 21: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Co em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com
atomização por plataforma.. .................................................................................... 110
Figura 22: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Cu em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com
atomização por plataforma ...................................................................................... 111
Figura 23: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Mn em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com
atomização por plataforma.. .................................................................................... 111
Figura 24: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Ni em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com atomização
por plataforma. ........................................................................................................ 112
Figura 25: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Pb em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com
atomização por plataforma. ..................................................................................... 112
Figura 26: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Co em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com
atomização por parede ............................................................................................ 113
Figura 27: Tela do software Aspect CS 1.4.0 mostrando o sinal de absorvância para
Ni em solução de concentração 20 μg L-1 em meio de HNO3 2% v/v, com atomização
por parede. .............................................................................................................. 114
Figura 28: Curvas de TP (-●-) e TA (-■-) para Co em solução de 5 μg L-1 em meio de
HNO3 2% v/v. .......................................................................................................... 115
Figura 29: Curvas de TP (-●-) e TA (-■-) para Cu em solução de 5 μg L-1 em meio de
HNO3 2% v/v... ........................................................................................................ 116
Figura 30: Tela do software Aspect CS 1.4.0 mostrando o registro do sinal de
absorvância para Cu em solução de concentração 5 μg L-1 em meio de HNO3 2%
v/v. Atomização por plataforma, TA = 2000ºC......................................................... 117
Figura 31: Tela do software Aspect CS 1.4.0 mostrando o registro do sinal de
absorvância para Cu em solução de concentração 5 μg L -1 em meio de HNO3 2%
v/v. Atomização por plataforma, TA = 2100ºC......................................................... 118
Figura 32: Curvas de TP (-●-) e TA (-■-) para Mn em solução de 5 μg L-1 em meio de
HNO3 2% v/v ........................................................................................................... 119
Figura 33: Curvas de TP (-●-) e TA (-■-) para Ni em solução de 5 μg L-1 em meio de
HNO3 2% v/v ........................................................................................................... 120
Figura 34: Curvas de TP (-●-) e TA (-■-) para Pb em solução de 5 μg L-1 em meio de
HNO3 2% v/v ........................................................................................................... 121
Figura 35: Curvas de PC para Co em meio de água ultrapura e solução de NaCl
3,5% m/v, com adição de 200 µL de suspensão de Chelex-100® 10% m/v ............ 123
Figura 36: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl
3,5% m/v, com adição de 200 µL de suspensão de Chelex-100® 10% m/v. ........... 123
Figura 37: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, com adição de 200 µL de suspensão de Chelex-100® 10% m/v ............ 124
Figura 38: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5%
m/v, com adição de 200 µL de suspensão de Chelex-100® 10% m/v ..................... 124
Figura 39: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl
3,5% m/v, com adição de 200 µL de suspensão de Chelex-100® 10% m/v ............ 125
Figura 40: Curvas de PC para Co em meio de água ultrapura e solução de NaCl
3,5% m/v previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 126
Figura 41: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl
3,5% m/v previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 127
Figura 42: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 127
Figura 43: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5%
m/v previamente descontaminada, com adição de 200 µL de suspensão de Chelex100® 10% m/v.......................................................................................................... 128
Figura 44: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl
3,5% m/v previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 128
Figura 45: Curvas de PC para Co em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 100 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 130
Figura 46: Curvas de PC para Co em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 131
Figura 47: Curvas de PC para Co em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 500 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 131
Figura 48: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 100 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 132
Figura 49: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 133
Figura 50: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 500 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 133
Figura 51: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 100 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 134
Figura 52: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 135
Figura 53: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 500 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 135
Figura 54: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5%
m/v, previamente descontaminada, com adição de 100 µL de suspensão de Chelex100® 10% m/v.......................................................................................................... 136
Figura 55: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5%
m/v, previamente descontaminada, com adição de 200 µL de suspensão de Chelex100® 10% m/v.......................................................................................................... 137
Figura 56: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5%
m/v, previamente descontaminada, com adição de 500 µL de suspensão de Chelex100® 10% m/v.......................................................................................................... 137
Figura 57: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 100 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 138
Figura 58: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100® 10% m/v. ............................................................................................ 139
Figura 59: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 500 µL de suspensão de
Chelex-100® 10% m/v ............................................................................................. 139
Figura 60: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 100 µL de suspensão de
Chelex-100® 10% m/v, também descontaminada. .................................................. 141
Figura 61: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 200 µL de suspensão de
Chelex-100 10% m/v, também descontaminada. .................................................... 141
Figura 62: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl
3,5% m/v, previamente descontaminada, com adição de 500 µL de suspensão de
Chelex-100® 10% m/v, também descontaminada. .................................................. 142
Figura 63: Curvas de PC para Co em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de
suspensão de Chelex-100® 10% m/v, também descontaminada.. .......................... 144
Figura 64: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de
suspensão de Chelex-100® 10% m/v, também descontaminada ............................ 144
Figura 65: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de
suspensão de Chelex-100® 10% m/v, também descontaminada ............................ 145
Figura 66: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de
suspensão de Chelex-100® 10% m/v, também descontaminada ............................ 145
Figura 67: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de
suspensão de Chelex-100® 10% m/v, também descontaminada. ........................... 146
Figura 68: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co nos diferentes experimentos ...................................................................... 147
Figura 69: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Cu nos diferentes experimentos. ..................................................................... 147
Figura 70: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Mn nos diferentes experimentos. .................................................................... 148
Figura 71: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Ni nos diferentes experimentos. ...................................................................... 148
Figura 72: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Pb nos diferentes experimentos. ..................................................................... 149
Figura 73: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Ni e Pb para amostra AP 1 após o experimento de pré-concentração
................................................................................................................................ 149
Figura 74: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Mn, Ni e Pb para amostra AP 2 após o experimento de préconcentração ........................................................................................................... 150
Figura 75: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Mn, Ni e Pb para amostra AP 3 após o experimento de préconcentração ........................................................................................................... 150
Figura 76: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Ni e Pb para amostra AP 4 após o experimento de pré-concentração
................................................................................................................................ 151
Figura 77: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Ni e Pb para amostra AP 5 após o experimento de pré-concentração
................................................................................................................................ 151
Figura 78: Espectro tridimensional para o registro gráfico dos sinais de absorvância
para Co, Cu, Mn, Ni e Pb para amostra AP 6 após o experimento de préconcentração ........................................................................................................... 152
Figura 79: Curva de PC para Co em solução de NaCl 3,5% m/v nas condições
otimizadas. .............................................................................................................. 153
Figura 80: Curva de PC para Cu em solução de NaCl 3,5% m/v nas condições
otimizadas. .............................................................................................................. 154
Figura 81: Curva de PC para Mn em solução de NaCl 3,5% m/v nas condições
otimizadas. .............................................................................................................. 154
Figura 82: Curva de PC para Ni em solução de NaCl 3,5% m/v nas condições
otimizadas. .............................................................................................................. 155
Figura 83: Curva de PC para Pb em solução de NaCl 3,5% m/v nas condições
otimizadas. .............................................................................................................. 155
LISTA DE TABELAS
Tabela 1: Teor de metais-traço presentes na água do mar e nas águas produzidas
no Mar do Norte ........................................................................................................ 38
Tabela 2: Concentrações médias de metais e metalóides em nível traço em água
produzida................................................................................................................... 39
Tabela 3: Parâmetros determinados em amostras de água produzida coletadas pela
PETROBRAS, na Unidade Sergipe/Alagoas ............................................................. 40
Tabela 4: Concentrações médias dos principais ânions inorgânicos presentes na
água do mar e na água produzida ............................................................................. 41
Tabela 5: Teor de compostos orgânicos presentes nas águas produzidas no Mar do
Norte. ........................................................................................................................ 42
Tabela 6: Teor de diferentes aditivos presentes nas águas produzidas no Mar do
Norte. ........................................................................................................................ 43
Tabela 7: Aplicações presentes na literatura para determinações de metais,
metalóides e P em amostras de água produzida ...................................................... 48
Tabela 8: Seletividade para alguns cátions divalentes .............................................. 58
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em
amostras salinas.. ..................................................................................................... 60
Tabela 10: Principais características de algumas das técnicas de Espectrometria
Atômica.. ................................................................................................................... 75
Tabela 11: Requisitos instrumentais e operacionais necessários para atender as
condições STPF e suas conseqüências... ................................................................. 84
Tabela 12: Diversas aplicações da técnica de HR-CS AAS... ................................... 97
Tabela 13: Comprimentos de onda utilizados nas determinações por HR-CS GF
AAS... ...................................................................................................................... 109
Tabela 14: Programações de temperatura empregadas nas determinações por HRCS GF AAS ............................................................................................................. 122
Tabela 15: Valores de absorvância para os brancos (experimentos individuais) com
PC em água e em solução de NaCl 3,5 % m/v, antes e depois da descontaminação
do NaCl. Média (n = 3) das absorvâncias individuais. ............................................. 129
Tabela 16: Valores de absorvância para os brancos (experimentos individuais) com
PC em água ultrapura e em solução de NaCl 3,5 % m/v descontaminada, antes e
depois da limpeza da resina Chelex-100®. Média (n = 3) das absorvâncias
individuais................................................................................................................ 143
Tabela 17: Características analíticas. ..................................................................... 156
Tabela 18: Determinação de Cu, Mn e Ni nos materiais de referência certificados de
águas salinas. ......................................................................................................... 157
Tabela 19: Determinação de Co, Cu, Mn, Ni e Pb em amostras de água de
produzida................................................................................................................. 158
Tabela 20: Resultados obtidos para os ensaios de recuperação de Co, Cu, Mn, Ni e
Pb em amostras de água de produzida após adição de 2μg L-1 ............................. 159
LISTA DE ACRÔNIMOS, SÍMBOLOS E UNIDADES
A
Ampère
AAS
Espectrometria de Absorção Atômica (do inglês, Atomic Absorption
Spectrometry)
Aint
Absorvância integrada
Abs
Absorvância
a.C.
antes de Cristo
APDC
pirrolidina
ditiocarbamato
de
amônio
(do
inglês,
ammonium
pyrrolidine dithiocarbamate)
bar
bar (unidade de pressão)
BRS
Bactérias redutoras de sulfato
BHAPPDI
Bi(2-hidroxiacetofenona)-1,2-propanodiimina
(do
inglês,
Bis(2-
inglês,
5-(2-
hydroxyacetophenone)-1,2-propanediimine)
BTAHQ
5-(2-benzotiazolilazo)-8-hydroxyquinolina
(do
benzothiazolylazo)-8-hydroxyquinolene)
CAS
Cromo Azurol S (do inglês, chromazurol S)
CCD
(Arranjo linear de) Dispositivo de carga acoplada (do inglês, Charge
Coupled Device)
CCT
Tecnologia da célula de colisão (do inglês, Collision Cell Technology)
CM-PEHA
Penta-etilenohexamina
carboximetilado
(do
inglês,
carboxymethylated pentaethylenehexamine)
CONAMA
Conselho Nacional do Meio Ambiente
CPE
Extração no Ponto Nuvem (do inglês, Cloud Point Extraction)
CRM
Material de referência certificado (do inglês, Certified Reference
Material)
CS
Fonte contínua (do inglês, Continuum Source)
CTAB
Brometo de cetil-trimetil amônio (do inglês, cethyltrimethylammonium
bromide)
CV
Vapor frio (do inglês, Cold Vapor)
Δλ
Faixa de comprimento de onda
DDC (DDTC)
Dietil-ditiocarbamato (do inglês, diethyldithiocarbamate)
DDPA
Dietil-ditiofosfato de amônio
DEM
2-(dietilamino) etil-metacrilato (do inglês, 2-(diethylamino) ethyl
methacrylate)
DEMON
Monocromador duplo com rede Echelle (do inglês, Double-Echelle
Monochromator)
DLLME
Microextração Líquido-Líquido Dispersiva (do inglês, Dispersive
Liquid-Liquid Micro-Extraction)
DOM
Matéria orgânica dissolvida (do inglês, dissolved organic matter)
DPTH
1-(di-2-piridil)metileno
tiocarbonohidrazida
(do
inglês,
1-(di-2-
pyridyl)methylene thiocarbonohydrazide)
DRC
Célula de reação dinâmica (do inglês, dinamic reaction cell)
DZ
ditizona
ou
difeniltiocarbazona
(do
inglês,
dithizone
ou
diphenylthiocarbazone)
EGDMA
etilenoglicol-dimetacrilato (do inglês, ethyleneglycoldimethacrylate)
E&P Forum
Fórum de Produção e Exploração na Indústria Petrolífera (do inglês,
Oil Industry International Exploration and Production Forum)
F AAS
Espectrometria de Absorção Atômica por Chama (do inglês, Flame
Atomic Absorption Spectrometry)
FE
Fator de enriquecimento
fg
fentograma (10-15 g)
FI
Injeção em fluxo (do inglês, Flow Injection)
FPC
Fator de pré-concentração
FZ
Ferrozina (do inglês, Ferrozine)
GF AAS
Espectrometria de Absorção Atômica com Forno de Grafite (do
inglês, Graphite Furnace Atomic Absorption Spectrometry)
GTA
Atomizador de tubo de grafite (do inglês, Graphite Tube Atomizer)
HCL
Lâmpada de catodo oco (do inglês, Hollow Cathod Lamp)
HEDC
bi(2-hidroxietil)ditiocarbamato
(do
inglês,
bis(2-
hydroxyethyl)dithiocarbamate)
HF-LPME
Microextração em Fase Líquida Suportada em Fibra Oca (do inglês,
Hollow Fiber Liquid Phase Micro-Extraction)
HG
Geração de hidretos (do inglês, Hydride Generation)
8-HQ
8-hidroxiquinolina (do inglês, 8-hydroxyquinoline)
8-HQS
ácido 8-hidroxiquinolino-5-sulfônico (do inglês, 8-hydroxyquinoline-5sulfonic acid)
HR
Alta resolução (do inglês, High Resolution)
HR-CS AAS
Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua (do inglês, High Resolution Continuum Source Atomic
Absorption Spectrometry)
HR-CS F AAS Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua e Chama (do inglês, High Resolution Continuum Source
Flame Atomic Absorption Spectrometry)
HR-CS GF AAS Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua e Forno de Grafite (do inglês, High Resolution Continuum
Source Graphite Furnace Atomic Absorption Spectrometry)
HR-CS F MAS Espectrometria de Absorção Molecular de Alta Resolução com Fonte
Contínua e Chama (do inglês, High Resolution Continuum Source
Flame Molecular Absorption Spectrometry)
HR-CS GF MAS Espectrometria de Absorção Molecular de Alta Resolução com
Fonte Contínua e Forno de Grafite (do inglês, High Resolution
Continuum
Source
Graphite
Furnace
Molecular
Absorption
Spectrometry)
HS
do inglês, Headspace
ICP-MS
Espectrometria de Massa com Fonte de Plasma Indutivamente
Acoplado
(do
inglês,
Inductively
Coupled
Plasma
Mass
Spectrometry).
ICP OES
Espectrometria
de
Emissão
Óptica
com
Fonte
de
Plasma
Indutivamente Acoplado (do inglês, Inductively Coupled Plasma
Optical Emission Spectrometry)
ID
Diluição isotópica (do inglês, isotopic dilution)
IDA
ácido iminodiacético (do inglês, iminodiacetic acid)
I-DPC
Difenilcarbazona
imobilizada
(do
inglês,
immobilized
diphenylcarbazone)
I-8-HQ
8-hidroxiquinolina imobilizada
IIP
Polímero ionicamente impresso (do inglês, ionic imprinted polymer)
ISE
Eletrodo íon-seletivo (do inglês, Ion-Selective Electrode)
IUPAC
União Internacional de Química Pura e Aplicada (do inglês,
International Union of Pure and Applied Chemistry)
K
Kelvin
λ
Comprimento de onda
L
Litro
LLE
Extração Líquido-Líquido (do inglês, Liquid-Liquid Extraction)
LOD
Limite de detecção (do inglês, limit of detection)
LOQ
Limite de quantificação (do inglês, limit of quantification)
LPME
Microextração em Fase Líquida (do inglês, Liquid Phase MicroExtraction)
LS
Fonte de linhas (do inglês, line source)
LS AAS
Espectrometria de Absorção Atômica com Fonte de Linhas (do
inglês, Line Source Atomic Absorption Spectrometry)
MAH
Metacriloil-histidina
dihidratado
(do
inglês,
methacryloylhistidinedihydrate)
MAS
Espectrometria de Absorção Molecular (do inglês, Molecular
Absorption Spectrometry)
MASE
Extração por Solvente Assistida por Membrana (do inglês,
Membrane-Assisted Solvent Extraction)
MESI
Extração por Membrana com Interface Sorvente (do inglês,
Membrane Extraction with Sorbent Interface);
MC
Multicoletor (do inglês, multicolector)
Mg
Miligrama (10-3 g)
µg
Micrograma (10-6 g)
MIP
Polímero molecularmente impresso (do inglês, molecularly imprinted
polymers)
mm
Milimetro (10-6 m)
MMLLE
Extração Líquido-Líquido Suportada em Membrana Microporosa (do
inglês, Microporous Membrane Liquid-Liquid Extraction)
MNP
Nanopartículas magnéticas (do inglês, magnetic nanoparticles)
MS
Espectrometria de Massa (do inglês, Mass Spectrometry).
ms
Milisegundo (10-3 s)
NAA
Análise por Ativação de Nêutrons (do inglês, Neutron Activation
Analysis)
ng
Nanograma (10-9 g)
nm
Nanometro (10-9 m)
OGP
Associação Internacional de Produtores de Óleo e Gás (do inglês,
The International Association of Oil & Gas Producers)
PADMAP
2-(2-pyridil-azo)-5-dimetilaminofenol (do inglês, 2-(2-pyridylazo)-5dimethylaminophenol)
PAN
1-(2-piridilazo)-2-naftol (do inglês, 1-(2-pyridilazo)-2-naphthol)
PAR
4-(2-piridilazo) resorcinol (do inglês, 4-(2-Pyridylazo) resorcinol)
PC
Pré-concentração
pg
Picograma (10-12 g)
pH
Potencial hidrogeniônico
pm
Picometro (10-12 m)
ppb
Partes por bilhão (μg L-1 ou μg kg-1)
ppm
Partes por milhão (mg L-1 ou mg kg-1)
ppq
Partes por quatrilhão (pg L-1 ou pg kg-1)
ppt
Partes por trilhão (ng L-1 ou ng kg-1)
1-prOH
1-propanol
PTFE
Politetraflúor etileno
PTFE(KR)
Politetraflúor etileno em reator entrelaçado (KR: do inglês, knotted
reactor)
S
Segundo
σ
Desvio-padrão
SAFe (Program (Programa de) Amostragem e Análise de Ferro (do inglês, Sampling
and Analysis of Fe)
SF
Setor magnético (do inglês, sector field)
SI
Injeção sequencial (do inglês, sequential injection)
SISNAMA
Sistema Nacional do Meio Ambiente
SLME
Extração por Líquido Suportado em Membrana (do inglês, Supported
Liquid Membrane Extraction)
S/N
(Razão) sinal/ruído (do inglês, signal-to-noise ratio)
SPE
Extração em Fase Sólida (do inglês, Solid Phase Extraction)
SRTXRF
Fluorescência de Raios-X com Reflexão Total da Radiação
Síncroton (do inglês, Synchrotron Radiation Total Reflection X-Ray
Fluorescence)
SS
Amostragem sólida (do inglês solid sampling)
STPF
(Conceito) Forno com Plataforma e Temperatura Estabilizada (do
inglês, Stabilized Temperature Platform Furnace)
TA
Temperatura de atomização
TMAH
Hidróxido de tetrametil amônio (do inglês, tetramethylammonium
hydroxide)
TOG
Teor de Óleos e Graxas
TP
Temperatura de pirólise
US EPA
Agência de Proteção Ambiental Norte-Americana (do inglês, United
States Environmental Protection Agency)
UV-Vis
Espectrofotometria de Ultravioleta-Visível
V
Volt
W
Watt
XRF
Fluorescência
de
Raios-X
(do
inglês,
X-Ray
Fluorescence).
RESUMO
A análise de amostras hipersalinas ainda é um problema analítico a ser resolvido,
tendo em vista que a presença de sais dissolvidos é fonte freqüente de
interferências em espectrometria atômica. Atualmente, tem ocorrido um grande
aumento da demanda para caracterização de águas de alta salinidade, como as
águas produzidas, pelo fato de estas serem um dos maiores descartes da indústria
de petróleo. Devido a isto, metodologias analíticas para sua caracterização têm sido
amplamente desenvolvidas para a determinação de metais-traço em amostras
salinas e dentre as técnicas analíticas destaca-se a Espectrometria de Absorção
Atômica de Alta Resolução com Fonte Contínua, uma renovação da AAS
convencional. Contudo, para a obtenção de resultados acurados, é imprescindível
que se faça a remoção dos sais presentes nessas matrizes hipersalinas. Essa
separação prévia pode ser realizada através do emprego de resinas qualantes, que
pré-concentram o analito e permitem a remoção da matriz. Sendo assim, este
trabalho visa à avaliação do uso da resina quelante comercial Chelex-100® na préconcentração de Co, Cu, Mn, Ni e Pb e posterior determinação destes por
Espectrometria de Absorção Atômica de Alta Resolução com Fonte Contínua e
Forno de Grafite (HR-CS GF AAS). A metodologia foi validada através do uso dos
materiais de referência certificados para água do mar CASS-4, CASS-5 e NASS-5.
Os limites de detecção obtidos, em µg L-1, foram de 0,006; 0,070; 0,024; 0,074; e
0,018 para Co, Cu, Mn, Ni e Pb, respectivamente. Amostras de água produzida
oriundas de plataformas de petróleo offshore foram analisadas e os resultados
mostraram que essas águas possuem baixas concentrações dos elementos
determinados ou os mesmos não foram detectados. Os valores encontrados são
muito inferiores aos limites preconizados pela legislação brasileira através da
Resolução CONAMA 357/05.
Palavras-chave: Água produzida. Chelex-100®. Pré-concentração. Metais-traço.
HR-CS AAS.
ABSTRACT
The analysis of hypersaline samples is still an analytical problem to be solved, once
the presence of dissolved salts is a frequent source of interferences in atomic
spectrometry. Actually, there is a large increase in the interest in the caracterization
of this kind of sample, as produced waters are one of the largest discharges of
petroleum
industry.
Hence,
analytical
methodologies
to
produced
water
caracterization have been widely developed to trace metals determination in saline
samples and among the analytical techniques, there is High Resolution Continuum
Source Atomic Absorption Spectrometry, a renovation of conventional AAS.
However, to obtain accurated results, it's necessary to remove the salts present in
this high salinity matrices. This previous separation can be done employing a
chelating resin, that preconcentrates the analyte(s) and allows matrix removal. In this
way, the aim this work is to evaluate the use of chelating resin Chelex-100® to
preconcentrate Co, Cu, Mn, Ni and Pb, for the later determination by High Resolution
Continuum Source Graphite Furnace Atomic Absorption Spectrometry (HR-CS GF
AAS). The methodology was validated by the use of sewater certified reference
materials CASS-4, CASS-5 e NASS-5. The detection limits in µg L-1, were 0,006;
0,070; 0,024; 0,074; and 0,018 for Co, Cu, Mn, Ni and Pb, respectively. Produced
water samples from offshore petroleum platforms were analysed and results showed
that this waters have low concentrations of these studied elements or could not be
detected. Found values are much lower when compared to limits from Brazilian
legislation, in this case CONAMA 357/05 Resolution.
Key words: Produced water. Chelex-100®. Preconcentration. Trace metals. HR-CS
AAS.
SUMÁRIO
1 INTRODUÇÃO E FUNDAMENTAÇÃO TEÓRICA ................................................ 29
1.1 O PETRÓLEO .................................................................................................... 30
1.1.1 A exploração de petróleo................................................................................. 30
1.2 A ÁGUA PRODUZIDA........................................................................................ 33
1.2.1 Origem............................................................................................................. 34
1.2.2 Composição .................................................................................................... 36
1.2.3 Destino final para a água produzida ................................................................ 43
1.2.4 - Descarte, impactos e legislação ambiental .................................................... 45
1.2.5 Caracterização de águas produzidas em relação a metais e metalóides ........ 47
1.3 A IMPORTÂNCIA DO PREPARO DE AMOSTRAS PARA A DETERMINAÇÃO
DE TRAÇOS E ULTRATRAÇOS .............................................................................. 49
1.3.1 A extração em fase sólida ............................................................................... 50
1.3.1.1 Pré-concentração de íons metálicos ............................................................ 52
1.3.1.2 Resinas quelantes ........................................................................................ 53
1.3.1.2.1 Resinas funcionalizadas com ácido iminodiacético (IDA).......................... 54
1.3.1.2.1.1 Chelex-100® ........................................................................................... 56
1.3.1.3 Aplicações .................................................................................................... 59
1.4 TÉCNICAS ANALÍTICAS APLICADAS À DETERMINAÇÃO DE METAIS ...... 73
1.4.1 Espectrometria de Absorção Atômica (AAS) ................................................... 76
1.4.1.1 Histórico ....................................................................................................... 77
1.4.1.2 Espectrometria de Absorção Atômica com Chama (F AAS) ........................ 80
1.4.1.3 Espectrometria de Absorção Atômica por Forno de Grafite (GF AAS) ......... 81
1.4.1.3.1 Histórico .................................................................................................... 81
1.4.1.3.2 Princípios................................................................................................... 82
1.4.1.3.3 O conceito STPF ....................................................................................... 83
1.4.1.3.4 Modificadores químicos ............................................................................. 85
1.4.1.3.5 Interferências ............................................................................................. 86
1.4.1.4 Espectrometria de Absorção Atômica com Fonte Contínua e Alta Resolução
(HR-CS AAS) ............................................................................................................ 87
1.4.1.4.1 Histórico .................................................................................................... 87
1.4.1.4.2 Instrumentação .......................................................................................... 88
1.4.1.4.2.1 Fonte ...................................................................................................... 89
1.4.1.4.2.2 Monocromador ....................................................................................... 91
1.4.1.4.2.3 Detector .................................................................................................. 92
1.4.1.4.2.4 Atomizadores ......................................................................................... 94
1.4.1.4.2.5 O software .............................................................................................. 94
1.4.1.4.3 Vantagens da técnica de HR-CS AAS....................................................... 94
1.4.1.4.4 Aplicações ................................................................................................. 95
2 JUSTIFICATIVA E OBJETIVO DO TRABALHO.................................................. 104
3 MATERIAIS E MÉTODOS................................................................................... 106
3.1 REAGENTES E SOLUÇÕES ........................................................................... 106
3.2 INSTRUMENTAÇÃO ....................................................................................... 107
3.3 PROCEDIMENTO EXPERIMENTAL ............................................................... 108
4 RESULTADOS E DISCUSSÃO ........................................................................... 110
4.1 ESCOLHA DO TIPO DE ATOMIZADOR .......................................................... 110
4.2 OTIMIZAÇÃO DAS TEMPERATURAS DE PIRÓLISE E ATOMIZAÇÃO ....... 115
4.2.1 Curvas de TP e TA para cobalto ................................................................... 115
4.2.2 Curvas de TP e TA para cobre ...................................................................... 116
4.2.3 Curvas de TP e TA para manganês .............................................................. 118
4.2.4 Curvas de TP e TA para níquel ..................................................................... 119
4.2.5 Curvas de TP e TA para chumbo .................................................................. 120
4.3 INFLUÊNCIA DA PRESENÇA DE NaCl NA PRÉ-CONCENTRAÇÃO ............. 122
4.4 DESCONTAMINAÇÃO DA SOLUÇÃO SALINA DE NaCl 3,5% (m/v) ............. 125
4.5 EFEITO DA QUANTIDADE DE RESINA CHELEX-100® ................................. 129
4.5.1 Efeito da massa de resina nos sinais de cobalto........................................... 130
4.5.2 Efeito da massa de resina nos sinais de cobre ............................................. 132
4.5.3 Efeito da massa de resina nos sinais de manganês ..................................... 134
4.5.4 Efeito da massa de resina nos sinais de níquel ............................................ 136
4.5.5 Efeito da massa de resina nos sinais de chumbo ......................................... 138
4.6 DESCONTAMINAÇÃO DA RESINA CHELEX-100® E O EFEITO NOS SINAIS
PARA Mn................................................................................................................. 140
4.7 EFEITO DO TEOR DE SALINIDADE ............................................................... 143
4.8 VERIFICAÇÃO DA ELIMINAÇÃO DA MATRIZ ATRAVÉS DOS ESPECTROS
TRIDIMENSIONAIS DO HR- CS AAS ..................................................................... 146
4.9 DETERMINAÇÃO QUALITATIVA DO CLORETO RESIDUAL ......................... 152
4.10 CARACTERÍSTICAS ANALÍTICAS ................................................................ 153
4.11 APLICAÇÃO A AMOSTRAS DE ÁGUA PRODUZIDA ................................... 157
4.12 ENSAIOS DE ADIÇÃO E RECUPERAÇÃO DE ANALITO ........................... 158
5 CONCLUSÕES ................................................................................................... 160
6 REFERÊNCIAS ................................................................................................... 162
29
1 INTRODUÇÃO E FUNDAMENTAÇÃO TEÓRICA
Atualmente a energia é essencial para a maior parte das atividades humanas.
A produção da energia hoje é feita a partir da exploração de diferentes recursos
naturais que provocam uma série de mudanças ambientais. A necessidade de
energia é uma realidade desde a Revolução Industrial, quando se iniciou o uso
intensivo de combustíveis fósseis, como carvão mineral e o petróleo. O uso do
petróleo aumentou em larga escala na indústria e o seu aumento explodiu após a
Segunda Guerra Mundial, quando o seu uso energético aumentou até chegar ao que
temos nos dias atuais. Além de grande importância na geração de energia, o
petróleo gera subprodutos que são matérias-primas para a manufatura de inúmeros
bens de consumo que têm um papel cada vez mais relevante na vida do ser humano
(GUEDES, 2010).
Atualmente, mais de 60% da matriz energética mundial é
referente à indústria do petróleo (somando-se óleo e gás natural). No Brasil, esse
número foi estimado em 54%. Esses números são ilustrados na Figura 1
(SCHIOZER, 2005).
Figura 1: Distribuição (em %) das matrizes energéticas em 2004 no Brasil e no mundo.
Fonte: SCHIOZER, 2005.
30
1.1 O PETRÓLEO
Apesar da existência do petróleo ter sido conhecida desde os tempos antigos,
foi somente no século XX que foi obtida a tecnologia para retirada de grandes
volumes deste combustível fóssil necessários para suprir as demandas de energia
devido à expansão da economia mundial (GABARDO, 2007 apud HUNT, 1995).
Etimologicamente a palavra “petróleo” origina-se do latim "petra" (pedra) e
"oleum" (óleo), ou seja, o "óleo que vem da pedra". O registro da participação do
petróleo na vida do homem remonta desde os tempos bíblicos: Nabucodonosor usou
o betume como material de liga na construção dos famosos Jardins Suspensos da
Babilônia, onde também os tijolos eram assentados com asfalto. O betume também
era largamente utilizado pelos fenícios na calefação de embarcações; os egípcios
utilizaram-no na pavimentação de estradas, para embalsamar os mortos, bem como
na construção das pirâmides. Já os gregos e romanos aplicaram-no para fins
bélicos. Já no Novo Mundo, o petróleo era conhecido dos índios pré-colombianos,
que o utilizavam na decoração e na impermeabilização de seus potes de cerâmica.
Incas, maias e outras civilizações antigas também estavam familiarizados com o
betume, dele se utilizando para diversos fins. Apenas no século XVIII o petróleo
passou a ser utilizado comercialmente, como, por exemplo, na indústria
farmacêutica e na iluminação pública. Os primeiros poços de petróleo foram
perfurados nos Estados Unidos, sendo o primeiro sucesso de exploração registrado
em 1859, por Drake (GOMES, 2009 apud MENDONÇA, 2004; THOMAS, 2004).
1.1.1 A Exploração de Petróleo
A geoquímica do petróleo é a aplicação dos princípios químicos para o estudo
da origem, migração, acumulação, e alteração do petróleo (óleo e gás) e o uso deste
conhecimento na exploração e produção de petróleo é imprescindível. Não há claras
evidências de quando os princípios geológicos e geoquímicos foram primeiramente
aplicados para a pesquisa de óleo. Desde o começo da história a descoberta de
exsudações naturais de óleo e gás tem sido registrada, e a presença de poços
perfurados rusticamente era comum nas áreas de tais exsudações, ou de poços
considerados surgentes (GABARDO, 2007; BEZERRA, 2004; GOMES, 2009).
31
A presença do petróleo foi observada com freqüência durante a produção de
sal: cerca de 600 anos a.C. e existe citação de que Confúcio mencionou a presença
de poços de óleo a centenas de metros de profundidade (GABARDO, 2007 apud
HUNT, 1995). Também em algumas regiões de extração de sal, o gás, proveniente
das exsudações, era queimado para evaporar a salmoura e produzir o sal. É
interessante mencionar que desde o ano de 1132 já existiam ferramentas de
perfuração chinesas que alcançavam profundidades de 1000 metros. No final do
século XVIII, o campo de óleo de Yenangyaung em Burma tinha mais de 500 poços
e produzia 40.000 toneladas de óleo anualmente. Em solo de Baku fluía óleo e gás o
que proporcionou o desenvolvimento da indústria do petróleo no Azerbaijão, e em
1870, a produção anual em Baku atingiu 28.000 toneladas. Nos EUA em 1859, o
coronel Edwin L. Drake inicia a indústria de óleo na América, com sua reconhecida
carreira perfurando próximo a Titusville na Pensilvânia. Em 1871 cerca de 90% da
produção mundial era de origem da Pensilvânia (GABARDO, 2007 apud HUNT,
1995).
No Brasil, a primeira concessão para extrair material betuminoso foi assinada
pelo Marquês de Olinda em 1858, através do Decreto n⁰ 2266, e concedida a José
Barros Pimentel. A aplicação desse material era para produção de querosene de
iluminação; essa primeira exploração ocorreu às margens do Rio Marau, na Bahia.
Posteriormente, a constatação de petróleo no recôncavo baiano viabilizou a
exploração de outras bacias sedimentares terrestres (GOMES, 2009 apud
CEPETRO, 2008).
Já a exploração propriamente dita do petróleo foi iniciada na localidade de
Lobato, no Estado da Bahia em 1939, quase um século após as perfurações terem
sido iniciadas nos EUA. A Figura 2 apresenta a manchete do jornal Estado da Bahia
em 21 de janeiro de 1939 registrando o início da produção brasileira de petróleo.
32
Figura 2: Notícia do jornal Estado da Bahia em 21 de janeiro de 1939, registrando o
início da exploração de petróleo no Brasil.
Fonte: GABARDO, 2007.
Estas explorações primárias de petróleo eram realizadas por exploracionistas
pioneiros com pouco ou nenhum conhecimento da geologia da área. Aos poucos, no
entanto, os princípios geológicos e geoquímicos foram evoluindo e o mais antigo
conceito é o da teoria anticlinal, que define que o óleo é mais facilmente trapeado
pelo simples fato do óleo ser menos denso que a água e, portanto ficar retido na
parte superior desta estrutura. Esse princípio foi substituído por mapeamento
através de processos geofísicos que melhor definiam também outras estruturas que
pudessem reter o petróleo. A descoberta dos grandes reservatórios de óleo
estratificado no leste do Texas fez geólogos e perfuradores pensarem que achar
óleo
requeria
um
conhecimento
detalhado
de
várias
ciências
da
terra:
sedimentologia, estratigrafia, paleontologia, geoquímica, mineralogia, petrologia,
geomorfologia, e geologia histórica (GABARDO, 2007 apud HUNT, 1995).
Com o fim das estruturas mais óbvias para serem exploradas, encontrar óleo
tornava-se cada vez mais difícil, e por isso ficava claro que era preciso entender
mais sobre a geoquímica do petróleo; nesta época começaram a ser formuladas
algumas teorias sobre suas prováveis fontes. Mas, apesar de todo o conhecimento
desenvolvido, muitas vezes a perfuração ainda encontra poço seco. O sucesso da
exploração de petróleo depende de certos fatores simultâneos: (1) a existência de
uma rocha geradora ativa (acúmulo da matéria orgânica), (2) reservatório
estruturado para reter o petróleo, (3) rocha capeadora ou selante, e (4) caminhos de
33
migração. A probabilidade de achar petróleo é o produto das probabilidades destes
fatores. Então, se um destes fatores é zero, o resultado será um poço seco,
independente de quão favoráveis sejam os outros três fatores (GABARDO, 2007).
Mais de 100 anos de investigações e pesquisas tem demonstrado que todas
as jazidas comerciais de petróleo conhecidas são originadas da decomposição da
matéria orgânica depositada em bacias sedimentares. As observações de campo de
geólogos no último século comprovam a idéia de que óleos são gerados em
folhelhos betuminosos e migram para arenitos. A teoria da relação do carbono foi o
primeiro conceito geoquímico que relacionava acumulações de óleo e gás ao
“metamorfismo”. Campos de óleo existem em áreas de baixa evolução térmica,
equivalente à maturidade do carvão (com menos de 60% de C fixados ou não
voláteis), enquanto que campos de gás ocorrem em mais alta maturidade (carbono
fixado entre 60 e 70%) (GABARDO, 2007 apud HUNT, 1995).
1.2 A ÁGUA PRODUZIDA
Os diferentes tipos de águas de subsuperfície são classificados por critérios
relacionados a alguns aspectos importantes das mesmas, como por exemplo,
indicações superficiais de suas composições químicas. (RODRIGUEZ, 1993).
É denominada água produzida toda a água gerada (carreada) junto com o
óleo, podendo ser constituída pela água de formação (também chamada de água
conata, sendo a água naturalmente presente na formação geológica do
reservatório de petróleo, que pode conter alta salinidade e presença de metais em
percentuais variados) e/ou pela água de injeção (aquela injetada no reservatório
em processos de recuperação secundária para aumento da produção) e/ou pela
água meteórica (que faz parte do ciclo hidrológico) (BEZERRA, 2004;
FIGUEIREDO, 2010 apud SILVA NETO et al., 2005). Pode estar presente na forma
livre, em fase diferente do óleo, ou em emulsão (BEZERRA, 2004 apud
FERNANDES JÚNIOR, 2002). Observa-se na Figura 3 alguns tipos de água na
exploração petrolífera offshore.
34
Figura 3: Esquema de alguns tipos de água na exploração petrolífera offshore.
Fonte: TEIXEIRA, 2007 apud SCHLUMBERGUER, 2000.
1.2.1 Origem
Na indústria do petróleo a geração de água é inevitável, ocorrendo em todas
as etapas do processo de produção: extração, transporte e refino do óleo.
(FIGUEIREDO, 2010 apud SILVA NETO et al., 2005). A água produzida é
considerada o rejeito de maior volume em todo processo de exploração e produção
do petróleo, configurando-se assim comum grande problema ambiental, operacional
e gerencial.
A origem básica da água produzida juntamente com o petróleo está
relacionada às condições ambientais existentes durante a gênese deste óleo.
Um
ambiente geológico marinho ou lacustre, em que tenha havido intensa deposição de
matéria orgânica, associada com posterior soterramento, e condições físicoquímicas apropriadas tende a reunir os condicionantes necessários para o
aparecimento do petróleo nas rochas matrizes. O petróleo gerado migra então para
rochas permeáveis adjacentes que,
trapeadas
estruturalmente
por rochas
impermeáveis, resultam em acumulações nas rochas reservatório. Durante milhares
de anos o petróleo se concentra, segregando-se da água, mas, mantendo muitas
vezes, contato com os aquíferos (FIGUEIREDO, 2010).
35
Ao longo da exploração de petróleo de jazidas em terra (onshore) ou no mar
(offshore), existe a geração concomitante do efluente aquoso, água produzida tem
sido a maior corrente de resíduos da indústria do petróleo (FIGUEIREDO, 2010 apud
GARCIA, 2006). Isto ocorre devido à geração de grandes volumes de água
associados à produção de petróleo. A quantidade deste efluente está relacionada
aos mecanismos natural ou artificial de produção e do estágio de vida do campo de
produção (FIGUEIREDO, 2010).
No mecanismo natural, a água é encontrada naturalmente na própria
formação geológica produtora, devido à existência de aquíferos subjacentes ao
petróleo, devido à água conata, residente nos poros das rochas-reservatório. Já no
mecanismo artificial, quando o poço está depletando, a água é injetada
artificialmente, para manter as condições de pressão na rocha reservatório, forçando
o petróleo a migrar. Este método conhecido por recuperação secundária de petróleo
(ou recuperação convencional) é um método utilizado para o aumento do fator de
recuperação de um campo, sendo, em grande parte dos casos, responsável pela
viabilidade econômica do seu projeto de desenvolvimento. (FIGUEIREDO, 2010).
O volume de água gerado em uma atividade offshore, geralmente é maior que
o de óleo, em torno de 2000 a 40000 m 3 dia-1, dependendo das dimensões do
reservatório, da área explorada e da capacidade da unidade exploradora
(SCHOLTEN; KARMAN; HUWER, 2000). Geralmente os campos de petróleo no
início da produção geram pequena quantidade de água que aumenta com o
decorrer do tempo, num processo de maturação, atingindo valores de 90% de
BSW (sedimentos de base e água), quando o campo se encontra no seu estágio
final de produção econômica (FIGUEIREDO, 2010 apud RAY; ENGELHARDT,
1992). No Brasil, em 2002, um volume anual estimado de 9,4 x 10 6 m3 de água de
produção foi descartado no mar por 7 plataformas fixadas na Bacia de Campos
(VEGUERIA et al., 2002).
A Figura 4 esquematiza a produção offshore de água produzida (ROCHA;
ROSA; BEZERRA, 2007).
36
Figura 4: Produção offshore com injeção de água.
Fonte: ROCHA; ROSA; BEZERRA, 2007.
1.2.2 Composição
A água produzida é conhecida por ser uma mistura complexa (BOESH;
RABALAIS, 1987).
Sua composição química é bastante variada, podendo ser influenciada pelas
características, profundidade e vida útil do campo produtor. Seus componentes são
oriundos do reservatório, da água injetada e de substâncias químicas usadas na
produção com a finalidade de evitar uma variedade de problemas nas operações
do campo (SOUSA, 2010; FIGUEIREDO, 2010 apud THOMAS et al., 2001;
GARCIA, 2006). Ela contém os mesmos sais e metais que a água do mar, embora
em razões e concentrações diferentes. Essas razões podem refletir a idade da
formação geológica (OGP, 2005; COLLINS, 1975).
As
águas
produzidas
apresentam
em
sua
constituição
diferentes
concentrações de cátions (Na+, K+, Ca2+, Mg2+, Ba2+, Sr2+, Fe2+, entre outros) e
ânions (cloreto, sulfato, carbonato, bicarbonato, etc.) responsáveis pelo potencial de
incrustação destas águas. Além destes íons, estas águas também contêm vários
elementos-traço, como cádmio, cobre, níquel, chumbo e zinco, bem como sulfeto e
37
N-amoniacal (OLIVEIRA; OLIVEIRA, 2000; FIGUEIREDO, 2010 apud CENPES,
2005).
A concentração da maioria dos metais está acima das concentrações
encontradas em água do mar de ambiente não contaminado. Por exemplo, cádmio,
cobre, níquel, chumbo e zinco podem estar presentes em concentrações mais de
1.000 vezes acima das encontradas na água do mar natural (ANDRADE, 2009
apud SWAN et al., 1994).
Já os radionuclídeos encontrados nas águas produzidas nos campos de
petróleo estão normalmente associados às ocorrências naturais de materiais
radioativos. A radioatividade dessas águas se deve a presença de traços dos íons
de
40K, 238U, 232Th, 226Ra
226Ra
e
228Ra.
Em presença dos ânions sulfato e carbonato, o
pode co-precipitar com os cátions Ca2+, Ba2+e Sr2+, formando incrustações
radioativas nas tubulações (OLIVEIRA; OLIVEIRA, 2000).
Sulfeto e N-amoniacal podem ser derivados em parte de atividade
microbiana nas linhas de produção. O mecanismo predominante de origem do
sulfeto nas águas de formação parece ser a atividade de bactérias redutoras de
sulfato (BRS). Embora a presença de amônia possa ser também de origem
bacteriana, a origem desta espécie nas águas produzidas pode também ser
dependente das condições geológicas da formação produtora (TIBBETTS et al.,
1992; SWAN; NEFF; YOUNG, 1994).
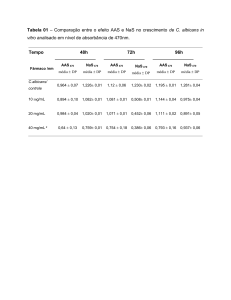
A Tabela 1 apresenta a concentração típica de diferentes metais-traço
dissolvidos nas águas produzidas nos campos de petróleo e gás do Mar do Norte,
enquanto que a Tabela 2 ilustra as concentrações médias, usualmente encontradas
em água produzida, de instalações produtoras de gás e de óleo, bem como suas
concentrações na água do mar. A Tabela 3 apresenta alguns parâmetros
determinados em amostras brasileiras de água produzida, coletadas pela
PETROBRAS, na Unidade Sergipe/Alagoas. E por fim, a Tabela 4 apresenta os
resultados médios para os principais ânions presentes em amostras de água
produzida e na água do mar.
38
Tabela 1: Teor de metais-traço presentes na água do mar e nas águas
produzidas no Mar do Norte.
Concentração de metais-traço (μg L-1)
Elemento
Água Produzida
Água do mar
Típica
Faixa
Ag
80
0 - 150
0,3
Cd
50
0 - 100
0,02
Cr
100
0 - 390
0,001
Cu
800
1 - 1500
0,2
Hg
3
0 - 10
0,001
Ni
900
0 - 1700
0,3
Pb
500
0 - 1500
0,03
Zn
1000
0 - 5000
0,6
Fonte: OLIVEIRA; OLIVEIRA, 2000.
39
Tabela 2: Concentrações médias de metais e metalóides em nível traço em água produzida.
Concentração nas plataformas de
Concentração nas plataformas de
Concentração na
produção de petróleo (μg L-1)
produção de gás (μg L-1)
água do mar (μg L-1)
Elemento-traço
Número de
Faixa
Média
Fe
-
-
-
-
As
0,25 - 34,2
7,6
9
-
Cd
0,03 - 25
0,6
8
Cr
0,18 - 5,3
2,2
Cu
0,25 - 9,5
Hg
dados
Faixa
Média
Número de
dados
Faixa
-
0,008 - 2,0
60
1
1-3
0,07 - 50
1,3
4
0,001 - 0,1
9
0,07 - 1600
419,5
4
0,1 - 0,55
2
8
0,14 - 0,6
0,4
3
0,03 - 0,35
0,04 - 0,13
0,3
8
1 - 89
23
12
0,00007 - 0,006
Ni
0,5 - 3,1
1,4
3
-
-
0
0,1 - 1
Pb
0,15 - 2,1
0,4
8
0,19 - 9
4,1
6
0,001 - 0,1
Zn
0,07 - 26,4
5,8
19
0,37 - 145
25,9
16
0,006 - 0,12
Fonte: OGP, 2005.
39
40
Tabela 3: Parâmetros determinados em amostras de água produzida
coletadas pela PETROBRAS, na Unidade Sergipe/Alagoas.
Faixa dos Resultados obtidos (mg L-1)
Parâmetro
Mínimo
Máximo
Salinidade
28.445
142.914
Densidade a 20/4*
1,020
1,125
pH
6,4
7,2
Alcalinidade total
72
638
Dureza total
5.240
50.336
Cloretos
17.240
86.614
Bicarbonatos
88
684
Sulfatos
5
227
Fe total
0,2
46,2
Al total
3,2
7,7
Cr total
< 0,01
0,1
Cu total
< 0,01
0,20
Mn total
0,6
20,5
Ba
10
868
Ca
1.318
17.808
Mg
439
1.440
Sr
25
846
Na
13.009
60.348
K
245
1.149
Cd
< 0,01
0,01
Pb
< 0,01
0,07
Ni
< 0,01
0,04
Zn
< 0,01
2,42
TOG
100
500
(*) Relação entre a massa específica do produto a 20°C e a massa específica da água a 4°C.
Fonte: GOMES, 2009 apud PETROBRAS 2009.
41
Tabela 4: Concentrações médias dos principais ânions inorgânicos presentes na
água do mar e na água produzida.
Faixa dos Resultados obtidos (mg L-1)
Ânion
Mundo
Água produzida
Oceano
Água do mar
do Mar do Norte
Atlântico
no mundo
Bicarbonato
771
615
365
28
Cloreto
60900
44600
45800
19000
Sulfato
325
814
481
900
Sulfeto
140
-
1,3
< 0,002
Nitrato
1
1
< 0,1
0,67
Fosfato
0
0
-
0,09
Fluoreto
-
-
2,15
1
Fonte: ANDRADE, 2009 apud E&P Forum, 1994; OGP 2005; GABARDO, 2007.
Os compostos orgânicos naturais presentes nas águas produzidas podem
ser divididos em quatro grupos principais: alifáticos (incluindo os naftênicos),
aromáticos, polares e ácidos graxos. A quantidade relativa e a distribuição de peso
molecular destes compostos variam de poço para poço. Os compostos alifáticos de
maior interesse são aqueles mais leves (< C5), pois são os mais solúveis em água e
contribuem para o total de carbono orgânico volátil (OLIVEIRA; OLIVEIRA, 2000).
Compostos aromáticos, tais como: benzeno, tolueno, xileno e naftalenos,
são relativamente solúveis na água, estando ainda presentes em pequenas
quantidades de hidrocarbonetos aromáticos polinucleares de alto peso molecular.
Os compostos aromáticos juntamente com os alifáticos, constituem os chamados
hidrocarbonetos da água produzida. Os compostos polares, como os fenóis, também
são relativamente solúveis na água. Todavia, como estes compostos estão
presentes em pequenas quantidades no petróleo, sua concentração na água
produzida é menor do que a dos compostos aromáticos (OLIVEIRA; OLIVEIRA,
2000). Na Tabela 5, apresenta-se o teor de diferentes compostos orgânicos
presentes nas águas produzidas no Mar do Norte.
42
Tabela 5: Teor de compostos orgânicos presentes nas águas produzidas no
Mar do Norte.
Campo de petróleo (mg L-1)
Campo de Gás (mg L-1)
Constituinte
Típica
Faixa
Típica
Faixa
Alifáticos (<C5)
1
0-6
1
0-6
Alifáticos (>C5)
5
0 - 30
10
0 - 60
Aromáticos (BTEX)
8
0 - 20
25
0 - 50
Naftalenos
1,5
0-4
1,5
0-4
Fenóis
5
1 - 11
5
0 - 22
Ácidos Graxos
300
30 - 800
-
-
Fonte: OLIVEIRA; OLIVEIRA, 2000.
Além dos compostos naturais presentes nas águas produzidas, uma grande
variedade de produtos químicos é adicionada durante o processo de produção.
Neste caso, estes produtos são geralmente chamados de aditivos e são
empregados para resolver ou prevenir problemas operacionais. Cada sistema de
produção é único na necessidade de utilização destes aditivos, gerando, desta
forma, efluentes com diferentes características físico-químicas.
Os principais aditivos adicionados durante o processo de produção de
petróleo
são:
inibidores
de
incrustação,
inibidores de
corrosão,
biocidas,
desemulsificantes, aditivos para o tratamento da água (coagulantes e floculantes),
inibidores de deposição de parafinas/asfaltenos e antiespumantes.
Os aditivos empregados durante o processamento do gás são, em sua maioria, os
inibidores de formação de hidratos, os redutores de umidade e os removedores de
H2S (OLIVEIRA; OLIVEIRA, 2000). Na Tabela 6, apresenta-se a concentração de
alguns produtos químicos presentes nas águas produzidas no Mar do Norte.
43
Tabela 6: Teor de diferentes aditivos presentes nas águas produzidas no Mar
do Norte.
Campo de petróleo (mg L-1)
Campo de Gás (mg L-1)
Constituinte
Típica
Faixa
Típica
Faixa
4
2 - 10
4
2 - 10
10
2 - 10
-
-
Desemulsificante
1
0-2
-
-
Polieletrólito
2
0 - 10
-
-
Metanol
-
-
2000
Glicol
-
-
1000
Inibidor de corrosão
Inibidor de
incrustação
1000 15000
500 - 2000
Fonte: OLIVEIRA; OLIVEIRA, 2000.
1.2.3 Destino final para a água produzida
A melhor opção para solucionar o problema da água produzida seria,
obviamente, procurar reduzir a sua produção. Todavia, isto é, em geral,
extremamente difícil. O fechamento dos poços de produção e os reparos nos
produtores de água são considerados soluções temporárias, que, ainda assim,
devem ser precedidas da análise pormenorizada do caso, sob pena de causar danos
permanentes ao reservatório.
Para reduzir o problema da água produzida, providências podem ser
tomadas, além de evitar-se a produção da água no poço, quais sejam: injetar a água
de volta no poço ou em poços de reinjeção; ou tratar a água para descarte no mar
ou para o uso na irrigação das plantações.
A injeção de água é um dos métodos mais utilizados para aumentar a
quantidade de óleo produzido, pois aumenta a pressão dos reservatórios de petróleo
e desloca o óleo para o poço produtor (SCHIOZER, 2005).
A Agência de Proteção Ambiental Norte-Americana (US EPA, do inglês
United States Environmental Protection Agency) também tem considerado a
44
reinjecão de água produzida, embora não exista a obrigatoriedade da implantação
do processo. Baseado na experiência do Mar do Norte, a reinjeção de água
produzida tem se mostrado uma alternativa atrativa. Dentre as razões que justificam
a reinjeção estão o crescente volume de água produzida e a conseqüente
necessidade de adaptação das plantas de tratamento a esses volumes, demandas
mais rigorosas dos órgãos reguladores e a dificuldade de enquadramento dos
contaminantes presentes nos limites da legislação. Os principais benefícios da
reinjeção de água produzida são: (i) a possibilidade de redução de volumes de água
tratada nas plataformas, (ii) a redução do volume de água do mar injetada e (iii) a
redução de problemas operacionais associados com incrustação e corrosão
(GARCIA, 1996). As Figuras 5 e 6 mostram, respectivamente, os perfis de produção
de óleo e água para um campo produtor típico no nordeste do Atlântico, e a
expectativa de injeção de água e produção de óleo e água para a Bacia de Campos
até 2015. Já Figura 7 esquematiza o caminho da água produzida e os destinos que
podem ser dados a ela pela indústria.
Figura 5: Perfis típicos de produção de óleo e água para um campo produtor no
nordeste do Atlântico.
Fonte: Adaptado de NATURE TECHNOLOGICAL SOLUTION, 200-.
45
Figura 6: Expectativa de injeção de água e produção de óleo e água na Bacia de
Campos.
Fonte: ROCHA; ROSA; BEZERRA, 2007 apud BEZERRA, 2002.
Figura 7: Possíveis destinos para a água produzida.
FONTE: NASCIMENTO, 2009.
1.2.4 Descarte, impactos e legislação ambiental
A água produzida pode ser descartada em corpos receptores ou ser utilizada
na injeção em poços de petróleo ou para a irrigação. Porém para todas essas
disposições, este efluente líquido deve ser adequadamente tratado. Para injeção
46
em poços de petróleo, a água deverá ter no máximo 5 mg/L em TOG (GOMES, 2009
apud PETROBRAS, 2009).
A Figura 8 apresenta o histórico e projeção da
produção e do descarte de água produzida na plataforma continental da Noruega. A
quantidade não descartada no mar foi destinada à re-injeção nos reservatórios
(NATURE TECHNOLOGICAL SOLUTION, 200- apud Departamento de Petróleo da
Noruega).
Figura 8: Histórico e projeção da produção e do descarte de água produzida na plataforma
continental da Noruega.
Fonte: Adaptado de NATURE TECHNOLOGICAL SOLUTION, 200-, apud Departamento de
Petróleo da Noruega.
Em 1993, a US EPA estabeleceu limites de concentração, em termos de
óleo e graxas livres, para o descarte de águas produzidas em ambiente offshore.
Atualmente estes limites são de 29 mg L-1 como média e de 42 mg L-1 como limite
máximo diário permitido. Em revisão, a Convenção de Paris para a prevenção de
poluição marinha por fontes baseadas em terra, nos oceanos Ártico e Atlântico NE
(PARCOM), reduziu o limite de teor de óleo e graxa (livre) médio mensal de 40 para
30 mg L-1. Todavia, no Mar do Norte o limite de teor de óleo e graxa (livre) continua
sendo de 40 mg L-1 como média mensal (OLIVEIRA; OLIVEIRA, 2000; TAVARES,
2003).
47
No Brasil, o Conselho Nacional do Meio Ambiente (CONAMA) é o órgão
consultivo deliberativo do SISNAMA, decisivo na formulação das normas relativas ao
complexo conjunto de atividades que formam o meio ambiente humano. Entre suas
competências principais, estão: estabelecer normas, critérios e padrões relativos ao
controle e à manutenção da qualidade do meio ambiente, com vistas ao uso racional
dos recursos ambientais; estabelecer normas e critérios para o licenciamento das
atividades efetivas ou potencialmente poluidoras/degradadoras ambientais; e decidir,
em última instância administrativa, em graus de recursos, sobre as infrações
ambientais (NASCIMENTO, 2009).
A Resolução CONAMA nº. 357, de março de 2005, dispõe sobre a
classificação dos corpos de água e diretrizes ambientais para o seu enquadramento,
bem como estabelece as condições e padrões de lançamento de efluentes
(CONAMA 357, 2005). Já a Resolução CONAMA nº. 393, de agosto de 2007, em
complemento à de nº 357/2005, dispõe sobre o descarte contínuo de água de
processo ou de produção em plataformas marítimas de petróleo e gás natural.
Porém, apesar de esta ser uma medida que mostra a importância do controle deste
tipo de efluente, atualmente esta resolução monitora apenas o teor de óleos e
graxas, que deverá obedecer à concentração média aritmética simples mensal de
até 29 mg L-1, com valor máximo diário de 42 mg L-1 (CONAMA 393, 2007).
Desse modo, ocorrendo a opção pelo descarte, após a consideração de
aspectos relevantes ao gerenciamento da água produzida, quais sejam, as
avaliações das propriedades dessa água, das características do poço e das
peculiaridades da área produtora, estabelece-se a necessidade do prévio
tratamento, com o fito de obedecer às condições, aos padrões e às exigências
dispostos nas Resoluções CONAMA nº. 357/2005 e nº. 393/2007 (NASCIMENTO,
2009).
1.2.5 Caracterização de águas produzidas em relação a metais e metalóides
A seguir, a Tabela 7 apresenta alguns trabalhos encontrados na literatura
onde diversos autores investigaram métodos analíticos para a determinação de
metais (como Ba, Cd, Co, Cr, Cu, Fe, Hg, Mn, Ni, Pb, V, Zn), metalóides (As, Se) e
fósforo em amostras de água produzida oriundas de diferentes locais. Nesta Tabela
48
são apresentados valores para os limites de detecção e/ou quantificação bem como
as técnicas analíticas empregadas para esse fim.
Tabela 7: Aplicações presentes na literatura para determinações de metais em
amostras de água produzida.
Analito(s)
Detecção
LOD(s) e/ou LOQ(s)
Referência
Cd, Cu, Ni, Pb
ICP OES
LODs = entre 0,03 µg L-1 (Cd)
e 2,1 µg L-1 (Pb)
ESCALEIRA et al.,
2008
Cr total
GF AAS
LOD = 0,45 µg L-1
LOQ = 1,5 µg L-1
OLIVEIRA;
SANTELLI, 2008
Co, Cr, Cu, Fe, Hg,
Mn, Ni, Pb, V Zn
SRTXRF
LODs = entre 20 ng L-1 (Ni) e
180 µg L-1 (Hg)
PIMENTEL et al.,
2008
Cd, Co, Cr, Mn
ICP OES
LOQs = entre 0,093 µg L-1
(Cd) e 1,2 µg L-1 (Cr)
BEZERRA et al.,
2007
As, Cd, Cu, Fe, Hg,
Mn, Ni, Pb, Zn
F AAS, GF AAS e
Voltametria
LODs = entre 0,05 µg L-1
(Hg) e 1 mg L-1 (Fe)
MANFRA et al.,
2007
Co, Cu, Fe, Mn, Ni,
Pb, Zn
F AAS
-
DÓREA et al., 2007
V
GF AAS
LOD = 1,9 µg L-1
LOQ = 6,3 µg L-1
OLIVEIRA;
MAGALHÃES, 2006
Pb
GF AAS
LOD = 1,5 µg L-1
LOQ = 5,0 µg L-1
OLIVEIRA;
SANTELLI, 2005
P orgânico
ICP-MS
LOD =0,20 µg L-1
ROCHA et al., 2004
As
GF AAS
LOD = 68 pg
SANT'ANA;
SANTELLI, 2002
Se
GF AAS
-
SANT'ANA et al.,
2002
Ba, Cr, Cu, Fe, Hg,
Ni, Pb
CV-AAS, F AAS,
GF AAS e ICP
OES
LODs = entre 0,003 µg L-1
(Cd) e 0,03 µg L-1 (Cr, Cu, Ni)
UTVIK, 1999
P orgânico
ICP-MS e ICP OES
0,5 µg L-1 (ICP-MS) e 7,9 µg
L-1 (ICP OES)
ROCHA et al., 1998
49
1.3 A IMPORTÂNCIA DO PREPARO DE AMOSTRAS PARA A DETERMINAÇÃO
DE TRAÇOS E ULTRATRAÇOS
Determinações acuradas de metais e ametais, especialmente em níveis traço,
são um dos trabalhos analíticos mais difíceis e complicados, uma vez que requerem
quesitos como versatilidade, especificidade, sensibilidade, reprodutibilidade e
acurácia nas mesmas. Embora o desenvolvimento da instrumentação eletrônica
tenha criado várias ferramentas de análise para a determinação de elementos-traço,
os métodos sofrem com o efeito de matriz, podendo acarretar em resultados
errôneos (GARG et al., 1999).
A determinação de elementos químicos em baixas concentrações é um desafio
freqüente para a Química Analítica. Apesar dos grandes progressos alcançados no
desenvolvimento de equipamentos analíticos altamente sensíveis, seletivos e com
limites de detecção cada vez menores, raras são as técnicas analíticas que aceitam
analisar uma amostra bruta, sem qualquer tratamento prévio. Uma matriz, a
depender de sua complexidade, pode danificar o instrumento utilizado para sua
análise e/ou inviabilizar a determinação do analito presente nesta amostra. Além
disso, a espécie de interesse pode estar presente em uma concentração muito
abaixo do limite de detecção da técnica empregada. Portanto, no desenvolvimento
de um método analítico para a determinação de analitos em amostras complexas e
em concentração abaixo do limite de detecção da técnica, as etapas de separação e
pré-concentração
tornam-se
imprescindíveis
(PALEOLOGOS;
GIOKAS;
KARAYANNIS, 2005; BEZERRA, 2006a; BEZERRA; FERREIRA, 2006b).
A determinação de elementos-traço em matrizes de alta complexidade – como
a água do mar e a água produzida, por exemplo – é um dos grandes desafios
enfrentados pela química analítica atual. No caso específico das amostras salinas, a
presença de sais dissolvidos pode causar sérias interferências, dificultando o
desenvolvimento de procedimentos com exatidão e precisão adequadas. Como
amostras de água em questão geralmente possuem elevada concentração de sais, o
uso direto das técnicas analíticas torna-se limitado, devido a alguns fatores,
principalmente interferências. Muitas vezes, para reduzir as interferências causadas
pela matriz, deve-se recorrer a métodos como: adição de padrão, padronização
interna ou o uso de modificadores químicos.
50
Entretanto, na maioria dos casos, principalmente tratando-se de amostras
salinas, uma etapa de separação da matriz é muitas vezes utilizada. Além disto,
muitos dos constituintes deste tipo de amostra se encontram em níveis inferiores ou
próximos ao limite de detecção, e então uma pré-concentração torna-se também
necessária. Daí o grande interesse dessas áreas para a Química Analítica e
Ambiental, particularmente pelas possibilidades de eliminação dos efeitos de matriz
e a utilização de uma técnica de aquisição menos onerosa, mas que inicialmente
não
apresentaria
limites
de
detecção
suficientemente
baixos
para
a
detecção/quantificação do analito. Por isso, diversos métodos de extração e préconcentração têm sido desenvolvidos, tais como a Deposição Eletroanalítica, a
Filtração por Membrana, a Troca Iônica, a Extração em Fase Sólida (SPE), a
Coprecipitação, a Extração Líquido-Líquido (LLE) e a Extração no Ponto Nuvem
(CPE), sendo alguns trabalhos desenvolvidos especialmente para análise de
amostras salinas (CHEN; DANADURAI; HUANG, 2001; GROTTI et al., 2002;
PALEOLOGOS; GIOKAS; KARAYANNIS, 2005; BEZERRA; FERREIRA, 2006b;
BEZERRA; CONCEIÇÃO; FERREIRA 2006c; AŞKUN et al., 2007; RAHMI et al.,
2007). Além destes, novos procedimentos têm surgido, como a Microextração em
Fase Líquida (LPME) e sua variação, a Microextração em Fase Líquida Suportada
em Fibra Oca (HF-LPME), Microextração Líquido-Líquido Dispersiva (DLLME),
Microextração em Gota Única (SDME) e sua variação, a HS-SDME; Extração por
Solvente Assistida por Membrana (MASE); Extração por Membrana com Interface
Sorvente (MESI); Extração por Líquido Suportado em Membrana (SLME) e Extração
Líquido-Líquido Suportada em Membrana Microporosa (MMLLE).
Dentre todos os procedimentos citados, a Extração em Fase Sólida tem se
consolidado junto ao conjunto de procedimentos de separação e pré-concentração
disponíveis na Química Analítica, sendo bastante empregada.
1.3.1 A extração em fase sólida
Na Extração em Fase Sólida, os solutos são extraídos de uma fase líquida
para uma fase sólida. A fase sólida em geral consiste de pequenas e porosas
partículas de um suporte sólido (geralmente sílica), ligada a uma fase orgânica ou
polímero orgânico, como poliestireno de ligações cruzadas. Na análise química é
mais comum empacotar o sólido extrator em um pequeno tubo e percolar a amostra
51
líquida através do tubo (FRITZ, 1999). Um aparato típico para SPE é apresentado na
Figura 9.
Figura 9: Aparato para a extração em fase
sólida.
Fonte: Adaptado de FRITZ, 1999.
Substâncias que tenham sido extraídas pelas partículas sólidas podem ser
eluídas com um solvente líquido apropriado. Usualmente, o volume de solvente
necessário para eluição completa dos analitos é muito menor do que o volume de
amostra original, de forma que a concentração dos analitos é então alcançada
(FRITZ, 1999).
A Extração em Fase Sólida possui diversas vantagens importantes,
principalmente quando comparada com a Extração Líquido-Líquido (FRITZ, 1999;
MALLA; ALVAREZ; BATISTONI, 2002; SKINNER; SALIN, 2003; VASSILEVA;
FURUTA, 2003; GONZALVEZ et al., 2010):
a) Manipulação mais rápida e fácil;
52
b) Uso de quantidades muito menores de solventes líquidos orgânicos /
dessorventes;
c) Requisitos menos rigorosos para separação;
d) Fatores de concentração mais altos – aumento da concentração do analito
que chega ao instrumento de detecção;
e) Menores riscos de contaminação;
f) Remoção de espécies concomitantes indesejáveis, em sistemas on line ou off
line;
g) Inserção dos analitos em uma matriz mais simples;
h) Facilmente automatizada;
i) Possibilidade de uso em sistema de circulação fechado;
j) Possibilidade de combinação com técnicas analíticas modernas, permitindo a
detecção simultânea e multielementar por Espectrometria de Massa com
Plasma Indutivamente Acoplado (ICP-MS) e por Espectrometria de Emissão
Ótica com Plasma Indutivamente Acoplado (ICP OES).
1.3.1.1 Pré-concentração de íons metálicos
Por muito tempo, a extração líquido-líquido foi o método mais popular para
pré-tratamento de amostras. Extração de metais de água do mar por extração
líquido-líquido de complexos metálicos com ditiocarbamato tem sido uma prática
analítica onipresente, mas intensamente laboriosa e sujeita a grande número de
dificuldades, necessitando da mistura da amostra com diversos reagentes
aumentando o risco de contaminação (PAULL; FOULKLES; JONES, 1994; FRITZ,
1999).
O uso da Extração em Fase Sólida é um modo atrativo de evitar muitas das
dificuldades associadas à extração líquido-líquido. Em alguns casos, solventes
orgânicos não são utilizados na SPE para metais. Existem várias possibilidades para
SPE de íons metálicos (FRITZ, 1999):
a) Troca iônica, incluindo a retenção de cátions ou ânions por troca iônica
simples, retenção de complexos metálicos iônicos ou resina de troca iônica, e
seletiva eluição dos íons metálicos através de reagentes complexantes
orgânicos ou inorgânicos.
53
b) Adição de reagentes para formação de complexos associados a íons ou
complexos organometálicos neutros, seguido por SPE dos complexos através
de um extrator sólido não-iônico.
c) Retenção dos íons metálicos por uso de uma resina quelante.
1.3.1.2 Resinas quelantes
A princípio, o modo ideal para isolar e pré-concentrar íons metálicos é
percolar a amostra através de uma pequena coluna ou membrana contendo uma
resina quelante. Os metais de interesse devem ser extraídos da solução pelos
grupos quelantes das partículas sólidas. Passar uma solução altamente ácida
através da resina para remover os quelatos metálicos da resina sólida deve resultar
em eluição rápida dos metais. Às vezes, de fato, a SPE com resinas quelantes é
eficaz. Mas o tamanho de partícula relativamente grande de polímeros quelantes e o
transporte de massa lento no interior das esferas do polímero frequentemente
resulta em procedimentos que no geral são ineficazes e lentos (FRITZ, 1999).
Existe um grande número de resinas quelantes para remoção de vários íons
metálicos de solução. Uma resina quelante ideal para SPE deve possuir as
seguintes propriedades: (a) alto grau de ligações cruzadas para boa estabilidade
física e partículas esféricas pequenas (possivelmente de aproximadamente 10 µm
de diâmetro), (b) poros com alta área superficial para uma cinética rápida, e com os
grupos quelantes na superfície ou próximos a ela para evitar impedimento estérico
na quelação do íon metálico (FRITZ, 1999).
A extração de íons metálicos usando resinas quelantes tem diversas
vantagens sobre outros métodos mais convencionais (PAULL; FOULKLES; JONES,
1994; GARG et al., 1999):
a) Determinação seletiva de metais será possível com uso de uma resina
quelante contendo um ligante que possua alta seletividade para o íon
metálico de interesse;
b) É ausente de dificuldade na separação das fases, que é decorrente da
solubilidade mútua entre as camadas de água e solvente orgânico;
54
c) O uso da resina quelante é um método econômico uma vez que utiliza uma
pequena quantidade de ligante e solvente extrator o que também aumenta a
sensibilidade do sistema;
d) A determinação de metais-traço em baixos níveis como ppb torna-se possível
pois o íon de interesse é enriquecido na fase sólida;
e) A concentração do íon metálico pode ser visualmente estimada a partir da
intensidade da coloração da fase sólida se o complexo metálico formado
possuir absorção na região do visível do espectro eletromagnético;
f) O uso de solventes orgânicos (que podem ser carcinogênicos) é evitado,
sendo a técnica considerada “ecologicamente correta” ("Green Chemistry");
g) Resinas quelantes retêm essencialmente a fração dissolvida lábil (disponível)
em solução. Como essa fração é a que melhor representa a quantidade de
metais disponível no momento para espécies aquáticas, como peixes, dando
informações importantes sobre o potencial toxicológico.
Dentre as resinas quelantes, pode-se citar as resinas funcionalizadas com
ácido iminodiacético (IDA, do inglês “iminodiacetic acid”), com 8-hidroxiquinolina,
com ácido hidroxâmico, as resinas de tioglicolato e materiais de fosfato-celulose. A
seguir, são apresentados alguns exemplos específicos para ilustrar as muitas
possibilidades do uso da SPE com resinas quelantes.
1.3.1.2.1 Resinas funcionalizadas com ácido iminodiacético (IDA)
Resinas quelantes contendo iminodiacetato – ou ácido iminodiacético (IDA) –
como grupo funcional são largamente utilizadas devido à sua forte capacidade de
adsorção de íons metálicos. A Figura 10 mostra o grupo funcional responsável pela
complexação.
Algumas
das
resinas
funcionalizadas
com
IDA
disponíveis
comercialmente são a Chelex-100® (com suporte de poli(estireno-divinilbenzeno)),
MetPac CC-1 (suporte de poli(estireno-divinilbenzeno) macroporoso com alto teor de
ligações cruzadas), Muromac A-1 (com suporte de poli(estireno-divinilbenzeno) e
alta ocorrência de ligações cruzadas), Prosep IDA (de vidro de porosidade
controlada), Toyopearl AF-Chelate-650M (com suporte de metacrilato macroporoso),
CHITOPEARL CI-03 (com suporte chitosan de ligações cruzadas altamente
55
macroporoso), Dowex A-1. (SAMUELSON, 1963; GAO et al., 2002; KATARINA et
al., 2008).
Figura 10: Grupo funcional quelante
das resinas funcionalizadas com IDA.
Como exemplo, a resina Dowex A-1 apresenta a seguinte sequência de
seletividade para íons metálicos: Pd2+ > Cu2+ >> Fe2+ > Ni2+ > Pb2+ > Mn2+ >> Ca2+ ≈
Mg2+ >> Na+ (SAMUELSON, 1963). De acordo com a Figura 11, pode-se verificar
que os quelatos são facilmente eluídos da resina após tratamento com ácido.
Figura 11: Aquisição de diferentes cátions divalentes pela resina
quelante Dowex A-1, em função do pH.
Fonte: Adaptado de SAMUELSON, 1963.
Juntamente com a 8-hidroxiquinolina, as resinas impregnadas com IDA têm
sido principalmente empregadas em estudos envolvendo água do mar. Infelizmente
a seletividade das resinas funcionalizadas com IDA é menos favorável a análise
56
desse tipo de amostra quando comparada à seletividade da 8-hidroxiquinolina (outro
agente quelante, que será discutido posteriormente) devido à separação incompleta
dos elementos alcalinos e alcalinos terrosos, e a remoção dos componentes da
matriz é essencial para o sucesso do método. (WARNKEN et al., 2000; WILLIE et
al., 2001; VASSILEVA; FURUTA, 2003; KATARINA et al., 2008).
1.3.1.2.1.1 Chelex-100®
A Chelex-100® foi originalmente investigada por Ryler e Taylor e desde então
tem sido bastante estudada e modificada, tanto para sistemas online e offline. Um
grande número de resinas similares a ela tem sido alvo de interesse de diversos
grupos de pesquisa, em geral resinas macroporosas de partículas grandes, como
por exemplo, a Lewatit TP 207 e a Chelamina (PAULL; FOULKLES; JONES, 1994).
A resina quelante Chelex-100® é um co-polímero de estireno-divinilbenzeno
imobilizado com grupos funcionais iminodiacetato que agem como grupos quelantes
na ligação com íons metálicos polivalentes. Em baixos valores de pH, tanto o
nitrogênio da imina quanto os grupos carboxílicos se encontram na forma protonada.
O nitrogênio protonado adquire carga positiva, podendo atrair ânions, enquanto que
os grupos carboxílicos mantêm-se neutros e não-reativos. À medida que ocorre um
aumento do pH, a sorção de ânions decresce e a de cátions cresce, até que em pH
acima de 12 a resina se torna unicamente um trocador catiônico (BioRad, 200-;
CEO; KAZEROUNI; RENGAN, 1993). A Figura 12 apresenta as formas
zwitteriônicas da Chelex-100® em função do pH.
Figura 12: Formas zwitteriônicas da Chelex-100® em função do pH.
Fonte: Bio-Rad, 200-.
57
Embora a capacidade de adsorção para metais da Chelex-100® seja grande,
suas partículas são um tanto grandes e o baixo teor de ligações cruzadas
poliméricas leva a dilatação e contração excessiva do leito da resina na coluna
quando ocorre uma variação de pH ou da composição iônica (GAO et al., 2002;
KATARINA et al., 2007).
Além disso, dificuldades com a retenção de sal associado à análise por ICPMS têm limitado seu uso (WARNKEN et al., 2000). Mas para reduzir o efeito dessas
interferências, os elementos da matriz adsorvidos na resina são usualmente
removidos através da passagem de uma solução tampão de acetato de amônio
através da resina quelante (RAHMI et al., 2007).
O fator de seletividade é a quantidade mensurada da afinidade que a resina
Chelex-100® apresenta para um cátion em particular, comparada com a afinidade
para seu cátion de referência (neste caso, Zn2+). A Tabela 8 apresenta uma série de
fatores de seletividade para alguns cátions divalentes.
58
Tabela 8: Seletividade para alguns cátions divalentes.
Elemento
Fator de Seletividade
Hg2+
1060
Cu2+
126
UO2+
5,70
Ni2+
4,40
Pb2+
3,88
Zn2+
1,00
Co2+
0,615
Cd2+
0,390
Fe2+
0,130
Mn2+
0,024
Ba2+
0,016
Ca2+
0,013
Sr2+
0,013
Mg2+
0,009
Na+
0,0000001
Fonte: Bio-Rad, 200-.
Os valores de seletividade dependem do meio: pH, força iônica e a presença
(ou não) de outras espécies formadoras de complexos. Assim por exemplo, o Hg2+
aparece no topo da série de seletividade na presença de íons nitrato, mas o extremo
oposto ocorre nas séries em que há a presença de cloreto no meio, devido à
formação de complexos. A ordem aproximada de seletividade para cátions em
soluções contendo cloreto e/ou nitrato é (Bio-Rad, 200-):
Cu2+ >> Pb2+ > Fe3+ > Al3+ > Cr3+ > Ni2+ > Zn2+ > Ag+ >
Co2+ > Cd2+ > Fe2+ > Mn2+ > Ba2+ > Ca2+ >>> Na+
A série de seletividade para cátions em meio contendo tampão de acetato de
sódio é (Bio-Rad, 200-):
59
Pd2+ > Cu2+ >> Fe2+ > Ni2+ > Pb2+ > Mn2+ >> Ca2+ = Mg2+ >>> Na+
A série de seletividade para cátions em soluções aquosas com pH = 4 é (BioRad, 200-).:
Hg2+ > Cu2+ > Pb2+ >>> Ni2+ > Zn2+ > Cd2+ > Co2+ > Fe2+
> Mn2+ > Ca2+ >>> Na+
Já para cátions em soluções aquosas com pH = 9 na presença de sulfato de
amônio de concentração igual a 1,5 mol L-1 é (Bio-Rad, [200?]).:
Co2+ > Ni2+ > Cd2+ > Cu2+ > Zn2+ Ca2+ >>> Na+
1.3.1.3 Aplicações
A seguir, a Tabela 9 apresenta algumas aplicações da SPE para a préconcentração de metais a partir de soluções salinas, em geral água do mar, com
salinidades similares a algumas amostras de água produzida.
60
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas.
Natureza
da
amostra
Água do
mar
Água do
mar
Água do
mar
Água do
mar
Analito(s)
Sistema analítico
Informações relevantes
Co
Complexo com BTAHQ e SPE
em discos de membrana de
C18. Detecção por
Espectrofotometria de UV-Vis
FE = 100;
Faixa linear = 0,01 - 0,38 µg mL-1;
Validação com GF AAS (método
de referência).
Cd(II), Co(II),
Cr(III), Ni(II),
Pb(II), Zn(II)
Complexo com PAN e SPE
com MNPs de Fe3O4
recobertas com ácido
decanóico. Detecção por FIICP OES
MNPs extraídas do meio através
da aplicação de campo magnético
externo;
Faixa linear: 1- 400 µg L-1 (todos);
FE = entre 116 (Co) e 150 (Zn);
Adição de padrão;
Metodologia aplicada também à
águas de poço, de torneira e
mineral.
U(VI), Th(IV)
e Zr (IV)
Complexo com Arsenazo(III) e
SPE em Amberlite XAD-2000
impregnada com oxima αbenzoína. Detecção por
Espectrofotometria de UV-Vis
Pb
Complexo com 8-HQS e SPE
em minicoluna empacotada
com florisil. Detecção por IDFI-ICP-MS.
LOD(s) e/ou LOQ(s)
(continua)
Referência
LOD = 3,1 ng mL-1
AMIN, 2010
LOQ = 9,7 ng mL-1
LODs: entre 0,2 µg L-1
(Zn) e 0,8 µg/L (Pb)
Calibração multivariada;
LODs:
Emprego da Adição de Padrão;
U = 0,50 µg L-1;
Validação por ICP OES;
Th = 0,54 µg L-1;
Metodologia aplicada também à
Zr = 0,48 µg L-1.
águas de poço e de torneira e
também à cerâmicas.
FARAJI, 2010
GHASEMI, 2010
HUANG, 2004
Validação com CRM: GBW 08607
LOD = 0,24 ng mL-1
60
61
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas.
Natureza
da
amostra
Água do
mar
Água do
mar
costeira
Água do
mar
Água do
mar
Analito(s)
(continuação)
Sistema analítico
Informações relevantes
LOD(s) e/ou LOQ(s)
Referência
Fe, Mn, Co,
Ni, Cu, Zn,
Cd, Pb
SPE em resina comercial
Toyopearl AF-Chelate-650M e
detecção por ID-HR-ICP-SFMS
Procedimento offline;
Métodologia combinando adição
de padrão (monoisotópicos Co e
Mn) e ID (outros elementos);
Validação: CRM NASS-5 (água do
mar), e com materiais de
referência do SAFe Program S1
(água superficial) e D2 (água de
1000 m de profundidade);
LODs: entre 0,0002 nmol
L-1 (Pb) e 0,026 nmol L-1
(Ni)
MILNE, 2010
Fe
SPE com nanopartículas de
TiO2 e ID-ICP-MS
Salinidade residual < 0,002%;
Validação: CRM CASS-2 (água do
mar) e co-precipitação com
Mg(OH)2 e ID-MS.
LOD = ~65 ng kg-1 e
~69mg kg-1
QUÉTEL, 2010
Cu(II), Ni(II) e
Cr (III)
SPE com Diaion SP-850
modificada com BHAPPDI e
detecção por F AAS
LODs:
Cu(II) = 7,8 µg L-1;
Ni(II) = 5,2 µg L-1;
Cr(III) = 6,2 µg L-1.
SHOKROLAHI,
2010
Cu
SPE com microcoluna
recheada com fibroína de seda
e detecção por SI-GF AAS
FE = 125 (todos)
FE = 27,3;
Faixa linear: 0,025 - 1,5 µg L -1;
Validação: CRM GBW 08608
(água de rio) e NASS-5 (água do
mar);
Metodologia aplicada também à
águas de caverna e de rio.
CHEN, 2009
LOD = 8,0 ng L-1
61
62
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas.
Natureza
da
amostra
Água do
mar
Água do
mar
superficial
Água do
mar
Analito(s)
Sistema analítico
Informações relevantes
Cu
SPE em minicoluna
empacotada com cotton após
formação do par iônico ternário
Cu-CAS-CTAB e detecção por
ICP OES
Eluição com 1-prOH em meio á
solução de HNO3;
Faixa linear: 0,5 – 100 µg L-1;
FE = 680;
FPC teórico = 500.
SPE com CM-PEHA
imobilizada em resina
quelante. Detecção por ICP
OES e F AAS
Validação com CRMs: EnviroMAT
EU-L-1
(água
residual)
e
EnviroMAT
ES-L-1
(água
subterrânea);
Faixa linear variando entre 0,001 –
1 µg mL-1 (Mn); 0,005 – 1 µg mL-1
(Cd, Co, Ni e V); 0,01 – 1 µg mL-1
(Fe e Pb); e 0,05 – 1 µg mL-1 (Cu,
Mo e Zn);
Metodologia aplicada também à
amostras de águas residuais
tratadas.
PC em sílica modificada com
grupamento aminoamidoxima
e detecção por F AAS
Faixa
de
concentração
de
aplicação do método: 9 - 91 µg L-1;
Metodologia aplicada também à
amostras de águas residuais
tratadas.
Cd, Co, Cu,
Fe, Mn, Mo,
Ni, Pb, V, Zn
(ao todo: 62
elementos)
Cu(II)
LOD(s) e/ou LOQ(s)
LOD = 0,04 µg L-1;
LODs: entre 0,003 µg L-1
(Mn) e 0,28 µg L-1 (Zn)
LOD = ~9 µg L-1;
(continuação)
Referência
FARAJI, 2009
KAGAYA, 2009
NGEONTAE, 2009
62
63
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Cu, Ni, Pb,
Zn
SPE com Ni-IIP e detecção por
ICP OES e ICP-MS
LODs (ICP OES): entre
0,03 µg L-1 (Zn) e 0,18 µg
L-1 (Pb);
IIP com partículas do complexo
LODs (ICP-MS): entre
ternário [Ni(II)-DEM-8-HQ];
0,0022 µg L-1 (Ni) e 0,009
IIP para reconhecimento de Ni,
µg L-1 (Zn);
mas aplicado para PC dos outros
analitos;
LOQs (ICP OES): entre
Validação com CRMs: SLEW-3 0,11 µg/L (Zn) e 0,60 µg
(água estuarina), e TM-23.3 e TM- L-1 (Pb);
24 (águas de lago).
LOQs (ICP-MS): entre
(continuação)
OTERO-ROMANÍ,
2009
0,0073 µg L-1 (Ni) e 0,031
µg L-1 (Zn);
Água do
mar
Água do
mar
sintética
Cu
Cu(II)
SPE com nanopartículas de
TiO2 coloidal e detecção por
GF AAS
Amostragem por suspensão;
Validação com CRM: GSBZ
50009-88:200924 (água);
Metodologia aplicável a água de
rio.
LOD = 0,29 µg L-1
QIAN, 2009
SPE com Cu(II)-IIP e detecção
por GTA-AAS
IIP formado pela copolimerização
do ácido salicílico + formaldeído +
complexo Cu(II)-PAR;
Faixa linear: 20 - 100 µg L-1;
Metodologia aplicada também para
águas de torneira e destilada.
LOD = 3,0 µg L-1
SINGH, 2009
63
64
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Água do
mar
Água do
mar
Co, Cd, Cr,
Mn, Ni, Zn
Mo
Cr total
SPE em minicoluna de silica
gel funcionalizada com DPTH
e detecção por ICP-MS.
Determinação simultânea dos
analitos;
Procedimento on line;
FE = entre 2,3 (Ni) e 32,9 (Zn);
Faixa linear: do LOQ até ao menos
60 µg L-1 (todos os elementos);
Validação com CRMs: SLRS-4
(água de rio), SLEW-3 (água
estuarina), NASS-5 (água do mar)
e TMDA-54.4;
Metodologia aplicada também à
amostras de água de rio.
SPE em I-8-HQ em sílica e
detecção por ID-ICP-SF-MS e
ID-ICP-MC-MS
Procedimento on line;
Validação com CRM: NASS-5
(água do mar);
1a aplicação do método de curva
de ID para quantificação de metais
traço reportada na literatura.
SPE em I-DPC em sílica e
detecção por ID-ICP-SF-MS
(continuação)
LODs: entre 0,006 µg L-1
(Co) e 0,530 µg L-1 (Cr)
TRUJILLO, 2009
LOQs: entre 0,019 µg L-1
(Co) e 1,770 µg L-1 (Cr)
-
Redução do Cr a Cr(III) com
NH2OH.HCl;
Procedimento on line;
Validação com CRMs: CASS-4
LOD proposto: 0,05 ng g-1
(água do mar) e NASS-5 (água do
mar);
Aplicação nos candidatos a CRM
CASS-5 e NASS-6.
YANG;
STURGEON ,
2009 (a)
YANG, 2009 (b)
64
65
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Água do
mar
Água do
mar
Água do
mar
costeira
Fe
SPE em resina NTA Superflow
e detecção por ID-ICP-MC-MS.
Fator de pré-concentração = 100
Validação com materiais de
referência do SAFe Program S1
(água superficial) e D2 (água de
1000 m de profundidade);
LOD = ~0,05 nmol L-1
(continuação)
JONG, 2008
Zn, Cd
SPE em sílica gel modificada
com 2,4,6 trimorfolil-1,3,5triazina. Detecção por F AAS
Faixa linear:
Cd =1 - 50 ng mL-1;
LODs:
Zn =0,5 - 20 ng mL-1;
Zn = 0,34 ng mL-1;
Método aplicado também em
Cd = 0,23 ng mL-1.
folhas de macieira (Ni) e urina
(Co).
MADRAKIAN,
2008
Al, Mn, Fe,
Co, Ni, Cu,
Zn, Cd, Pb
SPE em resina comercial
Nobias Chelate-PA1
modificada com grupo
funcional dos ácidos
etilenodiaminotriacético e
iminodiacético. Detecção por
ICP-MS.
Mn e Fe: ICP-MS em "DRC mode";
outros: "standard";
Validação com CRMs: NASS-5
(água do mar) e CASS-4 (água do
mar), e com materiais de
referência do SAFe Program S1
(água superficial) e D2 (água de
1000 m de profundidade);
LODs (sem PC): entre
0,29 ng kg-1 (Cd) e 15 ng
kg-1 (Zn)
SOHRIN, 2008
SPE em resina Chelex-100® e
detecção por GF AAS.
Especiação de V;
Eluição com NH4OH (V(V)) e
HClO4 (V(IV))
Faixa linear: até 10 nmol L-1;
Validação com CRM: CASS-4
(água do mar).
LODs (sem PC): ~0,05
nmol -1L
WANG, 2008
V(IV) e V(V)
65
66
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Cd, Cu, Ni,
Pb, Zn
Águas
salinas
Cd(II), Cu(II),
Cr(III), Pb(II),
Ni(II), Zn(II)
Água do
mar
Água do
mar
Água do
mar
(continuação)
Comparação entre 3 procedimen
tos de PC: SPE, extração por
Complexo com HEDC e SPE
solvente e co-precipitação;
com as resinas Amberlite XAD4 e Dowex Optipote V-493.
FPC para a SPE = 25;
Detecção por GF AAS
Validação com CRM: BCR-403
(água do mar).
-
KOMJAROVA,
2006
Seletividade semelhantes para
todos os analito, exceto Cr(III) por
sua valência.
-
WOODBERRY,
2005
LOD = 0,3 ng mL-1
ERSÖZ, 2004
SPE em Amberlite IRC 748 e
detecção por ICP-SF-MS.
MIP: [poly(EGDMA-MAH-Ni(II)];
Faixa linear: 0,3 - 25 ng mL-1;
FE = 72,66;
Extração seletiva mesmo na
presença de íons de raio iônico
semelhante.
Ni
SPE com colunas
empacotadas com MIP e
detecção por F AAS
Pb
Complexo com 8-HQS e SPE
em minicoluna empacotada
com florisil. Detecção por IDFI-ICP-MS.
Validação com CRM: GBW 08607
LOD = 0,24 ng mL-1
HUANG, 2004
Complexo com APDC e SPE
com resina Chromosorb-102.
Detecção por F AAS
Validação com CRM: GBW 07309
(sedimento);
Para água do mar, resultados
comparados com SNOEYNG;
JENKIS, 1980;
Método aplicado também para
água potável e sedimento.
LODs = entre 0,10 µg L-1
(Cd) e 11 µg L-1 (Fe)
SARAÇOĞLU,
2004
Bi, Cd, Co,
Cu, Fe, Ni,
Pb
66
67
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
(continuação)
Fe
Separação da matriz com
disco quelante e ID-ICP-CCTMS
Validação com CRMs: JAC-0031
(água de rio), SLEW-3 (água
estuarina), CASS-3 (água do mar)
e NASS-5 (água do mar).
LOD = 10 pg g-1
TAKAKU, 2004
Água do
mar
Bi, Pb, Ni
SPE com sílica modificada
com 3-aminopropiltrietoxisilano
e detecção por GF AAS
Uso de seringa como suporte de
preenchimento;
Adiçao de padrão.
LOD = 0,5 µg L-1 (todos)
TOKMAN, 2003
Água do
mar
Cd
SPE com sílica funcionalizada
com DPTH e detecção por ICP
OES
FPC = 86;
Método aplicado também a águas
residuais.
LOD = 1,1 µg L-1
CAMEL, 2003
apud ZOUGAGH,
2002
Água do
mar
Cd
SPE com sílica funcionalizada
com TS e detecção por ICP
OES
FPC = 62;
Método aplicado também a águas
residuais.
LOD = 4,3 µg L-1
CAMEL, 2003
apud ZOUGAGH,
2002
Água do
mar
Fe
SPE com sílica funcionalizada
com 8-HQ e detecção por
Espectrofotometria
LOD = 0,016 nmol L-1
CAMEL, 2003
apud WEEKS;
BRULAND, 2002
Cu, Cd
Complexo com APDC e SPE
com sílica-C18. Detecção por
GF AAS.
Fator de PC = 25 - 100
LOD = 6,5 - 1,26 µg L *
CAMEL, 2003
apud LIU;
HUANG, 1993
Cu, Cd, Co
Complexo com 1,10fenantrolina e SPE com sílicaC18. Detecção por F AAS.
FPC = 22 - 32;
Método aplicado também a
amostras
geológicas
e
de
mexilhão.
LOD = 0,3 - 6,0 µg L-1 *
CAMEL, 2003
apud ALI et al.,
1999
Água do
mar
CRMs de
água do
mar
CRMs de
água do
mar
-
-1
67
68
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
CRMs de
água do
mar
Cd
Complexo com PAR ou
PADMAP e SPE com sílicaC18. Detecção por GF AAS.
Água do
mar
Cr(III), Cr(VI),
Cr total
Complexo com DDTC e SPE
com sílica-C18. Detecção por F
AAS.
Água do
mar
(continuação)
LOD = 1,7 - 4 ng L-1 *
CAMEL, 2003
apud SU; HUANG,
1998
FPC = 90-500;
Método aplicado também a
amostras de efluentes industriais.
LOD = 20 ng L-1
CAMEL, 2003
apud RAO et al.,
1998
Cr(VI), Cr
total
Complexo com DDTC e SPE
com sílica-C18. Detecção por
GF AAS.
FPC = 12;
Método aplicado também a
amostras de água de rio, folhas de
tomateiro, mexilhões e CRM de
aço de baixo teor em carbono.
LOD = 1,6-1,8 ng L-1 *
CAMEL, 2003
apud SPERLING
et al., 1992
Água do
mar
Cu
SPE com sílica-C18 recoberta
com TAN. Detecção por GF
AAS.
FPC = 33
LOD = 5 ng L-1
CAMEL, 2003
apud QUEIROZ et
al., 2002
CRMs de
água do
mar
Fe(II), Fe(III)
SPE com sílica-C18 recoberta
com FZ. Detecção por
Espectrofotometria.
FPC = 6 - 60
LOD = 0,1 - 0,3 nmol L-1 *
CAMEL, 2003
apud BLEIN;
TRÉGUER, 1995
Cu
Complexo com APDC e SPE
em reatores PTFE. Detecção
por F AAS.
FPC = 340;
Método aplicado também a
amostras de água de rio e de
torneira.
LOD = 50 ng L-1
CAMEL, 2003
apud
ANTHEMIDIS et
al., 2001
Cr(VI)
Complexo com APDC e SPE
em reatores PTFE. Detecção
por F AAS.
FPC = 80;
Método aplicado também a
amostras de água de rio e de
torneira e efluentes industriais.
LOD = 800 ng L-1
CAMEL, 2003
apud
ANTHEMIDIS et
al., 2002
Águas
costeiras
Águas
costeiras
FPC = 25 - 50
68
69
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Pb
Complexo com APDC e SPE
em reatores PTFE. Detecção
por F AAS.
FPC = 330;
Método aplicado também a
amostras de água de rio e de
torneira,
sedimento
marinho;
tecidos de peixe e de mexilhão.
Cr(VI)
Complexo com APDC e SPE
em reator entrelaçado de
PTFE (PTFE (KR)). Detecção
por GF AAS.
FPC = 19;
Método aplicado também
amostras de água potável.
CRM de
água do
mar
Cr(IV)
Complexo com APDC e SPE
em reator entrelaçado de
PTFE (PTFE (KR)). Detecção
por GF AAS.
CRM de
água do
mar
Cr(IV)
Complexo com APDC e SPE
em esferas de PTFE.
Detecção por GF AAS.
CRMs de
água do
mar
Cu
Águas
estuarinas
Cu, Cd, Ni,
Zn, Mn
SPE em resina Toyopearl AFChelate-650M e detecção por
ICP-MS
Água do
mar
sintética
Cu, Cd, Pb,
Zn
SPE com trocador catiônico e
detecção por F AAS.
Águas
costeiras
Água do
mar
(continuação)
LOD = 800 ng L-1
CAMEL, 2003
apud
ZACHARIADIS et
al., 2002
-1
LOD = 4,2 ng L
CAMEL, 2003
apud NIELSEN;
HANSEN, 1998
FPC = 16,3;
Método aplicado também a CRM
de água natural.
LOD = 16 ng L-1
CAMEL, 2003
apud SOM-AUM
et al., 1998
FPC = 30,1;
Método aplicado também a CRM
de água natural.
LOD = 8,8 ng L-1
CAMEL, 2003
apud SOM-AUM et
al., 1998
LOD = 60 - 600 ng L-1 *
CAMEL, 2003
apud YEBRA et al.,
2001
LOD = 1,4 - 86 ng L-1 *
CAMEL, 2003
apud BECK et al.,
2002
LOD = 30 - 200 ng L-1*
CAMEL, 2003
apud FANG et al.,
1984
a
SPE em resina XAD-4
recoberta com PAN e detecção FPC = 29,1 - 296,1;
por F AAS.
-
FPC = 50 - 105
Método aplicado também a CRM
de água natural.
69
70
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
CRM de
água do
mar
Água do
mar
Água do
mar
Água do
mar
(continuação)
Fe, Ni, Cu,
Zn, Mo, Cd,
Pb, V, Mn,
Co
SPE em coluna empacotada
com resina comercial
Toyopearl AF-Chelate-650M e
detecção por FI-ICP-MS
Procedimento online;
Validação com CRMs: CASS-3
(água do mar) e NASS-5 (água do
mar), mas aplicado apenas para
otolitos de peixe.
LODs (otólitos) = entre
0,1 ng L-1 (Co) e 12 ng L-1
(Zn)
WILLIE, 2001
Mn, Ni, Cu,
Cd, Pb
SPE com resina comercial
Toyopearl AF-Chelate-650M e
detecção por ICP-MS
Procedimento online;
Uso de apenas 1 mL de amostra;
Validação com CRMs: CASS-4
(água do mar) e NASS-4 (água do
mar)
LODs = entre 0,06 pg mL1
(Cd) e 1,1 pg mL-1 (Mn)
WARNKEN, 2000
U(VI)
Complexo com 8-HQ e SPE
em cartuchos de C8. Detecção
por Polarografia de Pulso
Diferencial
Comparação entre diferentes tipos
de cartuchos adsorventes;
Adição de EDTA durante a SPE;
Eluição com CHCl3;
FPC >100;
Adição de padrão.
-
DOJOZAN, 1998
Fe, Co, Ni,
Cu, Zn, Cd
Complexo com HEDC e SPE
em colunas preenchidas com
C18 suportado poliestireno.
Detecção por HR-ICP-SF-MS
Paralelo com
Solvente.
LOD = entre 0,02 ng L-1
(Co) e 0,36 ng L-1 (Zn)
WELLS, 1998
a
Extração
por
70
71
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Água do
mar
Água do
mar
Mn, Co, Ni,
Cu, Zn, Cd,
Pb
Mn, Co, Cu,
Cd, Pb
Hg(II) e
CH3Hg(I)
(continuação)
SPE com I-8-HQ em tubo de
silicone e detecção por FI-ICPMS
Imobilização da 8-HQ na parede
interna do tubo de silicone;
Procedimento on line;
Validação com CRMs: CASS-3
(água do mar) e NASS-4 (água do
mar).
Metodologia empregada a baixa
pressão, evitando problemas de
"back pressure".
LOD = entre 0,003 ng L-1
(Co e Pb) e 0,054 ng L-1
(Ni)
WILLIE, 1998
SPE em resina comercial Met
Pac CC-1 e detecção por FIICP-MS
Procedimento online;
Estudo da matriz por ICP OES e
da viabilidade do tempo de PC por
F AAS;
Validação com CRMs: SLRS-2
(água de rio) e NASS-2 (água do
mar);
Aplicável também a águas de rio.
LOD = entre 17 ng L-1
(Cd) e 56 ng L-1 (Cu)
NICKSON, 1997
Complexo com DDC, APDC ou
DZ e SPE em sílica C18.
Detecção por CV-AAS
Comparativo
entre
3
complexantes: DDC, APDC e DZ;
LODs:
Faixa linear:
DDC = 16 ng L-1;
DDC e APDC = acima de 40
APDC = 18 ng L-1;
µg/L;
DZ = 67 ng L-1.
DZ = acima de 200 µg/L;
Adição de padrão;
GARCIA, 1994
71
72
Tabela 9: Aplicações da extração em fase sólida na pré-concentração de metais em amostras salinas
Água do
mar
Fe, Mn, Co,
Ni, Cu, Zn,
Cd, Pb
Dois procedimentos de SPE:
(1) Met Pac CC-1 (comercial);
e (2) I-8-HQ em sílica.
Detecção por ICP-MS.
Determinação simultânea dos
analitos;
Procedimento on line;
Validação com CRMs: CASS-2
(água do mar) e NASS-3 (água do
mar);
Água do
mar (água
oceânica
superficial)
Cd, Cu, Fe,
Mn, Ni, Pb,
Zn
Complexo com DOM e SPE
em C18. Detecção por F AAS
DOM natural.
LODs:
Met Pac CC-1: entre
1,6 ng L-1 (Pb) e 55
ng L-1 (Ni)
I-8HQ: entre 0,3
(Cd) e 47 ng L-1 (Fe)
LODs: entre 1 pmol kg-1
(Pb) e 126 pmol kg-1 (Zn)
(conclusão)
McLAREN, 1993
DONAT, 1986
72
73
1.4 TÉCNICAS ANALÍTICAS APLICADAS À DETERMINAÇÃO DE METAIS
As instrumentações analíticas utilizadas na caracterização química de
amostras ambientais são bastante variadas. A técnica ideal para determinação de
elementos químicos em matrizes biológicas e ambientais deve ser capaz de tanto
de explorar todos os elementos presentes na matriz como de abranger uma ampla
faixa de concentrações, do macro ao micro (SROGI, 2008). Com a evolução da
tecnologia analítica e conseqüente conhecimento da presença destes elementos
nestes baixos níveis, o termo “traço” foi criado para descrevê-los (BROWN;
MILTON, 2005).
Existem muitas motivações para o desenvolvimento de técnicas analíticas
capazes de realizar detecção e quantificação de espécies em níveis de traço. Como
exemplo, existem muitas áreas da ciência e da indústria em que a presença de
certos elementos mesmo em quantidades extremamente baixas podem causar
impactos muito significantes à saúde humana, à eficiência dos processos industriais
e também ao meio ambiente (BROWN; MILTON, 2005). Atualmente, isso
automatimaticamente leva à necessidade do cumprimento dos limites (cada vez
mais baixos) impostos pelas legislações, cada vez mais rígidas.
Apesar de as técnicas espectroanalíticas possuírem reconhecida aplicação
na determinação de traços de metais, quando a amostra em questão possui uma
elevada concentração de sais, como no caso de amostras de águas salinas, o uso
destas técnicas torna-se limitado, devido a alguns fatores, principalmente
interferências espectrais e não espectrais (MELO, 2003).
A escolha da técnica apropriada para a determinação de elementos traços
requer conhecimento das capacidades e limitações das diferentes técnicas
disponíveis, a ser considerado (MELO, 2003; CEOTTO, 2009):
Sensibilidade e limite de detecção;
Precisão e exatidão analítica;
Faixa de concentração;
Tempo;
Custo;
Grau de automação;
74
Habilidade necessária do operador;
Interferências analíticas e sua capacidade de controle;
Superação das contaminações.
As técnicas espectroanalíticas divergem em alguns desses parâmetros, o que
pode ser decisivo para a escolha daquela que irá se adequar melhor ao método que
se pretende utilizar. No entanto, um desses parâmetros parece ser fator comum de
preocupação em todas as técnicas estudadas quando a amostra possui uma matriz
complexa: são as interferências analíticas. A maioria dos métodos instrumentais de
análise não fornece sensibilidade satisfatória ou não estão livres de interferências
(que podem ser oriundas da presença de concomitantes na amostra) para
determinar diretamente elementos-traços em água de mar em níveis em torno de pg
L-1 ou ng L-1. Neste caso, faz-se necessário o uso de métodos para a préconcentração/eliminação de interferências da matriz (MELO, 2003).
As técnicas analíticas que podem ser utilizadas par determinação de metaistraço são: Potenciometria (com emprego de eletrodos íon-seletivo – ISE),
Voltametria de Redissolução (em geral utilizando técnicas polarográficas),
Fluorescência de Raios-X (XRF) e Análise por Ativação de Nêutrons (NAA), dentre
outras. Porém, as técnicas mais utilizadas para determinação de metais-traço em
águas salinas são as técnicas espectrométricas, que abrangem a Espectrometria de
Absorção Atômica com Chama (F AAS), a Espectrometria de Absorção Atômica com
Forno de Grafite (GF AAS) - também chamada de Espectrometria de Absorção
Atômica Eletrotérmica -, a Espectrometria de Emissão Óptica com Fonte de Plasma
Indutivamente Acoplado (ICP OES), e a Espectrometria de Massa com Fonte de
Plasma Indutivamente Acoplado (ICP-MS).
A Figura 13 ilustra, em forma de diagrama, os limites comuns em análise
quantitativa. A Tabela 10 traz as principais características de algumas das técnicas
de Espectrometria Atômica para a análise de amostras líquidas, enquanto que
Figuras 14 apresenta as faixas de determinação de traços.
75
Figura 13: Demarcações aproximadas em análise quantitativa comumente
usados.
Fonte: Adaptado de BROWN; MILTON, 2005.
Tabela
10:
Principais
características
de
algumas
das
técnicas
Espectrometria Atômica.
Característica
ICP-MS
ICP OES
AAS
Capacidade multi-elementar
+
+
-
Elementos-traço
++
+
++
Elementos-ultratraço
++
-
+
Limites de detecção
pg mL-1 – fg mL-1
ng mL-1
pg mL-1
Quantidade analito na amostra
ng – fg
µg – ng
ng – pg
++
-
-
109
108
109
Análise isotópica
(Análise por Diluição Isotópica)
Faixa dinâmica
Fonte: Adaptado de BECKER, 2005.
de
76
Figura 14: Faixa analítica para determinação de traços de algumas técnicas espectrométricas.
Fonte: adaptado de BECKER, 2005.
1.4.1 Espectrometria de Absorção Atômica (AAS)
Dentre as técnicas de Espectrometria Atômica, a mais popular é a
Espectrometria de Absorção Atômica (AAS), introduzida por Alan Walsh em 1955. A
AAS se tornou uma técnica bem estabelecida por sua capacidade de promover
determinações precisas, acuradas e bastante sensíveis de elementos em níveis de
traço e de ultratraço (BECKER, 2005; SROGI, 2008).
A Espectrometria de Absorção Atômica fundamenta-se na passagem de
radiação eletromagnética de um dado comprimento de onda, através de um vapor
atômico contendo átomos livres no estado fundamental. Tais átomos absorvem uma
fração desta radiação incidente, atingindo um ou mais estados excitados de maior
energia (OLIVEIRA, 2004 apud WELZ, 1985; EWING, 1972; SKOOG et al., 2002;
EWING, 1990).
A AAS, que por muitos anos foi a mais utilizada na determinação de metaistraço em amostras líquidas, pode ser realizada usando principalmente a atomização
77
por chama (F AAS) – com limites de detecção na faixa de baixo mg/L – e a
atomização por forno de grafite – na faixa de µg/L ou abaixo. A desvantagem da
AAS é a ausência da capacidade multielementar. Recentemente, a AAS de Alta
Resolução com Fonte Contínua (HR-CS AAS) foi introduzida no mercado analítico. A
vantagem desta nova técnica, usando uma fonte de radiação contínua e um detector
de dispositivo de carga acoplada (CCD), é que pode ser aplicado para
determinações multielementares (especificamente para a F AAS, funcionando como
um ICP OES sequencial) em matrizes mais complexas (BECKER, 2005). Detalhes
sobre esta técnica serão abordados mais adiante.
1.4.1.1 Histórico
A espectrometria de absorção atômica (AAS) foi proposta como técnica
analítica para determinações elementares em trabalhos independentes publicados
por Alan Walsh e Alkemade e Milatz em 1955. Entretanto, Walsh geralmente é
reconhecido como o “pai” da técnica, devido ao seu incansável esforço durante o
período de aproximadamente 1952 a 1962, não apenas para que sua idéia fosse
aceita como também para superar o preconceito (WELZ et al., 2005; LEPRI, 2009).
Em 1952, Alan Walsh começou a demonstrar interesse pela espectrometria
de absorção atômica como o resultado da interação de duas experiências que ele
vivenciou: uma delas trabalhando com análise espectroquímica de metais no
período de 1939-1946, e outra com espectroscopia molecular no período de 19461952. A interação entre estas duas experiências ocorreu quando o mesmo começou
a se perguntar: Por que espectros moleculares são usualmente obtidos em absorção
enquanto que espectros atômicos em emissão? A resposta a esta pergunta
evidenciou que não existiam boas razões para negligenciar o espectro de absorção
atômica; pelo contrário, este parece oferecer muito mais vantagens sobre o espectro
de emissão atômica (WALSH, 1955; WELZ et al., 2005; LEPRI, 2005).
Existia o atrativo de que a absorção é, ao menos para vapores atômicos
produzidos termicamente, virtualmente independente da temperatura do vapor
atômico e do potencial de excitação. Em adição a este fato, a técnica de
espectrometria
de
absorção
atômica
oferece
a
possibilidade
de
superar
interferências de excitação, que eram naquele tempo descritas por muitos como as
responsáveis por algumas interferências interelementares experimentadas em
78
espectroscopia de emissão quando se utilizava uma descarga elétrica como fonte de
radiação. A técnica de espectrometria de absorção atômica poderia ainda superar
problemas causados pela auto-absorção e auto-reversão, que tornavam difícil o uso
das linhas mais sensíveis em espectroscopia de emissão (WELZ et al., 2005; LEPRI,
2005).
Durante o desenvolvimento da técnica de AAS, Alan Walsh concluiu que para
medir os espectros de absorção utilizando uma fonte contínua de radiação uma
resolução espectral de cerca de 2 pm seria necessária, pois do contrário a grande
quantidade de radiação espúria que chegava ao detector causava uma acentuada
perda de sensibilidade e linearidade na curva de calibração. Entretanto, esta
resolução estava muito além das apresentadas pelos melhores espectrômetros que
ele dispunha em seu laboratório, e o mesmo propôs então o uso de fontes de linha
(LS) específicas para cada elemento com o perfil de emissão o mais estreito
possível. Desta forma, a função do monocromador era simplesmente a de separar a
linha analítica das outras linhas emitidas pela fonte, sem precisar possuir alta
resolução. Este conceito deu início à espectrometria de absorção atômica com
fontes de linha (LS AAS) (WELZ et al., 2005; LEPRI, 2009; SANTOS, 2009a). Assim,
fontes de emissão de linhas, especialmente lâmpadas de catodo oco (HCL) foram
desenvolvidas e são, até hoje, utilizadas em instrumentos comerciais. A técnica de
AAS convencional com fonte de linha (LS) desenvolveu-se a partir dos princípios de
Walsh, e pode ser considerada hoje uma técnica bem estabelecida e consolidada
(WELZ et al., 2005; BORGES, 2009).
O desenvolvimento e difusão dos instrumentos de LS AAS e o sucesso obtido
na utilização da técnica estão centrados em algumas vantagens características, que
incluem (WELZ; SPERLING, 1999; WELZ et al., 2005; BORGES, 2009):
Desenho relativamente simples e barato, permitindo a utilização de
monocromadores de média resolução e sistemas de detecção simples;
Alta seletividade e especificidade como conseqüência do uso de fontes de
emissão de linhas específicas para cada elemento e do princípio da
modulação,
Redução em interferências espectrais causadas por sobreposição de linhas
analíticas (em especial se comparado à emissão atômica);
79
Tolerância relativamente alta da chama e de atomizadores eletrotérmicos
frente a constituintes da matriz.
Embora estas qualidades caracterizem a robustez, seletividade e simplicidade
da LS AAS, algumas limitações estão associadas à técnica, incluindo (WELZ;
SPERLING, 1999; WELZ et al., 2005; BORGES, 2009):
Determinação de um elemento por vez, requerendo portanto uma lâmpada
para elemento;
Atenuação da radiação medida sobre intervalos espectrais estreitos
(correspondentes à largura da linha emitida pela fonte), restringindo a
disponibilidade de informação acerca do ambiente espectral;
Absorção total e fundo são medidos seqüencialmente, o que compromete a
avaliação do sinal para fundo que muda rapidamente com o tempo e requer
sistemas de correção de fundo capazes de detectar e eliminar interferências,
como a correção com lâmpada de deutério e correção por efeito Zeeman, que
acrescentam complexidade e custo elevado aos espectrômetros de AA.
Embora a correção de fundo por efeito Zeeman tenha atingido elevado nível
de desempenho, seu funcionamento não é ideal em todos os casos, e algumas
limitações práticas estão associadas a todos os sistemas de correção de fundo em
LS AAS (WELZ; SPERLING, 1999; BORGES, 2009).
Com o desenvolvimento da espectrometria de emissão óptica com fonte de
plasma indutivamente acoplado (ICP OES) e da espectrometria de massa com fonte
de plasma indutivamente acoplado (ICP-MS), surgiram questionamentos quanto ao
futuro da absorção atômica. Em 1989, Gary Hieftje se posicionou da seguinte forma
(HIEFTJE, 1989):
“...para que a AAS permaneça viável, em face à forte competição de
técnicas alternativas (ICP OES; ICP-MS), claramente torna-se
necessário uma renovação na instrumentação ou nos conceitos...”
“Se esta tendência continuar, eu não me surpreenderia ao ver a
remoção dos instrumentos comerciais de AAS do mercado por volta
do ano 2000.”
80
A Figura 15 mostra a projeção feita por ele para a AAS por volta dos anos
2000. Segundo ela as publicações utilizando esta técnica chegaria a zero, ou seja, a
técnica entraria em completo desuso.
Figura 15: Projeção feita por Hieftje para a AAS por volta dos
anos 2000.
Fonte: HIEFTJE, 1989.
1.4.1.2 Espectrometria de Absorção Atômica por Chama (F AAS)
A Espectrometria de Absorção Atômica com Chama trabalha através da
introdução da amostra em uma chama, onde seus compostos são dissociados em
seus átomos constituites. A radiação eletromagnética é direcionada para chama e é
parcialmente absorvida de forma característica pelos atomos presentes. A F AAS é
relativamente barata, de simples operação e pouco suscetível a interferências.
Entretanto, alguns elementos refratários não são possíveis de serem determinados
com boa sensibilidade, uma vez que a temperatura da chama não é alta o suficiente
para levar à atomização completa. As análises só podem ser procedidas em caso de
amostras liquidas e requerem considerável volume das mesmas; é uma técnica
relativamente lenta, e melhor empregada quando apenas um ou poucos elementos
precisam ser determinados. Quando um grande número de elementos é requerido,
81
outras técnicas podem ser substancialmente mais rápidas (BROWN; MILTON,
2005).
1.4.1.3 Espectrometria de Absorção Atômica com Forno de Grafite (GF AAS)
1.4.1.3.1 Histórico
O conceito de atomização eletrotérmica foi introduzido por L’vov em 1959,
mas tornou-se mais conhecido apenas a partir de uma publicação de 1961. Neste
trabalho, a amostra era depositada sobre a superfície de um eletrodo móvel de
grafite e, em seguida, introduzida em um tubo de grafite revestido com uma folha de
tântalo, o qual era aquecido eletricamente. Este sistema possibilitava a atomização
dos constituintes da amostra numa única etapa, fornecendo uma nuvem atômica
mais concentrada e, dessa maneira, uma melhor sensibilidade era alcançada, com
menor consumo da amostra (L’VOV, 1961).
Desde então o método de atomização eletrotérmico em forno de grafite teve
um acentuado desenvolvimento, objetivando sempre maior sensibilidade e redução
das interferências (WELZ; SPERLING, 1999; OLIVEIRA, 2004).
Um
atomizador
eletrotérmico
com
formato
conveniente
e
viável
comercialmente, proposto por Massmann (1968) permitiu selecionar condições
otimizadas nas determinações analíticas de diversos elementos. Nesse modelo de
atomizador, Massman utilizou um pequeno cilindro de grafite oco, posicionado de
forma que o feixe de radiação passasse ao longo do seu eixo longitudinal, e então,
fosse aquecido pela passagem de alta corrente elétrica e baixa voltagem
(MASSMANN, 1968).
Atualmente, os fornos possuem câmaras de refrigeração a água e de
atmosfera inerte. O forno de Massman era menos isotérmico do que aquele
originalmente proposto por L’vov. Assim, os limites de detecção encontrados por
Massman eram 10 vezes piores do que aqueles obtidos por L’vov. Isto tornava o
forno de Massman pouco atraente para a realização de medições analíticas (WELZ;
SPERLING, 1999; OLIVEIRA, 2004).
Na tentativa de tornar o tubo de grafite mais isotérmico durante a
atomização, L’vov propôs a inserção de uma plataforma de grafite no interior do
forno de Masssman. Nesta configuração, a amostra, introduzida sobre a plataforma,
82
é aquecida independentemente por irradiação a partir do aquecimento do gás inerte
pelas paredes do tubo. Dessa forma, a nuvem atômica é formada numa atmosfera
mais quente do que a superfície da plataforma, minimizando interferências na fase
vapor (WELZ, 1985).
1.4.1.3.2 Princípios
Na determinação de um elemento por GF AAS, a célula de absorção, um
tubo de grafite, tem como função converter os elementos de interesse presentes na
amostra em átomos livres, capazes de absorver radiação de freqüência específica
emitida pela fonte espectral, sendo a absorção proporcional à concentração dos
átomos livres, presentes no caminho ótico (WELZ; SPERLING, 1999; SANTOS,
2009a).
A técnica de GF AAS oferece limites de detecção de 2-3 ordens de grandeza
melhores que a espectrometria de absorção atômica com chama (F AAS). Esses
melhores limites de detecção devem-se ao maior tempo de permanência do analito
no atomizador e maior percentagem de atomização do analito presente na amostra
introduzida, em que virtualmente, 100% para GF AAS, enquanto que para F AAS
apenas 5% da solução aspirada chega à chama (WELZ; SPERLING, 1999;
DESSUY, 2007).
Uma quantidade definida da solução amostra, geralmente 5-50 μL, é
introduzida diretamente no forno de grafite, onde a temperatura vai sendo
aumentada
gradualmente
para
remoção
do
solvente
e
da
maioria
dos
concomitantes antes da atomização. A alíquota introduzida dentro do tubo de grafite
é atomizada em um tempo muito curto (tipicamente 1 s) e um sinal transiente é
estabelecido, cuja área (absorbância integrada) é proporcional à massa do analito
presente na alíquota inserida no tubo (WELZ; SPERLING, 1999; SANTOS, 2009a).
Assim, a otimização deste parâmetro se constitui em procedimento fundamental
para a obtenção de um programa de temperatura adequado.
Em GF AAS um programa de temperatura é usado para volatilizar os
componentes da amostra de uma forma seletiva, separando e/ou minimizando os
possíveis interferentes do analito. Para isso é necessário elaborar um programa de
aquecimento adequado para o atomizador, que deve contemplar as seguintes
83
etapas (WELZ; SPERLING, 1999; OLIVEIRA, 2004; DESSUY 2007; SANTOS,
2009a):
Secagem, para a evaporação do solvente e eliminação de constituintes
voláteis;
Pirólise, para eliminação da matriz da amostra;
Atomização, para a vaporização do analito na forma de átomos (etapa em
que ocorre a quantificação);
Limpeza do tubo de grafite, responsável pela eliminação de todo e qualquer
resíduo remanescente da amostra no tudo de grafite (efeito de memória).
Serve para a vaporização dos constituintes menos voláteis e remoção de
algum resíduo condensado nas partes frias do tubo antes do início de um
novo ciclo de medida.
A fase mais crítica do programa de temperatura é a pirólise, na qual devem
ser eliminados (química ou fisicamente) todos os componentes da amostra que
possam causar interferências de qualquer natureza. Aparentemente, este processo
torna-se mais eficiente quanto maior for a temperatura aplicada, porém, a aplicação
de temperaturas muito elevadas durante a etapa de pirólise pode
provocar a
volatilização do elemento de interesse, diminuindo a sensibilidade da determinação.
Assim, a otimização deste parâmetro se constitui em procedimento
fundamental para a obtenção de um programa de temperatura adequado (WELZ;
SPERLING, 1999; OLIVEIRA, 2004 apud WELZ, 1988). Para uma determinação
confiável em GF AAS é então essencial que o analito esteja presente em todas as
amostras na mesma combinação química, e que tenha estabilidade térmica mais
alta que os outros constituintes da amostra. A fim de se conseguir reprodutibilidade,
as temperaturas e os tempos de secagem, de pirólise e de atomização devem ser
determinados, experimentalmente, para cada elemento a ser determinado (WELZ;
SPERLING, 1999; OLIVEIRA, 2004).
1.4.1.3.3 O conceito STPF
Todos os progressos instrumentais introduzidos após a proposta do forno de
Massmann melhoraram sensivelmente as condições de atomização e a aceitação do
84
GF AAS. A consolidação dessas alterações, que garantiam um ambiente mais
isotérmico ao atomizador, veio com a proposta de Walter Slavin, que propôs as
condições STPF (“Stabilized Temperature Platform Furnace” - Forno com Plataforma
e Temperatura Estabilizada) que é um conjunto de condições que devem ser usadas
ao mesmo tempo, para garantir determinações livres de interferência no forno de
grafite (SLAVIN; MANNING; CARNRICK, 1981). As condições STPF traduziram, na
prática, as idéias de L´vov quanto a isotermicidade do atomizador (Tabela 11).
Tabela 11: Requisitos instrumentais e operacionais necessários para atender
as condições STPF e suas consequências.
Condições STPF
Consequëncia
Tubo de grafite com plataforma de
L'vov
Ambiente temporariamente isotérmico
Sinas de absorvância registrados em
área
Minimizar as variações cinéticas do
processos de atomização
Atomizador construído de grafite
pirolítico
Redução de perdas por difisão através da
parede do atomizador
Aquecimento transversal do tubo de
grafite
Redução das interferências químicas e
espectrais
Correção da radiação de fundo por
Efeito Zeeman
Redução das interferências espectrais
Uso de modificador químico
Evitar perdas do analito durante a etapa de
pirólise e auxiliar na redução de interferências
Interrupção do fluxo de gás durante a
etapa de atomização
Aumento do tempo de residência da nuvem
atômica na zona de observação
Alta velocidade de aquecimento na
etapa de atomização
Sinais estreitos e bem definidos
Eletrônica adequada para permitir a
integração do sinal transiente
Permitir registros dos sinais em tempo real
Fonte: SLAVIN; MANNING; CARNRICK, 1981; OLIVEIRA, 2004.
85
1.4.1.3.4 Modificadores químicos
O uso de modificadores tornou-se parte essencial da GF AAS com a
introdução do conceito STPF. O conceito de modificador químico (inicialmente
modificação da matriz) foi introduzido por Ediger em 1973 (DESSUY, 2007). São
definidos de acordo com as recomendações da IUPAC da seguinte forma: “Com a
finalidade de influenciar os processos que ocorrem no atomizador, reagentes
chamados modificadores químicos podem ser adicionados, ajudando a reter o
analito a temperaturas mais altas durante a pirólise, com a finalidade de remover
concomitantes indesejáveis ou melhorar a atomização” (SANTOS, 2009a).
O modificador químico é um reagente que é adicionado em excesso à
solução a ser medida no forno de grafite para converter o analito a uma forma
menos volátil (de tal modo que maiores temperaturas de pirólise possam ser
utilizadas) e/ou aumentar a volatilidade de componentes presentes na matriz. Ambas
ações servem para realizar uma separação mais efetiva do analito e de seus
concomitantes durante o pré-tratamento térmico (WELZ; SPERLING, 1999;
DESSUY, 2007). A princípio, todo e qualquer composto químico pode atuar como
modificador químico.
Schlemmer e Welz listaram alguns critérios para o uso de modificadores em
GF AAS (DESSUY, 2007 apud SCHLEMMER; WELZ, 1986):
O analito deve ser estabilizado nas mais altas temperaturas de pirólise
possível;
Aplicável ao maior número de elementos possível;
Disponível em alta pureza;
Não deve conter um elemento em altas concentrações que possa vir a ser
determinado em nível traço;
Não deve diminuir o tempo de vida do forno de grafite;
Não deve produzir sinal de fundo excessivo em torno do comprimento de
onda do analito.
86
1.4.1.3.5 Interferências
Embora essa seja uma técnica bastante confiável, ela pode sofrer
interferências causadas pelos concomitantes na amostras. Essas interferências
podem ser classificadas em (WELZ; SPERLING, 1999; SANTOS, 2009 apud
SLAVIN, 1982):
Interferências Espectrais - ocorrem quando a linha analítica, emitida pela
fonte, é absorvida por outra espécie que não o analito; ou quando uma
radiação,
que
não
aquela
emitida
pela
fonte
primária,
alcança
o
monocromador e não pode ser compensada. Exemplos de interferências são:
a ocorrência da sobreposição de linhas atômicas, o espalhamento por
partículas e a absorção molecular. Para minimizar esses problemas, utiliza-se
um programa adequado de temperaturas e um corretor de fundo, que pode
ser corretor continuo (lâmpada de deutério – D2) ou corretor de fundo
baseado no efeito Zeeman. Em todos os sistemas convencionais de correção
de fundo são realizadas duas medidas: a absorbância total (atômica e fundo)
e a absorbância de fundo. Dessa forma, alternando-se, rapidamente, a
medida da absorbância total e a do fundo, por diferença, é possível
determinar a absorbância correspondente aos átomos do analito.
Interferências Não-Espectrais – ocorrem quando há alteração no número de
átomos capazes de absorver. Suas causas são: composição, muitas vezes,
desconhecida da matriz; recombinação de átomos. Essas interferências
podem ser contornadas, desde que se use grafite recoberto piroliticamente,
plataforma
de
L’vov,
juntamente
com
modificadores
químicos,
preferencialmente em tubo aquecido transversalmente e adição padrão. Vale
ressaltar, no entanto, que as recomendações STPF, normalmente, são
suficientes para evitar esse tipo de interferência.
Pelo exposto, pode-se concluir que, no final da década de 80 a técnica de
GF AAS já era bem estabelecida e apresentava vantagens, em relação a outros
métodos disponíveis, como: pouca interferência, fácil operação, medidas rápidas e
baixo custo de operação.
87
1.4.1.4
Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua (HR-CS AAS)
1.4.1.4.1 Histórico
Os experimentos de Bunsen e Kirchhoff sobre o princípio da “reversão de
linhas” na segunda metade do século XIX foram conduzidos utilizando uma fonte
contínua
de
radiação.
Outros
pesquisadores,
como
Lockyer,
utilizaram
equipamentos semelhantes, o que se justifica pelo fato que fontes contínuas de
radiação serem as únicas fontes confiáveis disponíveis e por adequarem-se ao
propósito de detectar e medir a absorção da radiação, que caracterizava-se pelo
aparecimento de linhas negras no espectro contínuo projetado em um anteparo
(WELZ et al., 2005a; BORGES, 2009; LEPRI, 2009).
Apesar da consolidação da técnica de LS AAS, a pesquisa envolvendo a
utilização de fontes de emissão de radiação contínua em AAS continuou se
desenvolvendo. Em 1974, Keliher e Wohlers utilizaram pela primeira vez um
espectrômetro de alta resolução para AAS com fonte contínua (WELZ et al., 2005a;
BORGES, 2009).
Sistemas semelhantes foram estudados e desenvolvidos, e particularmente
as investigações efetuadas pelo grupo de Harnly contribuíram significativamente
para o desenvolvimento da técnica de CS AAS. A grande revolução para o
desenvolvimento da CS AAS ocorreu, entretanto, na segunda metade da década de
1990, com os trabalhos realizados pelo grupo de Becker- Ross, que identificou os
pontos fracos dos instrumentos utilizados pelos outros grupos de pesquisa: a baixa
intensidade de emissão no UV distante e a alta instabilidade apresentada pelos
arcos de xenônio convencionais, utilizados como fonte de radiação, que resultavam
em pobres limites de detecção, além das desvantagens da modulação de
comprimento de onda com placas de quartzo oscilantes (WELZ et al., 2005a;
BORGES, 2009; LEPRI, 2009).
Sendo assim, ao invés de tentar adaptar os componentes já existentes, eles
determinaram os requisitos para CS AAS, e então especificaram e desenvolveram o
instrumento atendendo a estes requisitos. O grupo começou com o projeto da fonte
contínua de radiação, passando pelo espectrômetro com monocromador duplo de
88
alta resolução e chegando finalmente ao detector com arranjo de dispositivo de
carga acoplada (CCD) (WELZ et al., 2005a; BORGES, 2009; LEPRI, 2009)
1.4.1.4.2 Instrumentação
Em 1996, Becker-Ross e seu grupo (HEITMANN et al., 1996) descreveram o
primeiro instrumento de HR-CS AAS com as configurações semelhantes às dos
equipamentos atuais. O aparelho foi adaptado tendo como base um modelo
comercial de um espectrômetro convencional de LS AAS, que teve o compartimento
de lâmpadas, monocromador e detector totalmente removidos e substituídos pelos
componentes do HR-CS AAS. A representação esquemática dos principais
componentes está mostrada na Figura 16.
Figura 16: Representação esquemática de um espectrômetro de absorção atômica de alta
resolução com fonte contínua. No esquema, têm-se: (1) lâmpada de arco curto de Xe; (2) espelhos
elipsoidais focalizadores; (3-4) atomizador (chama ou forno de grafite); (5) entrada do
monocromador; (6) espelhos parabolóides; (7) prisma; (8) fenda intermediária ajustável; (9) rede
echelle e (10) detector CCD.
Fonte: WELZ et al., 2005a.
89
1.4.1.4.2.1 Fonte
O primeiro componente característico do HR-CS AAS é a fonte de radiação.
Em princípio, diversas fontes de radiação poderiam ser utilizadas no HR-CS AAS,
mas o parâmetro mais crítico consiste na intensidade de emissão na região do UV
distante, até 190 nm. Assim, uma lâmpada de arco curto de Xenônio foi
especialmente desenvolvida para fornecer elevada potência radiante especialmente
na região do UV, e abrange a faixa de comprimentos de onda entre 190 e 900 nm. A
distância entre os eletrodos é tipicamente menor que 1 mm, e a pressão de Xe no
interior da lâmpada é de aproximadamente 17 bar, quando fria. Durante sua
operação, com um poder nominal de 300 W (tipicamente 20 V e 15 A), a pressão
interna da lâmpada aumenta por um fator de 3 a 4 (50 bar), e um hot-spot é gerado,
ou seja, um ponto de plasma com um diâmetro menor que 0,2 mm e temperatura de
aproximadamente 10.000 K gerado próximo à superfície do catodo. Devido ao
pequeno diâmetro do ponto de emissão, o feixe formado sobre a superfície do
eletrodo é instável em relação ao seu posicionamento. Para corrigir seu
posicionamento, há um sistema de estabilização ativa do feixe em relação à entrada
do monocromador, onde um pequeno espelho elipsoidal controlado por um
dispositivo piezoelétrico move-se para garantir que o feixe de radiação esteja
incidindo efetivamente no centro do atomizador. Com estas características, a
intensidade de emissão excede a de uma lâmpada de cátodo oco em 1 a 3 ordens
de grandeza, o que contribui para a obtenção de elevada razão sinal/ruído (S/N)
(WELZ et al., 2003; WELZ et al., 2005a; WELZ et al., 2005b; BORGES, 2005;
BORGES, 2009; LEPRI, 2009; SANTOS, 2009a; WELZ et al., 2010a).
A Figura 17 mostra os dois possíveis modos de operação da lâmpada de
arco curto de xenônio enquanto que a Figura 18 ilustra uma lâmpada de arco curto
de xenônio isolada e dentro de seu compartimento no equipamento de HR-CS AAS.
90
Figura 17: Foto de uma lâmpada de arco curto de xenônio operando em (A)
modo difuso e em (B) modo hot-spot.
Fonte: WELZ et al., 2005a.
Figura 18: Lâmpada de arco curto de xenônio (A) isolada e com detalhe nos
eletrodos e (B) dentro de seu compartimento no equipamento de HR-CS AAS.
Fonte: WELZ et al., 2005a.
91
1.4.1.4.2.2 Monocromador
Um monocromador de alta resolução denominado DEMON (Double-Echelle
MONochromator) constitui o segundo diferencial da técnica de HR-CS AAS. O
DEMON é constituído basicamente por um monocromador de prisma e um
monocromador com rede de difração Echelle, ambos dispostos em arranjo do tipo
Littrow. O prisma tem a função primordial de efetuar a pré-dispersão da radiação
emitida, selecionando a parte do espectro de interesse, que então passa por uma
fenda intermediária ajustável, e é direcionada à rede Echelle, que fornece a alta
resolução do intervalo espectral selecionado (melhor que 2 pm por pixel em 200
nm), onde é finamente dispersa (WELZ et al., 2003; WELZ et al., 2005a; WELZ et
al., 2005b; BORGES, 2005; BORGES 2009; WELZ et al., 2010a)
O caminho da radiação se faz da seguinte forma (identificações na Figura
16): um espelho parabólico fora do eixo (representado pelo nº 6, de comprimento
focal de 302 mm) forma um feixe luminoso paralelo e reflete o feixe de radiação para
um prisma (representado pelo nº 7). O prisma está montado em um arranjo Littrow e
é utilizado como pré-dispersor da radiação. Mais uma vez, o feixe é refletido pelo
espelho parabólico, e somente a radiação pré-selecionada passa através da fenda
intermediária (representada pelo nº 8), que é refletida por um segundo espelho
parabólico em direção à rede Echelle (representada pelo nº 9) (LEPRI, 2005; WELZ
et al., 2005a).
O arranjo dos componentes do monocromador permite uma montagem
altamente estável e compacta, e uma resolução típica de λ / Δλ = 140.000 pode ser
alcançada na região do UV. O ajuste preciso do comprimento de onda é realizado
pela rotação do prisma e da rede Echelle, através de motores de passos. Uma faixa
espectral de 190 nm (136ª ordem) a 900 nm (29ª ordem) é coberta e a largura de
banda instrumental (com uma largura de fenda de 23 μm) é determinada como
sendo 1,8 pm em 200 nm e 8,6 pm em 900 nm (WELZ et al., 2005a; BORGES,
2005; LEPRI, 2005; BORGES, 2009; LEPRI, 2009).
Obviamente, um monocromador de alta resolução, como o descrito acima,
requer um sistema ativo de estabilização de comprimento de onda para contornar
quaisquer problemas de flutuação. Neste sentido, uma lâmpada de neônio interna é
posicionada em frente à fenda intermediária, emitindo várias linhas relativamente
92
estreitas na faixa de 580 a 720 nm. Como a radiação que é emitida pela lâmpada de
Ne não passa pelo prisma pré-dispersor, as linhas são separadas pela rede Echelle
em várias ordens sobrepostas, o que implica no fato de que para cada posição da
rede há ao menos duas linhas de Ne que irão atingir o detector. Estas linhas são
então atribuídas a um pixel correspondente no detector e este sistema é utilizado
para estabilização, de maneira que a precisão é limitada apenas pelo motor de
passos, que ajusta a posição da rede (WELZ et al., 2005a; BORGES, 2005;
BORGES, 2009; LEPRI, 2009). A Figura 19 ilustra um monocromador do tipo
DEMON, de mesmo arranjo óptico do esquema apresentado na Figura 16.
Figura 19: Vista superior do monocromador
DEMON.
Fonte: WELZ et al., 2005.
1.4.1.4.2.3 Detector
Finalmente, a radiação dispersa pelo monocromador incide no detector, um
arranjo linear de dispositivos de carga acoplada (CCD), sensível na região do UV. O
detector possui 512 x 58 pixels, com dimensões individuais de 24 x 24 mm. A
resolução por pixel varia de acordo com a faixa espectral monitorada, e equivale a
1,6 pm pixel-1 em 200 nm. O detector é iluminado entre 1 – 10 ms, e os elétrons
gerados nos 58 pixels em cada coluna do detector, que correspondem a uma
93
estreita faixa de comprimento de onda, são transferidos simultaneamente para um
registro de medida, e então para um armazenador de carga. Este modo de leitura é
denominado de "full vertical binning mode" (WELZ et al., 2005a; BORGES, 2005;
BORGES, 2009; LEPRI, 2009). Uma representação esquematica do detector é
apresentada na Figura 20.
Figura 20: Representação esquemática do detector de arranjo linear de dispositivos de
carga acoplada.
Fonte: WELZ et al., 2005a.
Como cada pixel é equipado com um amplificador individual, o instrumento
opera de fato com 512 detectores independentes, 200 dos quais são e utilizados
para propósitos analíticos, sendo que uma linha atômica usualmente distribui-se por
cerca de 3 a 10 pixels (WELZ et al., 2005a; BORGES, 2005; BORGES, 2009).
Isto significa que todo o ambiente espectral a cerca de 200 pm ao redor da
linha analítica na região do ultra-violeta e cerca de 500 pm na região visível do
espectro torna-se “visível”, permitindo uma série de informações indisponíveis em
instrumentos convencionais. Com isso, é possível avaliar uma terceira dimensão do
fenômeno que ocorre no atomizador, de maneira que há três diferentes maneiras de
visualizar os dados em HR-CS AAS: (i) o tradicional sinal transiente (absorvância
integrada versus o tempo), (ii) o sinal de absorvância integrada versus comprimento
de onda, que permite visualizar qualquer absorção de radiação que tenha ocorrido
no intervalo espectral em análise, e (iii) a imagem tridimensional, que mostra a
absorvância como função do tempo e do comprimento de onda (WELZ et al., 2005a;
BORGES, 2005; BORGES, 2009).
94
1.4.1.4.2.4 Atomizadores
Os sistemas de atomização são os mesmos utilizados na LS AAS contendo,
portanto, as mesmas características e propriedades.
1.4.1.4.2.5 O software
O instrumento é controlado por um software que permite o processamento
total dos dados após a medida, o que é particularmente útil e interessante devido à
grande quantidade de informações obtidas com HR-CS AAS. Uma das
características mais relevantes do software é a sua capacidade de correção
automática para eventos contínuos, ou seja, eventos que afetam de maneira similar
todos os pixels do detector. Este tipo específico de correção considera que as
variações na intensidade de emissão da lâmpada de arco curto de Xe, bem como o
fundo contínuo são perfeitamente correlacionados no tempo dentro da pequena faixa
espectral de 0,3 – 0,6 nm que é gravada; este princípio é assegurado pelo fato que
os pixels convertem de maneira simultânea os fótons incidentes em fotoelétrons, o
que garante que variações proporcionais na intensidade sejam precisamente
convertidas em variações proporcionais nos sinais individuais de cada pixel. A esta
correção para eventos contínuos adiciona-se a alta intensidade de emissão da fonte
contínua, tornando-se desnecessária a modulação de radiação neste sistema, uma
vez que a radiação de corpo negro emitida pelo atomizador, por exemplo, é
obviamente um evento contínuo e pode ser facilmente corrigido por esse sistema
(WELZ et al., 2005a; BORGES, 2005; BORGES, 2009; LEPRI, 2005; LEPRI, 2009).
1.4.1.4.3 Vantagens da técnica de HR-CS AAS
Entre as principais vantagens oferecidas pela HR-CS AAS, incluem-se
(WELZ et al., 2005a; BORGES, 2005; LEPRI, 2005):
Uso de uma única fonte de radiação para todos os elementos cuja
determinação é possível por AAS;
95
Oferece uma melhora na razão sinal/ruído devido à elevada intensidade de
emissão da fonte de radiação, resultando em melhores precisão e limites de
detecção;
Pelo mesmo motivo, não há mais linhas “fracas”, portanto linhas secundárias
têm a mesma intensidade e podem ser usadas sem comprometimentos, por
exemplo, se a concentração do analito na amostra é elevada, reduzindo ou
eliminando a necessidade de diluição da mesma;
Toda a região espectral nas vizinhanças da linha analítica torna-se “visível”,
possibilitando muito mais informações do que as obtidas por instrumentos
convencionais de AAS;
A detecção utilizando arranjo CCD permite uma correção verdadeiramente
simultânea da radiação de fundo nas proximidades da linha analítica;
O software permite o processamento total pós-medida dos sinais, permitindo
selecionar pixels de referência adequados e definir limites de integração;
Possibilita de armazenamento de espectros de referência, por exemplo, de
espectro de absorção molecular com estruturas rotacionais finas, e a
subseqüente subtração deste do espectro de uma amostra, usando-se um
algoritmo de mínimos quadrados, sendo assim possível a correção de fundo
estruturado mesmo sob a linha analítica;
Correção automática para todos os eventos contínuos, tais como ruído da
lâmpada, absorção de fundo contínuo e outros fenômenos em banda larga
como emissão do atomizador;
Faixa de calibração com variação de até cinco ordens de grandeza;
Melhor desempenho analítico na determinação de elementos-traço em
amostras complexas;
Embora ainda não disponível comercialmente, se um detector bidimensional
apropriado for usado, o sistema permitirá em AAS medidas simultâneas
multielementares, prática comum em espectrometrias com fonte de plasma.
1.4.2.4.4 Aplicações
A seguir, a Tabela 12 apresenta algumas aplicações da técnica de HR-CS
AAS. Nela, é possível verificar sua ampla utilização na determinação de diversos
96
elementos nas mais variadas matrizes, de diversos graus de complexidade. Isto
mostra a versatilidade da técnica e o seu potencial uso na análise de amostras reais.
97
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
Analito(s)
Amostra(s)
Sistema Analítico
(continua)
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
Cu, Fe, Ni, Zn
Óleo vegetal
HR-CS-F AAS
-
LODs: entre 0,12 µg kg-1 (Cu e
Zn) e 0,62 µg kg-1 (Fe)
F
Pasta de dente
HR-CS-GF MAS
NH4H2PO4 + Pd +Zr
LOQ = 30 µg g-1
Ni, V
Óleo cru
HR-CS-GF AAS
-
LODs:
Ni = 3 µg g-1
V = 1 µg g-1
NUNES et al.,
article in press,
2011
GLEISNER et al.,
article in press,
2011
QUADROS et al.,
article in press,
2010
Sb
Material particulado
transportado pelo
ar
SS-HR-CS-GF AAS
Ru
LOD = 15 µg g-1
LOQ = 50 µg g-1
ARAÚJO et al.,
2010
Zn
Iogurte
HR-CS-F AAS
(amostragem por
suspensão)
-
LOD = 0,32 µg g-1
BRANDÃO et al.,
2010
Zn
Espécimes
individuais de
Daphnia magna
SS-HR-CS-GF AAS
-
LOD = 1,4 ng
BRICEÑO et al.,
2010
Co, V
Óleo cru não
diluído
SS-HR-CS-GF AAS
Pd + Triton X-100
LODs:
Co = 8 µg g-1; V = 1,2 µg g-1
DITTERT et al.,
2010
S
Amostras
biológicas
SS-HR-CS-GF MAS
W e Pd
S absoluto = 0,015 µg
S na am. sólida = 0,03 mg g-1
FERREIRA et al.,
2010
F (GaF)
Águas naturais de
baixa
complexidade
HR-CS-GF MAS
Pd+ Zr + NaOAc +
nitrato de Ru(III)nitrosila
LOD = 0,26 µg L
-1
GLEISNER;
WELZ; EINAX,
2010
97
98
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
(continuação)
Analito(s)
Amostra(s)
Sistema Analítico
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
P (avaliação do efeito
Zeeman na correção
de Bkg, com diferentes
modificadores)
NH4H2PO4
LS GF AAS e
HR-CS-GF AAS
NaF, Pd, Pd + Ca, Pd
+ ác. Ascórbico
-
LEPRI et al.,
2010
LEPRI et al.,
2010
Cr, Cu, Fe, Mn, Mo, Ni
eV
Carvão vegetal e
“black carbon”
SS-HR-CS-GF AAS
e ICP OES
-
LODs: entre 0,006 µg kg-1 (Ni) e
0,9 µg kg-1 (Fe)
LOQs: entre 0,02 µg kg-1 (Ni) e
3,2 µg kg-1 (Fe)
B, Ca, Cu, Fe, K, Mg,
Mn, Mo, P, S e Zn
Tecido de plantas
HR-CS-F AAS
-
LODs: entre 0,01 mg L-1 (Mo) e
106 mg L-1 (S)
OLIVEIRA et al.,
2010
Nanopartículas de Au
Tecido de
camundongo
SS-HR-CS-GF MAS
Pd
LOD = 5 pg (2 ng/g)
RESANO et al.,
2010
(Determ. simult.) Cd e
Fe
Lodo de esgoto
HR-CS GF AAS
(amostragem por
suspensão)
-
LOD: Cd = 0,03 µg g-1; Fe = 90
µg g-1
VIGNOLA et al.,
2010
(Determ. simult.) Cd e
Fe
Grãos e solos
HR-CS GF AAS
Ir-W
LOQ = 4 ng (Fe)
WELZ et al.,
2010b
Sb
CRMs de
sedimento
SS-HR-CS-GF AAS
Ir
LOD = 0,02 µg g-1
ARAUJO et al.,
2009
Ag
Amostras
geológicas
SS-HR-CS-GF AAS
-
LOD = 2 ng g-1
DITTERT et al.,
2009
(Det. simult.) Cr e Fe
Óleo cru
SS-HR-CS-GF AAS
-
LODs:
Cr = 1 µg kg-1; Fe = 0,6 mg kg-1
DITTERT et al.,
2009
98
99
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
(continuação)
Analito(s)
Amostra(s)
Sistema Analítico
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
I (BaI)
Pílulas
HR-CS GF MAS
-
LOD = 0,6 ng (I)
HUANG et al.,
2009
OLIVEIRA;
RAPOSO Jr.;
GOMES NETO,
2009
Ca, Mg, K, Cu, Fe, Mn,
Zn
Plantas
HR-CS F AAS
-
LODs: entre 0,4 mg L-1 (Ca e
Mg) e 7,7 mg L-1 (K e Cu)
Hg
Polímeros
SS-HR-CS-GF AAS
SS-LS-GF AAS
-
LODs :
SS-HR-CS-GF AAS = 0,6 µg g-1
SS-LS-GF AAS = 2,2 µg g-1
RESANO;
BRICEÑO;
BELARRA, 2009
P
CRMs sólidos de
amostras
biológicas
SS-HR-CS-GF AAS
SS-HR-CS-ET MAS
LODs :
SS-HR-CS-GF AAS = 5 µg g-1
SS-HR-CS-ET MAS = 20 µg g-1
LODs:
RESANO;
BRICEÑO;
BELARRA, 2009
Cd, Fe
Grãos de feijão e
solo
SS-HR-CS-GF AAS
Ir-W
Feijão: Cd = 2 µg kg-1; Fe = 4,5
mg kg-1
Solo: Cd = 14 µg kg-1; Fe = 170
mg kg-1
SANTOS et al.,
2009b
Cd, Fe
Grãos
SS-HR-CS-GF AAS
Ir-W
LODs: Cd = 0,6 µg kg-1; Fe =
0,5 mg kg-1
SANTOS et al.,
2009c
Ag, Cd, Co, Cu, Ni, Zn
Soluções-padrão
Célula de quartzo e
HG-HR CS AAS
Para P: Pd, ác.
ascórbico e W;
Para PO: W
8-Hidroxiquinolina
LODs: entre 1,5 µg L-1 (Cd) e
586 µg L-1 (Ni)
VILLANUEVAALONSO; PEÑAVÁZQUEZ;
BERMEJOBARRERA, 2009
99
100
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
(continuação)
Analito(s)
Amostra(s)
Sistema Analítico
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
Razão isotópica de B
(10B/11B)
Ligas de aço
HR-CS-F AAS
-
-
WILTSCHE et al.,
2009
P (avaliação de D2 na
correção de Bkg com
diferentes
modificadores)
NH4H2PO4
LS GF AAS e HR-CS
GF AAS
NaF, La, Pd + Ca, Pd
(o melhor)
-
DESSUY, et al.,
2008
Br (AlBr e CaBr)
Ámostra salina
(Mar Morto) e
Bromazepan
HR-CS GF MAS
Ba (para amostra
salina)
2ng (Br, ambos os compostos
de Br)
HUANG et al.,
2008
Especiação de S
vinho
HR-CS-F MAS
-
LOD = 1,8 mg L-1 SO2
HUANG et al.,
2008
RAPOSO
JUNIOR, et al.,
2008
Pb
H3PO4
HR-CS F AAS
-
LODs = 10 µg L-1 (λ = 217,0005
nm) e 17 µg L-1 (λ = 283,3060
nm)
Fe, Cu, Mn, Zn
Extratos de solo
HR-CS F AAS
-
LODs = entre 4,2 µg L-1 (Mn) e
147 µg L-1 (Fe)
RAPOSO
JUNIOR, et al.,
2008
Al
Produtos
farmacêuticos com
altos teores de Fe
e açúcar
HR-CS-GF AAS
-
LODs = 1,1 pg (λ = 309,271 nm)
e 1,4 pg (λ = 396,152 nm)
BOHRER et al.,
2007
100
101
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
(continuação)
Analito(s)
Amostra(s)
Sistema Analítico
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
P (avaliação do
processo de
atomização – uso de
plataformas de grafite
e tântalo)
NH4H2PO4
HR-CS GF AAS
NaF
-
DESSUY et al.,
2007
Cd (avaliação de
modificadores
químicos)
carvão
LS GF AAS e HR-CS
GF AAS (amostragem
por suspensão)
Pd-Mg; Ir; Ru; Ir-W;
Ru-W
LOD = 0,6 ng g-1 (HR-CS GF
AAS)
BIANCHIN et al.,
2006
Pb
CRMs de amostras
biológicas
SS-HR-CS-GF AAS
Ru
LOD = 0,01 µg g-1
BORGES et al.,
2006
Pb
carvão
SS-HR-CS-GF AAS
-
LOD = 0,008 µg g-1
BORGES et al.,
2006
LODs:
F = 9 pg; Cl = 70 pg
S = 2,3 ng; P = 0,9 ng
HEITMANN et al.,
2006
F, Cl, S, P
F (GaF)
Cl (InCl)
CRM de minério de
zinco e CRMs de
amostras
biológicas
CRMs: leite em pó
e sedimentos
marinhos
CRMs: leite em pó
e sedimentos
marinhos
HR-CS-GF AAS
Para F: Mg e Zr;
Para Cl: Sr
Para S: Ca e Zr
Para P: -
HR-CS-F MAS
-
LOD = 1 mg L-1 (F)
HUANG et al.,
2006
HR-CS-F MAS
-
LOD = 3 mg L-1 (Cl)
HUANG et al.,
2006
101
102
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
(continuação)
Analito(s)
Amostra(s)
Sistema Analítico
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
P
CRMS – espinho
de pinheiro e BCR
nº 33 (superfosfato)
HR-CS-F MAS
-
-
HUANG et al.,
2006
S (CS)
CRMS – ferro
fundido
HR-CS-F MAS
-
LOD = 2,4 mg L-1
HUANG et al.,
2006
P (avaliação de
modificadores
químicos)
NH4H2PO4
HR-CS GF AAS
La, NaF, Pd, Pd + ác.
Ascórbico;
Pd +
Ca.
-
LEPRI et al.,
2006
Especiação de V
óleo cru
HR-CS-GF AAS
-
LOD = 0,04 mg kg-1
LOQ = 0,12 mg kg-1
LEPRI et al.,
2006
Hg
Amostras
biológicas
HR-CS-GF AAS
KMnO4
LOD = 0,1 µg g-1
SILVA et al., 2006
LODs:
Ni = 0,02 µg g-1; V = 0,06 µg g-1
DAMIN et al.,
2005
Ni, V
óleo cru
HR-CS-GF AAS
Pd
P
CRMs – ferro
fundido
HR-CS-F MAS
-
LOD = 1,3 mg L-1
HUANG et al.,
2005
S total
vinho
HR-CS-F MAS
-
LOD = 2,4 mg L-1
HUANG et al.,
2005
Cd
carvão
SS-HR-CS-GF AAS
Ir
LOD = 2 ng g-1
LOQs:
Ni = 0,065 µg g-1; Se = 0,17 µg
g-1
SILVA et al., 2005
102
103
Tabela 12: Diversas aplicações da técnica de HR-CS AAS.
Analito(s)
Amostra(s)
Sistema Analítico
(conclusão)
Modificador Químico
LOD(s) e/ou LOQ(s)
Referência
-
LODs
SS-LS GF AAS = 0,020 µg
g-1
SS-HR-CS GF AAS = 0,005
µg g-1
LS GF AAS (TMAH) = 0,010
µg g-1
HR-CS GF AAS (TMAH) =
0,015 µg g-1
RIBEIRO et al.,
2005
Co
Amostras
biológicas
LS GF AAS e HR-CS
GF AAS (amostragem
sólida ou prétratamento com
TMAH)
Tl
sedimento
LS GF AAS e HR-CS
GF AAS
-
LOD = 0,01 µg g-1
SILVA et al., 2005
Ni
petróleo
LS GF AAS e HR-CS
GF AAS
-
LOD = 0,07 µg g-1
VALE et al., 2004
103
104
2 JUSTIFICATIVA E OBJETIVO DO TRABALHO
Este trabalho justifica-se pela necessidade de realização de estudos
aplicados ao conhecimento e a melhoria, de métodos analíticos quantitativos,
visando a caracterização de elementos químicos presentes em águas nos poços de
petróleo. A água produzida é considerada o maior rejeito de todo o processo de
produção de petróleo, configurando-se um grande problema operacional, gerencial e
ambiental. Portanto, a motivação deste trabalho consiste em identificar alguns
constituintes (elementos-traço) para uma melhor caracterização das águas
produzidas, o que pode auxiliar no seu tratamento mais efetivo, implicando na
redução de custos para seu descarte. Outro aspecto que se deve destacar é que o
conhecimento da origem destas águas pode permitir um melhor entendimento de
processos no sistema petrolífero, reduzindo o risco exploratório.
Deste modo, os resultados deste trabalho poderão contribuir de modo
significativo para um reconhecimento mais efetivo da água nos processos de
exploração e produção. Assim, dentro do contexto atual em que a indústria
petrolífera brasileira se encontra, este projeto assume relevância, visto que a sua
execução pode atender demandas específicas do setor.
Do ponto de vista técnico/científico, metodologias analíticas acuradas e
confiáveis para determinação de elementos-traço e em amostras de matrizes
complexas podem ser implementadas como procedimento de rotina melhorando os
trabalhos nos laboratórios que realizam tais análises.
O objetivo deste trabalho, portanto, é o desenvolvimento de metodologia(s)
analítica(s) para caracterização geoquímica parcial de efluentes salinos da indústria
do petróleo (águas produzidas) em relação a alguns constituintes inorgânicos
presentes como elementos-traço, que compõem essas águas.
Como objetivos específicos:
Desenvolvimento de um procedimento de separação/pré-concentração de Co,
Cu, Mn, Ni e Pb em amostras salinas baseado na Extração em Fase Sólida
com
resina
quelante
Chelex-100®,
a
interferências causadas pela matriz salina;
fim
de
minimizar/eliminar
as
105
Verificar a aplicabilidade da SPE em batelada como alternativa para a coluna;
Desenvolver
metodologias
analíticas
confiáveis
e
validadas
para
a
determinação dos elementos já mencionados em amostras salinas pela
técnica de Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua e Forno de Grafite (HR-CS GF AAS) para a determinação de alguns
constituintes inorgânicos, presentes como elementos-traço, que compõem
essas águas: cobalto, cobre, manganês, níquel e chumbo.
Aplicar as metodologias analíticas desenvolvidas a amostras de água
produzida de plataformas brasileiras offshore.
106
3 MATERIAIS E MÉTODOS
3.1 REAGENTES E SOLUÇÕES
Todas as soluções foram preparados com água ultra pura obtida de um
sistema Elga modelo PURELAB Ultra Analytic (Elga, High Wycombe, Bucks, UK) e
soluções-padrão estoque de grau analítico.
O ácido nítrico utilizado (Merck, Darmstadt, Germany) foi duplamente
destilado a sub-ebulição (ácido nítrico sub-boiling) e o hidróxido de amônio, grau
TraceSELECT® Ultra, for trace analysis, fornecido pela Fluka (Fluka, Milwaukee, WI,
USA).
Suspensão de Chelex-100® na forma Na+ (Bio-Rad Laboratories, Hercules,
Califórnia, USA) foi preparada a partir do reagente sólido com tamanho de partícula
entre 200-400 mesh. A mesma foi lavada com solução de HNO 3 de concentração
10% v/v (a fim de eliminar possível contaminação e convertê-la à forma H+) e em
seguida com água ultrapura até pH constante e igual ao desta.
O meio salino foi gerado a partir de diluição de uma solução estoque de
17,5% m/v, sendo esta preparada a partir de NaCl sólido grau P.A. (Merck,
Darmstadt, Alemanha). A mesma também foi descontaminada adicionando 10 mL de
suspensão de Chelex-100® e ajuste do pH, a fim de eliminar possível contaminação
presente no sal.
Soluções de Co, Cu, Mn, Ni, e Pb foram preparadas em capela de fluxo
laminar, a partir de diluição de soluções-padrão estoque de concentração 1.000 mg
L-1 ou 10.000 mg L-1 (CertiPrep SPEX, Metuchen, USA), até obtenção das
concentrações desejadas.
Para a avaliação qualitativa da presença de cloreto residual do procedimento
de pré-concentração, utiizou-se uma solução de AgNO3, (Vetec Química Fina, Rio
de Janeiro, Brasil).
Para validação da metodologia, fez-se uso dos seguintes materiais de
referência certificados: CASS-4 (Nearshore Seawater Reference Material for Trace
Metals), CASS-5 (Nearshore Seawater Reference Material for Trace Metals) e
107
NASS-5 (Seawater Reference Material for Trace Metals), todos certificados e
fornecidos pelo National Research Council Canadá (NRCC, Ottawa, Canadá).
As amostras de água produzida foram coletadas diretamente de plataformas
offshore brasileiras em frascos de polietileno. Em laboratório elas foram filtradas com
uso de membranas de Teflon com diâmetro de poro de 0,45 µm (Millipore, Bedford,
MA, USA) e sistema de filtração a vácuo para remoção do óleo remanescente e de
material particulado em suspensão. Por fim elas foram acidificadas até pH 1,6 com
HNO3 para preservação dos analitos nas amostras.
3.2 INSTRUMENTAÇÃO
Para ajuste do pH, empregou um medidor de pH da marca Analyser, modelo
300M (Analyser, São Paulo, Brasil).
Para acelerar o processo de decantação das partículas de resina, utilizou-se
uma centrífuga da marca CELM, modelo LS-3 plus, série 564.
Para descarte dos sobrenadantes, empregou uma bomba peristáltica da
marca Ismatec, modelo IPC contendo 12 canais.
Para a determinação dos elementos de interesse deste estudo foi empregado um
Espectrômetro de Absorção Atômica de Alta Resolução com Fonte Contínua modelo
contrAA 700 (Analytik Jena, Jena, Alemanha), com atomização por chama e por
forno de grafite, sendo este último o módulo utilizado. O sistema óptico é composto
por uma fonte de radiação, representada por uma lâmpada de arco curto de xenônio
(GLE, Berlim, Alemanha) operando em modo “hot-spot”; um monocromador duplo,
equipado com um prisma e uma rede Echelle (DEMON); e um detector de arranjo
linear CCD com 588 pixels, onde 200 são empregados para propósitos analíticos e
os outros usados para funções internas. Um amostrador automático para forno de
grafite modelo MPE60 foi utilizado na introdução das amostras no forno de grafite. O
espectrômetro foi operado em modo padrão e o software Aspect CS versão 1.4.0 foi
utilizado para a aquisição dos dados. Os experimentos foram conduzidos em tubos
de grafite com aquecimento tranversal, com (Analytik Jena, Jena, Alemanha, Part nº
407-A81.025) ou sem plataforma PIN integrada (Analytik Jena, Jena, Alemanha, Part
108
nº 407-A81.011), ambos revestidos piroliticamente, a depender do elemento a ser
determinado.
3.3 PROCEDIMENTO EXPERIMENTAL
Tubos graduados e recipientes novos de polietileno foram utilizados em todas
as etapas, para evitar contaminação. Os mesmos foram mantidos por 24 horas em
solução de ácido nítrico 10% v/v. Os vials utilizados no amostrador automático do
equipamento foram mantidos em solução detergente de Extran (MERCK) 10% v/v
por no mínimo 24h e posteriormente mantidos em solução de ácido nítrico 10% v/v
pelo mesmo período. Antes do uso, todos os frascos e vials foram rinsados com
água ultra pura e secos em capela de fluxo laminar.
A metodologia foi proposta da seguinte forma: em tubos tipo Falcon de 15 mL
contendo 15 mL das soluções (soluções-padrão e amostras), fez-se a adição da
suspensão de Chelex-100® e posteriormente ajuste do pH entre 5 - 7 com uso de
hidróxido de amônio e HNO3. Após este procedimento, as soluções foram agitadas
vigorosamente e submetidas à agitação mecânica por uma noite. Em seguida, foram
centrifugadas e o sobrenadante descartado; adicionou-se então 15 mL de solução
de NH4OH com pH entre 5-7 para a lavagem da resina. Após agitação essa mistura
foi centrifugada e o sobrenadante foi novamente descartado. À resina residual fez-se
a adição de 0,5 mL de solução de ácido nítrico destilado à sub-ebulição com
concentração igual a 10% v/v e o volume foi completado até 3 mL com água ultra
pura. As soluções foram agitadas vigorosamente e novamente centrifugadas. Estes
sobrenadantes foram então direcionados ao HR-CS GF AAS para realização das
determinações dos analitos. Os comprimentos de onda utilizados para cada
elemento são apresentados na Tabela 13.
109
Tabela 13: Comprimentos de onda utilizados nas
determinações por HR-CS GF AAS.
Elemento
Comprimento de onda da linha (nm)
Co
240,7254
Cu
324,7540
Mn
279,4817
Ni
232,0030
Pb
283,3060
110
4 RESULTADOS E DISCUSSÃO
4.1 ESCOLHA DO TIPO DE ATOMIZADOR
Em GF AAS, pode-se utilizar dois tipos de atomização: por parede ou por
plataforma. Para o instrumento empregado neste estudo, o fabricante disponibiliza
comercialmente tubos para ambos os tipos de atomização. Além disso, ele também
sugere qual seria o melhor tipo de atomização para cada elemento. No caso dos
analitos de interesse aqui, é indicada a atomização por plataforma para todos os
elementos.
Desse modo, procedeu-se um experimento para a verificação dessa
indicação. As Figuras 21, 22, 23, 24, e 25 apresentam os sinais de absorvância
obtidos para uma solução multielementar dos elementos de interesse na
concentração de 20 μg L-1, em meio de HNO3 2% v/v. Para esse experimento,
utilizou-se a temperatura de 200⁰C para a pirólise e para a atomização, foram
usadas as temperaturas indicadas pelo fabricante, escolhendo sempre a mais alta
em caso de uma faixa. As temperaturas de atomização foram portanto para Co =
2300 ⁰C; Cu = 2000 ⁰C; Mn = 1900 ⁰C; Ni = 2350 ⁰C; e Pb = 1800 ⁰C.
Figura 21: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Co em solução de concentração 20 μg L-1 em meio
de HNO3 2% v/v, com atomização por plataforma.
111
Figura 22: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Cu em solução de concentração 20 μg L-1 em meio
de HNO3 2% v/v, com atomização por plataforma.
Figura 23: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Mn em solução de concentração 20 μg L -1 em meio
de HNO3 2% v/v, com atomização por plataforma.
112
Figura 24: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Ni em solução de concentração 20 μg L -1 em
meio de HNO3 2% v/v, com atomização por plataforma.
Figura 25: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Pb em solução de concentração 20 μg L-1 em meio de
HNO3 2% v/v, com atomização por plataforma.
113
Observando as Figuras 21 e 24, com os sinais para Ni e Co, pode-se verificar
que ao fim do tempo de atomização o sinal não retorna totalmente para a linha de
base. Sendo assim, com esta mesma solução (20 μg L-1), a atomização destes dois
elementos foi realizada novamente, porém utilizando a atomização por parede. Os
resultados são apresentados nas Figuras 26 e 27.
Figura 26: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Co em solução de concentração 20 μg L-1 em meio
de HNO3 2% v/v, com atomização por parede.
114
Figura 27: Tela do software Aspect CS 1.4.0 mostrando o sinal de
absorvância para Ni em solução de concentração 20 μg L -1 em meio de
HNO3 2% v/v, com atomização por parede.
Através destes resultados, observa-se que, apesar de o fabricante indicar a
plataforma para todos os elementos de interesse, experimentalmente verifica-se
que, para Ni e Co, a atomização se torna mais eficiente quando é realizada através
da parede do tubo de grafite. Isso pode ser justificado pelo fato de que, na
atomização por plataforma, a temperatura é atingida por irradiação, e não por
aquecimento direto, como no caso da atomização por parede. Apesar de a
plataforma gerar um ambiente de atomização termicamente mais homogêneo, é
necessário um tempo maior para alcançar a temperatura desejada o acarreta em
uma etapa de atomização mais lenta e na necessidade de um tempo mais elevado
na etapa de atomização da programação de temperatura. Por esse motivo, em geral
se indica a atomização por parede para elementos com temperatura de atomização
mais elevadas, já que ela permite uma atomização mais rápida num mesmo
intervalo de tempo, quando comparada com a atomização por plataforma, o que
condiz com os resultados apresentados, uma vez que Co e Ni são os elementos
mais refratários da lista de analitos deste trabalho.
115
4.2 OTIMIZAÇÃO DAS TEMPERATURAS DE PIRÓLISE E ATOMIZAÇÃO
A fim de determinar quais seriam as temperaturas de pirólise (TP) e
atomização (TA) mais adequadas para cada elemento, construiu-se as curvas de
pirólise e de atomização. Para tal, utilizou uma solução multielementar de 5 μg L-1
em meio a HNO3 2% v/v contendo apenas os analitos de interesse. O meio da
solução foi escolhido devido ao extrato final do procedimento de pré-concentração
ser em meio muito similar a este. Como referência, foram utilizadas as temperaturas
indicadas pelo fabricante. Os resultados para cada analito são descritos a seguir.
4.2.1 Curvas de TP e TA para cobalto
Para cobalto, o fabricante indica as faixas de 1000 – 1300ºC para a
temperatura de pirólise e 2000 – 2300ºC para a temperatura de atomização, sendo
ambos os máximos obtidos na presença do modificador químico mais adequado.
Porém, visto que a matriz do extrato destinado ao HR-CS GF AAS é composta
quase que exclusivamente de solução de HNO3 (matriz mais simples) optou-se por
propor uma curva de pirólise a temperaturas mais baixas, de modo a dispensar o
uso de modificador químico. Para a construção da curva de pirólise para Co, fixou-se
a temperatura de atomização em 2300 ºC.
Já para a curva de atomização, optou-se por ampliar a faixa de temperatura.
Os resultados para a curva de TP e TA para Co são apresentados na Figura 28,
com atomização por parede.
Figura 28: Curvas de TP (-●-) e TA (-■-) para Co em solução de 5 μg L-1 em meio de HNO3 2%
v/v.
116
A partir dos resultados obtidos para TP, pode-se observar que não houve
variação do sinal entre as temperaturas de 200ºC e 600ºC, de forma que a
temperatura de 200ºC foi escolhida para os experimentos seguinte e para a
construção da curva de atomização para o cobalto. Temperaturas inferiores a 200ºC
não foram estudadas pelo fato de esta temperatura já estar muito próxima da
temperatura de secagem (110 ºC) utilizada na programação.
Para os resultados obtidos para TA, verifica-se que a temperatura ideal está
entre 2100 e 2300ºC, na ausência de modificador químico. Sendo assim, a
temperatura de atomização escolhida para Co foi 2200ºC.
4.2.2 Curvas de TP e TA para cobre
Para cobre, são indicadas pelo fabricante as temperaturas de 850ºC e 2000ºC
como
sendo
as
melhores
temperaturas
de
pirólise
e
de
atomização,
respectivamente, sendo ambas obtidas na ausência de modificador químico. Porém,
da mesma forma que para o Co, a matriz do extrato é composta quase que
exclusivamente de solução de HNO3, optou-se por propor uma curva de pirólise a
temperaturas mais baixas. Para a construção da curva de pirólise para Cu, fixou-se
a temperatura de atomização em 2000 ºC.
Já para a curva de atomização, optou-se por usar uma faixa de temperatura
tal que o valor central fosse aproximadamente a temperatura indicada pelo
fabricante. Os resultados para as curvas de TP e TA para Cu são apresentados na
Figura 29, com atomização por plataforma.
Figura 29: Curvas de TP (-●-) e TA (-■-) para Cu em solução de 5 μg L-1 em meio de HNO3 2%
v/v.
117
A partir dos resultados obtidos para TP, pode-se observar que, da mesma
forma que para o Co, não houve variação do sinal entre as temperaturas de 200ºC e
400ºC, de forma que a temperatura de 200ºC foi novamente escolhida, e também
usada para a construção da curva de atomização. Igualmente, temperaturas
inferiores a 200ºC não foram avaliadas pela proximidade com a temperatura de
secagem utilizada na programação.
Para os resultados obtidos para TA, verifica-se que a temperatura ideal está
entre 2000 e 2100ºC, na ausência de modificador químico. Porém, pode-se observar
pelos perfis dos sinais apresentados na Figuras 30 e 31 que, para TA = 2100ºC, o
sinal se torna mais estreito e ao fim do tempo de atomização o ele se mantém mais
próximo da linha de base quando comparado com TA = 2000ºC. Sendo assim, a
temperatura de atomização escolhida para Cu foi de 2100ºC.
Figura 30: Tela do software Aspect CS 1.4.0 mostrando o registro do
sinal de absorvância para Cu em solução de concentração 5 μg L-1
em meio de HNO3 2% v/v. Atomização por plataforma, TA = 2000ºC.
118
Figura 31: Tela do software Aspect CS 1.4.0 mostrando o registro do
sinal de absorvância para Cu em solução de concentração 5 μg L -1
em meio de HNO3 2% v/v. Atomização por plataforma, TA = 2100ºC.
4.2.3 Curvas de TP e TA para manganês
Para manganês, são indicadas 900ºC e 1900ºC como sendo as temperaturas
ótimas respectivamente para as temperaturas de pirólise e de atomização, sendo
ambas também obtidas na ausência de modificador químico. Porém, assim como
para Co e Cu, a matriz mais simples do extrato de pré-concentração remete à
proposição de uma curva de pirólise a temperaturas mais baixas. A construção da
curva de pirólise para Mn foi feita com temperatura de atomização de 1900 ºC.
Para a curva de atomização, procedeu-se tal qual para o Cu, optando-se por
usar uma faixa de temperatura de modo que o valor central fosse aproximadamente
a temperatura indicada pelo fabricante. Os resultados para as curvas de TP e TA
para Mn são apresentados na Figura 32, com atomização por plataforma.
119
Figura 32: Curvas de TP (-●-) e TA (-■-) para Mn em solução de 5 μg L-1 em meio de HNO3 2% v/v.
A partir dos resultados obtidos para TP, pode-se observar que novamente
não houve variação do sinal entre as temperaturas de 200ºC e 700ºC, e mais uma
vez 200ºC foi a temperatura escolhida para a etapa de pirólise e empregada também
na construção da curva de atomização. Também as temperaturas abaixo de 200ºC
não foram avaliadas por já estarem muito próximas da temperatura de secagem.
Para a TA, verifica-se através dos resultados que, na ausência de modificador
químico, a temperatura ótima de atomização se encontra entre 1800 e 2000ºC, de
modo que a escolhida para Mn foi a de 2000ºC.
4.2.4 Curvas de TP e TA para níquel
Para níquel, o fabricante indica como sendo 1100ºC a melhor temperatura de
pirólise e 2350ºC para a temperatura de atomização, ambas obtidas na ausência de
modificador químico. Porém, mediante a simplicidade da matriz dos extratos
inseridos no HR-CS GF AAS, mais uma vez se propôs uma curva de pirólise a
temperaturas mais baixas, e para sua construção utilizou-se 2350 ºC como
temperatura de atomização. No caso da curva de atomização, fez-se uso de uma
faixa de temperatura tal que o valor central fosse aproximadamente a TA indicada
pelo fabricante. As curvas de TP e TA para Ni são mostradas na Figura 33, com
atomização por parede.
120
Figura 33: Curvas de TP (-●-l) e TA (-■-) para Ni em solução de 5 μg L-1 em meio de HNO3 2% v/v.
A partir dos resultados obtidos para TP, pode-se observar que, mais uma
vez, não houve variação dos sinais de absorvância entre as temperaturas de 200ºC
e 400ºC, de forma que 200ºC foi novamente a temperatura escolhida para a pirólise
e usada na construção da curva de atomização para níquel. Temperaturas abaixo de
200ºC não foram avaliadas pela proximidade com a temperatura de secagem
utilizada na programação.
Para os resultados de temperatura de atomização na ausência de modificador
químico observa-se que a temperatura ideal se localiza entre 2300 e 2400ºC. Sendo
assim, para Ni, a temperatura de atomização escolhida foi de 2350ºC.
4.2.5 Curvas de TP e TA para chumbo
Por fim, para chumbo, o fabricante indica as faixas de 500 – 900ºC para a
temperatura de pirólise e 1500 – 1800ºC para a temperatura de atomização, onde
ambos os máximos são alcançados na presença do modificador químico mais
adequado. Entretato, a matriz composta quase que exclusivamente de solução de
HNO3 permite o estudo da curva de pirólise a temperaturas mais reduzidas, ainda
que na ausência de modificador(es) químico(s). E para a construção da curva de
pirólise para chumbo, foi usada a temperatura de atomização de 1800 ºC .
Já para a curva de atomização, ampliou-se a faixa de temperatura. As curvas
de TP e TA para Pb são apresentados na Figura 34, com atomização por
plataforma.
121
Figura 34: Curvas de TP (-●-l) e TA (-■-) para Pb em solução de 5 μg L-1 em meio de HNO3 2% v/v.
A partir dos dados de temperatura de pirólise, observa-se que não houve
variação dos sinais de absorvância entre as temperaturas de 200ºC e 600ºC, e
portanto 200ºC foi a temperatura escolhida. Temperaturas inferiores a 200ºC não
foram estudadas pelo fato de esta temperatura já estar muito próxima da
temperatura de secagem utilizada na programação.
Para os dados obtidos para temperatura de atomização, verifica-se que, se
trabalhando sem modificador químico, a temperatura ótima se encontra entre 1400 e
1700ºC, de modo que 1400ºC foi a temperatura escolhida para atomização de Pb.
Portanto, ao fim deste experimento obteve-se as melhores temperaturas de
pirólise e de atomização para cada um dos analitos, a serem utilizadas nos estudos
seguintes. A Tabela 14 apresenta a programação de temperatura utilizada para a
determinação de Co, Cu, Mn, Ni e Pb após a otimização de TP e TA.
122
Tabela 14: Programações de temperatura empregadas nas determinações por
HR-CS GF AAS.
Etapa
T (ºC)
Rampa (ºC/s)
Patamar (ºC)
Tempo (s)
Secagem
110
20
10
14,3
Pirólise
200
30
20
23,0
AZ*
200
0
5
5,0
Co
2200
2800
5
4,8
Cu
2100
2800
5
4,7
Mn
2000
2800
6
6,6
Ni
2350
2800
5
5,8
Pb
1400
2800
5
5,5
Co
2600
500
4
4,6
Cu
2500
500
4
4,6
Mn
2450
500
4
4,6
Ni
2600
500
4
4,5
Pb
2500
500
4
5,6
Atomização
Limpeza
(*) Autozero.
4.3 INFLUÊNCIA DA PRESENÇA DE NaCl NA PRÉ-CONCENTRAÇÃO
Com a finalidade de verificar o efeito da presença do NaCl na préconcentração dos elementos-traço de interesse, realizou-se o procedimento de préconcentração em soluções de concentração variando entre 0 e 10 μg L -1 (0; 1,0; 2,5;
5,0; 10,0 μg L-1) em meio de água ultrapura e, inicialmente, em meio de solução de
NaCl 3,5% m/v (salinidade igual a 35, simulando a da água do mar), com adição de
200µL de suspensão da Chelex-100® 10% m/v. A curva sem pré-concentração foi
123
realizada em meio de solução de HNO3 2% v/v. Os resultados são apresentados nas
Figuras 35 a 39.
A int
1,20
sem PC
PC H2O 1
1,00
PC H2O 2
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
0,80
0,60
0,40
0,20
0,00
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 35: Curvas de PC para Co em meio de água ultrapura e solução de NaCl 3,5% m/v,
com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int 0,7
sem PC
PC H2O - 1
0,6
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,5
PC NaCl 3,5% m/v - 2
0,4
0,3
0,2
0,1
0,0
0,0
2,5
5,0
7,5
10,0
[Cu] nominal (μg L-1)
Figura 36: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl 3,5% m/v,
com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
124
A int
1,4
sem PC
PC H2O 1
1,2
PC H2O 2
PC NaCl 3,5% m/v - 1
1,0
PC NaCl 3,5% m/v - 2
0,8
0,6
0,4
0,2
0,0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 37: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v, com
adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int0,25
sem PC
PC H2O - 1
PC H2O - 2
0,20
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
0,15
0,10
0,05
0,00
0,0
2,5
5,0
7,5
10,0
[Ni] nominal (μg L-1)
Figura 38: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5% m/v, com
adição de 200 µL de suspensão de Chelex-100® 10% m/v.
125
A int
0,40
sem PC
0,35
PC H2O - 1
0,30
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,25
PC NaCl 3,5% m/v - 2
0,20
0,15
0,10
0,05
0,00
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 39: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl 3,5% m/v, com
adição de 200 µL de suspensão de Chelex-100® 10% m/v.
Através dos resultados obtidos e apresentados anteriormente observa-se que,
para Cu, Mn e Ni, o procedimento de PC é muito pouco afetado pela salinidade, ao
contrario de Co e Pb. No caso do Co verfica-se que ocorre um aumento na diferença
entre as absorvâncias à medida que a concentração aumenta. No caso de Mn e Pb,
observa-se que há possível contaminação proveniente do NaCl, sendo a situação do
chumbo a mais crítica, tendo em vista a diferença dos sinais de absorvância para
uma mesma concentração. Entretanto, ainda para o Pb, ao comparar os perfis com
e sem sal, observa-se também que há uma tendência ao paralelismo, o que pode
corroborar a idéia de contaminação pelo sal, pois sendo a concentração de NaCl a
mesma para todas as soluções, o "acréscimo" inerente à contaminação também é o
mesmo. Porém, apesar disso, verifica-se que há a tendência linear. Sendo assim,
optou-se por realizar a descontaminação dessa solução de NaCl antes do preparo
das soluções salinas para a pré-concentração.
4.4 DESCONTAMINAÇÃO DA SOLUÇÃO SALINA DE NaCl 3,5% (m/v)
A partir dos resultados obtidos no item acima, foi realizada a limpeza da
solução de NaCl 3,5% m/v, de acordo com procedimento descrito no item 3.1. Após
esta limpeza o experimento do item anterior foi novamente realizado, esperando se
126
obter melhores resultados. Para tal, realizou-se o procedimento de pré-concentração
em soluções de concentração variando entre 0 e 10 μg L-1 (0; 1,0; 2,5; 5,0; 10,0 μg
L-1) em meio de água ultrapura e em meio de solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100®
10% m/v. A curva sem pré-concentração foi realizada em meio de HNO3 2% v/v. Os
resultados são apresentados nas Figuras 40 a 44.
A int
1,4
sem PC
PC H2O - 1
1,2
PC H2O - 2
PC NaCl 3,5% m/v - 1
1,0
PC NaCl 3,5% m/v - 2
0,8
0,6
0,4
0,2
0,0
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 40: Curvas de PC para Co em meio de água ultrapura e solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
127
A int 0,9
sem PC
0,8
PC H2O - 1
PC H2O - 2
0,7
PC NaCl 3,5% m/v - 1
0,6
PC NaCl 3,5% m/v - 2
0,5
0,4
0,3
0,2
0,1
0,0
0,0
2,5
5,0
7,5
[Cu] nominal (μg L-1) 10,0
Figura 41: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int 2,0
sem PC
1,8
PC H2O - 1
PC H2O - 2
1,6
PC NaCl 3,% m/v - 1
1,4
PC NaCl 3,% m/v - 2
1,2
1,0
0,8
0,6
0,4
0,2
0,0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 42: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
128
A int
0,35
sem PC
PC H2O - 1
0,30
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,25
PC NaCl 3,5% m/v - 2
0,20
0,15
0,10
0,05
0,00
0,0
2,5
5,0
7,5
[Ni] nominal (μg L-1)
10,0
Figura 43: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int 0,6
sem PC
PC H2O - 2
0,5
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,4
PC NaCl 3,5% m/v - 2
0,3
0,2
0,1
0,0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 44: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl 3,5% m/v
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
Quantitativamente, Tabela 15 apresenta os valores de absorvância
integrada para os "brancos" (soluções de concentração nominal igual a 0 μg L-1). Os
valores são as médias das absorvâncias individuais de medida, realizadas em
duplicata. Cada um deles representa um experimento individual.
129
Tabela 15: Valores de absorvância integrada para os brancos
(experimentos individuais) com PC em solução de NaCl 3,5 % m/v,
antes e depois da descontaminação do sal. Média (n = 3) das
absorvâncias integradas individuais.
PC em NaCl 3,5% m/v
Elemento
Antes da limpeza do sal
Após da limpeza do sal
A int 1
A int 2
A int 1
A int 2
Co
0,01298
0,01011
0,01844
0,01077
Cu
0,06882
0,07310
0,26591
0,07789
Mn
0,12622
0,13648
0,22098
0,15875
Ni
0,01653
0,02082
0,02706
0,01515
Pb
0,11585
0,11401
0,05924
0,04680
Através dos resultados obtidos nesta etapa, observa-se que dentre todos os
elementos em estudo, o Pb é aquele que é mais afetado pela contaminação do sal,
visto que limpeza da solução salina melhorou consideravelmente os valores de
absorvância dos brancos. Para os outros elementos, não se observou nenhuma
variação expressiva. No caso do Mn, isso remete à necessidade de identificar outra
fonte de contaminação (uma possibilidade seria a resina Chelex-100®), devido ao
fato de seus valores para brancos continuarem bastante elevados apesar da limpeza
do sal.
4.5 EFEITO DA QUANTIDADE DE RESINA CHELEX-100®
A fim de avaliar a influência da massa de resina na eficiência do procedimento
de pré-concentração, foi feito um experimento variando o volume de suspensão de
resina adicionado. Para tal, realizou-se o procedimento de pré-concentração em
soluções de concentração variando entre 0 e 10 μg L-1 (0; 1,0; 2,5; 5,0; 10,0 μg L-1)
em meio de água ultrapura e em meio de solução de NaCl 3,5% m/v previamente
descontaminada, com o volume de suspensão de Chelex-100® 10% m/v variando
130
entre 100 µL, 200 µL e 500 µL. A curva sem pré-concentração foi feita em meio de
HNO3 2% v/v. Os experimentos foram realizados em duplicada a fim de se avaliar
também a precisão dos resultados.
4.5.1 Efeito da massa de resina nos sinais de cobalto
Os resultados para o efeito da variação da massa da resina para a PC na
determinação de cobalto são apresentados nas Figuras 45 a 47.
A int 1,4
100 μL
sem PC
PC H2O - 1
1,2
PC H2O - 2
PC NaCl 3,5% m/v - 1
1
PC NaCl 3,5% m/v - 2
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 45: Curvas de PC para Co em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10% m/v.
131
A int
200 μL
1,4
sem PC
PC H2O - 1
1,2
PC H2O - 2
PC NaCl 3,5% m/v - 1
1
PC NaCl 3,5% m/v - 2
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 46: Curvas de PC para Co em meio de água ultrapura e solução de NaCl 3,5%
m/v, previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100®
10% m/v.
A int
1,4
500 μL
Série1
1,2
PC H2O - 1
PC H2O - 2
1
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 47: Curvas de PC para Co em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 500 µL de suspensão de Chelex-100® 10% m/v.
Observa-se para o Co que apesar de os valores individuais não serem
diferentes nos três experimentos, no conjunto, há uma maior repetitividade das
absorvâncias quando uma quantidade maior de resina (500 µL) é utilizada.
132
4.5.2 Efeito da massa de resina nos sinais de cobre
Os resultados para o efeito da variação da massa da resina para a PC na
determinação de cobre são apresentados nas Figuras 48, 49 e 50.
A int 1,2
100 μL
sem PC
1,0
PC H2O - 1
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,8
PC NaCl 3,5% m/v - 2
0,6
0,4
0,2
0,0
0,0
2,5
5,0
7,5
10,0
[Cu] nominal (μg L-1)
Figura 48: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10% m/v.
133
A int 1,2
200 μL
sem PC
1
PC H2O - 1
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,8
PC NaCl 3,5% m/v - 2
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Cu] nominal (μg
L-1)
Figura 49: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int 1,2
500 μL
Série1
1
PC H2O - 1
PC H2O - 2
PC NaCl 3,5% m/v - 1
0,8
PC NaCl 3,5% m/v - 2
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Cu] nominal (μg L-1)
Figura 50: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 500 µL de suspensão de Chelex-100® 10% m/v.
Observa-se para o cobre que apesar de os valores de absorvância não
serem diferentes nos três experimentos, no geral, verifica-se visualmente que há
134
uma maior repetibilidade dos sinais quando a maior quantidade de resina (500 µL)
é adicionada.
4.5.3 Efeito da massa de resina nos sinais de manganês
Os resultados para o efeito da variação da massa da resina para a PC na
determinação de manganês são apresentados nas Figuras 51 a 53.
A int 2
1,8
100 μL
sem PC
PC H2O - 1
1,6
PC H2O - 2
PC NaCl 3,5% m/v 1
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 51: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10%
m/v.
135
A int
2
200 μL
sem PC
1,8
PC H2O - 1
1,6
PC H2O - 2
PC NaCl 3,5% m/v 1
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 52: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5%
m/v, previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100®
10% m/v.
A int 2
500 μL
sem PC
1,8
PC H2O - 1
PC H2O - 2
1,6
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 53: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 500 µL de suspensão de Chelex-100® 10%
m/v.
136
Observa-se para o manganês que mesmo sendo os valores de
absorvância muito próximos, há uma maior repetibilidade dos sinais quando a
maior quantidade de resina (500 µL) é adicionada, princialmente para os pontos
de concentrações mais baixas, como 1 e 2,5 μg L -1, independente da linearidade
dos pontos.
4.5.4 Efeito da massa de resina nos sinais de níquel
Os resultados para o efeito da variação da massa da resina para a PC na
determinação de manganês são apresentados nas Figuras 54, 55 e 56.
A int 0,3
100 μL
sem PC
PC H2O - 1
0,25
PC H2O - 2
PC NaCl 3,5 % m/v - 1
PC NaCl 3,5 % m/v - 2
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Ni] nominal (μg L-1)
Figura 54: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10% m/v.
137
0,3
A int
200 μL
0,25
sem PC
PC H2O - 1
PC H2O - 2
0,2
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Ni] nominal (μg L-1)
Figura 55: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int
0,3
500 μL
sem PC
0,25
PC H2O - 1
PC H2O - 2
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
[Ni] nominal (μg L-1)
10,0
Figura 56: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 500 µL de suspensão de Chelex-100® 10% m/v.
138
Para o níquel, os resultados mostram o aumento da massa de resina não
afeta os sinais de absorvância, de onde se conclui que, no caso deste elemento, a
menor massa de resina é sufciente para a obtenção de resultados satisfatórios.
4.5.5 Efeito da massa de resina nos sinais de chumbo
Os resultados para o efeito da variação da massa da resina para a PC na
determinação de chumbo são apresentados nas Figuras 57, 58 e 59.
A int
0,5
sem PC
100uL
PC H2O - 1
0,45
PC H2O - 2
PC NaCl 3,5 % m/v - 1
0,4
PC NaCl 3,5 % m/v - 2
0,35
0,3
0,25
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg
L-1)
Figura 57: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10% m/v.
139
A int 0,5
200uL
sem PC
0,45
PC H2O - 1
0,4
PC H2O - 2
PC NaCl 3,5 % m/v - 1
0,35
PC NaCl 3,5 % m/v - 2
0,3
0,25
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 58: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 200 µL de suspensão de Chelex-100® 10% m/v.
A int 0,5
500uL
0,45
sem PC
0,4
PC H2O (1)
PC H2O (2)
0,35
PCNaCl (1)
0,3
PC NaCl (2)
0,25
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 59: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 500 µL de suspensão de Chelex-100® 10% m/v.
Da mesma forma que para o Ni, os resultados para Pb mostram o aumento
da massa de resina também não afeta consideravelmente os sinais de
140
absorvância, concluindo-se que, também para este elemento, a menor massa de
resina é sufciente para a obtenção de resultados satisfatórios.
Sendo assim, devido à melhoria dos resultados para Co e Cu, a pouca
influência nos resultados de Mn e a ausência de influência nos resultados de Ni e
Pb, o volume de 500 µL de suspensão de Chelex-100® 10% v/v foi escolhido para
os experimentos seguintes, afim de atender às necessidades dos dois primeiros
elementos.
4.6 DESCONTAMINAÇÃO DA RESINA CHELEX-100® E O EFEITO NOS SINAIS
PARA Mn
Através dos resultados obtidos nos itens 4.4 e 4.5 que, apesar da
descontaminação da solução salina, os sinais dos brancos para Mn se mantêm
bastante altos. Haja vista que o sal pode não ser a única fonte de contaminação,
procedeu-se a limpeza da resina a fim de se remover possível contaminação
responsável por essa absorvância elevada, e consequentemente, melhorar os
resultados. Para tal, realizou o procedimento de limpeza com solução de HNO 3,
como já descrito no item 3.1. Esse procedimento, além de remover as impurezas,
converte a resina da sua forma Na+ à forma H+, mais indicada para os experimentos
de PC. Os resultados para esta etapa são apresentados nas Figuras 60, 61 e 62.
141
A int 2
100 μL
sem PC
1,8
PC com H2O - 1
PC com H2O - 2
1,6
PC NaCl 3,5% m/v
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 60: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminada, com adição de 100 µL de suspensão de Chelex-100® 10% m/v,
também descontaminada.
A int 2
200 μL
sem PC
1,8
PC H2O - 1
1,6
PC NaCl 3,5% m/v
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 61: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminadas, com adição de 200 µL de suspensão de Chelex-100® 10%
m/v, também descontaminada.
.
142
A int
2
500 μL
1,8
sem PC
PC H2O - 1
1,6
PC H2O - 2
1,4
PC NaCl 3,5% m/v - 1
PC NaCl 3,5% m/v - 2
1,2
1
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Mn] nominal (μg L-1)
Figura 62: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl 3,5% m/v,
previamente descontaminadas, com adição de 500 µL de suspensão de Chelex-100® 10%
m/v, também descontaminada.
Quantitativamente, Tabela 16 apresenta os valores de absorvância
integrada para os "brancos" antes e depois da limpeza da resina (soluções de
concentração nominal igual a 0 μg L-1). Os valores são as médias das absorvâncias
integradas individuais de medida, realizadas em duplicata. Cada um deles
representa um experimento individual.
143
Tabela 16: Valores de absorvância integrada para os brancos (experimentos
individuais) com PC em água ultrapura e em solução de NaCl 3,5 % m/v
descontaminada, antes e depois da limpeza da resina Chelex-100®. Média (n = 3)
das absorvâncias integradas individuais.
PC em água ultrapura
PC em NaCl 3,5% m/v descontaminado
Volume de
suspensão de
Antes da limpeza
Após da limpeza da
Antes da limpeza da
Após da limpeza da
Chelex-100®
da Chelex-100®
Chelex-100®
Chelex-100®
Chelex-100®
(μL)
A int 1
A int 2
A int 1
A int 2
A int 1
A int 2
A int 1
A int 2
100
0,23621
0,57250
0,09090
0,03715
0,33497
0,34286
0,03348
-
200
0,46792
0,45533
0,01578
-
0,43965
0,44113
0,0375
0,09912
500
0,03077
0,01638
0,01645
0,01574
0,05938
0,32848
0,03898
0,15336
Com os resultados apresentados anteriormente, observa-se que os sinais
dos brancos foram parcialmente reduzidos, porém, ainda distante do ideal. Também
se observa novamente a ausência da linearidade das curvas para Mn.
4.7 EFEITO DO TEOR DE SALINIDADE
A fim de avaliar se a diferença de salinidade influencia na etapa de préconcentração e nos sinais de absorvância dos elementos estudados, realizou-se um
experimento variando a salinidade das soluções. A faixa de salinidade foi escolhida
a fim de contemplar as amostras de água produzida a serem analisadas ao fim da
otimização da metodologia. Para tal, realizou-se o procedimento de préconcentração em soluções de concentração variando entre 0 e 10 μg L-1 (0; 1,0; 2,5;
5,0; 10,0 μg L-1) em meio de água ultrapura e em meio de solução de NaCl nas
concentrações de 1,75% m/v e 7,0% m/v (respectivamente, salinidades de 17,5 e
70) , todas previamente descontaminadas, com adição de 500µL de suspensão da
Chelex-100® 10% m/v, também descontaminada em etapa anterior. A curva sem
pré-concentração foi feita em meio de HNO3 2% v/v. Os experimentos foram
144
realizados em duplicada e, a fim de se avaliar também a precisão dos resultados,
ambos os resultados são apresentados a seguir, nas Figuras 63 a 67.
A int
1,4
Sem PC
PC - H2O 1
1,2
PC - H2O 2
PC NaCl - 1,75%m/v (1)
PC NaCl - 1,75%m/v (2)
1
PC NaCl - 7%m/v (1)
PC NaCl - 7%m/v (2)
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Co] nominal (μg L-1)
Figura 63: Curvas de PC para Co em meio de água ultrapura e solução de NaCl de diferentes
salinidades, previamente descontaminadas, com adição de 500 µL de suspensão de Chelex100® 10% m/v, também descontaminada.
1,4
A int
Sem PC
PC - H2O 1
PC - H2O 2
1,2
PC NaCl - 1,75%m/v (1)
PC NaCl - 1,75%m/v (2)
1
PC NaCl - 7%m/v (1)
PC NaCl - 7%m/v (2)
0,8
0,6
0,4
0,2
0
0,0
2,5
5,0
7,5
10,0
[Cu] nominal (μg L-1)
Figura 64: Curvas de PC para Cu em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de suspensão
de Chelex-100® 10% m/v, também descontaminada.
145
A int
0,6
Sem PC
PC - H2O 1
PC - H2O 2
0,5
PC NaCl - 1,75%m/v (1)
PC NaCl - 1,75%m/v (2)
PC NaCl - 7%m/v (1)
0,4
PC NaCl - 7%m/v (2)
0,3
0,2
0,1
0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 65: Curvas de PC para Mn em meio de água ultrapura e solução de NaCl de
diferentes salinidades, previamente descontaminadas, com adição de 500 µL de suspensão
de Chelex-100® 10% m/v, também descontaminada.
A int
0,35
Sem PC
PC - H2O 1
PC - H2O 2
0,3
PC NaCl - 1,75%m/v (1)
PC NaCl - 1,75%m/v (2)
PC NaCl - 7%m/v (1)
0,25
PC NaCl - 7%m/v (2)
0,2
0,15
0,1
0,05
0
0,0
2,5
5,0
7,5
10,0
[Ni] nominal (μg L-1)
Figura 66: Curvas de PC para Ni em meio de água ultrapura e solução de NaCl de diferentes
salinidades, previamente descontaminadas, com adição de 500 µL de suspensão de Chelex100® 10% m/v, também descontaminada.
146
A int
0,6
Sem PC
PC - H2O 1
PC - H2O 2
0,5
PC NaCl - 1,75%m/v (1)
PC NaCl - 1,75%m/v (2)
PC NaCl - 7%m/v (1)
0,4
PC NaCl - 7%m/v (2)
0,3
0,2
0,1
0
0,0
2,5
5,0
7,5
10,0
[Pb] nominal (μg L-1)
Figura 67: Curvas de PC para Pb em meio de água ultrapura e solução de NaCl de diferentes
salinidades, previamente descontaminadas, com adição de 500 µL de suspensão de Chelex100® 10% m/v, também descontaminada.
De acordo com os resultados apresentados verifica-se que não há diferença
considerável entre os sinais de absorvância obtidos para as duas salinidades.
4.8 VERIFICAÇÃO DA ELIMINAÇÃO DA MATRIZ ATRAVÉS DOS ESPECTROS
TRIDIMENSIONAIS DO HR- CS GF AAS
Através das Figuras 69 a 72 pode-se verificar a diferença nos perfis dos
sinais para os cinco elementos estudados nos diferentes meios: em solução de
HNO3 2% v/v (sem pré-concentração), nos extratos de PC de soluções em água
ultrapura e de solução salina e na própria solução salina. Já as Figuras 73 a 78
apresentam os perfis tridimensionais para os sinais dos analitos nas amostras de
água produzida após o procedimento de pré-concentração.
147
Figura 68: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co nos
diferentes experimentos.
Figura 69: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Cu nos
diferentes experimentos.
148
Figura 70: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Mn nos
diferentes experimentos.
Figura 71: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Ni nos
diferentes experimentos.
149
Figura 72: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Pb nos
diferentes experimentos.
Figura 73: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu,
Ni e Pb para amostra AP 1 após o experimento de pré-concentração.
150
Figura 74: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu,
Mn, Ni e Pb para amostra AP 2 após o experimento de pré-concentração.
Figura 75: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu,
Mn, Ni e Pb para amostra AP 3 após o experimento de pré-concentração.
151
Figura 76: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu, Ni
e Pb para amostra AP 4 após o experimento de pré-concentração.
Figura 77: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu, Ni
e Pb para amostra AP 5 após o experimento de pré-concentração.
152
Figura 78: Espectro tridimensional para o registro gráfico dos sinais de absorvância para Co, Cu, Ni
e Pb para amostra AP 6 após o experimento de pré-concentração.
Observa-se claramente que o procedimento de pré-concentração elimina toda
a matriz da solução salina, permitindo a utilização deste procedimento para a
determinação do analito. Essa conclusão é de vital importância especialmente para
Co, Mn e Ni, em que a presença de NaCl é responsável por ruído intenso por conta
do alto espectro de fundo contínuo, precisa ser corrigido via software. Porém
independente dessa capacidade do software, não há como evitar o grande deposito
de sais no equipamento, especial e principalmente no atomizador.
4.9 DETERMINAÇÃO QUALITATIVA DO CLORETO RESIDUAL
Para a verificação da eficiência do procedimento de separação da matriz,
procedeu-se um ensaio analítico qualitativo que consistiu na identificação da
presença de cloreto nos extratos finais através da precipitação do mesmo na forma
de cloreto de prata, utilizando uma solução aquosa de AgNO 3. Nenhuma turvação foi
observada, de modo que se pode afirmar que a eliminação da matriz foi realizada
com sucesso.
153
4.10 CARACTERÍSTICAS ANALÍTICAS
Para a determinação das carctrísticas analíticas, realizou-se um experimento
de pré-concentração com soluções em meio de NaCl 3,5% m/v com as melhores
condições experimentais, definidas anteriormente.
Mediante o fato de que 10 μg L-1 pode ser uma concentração alta a ser préconcentrada, como no caso do Mn, em que claramente se observa o desvio da
linearidade (por ser determinado em um comprimento de onda bastante sensível),
optou-se por reduzir a faixa de concentrações, passando a se trabalhar portanto
entre 0 e 5 μg L-1.
As Figuras 79 a 83 apresentam as curvas de pré-concentração para os cinco
analitos de interesse.
A int 2,5
Sem PC
PC NaCl - 3,5% m/v
2
y = 0,415x + 0,0287
R² = 0,9964
1,5
1
y = 0,1289x + 0,0006
R² = 0,9996
0,5
0
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
[Co] nominal (μg L-1)
Figura 79: Curva de PC para Co em solução de NaCl 3,5% m/v nas condições otimizadas.
154
A int 1,2
Sem PC
PC NaCl 3,5% m/v
1
y = 0,1666x + 0,1599
R² = 0,999
0,8
0,6
y = 0,0475x + 0,0022
R² = 0,9983
0,4
0,2
0
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
[Cu] nominal (μg L-1)
Figura 80: Curva de PC para Cu em solução de NaCl 3,5% m/v nas condições otimizadas.
A int
1,6
Sem PC
PC NaCl 3,5% m/v
1,4
y = 0,2778x + 0,1142
R² = 0,9993
1,2
1,0
0,8
0,6
y = 0,0644x + 0,0104
R² = 0,9964
0,4
0,2
0,0
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
[Mn] nominal (μg L-1)
Figura 81: Curva de PC para Mn em solução de NaCl 3,5% m/v nas condições otimizadas.
155
A int
0,30
Sem PC
PC NaCl 3,5% m/v
0,25
y = 0,045x + 0,0285
R² = 0,9985
0,20
0,15
y = 0,013x + 0,0034
R² = 0,9978
0,10
0,05
0,00
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
[Ni] nominal (μg L-1)
Figura 82: Curva de PC para Ni em solução de NaCl 3,5% m/v nas condições otimizadas.
A int
0,4
Sem PC
PC NaCl 3,5% m/v
0,35
y = 0,0648x + 0,021
R² = 0,9993
0,3
0,25
0,2
0,15
y = 0,0188x + 0,0001
R² = 0,9955
0,1
0,05
0
0
0,5
1
1,5
2
2,5
3
3,5
4
4,5
5
[Pb] nominal (μg L-1)
Figura 83: Curva de PC para Pb em solução de NaCl 3,5% m/v nas condições otimizadas.
O método desenvolvido possibilita determinar Co, Cu, Mn, Ni e Pb em
amostras salinas com limites de detecção (LOD) e de quantificação (LOQ)
apresentados na Tabela 17, calculados de acordo com as recomendações da
156
IUPAC. A mesma também apresenta os fatores de pré-concentração tomando por
base 15 mL de amostra e volume final do extrato de 3,0 mL, além da repetibilidade
(%RSD, n = 10) em extratos de pré-concentração contendo inicialmente 2,0 μg L–1
em meio de NaCl 3,5% m/v.
Tabela 17: Características analíticas.
Fator de
Pré-Concentração
LOD
LOQ
Repetibilidade - 2 μg L–1
(μg L–1)
(μg L–1)
(%)
Co
3,2
0,006
0,020
3,5
Cu
3,5
0,070
0,24
4,0
Mn
4,3
0,024
0,08
9,0
Ni
3,5
0,074
0,25
5,3
Pb
3,5
0,018
0,06
5,9
Analito
A exatidão do método foi verificada por análise de diferentes materiais de
referência certificados: CASS-4 (Nearshore Seawater Reference Material for Trace
Metals), CASS-5 (Nearshore Seawater Reference Material for Trace Metals) e
NASS-5 (Seawater Reference Material for Trace Metals).
A Tabela 18 mostra os resultados obtidos na determinação de Cu, Mn e Ni
nos CRMs acima citados. Os outros elementos (Co e Pb) se apresentam em
concetrações extremamente baixas, não sendo portanto possíveis de serem
determinados. Para estes dois últimos, seria mais adequado o uso da técnica de
ICP-MS, que possui maior sensibilidade, podendo detectar concentrações a níveis e
partes por trilhão (ppt) e até partes por quatrilhão (ppq).
157
Tabela 18: Determinação de Cu, Mn e Ni nos materiais de referência certificados
de águas salinas.
CRM
Salinidade
CASS-4
CASS-5
NASS-5
Resultados (μg L–1)
Tipo de
dado
Cu
Mn
Ni
Obtido
0,62 ± 0,08
3,4 ± 0,3
0,30 ± 0,04
Certificado
0,592 ± 0,055
2,78 ± 0,19
0,314 ± 0,03
Obtido
0,39 ± 0,04
2,8 ± 0,4
0,41 ± 0,09
Certificado
0,380 ± 0,028
2,62 ± 0,20
0,330 ± 0,023
Obtido
0,31 ± 0,06
0,90 ± 0,06
0,32 ± 0,08
Certificado
0,297 ± 0,046
0,919 ± 0,057
0,253 ± 0,028
30,7
33,5
30,4
Assim, estes resultados demonstram que a metodologia proposta é eficiente
na determinação dos metais em estudo em amostras de águas salinas.
4.11 APLICAÇÃO A AMOSTRAS DE ÁGUA PRODUZIDA
A metodologia desenvolvida foi empregada na análise de amostras de água
produzida
de
plataformas
brasileiras
offshore
com
salinidade
aproximadamente 70. Os resultados são apresentados na Tabela 19.
de
até
158
Tabela 19: Determinação de Co, Cu, Mn, Ni e Pb em amostras de água de
produzida.
Resultados (μg L–1)
Amostra
Salinidade
Co
Cu
Mn
Ni
Pb
AP 1
68
< 0,020
0,26 ± 0,03
-
< 0,25
< 0,06
AP 2
75
< 0,020
0,27 ± 0,05
2,25 ± 0,09
0,5 ± 0,1
< 0,06
AP 3*
75
< 0,020
< 0,24
13 ± 2
< 0,25
0,18 ± 0,06
AP 4
72
< 0,020
< 0,24
-
< 0,25
0,32 ± 0,09
AP 5
52
< 0,020
0,28 ± 0,05
-
0,33 ± 0,09
0,20 ± 0,05
AP 6
52
< 0,020
< 0,24
-
< 0,25
< 0,06
(*) Amostra diluída na proporção de 1:5 para determinação de Mn.
A determinação de Mn foi realizada apenas nas amostras AP 2 e AP 3, pois
nas outras as concentrações se mostraram extremamente altas, não se tratando
portanto, de uma determinação de traços, podendo portanto serem determinadas
por técnicas analíticas alternativas como F AAS e/ou ICP OES.
4.12 ENSAIOS DE ADIÇÃO E RECUPERAÇÃO DE ANALITO
Com a finalidade de se garantir a maior confiabilidade possível dos
resultados obtidos, além da validação da metodologia utilizando três materiais de
referência certificados, realizaram-se também ensaios de adição e recuperação de
analito para algumas das amostras de água produzidas analisadas. Esses ensaios
foram realizados pois apesar de terem sido realizados experimentos para determinar
a salinidade máxima das amostras e existir similaridade entre as matrizes das
amostras e dos CRMs, ainda assim não houvree nenhum experimento para
verificação da acurácia que envolvesse as amostras.
Para tal, portanto, fez-se a adição de uma solução multielementar contendo
os cinco analitos de interesse tal-que a concentração final atingisse 2 μg L-1. Os
resultados são apresentados na Tabela 20.
159
Tabela 20: Resultados obtidos para ensaios de recuperação de Co, Cu, Mn, Ni
e Pb em amostras de água de produzida após adição de 2 μg L-1.
Recuperação (%)
Amostra
Salinidade
Co
Cu
Mn
Ni
Pb
AP 2
75
96 ± 10
100 ± 6
93 ± 10
79 ± 2
105 ± 5
AP 3*
75
97 ± 6
99 ± 6
105 ± 10
82 ± 4
83 ± 3
AP 4
72
101 ± 1
83 ± 8
-
81 ± 5
97 ± 5
(*) Amostra diluída na proporção de 1:5 para determinação de Mn.
160
5 CONCLUSÕES
Através do presente trabalho, foi possível estudar uma metodologia,
relativamente
simples,
para
pré-tratamento
e
posterior
análise
de
águas
hipersalinas, para a determinação de metais como Pb, Mn, Ni, Co e Cu, com o uso
da Espectrometria de Absorção Atômica de Alta Resolução com Fonte Contínua e
Forno de Grafite – HR-CS GF AAS.
Para superar os problemas relacionados à matriz salina das amostras, fez-se
uso da resina quelante Chelex-100®, bastante conhecida quando se trata de préconcentração de elementos-traço em amostras salinas.
Neste estudo pôde-se
verificar que a eficiência da Chelex-100® não foi excelente para pré-concentrar os
metais estudados, talvez devido às baixas concentrações utilizadas, mas se mostrou
eficaz em eliminar toda a matriz da amostra. Isto é importante, pois além da alta
concentração de sais presentes na matriz acarretar em interferências nos sinais
analíticos, o alto teor salino gera depósitos de sais em diversos pontos do sistema
de atomização do equipamento, podendo deteriorá-lo rapidamente. Neste trabalho
verificou-se que em soluções contendo concentrações de NaCl até 7 % (salinidade
de 70) não houve variação na retenção dos analitos quando comparada à soluções
aquosas não salinas (padrões aquosos).
A utilização de Chelex-100® em batelada evita os problemas encontrados
com a sua utilização em coluna, devido aos efeitos de inchamento da resina
(swelling) quando se modifica o meio reacional (neutro ou ligeiramente alcalino para
a pré-concentração e ácido na etapa de dessorção).
Os fatores de pré-concentração encontrados foram de 3,2 para Co; 3,5 para
Cu, Ni e Pb; e 4,3 para Mn, quando comparado ao valor teórico de 5 (15 mL de
amostra para 3 mL de extrato). Este fatores poderão ser melhorados com o aumento
do volume da amostra utilizada na análise.
Na determinação dos analitos por HR-CS GF AAS observou-se sinais
melhores definidos para Ni e Co utilizando atomização a partir da parede do tubo de
grafite, enquanto que, para os demais analitos (Pb, Mn e Cu), a utilização de
plataforma permitiu a atomização eficiente. Como a matriz final de análise é bem
simples (ácido nítrico 2 % usado para dessorver os analitos da resina) quando
161
comparada às amostras originais, não foi necessária a utilização de modificador
químico para as quantificações por HR-CS GF AAS, bastando-se utilizar as curvas
de pirólise e de atomização para o estabelecimento dos programas de temperatura.
Os limites de detecção e de quantificação encontrados (em g L-1), utilizando
todo o procedimento de pré-concentração foram de: 0,006 e 0,020; 0,070 e 0,24;
0,024 e 0,08; 0,074 e 0,25; e 0,018 e 0,060, para Co, Cu, Mn, Ni e Pb,
respectivamente.
Os resultados satisfatórios obtidos na análise de diferentes materiais de
referência certificados – CRMs, valida a metodologia desenvolvida e garante a
confiabilidade do seu uso na pré-concentração e determinação de Cu, Mn e Ni em
amostras salinas, dentre as quais amostras de água do mar.
As amostras de água produzida analisadas mostraram que, os teores dos
elementos-traço determinados não apenas se encontram dentro da faixa de
concentração observada mundialmente, como também satisfazem a legislação
brasileira vigente (CONAMA 357/05) para o descarte de efluentes em corpos
hídricos.
Dada a importância do conhecimento da composição das águas produzidas
de alta salinidade, o desenvolvimento de métodos analíticos ainda se faz necessário
visando auxiliar na caracterização dessas águas.
Deve-se mencionar que a
Resolução CONAMA 393/07, que trata do descarte de águas produzidas, está sendo
modificada para incluir novas espécies químicas que devem ser analisadas, entre
elas alguns metais, antes do seu descarte final. Assim, os métodos aqui
desenvolvidos podem se tornar ferramentas analíticas de importância na
caracterização destas águas e no estabelecimento de valores para apoiar as futuras
legislações.
Por fim, deve-se mencionar que a metodologia aqui proposta pode ser
aplicada e os analitos determinados em efluentes hídricos salinos, independente do
tipo de GF AAS (LS ou CS) disponível.
162
6 REFERÊNCIAS
AMIN, A. S. Study on the Solid Phase Extraction and Spectrophotometric
Determination of Cobalt with 5-(2-Benzothiazolylazo)-8-hydroxyquinolene. Arabian
Journal
of
Chemistry,
Article
in
Press,
Corrected
Proof,
2010.
doi:
10.1016/j.arabjc.2010.12.008.
AMORIM FILHO, V. R.; GOMES NETO, J. A. Evaluation of Lubricating Oil
Preparation Procedures for the Determination of Al, Ba, Mo, Si and V by HighResolution Continuum Source F AAS. Analytical Sciences, Tokyo, v. 25, p. 95-100,
2009.
ANDRADE, Vívian Tavares de.
Avaliação da toxicidade de água produzida
tratada por processo evaporativo com a finalidade de reúso em solo. Rio de
Janeiro, 2009. 144 f. Tese (Doutorado em Engenharia Qumica) - Programa de PósGraduação em Engenharia Química, Instituto Alberto Luiz Coimbra de PósGraduação e Pesquisa de Engenharia (COPPE), Universidade Federal do Rio de
Janeiro, Rio de Janeiro, 2009.
ARAUJO, R. G. O.; WELZ, B.; VIGNOLA, F.; BECKER-ROSS, H. Correction of
structured molecular background by means of high-resolution continuum source
electrothermal atomic absorption spectrometry - Determination of antimony in
sediment reference materials using direct solid sampling. Talanta, London, v. 80, p.
846–852, 2009.
ARAUJO, R. G. O.; WELZ, B.; CASTILHO, I. N. B.; VALE, M. G. R.; SMICHOWSKI,
P.; FERREIRA, S. L. C.; BECKER-ROSS, H. Determination of antimony in airborne
particulate matter collected on filters using direct solid sampling and high-resolution
continuum source graphite furnace atomic absorption spectrometry. Journal of
Analytical Atomic Spectrometry, London, v.25, p. 580-584, 2010.
AŞKUN, H.; GÜLBAKAN, B.; ÇELIKBIÇAK, Ö.; UZUN, C.; GÜVEN, O.; SALIH, B.
Preconcentration and matrix elimination for the determination of Pb(II), Ni(II) and
163
Co(II) by 8-hydroxyquinoline anchored poli(styrene-divinylbenzene) microbeads.
Journal of Applied Polymer Science, New York, v. 107, p. 2714-2722, 2007.
AZEREDO, L. C.; AZEREDO, M. A. A.; CURTIS, A. J. Utilização da 8hidroxiquinolina em técnicas de pré-concentração de íons metálicos em colunas.
Química Nova, São Paulo, v. 19, n. 4, p. 383-387, 1996.
BECKER, J. S. Trace and ultratrace analysis in liquids by atomic spectrometry.
Trends in Analytical Chemistry, Amsterdam, v. 24, p. 243-254, 2005
BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U. Observation, identification and
correction of structured molecular background by means of continuum source AASDetermination of selenium and arsenic in human urine. Journal of Analytical
Atomic Spectrometry, London, v. 15, p. 137-141, 2000.
BEZERRA, Magna Angélica dos Santos. Desenvolvimento de um destilador solar
para tratamento de águas de produção de petróleo com vistas a sua utilização
na agricultura e geração de vapor. Natal, 2004. 90 f. Dissertação (Mestrado em
Engenharia Química) - Programa de Pós-Graduação em Engenharia Química,
Departamento de Engenharia Química, Universidade Federal do Rio Grande do
Norte, Natal, 2004.
BEZERRA, Marcos de Almeida. Determinação de metais traço em efluentes de
refinaria, vegetais digeridos e vinhos por espectrometria atômica, após préconcentração por Extração no Ponto Nuvem e otimização multivariada.
Salvador, 2006. 139 f. Tese (Doutorado em Ciências - Química Analítica) - Programa
de Pós-Graduação em Química, Instituto de Química, Universidade Federal da
Bahia, Salvador, 2006a.
BEZERRA, M. A.; FERREIRA, S. L. S. Extração em Ponto nuvem: princípios e
aplicações em química analítica. Vitória da Conquista: Edições UESB, 2006b. 168 p.
BEZERRA, M. A.; CONCEIÇÃO, A. L. B.; FERREIRA, S. L. C. Development of preconcentration procedure using cloud point extraction for manganese determination in
164
saline effluents of petroleum refinery by flame atomic absorption spectrometry.
Microchimica Acta, Austria, v. 154, p. 149-152, 2006c.
BEZERRA, M. A.; MAÊDA, S. M. N.; OLIVEIRA, E. P.; CARVALHO, M. F. B.;
SANTELLI, R. E. Internal standardization for the determination of cadmium, cobalt,
chromium and manganese in saline produced water from petroleum industry by
inductively coupled plasma optical emission spectrometry after cloud point extraction.
Spectrochimica Acta Part B, Oxford, v. 62, p. 985–991, 2007.
BIANCHIN, L.; NADVORNY, D.; SILVA, A. F.; VALE, M. G. R.; SILVA, M. M.;
SANTOS, W. N. L.; FERREIRA, S. L. C.; WELZ, B.; HEITMANN , U. Feasibility of
employing permanent chemical modifiers for the determination of cadmium in coal
using slurry sampling electrothermal atomic absorption spectrometry. Microchemical
Journal, New York, v. 82, p. 174-182, 2006.
Bio-Rad. Chelex® 100 and Chelex 20 Chelating Ion Exchange Resin: Instruction
Manual, [200-].
BOESH, D. F.; RABALAIS. N. N. Long-term Environmental Effects of Offshore Oil
and Gas Development. London: Elsevier Applied Science, 1987. 708 p.
BOHRER, D.; HEITMANN, U.; HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.;
WELZ, B.; BERTAGNOLLI, D. Determination of aluminum in highly concentrated iron
samples: Study of interferences using high-resolution continuum source atomic
absorption spectrometry. Spectrochimica Acta Part B, Oxford, v. 62, p. 1012-1018,
2007.
BORGES, Daniel Lazaro Gallindo. Determinação de elementos traço em carvão
por Espectrometria de Absorção Atômica de Alta Resolução com Fonte
Contínua e por Espectrometria de Massa com Plasma Indutivamente Acoplado
e vaporização eletrotérmica. Florianópolis, 2005. 72 f. Dissertação (Mestrado em
Química) - Programa de Pós-Graduação em Química, Centro de Ciências Físicas e
Matemáticas, Universidade Federal de Santa Catarina, Florianópolis, 2005.
165
BORGES, Daniel Lazaro Gallindo. Análise direta de sólidos por espectrometria
de absorção atômica de alta resolução com fonte contínua e investigação de
compostos
organometálicos
por
análise
direta
em
tempo
real
com
espectrometria de massa. Florianópolis, 2009. 159 f. Tese (Doutorado em
Química) - Programa de Pós-Graduação em Química, Centro de Ciências Físicas e
Matemáticas, Universidade Federal de Santa Catarina, Florianópolis, 2009.
BORGES, D. L. G.; SILVA, A. F.; CURTIUS, A. J.; WELZ, B.; HEITMANN, U.
Determination of Lead in Coal Using Direct Solid Sampling and High-Resolution
Continuum
Source
Graphite
Furnace
Atomic
Absorption
Spectrometry.
Microchimimica Acta, Austria, v. 154, p. 101–107, 2006.
BORGES, D. L. G.; SILVA, A. F.; WELZ, B.; CURTIUS, A. J.; HEITMANN, U.
Determination of lead in biological samples by high-resolution continuum source
graphite furnace atomic absorption spectrometry with direct solid sampling. Journal
of Analytical Atomic Spectrometry, London, v. 21, p. 763-769, 2006.
BRANDÃO, G. C.; JESUS, R. M.; SILVA, E. G. P.; FERREIRA, S. L. C. Use of slurry
sampling for the direct determination of zinc in yogurt by high resolution-continuum
source flame atomic absorption spectrometry. Talanta, London, v. 81, p. 1357-1359,
2010.
BRICEÑO, J.; BELARRA, M. A.; DE SCHAMPHELAERE, K. A. C.; VANBLAERE, S.;
JANSSEN, C. R.; VANHAECKE, F.; RESANO, M. Direct determination of Zn in
individual Daphnia magna specimens by means of solid sampling high-resolution
continuum source graphite furnace atomic absorption spectrometry. Journal of
Analytical Atomic Spectrometry, London, v. 25, p. 503-510, 2010.
BROWN, R. J. C. ; MILTON, M. J. T. Analytical techniques for trace element
analysis: an overview. Trends in Analytical Chemistry, Amsterdam, v. 24, p. 266274, 2005.
CAMEL, V. Solid phase extraction of trace elements. Spectrochimica Acta Part B,
Oxford, v. 58, p. 1177–1233, 2003.
166
CEO, R. N.; KAZEROUNI, M. R.; RENGAN, K. Sorption of silver ions by Chelex-100
chelating resin. Journal of Radioanalytical and Nuclear Chemistry, Switzerland, v.
172, p. 43-48, 1993.
CEOTTO, Caio de Sousa. Comparação de técnicas analíticas para determinação
de elementos traço em soluções de amostras ambientais. Vitória, 2009. 43 f.
Trabalho de Conclusão de Curso (Graduação em Química) - Curso de Química,
Departamento de Química, Centro de Ciências Exatas, Universidade Federal do
Espírito Santo, Vitória, 2009.
CHEN, C. Y.; DANADURAI, K. S. K.; HUANG, S. D. Direct and simultaneous
determination of copper, manganese and molybdenum in seawater with a
multielement electrothermal atomic absortion spectrometer. Journal of Analytical
Atomic Spectrometry, London, v. 16, p. 404-408, 2001.
CHEN, X.-W.; HUANG, L.-L.; HE, R.-H. Silk fibroin as a sorbent for on-line extraction
and preconcentration of copper with detection by electrothermal atomic absorption
spectrometry. Talanta, London, v. 78, p. 71–75, 2009.
COLLINS, A. G. Geochemistry of Oilfield Water. New York: Elsevier Scientific
Publ., 1975.
CONAMA (Conselho Nacional de Meio Ambiente, Brasil). Resolução CONAMA nº
357. Dispõe sobre a classificação dos corpos de água e diretrizes ambientais para o
seu enquadramento, bem como estabelece as condições e padrões de lançamento
de efluentes, e dá outras providências. 2005. 27 p.
CONAMA (Conselho Nacional de Meio Ambiente, Brasil). Resolução CONAMA nº
393. Dispõe sobre o descarte contínuo de água de processo ou de produção em
plataformas marítimas de petróleo e gás natural, e dá outras providências. 2007. 3 p.
DAMIN, I. C. F.; VALE, M. G. R.; SILVA, M. M.; WELZ, B.; LEPRI, F. G.; SANTOS
W. N. L.; FERREIRA, S. L. C. Palladium as chemical modifier for the stabilization of
167
volatile nickel and vanadium compounds in crude oil using graphite furnace atomic
absorption spectrometry. Journal of Analytical Atomic Spectrometry, London, v.
20, p. 1332-1336, 2005.
DESSUY, Morgana Bazzan. Investigação do comportamento de modificadores
químicos para fósforo em forno de grafite usando espectrometria de absorção
atômica de fonte de linha e fonte contínua de alta resolução. Porto Alegre, 2007.
88 f. Dissertação (Mestrado em Química) - Programa de Pós-Graduação em
Química, Instituto de Química, Universidade Federal do Rio Grande do Sul, Porto
Alegre, 2007.
DESSUY, M. B.; VALE, M. G. R.; LEPRI, F. G.; WELZ, B.; HEITMANN, U.
Investigation of phosphorus atomization using high-resolution continuum source
electrothermal atomic absorption spectrometry. Spectrochimica Acta Part B,
Oxford, v. 62, p. 429–434, 2007.
DESSUY, M. B.; VALE, M. G. R.; LEPRI, F. G.; BORGES, D. L. G.; WELZ, B.;
SILVA, M. M.; HEITMANN, U. Investigation of artifacts caused by deuterium
background correction in the determination of phosphorus by electrothermal
atomization using high-resolution continuum source atomic absorption spectrometry.
Spectrochimica Acta Part B, Oxford, v. 63, p. 337-348, 2008.
DITTERT, I. M.; SILVA, J. S. A.; ARAUJO, R. G. O.; CURTIS, A. J.; WELZ, B.;
BECKER-ROSS, H. Direct and simultaneous determination of Cr and Fe in crude oil
using high-resolution continuum source graphite furnace atomic absorption
spectrometry. Spectrochimica Acta Part B, Oxford, v. 64 p., 537–543, 2009.
DITTERT, I. M.; SILVA, J. S. A.; ARAUJO, R. G. O.; CURTIS, A. J.; WELZ, B.;
BECKER-ROSS, H. Simultaneous determination of cobalt and vanadium in undiluted
crude oil using high-resolution continuum source graphite furnace atomic absorption
spectrometry. Journal of Analytical Atomic Spectrometry, London, v.25, p. 590595, 2010.
DOJOZAN, D.; POURNAGHI-AZAR, M. H.; TOUTOUNCHI-ASR, J. Preconcentration
168
of trace uranium from seawater with solid phase extraction followed by differential
pulse polarographic determination in chloroform eluate. Talanta, London, v. 46, p.
123–128, 1998.
DÓREA, H. S.; BISPO, J. R. L.; ARAGÃO, K. A. S.; CUNHA, B. B.; NAVICKIENE, S.;
ALVES, J. P. H.; ROMÃO, L. P. C.; GARCIA, C. A. B. Analysis of BTEX, PAHs and
metals in the oilfield produced water in the State of Sergipe, Brazil. Microchemical
Journal, New York, v. 85, p. 234–238, 2007.
DONAT, J. R.; STATHAM, P. J.; BRULAND, K. W. An evaluation of a C-18 solid
phase extraction technique for isolating metal-organic complexes from central north
pacific ocean waters. Marine Chemistry, Amsterdam, v. 18, p. 85-99, 1986.
ERSÖZ, A.; SAY, R.; DENIZLI, A. Ni(II) ion-imprinted solid-phase extraction and
preconcentration in aqueous solutions by packed-bed column. Analytica Chimica
Acta, Amsterdam, v. 502, p. 91–97, 2004.
ESCALEIRA, L. A.; SANTELLI, R. E.; OLIVEIRA, E. P.; CARVALHO, M. F. B.;
BEZERRA, M. A. Preconcentration procedure for determining trace amounts of Ni,
Cd, Pb and Cu in high-salinity waters after cloud-point extraction. International
Journal of Environmental Analytical Chemistry, New York, v. 89, p. 515 - 527,
2008.
FANG, Z. Flow Injection Atomic Absorption Spectrometry. Inglaterra: John Wiley
& Sons Ltd., 1995. 306 p.
FARAJI, M.; YAMINIA, Y.; SHARIATI, S. Application of cotton as a solid phase
extraction sorbent for on-line preconcentration of copper in water samples prior to
inductively coupled plasma optical emission spectrometry determination. Journal of
Hazardous Materials, Amsterdam, v. 166, p. 1383–1388, 2009.
FARAJI, M.; YAMINI, Y.; SALEH, A.; REZAEE, M.; GHAMBARIAN, M.; HASSANI, R.
A nanoparticle-based solid-phase extraction procedure followed by flow injection
inductively coupled plasma-optical emission spectrometry to determine some heavy
169
metal ions in water samples. Analytica Chimica Acta, Amsterdam, v. 659, p. 172–
177, 2010.
FERREIRA, H. S.; LEPRI, F. G.; WELZ, B.; CARASEK, E.; HUANG, M.-D.
Determination of sulfur in biological samples using high-resolution molecular
absorption spectrometry in a graphite furnace with direct solid sampling. Journal of
Analytical Atomic Spectrometry, London, v. 25, p. 1039-1045, 2010.
FIGUEIREDO, Kyteria Sabina Lopes de. Estudo da água produzida em diferentes
zonas de produção de petróleo, utilizando a hidroquímica e a análise
estatística de parâmetros químicos. Natal, 2010. 123 f. Dissertação (Mestrado em
Química) - Programa de Pós-Graduação em Química, Departamento de Química,
Universidade Federal do Rio Grande do Norte, Natal, 2010.
FRITZ, J. S. Analytical Solid-Phase Extraction. EUA: WILEY-VCH, 1999. 209 p.
GABARDO, Irene Terezinha. Caracterização química e toxicológica da água
produzida descartada em plataformas de óleo e gás na costa brasileira e seu
comportamento dispersivo no mar. Natal, 2007. 250 f. Tese (Doutorado em
Química) - Programa de Pós-Graduação em Química, Centro de Ciências Exatas e
da Terra, Universidade Federal do Rio Grande do Norte, Natal, 2007.
GAO, Y.; OSHITA, K.; LEE, K.-H.; OSHIMA, M.; MOTOMIZU, S. Development of
column-pretreatment
chelating
resins
for
matrix
elimination/multi-element
determination by inductively coupled plasma – mass spectrometry. Analyst, London,
v. 127, p. 1713-1719, 2002.
GARCIA, M. F.; GARCIA, R. P.; GARCIA, N. B.; SANZ-MEDEL, A. On-line
preconcentration of inorganic mercury and methylmercury in sea-water by sorbentextraction and total mercury determination by cold vapour atomic absorption
spectrometry. Talanta, London, v. 41, p. 1833-1839, 1994.
GARCIA, R. Estado da arte da reinjeção de água produzida. Rio de Janeiro: [s.n.],
1996. 48 p. (Relatório parcial de projeto PETROBRÁS).
170
GARG, B. S.; SHARMA, R. K.; BHOJAK, N.; MITTAL, S. Chelating resins and their
applications in the analysis of trace metal ions. Microchemical Journal, New York,
v. 61, p. 94-114, 1999.
GHASEMI, J. B.; ZOLFONOUN, E. Simultaneous spectrophotometric determination
of trace amounts of uranium, thorium, and zirconium using the partial least squares
method after their preconcentration by α-benzoin oxime modified Amberlite XAD2000 resin. Talanta, London, v. 80, p. 1191–1197, 2010.
GINÉ, Maria Fernanda. Espectrometria de Emissão Atômica com Plasma
Acoplado Indutivamente ICP-AES. Piracicaba: CENA, 1998. 143 p.
GINÉ, Maria Fernanda. Espectrometria de massas com fonte de plasma (ICPMS). Piracicaba: CENA, 1999. (Série Didática, v. 4).
GLEISNER, H.; WELZ, B.; EINAX, J. W. Optimization of fluorine determination via
the molecular absorption of gallium mono-fluoride in a graphite furnace using a highresolution continuum source spectrometer. Spectrochimica Acta Part B, Oxford, v.
65, p. 864-869, 2010.
GLEISNER, H.; EINAX, J. W.; MORÉS, S.; WELZ, B.; CARASEK, E. A fast and
accurate method for the determination of total and soluble fluorine in toothpaste
using high-resolution graphite furnace molecular absorption spectrometry and its
comparison with established techniques. Journal of Pharmaceutical and
Biomedical Analysis, Amsterdam, v. 54, p. 1040-1046, 2011.
GOMES, Emiliano Almeida. Tratamento combinado da água produzida de
petróleo por eletroflotação e processo fenton. Aracaju, 2009. 95 f. Dissertação
(Mestrado em Engenharia de Processos) - Programa de Pós-Graduação em
Engenharia de Processos, Universidade Tiradentes, Aracaju, 2009.
171
GONZALVEZ, A.; ARMENTA, S.; CERVERA, M. L.; de la GUARDIA, M. Nonchromatographic speciation. Trends in Analytical Chemistry, Amsterdam, v. 29, p.
260-268, 2010.
GROTTI, M.; ABELMOSCHI, M. L.; SOGGIA, F.; FRACHE, R. Determination of trace
metals in sea-water by electrothermal atomic absorption spectrometry following solidphase extraction: quantification and residual matrix effects. Journal of Analytical
Atomic Spectrometry, London, v. 17, p. 46-51, 2002.
GUEDES, Lívia Ferreira de Melo. Separação em fase sólida para a determinação
de ânions por Cromatografia de Íons em amostras salinas, ambientais e da
indústria do petróleo. Niterói, 2010. 76 f. Dissertação (Mestrado em Geociências Geoquímica Ambiental) - Programa de Pós-Graduação em Geociências, Instituto de
Química, Universidade Federal Fluminense, Niterói, 2010.
HEITHMAR, E. M.; HINNERS, T. A.; ROWAN, J. T.; RIVIELLO, J. M. Minimization of
interferences in Inductively Coupled Plasma Mass Spectrometry using on-line
preconcentration. Analytical Chemistry, Washington, v. 62, p. 857-854, 1990.
HEITMANN, U.; BECKER-ROSS, H.; FLOREK, S.; HUANG, M.-D.; OKRUSS, M.
Determination of non-metals via molecular absorption using high resolution
continuum source absorption spectrometry and graphite furnace atomization.
Journal of Analytical Atomic Spectrometry, London, v. 21, p. 1314-1320, 2006.
HIEFTJE, G. M. Atomic absorption spectrometry - Has it gone or where is it going?
Journal of Analytical Atomic Spectrometry, London, v. 3, p. 117-122, 1989.
HILL, S. J. Inductively coupled plasma spectrometry and its applications.
England: Sheffield Academic Press, 1999. 370 p.
HUANG, Z.-Y.; CHEN, F.-R.; ZHUANG, Z.-X.; WANG, X.-R.; LEE, F. S. C. Trace
lead measurement and on-line removal of matrix interference in seawater by isotope
dilution coupled with flow injection and ICP-MS. Analytica Chimica Acta,
Amsterdam, v. 508, p. 239–245, 2004.
172
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
Direct determination of total sulfur in wine using a continuum-source atomicabsorption spectrometer and an air–acetylene flame. Analytical and Bioanalytical
Chemistry, Heidelberg, v. 382, p. 1877–1881, 2005.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
Determination of phosphorus by molecular absorption of phosphorus monoxide using
a high-resolution continuum source absorption spectrometer and an air–acetylene
flame. Journal of Analytical Atomic Spectrometry, London, v. 21, p. 338-345,
2006.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
Determination of sulfur by molecular absorption of carbon monosulfide using a highresolution continuum source absorption spectrometer and an air-acetylene flame.
Spectrochimica Acta Part B, Oxford, v. 61, p. 181–188, 2006.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
Determination of halogens via molecules in the air–acetylene flame using highresolution
continuum
source
absorption
spectrometry:
Part
I.
Fluorine.
Spectrochimica Acta Part B, Oxford, v. 61, p. 572–578, 2006.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
Determination of halogens via molecules in the air–acetylene flame using highresolution
continuum
source
absorption
spectrometry,
Part
II:
Chlorine.
Spectrochimica Acta Part B, Oxford, v. 61, p. 959–964, 2006.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
The influence of calcium and magnesium on the phosphorus monoxide molecular
absorption signal in the determination of phosphorus using a continuum source
absorption spectrometer and an air–acetylene flame. Journal of Analytical Atomic
Spectrometry, London, v. 21, p. 346-349, 2006.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.;
PATZ, C.-D. Determination of sulfur forms in wine including free and total sulfur
173
dioxide based on molecular absorption of carbon monosulfide in the air–acetylene
flame. Analytical and Bioanalytical Chemistry, Heidelberg, v. 390, p. 361-367,
2008.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; OKRUSS, M.
High-resolution continuum source electrothermal absorption spectrometry of AlBr and
CaBr for the determination of bromine. Spectrochimica Acta Part B, Oxford, v. 63,
p. 566-570, 2008.
HUANG, M.-D.; BECKER-ROSS, H.; FLOREK, S.; OKRUSS, M.; WELZ, B.;
MORÉS, S. Determination of iodine via the spectrumof bariummono-iodide using
high-resolution continuum source molecular absorption spectrometry in a graphite
furnace. Spectrochimica Acta Part B, Oxford, v. 64 p. 697–701, 2009.
JARVIS, K. E.; GRAY, A. L.; HOUK, R. S. Handbook of Inductively Coupled
Plasma Mass Spectrometry. New York: Blackie & Son Ltd., 1992.
JONG, J.; SCHOEMANN, V.; LANNUZEL, D.; TISON, J.-L.; MATTIELLI, N. Highaccuracy determination of iron in seawater by isotope dilution multiple collector
inductively coupled plasma mass spectrometry (ID-MC-ICP-MS) using nitrilotriacetic
acid chelating resin for pre-concentration and matrix separation. Analytica Chimica
Acta, Amsterfam, v. 623, p. 126–139, 2008.
KAGAYA, S.; MAEBA, E.; INOUE, Y.; KAMICHATANI, W.; KAJIWARA, T.; YANAI,
H.; SAITO, M.; TOHDA, K. A solid phase extraction using a chelate resin
immobilizing
carboxymethylated
pentaethylenehexamine
for
separation
and
preconcentration of trace elements in water samples. Talanta, London, v. 79, p. 146–
152, 2009.
KATARINA, R. K.; TAKAYANAGI, T.; OSHIMA, M.; MOTOMIZU, S. Sample
pretreatment using chitosan-based chelating resin for the determination of trace
metals in seawater samples by Inductively Coupled Plasma – Mass Spectrometry.
Analytical Sciences, Tokyo, v. 24, p. 1537-1544, 2008.
174
KOMJAROVA, I.; BLUST, R. Comparison of liquid–liquid extraction, solid-phase
extraction and co-precipitation preconcentration methods for the determination of
cadmium, copper, nickel, lead and zinc in seawater. Analytica Chimica Acta,
Amsterdam, v. 576, p. 221–228, 2006.
LANCASTER, H. L.; MARSHALL, G. D.; GONZALO, E. R.; RŮŽIČA, J.; CHRISTIAN,
G. D. Trace metal Atomic Absorption Spectrometry analysis utilizing sorbent
extraction on polymeric-based supports and renewable reagents. Analyst, London,
v. 119, p. 1459-1465, 1994.
LEPRI, Fábio Grandis. Espectrometria de absorção atômica de alta resolução
com fonte contínua como ferramenta analítica para o desenvolvimento de
método para determinação de níquel e Vanádio por espectrometria de
absorção atômica em forno de grafite em amostras de óleo cru. Florianópolis,
2005. 91 f. Dissertação (Mestrado em Química) - Programa de Pós-Graduação em
Química, Departamento de Química, Centro de Ciências Físicas e Matemáticas,
Universidade Federal de Santa Catarina, Florianópolis, 2005.
LEPRI, Fábio Grandis. Investigações sobre a determinação de enxofre em
materiais biológicos, estabilização, atomização e correção de fundo baseada
no efeito Zeeman para o fósforo e determinação de elementos traço em carvão
utilizando espectrometria de absorção atômica e molecular de alta resolução
com fonte contínua. Florianópolis, 2009. 131 f. Tese (Doutorado em Química) Programa de Pós-Graduação em Química, Departamento de Química, Centro de
Ciências Físicas e Matemáticas, Universidade Federal de Santa Catarina,
Florianópolis, 2009.
LEPRI, F. G.; DESSUY, M. B.; VALE, M. G. R.; BORGES, D. L. G.; WELZ, B.;
HEITMANN, U. Investigation of chemical modifiers for phosphorus in a graphite
furnace using high-resolution continuum source atomic absorption spectrometry.
Spectrochimica Acta Part B, Oxford, v. 61, p. 934–944, 2006.
LEPRI, F. G.; WELZ, B.; BORGES, D. L. G.; SILVA, A. F.; VALE, M. G. R.;
HEITMANN, U. Speciation analysis of volatile and non-volatile vanadium compounds
175
in Brazilian crude oils using high-resolution continuum source graphite furnace
atomic absorption spectrometry. Analytica Chimica Acta, Amsterdam, v. 558, p.
195–200, 2006.
LEPRI, F. G.; BORGES, D. L. G.; ARAUJO, R. G. O.; WELZ, B.; WENDLER, F.;
KRIEG, M.; BECKER-ROSS, H.
Determination of heavy metals in activated
charcoals and carbon black for Lyocell fiber production using direct solid sampling
high-resolution continuum source graphite furnace atomic absorption and inductively
coupled plasma optical emission spectrometry. Talanta, London, v. 81, p. 980-987,
2010.
LEPRI, F. G.; WELZ, B.; DESSUY, M. B.; VALE, M. G. R.; BOHRER, D.; LOOSVOLLEBREGT, M. T. C.; HUANG, M.-D.; BECKER-ROSS, H. Investigation of the
feasibility to use Zeeman-effect background correction for the graphite furnace
determination of phosphorus using high-resolution continuum source atomic
absorption spectrometry as a diagnostic tool. Spectrochimica Acta Part B, Oxford,
v. 65, p. 24-32, 2010.
L'VOV, B. V. The analytical use of atomic absorption spectra. Spectrochimica Acta,
London, v. 17, p. 761-770, 1961.
MADRAKIAN, T.; ZOLFIGOL, M. A.; SOLGI, M. Solid-phase extraction method for
preconcentration of trace amounts of some metal ions in environmental samples
using silica gel modified by 2,4,6-trimorpholino-1,3,5-triazin. Journal of Hazardous
Materials, Amsterdam, v. 160, p. 468–472, 2008.
MALLA, M. E.; ALVAREZ, M. B.; BATISTONI, D. A. Evaluation of sorption and
desorption characteristics of cadmium, lead and zinc on Amberlite IRC-718
iminodiacetate chelating ion exchanger. Talanta, London, v. 57, p. 277-287, 2002.
MANFRA, L.; MOLTEDO, G.; LAMBERTI, C. V.; MAGGI, C.; FINOIA, M. G.;
GIULIANI, S.; ONORATI, F.; GABELLINI, M.; DI MENTO, R.; CICERO, A. M. Metal
Content and Toxicity of Produced Formation Water (PFW): Study of the Possible
176
Effects of the Discharge on Marine Environment. Archives of Environmental
Contaminant and Toxicology, New York, v. 53, p. 183-190, 2007.
MASSMANN, H. Vergleich von Atomabsorption und Atonxlluoreszenz in der
Graphitkiivette. Spectrochimica Acta, London, v. 23B, p. 215-226, 1968.
MATUSIEWICZ, H.; KRAWCZYK, M. Sequential Multi-Element Determination of
Hydride-Forming Elements (As, Bi, Cd, In, Pb, Se, Te, Tl) by High-Resolution
Continuum Source Atom Trapping-Flame Atomic Absorption Spectrometry. Chem.
Anal. (Warsaw), v. 54, p. 949-974, 2009.
McLAREN, J. W.; LAM, J. W. H.; BERMAN, S. S.; AKATSUKA, K.; AZEREDO; M. A.
On-line Method for the Analysis of Sea-water for Trace Elements by Inductively
Coupled Plasma Mass Spectrometry. Journal of Analytical Atomic Spectrometry,
London, v. 8, p. 279-286, 1993.
McNAUGHT,
A.D.
WILKINSON,
A.
(Eds.).
Compendium
of
Chemical
Terminology. Genebra: IUPAC 2005.
MELO, Adriana Santana Queiroz. Métodos analticos para avaliação e controle de
vanádio e cobre em água de mar e efluentes de refinaria de petróleo. Salvador,
2003. 176 f. Tese (Doutorado em Ciências) - Programa de Pós-Graduação em
Química, Universidade Federal da Bahia, Salvador, 2003.
MILNE, A.; LANDING, W.; BIZIMIS, M.; MORTON, P. Determination of Mn, Fe, Co,
Ni, Cu, Zn, Cd and Pb in seawater using high resolution magnetic sector inductively
coupled mass spectrometry (HR-ICP-MS). Analytica Chimica Acta, Amsterdam, v.
665, p. 200–207, 2010.
NASCIMENTO, Lívia Melo do. O princípio constitucional da eficiência aplicado à
outorga e à cobrança da água produzida na exploração petrolífera. Natal, 2009.
216 f. Dissertação (Mestrado em Direito Constitucional) - Programa de PósGraduação em Direito - Centro de Ciências Sociais Aplicadas, Universidade Federal
do Rio Grande do Norte, Natal, 2010.
177
NATURE TECHNOLOGICAL SOLUTION. Introduction to produced water
treatment.
Disponivel
em:
<http://www.naturetechsolution.com/images/introduction_to_produced_water_treatm
ent.pdf>. Acesso em: 21/Dez/2010.
NICKSON, R. A.; HILL, S. J.; WORSFOLD, P. J. Behaviour of matrix cations (Ca2+,
K+, Mg2+ and Na+) during on-line preconcentration and atomic spectrometric
detection of trace metals in natural waters. Analytica Chimica Acta, Amsterdam, v.
35, p. 311-317, 1997.
NGEONTAE, W.; AEUNGMAITREPIROM, W.; TUNTULANI, T.; IMYIM, A. Highly
selective preconcentration of Cu(II) from seawater and water samples using
amidoamidoxime silica. Talanta, London, v. 78, p. 1004–1010, 2009.
NÖLTE, J. ICP Emission Spectrometry: A Pratical Guide. Weinheim: Willey-VCH,
2003. 267 p.
NUNES, L. S.; BARBOSA, J. T. P.; FERNANDES, A. P.; LEMOS, V. A.; SANTOS,
W. N. L.; KORN, M. G. A.; TEIXEIRA, L. S. G. Multi-element Determination of Cu, Fe,
Ni and Zn Content in Vegetable Oils Samples by High-Resolution Continuum Source
Atomic Absorption Spectrometry and Microemulsion Sample Preparation. Food
Chemistry,
article
in
press,
corrected
proof,
2011.
doi:
10.1016/j.foodchem.2010.12.147.
OGP. The International Association of Oil Gas Producers. Fate and effects of
naturally occurring substances in produced water on marine environment.
Report 364. February 2005. [s.l.]: OGP, 2005.
OLIVEIRA, Eliane Padua. Aplicação da Espectrometria de Absorção Atômica
com Forno de Grafite na determinação direta de manganês, chumbo e cromo
em águas de produção. Niterói, 2004. 107 f. Dissertação (Mestrado em
Geociências - Geoquímica Ambiental) - Departamento de Geoquímica, Instituto de
Química, Universidade Federal Fluminense, Niterói, 2004.
178
OLIVEIRA, E. P.; SANTELLI, R. E. Direct determination of lead in produced waters
from petroleum exploration by electrothermal atomic absorption spectrometry X-ray
fluorescence using Ir–W permanent modifier combined with hydrofluoric acid.
Analytica Chimica Acta, Amsterdam, v. 545, p. 85-91, 2005.
OLIVEIRA, E. P.; SANTELLI, R. E. Combined use of Pd and HF as chemical
modifiers for the determination of total chromium in produced waters from petroleum
exploration by ET AAS. Microchemical Journal, New York, v. 89, p. 116–122, 2008.
OLIVEIRA, R. C. G. de; OLIVEIRA, M. C. K. de. Remoção de contaminantes tóxicos
dos efluentes líquidos oriundos da atividade de produção de petróleo no mar;
Boletim Técnico PETROBRAS, v. 43, p. 29-136, 2000.
OLIVEIRA, S. R.; RAPOSO JR., J. R.; GOMES NETO, J. A. Fast sequential multilement determination of Ca, Mg, K, Cu, Fe, Mn and Zn for foliar diagnosis using highresolution continuum source flame atomic absorption spectrometry: Feasibility of
secondary lines, side pixel registration and least-squares background correction.
Spectrochimica Acta Part B, Oxford, v. 64, p. 593–596, 2009.
OLIVEIRA, S. R.; GOMES NETO, J. A.; NÓBREGA, J. A.; JONES, B. T.
Determination of macro- and micronutrients in plant leaves by high-resolution
continuum source flame atomic absorption spectrometry combining instrumental and
sample preparation strategies. Spectrochimica Acta Part B, Oxford, v. 65, p. 316320, 2010.
OTERO-ROMANÍ, J.; MOREDA-PIÑEIRO, A.; BERMEJO-BARRERA, P.; MARTINESTEBAN, A. Inductively coupled plasma–optical emission spectrometry/mass
spectrometry for the determination of Cu, Ni, Pb and Zn in seawater after ionic
imprinted polymer based solid phase extraction. Talanta, London, v. 79, p. 723–729,
2009.
PALEOLOGOS, E. K.; GIOKAS, D. L.; KARAYANNIS, M. I. Micelle-mediated
separation and cloud-point extraction. Trends in Analytical Chemistry, Amsterdam,
v. 24, p. 426-436, 2005.
179
PAULL, B.; FOULKLES, M.; JONES, P. High performance chelation ion
chromatographic determination of trace metals in coastal sea-water using dyeimpregnated resin. Analyst, London, v. 119, p. 937-941, 1994.
PIMENTEL, P. M.; ANJOS, M. J.; MELO, D. M. A.; MELO, M. A. F.; GONÇALVES
JÚNIOR, L. M.; SILVA JÚNIOR, C. N.; LOPES, R. T. Multi-elemental analysis of
produced water by synchrotron radiation total reflection X-ray fluorescence. Talanta,
London, v. 74, p. 1231–1235, 2008.
QUIAN, S.; ZHANG, S.; HUANG, Z.; XIAO, M.; HUANG, F. Preconcentration of ultratrace copper in water samples with nanometer-size TiO2 colloid and determination by
GFAAS with slurry sampling. Microchimica Acta, Austria, v. 166, p. 251-254, 2009.
QUÉTEL, C. R.; VASSILEVA, E.; PETROV, I.; CHAKAROVA, K.; HADJIIVANOV, K.
I. First results on Fe solid-phase extraction from coastal seawater using anatase
TiO2 nano-particles. Analytical and Bioanalytical Chemistry, Heidelberg, v. 396, p.
2349–2361, 2010.
RAHMI, D.; ZHU, Y.; FUJIMORI E.; UMEMURA, T.; HARAGUCHI, H. Multielement
determination of trace metals in seawater by ICP-MS with aid of down-sized chelating
rein-packed minicolumn for preconcentration. Talanta, London, v. 72, p. 600-606,
2007.
RAPOSO JÚNIOR, J. L.; OLIVEIRA, S. R.; CALDAS, N. M.; GOMES NETO, J. A.
Evaluation of alternate lines of Fe for sequential multi-element determination of Cu,
Fe, Mn and Zn in soil extracts by high-resolution continuum source flame atomic
absorption spectrometry. Analytica Chimica Acta, Amsterdam, v. 627, p. 198–202,
2008.
RAPOSO JÚNIOR, J. R.; OLIVEIRA, S. R.; NÓBREGA, J. A.; GOMES NETO , J. A.
Internal standardization and least-squares background correction in high-resolution
continuum source flame atomic absorption spectrometry to eliminate interferences on
180
determination of Pb in phosphoric acid. Spectrochimica Acta Part B, Oxford, v. 63,
p. 992–995, 2008.
REIS, B. F.; MIRANDA, C. E. S.; BACCAN, N. Pré-concentração empregando
extração fase líquida-fase sólida em sistemas de análise em fluxo com detecção
espectrométrica. Química Nova, São Paulo, v. 19, n.6, p. 623-635, 1996.
RESANO, M.; BRICEÑO, J.; BELARRA, M. A. Direct determination of Hg in polymers
by solid sampling-graphite furnace atomic absorption spectrometry - A comparison of
the
performance
of
line
source
and
continuum
source
instrumentation.
Spectrochimica Acta Part B, Oxford, v. 64 p. 520–529, 2009.
RESANO, M.; BRICEÑO, J.; BELARRA, M. A. Direct determination of phosphorus in
biological samples using a solid sampling-high resolution-continuum source
electrothermal spectrometer: comparison of atomic and molecular absorption
spectrometry. Journal of Analytical Atomic Spectrometry, London, v. 24, p. 13431354, 2009.
RESANO, M.; MOZAS, E.; CRESPO, C.; BRICEÑO, J.; MENOYO, J. C.; BELARRA,
M. A. Solid sampling high-resolution continuum source graphite furnace atomic
absorption spectrometry to monitor the biodistribution of gold nanoparticles in mice
tissue
after
intravenous
administration.
Journal
of
Analytical
Atomic
Spectrometry, London, v. 25, p. 1864-1873, 2010.
RIBEIRO, A. S.; VIEIRA, M. A.; SILVA, A. F.; BORGES, D. L. G.; WELZ, B.;
HEITMANN, U.; CURTIS, A. J. Determination of cobalt in biological samples by linesource and high-resolution continuum source graphite furnace atomic absorption
spectrometry using solid sampling or alkaline treatment. Spectrochimica Acta Part
B, Oxford, v. 60, p. 693-698, 2005.
RIBEIRO, Guilherme Araújo. Utilização do modelo aera-werf para a avaliação do
risco ecológico em ambientes aquáticos relacionados com atividades
petrolíferas. Vitória, 2008. 86 f. Trabalho de Conclusão de Curso (Graduação em
Engenharia Ambiental) - Departamento de Engenharia Ambiental, Universidade
181
Federal do Espírito Santo, Vitória, 2008.
ROCHA, A. A.; MIEKELEY, N.; BEZERRA, M. C. M.; KÜCHLER, I. V. An automated
system for preconcentration/matrix-removal followed by ICP-MS determination of
organic phosphorus in oil production water. Microchemical Journal, New York, v.
78, p. 65– 70, 2004.
ROCHA, A. A.; MIEKELEY, N.; SILVEIRA, C. L. P.; BEZERRA, M. C. M.
Determinação de fósforo orgânico em águas de produção petrolífera por ICP- AES e
ICPMS após pré-concentração em coluna de sílica-C18. Química Nova, São Paulo,
v. 21, p. 584-589, 1998.
ROCHA, A. A.; ROSA, K. R. S. A.; BEZERRA, M. C. M. Incrustração inorgânica na
produção de petróleo. In: SEMANA ACADÊMICA DE QUÍMICA, 20., 2007, Niterói.
Slide de apresentação. Niterói, RJ: Instituto de Química da UFF, 2007.
RODRIGUEZ, Monica Rebelo. Caracterização dos fluidos H2S e água em
reservatórios carbonáticos. Campinas, 1993. 166 f. Dissertação (Mestrado em
Geoengenharia de Petróleo) - Instituto de Geociências, Universidade Estadual de
Campinas, 1993.
SAMUELSON, O. Ion Exchange Separations in Analytical Chemistry. New York:
John Willey & Sons Inc., 1963. 474 p.
SANT’ANA, O. D.; CARVALHO, M. F. B.; SANTELLI, R. E. Selenium determination
by electrothermal atomic absorption spectrometry in petroleum refinery aqueous
streams containing volatile organic compounds. Microchemical Journal, New York,
v. 71, p. 21-28, 2002.
SANT’ANA, O. D.; SANTELLI, R. E. Determination of arsenic in petroleum refinery
streams by electrothermal atomic absorption spectrometry after multivariate
optimization based on Doehlert design. Spectrochimica Acta Part B, Oxford, v. 57,
p. 1967–1978, 2002.
182
SANTOS,
Lisia
espectrometria
Maria
de
Gobbo
absorção
dos.
Estudo
atômica
na
de
diferentes
determinação
técnicas
de
da
elementos
inorgânicos em matrizes de interesse sanitário. Rio de Janeiro, 2009. 145 f. Tese
(Doutorado em Vigilância Sanitária) - Programa de Pós-Graduação em Vigilância
Sanitária, Instituto Nacional de Controle de Qualidade em Saúde, Fundação
Oswaldo Cruz, Rio de Janeiro, 2009a.
SANTOS, L. M. G.; WELZ, B.; ARAUJO, R. G. O.; JACOB, S. C.; VALE, M. G. R.;
MARTENS, A.; MARTENS, I. B. G.; BECKER-ROSS, H. Simultaneous Determination
of Cd and Fe in Beans and Soil of Different Regions of Brazil Using High-Resolution
Continuum Source Graphite Furnace Atomic Absorption Spectrometry and Direct
Solid Sampling. Journal of Agricultural and Food Chemistry, Easton, v. 57, p.
10089–10094, 2009b.
SANTOS, L. M. G.; ARAUJO, R. G. O.; WELZ, B.; JACOB, S. C.; VALE, M. G. R.;
OKRUSS, M.; BECKER-ROSS, H. Simultaneous determination of Cd and Fe in
grain products using direct solid sampling and high-resolution continuum
source electrothermal atomic absorption spectrometry. Talanta, London, v.
78, p. 577-583, 2009.
SARAÇOĞLU, S.; ELÇI, L. Column solid-phase extraction with Chromosorb-102
resin and determination of trace elements in water and sediment samples by flame
atomic absorption spectrometry. Analytica Chimica Acta, Amsterdam, v. 452, p.
77–83, 2002.
SCHIOZER, D. J. Pesquisa na Área de Petróleo no Brasil. Revista ABCM
Engenharia, v. 10, p. 4-6, 2005.
SCHOLTEN, M. C. T.; KARMAN, C. C.; HUWER, S. Ecotoxicological risk
assessment related to chemicals and pollutants in off-shore oil production.
Toxicology Letters, Amsterdam, v. 112-113, p. 283-288, 2000.
SHOKROLAHI, A.; GHAEDI, M.; SHABANI, R.; MONTAZEROZOHORI, M.;
183
CHEHREH, F.; SOYLAK, M.; ALIPOUR, S. A preconcentration procedure for copper,
nickel and chromium ions in some food and environmental samples on modified
Diaion SP-850. Food and Chemical Toxicology, v. 48, p. 482–489, 2010.
SILVA, A. F.; BORGES, D. L. G.; WELZ, B.; VALE, M. G. R.; SILVA, M. M.;
KLASSEN, A.; HEITMANN, U. Method development for the determination of thallium
in coal using solid sampling graphite furnace atomic absorption spectrometry with
continuum source, high-resolution monochromator and CCD array detector.
Spectrochimica Acta Part B, Oxford, v. 59, p. 841-850, 2004.
SILVA, A. F.; BORGES, D. L. G.; LEPRI, F. G.; WELZ, B.; CURTIS, A. J;
HEITMANN, U. Determination of cadmium in coal using solid sampling graphite
furnace
high-resolution
continuum
source
atomic
absorption
spectrometry.
Analytical and Bioanalytical Chemistry, Heidelberg, v. 382, p. 1835-1841, 2005.
SILVA, A. F.; LEPRI, F. G.; BORGES, D. L. G.; WELZ, B.; CURTIUS, A. J.;
HEITMANN, U. Determination of mercury in biological samples using solid sampling
high-resolution continuum source electrothermal atomization atomic absorption
spectrometry with calibration against aqueous standards. Journal of Analytical
Atomic Spectrometry, London, v. 21, p. 1321-1326, 2006.
SILVA, F. V.; TREVIZAN, L. C.; SILVA, C. S.; NOGUEIRA, A. R. A; NÓBREGA, J.
A.; Evaluation of inductively coupled plasma optical emission spectrometers with
axially and radially viewed configurations. Spectrochimica Acta Part B, Oxford, v.
57, p. 1905-1913, 2002.
SILVA, M. M.; DAMIN, I. C. F.; VALE, M. G. R.; WELZ, B. Feasibility of using solid
sampling graphite furnace atomic absorption spectrometry for speciation analysis of
volatile and non-volatile compounds of nickel and vanadium in crude oil. . Talanta,
London, v. 77, p. 1877-1885, 2007.
SINGH, D. K.; MISHRA, S. Synthesis of a New Cu(II)-Ion Imprinted Polymer for Solid
Phase Extraction and Preconcentration of Cu(II). Chromatographia, New York, v.
70, p. 1539–1545, 2009.
184
SKINNER, C. D.; SALIN, E. D. Preconcentration and absorption of metal chelates
with analysis by direct sample insertion inductively coupled plasma atomic emission
spectrometry. Journal of Analytical Atomic Spectrometry, London, v. 18, p. 495500, 2003.
SKOOG, D. A. Princípios de Análise Instrumental. 8. ed. Porto Alegre: Bookman,
2006. 836 p.
SKOOG, D. A.; HOLLER, F. J.; NIEMAN, T. A. Princípios de Análise Instrumental.
Brasil: Bookman, 2002. 836 p.
SLAVIN, W.; MANNING, D. C.; CARNRICK, G. R. The stabilized temperature
platform furnace. Atomic Spectroscopy, Connecticut, v. 2, p. 137-145, 1981.
SOHRIN, Y.; URUSHIHARA, S.; NAKATSUKA, S.; KONO, T.; HIGO, E.; MINAMI, T.;
NORISUYE, K.; UMETANI, S. Multielemental Determination of GEOTRACES Key
Trace
Metals
in
Seawater
by
ICPMS
after
Preconcentration
Using
an
Ethylenediaminetriacetic Acid Chelating Resin. Analytical Chemistry, Washington,
v. 80, p. 6267–6273, 2008.
SOUSA, Magna Angélica dos Santos Bezerra. Estudo da viabilidade da destilação
solar para polimento de águas produzidas de petróleo. Natal, 2010. 133 f. Tese
(Doutorado em Engenharia Química) - Programa de Pós-Graduação em Engenharia
Química, Departamento de Engenharia Química, Universidade Federal do Rio
Grande do Norte, Natal, 2010.
SROGI, K. Developments in the Determination of Trace Elements by Atomic
Spectroscopic Techniques. Analytical Letters, Tokyo, v. 41, p. 677-724, 2008.
SU, N.; BRADSHAW, J. S.; ZHANG, X. X.; SONG, H.; SAVAGE, P. B.; XUE, G.;
KRAKOWIAK, G. E.; IZATT, R. M. Syntheses and metal ion complexation of novel 8hydroxyquinoline containing Diaza-18-crown-6 ligands and analogues. Journal of
Organic Chemistry, Washington, v. 64, p. 8855-8861, 1999.
185
SWAN, J. M.; NEFF, J. M; YOUNG, P. C. (Eds.). Environmental Implications of
Offshore Oil and Gas Development in Australia: The Findings of an Independent
Scientific Review. Sydney: Australian Petroleum Exploration Association, 1994. 696
p.
TAKAKU, Y.; HAYASHI, T.; OTA, I.; HASEGAWA, H.; UEDA, S. Determination of
trace levels of iron in a seawater sample using isotope dilution / inductively coupled
plasma mass spectrometry. Analytical Sciences, Tokyo, v. 20, p. 1025-1028, 2004.
TAVARES, Wilson Hermínio. Estudo dos impactos do descarte da água
produzida no entorno das plataformas maritimas de produção de Petróleo,
como ferramenta de gestão ambiental. Niterói, 2003. 76 f. Dissertação (Mestrado
em Sistemas de Gestão - Sistema de Gestão em Meio Ambiente) - Programa de
Pós-Graduação Sistemas de Gestão, Universidade Federal Fluminense, Niterói,
2003.
TEIXEIRA,
Heloisa
Maria
Fontenelle.
Desenvolvimento
e
aplicação
de
metodologias para caracterização multielementar de água conata em amostras
de petróleo. Rio de Janeiro, 2007. 234 f. Tese (Doutorado em Química) - Programa
de Pós-Graduação em Química, Departamento de Química, Pontifícia Universidade
Católica do Rio de Janeiro, Rio de Janeiro, 2007.
TIBBETTS, P. J. C.; BUCHANAN, I. T.; GAWEL, L. J.; LARGE, R. A comprehensive
determination of produced water composition. In: RAY, J. P.; ENGELHARDT, F. R.,
(Eds.). Produced Water. Technological/Environmental Issues and Solutions. New
York: Plenum Press, 1992 p. 97-112.
THOMAS, J. E. Fundamentos da Engenharia de Petróleo. 2. ed. Rio de Janeiro:
Editora Interciência, 2004. 271 p.
TOKMAN, N.; AKMAN, S.; OZCAN, M. Solid-phase extraction of bismuth, lead and
nickel from seawater using silica gel modified with 3- aminopropyltriethoxysilane filled
in a syringe prior to their determination by graphite furnace atomic absorption
spectrometry. Talanta, London, v. 59, p. 201-205, 2003.
186
TREVIZAN, L. C.; NÓBREGA, J. A. Inductively Coupled Plasma Optical Emission
Spectrometry with Axially Viewed Configuration: an Overview of Applications,
Journal of Brazilian Chemical Society, São Paulo, v. 18, p. 678-690, 2007.
TRUJILLO, I. S.; ALONSO, E. V.; CORDERO, M. T. S.; PAVÓN, J. M. C.; de
TORRES, A. G. On-line solid-phase chelation for the determination of six metals in
sea-water by inductively coupled plasma mass spectrometry. Journal of Analytical
Atomic Spectrometry, London, v. 25, p. 1063–1071, 2010.
TSAKOVSKI, S.; BENKHEDDA, K.; IVANOVA, E.; ADAMS, F. C. Comparative study
of
8-hydroxyquinoline
derivatives
as
chelating
reagents
for
flow
injection
preconcentration of cobalt in a knotted reactor. Analytica Chimica Acta,
Amsterdam, v. 453, p. 143-154, 2002.
UTVIK, T. I. R. Chemical characterisation of produced water from four offshore oil
production platforms in the North Sea. Chemosphere, Oxford, v. 39, p. 2593-2606,
1999.
VALE, M. G. R.; DAMIN, I. C .F.; KLASSEN, A.; SILVA, M. M.; WELZ, B.; SILVA, A.
F.; LEPRI, F. G.; BORGES, D. L. G.; HEITMANN, U. Method development for the
determination of nickel in petroleum using line-source and high-resolution continuumsource graphite furnace atomic absorption spectrometry. Microchemical Journal,
New York, v. 77, p. 131-140, 2004.
VASSILEVA, E.; FURUTA, N. Application of iminodiacetate chelating resin Muromac
A-1 in on-line preconcentration and Inductively Coupled Plasma Optical Emission
Spectrometry determination of trace elements in natural waters. Spectrochimica
Acta Part B, Oxford, v. 58, p. 1541-1552, 2003.
VERGUERÍA, S. F. J.; GODOY, J. M.; MIEKELEY, N. Environmental inpact in
sediments and seawater due to discharges of Ba, 226Ra, 228Ra, V, Ni e Pb by
produced water from de Bacia de Campos Oil Field Offshore Platforms.
Environmental Forensics, v. 3, p. 115-123, 2002.
187
VIGNOLA, F.; BORGES, D. L. G.; SILVA, A. F.; CURTIUS, A. J.; WELZ, B.;
BECKER-ROSS, H. Simultaneous determination of Cd and Fe in sewage sludge by
high-resolution continuum source electrothermal atomic absorption spectrometry with
slurry sampling. Microchemical Journal, New York, v. 95, p. 333–336, 2010.
VILLANUEVA-ALONSO, J.; PEÑA-VÁZQUEZ, E.; BERMEJO-BARRERA, P. Use of
high resolution continuum source atomic absorption spectrometry as a detector for
chemically generated noble and transition metal vapors. Spectrochimica Acta Part
B, Oxford, v. 64, p. 659–665, 2009.
WALSH, A. The application of atomic absorption spectra to chemical analysis.
Spectrochimica Acta, London, v. 7, p. 108-117, 1955.
WANG, X.; BARNES, R. Chelating Resins for on-line flow injection preconcentration
with Inductively Coupled Plasma Atomic Emission Spectrometry. Journal of
Analytical Atomic Spectrometry, London, v. 4, p. 509-518, 1989.
WANG, D.; SAÑUDO-WILHELMY, S. A. Development of an analytical protocol for
the determination of V (IV) and V (V) in seawater: Application to coastal
environments. Marine Chemistry, Amsterdam, v. 112, p. 72–80, 2008.
WARNKEN, K. W.; TANG, D.; GILL, G. A.; SANTSCHI, P. H. Performance
optimization of a commercially available iminodiacetate resin for the determination of
Mn, Ni, Cu, Cd and Pb by on-line preconcentration inductively coupled plasma-mass
spectrometry. Analytica Chimica Acta, Amsterdam, v. 423, p. 265-276, 2000.
WELLS, M.; BRULAND, K. W. An improved method for rapid preconcentration and
determination of bioactive trace metals in seawater using solid phase extraction and
high resolution inductively coupled plasma mass spectrometry. Marine Chemistry,
Amsterdam, v. 63, p. 145–153, 1998.
WELZ, B. Atomic Absorption Spectrometry. 2. ed. Weinheim: VCH Verlag, 1985.
506 p.
188
WELZ, B.; SPERLING, M. Atomic Absorption Spectrometry. 3. ed. Weinheim:
Wiley-VCH, 1999. 941 p.
WELZ, B.; VALE, M. G. R.; SILVA, M. M.; BECKER-ROSS, H.; HUANG, M.-D.;
FLOREK, S.; HEITMANN, U. Investigation of interferences in the determination of
thallium in marine sediment reference materials using high-resolution continuumsource
atomic
absorption
spectrometry
and
electrothermal
atomization.
Spectrochimica Acta Part B, Oxford, v. 57, p. 1043–1055, 2002.
WELZ, B.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U.; VALE, M. G. R. HighResolution Continuum-source Atomic Absorption Spectrometry – What Can We
Expect? Journal of Braziliam Chemical Society, São Paulo, v. 14, p. 220–229,
2003.
WELZ, B.; BECKER-ROSS, H.; FLOREK, S.; HEITMANN, U. High-Resolution
Continuum Source AAS: The Better way to do atomic absorption spectrometry.
New York: Wiley-VCH, 2005a.
WELZ, B. High-resolution continuum source AAS: the better way to perform atomic
absorption spectrometry. Analytical and Bioanalytical Chemistry, Heidelberg, v.
381, p. 69-71, 2005b.
WELZ, B.; MORÉS, S.; CARASEK, E.; VALE, M. G. R.; OKRUSS, M.; BECKERROSS, H. High-Resolution Continuum Source Atomic and Molecular Absorption
Spectrometry - A Review. Applied Spectroscopy Reviews, New York, v. 45, p. 327354, 2010a.
WELZ, B.; SANTOS, L. M. G.; ARAUJO, R. G. O.; JACOB, S. C.; VALE, M. G. R.;
OKRUSS, M.; BECKER-ROSS, H. Unusual calibration curves observed for iron using
high-resolution continuum source graphite furnace atomic absorption spectrometry.
Spectrochimica Acta Part B, Oxford, v. 65, p. 258-262, 2010b.
189
WILLIE, S. N.; TEKGUL, H.; STURGEON, R. Immobilization of 8-hydroxyquinoline
onto silicone tubbing for the determination of trace metals in sea water using flow
injection ICP-MS. Talanta, London, v. 47, p. 439-445, 1998.
WILLIE, S. N.; LAM, J. W. H.; YANG, L.; TAO, G. On-line removal of Ca, Na and Mg
from iminodiacetate resin for the determination of trace elements in seawater and fish
otoliths by flow injection ICP-MS. Analytica Chimica Acta, Amsterdam, v. 447, p.
143–152, 2001.
WILTSCHE, H.; PRATTES, K.; ZISCHKA, M.; KNAPP, G. Estimation of boron
isotope
ratios
using
high
resolution
continuum
source
atomic
absorption
spectrometry. Spectrochimica Acta Part B, Oxford, v. 64, p. 341–346, 2009.
WOODBERRY, P.; STEVENS, G.; SNAPE, I.; STARK, S. Removal of metal
contaminants from saline waters at low temperature by an iminodiacetic acid ionexchange resin, Thala Valley Tip, Casey Station, Antarctica. Solvent Extraction and
Ion Exchange, v. 23, p. 289–306, 2005.
YANG, L.; STURGEON, R. E. High accuracy and precision isotope dilution mass
spectrometry: An application to the determination of Mo in seawater. Journal of
Analytical Atomic Spectrometry, London, v. 24, p. 1327–1335, 2009.
YANG, L.; WILLIE, S.; STURGEON, R. E. Determination of total chromium in
seawater with isotope dilution sector field ICP-MS following on-line matrix separation.
Journal of Analytical Atomic Spectrometry, London, v. 24, p. 958–963, 2009.