EXERCÍCIO – V OU F
Uma amostra com massa de 308,5 mg contém ácido malônico (massa molecular
104,66 g mol-1), hidrogeno malonato de sódio (massa molecular 126,04 g mol-1) e
água. Para a titulação até o primeiro ponto final foram gastos 18,06 mL de NaOH
0,1000 mol L-1. Para atingir-se o segundo ponto final foi necessária a adição de
mais 25,14 mL do mesmo titulante. Essa amostra contém 61,3, 28,9 e 9,8% de
ácido malônico, hidrogeno malonato de sódio e água.
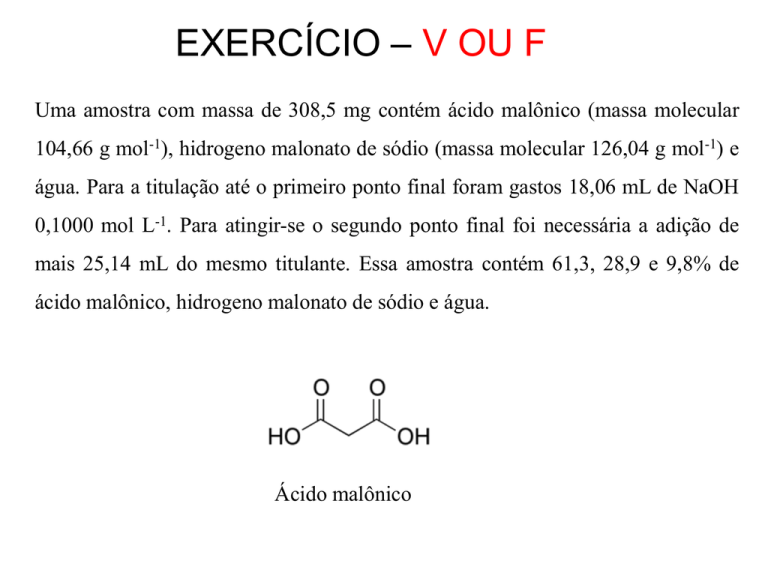
Ácido malônico
EXERCÍCIO – ALTERNATIVA
Um técnico em química recebeu para análise em laboratório uma amostra
contendo 0,1905 g de um metal bivalente desconhecido. Para prosseguimento
dessa análise, toda a massa desse metal foi dissolvida em 10,0 mL de H2SO4 0,500
mol L-1. O excesso do H2SO4 foi então titulado e neutralizado por 16,0 mL de
KOH 0,250 mol L-1. Qual foi o metal determinado pelo técnico em sua análise. Se
necessário utilize a tabela periódica.
a) Zn
b) Ni
c) Fe
d) Co
e) Cu
EXERCÍCIO
Uma amostra de atum enlatado, com massa igual a 0,992 g, foi analisada pelo
método Kjeldahl; foi requerido um volume igual a 22,66 mL de HCl 0,1224 mol
L-1 para titular a amônia liberada. Calcular a porcentagem de nitrogênio na
amostra.












