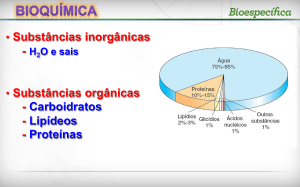
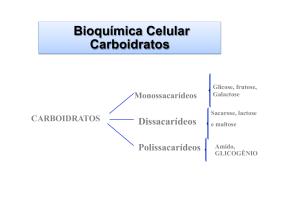
As glicoproteínas, os glicolipídeos e os glicosaminoglicanos contêm resíduos de
monossacarídeos. Alguns exemplos de glicoproteínas e glicolipídeos:
Metabolismos do
glicuronato, dos
aminoaçúcares, da galactose
e da frutose
cerebrosídeo
Porção oligossacarídica de uma
glicoproteína N-linked
C ou P
[email protected]
Departamento de Bioquímica da Faculdade de Medicina do Porto
A ligação entre a N-acetil-glicosamina e o grupo amida
da asparagina da proteína é glicosídica tipo N.
Espaço extracitoplasmático
C ou P
= ceramida ou proteína da membrana.
Nos exemplos, a ligação entre a glicose e
o grupo hidroxilo
1-da ceramida (nos glicolipídeos) e
2-da treonina ou da serina da proteína
(nas glicoproteínas O-linked)
é glicosídica tipo O.
As ligações entre as unidades
glicídicas do oligossacarídeo
componente das glicoproteínas e
glicolipídeos são glicosídicas de tipo
O.
2
Os glicosaminoglicanos (=mucopolissacarídeos) são cadeias lineares de unidades
dissacarídicas que se repetem. As unidades glicídicas ligam-se umas à outras através
de ligações glicosídicas de tipo O.
Exemplos de glicosaminoglicanos (e de um proteoglicano):
Nos glicolipídeos e nas glicoproteínas das membranas a cadeia oligossacarídica está
sempre no espaço extra-citoplasmático.
resíduos de ácido Nacetil-neuramínico
C ou P
C ou P
Espaço
citoplasmático
1- O ácido hialurónico contém milhares de unidades dissacarídicas
(→ ácido glicurónico → N-acetil-glicosamina →)
e não faz parte de proteoglicanos.
Gangliosídeo
resíduo de L-fucose
2- O sulfato de heparano contém dezenas de unidades dissacarídicas
(ácido glicurónico ou L-idurónico → N-acetil-glicosamina ou N-sulfil-glicosamina).
Alguns grupos hidroxilo estão esterificados com o sulfato.
Alguns grupos sulfato formam ligações sulfamida com o grupo amina da glicosamina (N-sulfil-glicosamina).
Glicoproteína
transmembranar
(N-linked)
É sempre um componente de proteoglicanos.
Glicoproteína transmembranar
(O-linked)
Os resíduos de ácido acetil-neuramínico e de L-fucose estão, tipicamente, nas extremidades
que estão em posição distal relativamente à ceramida ou à cadeia polipeptídica.
3
A cadeia polissacarídica liga-se à
parte proteica (resíduo de serina
ou treonina) através de uma
ponte trissacarídica
(→ Gal → Gal → Xilose →
hidroxilo de serina ou treonina).
4
Exemplos de substratos dadores de glicosil-transférases:
UDP-N-acetil-glicosamina
CMP-N-acetil-neuramínico
Na síntese das glicoproteínas, glicolipídeos e glicosaminoglicanos participam
glicosil-transférases (glycosyltransferases). “Glicosil-transférase” é um termo genérico...
Possíveis substratos dadores
de unidades glicídicas na
atividade das glicosiltransférases:
Substratos
aceitadores
UDP-glicose
UDP-N-acetil-glicosamina
UDP-galactose
UDP-N-acetil-galactosamina
UDP-glicurónico
UDP-xilose
GDP-manose
GDP-fucose
CMP-N-acetil-neuramínico
proteínas
ceramidas
difosfato
uridina
monossacarídeo ligado à proteína ou à ceramida
ou o oligossacarídeo em fase de elongação
UDP ou
GDP ou
CMP
(ribose +
uracilo)
glicose → aceitador
N-acetil-glicosamina → aceitador
galactose → aceitador
N-acetil-galactosamina → aceitador
glicurónico → aceitador
xilose → aceitador
manose → aceitador
fucose → aceitador
N-acetil-neuramínico → aceitador
citidina
(ribose +
citosina)
N-acetil-glicosamina
fosfato
GDP-fucose
difosfato
guanidina
(ribose +
guanina)
L-fucose
N-acetil-neuramínico
As glicosil-transférases podem ter denominações um pouco mais específicas como, por exemplo,
galactosil-transférases, glicuronil-transférases, xilosil-transférases, manosil-transférases, fucosiltransférases e sialil-transférases.
5
A ligação entre o resíduo glicídico e o fosfato é glicosídica de tipo O (envolve o carbono
anomérico do açúcar
que vai ser transferido). Na ação das glicosil-transférases
rompe-se esta ligação para se formar outra ligação glicídica de tipo O com o substrato aceitador.6
Na síntese das cadeias glicídicas, o produto de uma glicosil-transférase é o substrato aceitador
da glicosil-transférase que vai atuar a seguir.
O UDP-glicurónico forma-se a partir da glicose via glicose → glicose-6-P → UDP-
Sulfil-transférases atuam na cadeia em
elongação transferindo sulfato para hidroxilos
C4 ou C6 da N-acetil-galactosamina
Exemplo do processo de síntese do
sulfato de condroitina:
3-fosfoadenosil5-fosfosulfato
n UDP-glicurónico
Repetição alternada que forma sequência de
dissacarídeos (→GluA→GalNAc→)n
n UDP-N-acetilgalactosamina
glicose → UDP-glicurónico. A conversão UDP-glicose → UDP-glicurónico é catalisada
por uma desidrogénase dependente do NAD+ (que envolve 4 eletrões).
O UDP-glicurónico é substrato dador na ação de glicosil-transférases que atuam no processo de síntese de
glicosaminoglicanos e na formação de glicuro-conjugados de excreção urinária ou biliar.
UDP-N-acetilgalactosamina
2 NAD
+
UDP-glicose
UDP-glicurónico
UDP-galactose
UDP-xilose
UDP
UDP
UDP
Pirofosforílase
do UDPglicose
3-fosfoadenosil5-fosfato
UDP-galactose
UDP
UDP
ATP
proteína
ADP
glicose
UDP
Glicuroniltransférases
2 NADH
glicuronil-xenobiótico ou
glicuronil-bilirrubina
UDP-glicurónico
Desidrogénase do UDP-glicose
H2O
PPi
2 Pi
UTP
glicose-1-P
n UDP
Na síntese do sulfato de
condroitina também atuam
sulfil-transférases que
adicionam resíduos de sulfato
ao heteropolissacarídeo
oligossacarídeo de
glicosaminoglicano (n+1 resíduos)
oligossacarídeo de
glicosaminoglicano (n resíduos)
Mútase
glicose-6-P
Síntase do
UDP-xilose
CO2
UDP-xilose
proteína de
proteoglicano
Xilosiltransférase
xenobiótico ou
bilirrubina
UDP
Xilose ligada a resíduo serina
ou treonina da proteína de um
proteoglicano
Hexocínase
O UDP-xilose forma-se por descarboxilação do UDP-glicurónico. A xilose é o monossacarídeo que se liga
7
diretamente à serina (ou treonina) da proteína de proteoglicanos: a transferência de xilose para a proteína
aceitadora é o primeira reação no processo de síntese da maioria dos proteoglicanos.
8
O UDP-xilose é inibidor competitivo da desidrogénase de UDP-glicose.
O UDP-N-acetil-glicosamina e o UDP-N-acetil-galactosamina formam-se a
O CMP-N-acetil-neuramínico forma-se a partir da UDP-N-acetil-glicosamina.
partir da frutose-6-fosfato.
No processo consome-se fosfoenolpiruvato que é o dador de 3 dos carbonos constituintes do
ácido N-acetil-neuramínico.
A última etapa é a transferência de citidilato (CMP)
H2O
para o ácido N-acetil-neuramínico por ação de uma
Ganglicosídeo ou
pirofosforílase.
Glicoproteína com ácido
Aceitador (n+1 resíduos)
O dador
Glicosil-transférases
UDP
1-do grupo amina é a glutamina,
2-do acetilo, o acetil-CoA
UDP
Aceitador
(n resíduos)
siálico numa extremidade da
cadeia glicídica
UDP-N-acetil-galactosamina
Aceitador
(n resíduos glicídicos)
PPi
Pirofosforílase
UTP
ATP
N-acetil-neuramínico
CTP
Sialiltransférases
Hexocínase
N-acetil-glicosamina-1-P
ATP
Isomérase
Mútase
acetil-CoA
glutamina
frutose-6-P
glicosamina-6-P
Síntase da
glicosamina-6-P
glicose
N-acetil-glicosamina-6-P
ADP
Hexocínase
AcetilCoA
transférase
glutamato
N-acetil-neuramínico-9-P
fosforílase
N-acetil-manosamina-6-P
ADP
cínase
ATP
N-acetil-manosamina
hidrólase
UDP
H2O
UDP-N-acetil-manosamina
CMP-N-acetilneuramínico
CMP
glicose-6-P
Pi
Pirofosfosforílase
PPi
ADP
glicose
H2O
Pi
UDP-N-acetil-glicosamina
4-epimérase
3-e do uridilato, o UTP.
Neuraminidases
2-epimérase
glicose-6-P
glutamina + acetil-CoA + UTP
UDP-N-acetilglicosamina
frutose-6-P
glutamato + CoA + PPi
A enzima “marca-passo” da via metabólica é
a Síntase da glicosamina-6-fosfato que é
inibida pela UDP-N-acetil-glicosamina.
piruvato
fosfoenolpiruvato
9
O GDP-manose e o GDP-fucose formam-se a partir da frutose-6-fosfato.
Na conversão da frutose-6-fosfato em GDP-manose estão
ADP
ATP
envolvidas duas isomérases e uma pirofosforílase. O substrato
glicose
glicose-6-P
dador de guanilato (GMP) é o GTP.
Isomérase
Isomérase
Mútase
Na conversão
da GDPmanose em
GDP-fucose
estão
envolvidas uma
desidrátase e
uma redútase.
GDP-manose
H2O
Glicogénio (n+1 resíduos) 3- Quando se ingere
Manosiltransférases
Desidrátase
NADPH
Aceitador
(n resíduos)
NADP+
Glicogénio (n resíduos)
Aceitador
(n+1 resíduos)
GDP
Uridil-transférase da
galactose-1-fosfato
ADP
GTP
L-fucose-1-P
Pirofosforílase
Tipicamente, o resíduo de L-fucose fica situado numa extremidade da cadeia oligossacarídica, quase sempre
como resíduo único constituinte de uma ramificação. Aquando da ação de fucosídases liberta-se L-fucose
11
que pode ser reativada a GDP-fucose via cínase da L-fucose e de uma pirofosforílase.
PPi
UDP-galactose
UTP
Mútase
ATP
L-fucose
Cínase da L-fucose
Pirofosforílase do
UDP-glicose
glicose-1-P
H2 O
fucosídases
PPi
Síntase do glicogénio
UDP-glicose
4-epimérase
Fucosiltransférases
GDP-fucose
UDP
ADP
Pirofosforílase
galactose-1-fosfato
GDP-4-ceto-6-desoxi-manose
Redútase
A ação da 4-epimérase permite que a UDP-galactose formada na ação da uridil-transférase da galactose-1fosfato se converta em UDP-glicose. No processo de formação de glicose-1-fosfato a partir de galactose, o
par UDP-galactose /UDP-glicose tem um papel “pseudo-catalítico”.
ATP
Cínase da galactose
GTP
PPi
10
Maioritariamente no fígado, a galactose da dieta converte-se em glicose-1fosfato via ação da cínase da galactose e da uridil-transférase da galactose-1-fosfato.
galactose
manose-1-P
manose-6-P
frutose-6-P
Os resíduos de ácido N-acetil-neuramínico estão, quase
sempre, nas extremidades das cadeias oligossacarídicas.
piruvato
glicose-6-P
glicose
H2O
Pi
Glicose-6-fosfátase
galactose, a massa de
glicogénio aumenta
porque parte da glicose-1fosfato se converte em
UDP-glicose que é dador
de glicose na ação da
síntase do glicogénio.
1-Quando se ingere galactose, a
glicemia aumenta (ligeiramente)
porque parte da glicose-1-fosfato se
converte em glicose-6-fosfato que, por
sua vez, no fígado, sofre a ação da
glicose-6-fosfátase, libertando glicose.
2-Uma parte da glicose-6-fosfato segue a
via glicolítica e o lactato plasmático
aumenta…
lactato, CO2
12
A galactose é, a par com a glicose e outras oses, um importante constituinte de
glicolipídeos, glicoproteínas e proteoglicanos. Alguns exemplos:
No entanto, a galactose não é um nutriente essencial porque o UDP-galactose
(um substrato da galactosil-transférases) é sintetizado a partir da glicose.
Na verdade, mesmo quando se ingere galactose, os resíduos de galactose dos gliconjugados
que contêm galactose provêm da glicose do sangue que entra nas células e se converte em
UDP-galactose (o dador de galactose na ação das galactosil-transférases).
Globosídeo
Aceitador (n+1 resíduos)
Glicoproteína
Aceitador
(n resíduos)
UDP-glicose
Pirofosforílase do
UDP-glicose
4-epimérase
Porção glicídica (glicosaminoglicano) de proteoglicanos
PPi
UDP
A galactose faz parte da
ponte trissacarídica que, na
maioria dos proteoglicanos,
liga a “cadeia de unidades
dissacarídicas” repetitivas à
proteína.
13
Glicose-6-fosfátase
glicose
As enzimas que
catalisam a conversão
da frutose em frutose1-P (cínase da frutose),
a cisão desta em
dihidroxiacetona-P e
gliceraldeído (aldólase
B) e a fosforilação
deste em gliceraldeído3-P (cínase do
gliceraldeído) só
existem no fígado, rim
e enterócitos.
ATP
frutose
Pi
ADP
Glicogénio
glicose-1-P
glicose-6-P
Isomérase das
hexoses-P
H2O
ATP
ADP
hexocínase
dissacarídica repetitiva no sulfato de
queratano (um glicosaminoglicano).
UDP-glicose
Mútase
Síntase da lactose
A galactose faz parte da unidade
A ingestão de frutose leva ao aumento (modesto) da
glicemia. Outros destinos da frutose da dieta são a (1)
formação de lactato, (2) oxidação a CO2 e (3.1) a síntese de
glicogénio e (3.2) de ácidos gordos.
UTP
glicose-1-P
glicose-6-P
Após o nascimento do bebé produz-se na mama da mãe uma proteína
(lactalbumina) que se liga à galactosil-transférase e que lhe modifica a
especificidade: o substrato aceitador passa a ser a glicose e começa a formar-se
lactose.
Ao contrário da glicose e da galactose (que podem fazer
parte de glicoconjugados) o papel biológico da frutose
é exclusivamente energético.
A frutose existe no sémen porque nas
vesículas seminais existe uma via
metabólica que, via sorbitol, converte
glicose em frutose.
14
Glut5
NADH
Desidrogénase
do sorbitol
NAD+
frutose-6-P
Hexocínases
ATP
Pi
ADP
frutose-1-P
frutose
Redútase
das aldoses
H2O
frutose-1,6-bisfosfato
NADPH
Aldólases A e B
Aldólase B
sorbitol (é um poliálcool)
dihidroxiacetona-P
Isomérase das trioses-P
gliceraldeído
NADP+
Frutose-1,6-bisfosfátase
Cínase da frutose
gliceraldeído-3-P
Cínase do gliceraldeído
ATP
ADP
glicose
piruvato
acetil-CoA
ácidos gordos
CO2
lactato
O facto de os espermatozoides consumirem frutose e de o líquido seminal conter
este açúcar dá aos gâmetas masculinos uma vantagem competitiva sobre outras
células (nomeadamente fungos e bactérias) que povoam a vagina normal
contribuindo para a sua sobrevivência (e para a sobrevivência dos genes neles
contidos).
16
Bibliografia consultada
Murray, R. K., Granner, D. K., Mayes, P. A. & Rodwell, V. W. (2012) Harper's Illustrated Biochemistry, 29th edn, Lange, New York.
Nelson, D. L. & Cox, M. M. (2013) Lehninger Principles of Biochemistry, sixth edition edn, W. H. Freeman and Company, New York.
Devlin, T. M. (2006) Textbook of Biochemistry with Clinical Correlations, 6th edn, John Wiley & Sons, New York.
Baynes, J. W. & Dominiczac, M. H. (2005) Medical Biochemistry, 2 edn, Elsevier Philadelphia
Bais, R., James, H. M., Rofe, A. M. & Conyers, R. A. (1985) The purification and properties of human liver ketohexokinase. A role for
ketohexokinase and fructose-bisphosphate aldolase in the metabolic production of oxalate from xylitol, Biochem J. 230, 53-60.
Chong, M. F., Fielding, B. A. & Frayn, K. N. (2007) Mechanisms for the acute effect of fructose on postprandial lipemia, Am J Clin Nutr. 85,
1511-20.
Douard, V. & Ferraris, R. P. (2008) Regulation of the fructose transporter GLUT5 in health and disease, Am J Physiol Endocrinol Metab. 295,
E227-37.
Eixelsberger, T., Sykora, S., Egger, S., Brunsteiner, M., Kavanagh, K. L., Oppermann, U., Brecker, L. & Nidetzky, B. (2012) Structure and
mechanism of human UDP-xylose synthase: evidence for a promoting role of sugar ring distortion in a three-step catalytic conversion of UDPglucuronic acid, J Biol Chem. 287, 31349-58.
Gitzelmann, R., Steinman, B. & Van der Berghe, G. (1995) Disorders of fructose metabolism in The metabolic and molecular bases of inherited
disease. (Scriver, C., Beaudet, A., Sly, W. & Valle, D., eds) pp. 905-933, McGraw-Hill, New York.
Grossbard, L. & Schimke, R. T. (1966) Multiple hexokinases of rat tissues. Purification and comparison of soluble forms, J Biol Chem. 241, 354660.
Jones, A. R. & Connor, D. E. (2000) Fructose metabolism by mature boar spermatozoa, Reprod Fertil Dev. 12, 355-9.
Maccioni, H. J., Quiroga, R. & Spessott, W. (2011) Organization of the synthesis of glycolipid oligosaccharides in the Golgi complex, FEBS Lett.
585, 1691-8.
Milewski, S. (2002) Glucosamine-6-phosphate synthase--the multi-facets enzyme, Biochim Biophys Acta. 1597, 173-92.
Ramakrishnan, B., Boeggeman, E. & Qasba, P. K. (2002) Beta-1,4-galactosyltransferase and lactose synthase: molecular mechanical devices,
Biochem Biophys Res Commun. 291, 1113-8.
Rentmeister, K., Schmidbauer, S., Hewicker-Trautwein, M. & Tipold, A. (2004) Periventricular and subcortical leukoencephalopathy in two
dachshund puppies, J Vet Med A Physiol Pathol Clin Med. 51, 327-31.
Schadewaldt, P., Hammen, H. W., Loganathan, K., Bodner-Leidecker, A. & Wendel, U. (2000) Analysis of concentration and (13)C enrichment of
D-galactose in human plasma, Clin Chem. 46, 612-9.
Segal, S. & Berry, G. T. (1995) Disorders of galactose metabolism. in The metabolic and molecular bases of inherited disease. (Scriver, C.,
Beaudet, A., Sly, W. & Valle, D., eds) pp. 967-1000, McGraw-Hill, New York.
Sunehag, A., Tigas, S. & Haymond, M. W. (2003) Contribution of plasma galactose and glucose to milk lactose synthesis during galactose
ingestion, J Clin Endocrinol Metab. 88, 225-9.
Tanner, M. E. (2005) The enzymes of sialic acid biosynthesis, Bioorg Chem. 33, 216-28.
17