O tratamento da encefalopatia
hepática reavaliado
Apoio:
Realização:
SOCIEDADE BRASILEIRA
DE HEPATOLOGIA
Hepato 4 13 03 07 LAYOUT 01_SAID1 1
FEDERAÇÃO BRASILEIRA DE
GASTROENTEROLOGIA
13.03.07 14:03:44
Hepato 4 13 03 07 LAYOUT 01_SAID2 2
13.03.07 14:03:57
Editorial
A Sociedade Brasileira de Hepatologia tem como um de
seus objetivos primordiais a promoção de Educação Médica
Continuada de elevada qualidade científica. Neste projeto
ela se propõe a fazê-lo através de discussão de casos
clínicos, entrevistas e revisões de atualização sobre temas
fundamentais em Hepatologia, abordados por renomados
especialistas da área.
A Zambon participa desta iniciativa, levando à classe
médica a melhor mensagem técnico-científica, com o apoio
da Sociedade Brasileira de Hepatologia.
Nesta edição o médico terá a oportunidade de atualizar
seus conhecimentos através da informação mais precisa
e atual sobre um importante problema: O tratamento da
encefalopatia hepática reavaliado.
João Galizzi Filho
Presidente
Realização:
Apoio:
FEDERAÇÃO BRASILEIRA DE
GASTROENTEROLOGIA
SOCIEDADE BRASILEIRA
DE HEPATOLOGIA
Cortesia:
Atha Comunicação e Editora – e-mail: [email protected]
Criação e Coordenação editorial
Hepato 4 13 03 07 LAYOUT 01_SAID3 3
13.03.07 14:03:57
O tratamento da encefalopatia
hepática reavaliado
Dr. Heitor Rosa
Professor Titular de Gastroenterologia da Faculdade de Medicina, Diretor da Faculdade
de Medicina da Universidade Federal de Goiás.
Introdução
Poucos tratamentos são tão antigos quanto o da encefalopatia hepática (EH), e a cada século ou década
são acrescentadas novas orientações em função dos conhecimentos recém-adquiridos ou das teorias propostas. Por mais que avancemos nas descobertas das expressões gênicas ou demonstrações moleculares, o amoníaco permanece como elemento central e insensível aos esforços para combatê-lo. Graças aos
protocolos controlados e à obediência às normas éticas, diminuiu o número de vítimas de novas, porém
nem sempre boas, idéias.
A revisão aqui apresentada é um resumo crítico dos procedimentos ou tendências atuais, armas disponíveis de razoável sucesso.
Diagnóstico diferencial
A EH típica é facilmente diagnosticada e raramente
comporta um diagnóstico diferencial. Porém há situações que exigem grande atenção, seja pela forma inusitada de aparecimento e evolução da síndrome, seja
pela falta de resposta ao tratamento convencional.
Nessas condições costumam faltar os chamados fatores precipitantes.
É interessante lembrar que o cirrótico está sujeito a diversas outras condições, como qualquer doente. Dessa
forma, a encefalopatia atípica deve ser diferenciada das
seguintes situações:
• infecções como meningites, abscessos intracranianos e encefalites;
• distúrbios metabólicos como hiponatremia grave,
uremia, hipoglicemia ou anóxia;
• lesões intracranianas secundárias a quedas e a outros acidentes, como hematoma subdural e sangramento intracraniano (considerar também a possibilidade de tumores);
• encefalopatia tóxica relacionada ao álcool, nas formas
agudas, abstinência e encefalopatia de Wernicke;
• hiperamoniemia por outras causas e relacionadas a
lesões musculares e renais;
• síndromes convulsivas.
Tratamento
Medidas gerais
As medidas para tratamento da EH dependem do estágio ou do quadro clínico, que pode variar desde uma
discreta alteração de comportamento, memória ou
“falta” de concentração até o estado de inconsciência.
Qualquer que seja a situação devem ser considerados
alguns procedimentos rotineiros:
• Nos casos leves ou em pacientes idosos, certificar-se
de que as alterações mentais (memória, concentração)
estão realmente relacionadas à cirrose.
• Investigar minuciosamente um provável fator precipitante, por exemplo sangramentos, infecção sistêmica
ou ascítica, medicamentos contra-indicados ou superdosagem, obstipação, entre outros.
• Nas situações graves (EH de grau IV) observar atentamente a necessidade de assistência ventilatória.
• Conduta na agitação incontrolável, que dificulta o acesso venoso ou sua manutenção, enteróclise e outros procedimentos. Na experiência do autor, a sedação pode
ser feita com segurança com a administração de 1 a 2
mg de midazolam IV, com o cuidado de ter à mão o seu
antagonista (flumazenila), o que é uma vantagem desse
medicamento. Alguns autores recomendam a injeção de
4
Hepato 4 13 03 07 LAYOUT 01_SAID4 4
13.03.07 14:04:01
haloperidol, entretanto sua eliminação é muito demorada e dificulta a avaliação da resposta ao tratamento.
• Nas formas típicas de EH, acreditamos que a dosagem da amoniemia pode ser dispensável, assim como
o EEG. Esses parâmetros são reservados mais para os
ensaios clínicos controlados do que para a avaliação da
efetividade do tratamento, que se observa pelo despertar do paciente.
O tratamento básico e consensual da EH consiste em
medidas que visam a combater a hiperamoniemia e
sua produção, independentemente do estágio clínico.
Dieta
É um dos pontos mais controversos ao longo de dezenas de anos. A dieta aprotéica (de graus II, III e IV) e a
hipoprotéica (de grau I ou convalescença) foram, e têm
sido, prescritas consensualmente como meio de combater a produção de amônia produzida pela proteína
animal. Esse comportamento tem mudado radicalmente, a partir das observações e correlações em estudos
controlados sobre o papel do estado de nutrição no
cirrótico e a redução protéica.
A baixa ingestão de proteína agrava o estado nutricional e favorece o maior catabolismo muscular e as infecções. Tais fatos nos obrigam a reavaliar a tradição da
proscrição protéica. Em nossas observações, aos pacientes em fase pré-comatosa ou de grau I permitimos
a ingestão de 40 a 70 g de proteína “branca” (peixe,
frango), mais palatável, complementada por proteínas
de origem vegetal (aminoácidos de cadeia ramificada).
Nos casos graves a alimentação de alto teor protéico
deve ser feita por sonda nasoentérica. Outra vantagem
desses suplementos é o teor de fibras. O fornecimento
de proteínas, dessa forma e associada às outras medidas (ver abaixo), não parece influenciar o estado de
consciência.
Laxantes
Outra medida consagrada e até o momento obrigatória é a prescrição de laxantes ou catárticos.
A lactulose constitui-se quase em padrão-ouro para
comparação com outras medidas terapêuticas, como
certos antibióticos e probióticos. Ela é um dissacarídeo
sintético não-absorvível já em uso há quase 40 anos;
considerada como prebiótico, é usada com a finalidade de diminuir ou impedir a formação de amônia nos
intestinos, cujo mecanismo de ação se processa por
sua conversão em ácido láctico, facilitando a transformação do radical amônio (NH4+) em NH3, o qual é eliminado na luz intestinal. Essa acidificação (H+) dificulta
a produção de coliformes amoniogênicos e aumenta os
lactobacilos não-amoniogênicos. O resultado paralelo é
a limpeza intestinal, dependente da dose: evacuações
amolecidas ou diarréia intensa, cólicas e grande produção de gases, especialmente H2.
Nos pacientes compensados, uma dose de 30 ml/dia
é suficiente para evitar a coprostase; nas formas graves, pode-se administrar, via sonda nasogástrica ou
nasoentérica, 40 ml três a quatro vezes ao dia. A lactulose também é usada como enema, pelo menos no
início do tratamento, para um efeito mais rápido; nessa
situação recomendamos 250 ml do laxante em 600 a
700 ml de água morna, a cada 6 a 8 horas.
O lactitol é outro dissacarídeo, semelhante à lactulose,
e segundo alguns autores tem a vantagem da menor
produção de gases e, portanto, menor distensão abdominal. Também é apreciável seu efeito sobre o aumento da produção de lactobacilos e bifidobacterium.
A prescrição é feita em situações semelhantes às descritas para a lactulose, e as doses variam de 5 a 40
g/dia (oral ou enema).
Estudos controlados atuais têm colocado em dúvida
o real benefício desses açúcares e sugerido que seus
efeitos são iguais ou inferiores aos de certos antibióticos, como a rifaximina. Enquanto se procuram evidências seguras, lembramos que a relação custo-benefício
deve ser considerada antes da adoção de novos produtos mais caros.
Antibióticos
O principal representante é a neomicina, largamente
conhecida e de prescrição e cuidados tradicionais. Alguns autores a consideram de segunda linha, administrando-a após observação do efeito da lactulona. Somos favoráveis à concomitância de seu uso a partir do
grau II. Outros antibióticos têm sido considerados, eles
sim de segunda linha, como metronidazol, paromomicina, certas quinolonas e até a vancomicina.
Há um grande número de trabalhos recentes, parcialmente ou bem controlados que comparam os efeitos
da rifamixina (rifamicina) com os da lactulose ou do lactitol. Este antibiótico não é absorvível no trato intestinal e possuiu atividade in vitro contra bactérias aeróbicas e anaeróbicas. Seu principal uso é na diarréia dos
viajantes e na síndrome do instestino irritável. Estudos
controlados dão-lhe a mesma eficácia dos dissacarídeos na EH, em doses de 400 mg cada 8 horas e supostamente indicada para uso crônico. Entretanto, a relação custo-benefício, comparada à da lactulose ou da
neomicina, nos faz refletir sobre sua prescrição sem
evidências incontestáveis. Parece que seu uso não conduz à resistência microbiana.
5
Hepato 4 13 03 07 LAYOUT 01_SAID5 5
13.03.07 14:04:02
Outras alternativas paralelas
Além dos antibióticos (neomicina) e dos prebióticos
(lactulona), há uma corrida de ensaios com probióticos.
Estes são microrganismos vivos não-patogênicos que
fermentam os açúcares não absorvidos no delgado;
são conhecidos cinco grupos em relação aos produtos
de fermentação. Aqueles produtores de CO2 e ácido
láctico (como os lactobacilos) são os mais indicados na
EH, sem nenhum dos inconvenientes dos antibióticos
ou prebióticos (ausência de efeitos colaterais, uso crônico benéfico e barato). Faltam estudos que avalizem
sua eficácia nas formas agudas graves.
Outra alternativa com inteligente racional é o uso de uma
mistura de L-ornitina e L-arginina (LOLA), ambas substratos para glutamato transaminase; após sua administração, espera-se um aumento dos níveis de glutamato e,
dessa forma, sua conversão em glutamina, reação catalisada pela glutamina sintetase. Dessa forma a amônia é
captada e eliminada. Existem numerosos e crescentes
ensaioscom essa mistura, relacionando-a a testes psicométricos, PEV e níveis de amônia. A LOLA se apresenta comercialmente em pó (sachês) para uso doméstico
e injetável, para as formas mais agudas ou graves da
doença. Nossas observações abertas, como pré-estudo,
são favoráveis a um amplo estudo controlado.
A carnitina é outro agente metabólico que se candidata ao arsenal terapêutico da EH, sendo alvo de vários
estudos controlados e semicontrolados. É um derivado
acetilado (acetil-L-carnitina/ALC) que possui inúmeras
funções, algumas das quais usadas como racionais
para os ensaios na EH. A ALC é um importante betaoxidante dos ácidos graxos do fígado. Tem ações neurobiológicas como a de facilitar a velocidade de condução
nervosa (transmissão sináptica nos neurotransmissores, metabolismo energético cerebral – fatores neurotróficos e neurormonais) e a de acetilação dos radicais
(-NH2), previne as alterações Na+/K+-ATPase, induz a
ureagênese, etc. Tais fatos parecem justificar a volta
à terapêutica da transmissão neural (complexo GABA).
Os ensaios controlados ainda devem provar uma relação efetiva entre a melhora da neutrotransmissão e o
estado de consciência.
Oligoelementos como o zinco têm sido usados na EH,
após se observar sua deficiência na cirrose alcoólica!
Esse metal aumenta a atividade da ornitina transcarbamilase no ciclo da uréia, daí sua maior produção (ureagênese) e, conseqüentemente, maior captação de NH3
e sua eliminação. O racional é bom, mas não se aplica
às formas graves de EH, e para o uso caseiro diário seu
provável efeito tem muitos elementos que confundem.
Já está bem demonstrada a participação do manganês
na EH, por meio da hiperintensidade de sinal em T1 na
ressonância cerebral magnética, assim como a hipermanganesemia e suas prováveis conseqüências. Seu
papel na gênese ou na perpetuação da EH poderá ficar
bem demonstrado quando um possível agente quelante
desse metal for usado para eliminá-lo, a exemplo da penicilamina-cobre, e demonstrar a relação com o estado
de consciência ou manifestações extrapiramidais.
Situações mais reflexivas
O desenvolvimento teórico e o experimental laboratorial são muito mais rápidos do que a aplicação prática.
É assim que vemos as provas se acumularem sobre outros parâmetros etiopatogênicos da EH, como as participações do estresse oxidativo (óxido nítrico e citocinas
pró-inflamatórias) e a produção de neuroesteróides.
Se do ponto de vista teórico essas variáveis parecem
corretas, razoáveis e mais outras justas peças desse
imenso quebra-cabeça, a terapêutica eficaz parece longe de ser usada no dia-a-dia.
Recentemente novos estudos, agora invasivos, propõem a embolização parcial da artéria esplênica como
um complemento ao tratamento da EH crônica.
Conclusão
Se o leitor fizer uma reflexão analítica considerando as
diversas causas e os diversos fatores correlatos na
produção da EH, o resultado pode ser a conclusão de
que deveríamos usar uma verdadeira teriaga hepática
para combater tantos elementos.
Evidentemente, não pode nem poderá ser assim. As alterações bioquímicas na EH são como uma constelação
de reações interligadas, quase infinitas. Onde se procurar nessa imensa cadeia metabólica vai se encontrar
um defeito físico-químico. A falta de bom senso pode levar à desorientação total, no equívoco das evidências e
da visão da verdade sob milhares de facetas. As pesquisas devem e vão progredir incessantemente, felizmente, e serão objetos metanalíticos. Porém, é necessário
compreender que as evidências de metanálise são uma
verdade estatística, mas não necessariamente a verdade intrínseca ou absoluta ou permanente.
Lembramos que a EH é apenas uma síndrome, que aparece e desaparece em função da evolução geralmente
inexorável da cirrose.
O leitor pode notar que centralizamos o tratamento no
amoníaco, e por isso mesmo achamos muito inspirado
o título do trabalho de Shawcross, Butterworth et al:
“Amônia e encefalopatia hepática: quanto mais as coisas mudam, mais elas permanecem do mesmo jeito”
(Metab Brain Dis 2005;20:169-79).
6
Hepato 4 13 03 07 LAYOUT 01_SAID6 6
13.03.07 14:04:02
Estudo comentado
Durval Rosa Borges
Professor Titular, Disciplina de Gastroenterologia Departamento de Medicina
Universidade Federal de São Paulo.
Medical treatment of cholestatic liver diseases: From pathobiology
to pharmacological targets.
Gustav Paumgartner
World Journal of Gastroenterology 2006; 12: 4445-4451
Este editorial cobre cinco tópicos: mecanismos moleculares
da formação da bile, mecanismos moleculares da colestase,
respostas adaptativas à colestase, alvos da terapêutica farmacológica e tratamento farmacológico de doenças hepáticas crônicas colestáticas.
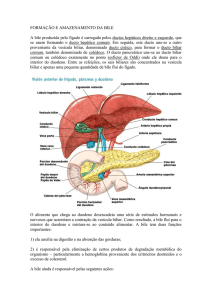
Mecanismos moleculares da formação da bile: a bile hepatocelular é resultado do transporte ativo de solutos para os
canalículos biliares, estabelecendo gradiente osmótico entre a bile canalicular e o plasma sinusoidal. A mais importante força impulsora da formação da bile hepatocelular é a
secreção de ácidos biliares do sangue sinusoidal para a bile.
Vários transportadores estão envolvidos nesta ação.
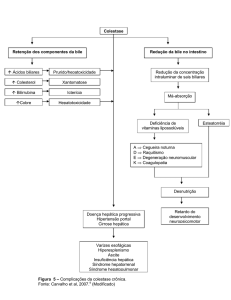
Mecanismos moleculares da colestase: a colestase, definida
como diminuição do fluxo biliar, tem como conseqüência a
retenção de ácidos biliares, bilirrubina e outros coléfilos no
fígado e no sangue e deficiência de ácidos biliares no intestino. Diferentes formas de colestase podem ser causadas
por: 1) deficiência na secreção biliar; 2) obstrução ao fluxo biliar; ou 3) uma combinação das duas. A deficiência na
secreção biliar pode ser inata (colestase intra-hepática progressiva familial, colestase intra-hepática benigna recorrente, fibrose cística) ou adquirida (inflamação, toxinas, drogas
ou hormônios). Nas doenças inflamatórias (sepses, infecções bacterianas, hepatites virais) ou nas hepatites induzidas por toxinas ou drogas, as citocinas inflamatórias (TNF-α
e IL-1β) diminuem a secreção biliar. Drogas (ciclosporina A,
glibenclamida, troglitazona, bosentana) podem causar colestase por inibir a função de proteínas transportadoras hepatobiliares. A obstrução do fluxo biliar pode também ser inata
(fibrose cística, colestase intra-hepática progressiva familial
ou adquirida (colangite esclerosante primária, síndrome do
desaparecimento de duto biliar). A colestase obstrutiva mais
freqüente é a causada por cálculos ou tumores.
Respostas adaptativas à colestase: para compensar a perda da capacidade excretora biliar na colestase e para limitar
o acúmulo hepatocelular de substâncias biliares potencialmente tóxicas, processos adaptativos ocorrem no fígado, no
rim e no intestino. No fígado há modulação na expressão
dos transportadores envolvidos na captação e excreção de
ácidos biliares e outros ânions orgânicos.
Alvos da terapêutica farmacológica: a conseqüência comum
a todas as formas de colestase é a retenção de ácidos biliares no hepatócito. Os seguintes alvos farmacológicos foram
identificados para o tratamento da colestase intra-hepática:
1) estímulo da secreção biliar ortógrada ou estímulo retrógrado da secreção de ácidos biliares para a circulação
sistêmica e posterior excreção renal; 2) estímulo do metabolismo de ácidos biliares hidrofóbicos a produtos mais
hidrofílicos e menos tóxicos; 3) proteção dos colangiócitos
de efeitos tóxicos da bile; 4) inibição da apoptose causada
por níveis elevados de ácidos biliares citotóxicos; 5) inibição
da fibrose causada pelo vazamento de ácidos biliares para
o espaço peribiliar.
O estímulo à secreção de ácidos biliares e de outros compostos potencialmente tóxicos pode ser obtido aumentando-se a expressão de transportadores e/ou sua função, em
diferentes níveis (transcrição, tradução, direcionamento e
ativação protéica). O ácido ursodeoxicólico (AUDC) estimula
o direcionamento de transportadores à membrana canalicular, protege os colangiócitos e inibe a apoptose. A rifampicina estimula a atividade metabólica do citocromo CYP3A.
Tratamento farmacológico de doenças hepáticas crônicas
colestáticas: o autor usa como modelo o tratamento da cirrose biliar primária. Como não é conhecida sua etiologia, o
tratamento objetiva inibir o processo patogênico e retardar
a progressão da doença. O AUDC é a única droga aprovada
para esses fins. Em doses de 13-15 mg/kg/dia melhora
os testes hepáticos marcadores de colestase, o escore de
risco e a histologia hepática (inibindo a progressão histológica nos estágios iniciais da doença). O tratamento por até
4 anos pode retardar o momento de transplante ou o óbito.
Doses inferiores a 10 mg/kg/dia não são eficazes. Esse
tratamento parece também ser benéfico em outras doenças colestáticas, como a colangite esclerosante primária, a
colestase intra-hepática da gravidez, a doença hepática da fibrose cística, a colestase intra-hepática progressiva familial
e algumas formas da colestase induzida por drogas.
Comentário. A esquistossomose é importante causa de doença hepática não caracterizada pela presença de colestase stricto sensu, evoluindo quase sempre sem prurido ou
icterícia. Recente revisão sobre doenças colestáticas anictéricas não incluiu a esquistossomose entre as possíveis
causas etiológicas(1). Por outro lado, é comum encontrar
elevação da γ GT sérica, não relacionada à carga parasitária(2), de mecanismo diferente do observado no alcoolismo(3)
e sensível ao ácido ursodeoxicólico, com resposta rápida e
reversível(4).
Referências
1.
2.
Dupas B, Gournay J, Frampas E, Leaute F, Le Borgne J. Anicteric
cholestasis: imaging and diagnostic strategy. J Radiol 2006; 87:
441-459.
Amaral ACC, Köpke-Aguiar LA, Souza MRA, Toledo CF, Borges
DR. Serum gamma-glutamyltransferase alteration in hepatic
schistosomiasis doesn’t correlate with parasitic load and precedes
ultrasound alterations. Arq Gastroenterol 2002; 39: 27-31.
3.
4.
Martins RD, Borges DR. Ethanol challenge in non-alcoholic patients
with schistosomiasis. J Clin Pathol 1993; 46: 250-253.
Ribeiro PJ, Narciso JL, Toledo CF, Borges DR. Gammaglutamyltransferase decreases in patients with the chronic form of
schistosomiasis mansoni treated with ursodeoxycholic acid. J Clin
Pathol 2005; 58: 783-784.
7
Hepato 4 13 03 07 LAYOUT 01_SAID7 7
13.03.07 14:04:03
202150 – URSACOL/BOLETIMSBH04/MAR07
Realização:
Apoio:
FEDERAÇÃO BRASILEIRA DE
GASTROENTEROLOGIA
SOCIEDADE BRASILEIRA
DE HEPATOLOGIA
Cortesia:
Hepato 4 13 03 07 LAYOUT 01_SAID8 8
13.03.07 14:04:03