HOSPITAL MOINHOS DE VENTO - INSTITUTO DE EDUCAÇÃO E PESQUISA
Assistência de Enfermagem no Período Perioperatório I
Enfermagem na Doação e
Transplante de órgãos e
tecidos
Breve História dos Transplantes
...: Deus cria Eva a partir de uma costela de Adão
1822: ocorre o primeiro
autotransplante de pele
1869: o cirurgião suíço
"Creazione della Dona" de
Caterina Giorgetti
Taís Maria Nauderer
Agosto 2010
280: Os médicos gêmeos Cosme e Damião fazem um
transplante da perna de um doador morto (negro) para um
paciente branco. Por esse milagre, Cosme e Damião foram
elevados à categoria de santos da Igreja Católica e são os
patronos das Faculdades de Medicina
1900:
Karl Landsteiner, imunologista austríaco, define a
classificação do sangue em quatro tipos: A B, AB, e O
1902: São realizado transplantes renais experimentais em cães, em
Viena
1905: Alexis Carrel desenvolve uma técnica para unir
vasos de sanguíneos para restabelecer a circulação,
técnica que foi fundamental para os transplantes
1914: torna- se possível o armazenamento de
sangue
1954: acontece o primeiro transplante de rim entre
gêmeos idênticos
1959: reconhecido pela 1ª vez o critério de morte
encefália como morte do indivíduo, em Paris
1940: Karl Landsteiner, Philip Levine e Alexander
Wiener descobrem um antígeno no sangue de
macacos de gênero Rhesus, que ficou conhecido com
Fator Rh
1944: Criado o primeiro banco de olhos humano
1800s: A medula óssea é administrada via oral a
pessoas com anemia e leucemia. Embora sem
sucesso, essa tentativa de tratamento conduziu a
outras tentativas até se chegar ao transplante de
medula, posteriormente
1964: realizado o primeiro transplante renal
no Brasil com doador cadáver, no Rio de
Janeiro, quando Sérgio Vieira Miranda, 18
anos, portador de pielonefrite crônica,
recebeu um rim de uma criança de nove
meses, portadora de hidrocefalia
1967: realizado o primeiro transplante cardíaco em ser
humano, retirando o coração de uma mulher de 25 anos,
morta em acidente automobilístico, e implantando-o no
peito de um dentista. A doadora era uma mulher branca;
o receptor, um homem negro
Acontece o primeiro transplante de fígado no mundo, nos
EUA
Comitê de Harvard normatiza a definição de morte como
morte encefálica
1983: desenvolvimento da ciclosporina
Jacques Louis Reverdin
realiza
o
primeiro
alotransplante de pele
fresca
são relatados
os primeiros casos de
transplantes de córnea
1880/1905:
1989: são realizado os primeiros transplantes de
pulmão e de rim e pâncreas combinado da América
Latina, na Santa Casa de Porto Alegre. Os
receptores receberam os órgãos um doador morto
em acidente de motocicleta
1993: acontece o primeiro transplante de pulmão
com doador vivo. Um lobo da mãe e outro do pai
são transplantados para uma criança
2000: é realizado o primeiro transplante de
intestino no Brasil no Programa de Transplante de
Fígado e Intestino da Santa Casa de Misericórdia de
São Paulo. O receptor foi uma criança que recebeu o
intestino delgado de outra criança
2002: anunciado o nascimento de porcos
clonados com modificações genéticas para
prevenir a rejeição no caso de transplantes em
humanos
1
Existe a lenda de um camponês culpado por roubar um cavalo
que pertencia ao rei. Quando sentenciado à morte, apresentou a
seguinte objeção: “Se Vossa Majestade poupar a minha vida,
prometo que ensinarei seu cavalo a falar”. O rei aceitou o apelo,
dando ao homem um ano para completar a tarefa, após o qual,
se fracassasse, a execução seria levada a cabo. Quando alguém
salientou que havia poucas chances de ensinar o cavalo a falar e
que com certeza do rei o executaria, o camponês respondeu: “Em
um ano muito pode acontecer; eu posso morrer, o rei pode
morrer ou o cavalo pode aprender a falar. Porém a alternativa, é
minha morte imediata”. O camponês tinha uma tarefa difícil,
quase impossível.
Todos aqueles que se submetem à cirurgia dos transplantes
admitem que é a única opção terapêutica a ser realizada
Aspectos atuais
O índice de sucesso dos transplantes
de órgãos ultrapassa os 80%, devido a
avanços nas áreas de terapia intensiva,
da imunologia e da farmacologia.
O Brasil é o segundo país do mundo
em número de transplantes, sendo
superado somente pelos Estados Unidos.
O Brasil dispõe do maior programa
público de transplantes.
Epidemiologia no Brasil
O crescimento da taxa de doação no país, a partir de 2007, é
marcante (60%).
Metas propostas para 2009 – de 8,5 doadores efetivos por milhão
de população (pmp), de 4.000 transplantes de rim e de 1.300 de
fígado – foram superadas.
2009: 1.658 doadores (8,7 pmp) e com 4.259 transplantes renais
e 1.322 hepáticos.
Esses são os melhores resultados já obtidos no país
2010: objetivo de 10 doadores pmp, de 4.800 transplantes renais
e de 1.500 transplantes hepáticos, desde que se mantenha o
empenho de todos os setores envolvidos.
2009: crescimento de 26% na taxa de doação, devido ao
aumento de 16% na taxa de efetivação, que passou de 22% para
25,5% (ainda distante do objetivo de 40%) e um aumento de 8%
na taxa de notificação, que passou de 32,5 pmp para 34,2 pmp
(também, ainda longe da meta prevista para 2017 de 50
notificações pmp).
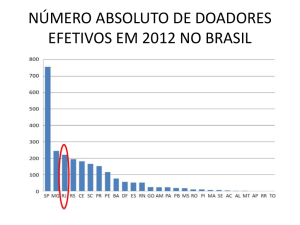
Rio Grande do Sul
O
Rio
Grande
do
Sul,
que
historicamente foi o estado com a
maior taxa de doadores do país, e nos
últimos três anos, ao contrário do que
acontece no Brasil, vem apresentando
uma queda constante na taxa de
doação.
Fonte: Associação Brasileira de Transplantes de Órgãos
Fonte: Associação Brasileira de Transplantes de Órgãos
2
Fonte: Associação Brasileira de Transplantes de Órgãos
Fonte: Associação Brasileira de Transplantes de Órgãos
Fonte: Associação Brasileira de Transplantes de Órgãos
2010
Primeiro
semestre/2010:
quase
alcançando o objetivo previsto para
esse ano de 10 doadores por milhão
de população (pmp)
Atualmente 9,9 pmp, e taxas recordes
de transplante de rim, de fígado e de
pulmão.
Fonte: Associação Brasileira de Transplantes de Órgãos
Fonte: Ministério da saúde, Brasil
3
Aspectos gerais do Tx
Listas de espera
Os pacientes candidatos a receber um órgão para
A principal razão para o aumento dos
transplante no Brasil são organizados através de
uma fila única, com a finalidade de facilitar o
processo de distribuição dos órgãos
O processo de doação de órgãos e transplantes é
complexo, pois além da ordem da fila, há a
necessidade de total compatibilidade entre o
receptor e o órgão doado
A fila de espera por um fígado é organizada de
forma diferente em relação aos outros órgãos no
Brasil (portaria do MS nº 1.160: a distribuição de
fígado de doadores cadáveres para transplante
segue o critério de gravidade de estado clínico do
paciente)
pacientes em lista de espera e o
aumento do tempo de espera por um
órgão, relaciona-se com a demanda,
que é muito superior ao número de
doadores ou de órgãos doados.
16 pacientes morrem diariamente na
fila de espera por órgãos nos EUA
Fonte: Associação Brasileira de Transplantes de Órgãos
Aspectos econômicos
A problemática dos transplantes de órgãos pode ser mais
bem compreendida com a observação de algumas das
características econômicas dos órgãos transplantáveis.
1. São essenciais.
2. Não podem ser estocados por muito tempo
3. Têm pouco uso. Portanto, existe baixo custo de
oportunidade, pois não há muito o que fazer com os
órgãos doados, que se deterioram rapidamente.
Fonte: Associação Brasileira de Transplantes de Órgãos
Fonte: Ministério da saúde, Brasil
4
4. Têm poucos substitutos, com exceção de rins que,
durante algum tempo, e com baixa qualidade de
vida, admitem as terapias renais substitutivas.
5. Os candidatos a receptores não comandam a
aquisição dos órgãos. A aquisição é comandada
pelos profissionais de saúde, o que configura um
modelo do tipo principal/agente.
6. Existe elevada “capacidade ociosa”, pois há um
desperdício considerável de órgãos. No Brasil, de
cada 8 potenciais doadores, apenas 1 é notificado e
somente 20% destes são utilizados como doadores
de múltiplos órgãos.
8. Os doadores não comandam a oferta. São os
profissionais de saúde que, em última instância,
decidem se um órgão doado pode ser aproveitado e
para quem ele pode ser cedido.
Legislação
O
problema da captação, alocação e
qualidade dos órgãos para transplante em
nosso meio é fortemente vinculado à
desinformação do meio médico e da
população em geral
Muitos profissionais de saúde desconhecem
ou ignoram a legislação vigente sobre
transplantes e não notificam a ocorrência de
morte encefálica às centrais de transplante
de órgãos.
feita pelo Sistema Nacional de Transplantes
(SNT), que gerencia as Centrais de
Notificação, Captação e Distribuição de
Órgãos e Tecidos (CNCDO) no nível estadual
O doador deve estar com diagnóstico de ME
(natural ou violenta) definido por equipe
médica, seus órgãos devem estar em
funcionamento e o transplante deve ser
autorizado pelo SNT e pelo SUS
A doação entre pessoas vivas não é
responsabilidade do SNT
tipo de doação: todo cidadão legalmente capaz
passava a ser doador, a menos que não houvesse
seu consentimento, sendo necessário expressar sua
vontade de não doação na carteira nacional de
habilitação ou no registro geral, a chamada doação
presumida.
Já em 1998, em virtude da grande polêmica gerada
por essa legislação, foi editada medida provisória
que transformou a doação presumida em doação
consentida: a família deve ser consultada para a
realização da doação, sendo sua decisão soberana
sobre a vontade expressa pelo doador, em vida.
Aspectos que influenciam o
consentiumento
Coordenação processo Brasil
A coordenação de transplantes pelo SUS é
Legislação brasileira - Lei nº 9.434/97 modificou o
A partir dos CNCDOs o processo de doação é organizado nas
instituições de saúde hospitalares através de Comissões Intra
Hospitalares de Doação de Órgãos e Tecidos para Transplante
(CIHDOTT)
Mitos populares também influenciam o
consentimento dos familiares em doar
os órgãos.
É obrigatória a existência de uma comissão intra-hospitalar de
transplante em todo hospital brasileiro com mais de oitenta leitos.
Essa comissão deve ser composta por três profissionais de nível
superior, dentre os quais um médico ou um enfermeiro será o
coordenador.
– O diagnóstico de morte encefálica foi
As atividades da comissão incluem: identificação e manutenção do
potencial doador; a agilidade do diagnóstico de morte encefálica; a
abordagem da família do doador; o contato com a Central de
Transplante e com o Departamento Médico Legal; o contato com as
equipes de retirada e do agendamento do procedimento cirúrgico de
retirada dos órgãos; o transporte dos mesmos e a devolução do
corpo à família
– Razões religiosas
dado ao paciente para forçar uma doação
– Medo de ter o tratamento negligenciado
ao ser identificado como doador
5
Religião, Doação e
Transplante
MORTE ENCEFÁLICA
As religiões encorajam a doação de órgãos e
tecidos como uma atitude de preservação da
vida e um ato caridoso de amor ao próximo,
considerando este ato uma decisão individual
de seu seguidores.
Testemunhas de Jeová
- órgão ou tecido é transplantado
sem a presença de sangue.
Japão
- outro conceito de morte encefálica
Acreditou-se, durante séculos, que a
morte se concretizava no momento
em que as funções cardíacas e
respiratórias extinguiam-se, ou seja,
morria-se
somente
quando
os
batimentos cardíacos e a respiração
cessassem
MORTE ENCEFÁLICA
Embora
a respiração e os batimentos
cardíacos sejam vitais para o ser humano,
os avanços da medicina mostraram que a
atividade cerebral é fundamental para
manter o funcionamento do organismo
Ad Hoc Committee of the Harvard Medical
School classifica como “coma irreversível”
No Brasil, o conceito de morte encefálica
passou a ter o valor de morte clínica a partir
de 1990, segundo determinação do CFM
Judeus - o rabino participa da retirada.
MORTE ENCEFÁLICA
MORTE ENCEFÁLICA
TESTES PARA ME
Fotomotor: deve-se observar se existe fotorreação das pupilas ao
Segundo
o CFM, o intervalo entre as
avaliações clínicas para diagnosticar a ME é
definido de acordo com a idade do paciente:
– Para crianças de 7 dias a dois meses de idade
incompletos, intervalo de 48 horas;
– Para crianças de 2 meses a 1 ano incompleto,
intervalo de 24 horas;
– Para crianças de 1 ano a 2 anos incompletos o
intervalo deve ser de 12 horas.
– Acima de 2 anos o intervalo é de 6 horas
Para se constatar a ME de um paciente com
diagnóstico de coma irreversível e que
possa ser estabelecida sua causa, são
realizados testes clínicos com a finalidade
de detectar a ausência de função encefálica
Os testes só podem ser realizados se o
paciente
estiver
hemodinamicamente
estável e devem ser realizados duas vezes,
por médicos diferentes (sendo que pelo
menos um deles deve ser neurologista)
incidir feixe de luz sobre as mesmas. No paciente com ME não há
fotorreação, as pupilas permanecem fixas com tamanho que varia
do médio (4 a 6 mm) ao dilatado (6 a 8 mm).
Córneo-palpebral: são abertas as pálpebras do paciente e com
um instrumento delicado (SWAB) é realizado um estímulo da
córnea. Não ocorrendo o fechamento reflexo das pálpebras indica
morte encefálica.
Óculo-cefálico: são abertas as pálpebras e realizados movimentos
rápidos no sentido horizontal e vertical com o cabeça, observandose ausência de movimentos oculares (olhos de boneca). Este teste
não deve ser realizado em pacientes com suspeita ou confirmação
de lesão cervical.
Traqueal (pode ser realizado de várias maneiras): aspirando-se a
cânula orotraqueal ou traqueostomia, com fricção da traquéia ou
colocando-se abaixador de língua na região posterior da língua do
paciente. A ausência do reflexo de tosse com qualquer um destes
testes indica ME.
6
TESTES PARA ME
Óculo-vestibular: deve-se certificar que não há obstrução do
canal auditivo, pois isto dificulta a realização do exame. Eleva-se a
cabeceira do paciente a 30º, são injetados 50 ml de líquido frio
(como SF) no conduto auditivo externo. Observa-se por um minuto
a ausência de movimentos oculares, o que também confirma o
diagnóstico de ME. Este teste deve ser realizado nos dois ouvidos
com um intervalo mínimo de cinco minutos.
Prova da apnéia: devem ser tomadas algumas medidas para
garantir a segurança: monitorização cardíaca, monitorização da
pressão arterial e monitorização da oxigenação sangüínea.
Teste: ventila-se o paciente com O2 a 100% durante dez minutos;
é realizada uma gasometria arterial e instalado oxímetro de pulso,
então é desconectado o ventilador e instalado cateter de oxigênio
com fluxo de 6l/min; observa-se, então, durante dez minutos, se há
movimentos respiratórios; realiza-se outra gasometria arterial e
conecta-se o paciente novamente ao respirador. O teste será
positivo se não forem constatados movimentos respiratórios
durante o tempo em que o ventilador fica desconectado do paciente
e o nível de PCO2 da segunda gasometria for superior a 55 mm HG
Diagnóstico clínico de
Morte Encefálica
Diagnóstico Clínico de
Morte Encefálica
EXAMES PARA ME
Os
exames
complementares
para
comprovação de ME são os seguintes
a
EEG, Potencial Evocado Auditivo de Tronco
Encefálico: demonstra ausência de atividade
elétrica cerebral;
Angiografia
Cerebral,
Cintilografia
Radioisotópica,
Doppler
Transcraniano,
Ressonância
Magnética
de
crânio:
demonstra ausência de perfusão sangüínea
cerebral;
Pet-scan: demonstra ausência de atividade
metabólica.
Diagnóstico gráfico de
Morte Encefálica
Diagnóstico gráfico de
Morte Encefálica
Angiografia com fluxo
sangüíneo cerebral
Doppler transcranino com
fluxo sangüíneo cerebral
Angiografia com ausência de
fluxo sangüíneo cerebral
Doppler transcranino sem
fluxo sangüíneo cerebral
7
Processo de Doação de Órgãos
ÓRGÃOS E TECIDOS DOÁVEIS
Pâncreas, vasos sanguíneos, intestino, pele, coração,
válvulas cardíacas, córneas, medula óssea, fígado,
rim
DOAÇÃO EM VIDA
Rim, medula óssea, fígado e pulmão.
DOADOR CADÁVER
Identificação do potencial doador: morte violenta
ou não, suspeita de lesão irreversível do encéfalo
Atividade
Em trios, realizar leitura e destaque dos
principais aspectos dos texto fornecido
os artigos de pesquisa, identificar
objetivo, método, resultados e conclusões
Para os artigos de reflexão, identificar
principais conceitos
Ao final da análise, compor a opinião do
grupo em relação ao tema lido no artigo
Para
8
Imunologia dos Transplantes
Autoenxerto : Transplante de órgãos
ou tecidos procedentes do próprio
indivíduo
Não se desenvolve reações
Autólogo
Exemplos:
Ponte de Safena/Mamária
Enxerto de pele
Medula óssea
IMUNOLOGIA DOS TRANSPLANTES
Xenoenxerto
Transplantes entre indivíduos de espécies
diferentes
Enxerto fortemente rejeitado
IMUNOLOGIA DOS TRANSPLANTES
IMUNOLOGIA DOS TRANSPLANTES
Isoenxerto
Aloenxerto
Transplante
de órgãos ou tecidos entre
indivíduos geneticamente idênticos
Singênico
Não há desenvolvimento de resposta
Transplantes entre indivíduos da mesma
IMUNOLOGIA DOS TRANSPLANTES
REJEIÇÃO
espécie
Enxerto é rejeitado
Grande maioria dos enxertos
Processo que resulta da reação do sistema imune
do receptor aos antígenos do doador que estão
ausentes no receptor
Diferença antigênicas entre receptor e doador
levam a uma resposta imune específica no
receptor, levando a rejeição do enxerto (antígenos
de histo compatibilidade)
Principal tipo de célula envolvida: LINFÓCITOS T e
B
Principais barreiras de histo compatibilidade na
espécie humana são os sistemas ABO e HLA (tx
renal)
9
Testes para pesquisa de
compatibilidade
Testes: Crossmacth
Tipagem sanguínea
Compatibilidade do grupo sanguíneo
ABO
HLA
Processo de Doação de Órgãos
CONTRA-INDICACAO À DOAÇÃO
Absolutas
–
–
–
–
–
–
infecção não controlada
HIV positivo
neoplasia maligna
hipotermia
hipotensão
intoxicação exógena
Relativas
–
–
–
–
idade
peso
doenças pré-existentes (cirrose, diabetes, etc)
doenças virais como hepatite
10
Processo de doação de órgãos RS
Hospitais
de Referência Trimestral para
receber potenciais doadores e principais
equipes de retirada transplante no RS: HSL,
Santa Casa, HCPA
Comissões Intra-hospitalares de Doação de
Órgãos e Tecidos para Transplantes atuante
nas três instituições
Coordenação da RMO (HCPA)
Exemplo HCPA:
Esquema de sobreaviso 24h/dia
Enfermeiros assistenciais no HCPA
– Início: Na confirmação da RMO, cerca de 2h
antes do início da cirurgia
– Término: Entrega do corpo à família
– Tempo: de 04 a 10h
Atividades administrativas e técnicas
– Responsabilidade
pela
legalidade
do
procedimento
Referência da CNCDO para comunicação
com o HCPA
Atuação dos enfermeiros no
processo de transplante
Legislação para Enfermagem
Resolução COFEN 292/2004:
normatiza a Atuação
do Enfermeiro na Captação e Transplante de
Órgãos e Tecidos
Incumbências: receber e coordenar as equipes de
retiradas de órgãos, zelando pelo cumprimento da
legislação
vigente
e
ainda
executar
e/ou
supervisionar o acondicionamento do órgão até a
cirurgia de implante do mesmo ou transporte para
outra instituição.
Esta resolução além de respaldar a atuação do
enfermeiro no processo de doação, faculta-lhe a
oportunidade de contribuir para desenvolvimento
do mesmo.
Identificação do
potencial doador
(emergência e UTI)
Abordagem da
família para
consentimento
Manutenção da vida
do potencial doador
(UTI)
Coordenação da
RMO
Coordenação da RMO no HCPA
Enfermeiro
do BC aciona Enfermeiro
Coordenador (EC) por telefone, informando
órgãos a serem retirados e horário de início
da cirurgia
EC chega ao HCPA com 1h de antecedência
– CTI: verificação dos documentos legais
• Termo de consentimento (assinatura de familiar de 1°
grau, duas testemunhas, ambos pais)
• Termo de declaração de ME
• Atestado de óbito ou Laudo de encaminhamento ao
DML
• Laudo do exame comprobatório
Obs: nome legível, assinatura, especialidade e CRM
• Historia do doador
• Exames e sorologias do doador
• Coleta de HLA (TX Renal)
Assistência aos
candidatos a
transplantes –
possíveis receptores
Assistência nas
cirurgias de remoção e
de transplante (BC)
Assistência aos
transplantados (UTI,
unidade de internação,
ambulatório)
Retirada de Múltiplos Órgãos
A seqüência de RMOT está relacionada às especificidades de cada
órgão, como o tempo de isquemia fria e a complexidade do
procedimento cirúrgico.
O primeiro órgão a ser removido é o coração, seguido pelo
pulmão, fígado, pâncreas, rins e córnea.
A isquemia fria corresponde a uma proteção significativa aos
tecidos, se bem conduzida, especialmente se associadas às
soluções nutrientes geladas, como por exemplo as usadas no
transplante cardíaco.
Após a ME, o tempo em que os órgãos resistem é variável.
TEMPO DE ISQUEMIA FRIA
Coração: 4 h
Pulmão: 4 -6 h
Fígado: 12 h
Pâncreas: Até 20 h
Rins: Até 24 h
11
Retirada de Múltiplos Órgãos
Retirada de Múltiplos Órgãos
Retirada de Múltiplos Órgãos
Os passos cirúrgicos e a seqüência de atuação das
A RMO do doador exige a mesma técnica
asséptica
inerente
aos
demais
procedimentos cirúrgicos.
A
tricotomia
deverá
ser
realizada
imediatamente ao início da cirurgia desde a
região mentoniana até a região dos joelhos.
A assepsia abrange o pescoço, a face
anterior e lateral do tronco, abdômen e
membros inferiores até os joelhos. Os
campos cirúrgicos são fixados diretamente
na pele, após a anti-sepsia
equipes
deverá
ser
previamente
estabelecida
e
rigorosamente seguida.
A equipe de anestesia será a primeira a adentrar a sala
cirúrgica, pois promoverá o relaxamento muscular e o
controle das condições hemodinâmicas do doador.
A próxima equipe deverá ser a de cirurgia cardíaca e
pulmonar, que realizarão a esternotomia e inspeção dos
órgãos torácicos.
Os órgãos abdominais deverão ser os próximos a serem
inspecionados, através da abertura da parede abdominal
pelas equipes de fígado, pâncreas, rins e intestino, após
esta inspeção o fígado e o pâncreas são dissecados e
preparados para posterior perfusão
Acondicionamento e
armazenagem dos órgãos
Acondicionamento e
armazenagem dos órgãos
Coração
O coração retirado deverá ser colocado em um saco plástico estéril com
soro fisiológico a 4ºC, até ficar completamente imerso, amarrando a
abertura deste com fita cardíaca. Após, é colocado em um segundo saco
plástico com soro fisiológico gelado e amarrado também com fita
cardíaca. Ainda é colocado em um terceiro saco plástico lacrado, que
deverá conter uma etiqueta com o horário da cardioplegia
Para a realização do transporte desse enxerto deverão ser utilizados
recipientes térmicos contendo blocos de gelo suficientes para cobri-lo.
Pulmões
A remoção é feita em bloco, ou seja, os dois pulmões ligados ao átrio
esquerdo são colocados em um saco plástico estéril contendo três litros
de soro fisiológico a 10ºC. Este é hermeticamente fechado e o conjunto é
colocado em mais dois sacos estéreis e mantido em geladeira térmica
Fígado e Pâncreas
O acondicionamento desses órgãos deverá ocorrer separadamente,
utilizando solução de UW à 4ºC. Cada saco plástico estéril será
preenchido com um litro da solução de preservação e lacrado com fita
cardíaca. Esse saco deverá ser envolvido em outro e novamente lacrado
com fita cardíaca. Até a utilização dos enxertos estes deverão
permanecer em geladeira térmica, coberto com gelo não estéril
Rins
Cada rim deverá ser mantido em um saco plástico estéril contendo 500
ml de solução de UW ou solução de Euro- Collins a 4ºC. O primeiro saco
estéril deverá ser lacrado com fita cardíaca e acondicionado em um novo
saco contendo gelo moído. Imediatamente deverão ser armazenados a
4ºC em geladeira térmica com gelo não estéril
Córneas
As córneas devem ser armazenadas em solução de preservação a 4ºC,
em frascos estéreis. O frasco (em câmara úmida) deverá ser forrado com
gaze umedecida em solução salina para receber o globo ocular após sua
enucleação. A irrigação do globo ocular deverá ser feita com solução
salina e antibiótico (Cloranfenicol)
As soluções de preservação de órgãos e tecidos devem
ser resfriadas a 4º C e infundidas nesta temperatura. Os
tipos de soluções utilizadas e a quantidade que deverá
ser infundida na veia porta e na aorta, de acordo com
cada órgão a ser armazenado são
–Perfusão do coração e pulmões:
- Solução Saint Thomas 1 e Saint Thomas 2 ;
- Soluções preparadas contendo potássio, tamponadas com bicabornato;
-Pulmonar: solução com Dextran e potássio na dosagem normal a do plasma.
–Perfusão dos Órgãos Intra-abdominais:
-
Solução de Wisconsin (UW): seu custo é elevado, pois para cada doador utiliza cinco
litros dessa solução. Apresenta maior tempo de armazenamento dos órgãos e aumento
significativo na taxa de sobrevida dos enxertos.
- Solução de Euro Collins: esta solução apresenta a vantagem de ter seu custo inferior ao da
UW, porém seu tempo de armazenamento é reduzido a metade.
– Bloco Cirúrgico:
• Contatar CNCDO para confirmação
• Verificar sala cirúrgica, materiais, soluções de manutenção,
frasqueiras, gelo
• Contatar equipes cirúrgica e anestésica para confirmação do
horário
• Receber equipes
• Autorizar e receber doador
• Revisar documentação legal novamente
• Auxiliar na profilaxia antimicrobiana
• Acompanhar procedimento (realizar perfusão hepática com
Belzer e renal com Collins)
• Coletar 2 amostras para Cross-Match
• Encaminhar
Imunologia HCPA (bipar farmacêutica)
e
contatar CNCDO para encaminhar à Santa Casa
• Contatar equipes urologia e oftalmologia após perfusão
hepática para informar estimativa de horário
• Contatar família para informar estimativa de horário
12
• Contatar DML, se necessário
• Preencher relatórios
• Identificar exames, órgãos, frasqueiras
• Certificar
que todas equipes preencheram
descrições e relatórios
• Verificar fechamento do corpo e tamponamento
• Transportar corpo ao morgue
– Morgue
• Contatar segurança
• Acompanhar necrópsia, se necessário
• Entregar corpo à família, com documentação
• Comunicar CNCDO término do processo
Contato permanente com CNCDO – média de 20
ligações em cada processo
Assistência na prevenção de
complicações de Tx cardíaco
Protocolos específicos para cirurgias
de remoção e transplantes
Transplante Cardíaco
Período intra-operatório
A atuação da enfermagem nesse período tem como
objetivos: avaliar, detectar e intervir precocemente
nas
possíveis
complicações
intra-operatórias;
assegurar o posicionamento em mesa cirúrgica livre de
danos devido ao tempo cirúrgico prolongado (5 a 6
horas); realizar tricotomia em sala de cirurgia,
utilizando tricotomizador elétrico; realizar a sondagem
vesical de demora utilizando dispositivo fechado, com
técnica asséptica; monitorar hemorragias e perdas de
líquidos, bem como a entrada de soluções parenterais
(soroterapia,
hemoterapia
e
medicamentos);
administrar hemoderivados junto à equipe da
anestesia;
Realizar
coleta de exames laboratoriais de
urgência; prevenir a ocorrência de hipotermia por
meio da administração de soluções parenterais
aquecidas (as soluções podem ser aquecidas em
microondas por até 60 segundos, evitando-se a
desnaturação de seus componentes a qual ocorre
quando a temperatura atinge 42ºC) ou a utilização
de insuflação de ar aquecido; prevenir a ocorrência
de lesões ulcerativas por pressão, utilizando-se
dispositivos acolchoados (gel ou espuma), ou
curativos protetores (hidrocolóide), protegendo-se
as saliências ósseas (regiões occipital, escapular,
cubital, sacral, calcâneos).
13
Nefrectomia doadora
Incisão anterior, transperitoneal
Mesmos cuidados técnicos adotados
na nefrectomia com doador vivo
da aorta - perfusão
renal
solução Euro-Collins gelada
(4co)
Rins
mantidos em geladeira ou
recipientes com gelo e dentro de
caixas com isolamento térmico.
Clampeamento
Complicações do Tx Renal
Complicações: rejeição
Função reduzida ou ausente do enxerto nos
1. Hiperaguda (atualmente rara)
primeiros dias de P.O. pode ser causada por
hipovolemia,
hipertensão,
obstrução
urinária intrínseca ou extrínseca, fístula
urinária, trombose arterial ou venosa da
artéria renal, necrose tubular aguda ou
rejeição
Para estabelecer o diagnóstico, medidas
rápidas, uma vez que a futura viabilidade do
enxerto pode depender da rapidez com que
o tratamento é instituído
2. Aguda (a mais comum) – pode ser tratada
em 80% dos casos
1. Normal aparece nos primeiros dias, mas pode
ocorrer até um ano após o Tx.
arterial, febre, aumento de
volume renal, dor, diminuição do volume
urina, aumento de peso.
2. Hipertensão
3. Crônica – tempo aparecimento é muito
variável; difícil diagnóstico - biópsia por
punção órgão; prognóstico ruim.
14
Complicações: infecção
Vários
fatores, o mais importante é a
imunossupressão.
Infeccão, pulmonar, diagnóstico difícil,
sombra anormal ao Rx tórax (febre e
leucocitose podem estar ausente)
ITU 26 à 61% dos casos de Tx renal
A alta incidência de ITU é atribuída a
ureteroneocistotomia, cateterização vesical
e a hipotonia da bexiga
Sepse: mesmos sinais e sintomas dos
pacientes não transplantados
– Alta taxa de mortalidade
Imunossupressão
Drogas de indução e de manutenção
– tacrolimus
ou ciclosporina,
azatioprina e prednisona.
micofenolato ou
Para saber mais...
CIDOTT/HCPA: www.hcpa.ufrgs.br
Associação Brasileira de Transplante de Órgãos:
www.abto.org.br
Sistema Nacional de Transplantes - Ministério da
Saúde:
portal.saude.gov.br/portal/saude/area.cfm?id_area
=1004
Campanha Doe Vida - Ministério da Saúde:
www.doevida.com.br
Aliança Brasileira pela Doação de Órgãos e Tecidos:
www.adote.org.br
NATCO – The Organization for Transplant
Professionals: www.natco1.org
[email protected]
15