1
Aminoácidos e Proteínas
As proteínas, além de constituírem o componente celular mais abundante, são as moléculas
mais diversificadas quanto a sua forma e função. Praticamente todos os processos vivos dependem
dessa classe de moléculas.
Alguns exemplos:
- Colágeno e Elastina - formam os componentes do esqueleto celular e estrutura de sustentação.
- Enzimas - catalisadores biológicos
- Transporte de moléculas - ex: hemoglobina - transporta oxigênio
- atuam no mecanismo contrátil dos músculos- actina e miosina
- controlam a atividade dos genes (expressão gênica), entre outros.
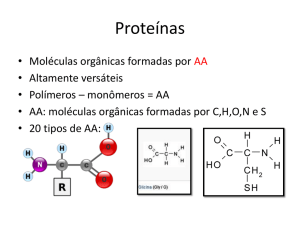
As proteínas são sintetizadas a partir de 20 aminoácidos diferentes:
Os aminoácidos são compostos que apresentam, na sua molécula, um grupo amino (-NH2) e um
grupo carboxila (-COOH); a única exceção é a prolina, que contem um grupo imino (-NH-) no lugar
do grupo amino.
As propriedades das cadeias laterais dos aminoácidos.
As cadeias laterais dos aminoácidos são importantes para a conformação das proteínas e, portanto,
para sua função.
Os aminoácidos são classificados, de acordo com a polaridade do grupo R, em duas grandes
categorias: aminoácidos apoIares (com grupo R hidrofóbico) e aminoácidos polares (com grupo R
hidrofílico).
Os aminoácidos apoIares -Têm geralmente uma localização interna na molécula de proteína.
Os aminoácidos classificados como polares são os que têm, nas cadeias laterais, grupos com carga
elétrica líquida que os capacitam a interagir com a água. São geralmente encontrados na superfície da
molécula proteica.
Estes aminoácidos são subdivididos em três categorias:
- aminoácidos básicos – (grupo R carregado positivamente)
- aminoácidos ácidos - (grupo R carregado negativamente)
- aminoácidos polares sem carga.
1
2
Algumas observações sobre os aminoácidos:
Grupo dos aminoácidos apolares - têm grupos R constituído por cadeias orgânicas com caráter de
hidrocarboneto, que não interagem com a água. Têm geralmente uma localização interna na molécula
de proteína.
A glicina é um aminoácido de estrutura mais simples, permitindo assim um mínima restrição
estérica na estrutura de uma proteína.
A prolina é um aminoácido de estrutura mais complexa o que reduz a flexibilidade estrutural da
proteína.
Os grupos R aromáticos - são relativamente não polares (hidrofóbicos).
Grupo R polar, mas não carregado - são hidrofílicos, porque eles contêm grupos funcionais que
formam ponte de hidrogênio com a água.
Ligação Dissulfeto. A cadeia lateral da cisteína(contêm o grupo sulfidrila (-SH), o qual é um
componente importante do sítio ativo de muitas enzimas. Nas proteínas, os grupos-SH de duas
cisteínas podem torna-se oxidados e formar um dímero (união de duas moléculas de cisteínas por uma
ponte de dissulfeto (-S-S), formando a cistina).
Podemos notar que em todos os aminoácidos, exceto a glicina, o carbono ? é assimétrico, ligado a
quatro grupos diferentes:
- um grupo carboxila
- um grupo amino
- um grupo R (radical)
- hidrogênio
O átomo do carbono ? é um carbono quiral ou opticamente ativo. A glicina é é exceção, pois seu
carbono
Os centros quirais geram enantiômeros - moléculas que não sobreponíveis às suas imagens
espetaculares.
Em geral os bioquímicos usam a convenção de Fischer para descrever as diferentes formas de
moléculas quirais.
L - (levorrotatório) rotação da luz polarizada para a esquerda
D - (dextrorrotatório) rotação da luz polarizada para a direita
A molécula protéica é formada por mais de 50 aminoácidos ligados entre si através das
ligações peptídicas.
Os aminoácidos encontrados nas proteínas têm configuração esteroquímica L, são Laminoácidos.
Os D-aminoácidos foram encontrados apenas em pequenos peptídios da parede de células
bacterianas e alguns peptídios com função de antibióticos.
Em solução aquosa os aminoácidos estão ionizados, e podem agir como ácidos e bases
2
3
Os aminoácidos que têm um único grupo amino e um único grupo carboxíla, são
conhecidos como “zwitterions”, moléculas que carregam grupos de polaridades opostas. Um
aminoácido zwitterions em pH fisiológico, tem o grupo amino protonado e o grupo carboxila
desprotonado
PROTEÍNAS
Proteínas: são macromoléculas polipeptídicas, isto é, são moléculas muito grandes, formadas pela
união do grupo carboxila de um aminoácido com o grupo amina do outro aminoácido, chamada de
ligações peptídicas.
Um dipeptídeo formado continua tendo um grupo amina numa das terminações e um grupo
carboxila na outra.
Nestas terminações podem ser adicionadas novos aminoácidos originado:
- tripeptídeo, tetrapeptídeo, até chagar em oligopeptídio.
polipeptídeos.- mais de 10 aminoácidos na molécula denominamos
Estruturas das Proteínas:
Níveis de estruturas:
- Estrutura primária: è a seqüência de aminoácidos ao longo da cadeia polipeptídica. Cada proteína
é diferente das outras por sua estrutura primária.
Exemplo:
Arg - Leu - Ala – Arg - Asp - Ala - Gly -...
- Estrutura secundária:As moléculas de proteínas são formadas de longas cadeias de aminoácidos
que podem se enrolar sobre si mesma em forma de α-hélice ou folha β-pregueada.
Estrutura terciária:A cadeia polipeptídica pode apresentar dobras sobre si mesma adquirindo uma
conformação espacial própria.
Estrutura quaternária:é um grau de organização mais alto, determinado pela combinação de duas ou
mais cadeias polipeptídicas Exemplo: A Hemoglobina que é um tetrâmero, formado por duas cadeias
α-hélice e duas cadeias β-pregueada.
Estado nativo da proteína - A forma espacial de cada proteína é a principal responsável por
suas propriedades biológicas (enzimáticas ou estruturais).
Desnaturação da proteína.Quando ocorre a sua desorganização espacial, a proteína perde
suas propriedades biológicas.
O dobramento das cadeias e, portanto, a conformação das moléculas, depende:
- atrações eletrônicas entre cadeias laterais de aminoácidos
- formação de pontes de hidrogênio ou pontes de dissulfeto entre eles;
- ligações hidrofóbicas entre cadeias laterais de aminoácidos que não se misturam com a água.
3
4
Degradação e Excreção de Proteínas
Introdução:
Os aminoácidos contêm nitrogênio além dos átomos de carbono, hidrogênio e oxigênio. Este
nitrogênio não pode ser armazenado e os aminoácidos em excesso às necessidades de biossíntese das
células são imediatamente degradados.
A primeira fase do catabolismo (degradação) dos aminoácidos envolve a remoção dos grupos
alfa-aminos por transaminação e desaminação oxidativa, formando amônia e ceto-ácidos
correspondentes. Uma porção da amônia livre é excretada na urina, mas a maior parte é usada na
síntese de uréia.
Os esqueletos de carbonos dos ceto-ácidos são convertidos em produtos intermediários de rotas
produtoras de energia.
A seguir estudaremos os processos citados acima.
Transaminação:
É o processo pelo qual um aminoácido (aa) transfere seu grupo amino para um cetoácido (ka).
Desta forma, o aminoácido converte-se em um cetoácido e o cetoácido converte-se um aminoácido,
formando assim outro aminoácido com outra cadeia lateral (R2).
As enzimas que catalisam estas reações são chamadas de transaminases ou aminotransferases.
Cada aminoácido depende de uma enzima específica (transaminase) que catalisa a sua conversão em
cetoácido. Duas transaminases mais largamente distribuídas no tecido é a TGP (transaminases –
glutamico-pirúvica) e a TGO (transaminase- glutâmico-oxalética).
Portanto, a transaminação é uma das maneiras pelo quais os aminoácidos não essenciais são
produzidos, desde que exista o cetoácido de cadeia lateral correspondente.
Os grupos amino na sua maioria dos aminoácidos são, conseqüentemente, direcionados para a
formação de glutamato e de aspartato.
No processo de transaminação, o piridoxal fosfato (PAL), ao se ligar com o grupo amina do
aminoácido, com a função de transportará a amina para o cetoácido, torna-se momentaneamente em
piridoxamina (PAM), e após realizar o transporte o piridoxamina (PAM) retorna a sua condição
original, ou seja, piridoxal fosfato (PAL).
As aminotransferases são enzimas intracelulares, havendo, baixo níveis dessas enzimas no
plasma que representam a liberação dessas enzimas durante a renovação celular normal.
Quando há um aumento dos níveis plasmático dessa enzimas indica lesão em células ricas nessas
enzimas.
Exemplos:
-Trauma físico e processos patólógico que podem provocar lise celular, resultando na liberação das
enzimas aminotransferases para o sangue.
Doenças Hepáticas – Os níveis sanguíneos de TGO e TGP estão elevados em quase todas as
doenças hepáticas, mas estão especialmente altos em doenças que causam necrose celular como a
hepatite viral grave, lesão tóxica e colapso circulatório prolongado.
A TGO (AST) é mais específica para as doenças hepáticas, pois, o fígado contém maiores
quantidades dessa enzima.
Doenças não hepática – As aminotransferases podem estar elevadas em doenças não hepáticas, como
infarto do miocárdio e doenças musculares. Essas doenças, no entanto, são geralmente clinicamente
distintas das doenças hepáticas.
4
5
Desaminação Oxidativa:
Para que o aminoácido seja degradado é necessário que ocorra a eliminação da sua fração
amínica. A este processo chamamos de desaminação oxidativa.
A desaminação é o processo pelo qual o aminoácido libera o grupo amina (NH3+) na forma de
amônia (NH4+) e se transforma em um cetoácido. Estas reações são catalisadas pelas enzimas
desidrogenases, ou desaminases que possuem como coenzima o NADP.
O glutamato será desaminado, ou seja, o grupo amina (originário dos aminoácidos) foi liberado
na forma de amônia. Esta reação foi catalisada pela enzima Glutamato desidrogenase.
Alguns aminoácidos são desaminados por reações especiais, tais como: glicina, histidina,
lisina, prolina, serina e treonina que não participam de reações de trasaminação e seu grupo amina é
removido reações particulares de cada um deles.
Destinos da cadeia carbônica dos aminoácidos:
Após a retirada da parte nitrogenada (como amônia no processo de desaminação oxidativa), a
cadeia carbônica remanescente do aminoácido será encaminhada para o metabolismo energético,
integrando-se com o metabolismo de carboidrato e lipídios. Aqueles que produzem glicose são
chamados glicogênios e os que produzem Acetil-CoA serão chamados de cetogênicos.
São considerados Glicogênicos – Alanina Arginina, Aspartato, Cisteína, Glutamato, Glicina,
Histidina, Metionina, Prolina, Serina, Treonina e Valina.
São considerados Cetogênicos – Leucina
São considerados Glicogênicos e Cetogênicos – Isoleucina, Lisina, Fenilalamina, tirosina e
Triptofano.
Ciclo da Uréia
A uréia é o principal composto nitrogenado encontrado na urina, é altamente solúvel em água.
Os dois átomos presentes na fórmula da uréia são provinientes da amônia (NH4+) e aspartato.
A síntese da uréia é feita no fígado, através do processo chamado de ciclo da uréia. A síntese se
inicia na matriz mitocondrial, até a formação do carbamoil-fosfato e depois é transportado para o
citosol e reage com a ornitina, originando a citrulina. A citrulina recebe o grupo amino do aspartato
originando a arginina. A arginina sofre uma cisão levando a formação da uréia e ornitina.
As enzimas envolvidas são: carbamoil-fosfato sintetase, ornitina transcabamoilase,
arginossucinato sintetase, arginossucinato liase, arginase.
A conversão da maior parte da amônia em uréia é fundamental para manter baixa a
concentração desse íon nos tecidos, pois a amônia é tóxica para os tecidos, principalmente para o
cérebro.
5
6
Enzimas
Enzimas -são catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a
sua velocidade. A presença de enzimas nas reações celulares aumenta a velocidade da reação por
serem altamente específicas.
Propriedades gerais das enzimas:
1- Velocidade das reações mais rápida - as reações catalisadas por enzimas são de 106 a 1012 vezes
mais rápidas que as correspondentes não catalisadas.
2- Condições de reações mais brandas – as reações catalisadas por enzimas ocorrem em
temperaturas inferiores a 100 °C e pH quase neutro.
3- Maior especificidade da reação
4- Capacidade de regulação – As atividades catalíticas de muitas enzimas pode ser regulada na sua
concentração celular e sua atividade, permitindo assim ajuste em diferentes condições fisiológicas. Os
mecanismos desses processos regulatórios incluem o controle alostérico, a modificação covalente de
enzimas e a variação nas quantidades de enzimas sintetizadas.
Classificação e nomenclatura das enzimas:
As enzimas são comumente denominadas adicionando o sufixo ase ao nome do substrato da enzima
ou a uma expressão que descreva a sua ação catalítica. Esta denominação apresenta exceções como é o
caso das enzimas digestivas: tripsina, pepsina, etc...
Especificidade dos substratos.
As forças não-covalentes por meio das quais os substratos e outras moléculas se ligam às
enzimas são similares em caráter às forças que regem a conformação das próprias proteínas. Ambas
envolvem interações de van der Waals, interações eletrostáticas, pontes de hidrogênio e interações
hidrofóbicas. Em geral o sítio de ligação do substrato a enzimas consiste em um sulco na superfície da
enzima, complementar ao formato do substrato (complementaridade geométrica). Além disso, os
resíduos de aminoácidos que formam o sítio de ligação estão organizados de modo a formar interações
de atração específicas com o substrato (complementaridade eletrônica).
A ligação do substrato na enzima se dá em uma pequena e bem definida região da enzima
chamada de centro ativo (ou sítio ativo da enzima). O substrato deve ter a forma espacial adequada
para se se alojar no centro ativo da enzima. Com isto esta ligação permite uma especificidade para a
catálise. Há enzima que aceitam como substrato qualquer açúcar de 6 carbono, enquanto outras só
reconhecem em desses substrato, a glicose.
6
7
Os fatores que interferem na atividade enzimática:
1- pH
A maioria das enzimas apresenta um valor de pH para qual a atividade da enzima é máxima. A
velocidade diminui a medida que o pH se afasta do valor ótimo, que é característico para cada enzima.
Geralmente o pH é neutro.
O pH ótimo depende do número e tipo de grupos ionizáveis que uma enzima apresenta e da seqüência
em que estão organizados, ou seja,dependem de sua estrutura primária.
2- Temperatura
A temperatura também interfere na atividade da enzima. Se aumentarmos muito a temperatura
a enzima pode perder sua forma nativa que permite desempenhar sua função levando a um processo
de desarranjo estrutural (perda da estrutura terciária) chamado de Desnaturação. A desnaturação
provoca drásticas alterações conformacionais na molécula, acarretando na perda da catálise.
Ex: acima de 50 a 55 °C a maioria das proteínas globulares são desnaturadas.
3- Concentração do Substrato.
Co-fatores:
Muitas enzimas necessitam de associação com co-fatores não protéicos (moléculas ou íons)
para exercer seu papel catalítico.
Os cofatores comumente encontrados incluem íons metálicos (Cu2+, Fe3+ ou Zn2+ etc) ou
moléculas orgânicas, não protéicas, de complexidade variada, que recebem o nome de coenzimas,
tal com o NAD+.
As coenzimas são co-fatores que se associam temporariamente com uma dada molécula
enzimática, de maneira que elas funcionam como co-substratos.
Outros co-fatores são conhecidos como grupos prostéticos, que estão permanentemente ligados a
sua proteína geralmente através de ligações covalentes. Ex: heme o citrocromo c é fortemente ligado a
proteína por uma extensa rede de interações hidrofóbicas e pontes de hidrogênio junto a ligações
covalentes entre o heme e regiões específicas das proteínas.
O conjunto da enzima com o seu co-fator apropriado e cataliticamente ativo é o chamado de
holoenzima. A proteína enzimaticamente inativa resultante da remoção do co-fator da holoenzima é
chamada de apoenzima; portanto a apoenzima é a porção protéica da holoenzima.
Apoenzima (inativa) + co-fator « holoenzima (ativa)
INTERAÇÃO ENZIMA-SUBSTRATO
Geralmente há uma grande diferença de tamanho entre as moléculas de enzimas e as de seus
substratos. As enzimas são macromoléculas protéicas - mesmo as mais simples são formadas de mais
de uma centena de aminoácidos - e seus pesos moleculares variam de 10.000 a alguns milhões,
enquanto o peso molecular dos substratos é muitas ordens de grandeza inferior.
Embora o total da molécula enzimática seja necessário para o papel catalítico, a ligação com o
substrato dá-se apenas em uma região pequena e bem definida da enzima. Esta região à qual o
substrato se liga é chamada centro ativo (ou sítio ativo) da enzima. O centro ativo é formado por
resíduos de aminoácidos, trazidos à proximidade uns dos outros pelos dobramentos da cadeia
polipeptídica que definem a estrutura terciária da proteína. O centro ativo, assim organizado, constitui
uma cavidade com forma definida, que permite à enzima "reconhecer" seu substrato. De fato, uma
molécula, para ser aceita como substrato, deve ter a forma espacial adequada para alojar-se no centro
ativo e grupos químicos capazes de estabelecer ligações precisas com os radicais do centro ativo.
7
8
As enzimas aceleram a velocidade da reação por diminuir sua energia de ativação.
A velocidade das reações é explicada pela teoria das colisões. Esta teria estabelece que, para a
molécula reagir, as moléculas presentes em uma solução devem colidir com orientação apropriada e
que a colisão deve levá-las a adquirir uma quantidade mínima de energia que lhes permita atingir os
estados reativos, chamados de estado de transição. Para levar todas as moléculas de um mol até o
estado de transição necessita uma quantidade de energia, chamada de energia de ativação.
A energia de ativação é, portanto a barreira que separa os reagentes dos produtos. A
velocidade de uma reação será diretamente proporcional ao número de moléculas com energia
de ativação igual ou maior do que a energia do estado de transição.
Pode-se aumentar a velocidade de uma reação de 3 maneira:
1aumentando a concentração de moléculas em solução
2elevando a temperatura
3diminuição da energia de ativação – pode ser usados catalisadores.
Os catalisadores são substâncias que aceleram a velocidade de uma reação, sem alterar a
proporção entre reagente e produtos encontrada no final da reação e sem serem efetivamente
consumidos durante o processo.
A presença de um catalisador pode alterar essa velocidade e pode alterar também a quantidade de
energia que deve ser emprestada ao sistema para início das reações (energia de ativação).
Cinética da reação enzimática.
O estudo da cinética das reações baseia-se na velocidade das reações, que é diretamente
proporcional a concentração do reagente. Como a medida que se processa a reação a concentração do
reagente diminui e portanto a velocidade também, passando a ser proporcional a nova concentração,
estabeleceu-se a velocidade inicial (v0) proporcional a concentração inicial de A.
A reação enzimática processa-se em duas etapas:
1- A enzima (E) e substrato (S) formam um complexo transitório (ES)
O produto é liberado (P) e a enzima volta na forma
E+S
«
ES ® P + E
Os pressupostos acima foram estabelecidos por Michaellis e Menten, que com tratamento
matemático desvendaram a cinética de um grupo de enzimas chamadas de enzimas michaelianas.
As enzimas estão muito mais diluídas em solução do que o substrato e os números de moléculas
de enzimas é muito inferior ao do substrato
Com maiores concentrações de substrato, a velocidade de formação do Produto é cada vez maior,
porque estará formando cada vez mais complexo ES.
Se a quantidade de substrato for muito grande, a quantidade, a concentração de E será
praticamente nula, encontrando-se toda a enzima disponível sob a forma de ES.
Maior concentração possível do complexo ES é na situação onde há formação de 100% e a
reação será processada na maior velocidade possível. Esta concentração é dita saturante e, a partir
dela novas concentrações de substrato não terá efeito sobre a velocidade da reação, que atingiu seu
valor máximo – Velocidade máxima (Vmax). Assim a velocidade da reação é sempre proporcional à
concentração de ES.
A velocidade inicial é obtida medindo-se a quantidade de produto formado em tempos
suficientemente curtos para que no máximo 5% do substrato tenha sido transformado em produto.
8
9
Constante de Michaelis (Km)
Km é a concentração do substrato na qual a velocidade da reação corresponde a metade da
velocidade máxima. Portanto uma enzima que tiver o menor valor de Km, ela atingirá a máxima
eficiência catalítica em baixas concentrações do substrato.
Ex: a hexoquinase pode aceitar a glicose ou a frutose como substrato. Mas o Km para a glicose é
0,15 mM e para a frutose é 1,5 mM. Isto significa que para a frutose ser substrato para a hexoquinase é
necessário uma concentração de 10 vezes maior (1,5 mM) do que a glicose (0,15mM), portanto a
hexoquinase tem uma maior afinidade pela glicose do que pela frutose
Equação de Michaelis – Menten
Vo = Vmáx [S]
Km + [S]
Inibidores da atividade enzimática.
A atividade enzimática pode ser diminuída por um grande número de substância, genericamente
chamadas de inibidores. A atividade da enzima depende da concentração do inibidor em um
determinado instante, portanto como os inibidores são produzidos pelas próprias células, a variação da
sua concentração é um recurso usado para controlar as velocidades das reações enzimáticas.
Inibidores Irreversíveis – são aqueles que reagem geralmente através de ligações covalentes com as
moléculas das enzimas, destruindo-as parcialmente.
Um exemplo de inibidores irreversíveis é a penicilina seu inibidor liga-se especificamente a enzimas
da via de síntese da parede bacteriana, inibindo-as, desprovidas de parede as células ficam sujeita a
lise bacteriana.
Inibidores reversíveis – são aqueles em que a inibição está relacionada com um equilíbrio entre
enzima- inibidor. Podem ser competitivo e não competitivo.
Inibição competitiva ( Ic )- ocorre quando o inibidor e o substrato tem estruturas semelhantes entre si
e competem pelo centro ativo da enzima. Neste caso a velocidade máxima permanecerá inalterada e o
valor de Km (afinidade da enzima pelo substrato) será aumentada.
O complexo EI não gera produto e, portanto, a atividade enzimática estará diminuída de acordo
com a fração de enzima que estiver ligada ao inibidor, mas se a molécula estiver ligada ao substrato
formará o complexo ES e haverá produto, ou seja, nesta situação encontramos frações de enzimas
ligadas ao substratos e outras enzimas ligadas ao inibidor.
A velocidade máxima da reação será a mesma da reação efetuada sem a presença do inibidor,
porem irá necessitar de uma maior concentração do substrato do que as reações sem a presença do
inibidor, isto mostra que aparentemente há uma alteração no Km.
Inibição não competitiva (INC) - o inibidor combina-se reversivelmente com a molécula da enzima
em um outro ponto da estrutura, que não seja o seu centro ativo. Estes inibidores não são semelhantes
estruturalmente à molécula do substrato. Neste caso a velocidade será alterada e o valor de Km
(afinidade da enzima pelo substrato) permanecerá inalterado.
O ponto de ligação do inibidor não competitivo é a cadeia lateral do aminoácido. Ex: o grupo
OH da serina e o SH da cisteína.
9
10
Com a ligação do inibidor na enzima, ela se comporta como se houve menor
quantidade de enzima (neste caso enzima ativa) o que faz com que a velocidade da reação diminua em
comparação a ausência do inibidor para qualquer concentração de substrato. O valor de Km parece
coincidir com o valor do novo km proporcionado pela diminuição da velocidade.
Inibição alostérica não obedecem à cinética de Mochaellis-Menten
As enzimas alostéricas apresentam normalmente 2 centros ativos: um para o substrato a ser
transformado e outro para um inibidor que regula sua atividade, daí o seu nome. Geralmente as
enzimas alostéricas possuem estrutura quaternária, e não seguem a cinética de Michaelis-Menten,
mostrando-se uma curva sigmóide.
Nas enzimas alostéricas, a ligação do substrato a um centro ativo pode afetar as propriedades dos
outros centros ativos na mesma molécula de enzima. A atividade destas enzimas pode ser regulada por
inibidores, que se ligam a locais que não são os centros catalíticos.
Ex: A ligação do oxigênio à hemoglobina é afetada por H+ e CO2.
Introdução: Estrutura dos ácidos nucleicos
O DNA é uma macromolécula filamentar muito longa, feita de um grande número de
unidades de desoxirribonucleotídeos.
Os nucleotídeos são compostos por: um açúcar (pentose), a desoxirribose (DNA) ou a ribose
(RNA), uma base nitrogenada (base nitrogenada heterocíclica) ligada ao carbono 1’ da pentose e um
ou até 3 grupos fosfatos (PO4-), ligados ao carbono 5’ da pentose.
As bases nitrogenadas podem ser:
Purinas – adenina (A) e guanina (G)
Pirimidinas – citosina (C) e timina (T) ou uracila (U)
As bases ligam-se ao carbono 1’ da pentose através de uma ligação glicosídica b. A molécula
composta pela base nitrogenada ligada ao açúcar, sem grupos fosfato, é denominada nucleosídeo.
Os desoxirribonucleotídeos são denominados de acordo com a base nitrogenada componente.
Na molécula de DNA, os desoxirribonucleotídeos formam cadeias ligadas entre si por pontes
fosfodiésteres estabelecidas entre o grupo fosfato e o grupo OH (hidroxila) do carbono 3’ do
nucleotídeo adjacente.
Estrutura do RNA
Existem semelhanças entre a estrutura do RNA e do DNA. Ambos são polímeros lineares de
subunidades ligadas entre si por ligações fosfodiésteres 5’ ® 3’. Entretanto, na molécula de RNA, o
açúcar presente é a ribose, e a timina (T) é substituída pela uracila (U). As outras 3 bases adenina,
citosina e guanina estão presentes. O RNA está normalmente na forma de fita simples, embora
pareamento entre C e G e entre A e U possam ocorrer entre regiões da própria cadeia, formando
estruturas secundárias que são importantes na função dos RNAs e no reconhecimento proteínas-RNA.
Alguns RNA podem formar fita dupla. Alguns vírus podem ter RNA de fita dupla no genoma.
METABOLISMO DOS NUCLEOTÍDIOS:
Os ácidos nucléicos encontram-se em todas as células. As vias de biossíntese de seus
precursores diretos, os nucleotídeos, são comuns a todos os seres vivos, mas há diferença dos produtos
nitrogenados formados que podem ser excretados ou não.
Uma das bases nitrogenadas mais importantes é derivada do grupo das purinas ou
pirimidinas que representam a estrutura ao lado.
10
11
·
As bases nitrogenadas podem ligar-se a pentoses, formando os nucleosídeos (ose =
açúcar) correspondente, através de ligações glicosídicas.
·
Quando há ligação dos nucleotídeos, há a formação do DNA ou RNA.
Digestão dos ácidos nucléicos:
As bases nitrogenadas, metabolicamente são derivadas dos aminoácidos. São, portanto,
produtos endógenos, isto é, não são necessariamente recebidas pela dieta, embora possa estar presente
nos produtos de origem animal ou vegetal.
Os ácidos nucléicos da dieta, contudo, são digeridos na seguinte seqüência de eventos:
Degradação dos ácidos nucléicos da dieta no intestino delgado.
Biossíntese de novos nucleotídios púricos:
As purinas são constituídos de uma série de compostos, incluindo aminoácidos (aspartato,
glicina, glutamina), CO2, e derivados do tetraidrofolato (ácido fólico). O anel de purina é constituído
por uma série de reações que adicionam os carbonos e nitrogênio à ribose 5- fosfato. Ribonucleotídio
da hipoxantina ou ácido inosínico (IMP) é o primeiro produto formado.
Síntese de GTP e ATP:
Ácido inosínico (IMP) constitui um composto-chave na seqüência metabólica dos purinoribonucleotídios: ácidos adenílico (AMP), ácido guanílico (GMP) e seus derivados di- e trifosfstos
(ADP, ATP, GDP, GTP) .
11
12
Metabolismo das Bases Pirimídicas:
Ao contrário da síntese do anel de purina, em que o anel é construído sobre a ribose 5’-fosfato
preexistente, o anel de pirimidina é sintetizado antes de ser ligado à ribose 5’-fosfato. As fontes de
carbono e de nitrogênio são o carbamil-fosfato e aspartato.
Porfirinas
Do grupo das metaloporfirinas, fazem parte as metaloporfirinoproteínas, entre as quais
se encontra algumas proteínas de grande importância biológicas como:
Hemoglobina – transporte de oxigênio
Citocromos – envolvidos no transporte de elétrons na cadeia respiratória entre outras
Mioglobina – armazenamento de oxigênio no sangue
Citocromo P450 – Hidroxilação de xenobióticos
Catalase - degradação de Peróxido de hidrogênio (H2O2)
O grupo prostéico das metaloporfirinoproteínas é constituído pela porfirina à qual se liga
um átomo de metal. O Heme é sintetizado a partir da porfirina e ferro e seus produtos de degradação
são os pigmentos biliares e ferro.
As porfirinas são um composto cíclicos formados pela ligação de quatro anéis de pirrólicos
ligadas entre si por radical metileno. Os nitrogênios centrais podem formar ligações com metais do
tipo encontrados nos complexos metálicos.
Os aminoácidos além de servir para a formação das proteínas são precursores de compostos
nitrogenados, de importância biológica, tais como porfirinas e bases nitrogenadas (purinas e
pirimidinas).
As porfirinas são moléculas que se associam facilmente a íons metálicos, geralmente o ferro,
formando as metalporfirinas.
Nos mamíferos a principal porfirina é o heme que participa do grupo prostético de algumas
proteínas importantes, tais como, hemoglobina, mioglobina, onde, funcionam como transportadores de
oxigênio, gás carbônico e elétrons.
Síntese do Heme:
O Heme é sintetizado a partir do succinil-CoA derivado do Ciclo de Krebs (ciclo do ácido
cítrico) e do aminoácido glicina. A ALA sintase é a enzima controladora da velocidade da síntese da
porfirina no fígado de mamíferos. A síntese do ALA ocorre na mitocôndria.
No citossol, 2 moléculas de ALA são condensadas pela enzima ALA desidratase, formando 2
moléculas de água e uma de porfobiinogêneo (PBG). A ALA desidratase é uma enzima que contêm
zinco e é sensível aochumbo, como pode ocorrer no envenenamento por esse metal.
Quatro moléculas de porfobiinogêneo (PBG) condensam para formar o hidroximetilbilano
(HMB). Essa reação é catalizada pela uroporfirinogêneo sintase uroporfirinogêneo I, II e III. O
uroporfirinogêneo III é convertido a coproporfirinogêneo III.
Porfirias:
As porfirias são causadas por defeitos herdados (ou eventualmente adquiridos) na síntese do
Heme, resultando no acúmulo e na excreção aumentada de porfirinas ou precursores de porfirina. Com
12
13
exceção da porfiria eritropoiética congênita, uma doença genética autossômica recessiva,
todas as porfirias são herdadas como distúrbios autossômicos dominantes.
As porfirias são classificadas como eritropoiéticas ou hepáticas, dependendo da deficiência enzimática
ocorrer nas células eritropoiéticas ou hepáticas. As porfirinas hepáticas podem ser classificadas como
aguda ou crônicas. Os indivíduos geralmente apresentam fotossensibilidade, ou seja, sua pele
apresenta prurido e a sensação de queimação quando exposta a luz visível.
Porfiria crônica- (porfiria cutânia tardia) é a mais comum atingindo o fígado e os tecidos
eritróides. O acúmulo de porfirinas leva a sintomas cutâneos e mudança na coloração da urina
que se torna de vermelha a marrom sob luz natural.
Porfirina hepática aguda - sintomas gastrointestinais, neurológicos e cardiovasculares.
Podem causar o acúmulo de ALA e porfirinogênio, aumentando a síntese do ALA –sintase
Porfirias eripoiéticas - são caracterizadas por erupções e vesículas na pele que aparecem no
início da infância. Essa doença é complicada por cirrose hepática e progressiva insuficiência
hepática.
Degradação do Heme:
Em condição fisiológicas à uma renovação da hemoglobina no organismo,. A hemoglobina libera a
globina (parte protéica) que é degradada Geraldo os aminoácidos. O Heme libera o ferro que é
reutilizado no nosso organismo. A parte porfirínica do heme (livre do ferro) é degradada,
principalmente nas células reticulo endoteliais do fígado, baço e medula óssea.
O catabolismo do heme (degradação) pode ser ilustrado a seguir:
Processos patológicos envolvendo as porfirinas.
13
14
Icterícias: em condições anormais tanto a bilirrubina ligada à albumina (BI = bilirrubina
indireta) ou ligada ao ácido glicorônico (BD = bilirrubina direta) podem atingir altos níveis no sangue
(hiperbilirrubinemia) e depositando-se nos tecidos normais dando-lhes a aspecto amarelado (icterícia),
Embora não seja doença, a icterícia é normalmente, um sintoma da existência de um distúrbio
subjacente.
Tipos de icterícia: pode ser classificada em 3 tipos, mas na prática clínica, a icterícia é mais complexa
do que o indicado na classificação. Por exemplo, o acúmulo de bilirrubina pode ser um resultado de
defeitos em mais de um passo de seu metabolismo.
Icterícia hemolítica:há destruição excessiva dos eritrócidos (hemácias), por exemplo, em paciente
com anemia falciforme, deficiência de piruvato-quinase, de glicose-6-fosfato-desidrogenase ou
malária, causa o aumento da hemólise, com sobrecarga para o fígado, pois a produção de bilirrubina é
maior do que a capacidade do fígado de conjugá-la. Os níveis de bilirrubina conjugada aumentam no
sangue causando a icterícia e aumenta também o urobilinogênio fecal e urinário
Icterícia hepática:quando houver lesão das células hepáticas (hepaócitos), por exemplo, em hepatites
ou cirrose, havendo um aumento da Bilirrubina conjugada (Bilirrubina indireta, BI) e Bilirrubina não
conjugada (Bilirrubina direta, BD). A bilirrubina conjugada. A uma diminuição do uribilinogênio fecal
(fezes claras) e aumento do urinário (urina escura), com presença de bilirrubina na urina. Os níveis de
AST (TGO) e ALT (TGP) apresentam-se elevados, e o paciente pode ter náuseas e anorexia.
Icterícia obstrutiva: quando houver obstrução das vias biliares dificultando o lançamento da BD para
o intestino, por exemplo, tumor hepático ou cálculos biliares causando um bloqueio nos ductos
biliares, impedindo a passagem da bilirrubina para o intestino. Os pacientes com icterícia obstrutiva
apresentam dor gastrointestinal e náusea e produz fezes claras, cor de argila. O fígado reflui à
bilirrubina para o sangue. Esse composto é então excretado na urina. Portanto, há uma aumento de
Bilirrubina no sangue causando a icterícia, fezes branca e presença de bilirrubina na urina.
Icterícia neo-natal- Em especial em bebês prematuros, pois freqüentemente
acumulam
bilirrubina no sangue, pois a atividade da bilirrubina-glicoronil-trasferase hepática é baixa ao
nascimento, alcançando os níveis semelhante aos adultos em 4 semanas. Bilirrubina elevada nos
recém-nascidos pode levar encefalopatias tóxicas (kernicterus). Desse modo quando a aumento
significante de bilirrubina, os recém-nascidos são tratados com luz fluorescente azul que converte a
bilirrubina em isômeros solúveis em água, para facilitar a excreção.
Vitaminas
Visão geral:
As vitaminas são compostos orgânicos não relacionados quimicamente necessários em
pequenas e que, geralmente, não podem ser sintetizados pelo organismo, devendo, portanto ser
fornecidos pela dieta.
As vitaminas são requeridas para a fazer várias funções específicas na célula.
Quando a ingestão for inadequada de vitaminas e sais minerais, resulta em doenças clínicas
por deficiência, e quando a ingestão ultrapassar a capacidade metabólica do organismo (alta ingestão
de vitaminas e sais minerais) podem ocorrer sinais de toxidade.
14
15
Classificação das vitaminas:
As vitaminas se dividem em 2 grupos principais: as Lipossolúveis e Hidrossolúveis.
Lipossolúveis: são vitaminas associadas aos lipídios (encontradas em animais e vegetais ricos em
gordura),são absorvidos juntamente com os lipídios e, como estes são transportados pelas
lipoproteínas plasmáticas. A absorção dessas vitaminas se dá no intestino, sendo facilitada pela ação
emulsificante da bile. Após a absorção, são transportadas pelo sangue e distribuídas para os tecidos
sob forma de um complexo protéico.
Devido a sua insolubilidade, elas não são facilmente excretadas na urina, pôr isso são armazenadas no
fígado e tecido adiposo . A ingestão excessiva dessas vitaminas causa hipervitaminoses.
São elas:
Vitamina A (retinol), D (ex: D3- Colecalciferol), E (Tocoferóis) e K (fitoquinona, menaquinona).
Hidrossolúveis: São vitaminas que são facilmente absorvidas e transportadas no sangue. São
facilmente excretadas pela urina, portanto não são tóxicas quando ingeridas em grande quantidade.
São elas:
Vitamina C, B1, B2, B3 Biotina, B6, B12, ácido pantotênico, ácido fólico
VITAMINAS LIPOSSOLÚVEIS:
VITAMINA A ou RETINOL: - Sinônimos: os retinol, b-caroteno
A vitamina A, obitida a partir dos Carotenóides da dieta (vegetais),
Envolvida nas reações da visão e no crescimento
Controle da diferenciação e reciclagem celular
Os retinóides ocorrem na natureza ou são produzidos sinteticamente.
Absorção - Depois de absorvida a vit. A é levada ao fígado e distribuída (albumina-Retinol)
para os tecidos. A deficiência de albumina na desnutrição pode determinar a deficiência de
vitamina A.
Principais funções:
Importante para as funções da retina, principalmente para a visão noturna. - - indispensável à
manutenção da integridade do epitélios.
Principais fontes de vitamina A - Fígado , leite e derivados, vegetais e fritas amarelas, ex: é a
cenouras entre outras.
Algumas manifestações de carência:
cegueira noturna.
queratinização da córnea e pele o que propicia um aumento de infeções. Pode haver uma
diminuição da elasticidade pulmonar dificultando a respiração.
15
16
Pele e Mucosas- a queratinização e a secura da pele torna as mucosas suceptíveis a
infecções e degeneração das fibras periodontais.
A vitamina A em excesso é tóxica podendo causar:
- cefaléia, náuseas
- secura de pele e descamação
- alteração no fígado (hepatomegalia), entre outros
VITAMINA E:- Sinônimos: tocoferol
Principais funções:
A vitamina E age como antioxidante seqüestrador de radicais livres em membranas celulares e
lipoproteínas
Outras ações:
Cadeia respiratória: impede a oxidação da coenzima Q.
Síntese do Heme: parece participar da regulação da síntese do Heme, controlando a indução e
inibição da enzima marca-passo (Ala-Sintase).
Os tocoferóis são apolar e são transpotados por proteínas plasmáticas, principalmente associadas a
quilomícrons e a VLDL e por agirem como antioxidantes podem previnir a oxidação da LDL ,
protegendo asssm, o desenvolvimeto de doenças cardíacas.
Principais fontes: azeites vegetais, germe de trigo, óleo de semente de girassol e açafrão, éleo de
milho e soja e verduras frescas, entre outros. O leite de mulher contém vitamina é suficiente para o
filho em aleitamento ao peito, ao contrário do leite de vaca.
Manifestações de carência: não é conhecida em humanos
Manifestações de excesso: a vitamina E mesmo em altas doses não é tida como tóxica, mas, se
ingerida em excesso, pode, eventualmente, competir na absorção e reduzir a disponibilidade das outras
vitaminas lipossolúveis, além do ferro dos alimentos, e, assim, colaborar para o desencadeamento de
anemias.
VITAMINA K: - Sinônimos: a vitamina K é composta de 3 tipos, a K1 (Fitonadione), a K2
(menaquinonas) e a K3 (menadione).
Principais funções: A vitamina K atua:
- na produção de protrombina, fator importante na coagulação do sangue.
- é importante para a síntese de proteínas ósseas ligadoras de cálcio.
Principais fontes: verduras e fígado.
Manifestações de carência:
A carência da vitamina K manifesta-se por tendência ao sangramento (leva um maior tempo para a
coagulação)
16
17
Manifestações de excesso : as vitaminas K1 e K2 não são tóxicas, mesmo em altas doses.
Já a vitamina K3 em altas doses pode provocar anemia e lesões no fígado.
VITAMINA D:
Sinônimos: Calciferol
Principais funções: a vitamina D age com um hormônio na regulação do cálcio dos ossos e sangue.
São pró-vitaminas que na luz ultravioleta adquire a forma ativa.
Principais fontes: o organismo humano é capaz de sintetizar a vitamina D a partir do colesterol, por
isso, poderia deixar de ser considerada uma vitamina segundo a definição das mesmas. Nas regiões em
que há pouca radiação solar o corpo humano tem a necessidade de complementar as carências
alimentares e/ou ambientais. As principais fontes são fígado, óleos de peixes e gema de ovos. Existem
no mercado produtos lácteos "enriquecidos" de vitaminas D, o que num país ensolarado como o Brasil
é dispensável.
Manifestações de carência: a carência de vitamina D provoca, nas crianças, o raquitismo e nos
adultos a osteomalácia (amolecimento dos ossos). Nos idosos leva à osteoporose.
Manifestações de excesso: doses exageradas de vitamina D provocam a hipercalcemia (excesso de
cálcio no sangue) o que favorece o depósito de cálcio nos vasos (arteriosclerose) e ainda a eliminação
aumentada de cálcio na urina o que por sua vez favorece a formação de cálculos urinários. Altos teores
de cálcio no sangue alteram as funções do coração e dos nervos.
Tanto o excesso como a carência de vitamina D altera a formação dos ossos.
VITAMINA F:
Principais funções: protetores cutâneos e interferem no crescimento do corpo humano.
São muito usados para tratar as peles secas, peles rachadas e envelhecidas.
Principais fontes: o nome de vitamina F vem por serem os ácidos graxos essenciais encontrados em
gorduras. É encontrada principalmente no óleo de milho, de girassol, de soja, de caroço de uva, de
germe de trigo, nos óleos de oliva e de peixes, e destes, principalmente, nos de água fria.
Manifestações de carência: alterações da pele e do crescimento corporal.
Manifestações de excesso: não são descritas.
17
18
Vitaminas Hidrossolúveis
VITAMINA C:
Sinônimos: ácido ascórbico.
Principais funções: participa na formação de catecolaminas; aumenta a absorção de ferro pelo
intestino.
Principais fontes: frutas e verduras frescas.
Manifestações de carência: lesões do colágeno. O escorbuto, hemorragias na cavidade bucal,
cicatrização deficiente, fragilidade óssea, um mal clássico dos marinheiros de longo curso, é, hoje em
dia, uma doença praticamente desconhecida.
Manifestações de excesso: formação de cálculos de oxalato nos rins. Note-se que a dose diária
recomendada é de 60 mg/dia. Alguns produtos comerciais contêm até 2000 mg por comprimido, o que
significa a ingestão de 35 ou mais vezes o dose diária recomenda.
O efeito preventivo ou curador de doenças virais, como gripe, a prevenção de câncer, reduzir risco de
doença cardíaca e catarata, o aumento das defesas orgânicas, tudo isso não está comprovado como
sendo um efeito terapêutico útil da vitamina C.
As chances de obter um benefício para a saúde com o uso de altas doses de vitamina C são bem
menores do que as de se conseguir uma doença a mais.
Alimentos ricos em vitamina C: mamão papaia. Brócolis, suco de laranja, morangos, laranja, kiwi,
entre outros.
VITAMINAS DO COMPLEXO B: São substâncias hidrossolúveis facilmente absorvidas pelo
intestino e depois transportadas até sei tecido alvo onde são transformadas em seus derivados, as
coenzimas.
VITAMINA B 1
Sinônimos: Tiamina
Coenzimas de descarboxilase e transferases - forma de Pirofosfato de Tiamina (TTP)
Principais funções: atua principalmente no metabolismo energético dos açúcares.
Principais fontes: carnes, cereais, nozes, verduras e cerveja. Nota: alguns peixes e crustáceos e chás
pretos podem conter fatores anti-tiamina.
Manifestações de carência: a doença carencial clássica é o Beribéri que se manifesta principalmente
em alcoólatras desnutridos e nas pessoas mal-alimentadas dos países pobres.
aumento de ácido pirúvico e lático
SNC – degeneração das fibras mielinicas (barberi)
18
19
Nas crianças de peito a falta de vitamina B1 pode aparecer por ser o leite materno muito
pobre em tiamina, principalmente se a mãe não receber suplemento de vitamina B1.
Manifestações de excesso: mesmo em doses elevadas, a tiamina não é tóxica. Os eventuais excessos
ingeridos são eliminados pelos rins.
VITAMINA B 2:
Sinônimos: Riboflavina
Sob a forma de FAD (flavina – adenina – dinucleotídeo) e FMN (riboflavina – mononucleotídieo),
consttitui a coenzima de numerosas enzimas.
Principais funções: exerce função de transporte de hidrogênio e de elétrons nas reações de oxidoredução na cadeia respiratória. Adimite-se ainda que a riboflavina age no metaboliamo de aminoácidos
e ácidos graxos, por fazer parte do grupo prostético e coenzimas das enzimas. EX: acil-CoAdesidrogenase.
Principais fontes: leite, carne e verduras.
Nota: a radiação solar (UV) inativa a riboflavina.
Manifestações de carência: muito raras. Podem aparecer em gestantes, nos esportistas de alta
performance ou em doenças digestivas que alterem a sua absorção. As primeiras manifestações de
carência são inflamações da língua, rachaduras nos cantos da boca, lábios avermelhados, dermatite
seborréica da face, tronco e extremidades, anemia e neuropatias. Nos olhos, pode surgir a neoformação
de vasos nas conjuntivas, além de catarata.
As carências de vitamina B2 costumam acompanhar a falta de outras vitaminas.
Manifestações de excesso: não é tóxica, mesmo em altas doses. Os excessos são eliminados pelos rins.
VITAMINA B 6:
Sinônimos: Piridoxina, Piridoxol, Piridoxamina e Piridoxal.
Sob forma piridoxal fosfato (PAL) e Piridoxamina (PAM). – coenzimas das transzaminases e
descarboxilases dos metabolismo proteico.
Principais funções: a vitamina B6 é uma coenzima e interfere principalmente no metabolismo das
proteínas.
Principais fontes: cereais, carnes, frutas e verduras. O cozimento reduz os teores de B6 dos alimentos.
Manifestações de carência: são muito raras, são lesões seborréicas em torno dos olhos, nariz e boca,
acompanhadas de glossite e estomatite. Distúrbios do crescimento e anemia são atribuídos à carência
de vitamina B6, entre outros.
19
20
Manifestações de excesso: a Piridoxina tem baixa toxicidade aguda, mas doses de 200
mg/dia, tanto por via oral como parenteral, podem provocar intoxicações neurológicas, surgindo
sintomas como formigamentos nas mãos e diminuição da audição.
VITAMINA B 12:
Sinônimos: cobalaminas, hidroxicobalamina, cianocobalamina
Principais funções: essencial para o crescimento de replicação celular. Importante na formação das
hemácias (os glóbulos vermelhos do sangue).
Principais fontes: carne e fígado. É também produzida pela flora do intestino grosso, mas lá não é
absorvida. A absorção se dá no intestino delgado depois dela ter sido ativada no estômago aonde chega
com a ingestão de alimentos. A vitamina B12 necessita do chamado "fator intrínseco", existente nos
estômagos normais, para ser absorvida. A vitamina B 12 formada nos intestinos, por não ter sido
ativada pelo fator intrínseco quase não é absorvida.
Os vegetais, per se, não contêm vitamina B12, isso poderia levar os vegetarianos a apresentarem a sua
falta. Contudo isso nem sempre acontece porque bactérias contaminantes dos vegetais ou mesmo as do
trato intestinal, agindo sobre os restos desses vegetais, formam a vitamina B12 e, assim, suprem
parcialmente o organismo daqueles que não ingerem carne, fígado, ovos ou leite e seus derivados.
Manifestações de carência: anemia macrocítica é a principal manifestação. Existem evidências de
que níveis baixos de vitamina B12 estariam associados a uma maior incidência de doenças vasculares
e cancerosas.
Manifestações de excesso: não são citadas na literatura médica.
ALERTAS
A vitamina B12 é indicada por alguns para tratar dores musculares ou articulares. A sua eficácia
como analgésico nestas situações não está confirmada.
São relatados casos de reações alérgicas ao uso da vitamina B12, principalmente se usada via
injetável.
Só faça reposição de vitamina B12 sob a supervisão e orientação de um médico.
Vitamina B5 - ÁCIDO PANTOTÊNICO:
Sinônimos: Coenzima A.
Principais funções: atua no metabolismo intermediário de carboidratos , proteínas e lipídios. Interfere
na produção de energia dentro das células e na produção de hormônios.
Principais fontes: carnes, ovos, frutas, cereais e verduras, sendo encontrada, praticamente, em todos os
alimentos.
Manifestações de carência: são muito raras. As carências podem ser produzidas experimentalmente
com alimentos artificiais, pelo uso de alguns antibióticos, nesses casos surgem cansaço, distúrbios do
equilíbrio e do sono, cãibras e distúrbios digestivos, como flatulência e cólicas abdominais. Pessoas
com dietas normais não têm carência de ácido pantotênico.
20
21
Manifestações de excesso: o excesso de ingestão pode provocar diarréia. Como acontece
com as demais vitaminas hidrossolúveis, os excessos são eliminados pelos rins, na urina.
Vitamina B3 - NIACINA E NIACINAMIDA (FATOR PP):
Sinônimos: ácido nicotínico e niacinamida e fator PP. Também denominados de vitaminas da
inteligência.
Sob forma de NAD (nicotinamida adenina dinucleotídeo) e NADP (nicotinamida adenina
dinucleotídeo fosfato)
Principais funções: influencia a formação de colágeno e a pigmentação da pele provocada pela
radiação ultravioleta. No cérebro, a niacina age na formação de substâncias mensageiras, como a
adrenalina, influenciando a atividade nervosa.
Principais fontes: carnes e cereais. Origina-se do metabolismo do triptofano: 60 mg de triptofano
produzem 1 mg de Niacina.
Manifestações de carência: a doença dos 3 "D", composta por Diarréia, Demência e Dermatite. A
língua pode apresentar cor avermelhada, ulcerações e edema. Pode haver salivação excessiva e
aumento das glândulas salivares. Podem aparecer dermatites parecidas com queimaduras de pele,
diarréia, esteatorréia, náuseas e vômitos. No sistema nervoso, aparecem manifestações como cefaléia,
tonturas, insônia, depressão, perda de memória e, nos casos mais severos, alucinações, demência e
alterações motoras e alterações neurológicas com períodos de ausência e sensações nervosas alteradas.
Manifestações de excesso: a Niacina não costuma ser tóxica, mesmo em altas doses, mas pode
provocar coceira, ondas de calor, hepatotoxicidade, distúrbios digestivos e ativação de úlceras
pépticas.
Observação: a denominação PP significa Previne Pelagra, manifestação encontrada principalmente em
alcoólatras de destilados quando mal-alimentados.
Ácido Fólico:
Sua forma ativa, ácido tetradrofólico, o ácido fólico atua como aceptor de várias unidades
monocarbônicas do metabolismo.
Atua na síntese de bases nitrogenadas de ácidos nucleicos e é coenzima fundamental na trnasformação
e síntese de diversos aminoácidos, como a glicina e serina.
Manifestações de carência: anemiamacrocítica.
21