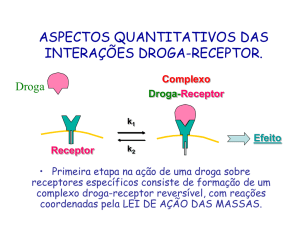
Farmacodinâmica I – Receptores
Vimos que os fármacos agonistas e antagonistas atuam nos receptores
farmacológicos e esses receptores farmacológicos são um dos 3 tipos de alvos
protéicos (enzima, canal iônico e molécula transportadora) que os fármacos podem se
ligar.
Os fármacos podem se ligar nos receptores farmacológicos que são aquelas
proteínas funcionalmente silenciosas que respondem a ligantes endógenos. Quando
um fármaco se liga nesse tipo de receptor, ele pode sofrer uma ação agonista ou sofrer
uma ação antagonista nesse receptor. O agonista é o fármaco que se liga e induz uma
resposta do receptor (se a resposta é abrir um canal iônico, quando ativado vai
acontecer isso. Se a resposta do receptor é ativar uma proteína G, isso vai acontecer).
O antagonista se liga no receptor e, simplesmente, não deixa o antagonista se ligar.
Dizemos que a eficácia do antagonista no receptor é zero, ele não faz efeito, ele só
bloqueia o receptor. Não faz resposta no receptor, porém me dá um efeito
farmacológico pela ausência da ação do agonista naquele receptor. Desenhamos
semana passada, a ligação da acetilcolina no receptor M2 do coração e a atropina
como antagonista. Qual é a resposta farmacológica quando uso acetilcolina? Posso
usá-la terapêuticamente, ela faz bradicardia. Qual é a resposta farmacológica quando
uso atropina? Taquicardia. Mas a atropina causa taquicardia no receptor? Não, ela só
impede a bradicardia da acetilcolina, pois vou ver a taquicardia da adrenalina e
noradrenalina que continuam fazendo ação.
Um fármaco pode ser agonista e antagonista do receptor. Se ele for agonista,
ele vai desencadear qualquer mecanismo de transdução de sinal desse receptor. E se
for antagonista, simplesmente bloqueia a resposta. O mesmo fármaco pode ser
agonista e antagonista, dependendo do receptor que ele atua. Um bom exemplo é o
álcool que ora é agonista do receptor GABA A que aumenta a inibição da célula, ora é
antagonista do receptor GLUTAMATO, ele inibe a atividade excitatória do glutamato no
seu receptor, aí no final eu tenho uma resposta depressora do SNC.
Um fármaco pode ser agonista total ou agonista parcial de determinado receptor.
Mas o que é um agonista total? É um fármaco que se liga no receptor e produz a
resposta máxima que aquele receptor é capaz de dar. O que é um agonista parcial? É
um fármaco que se liga no receptor e produz uma resposta menor que a máxima que
aquele receptor é capaz de dar. Qual é a diferença entre esses dois fármacos? A
diferença está na eficácia. Consideramos que os agonistas totais têm eficácia máxima,
são drogas de grande eficácia, não precisa aumentar muito a dose do fármaco para ter
efeito máximo. Os agonistas parciais são drogas de baixa eficácia, por mais que eu
aumente a dose, nunca consigo ter uma resposta máxima daquele receptor porque ele
é justamente um agonista parcial, vai dar uma resposta sempre menor que a máxima.
Conforme vou aumentando a dose do agonista total na solução, conforme ele
chega em uma certa concentração, eu consigo a resposta máxima. Já o agonista
parcial, por mais que aumente a concentração dele na solução, eu nunca vou ter uma
resposta máxima, sempre a resposta será menor que a máxima.
Se eu relacionar resposta por ocupação de receptor ao invés de estar dosando a
quantidade de droga na solução (eu coloquei um marcador que meça para mim
quantos receptores foram ocupados naquele tecido); o agonista total, mesmo que ele
ocupe menos de 50% dos receptores de um tecido, ele me dá a resposta máxima. Já o
agonista parcial, mesmo que ocupe 100% dos receptores daquele tecido, eu não
consigo a resposta máxima.
Qual é a diferença entre esses fármacos? Usamos agonistas parciais na prática?
Sim, existem muitos fármacos que na verdade são agonistas parciais. Exemplos: os
beta bloqueadores, na maioria das vezes eles são bloqueadores dos receptores Beta1
no coração, mas isso não é verdade, tem alguns que são na verdade agonistas parciais
do receptor Beta1 no coração. Concorda comigo que tanto um beta bloqueador quanto
um agonista parcial dá bradicardia!? Sabemos que receptor beta1 no coração quando
ativado, ele dá taquicardia, se eu bloquear ele e não deixar a noradrenalina se ligar, eu
vou ter bradicardia – isso é o que faz o beta bloqueador. Se eu der um agonista parcial
desse receptor beta1 no coração, eu também vou ter bradicardia porque ele vai ativar o
receptor menos que o meu ligante endógeno, e se eu ativar menos, o coração bate
menos e vou ter o efeito de bradicardia. Então, nem sempre eu preciso usar um
antagonista de receptor para ter o efeito contrário do ligante endógeno. Se eu usar um
agonista parcial, eu também vou ter um efeito contrário do ligante endógeno. Existem
fármacos que usamos que são antagonistas e existem fármacos que usamos que são
agonistas parciais de receptor e existem fármacos que são agonistas totais.
Adrenalina(+)
Receptor
Beta1
Receptor
M2
Propanolol (-)
100bat/min
Atenolol(+/-)
Bradicardia (90bat/min)
180 bat/min
Tenho 3 tipos de fármacos que se ligam no receptor Beta1: se eu der um
agonista total que é a adrenalina (ela me dá a resposta máxima de taquicardia que o
receptor pode me dar, por exemplo 180 bat/min, porque ela é agonista total). Se eu der
o beta bloqueador que é o propanolol, ele é antagonista desse receptor, vou ter uma
bradicardia, por exemplo 90 bat/min, porque o propanolol impediu a ligação da
adrenalina nesse receptor. Se eu usar um outro fármaco que seja agonista parcial, o
atenolol (não tenho certeza se ele é agonista parcial), ele vai ativar esse receptor de
uma maneira menor que a adrenalina, por exemplo 100 bat/min, porque ele é uma
agonista parcial, então por mais que eu aumente a dose de atenolol e ele ocupe todos
os receptores do tecido, nunca vou conseguir que ele tenha os mesmos 180bat/min
que a adrenalina faz. Bom, tenho que perceber que o atenolol (agonista parcial) reduziu
os batimentos cardíacos em relação ao agonista total (adrenalina). A adrenalina que se
liga o tempo todo no coração e me daria esse batimento (180 bat/min), vou ter um
batimento menor usando o propanolol (100 bat/min). Então, se eu comparar o
propanolol com a adrenalina, eu tenho um efeito de bradicardia; claro que o efeito de
bradicardia do antagonista é maior, mas sempre quando eu comparo o agonista parcial
com o agonista total, eu vou ter uma bradicardia, sempre vai diminuir o batimento. Ou
seja, às vezes eu uso um beta bloqueador que é um agonista parcial, ele vai dá
bradicardia, talvez não tanto como o antagonista, mas também me dá bradicardia. Eu
posso usar essa estratégia para ter o efeito de bradicardia também. {Quando dou esse
agonista parcial (atenolol), ele ocupa mais receptores que a adrenalina (agonista total),
o que significa que ela também, ao mesmo tempo continua ocupando receptores, só
que ocupa bem menos receptores que o atenolol. Eu não consigo ter a mesma ligação
que a adrenalina teria se eu não estivesse dando esse agonista parcial, porque agora
tenho outra droga para competir, então eu não tenho o efeito total da adrenalina}.
Tenho afinidade tanto quando comparo o agonista total como o parcial. O a
gonista parcial chega a ter até mais afinidade pelo receptor do que o agonista total,
pois ele pode ocupar todos os receptores, apesar de não ter uma resposta máxima, já
o agonista total, com 50%de afinidade pelo receptor já pode proporcionar uma resposta
máxima. Ou seja, ambos têm afinidade pelo receptor, a diferença está na eficácia da
droga, na capacidade de produzir resposta. Existem fármacos com uma afinidade
maior do que outros fármacos, mas todos precisam ter afinidade para poderem se ligar.
O agonista parcial causa o mesmo efeito farmacológico que o antagonista,
porém o causa em intensidade diferente.
O que é afinidade? É a capacidade do fármaco se ligar ao receptor. Tanto
agonistas, seja total ou parcial, como antagonistas têm afinidade pelo receptor, todos
têm que ter afinidade.
O que é eficácia? É a capacidade do fármaco, uma vez ligado, induzir uma
resposta no receptor. Eficácia no receptor é diferente de eficácia clínica, estamos
falando sobre a eficácia no receptor (ou seja, ligou, logo induz um mecanismo de
resposta nesse receptor). Tanto agonista total como o parcial tem eficácia, mas o
antagonista não tem eficácia, pois para o antagonista a eficácia é zero, não induz
nenhuma resposta no receptor. A eficácia clínica é diferente, é o efeito farmacológico
resultante dessa interação fármaco-receptor, é o efeito farmacológico que eu vejo no
paciente. Então, na eficácia clínica tanto agonistas, seja total ou parcial, como
antagonistas têm eficácia clínica, porque se o antagonista não tivesse eficácia clínica,
não serviria para nada, não adiantaria eu estar usando ele.
O que é potência? É a quantidade de droga necessária para produzir 50% da
resposta máxima do receptor. Então, agonistas totais e parciais têm potência.
Antagonista, nessa definição, não tem potência.
O que é uma droga agonista inversa? São drogas com eficácia negativa, é
diferente dos agonistas que têm eficácia positiva e é diferente dos antagonistas que
têm eficácia zero. Temos em abundância no SNC o receptor GABA A (receptor do
aminoácido GABA e do cloro), ele é um receptor de membrana, está numa membrana
celular, é uma proteína que tem 4 ou 5 subunidades que se arranja de forma
oligomérica, forma um poro no seu interior. O receptor GABA A tem um domínio de
ligação, onde o GABA (aminoácido) e o cloro se ligam. O GABA quando se liga, ele é
um tipo de agonista dessa reação e provoca abertura desse poro, promove a entrada
de íons cloreto no neurônio (se eu aumentar a quantidade de entrada de carga
negativa no neurônio, eu vou hiperpolarizar, vou diminuir a excitação desse neurônio),
por isso que o GABA é um aminoácido inibitório, inibe o neurotransmissor. Nesse
receptor GABA A existem outros sítios de ligação, ele se liga a 3 tipos de fármacos: o
diazepam (benzodiazepínico), é agonista de um dos 3 sítios do GABA A, na verdade é
o mesmo receptor do GABA, só que o GABA se liga em um sítio e o diazepam se liga
em outro sítio de ligação. {Pesquisadores tentam descobrir como a dor endógena que
nós produzimos se liga no sítio de ligação dessa proteína. Praticamente para todos os
sítios de ligação onde o fármaco se liga nos receptores, nós temos um efeito
endógeno. Eles tentam descobrir qual seria o nosso benzodiazepínico endógeno}. Para
esse mesmo sítio de ligação do diazepam, nós temos outro fármaco muito utilizado na
clínica, chamado de Flumazenil (ele é antagonista desse receptor. Eu uso flumazenil
para casos de intoxicação por diazepam. Quando uma pessoa toma uma dose cavalar
desse agonista – diazepam – eu administro um antagonista para ocupar esse receptor
e para competir com o diazepam na ligação em outros receptores. Eu vou inibir a
depressão maior no SNC). O que o diazepam faz quando ele se liga como agonista,
qual o mecanismo de transdução de sinal dessa proteína? Ele aumenta ainda mais a
abertura do canal de cloreto. Quando o diazepam se liga, por ele ser agonista, ele vai
fazer com que o GABA tenha uma ação maior como depressor porque vai entrar muito
mais íon cloreto dentro da célula, ou seja, quando eu administro diazepam, ele
favorece a abertura do canal iônico, ele hiperpolariza, por isso é uma droga depressora
do SNC. Então, quando usamos diazepam, o que temos como efeito depressor?
Sedação, inibição da ansiedade, perda da coordenação motora, relaxamento muscular
e até amnésia, tudo isso é efeito do diazepam porque ele é depressor. O Flumazenil,
então se liga e não deixa o diazepam se ligar, ele é antagonista do receptor. {Um grupo
de pesquisadores pensou: se eu tenho um fármaco que é agonista desse receptor e
abre canais de íons cloreto, faz com que mais íons cloreto entrem na célula e isso faz
perda de memória, por que eu não posso ter um fármaco que feche o canal de cloreto,
pois assim melhoraria a memória? Eles desenvolveram um agonista inverso para esse
depressor, a Beta carbonila, porque como ela é um agonista inverso, quando ela se liga
no mesmo sítio de ligação do benzodiazepínico, ao invés dela promover a abertura do
canal, ela faz o fechamento do canal. Só que essa droga não passou dos testes préclínicos porque apesar dela realmente melhorar a memória, ela causava um efeito
ansiogênico e levava a convulsão}. Então, hoje, as beta carbonilas são usadas apenas
como meio de pesquisas farmacológicas. São um ótimo exemplo de fármaco agonista
inverso. A beta carbonila é droga de eficácia negativa; se a resposta do receptor que o
agonista dá, ela promove a abertura do canal, e eu faço um fármaco que atua no
mesmo lugar promovendo o fechamento do canal, ele é um agonista inverso. Qual é a
importância disso? Não sabemos muito bem, pois só pensavam em se desenvolver
fármacos que fossem agonistas e antagonistas dos receptores, mas agora se sabe da
possibilidade da criação de agonistas inversos, eu posso ativar um receptor
inversamente, ele pode dar uma resposta contrária a que um agonista é capaz de dar,
é mais uma estratégia para o desenvolvimento de fármacos. Existem fármacos que
tomamos há anos e anos, e que só depois disso se descobriu que eles são agonistas
inversos e não antagonistas dos receptores como se pensava. Um exemplo: antihistamínicos. Falávamos que eles são antagonistas de receptores H1 da histamina,
usados para a alergia, enjôo; mas na verdade se descobriu que vários deles são
agonistas inversos dos receptores de histamina. O efeito anti-alérgico deles, não se dá
por impedir que a histamina entre e se ligue, daí eu não tenho vasodilatação; eles
ativam o receptor inversamente de forma que diminui esses processos alégicos. Qual é
a diferença de um agonista inverso e de um antagonista se eles me dão o mesmo
efeito anti-alérgico? Na eficácia clínica não tem diferença, porém é uma nova estratégia
para o desenvolvimento de fármacos.
ClGABA(+)
(+)DIAZEPAM
(-)FLUMAZENIL
BETA CARBONILA (agonista inverso)
GABA A
Cl- Cl- Cl-
hiperpolariza ( excitação)
Tem como eu saber se o fármaco é agonista inverso ou antagonista se eu
realizar experimentos em órgão isolados. Quando eu ativo um receptor, posso detectar
que mecanismo de transdução de sinal foram ativados naquele receptor, vejo se abri
canal iônico, se ativei proteína G, vejo o que aconteceu. Verificando se o canal iônico
foi aberto ou fechado, tem como saber. Se ele foi fechado se ligando nesse mesmo
sítio de ligação, se eu diminuí a entrada de cloro na célula, ele é agonista inverso. É só
eu medir a entrada de cloro na célula.
O agonista inverso ativa o receptor inversamente. Eu sei que quando o agonista
diazepam se liga, eu tenho a abertura do canal de cloro, entra mais cloro. Eu sei que
quando o flumazemil se liga, não acontece nada, só não deixa o agonista ligar, então
ele é antagonista. Agora, a beta carbonila se liga no mesmo local que o diazepam e o
flumazemil se ligam, e ela promove o fechamento desse canal, ela ativa o receptor de
uma maneira inversa do que o ligante endógeno que é o GABA ativa, do que o
diazepam que é um fármaco ativa. Ela faz efeito contrário, então ela é agonista inverso.
O agonista, conforme eu vou aumentando a dose, ele vai ativando positivamente
o receptor. O agonista inverso, conforme eu vou aumentando a dose, eu vou ativando
negativamente o receptor. Para os antagonistas a eficácia é zero, embora eu tenha
uma afinidade. Agonista tem afinidade (capacidade de ligar), eficácia (capacidade de
produzir resposta no receptor) e potência (quantidade de droga necessária para
produzir 50% da resposta máxima do receptor).
Atividade intrínseca e eficácia é a mesma coisa? Depende do autor, alguns
consideram eficácia e atividade intrínseca como sinônimos, capacidade de produzir
resposta no receptor. Tem alguns autores que dizem que é diferente, dizem que a
eficácia não é possível de se quantificar, a atividade intrínseca sim. Como assim? A
eficácia da adrenalina para ativar esse receptor é estimular uma proteína G ligada a ele
que vai produzir segundos mensageiros na célula, que vai fazer essa célula contrair
mais forte; ou seja, é difícil de quantificar essa eficácia. A atividade intrínseca é quando
eu ativo esse receptor, e é capacidade que ele tem de contrair a célula, ou seja, eu
consigo medir a contração. Os dois desencadeiam um mecanismo de resposta da
célula, mas a diferença é que um eu consigo quantificar e o outro não. Eu uso como
sinônimo eficácia e atividade intrínseca.
Porcentagem
de
100
A
B
C
D
Resposta
[ ] Agonistas
Nesse gráfico estou relacionando a concentração de diferentes agonistas e a
porcentagem resposta (no receptor). Qual é o agonista total desse gráfico? Agonista
total é o fármaco que produz 100% da resposta do receptor e nesse gráfico todos
produzem a resposta máxima, todos são agonistas totais (A,B,C,D). A diferença entre
eles é a concentração para chegar a resposta, está na potência. O A, numa menor
concentração, eu consigo a resposta máxima. O D, eu preciso de uma maior
concentração para uma resposta máxima. Então, todos são agonistas totais, só que o
A é o mais potente e o D é o menos potente.
Porcentagem
de
Resposta
A
100
50
B
C
25
X
[ ] Agonistas
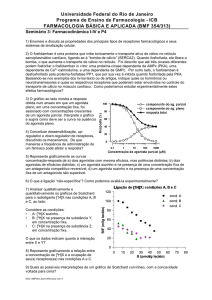
Nesse outro gráfico, qual é o agonista total? O agonista total é o A porque é o
único que eu consigo uma resposta máxima. O B e o C são agonistas parciais. Não
tem nenhum antagonista representado porque não daria para ver a resposta. Qual é o
mais potente? Todos são igualmente potente porque têm a mesma concentração para
atingir 50% da sua resposta máxima. Cada um tem uma resposta máxima diferente. O
A a resposta máxima é 100, o B a resposta máxima é 50 e o C a resposta máxima é
25. Todos eles, na concentração x conseguem 50% da resposta máxima. Então, A, B e
C são igualmente potentes, embora A seja agonista total, B e C agonistas parciais. A
resposta máxima de A é 100, com a concentração de X, eu tenho 50% da resposta
máxima. Em B a resposta máxima é 50, com a concentração X, tenho 25% da resposta
máxima e em C a resposta máxima é 25, com a concentração X, tenho 12,5% da
resposta máxima.
Farmacodinâmica II – Receptores Farmacológicos
Esse alvo protéico é o alvo protéico mais importante porque eles são o número
muito grande. Precisamos entender o que acontece num receptor farmacológico para
eu ter a resposta do fármaco. No caso da enzima, o fármaco pode inibir uma enzima,
pode enganar a enzima para ter uma resposta. No canal iônico, o fármaco bloqueia o
canal e não deixa entrar sódio. Na molécula transportadora, o fármaco bloqueia o
transporte e eu vou ter uma resposta. Vimos que o fármaco pode ser um agonista, um
antagonista ou um agonista inverso para ter uma resposta do receptor, mas o que
acontece dentro da célula para o receptor me dá essa resposta? Quais os mecanismos
que podem ser desencadeados dentro da célula para os receptores farmacológicos me
darem a resposta?
Vamos estudar então detalhadamente esses receptores. Eles são muito mais
complexos do que as enzimas, os canais iônicos ou as moléculas transportadoras.
Vimos que um agonista é total quando se liga ao receptor e dá a resposta máxima, é
parcial quando não consegue me dar uma resposta máxima e é inverso quando ativa o
receptor inversamente (drogas de eficácia positiva e drogas de eficácia negativa). Os
antagonistas se ligam aos receptores e bloqueiam a resposta, são as drogas de
eficácia zero. Vamos ver que um antagonista é um antagonista competitivo, vai
competir com o agonista, porém, ele pode fazer uma ligação reversível ou irreversível
nesse receptor.
Vamos ver os tipos de receptores, pois do mesmo modo que esses receptores
se dividem em enzimas, canais iônicos, moléculas transportadoras e receptores
farmacológicos; os receptores farmacológicos se subdividem em 4 grandes famílias de
receptores. E como eles são diferenciados nessas famílias? Primeiro, através da
estrutura molecular de cada um que é diferente, segundo, através do mecanismo de
transdução de sinal, o mecanismo que desencadeia a resposta na célula é diferente
para cada um deles.
Receptores tipo I: são conhecidos como receptores acoplados a canais iônicos
Receptores tipo II: são conhecidos como receptores acoplados a proteína G,
conhecidos também como a sigla GPCR
Receptores tipo III: são conhecidos como receptores ligados a proteína quinase
Receptores
tipo
IV:
são
conhecidos
como
receptores
nucleares
ou
intracelulares
Vamos estudar o que acontece quando um agonista se liga em qualquer um
desses 4 receptores. Vamos começar vendo os receptores em termos de estruturas
moleculares, como eles são diferentes:
Os receptores tipo I são receptores ligados a canais iônicos, eles são
constituídos de 4 ou 5 subunidades, são subunidades que se arranjam de forma
oligomérica na célula e formam um poro no interior da proteína. Cada subunidade
atravessa a membrana 4 vezes para formar um poro. Ele tem um domínio de ligação
sempre do lado externo da membrana e ele vai fazer com que o poro seja aberto
quando um fármaco ou um agonista se liga nesse receptor. Esse poro aberto vai fazer
com que entre ou saia íons. Esses receptores estão localizados sempre na membrana
celular.
Os receptores tipo II, mais importantes de todos os 4 porque compreendem a
maior família de receptores são conhecidos como receptores metabotrópicos porque
são acoplados a uma proteína G. Ele tem uma única subunidade que atravessa a
membrana 7 vezes, por isso eles também são conhecidos como receptores
heptaelicoidais, quer dizer que 7 alfas hélices atravessam a membrana. Eles têm um
domínio de ligação do lado externo da membrana e no lado interno, existe uma alça
citoplasmática dessa proteína que tem acoplamento com a proteína G.
Os receptores tipo III são os receptores ligados a quinase, têm atividade
enzimática. Temos uma única alfa hélice atravessando a membrana, eles estão sempre
na membrana. Temos um domínio de ligação na parte externa da membrana e também
temos um domínio catalítico, quer dizer, um domínio com atividade enzimática.
Os receptores tipo IV são conhecidos como nucleares ou intracelulares, pois
eles estão totalmente dentro da célula, tanto seu domínio de ligação quanto seu
domínio de interação com o DNA está dentro da célula. O fármaco para se ligar nesse
receptor tem que atravessar a membrana e penetrar na célula, ele tem que ser
altamente lipossolúvel.
RECEPTOR TIPO I: são também conhecidos como receptores ionotrópicos. São
canais iônicos regulados por ligantes e classificados como receptores. Quando um
fármaco atua nesse canal, falamos que seu alvo protéico é receptor farmacológico tipo
I. Quem são eles? São os receptores para os neurotransmissores natos. São
receptores para a acetilcolina, receptor GABA A, o receptor 5-HT3 da serotonina (único
receptor da serotonina que é ligado a canal), os receptores tipo aminoácidos,
aminoácidos excitatórios, o receptor NMDA. Esses receptores respondem a uma
velocidade de milisegundos. O ligante endógeno se ligou, abriu o canal, entrou íon,
acabou a ação dele. Quando ocorre a entrada de íon dentro de uma célula, uma célula
excitatória, o íon pode estimular essa célula fazendo polarização ou pode inibir essa
célula fazendo hiperpolarização, vai depender da carga do íon se for negativa ou se for
positiva.
Temos alguns fármacos importantes que atuam em receptores como esses. O mais
conhecido de todos é o receptor da acetilcolina. É constituído de 5 subunidades: 2
subunidades alfa, 1 beta, 1 gama e 1 sigma.
Receptor Nicotínico da
Acetilcolina
Hélices formando a comporta
Cada subunidade atravessa 4 vezes a membrana e forma um poro no seu
interior. Quando a acetilcolina se liga num receptor como esse, ela vai se ligar nas
subunidades alfa que vai promover mudança na conformação dessa proteína, vai fazer
com que esse poro se abra. O interior do receptor nicotínico tem uma negatividade,
essa carga negativa atrai íons de carga positiva. Então, o íon sódio que tem uma carga
positiva vai entrar por esse canal, atraído pela negatividade que vai fazer com que eu
despolarize o interior da célula. Despolarizando o interior da célula, vou ter excitação. A
acetilcolina é um ligante endógeno desse receptor. Temos um sítio de ligação
específico para o GABA, os benzodiazepínicos e os barbitúricos também atuam aí, o
álcool também, e mais um monte de fármacos. Quando o GABA se liga no seu sítio de
ligação, vai abrir os poros e o interior desse receptor se torna positivo e quando o poro
se abre, vai ocorrer a atração de íons de cargas negativas, vai aumentar a negatividade
da célula, vai hiperpolarizar e vamos ter uma inibição.
Tenho em milisegundos a ligação da acetilcolina nas junções neuromusculares e
o músculo contrai e relaxa conforme a concentração da acetilcolina em relação aos
receptores nicotínicos.
Nessa estrutura tridimensional está mostrando o plano da membrana, com essas
proteínas, aqui mostra o receptor nicotínico da acetilcolina e só onde a acetilcolina está
ligada, o poro está aberto e temos os íons entrando.
Vamos mostrar esse receptor nicotínico na junção neuromuscular. Quando a
acetilcolina se liga na junção neuromuscular, eu tenho um neurônio motor fazendo
conexão com uma fibra muscular estriada esquelética. Na sinapse tenho um neurônio
motor liberando acetilcolina e a acetilcolina se ligando nos seus receptores nicotínicos
que estão na célula da musculatura esquelética. Essa acetilcolina é liberada quando
chega um potencial de ação na fibra muscular e vai atuar nos receptores nicotínicos
(molécula ligada a canal), são liberadas 2 acetilcolina para abrir o canal. O poro aberto
faz entrar sódio e desse modo, a célula fica despolarizada e se contrai. Existem
fármacos que também se ligam nesse receptor nicotínico.
Então, quando a acetilcolina é liberada ela vai funcionar como agonista nesse
receptor nicotínico, ela promove a contração através da entrada de íons sódio. Os
índios colocam veneno na ponta das lanças para caçar animais, usam Curari que é
uma mistura de alcalóides. O principio ativo do curari que causa a paralisia é uma
substância conhecida como tubocurarina, ela é um antagonista do receptor nicotínico
na junção neuromuscular, não deixa a acetilcolina se ligar, o núcleo paralisa e ai eles
aproveitam para matar o animal. Na prática clínica, usamos drogas como essa em
anestesias. Quando o cirurgião necessita fazer uma cirurgia que precise da paralisia
total do músculo, por exemplo no músculo abdominal, ele administra atracúrio,
tecurônio, pancurônio, ou seja, drogas que sejam antagonistas do receptor nicotínico
na junção neuromuscular.
Ach
Receptor nicotínico
Tubocurarina
Atracúrio
Todos os antagonistas são antagonistas competitivos do receptor nicotínico, eles
ligam e se desligam. Se eu aumentar a dose de acetilcolina eu consigo desligá-los. Por
exemplo, no caso dessas drogas tubocurarina, atracúrio, se eu aumentar os níveis de
acetilcolina na fenda sináptica, eu consigo reverter o bloqueio, ou seja, isso mostra que
é um antagonista competitivo reversível. Mas como eu posso aumentar os níveis de
acetilcolina na fenda sináptica? Inibindo sua degradação, dando um anticolinesterásico.
Então, a neosignina é usada para reverter o efeito desses bloqueadores
neuromusculares. Por exemplo, quando acaba a cirurgia e o anestesista quer que
termine o efeito da anestesia, ele pode dar neosignina para acabar o efeito. Por que
esses anestésicos só são usados em cirurgias, em hospitais, em ambientes totalmente
monitorados? Porque eles causam a paralisia de toda a musculatura esquelética,
inclusive a do músculo respiratório, então, para a pessoa receber uma droga como
essa, ela precisa estar sendo ventilada artificialmente.
RECEPTOR TIPO II: São os mais importantes, são os receptores ligados a proteína
G, também conhecidos como GPCR. Esses receptores recebem vários nomes,
receptores metabotrópicos, receptores helicoidais. Constituem a maior família e eles
sempre têm acoplamento com uma proteína G. Mas o que é essa proteína G? A
proteína G é como um “carteiro”, ela pega a informação do remetente e leva para o
destinatário, ela é o elemento de comunicação entre o receptor e o efetor daquele
mecanismo de transdução. A proteína G faz interação com o nucleotídeo de guanina,
GDP e GTP. Existem inúmeros de exemplos de receptor como esse, coloquei apenas 3
exemplos aqui: o receptor muscarínico da acetilcolina (aquele que está no coração e
faz bradicardia), o receptor M2, todos os receptores das catecolaminas (são
neurotransmissores que tem o agrupamento catecol: adrenalina, noradrenalina,
dopamina, todos eles são ligados à proteína G). Quantos receptores têm a adrenalina e
a noroadrenalina? Têm 2, alfa e beta, só que eles têm vários subtipos de receptores. A
dopamina tem 4 tipos de receptores B1, B2, B3 e B4 (todos são ligados a proteína G).
Todos os receptores de serotonina, o receptor da angiotensina, da histamina. Na
estrutura, temos 7 alfa hélices atravessando a membrana, temos uma alça
citoplasmática mais longa do lado interno da membrana que faz interação com a
proteína G. Esses receptores são receptores de resposta rápida, não tão rápida como
os receptores tipo 1 que têm resposta em milisegundos, mas esses receptores ligados
à proteína G tem uma resposta em segundos.
Como eu disse, a proteína G é o carteiro, leva a informação do receptor para o
efetor. Ela é uma proteína constituída por 3 subunidades: alfa, beta e gama e essas
subunidades estão ancoradas na membrana. A subunidade alfa é a subunidade que
tem atividade enzimática, ela faz a hidrólise do GTP para o GDP quando ela é ativada.
A amplificação do sinal se dá porque a proteína G consegue se difundir pelo plano da
membrana quando ela está ativada e depois volta a ficar em repouso quando o
receptor não está mais ativado.
Esse desenho mostra um receptor metabotrópico ligado a sua proteína G
(constituída de 3 subunidades), ele está em fase de repouso. Aqui eu tenho 2 outros
alvos nessa célula, pode ser uma enzima, pode ser um canal iônico. Quando esse
receptor é ativado por um fármaco ou por um ligante endógeno qualquer, a subunidade
alfa que tem atividade enzimática, ela troca sua molécula de GDP por GTP e se torna
ativada. A subunidade beta e gama se difundem pela membrana junto com a
subunidade alfa, elas têm a capacidade de se amplificar pelo plano da membrana. A
subunidade alfa pode atingir um alvo qualquer que pode ser uma enzima que esteja na
membrana da célula e essa subunidade alfa ativada pode ativar ou inibir essa enzima.
As subunidades beta e gama podem ativar um alvo qualquer na célula que pode ser
uma outra enzima ou canal iônico. Uma vez que elas mandaram a informação e
ativaram seus alvos, a subunidade alfa hidrolisa o seu GTP e volta a ficar GDP e o
receptor volta em estado de repouso. Mas e o que acontece com os alvos? Vamos
entender melhor vendo cada tipo de receptor.
Função da proteína G. A proteína G consiste em 3 subunidades (alfa, beta, gama), que estão
ancoradas à membrana através de resíduos de lipídios. O acoplamento da subunidade alfa a um
receptor ocupado por agonista induz a troca do GDP ligado pelo GTP intracelular; a seguir, o
complexo alfa-GTP dissocia-se do receptor e do complexo de subunidades py (beta e gama
unidas) e interage com uma proteína-alvo (alvo 1, que pode ser uma enzima, como a adenilato
ciclase, ou um canal iônico). O complexo beta e gama também pode ativar uma proteína alvo (alvo
2). A atividade de GTPase da subunidade alfa é aumentada quando ocorre ligação da proteína
alvo, resultando em hidrólise do GTP ligado a GDP, quando ocorre a união da subunidade alfa
com o complexo py (beta e gama unidas).
EXEMPLO: Aqui mostra o receptor, a proteína G, o alvo dessa proteína G que
aqui é uma enzima e o que pode acontecer quando a proteína G ativa esse alvo:
vamos supor que o fármaco ou o ligante endógeno ativou o receptor, a proteína G foi
ativada e ativou uma enzima e essa enzima aumentou a produção de segundos
mensageiros. Quando isso acontece, eu posso ter vários efeitos na célula, posso ter
uma contração celular, posso ter uma despolarização ou hiperpolarização da célula ou
eu posso ter uma secreção, vai depender em que tipo de célula isso está acontecendo.
Se for uma célula contrátil, ela pode se contrair ou relaxar, se for uma célula secretora,
ela pode secretar o seu conteúdo, se for uma célula excitável ela pode ser excitada ou
inibida.
Se vários receptores são ligados à proteína G, por que eu tenho tantas
respostas diferentes dependendo do tipo de receptor que está sendo ativado? Porque
eu tenho proteína G diferentes, cada receptor é acoplado a um tipo de proteína G. Vou
mostrar 3 tipos de proteína G que são mais importantes: a proteína G S que estimula a
adenilato ciclase, a proteína G I que é essa enzima adenilato ciclase e a proteína G Q
que tem seletividade. Se o receptor for acoplado a uma proteína G S, sempre que ele
for ativado, ele vai estimular a adenilato ciclase que vai aumentar a produção de
segundos mensageiros na célula. Se o receptor for acoplado a uma proteína G I que é
inibitória, ele vai inibir a enzima adenilato ciclase e vai diminuir a produção de
segundos mensageiros na célula. Se o receptor for ligado a uma proteína G Q, vai
sempre ativar uma enzima conhecida como proteinoquinase. Vamos dar exemplos de
receptores que atuam em cada uma dessas subunidades: então os alvos da proteína G
podem ser a enzima adenilato ciclase, a fosfolipase, os canais iônicos de cálcio e
potássio (só na 6ed do Rang e Dale saiu esse quarto alvo protéico) e o sistema Hho
A/Hho quinase (não vamos estudar nenhum fármaco que tenha esse alvo).
O que acontece quando o receptor é acoplado a uma proteína G S que vai
estimular uma adenilato ciclase? A adenilato ciclase é uma enzima que está ligada a
membrana celular, quando ela é ativada, sempre vai acontecer: a enzima adenilato
ciclase vai utilizar o substrato ATP para produzir AMPcíclico dentro da célula e o
AMPcíclico aumentado vai causar vários efeitos dentro da célula. O AMPcíclico
também é degradado por enzimas conhecidas como fosfodiesterases que transformam
ele em 5´AMP e ele perde sua atividade. Curiosidade: existem fármacos que são
inibidores dessa enzima fosfodiesterase dentro da célula, exemplo da cafeína e o
fármaco Silbenacil (Viagra, ele é inibidor de fosfodiesterases nas células de
musculatura lisa dos vasos). Quando eu inibo essa enzima, eu aumento a quantidade
de AMPcíclico dentro da célula e tenho um relaxamento dessa musculatura lisa, por
isso que o vaso dilata, por isso que o viagra é vasodilatador.
Quando eu aumento a quantidade de AMPcíclico dentro da célula, eu peço
regular várias funções dessa célula: ele pode ativar ou inibir enzimas envolvidas no
metabolismo energético, ele pode ativar ou relaxar proteínas contráteis, e ele pode
estar envolvido no transporte de íons, abrir ou fechar canais de sódio. Mas como ele
faz isso? Através de um único mecanismo dentro da célula que é ativação de proteína
quinase naquela célula. Sempre quando AMPcíclico é formado, eu ter ativação da PKA
que é uma proteína quinase. E o que essas proteínas quinases regulam? Elas regulam
a função de várias proteínas dentro da célula, catalisando, fazendo fosforilação de
resíduos dessas proteínas.
Olha o desenho: aqui é o receptor ligado a uma proteína G S, quando esse
receptor é ativado, eu vou ter a ativação dessa proteína, a subunidade alfa vai ativar a
enzima adenilato ciclase que estava quietinha, ela vai transformar o ATP em
AMPcíclico. O aumento do AMPcíclico no citoplasma da célula vai ativar uma proteína
quinase que estava quietinha. Ela ativada, vai fosforilar outras proteínas.
Vamos entender o porquê quando usamos um fármaco broncodilatador, eu
tenho a broncodilatação. Temos receptor beta2 no pulmão e quando a adrenalina se
liga nesse receptor, eu tenho broncodilatação. Vamos entender como essa
broncodilatação acontece: esse receptor beta2 adrenérgico, ele está presente na
verdade na musculatura lisa que envolve o brônquio. Quando a adrenalina se liga
nesse receptor Beta2, em questão de segundos, (ele está acoplado na proteína G S)
ele vai ter efeito estimulatório. Ele vai ativar uma enzima, dentro dessa célula, chamada
adenilato ciclase. A adenilato ciclase vai aumentar a produção de AMPcíclico dentro da
célula. O AMPcíclico aumentado vai ativar a proteína quinase que estava quietinha no
citoplasma. As proteínas quinases vão fosforilar uma outra proteína na célula chamada
miosina de cadeia leve que são as proteínas responsáveis pela contração da célula.
Quando fosforila essa proteína, ela não consegue mais contrair, ela relaxa e eu vou ter
relaxamento da musculatura lisa que envolve o brônquio e vou ter broncodilatação. Isso
tudo acontece em 1 segundo, a adrenalina se ligou, ativou proteína G S, ativou
adenilato ciclase, produziu AMPcíclico, ativou PKA, fosforilou a miosina de cadeia leve,
relaxou a célula e o brônquio dilatou. Existem fármacos muito famosos que fazem isso:
Berotec que é o Fenoterol, o Aerolin que é o Sanol, eles são todos agonistas de
receptor Beta2, como a adrenalina usada no tratamento da asma, o Berotec na
inalação.
Explicação para os “pais”: o Berotec é o fenoterol, é um agonista beta2, ele se
liga num receptor ligado a proteína GS que estimula a adenilato ciclase, que aumenta a
produção de AMPcíclico dentro da célula, que vai ativar a proteína quinase, que vai
fosforilar a miosina de cadeia leve, que vai relaxar a célula e o brônquio vai dilatar.
Isso é o mecanismo de transdução de sinal que é ativado simplesmente quando
um fármaco se liga como agonista do receptor. E se o fármaco for antagonista desse
receptor, o que acontece? O propanolol é antagonista do receptor beta2, tanto que
asmático não pode usar propanolol porque vai bloquear esse receptor no brônquio e
vai impedir a broncodilatação natural, aí eu vou ter broncoconstrição e posso ter uma
crise asmática.
O Atroven é usado junto com o Berotec (para ter uma broncodilatação maior
porque você usa um fármaco que estimula a broncodilatação com um fármaco que
bloqueia o receptor que faz broncoconstrição. Você dá doses menores de cada um
para ter um efeito maior.), só que o atroven se liga em outro receptor, se liga em um
receptor muscarínico M1 que é o Ipratrópio, o nome comercial. O Ipratrópio é
antagonista desse receptor muscarínico M1, então ele se liga a esse receptor
muscarínico M1 e não deixa a acetilcolina (agonista natural desse receptor) se ligar. A
acetilcolina faz broncoconstrição e quando eu utilizo o antagonista, eu não deixo a
acetilcolina se ligar, eu vou ver só a adrenalina no pulmão, por isso que dá
brônquiodilatação.
M1
Adrenalina
Beta 2
Broncodilatação
O segundo alvo da proteína G.....próxima aula!