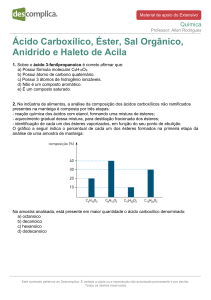
BIOQUÍMICA
LIPÍDEOS → produtos naturais de origem animal ou vegetal onde
predominam ésteres de ácidos graxos superiores.
Os lipídeos mais comuns são conhecidos como óleos e
gorduras.
ÁCIDOS GRAXOS SUPERIORES
- Possuem mais de 10 carbonos na cadeia
- Possuem cadeia normal
- São saturados ou insaturados por duplas
- São monocarboxílicos
- Tem número par de átomos de carbono
CLASSIFICAÇÃO
Glicéridos
Céridos
Fosfátidos
Cerobrósidos
1- GLICÉRIDOS
São misturas de ésteres onde temos:
→ parte alcoólica → glicerina ou propanotriol
→ parte ácida → ácidos graxos superiores
O
║
H 2C – O – C - R
O
║
HC- O–C-R
O
║
H 2C – O – C - R
PRINCIPAIS ÁCIDOS GRAXOS SATURADOS
Ácido láurico
Ácido palmítico
Ácido esteárico
C11H23 – COOH
C15H31 – COOH
C17H35 – COOH
INSATURADOS
Ácido oléico C17 H33 – COOH 1 dupla
Ácido linoleico C17H31 – COOH 2 duplas
Ácido linolênico C17H29 – COOH 3 duplas
Os glicerídeos representam os óleos e as gorduras naturais.
GORDURAS → ésteres de glicerina e ácidos graxos saturados.
ÓLEOS → ésteres de glicerina e ácidos graxos insaturados.
Na prática um glicerídeo é gordura. Quando na temperatura
ambiente é um sólido e será um óleo quando for um líquido na
mesma temperatura.
Em termos industriais há o interesse em transformar óleo em
gordura. Para isso, basta efetuar a hidrogenação catalítica - a
margarina é um exemplo.
PROPRIEDADES
SAPONIFICAÇÃO
Reação dos glicerídeos com NaOH ou KOH obtendo o sabão.
Glicerídeo + base → glicerina + sabão
Com NaOH obtém-se sabões sólidos ou também denominados
sabões duros.
Com KOH obtém-se sabões líquidos ou pastosos ou também
denominados sabões moles.
ÍNDICE DE SAPONIFICAÇÃO (IS)
É o número de miligramas de KOH necessário para saponificar
completamente 1 grama de óleo ou gordura.
Manteiga
→ IS = 210-230
Óleo de algodão → IS = 190-200
Óleo de linhaça → IS = 180-195
Toucinho
→ IS = 190-200
ÍNDICE DE IÔDO
É o número de gramas de iodo (I2) capaz de reagir com 100 gramas de
óleo ou gordura.
Sebo de Boi
I I = 30 - 50
Manteiga
I I = 25 - 50
Óleo de baleia
I I = 110 - 150
RANCIFICAÇÃO
Trata-se de uma série complexa de reações que se efetuam na
presença do oxigênio do ar e também catalisadas pelas bactérias
existentes no mesmo.
A característica desta reação é o desprendimento de um odor
desagradável.
2- CÉRIDOS
São conhecidos como ceras, podendo ser de origem animal ou
vegetal: cera de carnaúba, cera de abelha, etc.
Os céridos são formados por ésteres de ácidos graxos e
álcoois superiores.
Ácido graxo superior → C15H31 – COOH Ácido palmítico
Álcool superior→ C15H31 – CH2-OH Álcool cetílico
3- FOSFÁTIDOS
Conhecidos também como fosfolipídeos.
Na constituição dos ésteres desses lipídeos participam:
glicerina + ácido graxo + H3PO4 + amino álcool
4- CEREBRÓSIDOS
São lipídeos complexos, semelhantes aos fosfátidos.
As diferenças fundamentais entre um fosfátido e um
cerebrósido são:
a) Ao invés de glicerina temos → C6H12O6
b) Não possui ácido fosfórico.
Constituição do éster cerebrósido:
C6H12O6 + ácido graxo + amino álcool
Os cerebrósidos são encontrados em todas as células,
principalmente no tecido nervoso.
GLICÍDEOS OU GLÚCIDES OU AÇÚCARES OU
HIDRATO DE CARBONO
Encontrados em grande abundância no reino animal e vegetal.
O nome hidrato de carbono ou carboidrato deve-se ao fato de
os primeiros glicídeos descobertos obedecerem a fórmula
Cx(H2O)y.
Definição atual:
Função mista: poliálcool + aldeído
poliálcool + cetona
CLASSIFICAÇÃO
OSES
Aldoses → poliálcool + aldeído
Cetoses → poliálcool + cetona
OSÍDEOS
As oses não hidrolisam, enquanto que, os osídeos podem
sofrer hidrólise produzindo oses.
Holosídeos → quando a hidrólise só produz oses.
Sacarose + água → glicose + frutose
Maltose + água → glicose + glicose
Lactose + água → glicose + galactose
Amido + água → n glicose
Heterosídeos → quando a sua hidrólise produz oses ao lado de
outros compostos.
Amigdalina + água → 2 glicose + HCN + benzaldeido
A amigdalina é encontrada em amêndoas amargas.
PRINCIPAIS GLICÍDEOS
1- GLUCOSE OU GLICOSE OU DEXTROSE
Fórmula C6H12O6 - é encontrada no suco da uva e também em
diversos frutos.
Industrialmente é obtida pela hidrólise do amido.
( C6 H10O5 )n + n H2O → n C6H12O6
2- FRUTOSE OU LEVULOSE
É a mais importante cetose, encontrada no mel, e muitos
frutos.
A frutose tem apenas 3 carbonos assimétricos, logo são 8
isômeros ópticos com sua fórmula estrutural.
A frutose é um produto da hidrólise de muitos osídeos.
3- SACAROSE OU SUCROSE
Sua fórmula é C12H22O11 - sendo um dissacarídeo muito
importante é também chamado de açúcar comum.
Existe em grande quantidade na cana de açúcar e na beterraba,
de onde é extraído. A sacarose é constituída de uma molécula
de glicose e outra de frutose.
4- LACTOSE
Sua fórmula é C12H22O11 - conhecida como açúcar do leite. É um
dissacarídeo, isômero da sacarose, e também da maltose e
celobiose.
5- CELULOSE
Sua fórmula é ( C6H10O5 )n , tendo peso molecular médio de
400.000, sendo, portanto, um polímero natural - extraído da
madeira.
6- AMIDO
Sua fórmula é (C6H10O5 )n , tendo peso molecular médio entre
60.000 e 1.000.000, sendo também um polímero natural,
encontrado como produto reserva das plantas, nos cereais,
também nas raízes ou tubérculos, nesse caso é chamado de
fécula - é insolúvel na água fria.
7- GLICOGÊNIO
Sua fórmula é (C6H10O5)n , seu peso molecular médio é menor
que do amido, enquanto as plantas reservam amido, os
animais reservam glicogênio.
É encontrado principalmente no fígado e nos músculos.
Também é denominado amido animal.