,-Dicloração de acetofenonas utilizando ácido tricloro-isocianúrico
e desenvolvimento da reação de Knoevenagel em meio aquoso
José Yago Rodrigues Silva (IC), Gyslaine Sabrina de Lira Paes (IC), José Arimateia Nóbrega
*
(PQ)
DQ/UEPB - Av. das Baraúnas, 351, CEP 58.109-753, Campina Grande - PB Campus Universitário,
Bodocongó. *e-mail: [email protected]
Palavras-chave: Iodo Molecular; Tiocianação; Cetotiocianatos, reação de knoavenagel.
INTRODUÇÃO
,-dialocetonas
são
substâncias
cujas
aplicações
são
pouco
exploradas. Alguns exemplos representativos envolvem a obtenção de
derivados de diidrofuranos através de cicloadição [3+2] (YOSHIDA, 1984) e,
mais recentemente, a síntese de 1,4-dionas mediada pelo monobrometo de
índio (PEPPE, 2004). O pouco uso das dialocetonas deve-se, em parte, a
escassez de métodos altamente eficientes e experimentalmente simples para a
sua obtenção. Entre os mais recentes, podemos citar a dicloração de cetonas
com CuCl2 (NOBREGA, 2002). Interessados na química do ácido tricloroisocianúrico (1), um reagente estável, de fácil manipulação e facilmente
encontrado no comércio, apresentamos aqui o seu uso como reagente para a
dicloração de cetonas.
O
Cl
Cl
N
N
(1)
O
N
O
Cl
A condensação de Knoevenagel entre aldeídos e compostos metileno
ativos é uma importante e amplamente utilizada metodologia de formação de
ligação carbon-carbono em síntese orgânica, com várias aplicações em
química fina, reações hetero Diels-Alder e na produção de compostos
carbocíclicos e heterocíclicos com importância biológica (DEB, 2005). Diante
dessa importância e tendo como referência os princípios da química verde,
iremos mostrar nesse trabalho a viabilidade de desenvolver essa clássica
reação orgânica em meio aquoso, com ou sem catalisadores (Esquema 1).
H2O
onde: Y = Grupo elétron retirador
Esquema 1 – Reação de Knoevenagel
RESULTADOS E DISCUSSÃO
A reação de monocloração de cetonas utilizando (1) já encontra-se
descrita na literatura (HIEGEL, 1985). Entretanto, uma simples variação nas
condições experimentais possibilitou o desenvolvimento de uma nova extensão
para essa reação. Cetonas reagem com um equivalente molar de (1) em
acetonitrila e sob refluxo, para produzir os respectivos compostos ,diclorados. Para o pleno desenvolvimento dessas reações é necessária a
presença de um aditivo ácido, como o ácido p-toluenosulfônico (2 mmol).
Dessa forma, os tempos de reação são muito reduzidos e os rendimentos
otimizados. O esquema 2 resume essas informações.
O
O
CH3
R1
(1), TsOH
R2
CHCl 2
CH3CN, refluxo
1 - 2 horas
R1
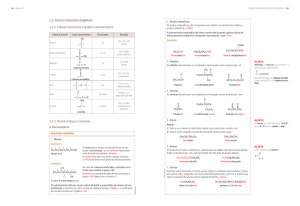
Esquema 2 – Dicloração de acetofenonas.
A tabela 1 apresenta os resultados obtidos. As cetonas utilizadas nas
reações foram acetofenonas com substituintes no anel na posição para. Os
rendimentos obtidos foram excelentes, não havendo, de uma forma geral, uma
grande influência se o substituinte tem características elétron retiradoras
(entradas 3 e 4) ou doadora (entrada 2). Entretanto, há um importante efeito
com a presença de substituintes metóxi. Esse grupo induz a cloração no anel
(entrada 5), a tal ponto que ao se utilizar a 3’,4’,5’-trimetóxiacetofenona, ocorre
cloração exclusivamente no anel aromático (formação da 2’,6’-dicloro-3’,4’,5’trimetóxi-acetofenona).
Tabela 1 – Resultados das diclorações.
Entrada
1
2
3
4
5
R1
H
CH3
NO2
Cl
OCH3
R2
H
H
H
H
Cl
Tempo (h)
1,5
1,5
2
2
1
Rendimento (%)
98
93
92
95
86
*
* Rendimento a partir do isolamento em coluna cromatográfica.
Com relação as condensações de Knoevenagel, relatamos aqui um
método muito simples e eficiente para a condensação de vários aldeídos
aromáticos com 2 tipos de compostos de metileno ativo, a malononitrila e o
cianoacetato de etila em água, com agitação e aquecimento (Esquema 3).
H2O
800C
Agitação
H2O
onde: Y = Grupo elétron retirador
Esquema 3 – Reação de Knoevenagel em meio aquoso.
As reações ocorreram de forma rápida e em ótimos rendimentos,
principalmente no caso da malononitrila. O procedimento experimental é
bastante simples: a uma solução em agitação do composto metileno ativo em
água (8 ml) foi adicionado o aldeído (1 equivalente). Após o tempo apropriado
em aquecimento (800C), o sólido produzido foi isolado por filtração simples e
seco. O material isolado foi identificado por ponto de fusão e por ressonância
magnética nuclear.
A tabela 2 apresenta os resultados obtidos. Os rendimentos são
expressivos e no caso da malononitrila, pode-se observar um tempo de reação
muito inferior ao do cianoacetato de etila. Neste último caso foi acrescentado
10% de DBU (1,8-Diazabicyclo[5.4.0]undec-7-ene) como catalisador.
Tabela 2 – Resultados das reações de Knoeavenagel.
Entrada
1
2
3
Y1
CN
CN
CN
Y2
CN
CN
CO2Et
R
4-OH-C6H4
4-OH-3-OCH3-C6H3
4-OH-C6H4
Tempo (min.)
3
4
40
Rendimento (%)
92
90
86
*
* Rendimento a partir do isolamento em coluna cromatográfica.
CONCLUSÕES
O ácido tricloro-isocianúrico é bastante eficiente para realizar a ,dicloração de aril cetonas e de 1,3-dionas. Os altos rendimentos e a
simplicidade experimental tornam esse método uma alternativa importante para
a obtenção dessa classe de compostos. A presença de radicais metóxi
favorece a cloração no anel.
A reação de knoavenagel em meio aquoso é eficiente e pode
representar uma importante alternativa como metodologia sintética para essa
importante reação orgânica.
REFERÊNCIAS
Deb, M. L. e Bhuyan, P. J. Uncatalysed Knoevenagel condensation in
aqueous medium at room temperature, Tetrahedron Letters, 2005, vol. 46,
pág. 6453.
Hiegel, G. A. e Peyton, K. B. J. C. Chlorination of Ketones with
Trichloroisocyanuric Acid, Synthetic Communications., 1985, vol. 5, pág.
385.
Nobrega, J. A.; Gonçalves, S. M. C. e Peppe, C. Selective Preparation of α,αdichloroketones with Copper(ii) Chloride, Synthetic Communications., 2002,
vol. 32, 3711 - 3717.
Peppe, C. e Chagas, R. P. Indium(I) Bromide-Mediated Reductive Coupling
of α,α-Dichloroketones to 1-Aryl-butane-1,4-diones, Synlett. 2004, 11871190.
Yoshida, J.; Yano, S. e Ozawa, T. Regioselective synthesis of dihydrofurans
from 2,2-dibromo-1,3-diketone and olefin using copper, Tetrahedron Lett.,
1984, vol. 25, pp 2817-2820.