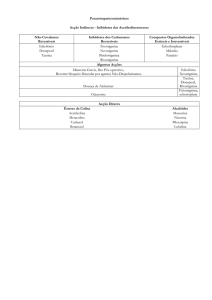
III – 1. Fármacos antivirais.
Aspectos gerais dos vírus: fases do ciclo replicativo viral; alvos macromoleculares de fármacos antivirais.
Fármacos inibidores da aspartil-protease (continuação)
Graham L. Patrick; An Introduction to Medicinal Chemistry 4/e, Oxford University Press, New York, 2009.
MF Simões, QF II, 11-12
1
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
3. Indinavir
L 704486
IC50 7.6 nM
Drug design
Hybrid formed from P’ halves of Saquinavir and L 685434
L 732 747
IC50 0.5 nM
Piperazine ring (better water solubility and oral bioavailability).
Benzyloxycarbonyl
Piperazine
high activity
Structure IV
IC50 0.3 nM
Benzyl group increases activity twofold and water
solubility is decreased
Benzyl group
S2'
S2
S3
Pyridine
2
S1
S1'
Indinavir
IC50 0.56 nM
Ki 0.34 nM
EC95 0.10 mM
•Pyridine ring (lipophilic) contains nitrogen, improves
water solubility and oral bioavailability.
•Potent inhibitor with negligible activity against
mammalian proteases
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
4. Nelfinavir
O
N
H H
N
O
O
H
N
H H
CONH2
Me
H
N
H
N
Ph
O
N
H
N
O
HO
H
OH
H
N
H
OH
H
H
AG 1310 Ki 21 nM
Saquinavir
S3
Extended
substituent
S1
S2'
Val-32
Ile-84
S
Me
O
O
H
N
S
Me
H
HO
N
H
N
OH
H
H
N
H
N
H
OH
H
H
3
O
H
N
HO
Asp-30
Nelfinavir
Ki 2.0 nM
EC50 0.008-0.20 mM
O
S2
Asp-25 Asp-25'
S1'
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
Ile-50
5. Palinavir
Ile-50'
O
H
S3
H
S1
S2'
Ph
O
N
H
N
H
N
O
H
N
N
O
OH
S2
O
S1'
Extended substituent
N
S3'
•Contains a hydroxyethylamine transition state isostere
•P half of molecule is similar to saquinavir
•Proline of saquinavir is replaced with an extended substituent (P1’). Extended substituent is
designed to occupy the S1’ and S3’ subsites
•Six subsites are occupied (S3-S3’)
•Amide oxygens and nitrogens form hydrogen bonds to groups in active site
•Amide oxygens form hydrogen bonds to the bridging water (Ile)
•Hydroxyl group forms hydrogen bonds to catalytic aspartates (with hydroxyethylamine)
4
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
6. Amprenavir and darunavir
Drug design
O
Ph
N
Ph
O
N
H H
N
H
OH
CONH2
*
O
H H
N
N
H
N *
N
H H
O
H
H
N
H H
H
*
O
N
OH O2S
CONH2
I
H
Isobutyl
sulfonamide
group
Saquinavir
Bis-tetrahydrofuryl
group
O
H
Ph
O
O
H
Ph
O
H
O
N
N
H H
Aniline group
Tetrahydrofuran
OR O2S
carbamate group
O
O
H
N
H H
N
OH O2S
NH2
Amprenavir (R=H) (IC50 12-80 nM)
Fosamprenavir (R=Phosphate)
5
Darunavir
NH2
•Mutations are less likely to lead to resistance
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
•Approved in 2003
Atazanavir
•First once daily administered protease inhibitor
P2’
Ph
O
P1
O
H
N
MeO
H
N
N
H
O
N
OH
N
H
OMe
O
P2
N
Extended
substituent
(P1’ and P3’)
Atazanavir
6
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
Tipranavir
•Não é um peptidomimético mas sim uma cumarina
Ile-50 Ile-50'
•4-Hydroxyl group forms hydrogen bonds to the catalytic aspartates
O
P2
O
4
•Lactone oxygens form hydrogen bonds directly to Ile-50 and Ile-50’ in
the enzyme flaps
P1'
•First PI to bind directly to flaps with no bridging water involved
OH
P1
Me
Asp-25
•Novel pharmacophore of hydrogen bonding interactions
Asp-25'
N
F3C
SO2HN
O
O
OH
Me
Ph
Me
Tipranavir
Ki 8 pM; IC50 30 mM
•Increased metabolic stability
•First protease inhibitor designed from a non-peptide lead compound
7
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
http://www.fda.gov/ForConsumers/byAudience/ForPatientAdvocates/HIVandAIDSActivities/ucm118915.htm
8
MF Simões, QF II, 11-12
III – 1. Fármacos antivirais. Fármacos inibidores da aspartil-protease, em vírus ARN. Inibidores peptídicos e inibidores
análogos dos péptidos: modo de acção, relação estrutura/actividade, design.
9
MF Simões, QF II, 11-12