TESE
INTERAÇÕES BEMISIA TABACI BIOTIPO B E
TOMATO CHLOROSIS VIRUS EM
CLONES DE BATATA
LILLIAN SILVEIRA PEREIRA
Campinas, SP
2016
ii
INSTITUTO AGRONÔMICO
CURSO DE PÓS-GRADUAÇÃO EM AGRICULTURA
TROPICAL E SUBTROPICAL
INTERAÇÕES BEMISIA TABACI BIOTIPO B
E TOMATO CHLOROSIS VIRUS EM
CLONES DE BATATA
LILLIAN SILVEIRA PEREIRA
Orientador: André Luiz Lourenção
Coorientador: Fernando Javier Sanhueza Sallas
Tese submetida como requisito parcial para
obtenção do grau de Doutor em Agricultura
Tropical e Subtropical, Área de Concentração
em Tecnologia da Produção Agrícola
Campinas, SP
Abril 2016
iii
AGRADECIMENTOS
A todos da minha família, meu infinito agradecimento, pois sempre acreditaram em minha
capacidade. Obrigada pelo amor incondicional!
Aos amigos e pessoas especiais, que tentaram compreender e ajudar nos dias mais difíceis.
Todo meu amor! E ao pequeno Billy, que esteve comigo em todos os momentos e se tornou
um anjo de quatro patas, ao final desse processo!
Ao Dr. André Luiz Lourenção, pela orientação e acima de tudo por acreditar em meu
potencial e estar sempre disposto a me ensinar. Devido ao seu companheirismo, amizade,
paciência, compreensão e apoio, este trabalho pôde ser concretizado. Muito obrigada!
Ao Dr. Fernando Javier Sanhueza Sallas pela co-orientação, e por estar sempre ao meu lado,
me pondo para cima e me fazendo acreditar que posso mais que imagino sem teu apoio e
atenção eu não conseguiria, Muito obrigada!
Ao Dr. Alberto Fereres, por todo ensinamento, amizade, dedicação e paciência, por me aceitar
como aluna pelo período em que passei em seu laboratório ICA-CSIC em Madri-Espanha.
Todo meu agradecimento!
Aos amigos e companheiros de laboratório ICA-CSIC, em especial Dra. Elisa Garzo pela
amizade e pela dedicação em me ensinar e me suportar todos os dias, a Dra. Aranzazu
Moreno por ser um exemplo de profissional e estar sempre disposta a ensinar, e ao amigo de
estância Jaime por ter feito do meu período em Madrid, os melhores e inesquecíveis.
Obrigada a todos e meu eterno carinho!
As brasileiras, Michele Timossi, Mauricélia Almeida e Nathalie Maluta, vocês são anjos na
minha vida, obrigada por me ajudarem em tudo e sempre, sem vocês eu não estaria aqui. Todo
carinho por vocês!
ii
Aos amigos de laboratório do Instituto Biológico em São Paulo, Thiago Pap, Thiago Navarro,
Daniele Gobatto, Ieda Mascarenhas e Adriano de Alencar, em especial a Samanta Zanotta por
toda ajuda nos testes moleculares, obrigada a todos pelas histórias de cursos, viagens e
congressos que contarei até aos bisnetos, vocês são partes de mim, e tornaram todo o processo
mais fácil e feliz.
Aos funcionários e amigos do Instituto Agronômico, Renata Berenguel e Nathalia Sgobi,
obrigada pelas horas de conversas e apoio, em especial ao Antônio Marcos de Souza, sem a
colaboração, ajuda técnica e ensinamentos, eu não teria sido capaz de fazer sozinha. Meus
eternos agradecimentos.
Aos professores da ESALQ, Dr. João Roberto Spotti Lopes, Dr. Jorge Alberto Marques
Rezende e Dr. José Mauricio Simões Bento, pela disponibilização dos laboratórios na
execução dos trabalhos e colaboração sempre que necessário.
A pesquisadora Dra. Maria Fernanda Gomes Villalba Peñaflor pelo ensinamento, colaboração
e ajuda nos ensaios de voláteis de plantas e análises estatísticas. Muito obrigada!
Ao engenheiro agrônomo Pedro Hayashi, pela disponibilização dos tubérculos-sementes, peça
chave para o sucesso desse trabalho.
Agradeço, a CAPES pelo apoio financeiro e à Pós-Graduação do Instituto Agronômico de
Campinas pela oportunidade.
Enfim agradeço a todos que colaboraram na execução deste trabalho, pois me ensinaram que
existe mais que vida científica e pesquisadores por trás de todo esse trabalho, existem vidas
humanas.
iii
SUMÁRIO
RESUMO.................................................................................................................................
vii
ABSTRACT.............................................................................................................................. viii
1 INTRODUÇÃO.....................................................................................................................
01
2 REVISÃO DE LITERATURA.............................................................................................. 03
2.1 A cultura da Batata.............................................................................................................
03
2.2 A Mosca-branca Bemisia tabaci (Genn.) ........................................................................... 04
2.2.1 Taxonomia de B. tabaci...................................................................................................
05
2.2.2 Aspectos biológicos de B. tabaci..................................................................................... 06
2.2.3 Interações mosca-branca e planta hospedeira.................................................................. 07
2.2.4 Danos causados pela mosca-branca................................................................................. 09
2.3 Transmissão de Fitovírus por Mosca-branca......................................................................
10
2.4 Compostos Voláteis de Plantas e Comportamento de Insetos............................................ 12
3 MATERIAL E MÉTODOS...................................................................................................
14
3.1 Locais de Realização do Estudo.........................................................................................
14
3.2 Clones de Batata Utilizados................................................................................................ 14
3.3 Produção, Manutenção e Infecção dos Clones de Batata...................................................
15
3.3.1 No Brasil..........................................................................................................................
15
3.3.2 Na Espanha......................................................................................................................
15
3.4 Manutenção da Colônia de Bemisia tabaci biótipo B......................................................... 16
3.4.1 No Brasil..........................................................................................................................
16
3.4.2 Na Espanha......................................................................................................................
16
3.5 Manutenção do Inóculo de ToCV....................................................................................... 17
3.5.1 No Brasil..........................................................................................................................
17
3.5.2 Na Espanha......................................................................................................................
18
3.6 Detecção de Tomato chlorosis virus................................................................................... 19
3.6.1 No Brasil - extração de RNA total para detecção de ToCV............................................
19
3.6.2 Nested RT-PCR...............................................................................................................
19
3.6.3 Na Espanha - extração de RNA total e RT-PCR em tempo real (TaqMan)....................
20
3.7 Efeito de Clones de Batata Infectados por ToCV sobre Parâmetros Biológicos de
Bemisia tabaci biótipo B........................................................................................................... 21
iv
3.7.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados.................
21
3.7.2 Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e infectadas..
22
3.7.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha.................................................................... 23
3.7.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas.............
24
3.7.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’................................................................................................................
24
3.7.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados..................................................................................................................................
27
3.8 Efeito de ToCV na Produção de Voláteis em Clones de Batata e Interação com Bemisia
tabaci biótipo B........................................................................................................................
27
3.8.1 Compostos voláteis de plantas sadias e infectadas..........................................................
27
3.8.2 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos.......................................................................................................................
29
4 RESULTADOS.....................................................................................................................
30
4.1 Efeito de clones de batata infectados por ToCV sobre parâmetros biológicos de Bemisia
tabaci biótipo B........................................................................................................................
30
4.1.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados.................
30
4.1.2 Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e infectadas..
31
4.1.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha.................................................................... 31
4.1.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas.............
32
4.1.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’................................................................................................................
33
4.1.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados..................................................................................................................................
36
4.2 Efeito de ToCV na Produção de Voláteis em Clones de Batata e Interação com Bemisia
tabaci biótipo B........................................................................................................................
37
4.2.1 Compostos voláteis de plantas sadias e infectadas..........................................................
37
4.2.2 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos.......................................................................................................................
37
5 DISCUSSÃO.........................................................................................................................
38
5.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados....................
38
v
5.2 Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e infectadas
39
5.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha.................................................................... 40
5.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas................
41
5.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’................................................................................................................
41
5.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados.................................................................................................................................
42
5.7 Compostos voláteis de plantas sadias e infectadas.............................................................
44
5.8 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos.......................................................................................................................
45
6 CONCLUSÕES.....................................................................................................................
47
7 REFERÊNCIAS BIBLIOGRÁFICAS..................................................................................
48
vi
Interações Bemisia tabaci biótipo B e Tomato chlorosis virus em clones de batata
RESUMO
A cultura da batata tem grande valor econômico, estimando-se rendimento de 88.782 kg/ha
para 2016. No entanto, é infectada por diversas doenças, destacando-se os fitovírus que são
perpetuados através da batata-semente, e disseminados por insetos vetores. A mosca-branca
Bemisia tabaci biótipo B representa um importante papel na transmissão de fitovírus. Dos
vírus transmitidos por essa mosca-branca na cultura da batata, o crinivírus Tomato chlorosis
virus (ToCV) causa clorose internerval das folhas, desenvolvendo pontos avermelhados e
necróticos, afetando a taxa fotossintética e, consequentemente, a produção final. Nesse
contexto, estudaram-se as inter-relações dessa mosca-branca com o vírus e a planta
hospedeira, considerando que a infecção viral afeta a fisiologia, a morfologia, a emissão de
voláteis da planta hospedeira,podendo modificar o comportamento alimentar e o ciclo de vida
do inseto vetor. No ensaio de atratividade dos adultos para os quatro tratamentos (‘Ágata’
sadia e infectada, Bach-4 sadia e infectada), como resultado, os dois clones de batata
infectados por ToCV são mais atrativos para adultos de B. tabaci biótipo B entre quatro e seis
horas após a infestação. Em ensaio de oviposição sem chance de escolha e com chance de
escolha para o inseto entre esses quatro tratamentos, não se constatou diferença no número de
ovos entre clones de batata sadios ou infectados. A movimentação do inseto vetor foi avaliada
das plantas sadias para as plantas infectadas e ao contrário, liberando-se os adultos em uma
planta e observando sua movimentação para a planta destino; no clone ‘Ágata’ há correlação
positiva na movimentação dos insetos de plantas infectadas para plantas sadias. Para o
comportamento alimentar da mosca-branca por meio da técnica Electrical penetration graph,
após registros para plantas de ‘Ágata’ sadias e infectadas, concluiu-se que os insetos fazem
mais picadas de prova e apresentam maior duração de atividade na fase floemática em plantas
infectadas. No ciclo de vida do inseto, desde a fase de ovo até a emergência dos adultos,
concluiu-se que plantas dos dois clones, quando infectadas, induzem menores tempos de
desenvolvimento. Por meio da extração dos voláteis dos quatro tratamentos, utilizando-se
cromatógrafo gasoso e identificados na biblioteca ‘Nist’ do software Workstation Toolbar,
concluiu-se que o tipo de volátil e sua quantidade diferem entre clones e entre plantas sadias e
infectadas. Em ensaio de dupla escolha, em que 20 insetos poderiam escolher entre planta
sadia ou infectada de ‘Ágata’ sem entrar em contato com a folha, na presença e ausência de
luz visível, observou-se que a preferência de adultos é maior para plantas infectadas na
ausência de luz.
Palavra-chave: Electrical penetration graph; mosca-branca; Solanun tuberosum; crinivirus;
voláteis
vii
Interactions Bemisia tabaci biotype B and Tomato chlorosis virus in potato clones.
ABSTRACT
The potato crop has great economic value, estimated yield of 88,782 kg / ha in 2016.
However, it is subjected to various diseases, highlighting the virus that are introduced through
the seed potatoes, and spread by insect vectors. Whitefly Bemisia tabaci biotype B, represents
an important role in virus transmission. Viruses transmitted by whitefly in the potato crop, the
Tomato chlorosis virus (ToCV) cause chlorosis internerval of leaves, developing reddish and
necrotic spots, affecting the photosynthetic rate and consequently the final production. In this
context, the interrelations of this whitefly were studied with the virus and the host plant,
whereas the viral infection affects the physiology, morphology, the emission of volatile host
plant and may modifies eating behavior and life cycle vector insect. In the test of the
attractiveness of adult for the four treatments ('Agata' healthy and infected, Bach-4 healthy
and infected), as a result, potato clones infected by ToCV are more attractive to adults of B.
tabaci biotype B between four and six hours of evaluation.In test oviposition no choice and
free choice for insect among these four treatments, there was no difference in the number of
eggs from healthy potato clones or infected. The insect vector movement was evaluated in
healthy plants for the infected plants and instead, freeing up the insect adult in a plant and
watching their movement to the plant destination; the clone 'Agata' there is a positive
correlation in the movement of insect infected plants to healthy plants. To feed whitefly
behavior by Electrical Penetration Graph technique, after records for 'Agata' healthy and
infected plants, it was concluded that the insects do more proof bites and have longer duration
of activity in the phloem phase in infected plants. In the insect's life cycle from the egg stage
to the adult emergence, it was found that two clones of the plants when infected induce
shorter development times. By means of extraction of volatiles from the four treatments using
a gas chromatograph and identified in library ' NIST " Workstation software Toolbar, it was
concluded the type of volatile and their quantity differ between clones and between healthy
and infected plants. In test double choice, 20 insects could choose between healthy plant or
infected of 'Agata' without contacting the leaves, in presence and absence of visible light, it
was found that adult preference is higher for infected plants in the absence light.
Keysword: Electrical penetration graph; whitefly; Solanun tuberosum; crinivirus; volatile.
viii
1 INTRODUÇÃO
A transmissão de patógenos de plantas por insetos vetores é um processo biológico
complexo envolvendo interações entre a planta hospedeira, o inseto vetor e o patógeno. Nessa
relação tritrófica, os vírus fitopatogênicos são dependentes da interação com o vetor, que pode
ser modificada tanto na planta quanto no inseto, afetando a transmissão e disseminação do
vírus (BLUA & PERRING, 1992; INGWELL et al., 2012; LUAN et al., 2013a).
As alterações causadas pelos vírus podem afetar a fisiologia, a morfologia, o estado
nutricional e a emissão de voláteis da planta hospedeira, além de modificar o comportamento
alimentar e a biologia do inseto vetor (BOSQUE-PERÉZ & EIGENBRODE, 2011; MAUCK
et al., 2012; CARMO-SOUZA et al., 2014;).
A batata (Solanum tuberosum L.) é afetada por diversas pragas e doenças, sendo que
entre as doenças se destacam as de etiologia viral. Aproximadamente 30 fitovírus podem
infectar esta hortaliça e a grande maioria pode ser introduzida através da batata-semente,
geralmente importada, e por insetos-vetores muito eficientes na disseminação e importantes
na epidemiologia das doenças de etiologia viral (FILGUEIRA, 2000).
Entre os principais problemas emergentes envolvendo insetos pragas em campos de
produção de batata, merece destaque a mosca-branca Bemisia tabaci (Genn.) biótipo B [= B.
argentifolii Bellows & Perring] (Hemiptera: Aleyrodidae), tanto pelos danos diretos (injeção
de toxinas, sucção de seiva) como pelos indiretos (desenvolvimento de fumagina nas folhas
pelas excreções açucaradas e transmissão de fitovírus) nas plantas hospedeiras
(LOURENÇÃO et al., 2003; SOUZA-DIAS et al., 2008; FREITAS et al., 2011).
Dentre os vírus transmitidos por mosca-branca, destaca-se o crinivírus Tomato chlorosis
virus (ToCV), relatado em lavouras de batata e transmitido por B. tabaci biótipo B (FREITAS
et al., 2011). Altas populações de B. tabaci biótipo B vêm sendo observadas nas principais
regiões produtoras de batata no Brasil, bem como a crescente detecção de plantas infectadas
por ToCV. Portanto, para desenvolvimento de métodos de controle eficientes de viroses na
cultura da batata, há a necessidade de se estudar as inter-relações dessa mosca-branca com
esse vírus e a planta hospedeira.
Testes que permitam observar a preferência para colonização da mosca-branca nos
diferentes clones de batata poderão auxiliar na seleção de plantas resistentes, juntamente com
a técnica de monitoramento eletrônico de atividade estiletar aplicada ao estudo do
comportamento alimentar de insetos. Por sua vez, estudos sobre voláteis emitidos pelas
1
plantas sadias e plantas infectadas com o vírus poderão contribuir para o entendimento da
atratividade do inseto para essas plantas.
Face ao exposto, o presente estudo teve por objetivo geral verificar se a infecção por
ToCV causa efeitos adversos em clones de batata. E os objetivos específicos são: verificar a
ocorrência de alteração da atratividade e da oviposição de adultos de B. tabaci aos clones de
batata sadios e infectados; verificar a movimentação dos insetos adultos entre as plantas dos
diferentes clones sadios e infectados; verificar o comportamento alimentar de B. tabaci nos
clones de batata sadios e infectados; verificar alteração no ciclo de vida de B. tabaci nos
clones de batata sadios e infectados; verificar diferença nos compostos voláteis emitidos por
clones sadios e infectados; verificar a atração dos insetos de B. tabaci frente aos voláteis
emitidos nos clone Ágata sadio e infectado. Informações dessa natureza podem auxiliar no
manejo desse vírus em campo, uma vez que o comportamento do vetor tem forte implicação
ecológica e evolucionária na transmissão de vírus para plantas hospedeiras.
Esses objetivos foram definidos com base nas seguintes hipóteses: a) Clones de batata
infectados por ToCV podem alterar suas características e modificar a atratividade e o
desenvolvimento de B. tabaci biótipo B? b) Há diferenças no comportamento alimentar de B.
tabaci biótipo B em plantas de batata sadias e infectadas por ToCV? c) Há diferenças nos
voláteis entre os clones de batata sadios e infectados por ToCV?
2
2 REVISÃO DE LITERATURA
2.1 A Cultura da Batata
A batata ou batata inglesa (Solanum tuberosum L.) tem seu centro de origem nas
regiões andinas da América do Sul, provavelmente em países como Peru, Bolívia e Chile
(FILGUEIRA, 2003). Por volta de 1570, a batata foi introduzida na Europa por meio de
colonizadores espanhóis e, cerca de 50 anos depois, foi levada da Europa para a América do
Norte, tornando-se um alimento popular. A difusão da cultura da batata para outros
continentes se deu pela colonização desses países pelos europeus (LOPES, 1997). A partir de
1907, têm-se os primeiros relatos de trabalhos científicos com essa cultura.
No Brasil, a área total plantada de batata em 2014 foi de 134.560 mil hectares, com
rendimento de 88 t/ha. A estimativa de área plantada para 2015 é de 129.570 mil hectares,
com rendimento de 87 t/ha, numa produção final esperada de 3.637.59 toneladas. Os estados
responsáveis pelas maiores produções são Minas Gerais, Goiás, São Paulo, Bahia e Rio
Grande do Sul, concentrando mais de 95% da produção do país (IBGE, 2015).
A batata representa um alimento rico em carboidratos (17,6%), contendo ainda
proteínas, minerais e vitaminas (A, B1, B2, C e niacina). De acordo com as características
botânicas, a batata é uma planta perene, mas é cultivada como anual. Segundo LOPES (1997),
uma planta de batata considerada normal apresenta o mesmo número de hastes quantos forem
os de brotos que emergirem da batata-semente, apresenta também folhas compostas, flores,
raízes estolões e tubérculos. De acordo com FILGUEIRA (2003), o sistema radicular da
batata é superficial, com as raízes se concentrando em até 30 cm de profundidade. Os estolões
são ramificações originadas de gemas situadas nas axilas de folhas rudimentares, na parte
subterrânea do caule. Ao final dos estolões se encontram os tubérculos, que são caules
adaptados para reserva de alimentos e reprodução (LOPES, 1997).
Os tubérculos apresentam olhos e lenticelas em sua superfície, sendo que em cada olho
está presente uma gema, de onde se originam brotações; já as lenticelas são os sistemas de
comunicação entre a parte interna do tubérculo e seu exterior, sendo a respiração sua principal
função. As folhas são compostas, com um pecíolo com folíolo terminal e por folíolos laterais
arredondados; características como pilosidade, coloração e tamanho variam de acordo com a
cultivar. As flores da batata são hermafroditas, sendo que o androceu e o gineceu amadurecem
ao mesmo tempo, facilitando assim a predominância da autopolinização, e dando origem a um
3
fruto verde medindo de 2 a 3 cm de diâmetro, com 40 a 240 minúsculas sementes (LOPES,
1997; FILGUEIRA, 2003).
O ciclo vegetativo da cultura pode ser precoce (<90 dias), médio (90-110 dias) ou tardio
(>110 dias), sendo que este período varia entre cultivares (PEREIRA & FORTES, 2004).
Quatro estádios de desenvolvimento da cultura da batata foram descritos por
FILGUEIRA (2003) após realização de ensaio com as cultivares Bintje, que apresenta ciclo
precoce, e Aracy, com ciclo tardio. O estádio I tem duração de uma a duas semanas após o
plantio, fase que abrange desde a batata semente brotada até a emergência das hastes, havendo
pouca exigência de água. O estádio II inicia-se entre a quarta e quinta semana após o plantio,
compreendendo o intervalo entre emergência e a tuberização; nesse estádio aumenta a
exigência de água e inicia-se a adubação, devido ao desenvolvimento radicular. O estádio III
ocorre a partir da oitava semana, quando se atinge o máximo desenvolvimento vegetativo;
nesse estádio há a máxima absorção de nutrientes pelo sistema radicular, podendo ocorrer
formação de flores, o que vai depender das condições agroclimáticas. O estádio IV é mais
longo, durando até a senescência da planta; nele ocorre o incremento em peso dos tubérculos
enquanto a parte aérea se mantiver viva, acontecendo, em sequência, o amarelecimento das
folhas entre a décima segunda e a décima quarta semanas. Durante os estádios III e IV, deve
haver os maiores cuidados fitossanitários, pois nesse período ocorre a maior incidência de
pragas e doenças.
No Brasil o cultivo da batata é realizado em três safras. Na primeira (das águas), o
plantio ocorre entre setembro-novembro com colheita de janeiro em diante. Nessa safra, a
irrigação é dispensável, mas umidade e temperatura elevadas fazem com que a parte
vegetativa seja consideravelmente aumentada, podendo provocar o acamamento da planta e
presença de folíolos menores, retardando a tuberização. Na segunda safra (da seca), o plantio
é realizado de fevereiro a abril com colheita na seca, sendo que no início do plantio a
pluviosidade pode ser suficiente para a demanda. Na terceira (de inverno), com plantio de
maio a julho e colheita em setembro, é necessário o uso de irrigação durante o ciclo, mas a
qualidade do tubérculo é superior e o preço é mais elevado quando comparado com os
produzidos em outras safras (CARVALHO DIAS, 1993).
2.2 A Mosca-Branca Bemisia tabaci (Genn.)
As moscas-brancas pertencem à ordem Hemiptera, subordem Sternorrhyncha e família
Aleyrodidae, e se dividem em duas subfamílias, Aleyrodicinae e Aleyrodinae. Essa família
4
possui cerca de 1500 espécies (INBAR & GERLING, 2008), sendo que a subfamília
Aleyrodicinae, a qual pertence a espécie Bemisia tabaci (Genn.), compreende mais de 90% do
total de moscas-brancas (MARTIN & MOUND, 2007).
2.2.1 Taxonomia de B. tabaci
A primeira descrição de B. tabaci foi feita por Gennadius na Grécia em 1889, com base
em material coletado em planta de fumo, sendo denominada, na ocasião, de Aleurodes tabaci
(BROWN et al., 1995b). É uma espécie cosmopolita, cujo centro de origem supõe-se ser o
Oriente ou o Paquistão, tendo sido introduzida na África, Europa e Américas pelo transporte
de material vegetal (BROWN & BIRD, 1992).
Em 2001, foi proposto que B. tabaci compreendia um complexo de 41 biótipos
(PERRING, 2001). Dentro desse complexo, foi detectado que B. tabaci biótipo B apresenta
taxa de reprodução 30% maior que B. tabaci biótipo A, tem maior gama de plantas
hospedeiras, desenvolve resistência a vários inseticidas, transmite maior número de fitovírus,
induz anomalias como o prateamento da folha em cucurbitáceas e amadurecimento irregular
em tomate, além de maior alimentação nas plantas, produzindo de quatro a cinco vezes mais
secreção açucarada ‘honeydew’ (BROWN et al., 1995b; COSTA & BROWN, 1990).
DE BARRO et al. (2011) apresentaram evidências de que B. tabaci é um complexo de
espécies e não de biótipos, com 11 grupos bem definidos, abrangendo 24 espécies
morfologicamente indistintas. Análises mais rigorosas em termos da amplitude de diversidade
genética com base na porção do gene mitocondrial citocromo oxidase (mtCOI) têm sido
realizadas para poder abranger a lacuna onde estão distribuídas as 24 espécies identificadas,
onde os biótipos B e B2 formariam uma espécie pertencente ao grupo Middle East Asia
Minor (MEAM1) e os biótipos Q, J e L ao grupo Mediterranean (MED).
No Brasil, MARUBAYASHI et al. (2013) verificaram a existência de espécies distintas
de B. tabaci através de análise da sequência do gene mtCOI, sendo elas MEAM1, New World
e New World 2. BARBOSA et al. (2015) encontraram B. tabaci biótipo Q no Rio Grande do
Sul, infestando plantas de pimenta (Capsicum annuum) em cultivo protegido e batata-doce
(Ipomea batatas) em campo aberto.
Apesar da proposta de se considerar B. tabaci um complexo de espécies, neste trabalho
adotar-se-á o táxon B. tabaci biótipo B pela maior familiaridade com essa denominação e para
facilitar a interpretação e a discussão dos resultados.
5
2.2.2 Aspectos biológicos de B. tabaci
B. tabaci apresenta ciclo biológico com metamorfose incompleta, compreendendo a fase
de ovo, quatro estádios ninfais e a fase adulta do inseto. A reprodução normalmente é
sexuada, sendo que de 12 a 48 horas após a emergência do inseto adulto já se inicia o
acasalamento, porém, podendo haver reprodução por partenogênese arrenótoca. Podem
ocorrer de 11 a 15 gerações ao ano, sendo que as condições climáticas influenciam no
desenvolvimento populacional (GILL, 1990; BYRNE & BELLOWS JÚNIOR, 1991).
Segundo GERLING (1990), as fêmeas preferem ovipositar na parte abaxial das folhas
mais jovens das plantas hospedeiras, podendo colocar de 40 a 300 ovos durante a fase adulta.
Durante a oviposição, a fêmea faz a inserção do pedicelo na folha, prendendo-o com uma
secreção adesiva, mantendo o ovo fixo no lugar. O desenvolvimento do ovo é dependente da
absorção da água e nutrientes da folha onde se aloja (BUCKNER et al., 2002). A fase de ovo,
em temperaturas oscilando entre 25 e 27°C, dura em torno de 5 a 8 dias (BETHKE et al.,
1991).
Eclodindo através de uma fenda formada da base do ovo até o ápice, as ninfas de
primeiro ínstar se movimentam pela superfície da folha, selecionam um local, inserem o
estilete por onde se alimentam de nutrientes encontrados no floema, mantendo-se nesse local
até o final de seu desenvolvimento ninfal. SUMMERS et al. (1996) relataram que a ninfa
recém-eclodida pode sobreviver cinco dias sem se alimentar no local escolhido dependendo
da temperatura e umidade ambiente, sob temperaturas entre 12 e 18ºC; já PRICE (1992)
observou sobrevivência de três horas após a eclosão para a maioria das ninfas, em temperatura
de 24 ± 2ºC.
Em seu primeiro ínstar, a ninfa é transparente, pequena e convexa e, no segundo, pode
dobrar de tamanho, se apresentando de forma achatada e transparente. No terceiro ínstar, sua
coloração se altera para fosca e deixa de ser achatada, apresentando uma forma mais globosa.
No último ínstar, pode-se observar o corpo do inseto formado, com coloração amarela, os
olhos vermelhos e as asas brancas dobradas; quando próximo ao momento de emergir, a
coloração se altera para um amarelo mais pronunciado (WALKER et al., 2010; BYRNE &
BELLOWS JÚNIOR, 1991). A metamorfose para a fase adulta, envolvendo grandes
modificações morfológicas, ocorre com a ninfa de quarto ínstar durante a fase de pupa
(GELMAM et al., 2002).
Os adultos apresentam dorso amarelo pálido, asas brancas com venação reduzida e
levemente separadas quando em repouso, pernas delgadas e olhos vermelhos, compostos e
6
divididos em duas partes por uma projeção cuticular. A fêmea é maior que o macho, com 1 a
2 mm de comprimento e 0,36 a 0,51 mm de largura, o corpo do adulto é coberto por uma
cerosidade branca secretada por glândulas do inseto (LÓPEZ, 1995; SOUZA &
VENDRAMIM, 2000).
2.2.3 Interações mosca-branca e planta hospedeira
O biótipo B dessa mosca foi introduzido no Brasil no início da década de 1990
(LOURENÇÃO & NAGAI, 1994). No estado de São Paulo, esse biótipo teve sua presença
observada em 1992 na região de Paulínia, nas culturas de abóbora, brócolis e berinjela e em
Ibiúna, em culturas de tomate nesse mesmo ano; em Ribeirão Preto, nas culturas de brócolis,
berinjela e jiló em 1994, e em Araçatuba e Presidente Prudente, nas culturas de tomateiro, em
plantas ornamentais e plantas da vegetação espontânea em 1995 (LOURENÇÃO, 1997).
A facilidade de adaptação a muitas plantas hospedeiras permite a ocorrência de B.
tabaci em diversas culturas e plantas invasoras (COSTA & BROWN, 1990; BROWN et al.,
1995b). Em regiões tropicais e subtropicais apresenta mais de 300 espécies de plantas
hospedeiras, cultivadas e não cultivadas. A maioria encontra-se nas famílias Compositae,
Euphorbiaceae, Fabaceae, Malvaceae e Solanaceae (MICHEREFF-FILHO et al., 2012;
SOTTORIVA et al., 2014).
A seleção da planta hospedeira tem sido descrita como uma sequência ou um processo
em cadeia que implica em etapas sucessivas que finalmente terminam na alimentação e/ou na
oviposição do inseto sobre a planta (LARA, 1991).
Segundo CHAPMAN et al. (1981) e LA POINTE & TINGEY (1984), a detecção de
substâncias químicas que se segue ao pouso do inseto na planta é o processo mais importante
na escolha do hospedeiro. A atração da mosca-branca pela planta ocorre inicialmente pela cor
e depois pelo odor da planta hospedeira (voláteis, semioquímicos, etc), e finalmente a
aceitação do hospedeiro após a picada de prova. Se o hospedeiro for adequado, a moscabranca permanecerá nele e, posteriormente, ocorrerão a alimentação e a oviposição
(BERLINGER, 1986).
A densidade de tricomas, a variação nutricional, diferenças entre cultivares, o
comportamento do adulto, a idade e espécie de mosca-branca, além de mudanças nas
condições ambientais, tornam a interação entre o inseto e a planta hospedeira muito complexa
(CHU et al., 2000ab; RODRIGUÉZ-LÓPEZ et al., 2011). A espessura da folha, o número de
feixes vasculares e a menor distância da superfície abaxial da folha ao feixe vascular também
7
interferem no comportamento de alimentação e de oviposição de adultos de B. tabaci biótipo
B (CHU et al., 1995; COHEN et al., 1996).
A mosca-branca responde negativamente à falta de nutrientes, reação confirmada pelo
fato de que a deficiência de fósforo em plantas de algodão foi responsável por redução de
40% na oviposição de B. tabaci biótipo B (SKINNER & COHEN, 1994).
Segundo WALKER & PERRING (1994), a oviposição da mosca-branca é determinada
na fase da penetração na cutícula, onde o inseto verifica a constituição química, idade e
qualidade da folha. Estudos da interação da mosca-branca com plantas hospedeiras são
importantes para avaliar o potencial de adaptação desta praga a diferentes espécies vegetais
(VILLAS BÔAS et al., 2002).
Durante a alimentação na planta hospedeira, caso essa esteja infectada por fitovírus,
pode ocorrer a aquisição do vírus pela mosca-branca, sendo mediada pela perfuração e sucção
realizada pelo aparelho bucal da mosca-branca adulta, denominado estilete, que penetra
através de espaços intercelulares até estabelecer locais de alimentação nos elementos crivados
do floema (FORBES, 1969). A transmissão do vírus ocorre quando o adulto abandona essa
planta e se alimenta em uma planta sadia.
A técnica de monitoramento eletrônico de atividade estiletar de insetos, denominada
“Electrical Penetration Graph” (EPG), é utilizada no estudo das interações entre os insetospraga, suas peças bucais e outros organismos. Esse método se converteu em uma das
ferramentas mais utilizadas no estudo do comportamento alimentar de insetos sugadores,
registrando fases distintas da atividade de penetração e alimentação (MC LEAN & KINSEY,
1964; GÁRZO, 2002). Essa técnica é empregada em várias frentes de pesquisa, tais como
avaliação da preferência alimentar de insetos por diferentes espécies de plantas, estudos com
metabólitos secundários, ação de inseticidas e transmissão de fitovírus (HOLBROOK, 1977;
RAMAN et al., 1979; LEONARD & HOLBROOK, 1978; LA POINTE & TINGEY, 1984;
FERERES et al., 1993, 2007; MARTÍN et al., 1997, BASS et al., 2014).
Diversos trabalhos foram realizados para determinar o comportamento da penetração
estiletar que resultam na inoculação de vírus pelos insetos vetores. MORENODELAFUENTE et al. (2013), realizando um estudo com B. tabaci biótipo Q e TYLCV,
demonstraram que ocorre uma alteração no comportamento alimentar de fêmeas do inseto
vetor quando adquirem o vírus, as quais passam menos tempo nos tecidos intercelulares e um
maior tempo nos tecidos floemáticos, aumentando o número de eventos de salivação e
ingestão.
8
2.2.4 Danos causados pela mosca-branca
No Brasil, B. tabaci é conhecida desde 1923 (BONDAR, 1928), ocorrendo em várias
culturas e plantas invasoras, no entanto em baixas infestações até a década de 60. Surtos
populacionais dessa mosca-branca foram verificados em algodoeiro em 1968 e em soja,
algodoeiro e feijoeiro na safra 1972/73 no norte do Paraná e na região sul de São Paulo
(COSTA et al., 1973).
O status de praga de B. tabaci tem aumentado consideravelmente nos últimos 20 anos,
devido às constantes invasões pelo biótipo B (DE BARRO et al., 2011; LIU et al., 2012) e
vem sendo responsável por perdas de bilhões de dólares anualmente (OLIVEIRA et al.,
2013). Dessa forma, há necessidade de atenção por parte da comunidade científica, visando
buscar alternativas de controle para o inseto, já que isso se torna difícil devido as suas
características biológicas, como ampla gama de hospedeiros, elevado potencial reprodutivo,
tamanho reduzido, capacidade de desenvolver resistência aos inseticidas e grande capacidade
de dispersão (JONES, 2003; BERRY et al., 2004; OLIVEIRA et al., 2013).
A ocorrência de B. tabaci na cultura da batata é conhecida há vários anos, mas suas
populações sempre foram pequenas, não causando graves danos às plantas (MOUND &
HALSEY, 1978; GALLO et al., 2002). No entanto, altas infestações do biótipo B de B. tabaci
em lavouras de batata têm sido constatadas a partir de 2001 (LOURENÇÃO et al., 2003).
B. tabaci biótipo B destaca-se como um dos mais destrutivos insetos-praga de culturas
protegidas ou plantações em campo (XU et al., 2011; PAN et al., 2012). Em ataques severos,
os danos causados pela mosca-branca podem ser divididos em diretos e indiretos. Os danos
diretos referem-se à alimentação de ninfas e adultos, causando definhamento das plantas,
além da injeção de toxinas que podem causar alterações bioquímicas e anatômicas, induzindo
desordens fisiológicas (INBAR & GERLING, 2008). Essas desordens incluem anomalias
como o amadurecimento irregular dos frutos em tomateiro e o prateamento das folhas em
aboboreiras (NAVAS-CASTILLO et al., 2011).
Os danos indiretos são devidos à formação de fumagina, fungo de coloração escura
(Capnodium sp.) que se desenvolve sobre o “honeydew” excretado pela mosca-branca e
interfere na fotossíntese e transpiração da planta hospedeira (HOFFMANN-CAMPO et al.,
2000; GALLO et al., 2002; CAMERON et al., 2013), além da transmissão de fitovírus.
Durante a alimentação a mosca-branca pode adquirir vírus presente na planta e, em seguida,
mover-se e se alimentar em outra planta sadia, inoculando o vírus adquirido (JONES, 2003;
NAVAS-CASTILLO et al., 2011).
9
2.3 Transmissão de Fitovírus por Mosca-branca
Dentre as mosca-brancas mais importantes como pragas, somente três, B. tabaci,
Trialeurodes vaporariorum e Trialeurodes abutilonea são conhecidas como vetoras de vírus,
destacando-se B. tabaci, que transmite mais de 150 espécies de vírus, das famílias
Geminiviridade (gênero Begomovirus), Closteroviridae (gênero Crinivrus) e Potiviridae
(gênero Ipomovirus) (NAVAS-CASTILLO et al., 2011; POLSTON et al., 2014).
ORLANDO & SILBERSCHMIDT (1945) confirmaram que a ocorrência de mosaico
em algodoeiro e de mosaico-amarelo/dourado em espécies de guanxuma (Sida spp.) foram
transmitidos pela mosca-branca B. tabaci.
Em solanáceas, COSTA & RUSSEL (1975)
realizaram no Brasil o primeiro relato de doença causada por geminivírus em tomateiro,
associando sua transmissão à mosca-branca. Nessa cultura, um dos fatores limitantes para a
produção se deve à transmissão, por B. tabaci, do vírus do encarquilhamento amarelo da folha
de tomateiro, um geminivírus, (Tomato yellow leaf curl virus - TYLCV), em diferentes
regiões geográficas do mundo (ZEIDAN et al., 1998). Esse vírus ainda não foi detectado no
Brasil, constituindo-se em praga quarentenária A1.
No Brasil, no início da década de 2000, a ocorrência mais frequente de geminivírus em
solanáceas transmitido por B. tabaci biótipo B foi de Tomato yellow vein streak virus
(TYVSV), causador do mosaico deformante nas folhas de tomateiro induzindo, entre outros
sintomas, o amarelecimento das nervuras e o enrolamento das folhas apicais. Em áreas de
produção de batata, observou-se transmissão de TYVSV de tomateiros infectados para plantas
de batata, causando o mosaico deformante da batata (SOUZA-DIAS,1996; SOUZA-DIAS &
IAMAOTI, 2005).
Posteriormente, outro geminivírus, Tomato severe rugose virus (ToSRV) tornou-se a
espécie predominante em várias regiões, como no estado de São Paulo e no Distrito Federal,
em tomateiro e batata, enquanto que a espécie Tomato chlorotic mottle virus (ToCMoV)
passou a ocorrer predominantemente no Nordeste (FERNANDES et al., 2008).
BARBOSA et al. (2011) descreveram, além da infecção de begomovírus em tomateiro,
a emergência de Tomato chlorosis virus (ToCV), vírus pertencente ao gênero Crinivírus,
transmitido por B. tabaci biótipo B e por T. vaporariorum, nos estados de São Paulo, Bahia,
Espírito Santo, Goiás, Minas Gerais e Rio de Janeiro. Em batata proveniente de produção no
estado de Goiás também foi relatada a presença de ToCV (FREITAS et al., 2011).
Tomato chlorosis virus (ToCV) é uma espécie do gênero
Crinivírus, família
Closteroviridae. Encontra-se limitado ao floema, com transmissão do tipo semi-persistente,
10
tendo como vetores moscas-brancas (Hemiptera: Aleyrodidae) de três espécies: B. tabaci, T.
vaporariorum e T. abutilonea (WISLER et al., 1998).
A transmissão de ToCV por T.
vaporariorum tem se mostrado menos eficiente em comparação à de B. tabaci biótipo B e de
T. abutilonea (WINTERMANTEL & WISLER., 2006).
O gênero Crinivírus apresenta partículas alongadas e flexuosas, com comprimentos que
variam de 650-850 nm, de RNA de fita simples, senso positivo e genoma bipartido
(MARTELLI et al., 2012). O RNA1 codifica duas proteínas responsáveis por funções de
replicação viral, onde inclui o domínio de uma protease tipo papaína, outra metiltransferase e
uma helicase, estas presentes na primeira ORF, e uma proteína RdRP expressa por um frame
shift ribossomal, este no final da primeira ORF. O RNA2 apresenta sete ORFs, onde algumas
das proteínas traduzidas atuam no movimento célula a célula, na transmissão por vetor ou
possuem um domínio de transmembrana (WINTERMANTEL et al., 2005; FAUQUET el al.,
2005).
Tomato chlorosis virus foi isolado em plantas de tomate e descrito pela primeira vez nos
Estados Unidos (WISLER et al., 1998). Posteriormente foi detectado em plantações de
tomate em Portugal (LOURO et al., 2000). Na Espanha, sintomas de amarelecimento em
tomate devido a ToCV foram observados na província de Málaga em 1997 (NAVASCASTILLO et al., 2000), sendo o vírus também
detectado em Porto Rico
(WINTERMANTEL et al., 2001), Itália (ACCOTTO et al., 2001), Grécia (DOVAS et al.,
2002), Taiwan (TSAI et al., 2004), Israel (SEVEG et al., 2004), México (ALVAREZ-RUIZ et
al., 2007), Cuba (MARTÍNEZ ZUBIAUR et al., 2008), Brasil (BARBOSA et al., 2008),
Costa Rica (CASTRO et al., 2009) e Hungria (BESE et al., 2011). Também foi relatado em
batata proveniente de Goiás, com transmissão por B. tabaci biótipo B (FREITAS et al., 2011).
LOZANO et al. (2004) fizeram o primeiro relato de ToCV infectando plantas de
pimentão em casa de vegetação infestada com B. tabaci na província de Almería, Espanha.
FORTES et al. (2012) investigaram a prevalência de ToCV em tomate e pimenta na Espanha
(províncias de Múrcia, Almería e Málaga) e a transmissão do vírus por B. tabaci; relataram
ainda a ocorrência de grande redução no rendimento de plantas de pimenta infectadas com
ToCV em condições experimentais.
Segundo BARBOSA et al. (2008), a presença de ToCV no Brasil foi observada no
período de 2006 a 2007 em plantações de tomate no município de Sumaré, SP. A seguir, foi
detectado em mais cinco estados brasileiros no período de 2007 a 2010: Bahia, Rio de Janeiro,
Minas Gerais, Espírito Santo e Goiás. O relato da presença do vírus nessas regiões do Brasil é
um forte indicativo de que esse agente pode estar amplamente disseminado no país, mas não
11
está sendo relatado devido aos sintomas em tomateiro serem muito semelhantes ao sintoma de
deficiência nutricional ocasionada pela ausência de magnésio (BARBOSA et al., 2011).
Além do tomateiro, o vírus apresenta uma gama de hospedeiras naturais e
experimentais que compreende 30 espécies de 13 famílias diferentes (FONT et al., 2004;
TSAI et al., 2004; MORRIS et al., 2006; WINTERMANTEL & WISLER, 2006;
SOLORZANO-MORALES et al., 2011; FONSECA et al., 2013).
Em plantas de batata, há somente duas notificações com constatação da infecção por
ToCV, sendo a primeira feita por FORTES & NAVAS-CASTILLO (2008) na Espanha e a
segunda por FREITAS et al. (2012), no Brasil, em duas plantas de batata cultivar ‘Ágata’.
FORTES et al. (2012) demonstraram que, em condições experimentais, B. tabaci biótipo Q é
vetor de ToCV em plantas de batata, sendo o vírus transmitido através dos tubérculos,
permanecendo as plantas de batata como fontes de vírus para transmissão para outras plantas.
Os principais sintomas ocasionados pela infecção de ToCV em tomateiro é a clorose
internerval das folhas inferiores, evoluindo para os ponteiros, com as folhas desenvolvendo
pontos avermelhados e necróticos e podendo ocorrer seu enrolamento (WISLER et al.,
1998). A transmissão de ToCV por B. tabaci biótipo B para solanáceas ainda não esta tão
clara e bem compreendida como a transmissão de begomovírus.
Em alguns estudos são relatadas diferenças entre biótipos de mosca-branca na
transmissão de vírus, contudo, outros trabalhos relatam não haver diferença, como o de
BERDIALES et al. (1999), em cujo estudo não foi encontrada diferença na transmissão do
Cucumber yellow stunting disorder virus (CYSDV) para pepino entre os biótipos B e Q de B.
tabaci. Já segundo COHEN et al. (1992), houve diferença na transmissão do Lettuce
infectious yellow virus (LIYV) entre os biótipos A e B, sendo o último com a melhor taxa de
transmissão.
2.4 Compostos Voláteis de Plantas e Comportamento de Insetos
Os estudos com metabólitos secundários foram iniciados por especialistas em química
orgânica do século XIX e início do século XX, visando à sua utilização para medicamentos,
venenos e compostos industriais. Em seguida, foi sugerido que esses metabólitos têm funções
importantes para os próprios vegetais, como proteção da planta contra a herbivoria e ação de
microorganismos patogênicos, além de servirem como atrativos para animais polinizadores e
dispersores de sementes, e agentes na competição planta-planta (TAIZ & ZEIGER, 2004).
12
Os metabólitos vegetais são divididos em três grupos químicos: terpenos, compostos
fenólicos e compostos nitrogenados. Os terpenos muitas vezes são tóxicos e deterrentes para
muitos insetos e mamíferos herbívoros; sendo assim, parecem exercer uma importante função
de defesa no reino vegetal (GERSHENZON & CROTEAU, 1992).
As plantas respondem à ação de insetos herbívoros sintetizando e emitindo compostos
voláteis com capacidade para alterar o comportamento de insetos. Os voláteis produzidos
pelas plantas podem ser percebidos tanto por inimigos naturais dos herbívoros, como um sinal
de alerta, mas também por outros herbívoros, afetando o comportamento destes conforme a
peculiaridade da espécie e as condições ambientais (TURLINGS et al., 1990).
Pesquisas revelam que os terpenos voláteis têm função protetora. Assim, em milho,
algodão, fumo e outros, certos monoterpenos e sesquiterpenos são produzidos e liberados pela
planta somente após o ataque de um herbívoro, repelindo herbívoros ovipositores e atraindo
os inimigos naturais destes insetos (TURLINGS et al., 1995; KESSLER & BALDWIN,
2001).
Os flavonoides são substâncias químicas fenólicas que ocorrem amplamente nas plantas
(HARBONE, 1994), desempenhando as mais variadas funções, tais como proteção à radiação
ultravioleta, a insetos, à doenças causadas por fungos, bactérias e vírus; atraentes para
polinização (pétalas coloridas); dispersantes de sementes (frutas vermelhas); controladores de
hormônios; estimulantes à produção de nódulos pelos rizóbios; inibidores enzimáticos,
antioxidantes e agentes alelopáticos (MARKHAM, 1982).
Dentro dos compostos fenólicos, os taninos são os que mais se destacam na defesa das
plantas contra herbívoros, pois são toxinas que reduzem significativamente o crescimento e
sobrevivência de muitos herbívoros, quando adicionados à dieta do inseto (TAIZ & ZEIGER,
2004).
Os alcaloides são compostos nitrogenados e também apresentam grande importância na
relação de defesa dos vegetais. Os alcaloides são tóxicos aos herbívoros e aumentam em
resposta ao dano inicial provocado pela herbivoria, fortalecendo a planta contra um ataque
subsequente (KARBAN & BALDWIN, 1997). Além dos alcaloides, os glicosídeos
cianogênicos e glucosinolatos não são tóxicos, mas decompõem-se e produzem venenos
voláteis quando a planta sofre herbivoria; os glicosídeos cianogênicos liberam o ácido
cianídrico (HCN) que inibe a alimentação dos insetos (TAIZ & ZEIGER, 2004).
A resposta das plantas a herbivoria reduz o desempenho ou a preferência de herbívoros
e essa resposta pode causar uma resistência cruzada para um ou mais ataques subsequentes
(KARBAN & BALDWIN, 1997).
13
3 MATERIAL E MÉTODOS
3.1 Locais de Realização do Estudo
Os ensaios foram realizados em três locais distintos. Em Campinas, no Centro
Experimental Central (CEC), do Instituto Agronômico (IAC), realizaram-se os ensaios de
atratividade e preferência para oviposição do vetor, desenvolvimento ovo-adulto e
movimentação entre os tratamentos dos adultos de B. tabaci biótipo B. Em Piracicaba, no
laboratório de Comportamento de Inseto e Ecologia Química, da ESALQ, realizou-se a
extração dos voláteis dos clones de batata. Em Madri, Espanha, no Instituto de Ciencias
Agricolas (ICA), do Consejo Superior de Investigaciones Cientificas (CSIC), realizaram-se os
ensaios de resposta do inseto vetor a emissão dos voláteis na preferência para pouso e ensaio
do comportamento alimentar do inseto vetor. O período de realização dos ensaios foi de 2013
a 2015.
3.2 Clones de Batata Utilizados
Os clones de batata foram oriundos do banco de germoplasma da Associação dos
Bataticultores de Vargem Grande do Sul, disponibilizados pelo engenheiro agrônomo Pedro
Hayashi.
‘Ágata’ – clone holandês originário do cruzamento entre ‘Bohm’ X ‘Sirco’. Apresenta
maturação precoce a muito precoce, rendimento alto, e baixo teor de matéria seca. As plantas
têm hastes finas, e cor verde muito pronunciada. A folhagem apresenta bom desenvolvimento
e folhas grandes, de aspecto fechado e de cor verde clara. Apresenta pouca inflorescência e as
flores são de cor branca. O tubérculo tem epiderme de coloração amarela predominantemente
lisa e olhos superficiais, polpa cor amarelo-claro. A definição do número de tubérculos ocorre
em torno de 15 dias, sendo considerada uma característica marcante de ‘Ágata’, com
produção de tubérculos uniformes em tamanho. O broto tem formas cilíndricas largas, de cor
violeta avermelhado e escassamente piloso. É o clone de mais rápido incremento de plantio na
bataticultura brasileira, sendo atualmente a mais plantada em todo país.
Bach-4 - híbrido resultante do cruzamento entre ‘Bannock Russet’ e a espécie Solanum
chacoense sbsp muelleri (Hawkes & Hjerting). Clone usado como base genética, sendo
conhecido seu comportamento somente em ambiente protegido. Planta muito vigorosa, haste
fortemente pigmentada, florescimento abundante, flores brancas. Possui forte tendência para o
14
crescimento indeterminado. Tubérculos graúdos, redondos, olhos profundos de cor roxa e
polpa amarelo claro. De acordo com ROCHA et al. (2012), é um clone com resistência
moderada a B. tabaci biótipo B.
3.3 Produção, Manutenção e Infecção dos Clones de Batata
3.3.1 No Brasil
Os tubérculos dos clones ‘Ágata’ e Bach-4 foram cultivados em vasos plásticos com 20
cm de diâmetro superior e 15 cm de altura, com capacidade para três litros e preenchidos com
mistura de terra e composto orgânico, adubados com fertilizantes, três vezes por semana. As
plantas foram mantidas em condições ambientais, em casa de vegetação protegidas com tela
antiafídeo para evitar infestação por outros insetos. As plantas de batata foram utilizadas com
15 a 20 dias após o plantio do tubérculo germinado.
Para a obtenção de plantas infectadas por ToCV foi realizada a inoculação com adultos
virulíferos de B. tabaci biótipo B. Cinquenta insetos adultos de B. tabaci foram confinados
por meio de clip-cage em plantas de tomate utilizadas como fonte de ToCV por um período
de acesso à aquisição (PAA) de 24 horas. Em seguida cortou-se a folha do tomateiro contendo
o clip-cage, mantendo-a em gelo por cinco minutos para reduzir a atividade do inseto e
facilitar o manuseio. Em seguida, o clip-cage foi acoplado em uma folha na planta de batata.
Nesta, os insetos tiveram um período de acesso a inoculação (PAI) de sete dias. Após esse
período, a folha contendo o clip-cage com os insetos foi eliminada. A confirmação da
infecção foi realizada por meio de RT-PCR após 25 a 30 dias da inoculação.
As plantas sadias passaram pelo mesmo processo de alimentação de insetos
acondicionados em clip-cage, utilizando-se 50 insetos previamente alimentados em tomateiro
sadio. Esse procedimento foi realizado para que todas as plantas utilizadas nos ensaios
passassem pelo mesmo processo de herbivoria, evitando assim qualquer condicionamento de
comportamento do inseto.
3.3.2 Na Espanha
Os tubérculos do clone ‘Ágata’ foram semeados em vasos com os mesmos padrões
daqueles utilizados no Brasil. Cada vaso foi preenchido com uma mistura de 3x1 de substrato
e vermiculita, adubados com fertilizante de fórmula 20-20-20 na proporção de 1 g/L, três
15
vezes por semana. As plantas foram mantidas por 15 dias em câmara climatizada com
fotoperíodo de 12 horas e temperatura de 24°C. A inoculação das plantas com ToCV por B.
tabaci foi realizada da maneira descrita para os ensaios conduzidos no Brasil. A confirmação
da infecção viral foi realizada através da extração total de RNA seguida de RT-PCR em
tempo real.
3.4 Manutenção da Colônia de B. tabaci biótipo B
3.4.1 No Brasil
Os insetos utilizados nos experimentos foram obtidos a partir de uma população de B.
tabaci biótipo B criada em plantas de couve-de-folhas (Brassica oleracea var. acephala),
mantida no Centro de Fitossanidade do IAC. Essa criação foi mantida em casa de vegetação
com dimensões de 3 x 5 m, constituída por base de alvenaria de 1 m de altura, laterais de tela
antiafídeo e teto de vidro, com bancadas de cimento, onde se acomodam os vasos contendo as
plantas de couve. Semanalmente as plantas em senescência eram trocadas por plantas novas a
fim de prover condições adequadas para o desenvolvimento do inseto. Essa população de B.
tabaci vem sendo periodicamente caracterizada molecularmente como pertencente ao biótipo
B (FONTES et al., 2010, 2012; VALLE et al., 2013).
3.4.2 Na Espanha
Os insetos adultos de B. tabaci biótipo B, de criação já existente e caracterizada
molecularmente, foram mantidos em plantas de berinjela (Solanum melongena) em gaiolas de
voil, em condições controladas de casa de vegetação (25±3°C). Foi mantida uma criação
estoque onde, quinzenalmente, as plantas de berinjela eram trocadas. Para a obtenção de
insetos com idades definidas, uma planta de berinjela foi colocada na gaiola de criação
estoque, por uma semana. Após esse período, os adultos foram retirados para que ficassem
somente os ovos na planta. Em seguida a planta foi acondicionada em uma nova gaiola,
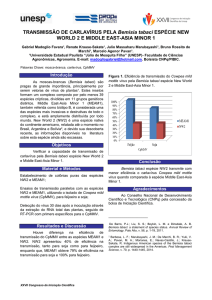
acompanhando-se diariamente o desenvolvimento do inseto até a idade adulta (Figura 1).
16
a
b
Figura 1. a) Criação de Bemisia tabaci biótipo B com idade definida em plantas de berinjela.
b) Criação estoque de Bemisia tabaci biótipo B em plantas de berinjela
3.5 Manutenção do Inóculo de ToCV
3.5.1 No Brasil
O isolado de ToCV foi obtido de tomateiro infectado oriundo do Departamento de
Fitopatologia e Nematologia da ESALQ, USP. A planta exibia sintomas típicos de infecção
por esse crinivírus, caracterizados como clorose internerval das folhas inferiores com
evolução para os ponteiros, pontos avermelhados e necróticos e enrolamento das folhas
(WISLER et al., 1998). A identificação do crinivírus como sendo ToCV foi comprovada por
RT-PCR e por análises de sintomas. Esse isolado de ToCV foi mantido através de
transmissão, por adultos de B. tabaci biótipo B para plantas de tomateiro e plantas de
batateira, em condições de casa de vegetação, no Centro de Fitossanidade, IAC.
Aproximadamente 300 adultos foram confinados na planta-fonte e mantidos em gaiola de
arame envolta por tecido voil por um PAA de 48 horas. Após o esse período, a gaiola foi
retirada e os insetos migraram para outras plantas de tomate e batata cultivadas na casa de
vegetação (Figura 2).
17
b
a
Figura 2. a) Planta de tomate infectada por Tomato chlorosis virus e infestada por
Bemisia tabaci biótipo B, coberta por tecido voil. b) Planta de tomate fonte de ToCV.
3.5.2 Na Espanha
O isolado viral de ToCV utilizado como fonte para a infecção foi oriundo do Instituto
de Hortofruticultura Subtropical y Mediterránea "La Mayora" do CSIC. A identificação do
crinivírus como sendo ToCV foi comprovada por RT- PCR em tempo real e por análises de
sintomas. A manutenção do isolado foi realizada em plantas de tomate. A inoculação do
tomateiro foi feita confinando-se 30 insetos em planta infectada por meio de clip-cage, por
um PAA de 48 horas. Em seguida, os insetos foram transferidos no clip-cage, para planta
sadia por um PAI de sete dias (Figura 3).
a
b
Figura 3. a) Planta de tomate infectada por Tomato chlorosis virus com clipcage acoplado para o período de acesso a inoculação por Bemisia tabaci
biótipo B. b) Planta de tomate utilizada como fonte de ToCV isolada em gaiola .
18
3.6 Detecção de Tomato chlorosis virus
3.6.1 No Brasil - extração de RNA total para detecção de ToCV
Para a confirmação da infecção por ToCV nas plantas de batata utilizadas nos ensaios
realizados no Brasil, realizou-se a extração total do RNA. Foi utilizado o protocolo do
fabricante do Trizol® LS (Invitrogem®). Discos foliares de 50 a 100 mg foram
acondicionados em tubos de microcentrífuga de 1,5 mL e macerados na presença de
nitrogênio líquido com o auxílio de pistilos plásticos. Em seguida adicionou-se 1 mL de
Trizol® agitando-se vigorosamente os tubos em vortex e incubados por cinco minutos em
temperatura ambiente. Após esse período, acrescentou-se 0,2 mL de clorofórmio em cada
tubo seguido de uma agitação manual por 15 segundos e incubação sob temperatura ambiente
por cinco minutos.
A suspensão foi centrifugada a 12000 g por 15 minutos, a 4°C. O sobrenadante foi
transferido para novo tubo com o auxílio de uma pipeta volumétrica e adicionaram-se 500 μL
de isopropanol seguindo agitação lenta e incubação em temperatura ambiente por dez
minutos. Em seguida os tubos foram centrifugados a 12000 g por dez minutos a 4°C para a
precipitação do RNA.
Descartou-se o sobrenadante e ao precipitado, foi adicionado 1 mL de etanol 75%,
seguindo-se centrifugação a 7500 g por cinco minutos a 4°C. O etanol foi descartado com
cuidado para evitar a eliminação do precipitado. Os tubos foram mantidos em temperatura
ambiente para a evaporação do etanol. Em seguida o precipitado foi ressuspendido em 30 μL
de água livre de RNAse ou água ‘DEPC’ para dissolver o RNA. Como controle positivo foi
utilizado RNA total extraído de tomateiros comprovadamente infectados e, como controle
negativo, foram utilizadas amostras de tomateiros sadios.
3.6.2 Nested RT-PCR
Para a detecção de ToCV realizou-se o Nested RT-PCR através do RNA total extraído
das amostras conforme item 3.6.1. Para realizar a síntese da primeira fita de cDNA (RT=
Reverse Transcription), 3 μL de RNA total foram misturados a 7 μL de água ‘Milli-Q’ tratada
com DEPC, 1 μL de desoxinucleosídeos trifosfatados (dNTP’s – 10 mM), 1 μL do
oligonucleotídeo
iniciador
específico
(antisenso)
HS-12
(5’-
19
CC(G/T)CCACCAAA(A/G)TCGTA-3') a 20 mM (DOVAS et al., 2002) em tubos do tipo
eppendorf® de 0,5 mL.
A mistura foi levada para o termociclador, onde incubou-se a 65°C por cinco minutos
e a 2°C por dois minutos. Em seguida, adicionaram-se 5 μL de Buffer First, 2 μL de DTT 0,1
M e 1 μL da enzima transcriptase reversa ‘Super Script 3rt’. A mistura foi incubada a 50°C
por 50 minutos e a 70°C por 15 minutos, sendo depois mantida a 4°C até a sua retirada do
termociclador. Para a primeira PCR, utilizaram-se 17,2 μL de água Milli-Q, 2,5 μL de tampão
10X da enzima Taq DNA polimerase, 0,5 μL de dNTP’s 10 mM, 3 μL de cDNA extraído, 0,8
μL
do
oligonucleotídeo
iniciador
específico
(senso)
HS-11
11
(5’-
GG(G/T)TT(A/G)GA(G/T)TT(C/T)GGTACTAC-3’), 0,8 μL do oligonucleotídeo iniciador
específico (antisenso) HS-12 (5’-CC(G/T)CCACCAAA(A/G)TCGTA-3') ambos a 20 mM
(DOVAS et al., 2002), 0,3 de enzima Taq DNA polimerase. Essa solução foi aquecida a 94°C
por três minutos e depois submetida a 35 ciclos de 94°C por 30 segundos, 49°C por 40
segundos, 72°C por 50 segundos e temperatura final de 72°C por dez minutos.
A segunda PCR foi realizada da mesma maneira, com a mesma quantidade de
reagentes, mudando os oligonucleotídeos que foram utilizados, sendo iniciadores específicos
ToC-5 (senso) (5’GGTTTGGATTTTGGTACTACATTCAGT-3’)
a 20 mM e ToC-6
(antisenso) (5’AAACTGCCTGCATGAAAAGTCTC - 3’) a 20 mM (DOVAS et al., 2002) na
proporção de 0,8 μL e 3,0 μL do produto da primeira reação de PCR.
O regime do
termociclador foi de um ciclo de 95°C por um minuto, 40 ciclos de 95°C por 20 segundos,
60°C por 15 segundos, 72°C por dez segundos, seguido de um ciclo de 72°C por dois
minutos, e temperatura final de 4°C.
O DNA foi corado com brometo de etídio e separado por eletroforese em gel de
agarose a 1% por cerca de 70 minutos. Os fragmentos de DNA amplificados (463 pb) foram
visualizados após a eletroforese em transiluminados de luz UV e as imagens foram
registradas.
3.6.3 Na Espanha - extração de RNA total e RT-PCR em tempo real (TaqMan)
Para confirmação da infecção por ToCV nas plantas de ‘Ágata’ foi realizada a extração
total de RNA de 0,2 g de folhas de cada amostra, de acordo com as instruções do Kit RT-PCR
AgPath –ID One-Step, sendo estocado em freezer a -80°C para futuras análises. Para a RTPCR
em
tempo
real
(TaqMan®),
(TCTCGAACCTGCTTATGAAAAGAAA),
os
primers
utilizados
foram
ToCVF
ToCVR
20
(ATGCAAGTTGGTTAACGTTGTACAGT)
e
ToCVTAQ
({FAM}-
TTTGTGCAAGGGTAACGAGGGCAAGG-{BHQ1}), para amplificar um fragmento de 80
pb do gene da capa proteica do ToCV, acesso no GenBank no. EU284744. Todos os primers
foram sintetizados pela MWG-Biotech (Ebersberg, Germany).
A reação da TaqMan® foi otimizada para um volume final de 25 μL usando a
SuperScriptTM III Platinum® One-Step qRT-PCR Kit (Invitrogen,Carlsbad, USA), contendo
0.3 μL de cada primer, 0.1 μL de TaqMan® e 2 μL de RNA total extraído. Com ciclos de 30
minutos à 50°C e três minutos a 94°C seguidos de 40 ciclos de dez segundos a 94°C e 30
segundos à 60°C. O teste foi desenvolvido e avaliado no CFX96 Real-time PCR Detection
System, usando placas de PCR de 96 cavidades (Bio-Rad Laboratories, Hercules, USA).
3.7 Efeito de Clones de Batata Infectados por ToCV sobre Parâmetros Biológicos de
Bemisia tabaci Biótipo B
3.7.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados
O experimento foi realizado em casa de vegetação do CEC-IAC, avaliando-se clones de
‘Ágata’ e Bach-4 com e sem infecção por ToCV. Utilizaram-se plantas com 40 DAP tratadas
conforme descrito no item 3.3.1. Foram utilizados quatro tratamentos (‘Ágata’ e Bach-4
sadios e ‘Ágata’ e Bach-4 infectados) e 15 repetições em blocos casualizados e cada parcela
foi representada por um vaso com uma planta.
Para promover a infestação, uma planta de soja altamente infestada por adultos de B.
tabaci biótipo B (em média 600 insetos), foi colocada no centro de cada bloco, em sistema de
arena, equidistante dos vasos de batata. A atratividade foi avaliada após 30 min, 2 h, 4 h, 6 h,
12 h, 24 h, 48 h e 72 h da liberação das moscas-brancas, contando-se os adultos presentes na
superfície abaxial das duas folhas superiores completamente desenvolvidas, com o auxílio de
um espelho, a fim de evitar contato com a folha e não perturbar os insetos.
Após a contagem foi realizada a análise estatística dos dados utilizando o cálculo de
GLM com medidas repetidas, comparadas por Bonferroni a 5% na interação tratamento versus
tempo, no software SPSS v. 20.
21
3.7.2 Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e
infectadas
O ensaio foi conduzido no laboratório do ICA/CSIC, com temperatura e iluminação
controladas em câmara de crescimento (25°C, fotoperíodo de 16:8 h de luz:escuro e 65% de
HR). Avaliou-se a preferência de adultos de B. tabaci biótipo B, com idade entre cinco e sete
dias, em folhas de batata ‘Ágata’ sadias e infectadas por ToCV. Realizaram-se doze
repetições, sendo cada uma representada por uma caixa acrílica contendo três folíolos
oriundos de plantas sadias e outros três de plantas infectadas. Os folíolos foram acoplados
separadamente, em recipiente plástico (2 cm de diâmetro x 1 cm de altura) contendo solução
nutritiva (0,25 g/L de Nutrichem 60, Miller Chemical, Hanover, PE, EUA.) para manter a
turgescência. Os folíolos foram dispostos com a superfície abaxial para baixo em ângulo que
tornasse toda a folha acessível para o inseto, e arranjados em formato de círculo em uma caixa
acrílica (25 x 25 cm) (Figura 4).
Trinta moscas-brancas adultas, sem distinção de sexo, foram liberadas no meio do
círculo formado pela disposição dos folíolos, depois de tratamento pelo frio a 4°C durante dez
minutos visando reduzir sua atividade e facilitar o manuseio. Em seguida, cada caixa foi
coberta com uma tampa de acrílico (25 × 25 × 10 cm), contendo uma abertura coberta por
tecido voil para ventilação.
Foi contado o número de moscas-brancas que pousaram em ambas as superfícies adaxial
e abaxial do folíolo após 30 min, 1 h, 2 h, 4 h, 8 h, 24 h e 48 h da liberação. Calculou-se o
número médio de insetos pousados em três folíolos de cada tratamento em condição de livre
escolha. Os dados foram submetidos a teste de Mann-Whitney U-testes em nível de
significância de 5%, utilizando o software SPSS v. 20.
Figura 4. Folíolos do clone de batata ‘Ágata’
sadios e infectados, dispostas alternadamente
em caixas acrílica para ensaio de atratividade
de Bemisia tabaci biótipo B.
22
3.7.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha
Para os testes de preferência à oviposição com chance de escolha, foram coletadas as
mesmas folhas avaliadas para o teste de atratividade dos insetos adultos. Foram utilizados
quatro tratamentos (‘Ágata’ e Bach-4 sadios e ‘Ágata’ e Bach-4 infectados) e 15 repetições
em blocos casualizados e cada parcela foi representada por um vaso com uma planta.
Realizou-se contagem de ovos da folha inteira com auxílio de um estereoscópio,
Tecnival® modelo SQF com aumento de 20 vezes. Após a contagem, foi realizada a medição
da área foliar para obtenção do número de ovos por cm² através do programa ImageJ®,
utilizando-se uma escala de 5 cm.
Os resultados da preferência para oviposição foram transformados em log X+1 e
analisados por comparação de médias através do Teste-t Student a 5% de probabilidade,
através do software SPSS v. 20.
Para a condição de obrigatoriedade, ou seja, sem chance de escolha para oviposição pela
mosca-branca, utilizaram-se os mesmos tratamentos e delineamento do teste de preferência
para oviposição com chance de escolha. Cada vaso foi protegido por uma gaiola de arame,
envolta por tecido voil (Figura 5). A infestação das plantas por B. tabaci biótipo B foi
realizada colocando-se aproximadamente 150 insetos adultos, de idade desconhecida, por
vaso. Os insetos foram capturados por meio de sugador oriundos da criação-estoque. Avaliouse a oviposição após sete dias, utilizando-se o método descrito no teste com chance de
escolha.
Figura 5. Clones de batata individualizados em gaiolas de
arame cobertas por tecido voil, no ensaio de oviposição de
Bemisia tabaci biótipo B em teste sem chance de escolha.
23
3.7.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas
Estudou-se o comportamento de migração e imigração de adultos de B. tabaci biótipo B
entre plantas de batata sadias e infectadas por ToCV dos clones Bach-4 e ‘Ágata’ em duas
fases. Na primeira, avaliou-se o efeito de migração da mosca-branca. Em uma gaiola coberta
por tecido voil isolou-se uma planta sadia junto com uma infectada. Sobre a planta sadia
foram liberados vinte insetos adultos com aproximadamente cinco dias de vida oriundos de
colônia em planta sadia de batata ‘Baraka’. Esse clone, diferente dos analisados, foi usado
visando minimizar qualquer efeito de preferência por parte do inseto. Os insetos passaram por
um jejum de 1 h antes de serem liberados na planta sadia. A movimentação dos insetos para a
planta infectada foi avaliada 5 min, 15 min, 30 min, 1 h, 6 h e 24 h após a liberação. A
contagem dos adultos foi realizada com o auxílio de um espelho, contando-se o número total
de insetos na parte abaxial das folhas de toda a planta infectada.
Na segunda fase, avaliou-se o efeito de imigração seguindo o mesmo procedimento
descrito para a primeira fase, exceto a liberação dos insetos, que ocorreu na planta infectada,
observando a movimentação para a planta sadia. Cada tratamento constituiu de 15 repetições,
com plantas de 40 DAP, conduzidos com tratos culturais descritos no item 3.3.1. Os dados
foram analisados através de correlação linear entre o número de adultos migrados e época de
avaliação. As médias e erros padrões foram obtidos através do software SPSS v. 20.
3.7.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’
Através da técnica de Eletrical Penetracion Graph (EPG) caracterizou-se o
comportamento alimentar de B. tabaci biótipo B em tecido vegetal do clone ‘Ágata’ sadio e
infectado. Foi realizado o monitoramento alimentar de adultos de B. tabaci biótipo B até a
obtenção de 15 registros válidos, ou seja, sem interferência ou alterações.
Os registros para ‘Ágata’ em plantas sadias e plantas infectadas foram obtidos no
laboratório ICA- CSIC. A produção das plantas de batata foi realizada seguindo descrição no
item 3.3.2 e os insetos utilizados foram os da criação descrita no item 3.4.2. O software
utilizado para a obtenção dos registros das ondas foi o Stylet+dDataq Di158U (Giga-8)
acoplado a um PC. Foram obtidos 15 registros válidos com duração de 8 h para os dois
tratamentos e os dados foram armazenados em um cartão de memória para posterior análise.
24
A planta, a mosca-branca e o amplificador foram mantidos dentro de uma gaiola de
Faraday para evitar qualquer ruído eletrônico que pudesse vir interferir nos resultados das
ondas obtidas (Figura 6).
a
b
Figura 6. a) Equipamento de Electrical Penetracion Graph giga 8. b) Planta
de batata do clone ‘Ágata’ infectada por ToCV, acoplada ao equipamento.
Os insetos adultos (3-5 dias de vida) foram capturados da criação em plantas de
berinjela com o auxílio de um sugador e colocados em microtubos (cerca de dez adultos por
microtubo). Em seguida foram colocados em gelo por cinco minutos para que diminuíssem a
movimentação. Os indivíduos utilizados foram sexados com o auxílio de lupa, sendo o
reconhecimento dos machos e das fêmeas feito através das diferenças anatômicas do abdômen
do inseto. A fêmea tem o abdômen arredondado e o macho em formato de "pinça" em sua
porção final. Os machos foram eliminados, utilizando-se somente as fêmeas devido a sua
melhor capacidade de alimentação.
Posteriormente as fêmeas foram colocadas sobre uma placa de Petri coberta por fita de
coloração preta e gelo em seu interior para imobilizá-las e permitir melhor manipulação. A
placa foi mantida abaixo de uma fonte de luz fria e de um microscópio estereoscópico (Nikon
SMZ2,). A conexão dos insetos aos eletrodos de cobre (3 cm x 1 mm de diâmetro) foi feita
através de um fio de ouro de aproximadamente 2 - 3 cm de comprimento e 11 - 12.5 µm de
diâmetro. Com a ajuda de uma pinça de ponta curva e um estilete entomológico, o fio de ouro
foi colado ao dorso do abdome do inseto. Para a fixação, utilizou-se uma gota de pintura de
prata condutora (16034 PelcoCollodia Silver, CA, EUA.). Os insetos foram deixados em
jejum durante 1 h, com o fio de ouro aderido, antes de dar início ao registro. Após o jejum dos
insetos, acoplou-se os eletrodos ao amplificador de sinais do equipamento.
25
As plantas de batata foram oferecidas aos insetos em vasos de 10 cm de diâmetro, sendo
colocado no substrato um segundo eletrodo de cobre de 10 cm de comprimento e 0,2 cm de
diâmetro para fechar o circuito eletrônico.
Após a obtenção, os registros de ondas do clone ‘Ágata’ foram analisados utilizando
Stylet+aDataq Di158U (Giga-8 EPG systems, Wageningen, The Netherlands).
Este aplicativo permite visualização das ondas obtidas nos registros, bem como fazer a
marcação dos diferentes eventos (tipos de onda) descritos por TJALLINGII (1990), que
correspondem à atividade dos estiletes do inseto em diferentes tecidos da planta. As
atividades foram identificadas baseando-se na análise da amplitude e da frequência de ondas
registradas. A observação e análise foram feitas empregando-se intervalos de tempo de dez e
15 segundos para ser mais precisa. Os dados da avaliação das marcas foram interpretados e
dispostos em forma de tabelas para realização da análise estatística.
Os parâmetros avaliados foram divididos em não sequenciais: número de np (não
prova); número de provas; número de pd (queda de potencial); número de C (caminhamento
do estilete); número de E1 (salivação); número de E2 (ingestão floemática); duração total de
np; tempo total de prova; duração total de pd; duração total de C; duração total de G (xilema);
duração total de F (descarrilhamento do estilete); duração total de E1; duração total de E2;
duração total de E (E1+E2). E parâmetros sequenciais: tempo da primeira prova desde o
começo do registro; tempo do início do registro até a primeira fase em E; tempo da primeira
prova até a primeira fase E; tempo do início da prova até a primeira fase E; tempo do começo
do registro até a primeira fase E2 sustentada (dez minutos); tempo da primeira prova até a
primeira fase E2 sustentada; tempo do início da prova até a primeira fase E2 sustentada;
tempo d início da prova para a primeira E2; duração de não prova após a prova da primeira
fase E2 sustentada; número de provas até primeira fase E1; número de provas depois da
primeira E; tempo para o início da primeira prova até a primeira pd e tempo desde o final da
última pd até o final da última prova.
Os parâmetros sequenciais e não sequenciais foram calculados para cada registro de
EPG usando o MS Excel workook (versão 4.4.1) desenvolvido por SARRIA et al. (2009). Em
seguida realizou a análise estatística de comparação entre médias dos resultados obtidos nos
parâmetros analisados de cada clone nos dois diferentes tratamentos (sadio e infectado). As
médias que resultaram em um valor normal foram comparadas por meio do teste-t student a
nível de 5% e, para as médias não normais, utilizou-se o teste não paramétrico de MannWhitney U-test a nível de significância de 5%, por meio do software SPSS v. 20 (SPSS Inc.,
Chicago, IL, EUA).
26
3.7.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados
O desenvolvimento ovo-adulto da B. tabaci biótipo B nos clones de batata ‘Ágata’ e
Bach-4 foi avaliado utilizando-se plantas com 40 DAP infectadas e sadias. As plantas foram
transferidas para a casa de vegetação com a criação de B. tabaci biótipo B, no Centro de
Fitossanidade do IAC, onde permaneceram por um período de quatro horas, para oviposição
dos insetos adultos. Após esse período, os adultos foram aspirados com o auxílio de sugador
(ponteira de 1 ml acoplada a uma mangueira de 30 cm de plástico teflon®), para evitar futura
oviposição e ovos com idades diferentes.
O delineamento foi de blocos ao acaso, com quatro tratamentos (plantas de ‘Ágata’ e
Bach-4 sadias e plantas de ‘Ágata’ e Bach-4 infectadas) e seis repetições. Cada parcela
constou de um vaso com uma planta cada. Foram utilizados dois folíolos por planta, sendo
que, em cada um deles, demarcou-se uma área contendo 20 ovos, totalizando 40 ovos por
planta, num total de 240 ovos por tratamento. A demarcação foi realizada por meio do auxílio
de microscópio estereoscópico (40X), demarcando-se com caneta vermelha de retroprojetor
(ponta de 1 mm). Em seguida, as plantas foram mantidas em casa de vegetação protegidas
com tela antiafídeo para evitar infestação por outros insetos.
Diariamente, foi inspecionada cada área demarcada de cada planta, anotando-se o
número de ovos, número de ninfas e o número de pupários vazios, indicando a emergência
dos adultos. Com base nesses dados determinou-se o número médio de dias necessários para o
completo desenvolvimento do inseto e a porcentagem de emergência de adultos nos diferentes
tratamentos.
As longevidades médias de cada fase do desenvolvimento foram submetidas à análise
de variância, sendo comparadas pelo teste de Tukey (p ≤ 0,05). Para os dados de viabilidade
de adultos emergidos dos quatro tratamentos, realizou-se o teste de Qui-quadrado (X²) a 5%
de probabilidade, utilizando-se o software SPSS v. 20.
3.8 Efeito de ToCV na Produção de Voláteis em Clones de Batata e Interação com
Bemisia tabaci biótipo B
3.8.1 Compostos voláteis de plantas sadias e infectadas
27
Foram avaliadas plantas com 30 DAP dos clones ‘Ágata’’ e Bach-4, sadias e infectadas
por ToCV, perfazendo quatro tratamentos. Os voláteis foram extraídos pela técnica de
aeração. As plantas foram transferidas para câmaras de vidro com capacidade para 2 L
(previamente lavadas com acetona seguindo-se lavagem com hexano), fechadas e acopladas
ao sistema de aeração. Por meio de um orifício lateral foi injetado ar comprimido filtrado por
carvão ativado a uma taxa de 1 L/min. O ar foi bombeado por um compressor de ar
controlado por um regulador de fluxo. A saída do ar, com taxa de 6 L/min se deu por um
orifício situado na parte superior da câmara de vidro. Nesse orifício foi acoplado um tubo de
vidro com filtro contendo polímeros adsorventes Super-Q® (25 mg, malha 80-100; Alltech
Associates Deerfield, IL, EUA) (TURLINGS et al., 1990; 1995) para captar os voláteis
emitidos pela planta. As plantas foram introduzidas nas câmaras com cuidado a fim de evitar
a liberação de voláteis de defesa induzida pelo contato com a parte vegetativa (Figura 7).
Figura 7. Sistema de extração de voláteis de plantas de batata
Os voláteis liberados pelas plantas nas câmaras foram coletados em intervalos de 12
horas, com temperatura controlada de 26°C e luz suplementar, visto que a produção de
voláteis pela planta é dependente da atividade fotossintética (ARIMURA et al., 2005).
Após a coleta dos voláteis, os filtros foram submetidos à extração com solvente
orgânico n-hexano (500 µl) os extratos foram pré-concentrados pelo fluxo de nitrogênio.
Posteriormente, em cada extrato foram adicionados 10 µL de Nonyl [padrão interno (PI)], e
armazenados em freezer (-20ºC) até o momento da análise.
A análise dos compostos voláteis se realizou em um cromatógrafo gasoso (Agilent
7890A) acoplado a um espectrômetro de massa (Agilent 5975C VL MSD com Triple-axis
28
Detector com linha de transferência 230°C, potencial de ionização de 70 eV). Foram injetados
2 µL da amostra em modo splitless em uma coluna HP-1MS (30 m x 0,25 mm x 0,25 µm),
utilizando hélio como gás de arraste a um fluxo constante de 1mL/min. Após a injeção da
amostra, a temperatura foi mantida a 40°C.
Os compostos foram tentativamente identificados pela comparação de seus espectros de
massas com os computadorizados na biblioteca ‘Nist’ do software Workstation Toolbar e pela
co-injeção de compostos padrões. Cada composto de plantas sadias e infectadas tiveram sua
área calculada no programa do software Workstation Toolbar.
3.8.2 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos
O ensaio foi conduzido no laboratório do ICA/CSIC, onde se avaliou a preferência de
adultos de B. tabaci biótipo B em folhas de plantas de batata do clone ‘Ágata’ sadias e
infectadas por ToCV, em função dos voláteis emitidos pelas folhas, sob condições de presença
de luz e ausência de luz. A presença de luz foi caracterizada por luz branca e a ausência foi
caracterizada pelo uso de luz infravermelho.
O delineamento experimental foi inteiramente casualizado. Foram realizados quatro
ensaios para o clone ‘Ágata’ sadio e infectado, com presença e ausência de luz. O primeiro e
segundo ensaios foram repetidos 20 vezes, sendo que a cada dez liberações os lados dos
tratamentos eram alternados. Os terceiro e quarto ensaios foram repetidos 40 vezes, também
alternando os lados dos tratamentos a cada dez repetições.
O primeiro ensaio realizou-se na presença de luz, com planta infectada ao lado de
ausência de planta. O segundo ensaio seguiu o mesmo padrão do primeiro, alterando a
presença de luz, por ausência de luz. Para o terceiro ensaio, na presença de luz, utilizou-se
planta infectada ao lado de planta sadia. No quarto ensaio foi adotado o mesmo padrão do
terceiro, alterando a presença de luz, por ausência de luz.
Uma placa de Petri de 12 cm de diâmetro foi demarcada ao meio e de cada lado se fez
um orifício de 5 cm de diâmetro, coberto com tela antiafídeo colocado pelo lado externo da
placa. A placa foi acomodada sobre um suporte de ferro vasado, de forma que ficasse
suspensa, com distância média de 30 cm da bancada e 30 cm da fonte de luz e com a
superfície livre para poder alojar as folhas das plantas de cada ensaio (Figura 8).
Para todos os ensaios foram utilizados 20 insetos adultos com idade entre cinco a sete
dias. Os insetos foram expostos ao frio (4°C) durante dez minutos para reduzir sua atividade e
29
facilitar o manuseio. As folhas foram colocadas com a parte abaxial sobre o orifício coberto
com a tela e presas por uma fita adesiva. Os insetos foram liberados no centro da placa, e o
número de vezes que os insetos entraram na superfície da folha foi registrado durante dez
minutos de escolha, com ajuda de um espelho acoplado abaixo da placa de Petri.
Os dados médios de cada ensaio, após a contagem total de insetos pousados em cada
tratamento, foram submetidos a análise de variância pelo teste ANOVA, e as médias
comparadas por Tukey a 5% utilizando-se o software SPSS v. 20.
b
a
Figura 8. a) Planta de batata do clone ‘Ágata’ sadia vs ‘Ágata’ infectada em ensaio na presença de luz. b) Planta
de batata do clone ‘Ágata’ sadia vs ‘Ágata’ infectada em ensaio na ausência de luz.
4 RESULTADOS
4.1 Efeito de clones de batata infectados por ToCV sobre parâmetros biológicos de
Bemisia tabaci biótipo B
4.1.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados
No primeiro tempo de avaliação (30 min) a maior atratividade dos insetos adultos
ocorre no tratamento ‘Ágata’ sadio, quando comparado com a dos outros tratamentos. Após
quatro horas de avaliação, ocorre maior atratividade para os clones infectados de ‘Ágata’ e de
Bach-4, quando comparados com os clones sadios. Entre os clones infectados, ‘Ágata’ tem
maior atratividade que o clone Bach-4. Durante os sete tempos de avaliação o clone Bach-4
sadio foi o menos atrativo para os insetos adultos.
30
Tabela 1. Número de adultos (adultos/10 cm² ) (médias ±EP) de Bemisia tabaci biótipo B em clones
de batata ‘Ágata’ e Bach-4 sadias e infectadas por Tomato chlorosis virus.
30 min
Tratamento
2h
4h
6h
12 h
24 h
72 h
0,8±0,9b
1,6±0,2a
3,7±0,6 a
5,0±0,8a
3,8±0,5a
4,2±0,7a
4,5±0,8a
‘Ágata’ Infectada
0,6±0,9b
1,4±0,1a
3,0±0,2
b
3,4±0,4b
3,7±0,2a
3,4±0,3a
4,1±0,5a
Bach-4 infectada
1,0±0,2a
1,8±0,3a
2,5±0,3b
2,8±0,5b
3,6±0,5a
3,0±0,4a
3,1±0,4a
‘Ágata’ sadia
0,4±0,4c
1,0±0,2a
1,4±0,3c
2,0±0,3c
2,8±0,6a
2,5±0,6a
2,7±0,8a
Bach-4 sadia
ns
ns
ns
p
0,003*
0,130
0,001*
0,001*
0,427
0,209
0,207 ns
Médias seguidas da mesma letra na coluna não diferem entre si ao nível de 5% de probabilidade por Bonferroni,
por meio do tese GLM com medidas repetidas. ns dados não significativos *dados significativos
4.1.2 Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e
infectadas
Não se observou diferença no número de insetos pousados em folíolos de plantas sadias
ou infectadas do clone ‘Ágata’ durante os sete tempos avaliados. Na primeira observação, aos
30 minutos, as médias variaram de 1,42 a 1,58 adultos por folíolo (sadios e infectados,
respectivamente); a seguir, houve aumento progressivo nas médias até a última avaliação,
após 24 h, quando os valores atingiram 3,41 e 5,71 (sadios e infectados) (Tabela 2).
Tabela 2. Teste de preferência para pouso de Bemisia tabaci biótipo B em condições de chance de
escolha (n:12). Madri, Espanha.
Tempo
‘Ágata’ sadia
‘Ágata’ infectada
p
30 min
1,42 ± 0,31a
1,58 ± 0,34a
0,72ns
1h
2,58 ± 0,62a
2,75 ± 0,75a
0,87 ns
2h
3,92 ± 0,65a
3,42 ± 0,67a
0,60 ns
4h
3,08 ± 0,62a
3,67 ± 0,67a
0,53 ns
6h
3,34 ± 0,62a
3,75 ± 0,60a
0,63 ns
12h
3,50 ± 0,57a
4,92 ± 0,67a
0,12 ns
24h
3,41 ± 0,49a
5,17 ± 0,92a
0,11 ns
Médias seguidas da mesma letra na coluna não diferem entre si ao nível de 5% de probabilidade por meio do
teste de Mann-Whitney. ns dados não significativos
4.1.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha
Em ambos os experimentos, com e sem chance de escolha, não foram observadas
diferenças na oviposição do inseto em plantas sadias e em plantas infectadas dos dois clones
avaliados (Tabela 3).
31
Tabela 3. Preferência de Bemisia tabaci biotipo B para oviposição (ovos/10 cm²) (médias ±EP) em
clones de batata ‘Ágata’ e Bach-4 sadias e infectadas por Tomato chlorosis virus, em teste com e sem
chance de escolha.
nº ovos/10 cm²
Tratamento
‘Ágata’ Infectada
Bach-4 infectada
‘Ágata’ sadia
Bach-4 sadia
Com chance
24,2±6,4a
28,8±3,7a
23,5±3,3a
23,3±6,1a
p
0,118ns
Sem chance
9,3±0,7a
9,8±0,6a
9,4±0,9a
10,2±0,8a
p
0,865 ns
Médias seguidas da mesma letra na coluna não diferem entre si ao nível de 5% de probabilidade, por meio de
teste t-Student. ns dados não significativos
4.1.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas
Para o clone ‘Ágata’, detectou-se correlação positiva tanto para o número de adultos
que movimentaram de plantas sadias e pousaram em plantas infectadas como o número de
adultos que se movimentam de plantas infectadas e pousam em plantas sadias (Figura 09).
Já para o clone Bach-4 não se verificou significância para nenhum dos movimentos,
Número de insetos pousados na planta
destino
sadia para infectada ou infectada para sadia (Figura 10).
6
Ágata' Sadia -> Infec.
y = 0,684x + 0,9686
R² = 0,944
5
Ágata' Infec -> Sadia
4
3
y = 0,1849x + 0,6078
R² = 0,9859
2
1
0
0
1
2
3
4
5
Tempos de observação
1(5min) 2(15min) 3(30min) 4(1h) 5(6h) 6(24h
6
Figura 9. Correlação entre o número de adultos de Bemisia tabaci biótipo B pousados em plantas
sadias após a liberação em planta infectada por Tomato chlorosis virus (‘Ágata’ Sadia/Infec) e
pousados em plantas infectadas após a liberação em planta sadias (‘Ágata’ Infec/Sadia)
32
Número de insetospousados na planta
destino
4
Bach-4 Sadia -> Infec
3
Bach-4 Infec -> Sadia
y = 0,0555x + 1,9922
R² = 0,008
2
y = -0,0924x + 0,9608
R² = 0,5775
1
0
0
1
2
3
4
5
6
Tempos de observação
1(5min) 2(15min) 3(30min) 4(1h) 5(6h) 6(24h)
Figura 10. Correlação entre o número de adultos de Bemisia tabaci biótipo B pousados em plantas
sadias após a liberação em planta infectada por Tomato chlorosis virus (Bach-4 Sadia/Infec) e
pousados em plantas infectadas após a liberação em planta sadias (Bach-4 Infec/Sadia)
4.1.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’
Dentre os parâmetros avaliados, houve diferença significativa no número de eventos
da onda por inseto (‘number of waveform events per insect’ – NWEI), para o número de
picadas de prova (pd), sendo maior nas plantas de ‘Ágata’ infectadas por ToCV, quando
comparados com plantas sadias (Tabela 4). Para a duração da onda em minutos por evento
(‘waveform duration (min) per event’ – WDE), obteve-se diferença no tempo de não-prova
(‘no probe’), e de prova (‘probe’), com maior duração em plantas infectadas. Também houve
diferença na duração da onda de caminhamento (C) em minutos, neste caso maior em plantas
sadias (Tabela 4). A duração em minutos da onda por evento (‘waveform duration (min) per
insect’ – WDI), apresentou diferença na fase floemática, sendo a maior duração em plantas
infectadas por ToCV (Tabela 5).
33
Tabela 4: Valores das variáveis não sequenciais (média±EP), para comportamento alimentar de adultos de Bemisia tabaci biótipo B em plantas de ‘Ágata’
sadias e infectadas por Tomato chlorosis virus, durante oito horas de registro.
Variáveis não sequenciais
PPW
NWEI
p
WDI
p
WDE
p
1
1
Não-prova
infectada
15\15
34,33±5,69
0,834
19260,54 ± 950,83
0,387
560,99 ± 66,87
0,002² *
sadia
infectada
sadia
infectada
sadia
16\16
15\15
16\16
15\15
16\16
42,00 ± 7,85
33,87 ± 5,72
41,44 ± 7,92
35,07 ± 5,59
42,69 ± 7,79
pd
infectada
sadia
10\15
6\16
2,73 ± 0,81
0,56 ± 0,22
0,025²
32,18 ±10,14
6,49 ± 1,53
0,023²
4,93 ± 0,23
4,33 ± 0,45
0,2751
F
infectada
sadia
2\15
1\16
0,20 ± 0,14
0,06 ± 0,06
0,488²
813,73 ± 167,31
153,76
0,2631
542,49 ± 101,17
153,76
0,1951
G
infectada
sadia
13\15
12\16
1,87 ± 0,27
1,63 ± 0,37
0,6111
3870,18 ± 894,54
2957,46 ± 1130,01
0,5351
2073,31 ± 382,01
1819,97 ± 409,98
0,6531
E1
infectada
sadia
4\15
3\16
0,40 ± 0,19
0,25 ± 0,14
0,57²
46,55 ± 9,13
40,85 ± 4,66
0,6411
31,25 ± 6,65
30,64 ± 7,88
E2
infectada
sadia
3\15
2\16
0,33 ± 0,19
0,06 ± 0,06
0,235²
8198,49 ± 2198,55
935,91 ± 729,65
0,871
4919,09 ± 1574,07
935,90 ± 729,65
Prova
C
0,4451
0,8431
20699,41 ± 1313,28
9539,39± 950,83
8001,80 ± 1328,14
3908,60 ± 554,04
4910,08 ± 875,51
0,361
0,3431
429,85 ± 52,59
281,67 ± 44,12
193,11 ± 28,06
111,25 ± 9,80
115,02 ± 14,18
0,003² *
0,005² *
0,9551
0,1951
*dados significativos ao nível de 5% de probabilidade; 1 – teste paramétrico teste-t Student a nível de 5% 2 – teste não paramétricos Mann-Whitney
U-test a 5%; PPW: proporção de indivíduos que produzem determinada onda; NWEI: número de eventos da onda por inseto; WDI: duração da onda em minutos
por inseto; WDE: duração em minutos da onda por evento. Non-probe: não atividade de prova, Probe: atividade de prova; C: caminhamento do estilete; pd:
picada de prova; F: descarrilhamento do estilete; G: atividade no xilema;E1: relacionado com atividade de salivação no floema; E2: relacionando com atividade
de ingestão no floema.
34
Tabela 5. Valores das variáveis sequenciais (média±EP), para comportamento alimentar de adultos de Bemisia tabaci biótipo B em plantas de ‘Ágata’ sadias e
infectadas por Tomato chlorosis virus, durante oito horas de registro.
Variáveis sequenciais
PPW
NWEI
p
WDI
p
Tempo da primeira prova desde o começo do registro
infectada
15\15
3882,43 ± 1105,72
0,8111
Duração da segunda prova
Tempo para o início da primeira prova até a primeira pd
Tempo do início da prova até a primeira fase E
Tempo da primeira prova até a primeira fase E2 sustentada
Tempo do início da prova para a primeira E2
Tempo da primeira prova até a primeira fase E
Número de provas até a primeira fase E1
Número de provas depois da primeira E
Duração total de E
Tempo do início do registro até a primeira fase em E
Tempo do começo do registro até a primeira fase E2 sustentada
Duração de não prova após a prova da primeira fase E2
sustentada
sadia
infectada
sadia
infectada
sadia
infectada
sadia
infectada
16\16
15\15
16\16
10\15
6\16
4\15
3\16
15\15
4250,28 ± 1054,98
443,20 ± 226,87
83,95 ± 35,39
9715,89 ± 2549,92
7167,56 ± 2498,15
718,85 ± 180,89
445,28 ± 177,02
21827,37 ± 1905,94
sadia
infectada
sadia
infectada
sadia
infectada
sadia
infectada
sadia
infectada
sadia
infectada
sadia
infectada
sadia
16\16
3\15
1\16
4\15
3\16
4\15
3\16
4\15
3\16
4\15
3\16
4\15
3\15
3\15
2\16
23918,11 ± 1200,39
910,92 ± 149,54
830,44
20832,00 ± 2154,81
21828,22 ± 1843,33
15,50 ± 4,34
22,33 ± 9,14
2,80 ± 1,82
1,88 ± 1,20
0,1391
0,240²
0,3411
0,722²
0,8131
0,7271
0,4921
0,886²
6936,52 ± 1784,05
663,64 ± 520,36
24714,44 ± 2138,01
26078,50 ± 1752,90
25709,80 ± 1739,86
28168,39 ± 535,34
infectada
3\15
740,75 ± 620,91
sadia
2\16
676,26
*dados significativos ao nível de 5% de probabilidade; 1 – teste paramétrico teste t-Student a nível de 5% 2 – teste não paramétricos Mann-Whitney U-test a 5%.
0,034¹*
0,6241
0,193²
0,9631
35
4.1.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados
A fase de ovo de B. tabaci biótipo B foi mais longa nas plantas sadias quando
comparadas com plantas infectadas, para os dois clones avaliados (Tabela 6). Nos ínstares
isoladamente, verificou-se diferença na duração apenas no quarto ínstar. Plantas sadias do
clone Bach-4 proporcionaram tempo maior em comparação com o clone ‘Ágata’, em plantas
sadias e infectadas. Considerando-se o ciclo ovo-adulto, plantas dos dois clones, quando
infectadas, induziram os menores tempos de desenvolvimento em comparação com plantas
sadias.
Tabela 6. Número médio de dias (média ±EP) de desenvolvimento ovo-adulto de Bemisia tabaci
biótipo B em folhas de batata dos clones Bach-4 e ‘Ágata’, sadios e infectados por Tomato chlorosis
virus.
Fase de desenvolvimento
Tratamento
‘Ágata’ infectada
Bach-4 infectada
‘Ágata’ sadia
Bach-4 sadia
p
Médias seguidas da
teste de Tukey
3º ínstar
4º ínstar
ciclo
completo
4,83 ± 0,05a
5,83 ± 0,04a
4,16 ± 0,03a
30,99 ± 0,05a
6,16 ± 0,02a
4,66 ± 0,04a
5,16 ± 0,03a
4,83 ± 0,05ab
30,99 ± 0,04a
7,16 ± 0,01b
6,33 ± 0,06a
4,55 ± 0,02a
6,33 ± 0,02a
4,00 ± 0,02a
32,32 ± 0,06 ab
7,00 ± 0,01b
4,83 ± 0,04a
4,50 ± 0,04a
5,33 ± 0,03a
5,66 ± 0,02b
33,00 ± 0,01b
ovo
1º ínstar
2º ínstar
5,83 ± 0,01a
6,16 ± 0,06a
5,83 ± 0,01a
0,001*
0,300
ns
0,927
ns
0,176
ns
0,013*
0,004
mesma letra na coluna não diferem entre si ao nível de 5% de probabilidade por meio do
Considerando-se a viabilidade das diferentes fases, observou-se tendência de
diminuição de insetos adultos viáveis durante a evolução do desenvolvimento para insetos em
plantas infectadas dos dois clones, embora não tenha sido detectada diferença pelo teste de
Qui-quadrado. A viabilidade para o ciclo ovo-adulto variou de 78,3 (Bach-4 infectada) a
88,3% (‘Ágata’ sadia) (Tabela 7).
Tabela 7. Viabilidade (%) das fases de ovo e de ninfa de B. tabaci biótipo B em folhas de batata dos
clones Bach-4 e ‘Ágata’, sadios e infectados por Tomato chlorosis virus.
Fase de desenvolvimento
Tratamento
‘Ágata’ infectada
Bach-4 infectada
‘Ágata’ sadia
Bach-4 sadia
ovo
100
100
100
100
1º ínstar
90,8
91,2
95,8
95
2º ínstar
90,4
91,2
95,4
93,2
3º ínstar
87,1
88,5
92,9
91,4
4º ínstar
83,3
81,8
88,8
89,2
X²
Médias de viabilidade a 5% de probabilidade, por meio de teste Qui-quadrado (X²).
ciclo completo
78,8
78,3
88,3
88,2
0,453ns
ns
não significativo
36
4.2 Efeito de ToCV na Produção de Voláteis em Clones de Batata e Interação com
Bemisia tabaci biótipo B
4.2.1 Compostos voláteis de plantas sadias e infectadas
Verificou-se que o tipo de volátil e sua quantidade diferiram entre clones e entre
plantas sadias e infectadas (Tabela 8). Detectaram-se dois principais compostos em plantas
sadias do clone ‘Ágata’ e oito principais em plantas sadias de Bach-4, sendo que nas plantas
infectadas alguns voláteis não foram detectados ou estavam presentes em quantidade menor,
como o transcarofileno no clone ‘Ágata’ e os compostos β-elemene, trans-alpha-bisabolone,
naphthalene 2-isopropyl, delta-cadinene e outro não identificado em Bach-4.
Tabela 8. Perfil dos compostos voláteis extraídos de plantas de ‘Ágata’ e Bach-4 sadias e infectadas
por Tomato chlorosis virus, detectados por GC-MS.
Tempo de
Conteúdo
Conteúdo relativo
retenção
Composto
Fórmula
relativo (área)
(área) planta
(min)
planta sadia
infectada
Clone ‘Ágata’
20,01
26,78
Ácido salicílico
Trans-carofileno
C7H603
C15H24
1,24
1,27
1,26
0
C10H18O
C15H24
C15H24
3,00
0,54
0,35
10,99
4,04
1,40
0
0,38
0
0
C13H14
1,40
0
C15H24
C15H24
8,06
2,32
1,82
0
Clone Bach-4
14,26
18,59
21,69
25,51
27,07
27,25
27,85
28,79
1,8 cineole
β-elemene
Trans alpha bisabolone
Naphthalene, 2isopropyl
Germacrene - D
Delta-cadinene
4.2.2 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos
Na presença de luz visível, os adultos dirigiram-se indistintamente para plantas sadias
e plantas infectadas (Tabela 9). Porém, em condições de ausência de luz, quando a orientação
37
foi somente pelos voláteis emitidos pelas plantas, houve preferência dos adultos por plantas
infectadas por ToCV.
Tabela 9. Preferência de Bemisia tabaci biotipo B por folhas sadias e infectadas de batata ‘Ágata’ em
ensaio de dupla escolha na presença de luz visível e luz infravermelha.
‘Ágata’
Infectada
Sadia
Infectada
Sadia
Tratamento
Infravermelha
Luz
Média±EP
1,75±0,2a
0,90±0,2b
1,58±0,2a
1,18±0,2a
p
0,006*
0,146 ns
Médias seguidas da mesma letra não diferem entre si ao nível de 5% de probabilidade por meio do teste Anova
ns
dados não significativos *dados significativos
5
DISCUSSÃO
5.1 Atratividade de B. tabaci biótipo B por clones de batata sadios e infectados
A diferença de atratividade de adultos de moscas-brancas pelas plantas hospedeiras
pode indicar mecanismos de resistência relacionados a fatores de morfológicos e químicos,
sendo que os metabólitos emitidos como voláteis das plantas podem atuar como repelentes ou
atrativos para os insetos vetores (CHERMENSKAYA et al., 2009). Vírus de plantas podem
modificar o comportamento de seus vetores indiretamente, causando mudanças na fisiologia,
morfologia e constituição bioquímica da planta hospedeira, o que, consequentemente, altera a
atratividade do inseto vetor (INGWELL et al., 2012).
No presente experimento, apenas na primeira avaliação (30 minutos) houve maior
número de adultos por plantas sadias do clone ‘Ágata’ em comparação com plantas infectadas
desse e do clone Bach-4 (Tabela 1). A partir de quatro horas, em todas as demais avaliações,
houve tendência de maior atratividade para plantas infectadas por ToCV dos dois clones,
sendo significativas as diferenças para quatro e seis horas em plantas infectadas. Sabe-se que
o clone ‘Ágata’ é suscetível a B. tabaci biótpo B e o clone Bach-4 apresenta resistência
moderada a esse inseto (SILVA et al., 2008; ROCHA et al., 2012); assim, essa diferença na
resistência poderia explicar a maior e a menor atratividade em plantas sadias de ‘Ágata’ e em
Bach-4, respectivamente, num primeiro momento. Também deve ser considerado que os
fatores químicos e morfológicos podem atuar isolada ou conjuntamente em etapas, no
decorrer de determinado tempo (PANDA & KHUSH, 1995), envolvendo diferentes estágios,
mediados por estímulos visuais (PROKOPY & OWENS, 1983), de olfato e de alimentação
38
(STÄDLER, 1986), podendo retardar o reconhecimento, pelo adulto da mosca-branca, da
planta hospedeira mais adequada, nas condições experimentais de livre escolha. De forma
similar às diferenças observadas entre plantas sadias e infectadas por ToCV do mesmo clone,
CARMO-SOUZA et al. (2014) também verificaram que plantas de abóbora infectadas por
Cucumber mosaic virus (CMV) foram mais atrativas para pulgões nos 30 primeiros minutos
de avaliação, num total de quatro horas; esses autores relacionaram o comportamento de
atratividade do inseto vetor ao tipo de transmissão do vírus estudado, visto que CMV é
transmitido de forma não persistente. Segundo MAUCK et al. (2012), os modos de
transmissão viral estão associados com a atratividade do inseto pelas plantas infectadas, sendo
os maiores pouso e alimentação sustentados para plantas com transmissão do tipo persistente.
No presente trabalho, observou-se atratividade crescente pelas plantas infectadas até o período
de seis horas. O tipo de transmissão viral de ToCV é semi-persistente, no qual o inseto deve
permanecer um tempo maior na planta infectada para adquirir o vírus e em seguida disseminálo para outras plantas.
5.2. Atratividade de B. tabaci biótipo B por folíolos de batata ‘Ágata’ sadias e infectadas
Comparando-se os resultados das análises aos 30 minutos, quatro e seis horas com os do
item 5.1, verifica-se que houve significância para aquele, mas não para este. Para explicar este
fato, sugere-se que o processo de seleção do inseto pode ter sido modificado pelo
microambiente criado no interior da caixa acrílica, afetando a capacidade do inseto de
distinguir entre plantas sadias e infectadas pela liberação dos voláteis, devido à proximidade
dos folíolos e baixa aeração no interior das caixas. Também deve ser considerado que, neste
caso, usaram-se folhas destacadas de plantas, o que pode ter interferido na emissão dos
voláteis. Com base nos resultados dos dois experimentos realizados com o mesmo objetivo,
mas com métodos diferentes, verifica-se que a melhor forma de se avaliar a atratividade de
adultos de mosca-branca seria utilizando-se plantas e não folhas destacadas.
Adicionalmente, alguns estudos demonstraram que estímulos visuais e olfativos
emitidos pelas plantas podem alterar a capacidade do inseto de discriminar entre planta não
infectada e planta infectada (EIGENBRODE et al., 2002; MEDINA-ORTEGA et al., 2009;
MAUCK et al., 2010).
39
5.3 Preferência de B. tabaci biótipo B para oviposição em clones de batata sadios e
infectados em teste com e sem chance de escolha
Nos dois experimentos, com e sem chance de escolha, conduzidos para avaliar eventuais
efeitos da infecção por ToCV dos clones ‘Ágata’ e Bach-4 sobre oviposição da mosca-branca,
não foram detectadas diferenças no número de ovos colocados, embora com tendência de
maior oviposição em plantas de Bach-4 infectadas (28,8 ovos/10 cm2) em comparação com
plantas sadias (23,3 ovos/10 cm2) desse mesmo clone. Assim, de acordo com os resultados
obtidos para os clones estudados, a seleção do sítio em plantas de batata para deposição dos
ovos por B. tabaci biótipo B provavelmente não seja um evento afetado pela infecção por esse
vírus.
À semelhança de outras espécies de insetos, a seleção de um substrato para oviposição
por adultos de B. tabaci biótipo B é uma fase crítica no seu ciclo biológico, principalmente
devido ao fato de as ninfas serem sésseis, com exceção do primeiro ínstar, quando há limitada
capacidade de dispersão dentro da planta (VAN LENTEREN & NOLDUS, 1990). Embora a
oviposição de um inseto vetor possa ser influenciada pelas variações morfológicas das
plantas, além de fatores abióticos, como a disponibilidade de luz e mudanças das condições
ambientais (CHU et al., 2000), a colocação de ovos pelas fêmeas deve estar relacionada
principalmente a fatores químicos da planta, uma vez que a alimentação e a oviposição de
moscas-brancas se processam na mesma folha. Na literatura encontram-se diversos estudos
em que é avaliada a preferência para oviposição de B. tabaci biótipo B em plantas de
expressão econômica visando à identificação de genótipos resistentes para uso em
melhoramento genético ou mesmo para plantio comercial em áreas com problemas de moscabranca caso se trate de cultivar, conforme relacionado por LOURENÇÃO et al. (2008),
VALLE et al. (2013) e PRADO et al. (2015). No caso específico de batata, SILVA et al.
(2008) avaliaram 24 genótipos do Banco de Germoplasma do IAC e relataram nãopreferência para oviposição de B. tabaci biótipo B em ‘Achat’ em testes com e sem chance de
escolha, ou seja, a menor oviposição se manteve estável em ambas as condições. A seguir,
ROCHA et al. (2012) também estudaram genótipos desse banco de germoplasma em relação a
essa mosca-branca, confirmando a menor oviposição em ‘Achat’ além de detectar baixo
número de ovos em ‘Baraka’, Bach-4 e HPC 9B.
40
5.4 Movimento de adultos de B. tabaci biótipo B entre plantas sadias e infectadas
A Hipótese de Manipulação do Vetor (“Vector Manipulation Hypothesis” – VMH)
(INGWELL et al., 2012) propõe que agentes patogênicos podem influenciar o comportamento
dos insetos vetores de duas formas distintas: diretamente, quando o patógeno está presente no
corpo do inseto vetor, e indiretamente, quando causa alterações na planta hospedeira para
influenciar o comportamento do inseto, o que poderia conferir maior eficiência de sua
transmissão. Esse efeito indireto foi observado no presente experimento para o clone ‘Ágata’,
em que ocorreu maior movimentação dos adultos de plantas infectadas para plantas sadias.
Conforme destacado por WU et al. (2014), a diminuição da qualidade nutricional da planta
contribui para a movimentação do inseto que, após se alimentar, se movimenta em busca de
outra hospedeira, com alto potencial de transmissão viral. Já a baixa movimentação dos
insetos em Bach-4 pode ser devida à presença de resistência moderada nesse clone a B. tabaci
biótipo B, e é bastante provável que substâncias secundárias estejam envolvidas nessa
resistência e que suas interações com o crinivírus sejam diferentes das que ocorreram com o
clone Ágata.
O comportamento alimentar do inseto vetor pode ser alterado depois de exposto a
plantas infectadas e de adquirir o vírus (INGWELL et al. 2012; MORENO-DELAFUENTE et
al., 2013). Em pesquisa com o psilídeo Diaphorina citri Kuwayama, a bactéria Candidatus
Liberibacter asiaticus e plantas de citrus, MANN et al. (2012) observaram que esse inseto
vetor foi atraído para as plantas infectadas; contudo, essa atração dos adultos ocorreu num
primeiro contato, pois após a alimentação, o psilídeo se dispersou para plantas não infectadas.
RAJABASKAR et al. (2014) relataram que Myzus persicae (Sulz.) livres de vírus são mais
atraídos para plantas de batata infectadas por Potato leafroll virus (PLRV) em comparação
com plantas livres de vírus; porém, insetos virulíferos são atraídos para plantas livres de vírus.
5.5 Comportamento alimentar de adultos de B. tabaci biótipo B em plantas sadias e
infectadas de ‘Ágata’
O comportamento alimentar de adultos de B. tabaci biótipo B foi alterado quando se
alimentaram em plantas de ‘Ágata’ infectadas por ToCV em comparação com plantas sadias
desse mesmo clone. Detectou-se maior número de picadas de prova (pd) nas plantas
infectadas; esse fato pode ser de extrema importância caso esse crinivírus possa estar presente
no tecido parenquimático, como ocorre para begomovírus (TOLOY, 2015), resultando em
incremento do processo de aquisição do vírus. Também se verificou maior tempo de
41
alimentação em fase floemática (E). Esse maior tempo é importante para o processo de
aquisição, visto que ToCV se encontra no floema das plantas infectadas e sua transmissão é
realizada de forma semipersistente, sendo necessário um tempo maior de alimentação do
inseto no floema das plantas infectadas para que possa adquirir o vírus. O maior número de
picadas de prova e o maior tempo de alimentação em plantas infectadas pode ser explicado
como interferência viral na planta afetando o comportamento do inseto, segundo INGWELL
et al. (2012). Embora detectadas, as diferenças apresentadas em tempos de prova, não prova e
caminhamento no comportamento alimentar de B. tabaci em clones de ‘Ágata’ não são
parâmetros significativos para indicar interferência do ToCV no comportamento da moscabranca.
Para B. tabaci biótipo Q, a infecção por Tomato yellow leaf curl vírus (TYLCV)
favorece o comportamento alimentar de adultos (MALUTA et al., 2014). Avaliando o
comportamento alimentar de adultos dos biótipos B e Q de B. tabaci em plantas de tomate
sadias e infectadas por TYLCV, LIU et al. (2013) observaram que insetos de ambos os
biótipos preferiram se alimentar em plantas infectadas; além disso, também verificaram 29%
mais provas em plantas infectadas, 2,5 vezes mais tempo de duração de fase floemática em
tomate infectado e 38% mais tempo de duração em fase de descarrilamento do estilete (F) nas
plantas de tomate infectadas.
5.6 Desenvolvimento ovo-adulto de B. tabaci biótipo B em clones de batata sadios e
infectados
A fase embrionária foi mais curta em plantas infectadas dos dois clones quando
comparada com plantas sadias de ‘Ágata’. Resultados semelhantes foram obtidos por
MALUTA et al (2014), que avaliaram o ciclo de B. tabaci biótipo Q em plantas de tomateiro
sadias e infectadas por TYLCV. Esses autores também verificaram que a fase de ovo foi mais
curta em plantas infectadas do que em plantas sadias. Os ovos de B. tabaci possuem uma
extensão do córion, denominada pedicelo, pelo qual a fêmea fixa o ovo à folha (BUCKNER et
al., 2002). Além da fixação, o pedicelo também possibilita a passagem de água e
possivelmente de solutos, fatores essenciais para o desenvolvimento dos ovos (WALKER et
al., 2010). Assim, conforme discutido por MALUTA et al. (2014), é possível que o período
embrionário mais curto em plantas infectadas possa ser explicado pela reação do ovo a
mudanças na composição química e no teor de água do tecido da planta afetada pelo vírus.
Ainda segundo MALUTA et al. (2014), apenas a fase de ovo foi afetada pela condição de
42
infecção da planta, não sendo detectadas diferenças com relação a plantas sadias no ciclo total
daquele biótipo de B. tabaci.
Sendo ToCV um crinivírus emergente em solanáceas apenas recentemente detectado em
vários estados brasileiros (BARBOSA et al., 2011), pouco se sabe, em nossas condições, de
suas interações com seu vetor mais disseminado, B. tabaci biótipo B, em plantas dessa
família, principalmente em batata. Com esses resultados, verifica-se que plantas de batata
infectadas com ToCV podem encurtar o período embrionário de moscas-brancas desse biótipo
e também o ciclo total, favorecendo o inseto. Reduções no ciclo total da mosca-branca podem
beneficiar esse inseto, desde que não haja efeitos negativos sobre outras características
biológicas. Com ciclo menor, haveria aumento do número de gerações num determinado
período, com consequente incremento nos seus níveis populacionais. A diminuição do ciclo
de vida do inseto na planta infectada pode ser uma ação viral, influenciada pelo tipo de
transmissão, sendo o ciclo de vida reduzido no caso de transmissão não persistente, e
prolongado em transmissão persistente (MAUCK et al., 2010, 2012; WU, et al., 2014).
Para outras espécies de insetos vetores, os efeitos de plantas infectadas por vírus podem
ser divergentes. Para o afídeo Acyrthosiphon pisum (Harris), seu ciclo de desenvolvimento em
plantas de ervilha infectadas por Pea enation mosaic virus (PEMV) foi menor que em plantas
sadias; já em plantas infectadas por Bean leaf roll virus (BLRV) não se observou alteração
significativa no seu ciclo (WU et al. 2014). Outros efeitos de plantas infectadas por vírus são
relatados na literatura, como aumentos na fecundidade e na longevidade de B. tabaci biótipo
B alimentada em tomateiro infectado por Tomato yellow leaf curl China virus (TYLCCNV)
(FANG et al., 2013) e também aumento na fecundidade de moscas-brancas desse biótipo
alimentadas com tomateiros infectados por Tomato mottle virus (ToMoV) (McKENZIE,
2002). Porém, efeitos negativos sobre a reprodução desse mesmo biótipo foram observados
em insetos alimentados em plantas infectadas por Tomato yellow leaf curl virus, isolado de
Israel (TYLCV-IL) (RUBINSTEIN & CZOSNEK, 1997). Contudo, esses parâmetros
biológicos não foram avaliados na presente pesquisa.
Outro parâmetro avaliado no presente experimento foi a viabilidade das diferentes fases
de desenvolvimento. Embora tenha se observado tendência de diminuição da viabilidade nos
diferentes ínstares em plantas infectadas, essa diferença não foi significativa. MALUTA et al.
(2014) observaram efeito positivo de plantas de tomate infectadas com TYLCV sobre B.
tabaci biótipo Q, as quais induziram aumento na longevidade dos machos e diminuição do
período ninfal sem alterar a viabilidade dos insetos.
43
5.7 Compostos voláteis de plantas sadias e infectadas
Muitas plantas liberam compostos orgânicos voláteis (VOCs), os quais são explorados
pelos herbívoros como sinais para a selecção de hospedeiro (BERNAYS E CHAPMAN,
1994). EIGENBRODE et al. (2002) relataram que emissões de voláteis de plantas de batata
infectadas por PLRV podem afetar o comportamento do inseto vetor M. persicae e sugeriram
que esse fenômeno pode ocorrer em outras relações de inseto vetor, vírus e planta hospedeira.
Neste experimento, houve grandes diferenças no tipo e na quantidade dos compostos
voláteis extraídos de plantas dos clones ‘Ágata’ e Bach-4, sadias e infectadas por ToCV.
Em plantas sadias e infectadas de ‘Ágata’, identificou-se a presença do ácido
salicílico (AS), o qual faz parte da rota de defesa da planta e na resistência sistêmica adquirida
(SAR), sendo também necessário para o desenvolvimento de sintomas. Aumentos nos níveis
de AS estão relacionados com a inoculação de patógenos nas plantas, pois coincidem com a
elevação da expressão de genes decodificadores de proteínas PR, estas relacionadas com a
patogenicidade (GAFFNEY et al., 1993; SHAH et al., 1999; DEMPSEY et al., 1999;
O’DONNELL et al., 2003). Ainda em ‘Ágata’, foi encontrado transcarofileno apenas em
plantas sadias; trata-se de um sesquiterpeno, composto metabólico secundário do grupo dos
terpenos.
Em plantas sadias de Bach-4, esses dois compostos extraídos em ‘Ágata’ não foram
encontrados; contudo, detectaram-se oito compostos, sendo cinco deles também
sesquiterpenos: β-elemene, trans-alpha-bisabolone, naphthalene 2-isopropyl, germacrene-D e
deltacadinene. Completando, os outros três compostos envolvem 1,8 cineole, um
monoterpeno, e dois não identificados.
Os efeitos dos terpenoides em insetos herbívoros, como ação tóxica, deterrentes na
alimentação e oviposição, têm sido objeto de estudo, sendo que muitos sesquiterpenos estão
relacionados com resistência a pragas (WESTON et al., 1989; EIGENBRODE & TRUMBLE,
1993; RAHIMI & CARTER, 1993; EIGENBRODE et al., 1994; FREITAS, 1999). A redução
da resistência em plantas infectadas por vírus tem sido proposta como uma manipulação do
vírus em seu benefício (STOUT et al. 2006). De acordo com FIRDAUS et al. (2012),
compostos como os derivados de ácido carboxílico (sesquiterpeno), em conjunto com a
quantidade de tricomas na área foliar, são responsáveis pela resistência de plantas a B. tabaci
biótipo B. SU et al. (2015) relataram a diminuição da capacidade de plantas de tomate
infectadas por TYLCV de produzir respostas de defesa à alimentação de B. tabaci biótipo Q.
44
Respostas de defesa induzidas por agentes patogênicos podem alterar os voláteis das
plantas e os compostos terpenoides, os quais desempenham papel fundamental na mediação
vetor-patógeno. Nesse sentido, experimentos com TYLCV em plantas de tomate, com
utilização de cromatografia gasosa [espectrômetro de massa (GCMS)] evidenciaram que
plantas livres da infecção viral emitem mais β-merceno, thymene, β-felandreno, β-cariofileno
e α-humuleno quando comparadas com plantas infectadas por TYLCV e que plantas
resistentes continham maior concentração do monoterpeno que plantas suscetíveis. (FANG et
al., 2013). O geminivírus Tomato yellow leaf curl China virus (TYLCCNV) em plantas de
tabaco (Nicotiana tabacum) suprime dois terpenoides, o que pode explicar a maior preferência
observada de B. tabaci biótipo B pelas plantas infectadas (WANG et al.,2012; ZHANG et al.,
2012; LUAN et al., 2013b). No presente experimento, os dois clones quando infectados por
ToCV apresentaram supressão dos compostos terpenos e também diminuição do conteúdo no
caso de Bach-4 (1,8 cineole e germacrene-D). O fato sugere que a não liberação de compostos
com ação desfavorável aos insetos pode favorecer a preferência da mosca-branca por plantas
infectadas e assim disseminar o vírus.
5.8 Dupla escolha de B. tabaci, na presença de luz e ausência de luz, em resposta aos
voláteis emitidos
O processo de seleção das moscas-brancas pela planta hospedeira pode consistir de
diferentes estágios, mediados por estímulos visuais referentes às cores das folhas (PROKOPY
& OWENS, 1983), olfativos devido a voláteis emitidos, e alimentar, quando o adulto faz a
picada de prova (STÄDLER, 1986). Insetos herbívoros usam, além da via visual, a via
química para localizar a sua planta hospedeira preferencial, para então se alimentar e se
reproduzir (RADCLIFLE & RAGSDALE, 2002; POWELL et al., 2006).
Estudos têm mostrado que a infecção por alguns vírus pode afetar as vias químicas das
plantas e assim torná-las mais ou menos atrativas para os insetos vetores (JIMÉNEZMARTÍNEZ et al., 2004b, MAUCK et al., 2010). Os vírus podem afetar a resposta de defesa
das plantas para o seu próprio benefício de disseminação (ZARATE et al., 2007;
SARMENTO, 2011). Essas alterações induzidas por vírus podem explicar os resultados
obtidos no experimento realizado com o clone ‘Ágata’, envolvendo plantas sadias e infectadas
por ToCV, na presença e na ausência de luz. Sabe-se que, em presença de luz visível, a
mosca-branca pode se orientar tanto por fatores físicos como químicos, ou mesmo uma
combinação de ambos, envolvendo etapas no decorrer de um dado tempo (PANDA &
45
KHUSH, 1995). Para outros insetos, como D.citri Kuwayama, vetor do agente causal do
‘greening’, adultos são atraídos para plantas infectadas por C. Liberibacter asiaticus,
indicando forte influência dos voláteis emitidos pela planta na preferência desse inseto,
embora sem diferenças entre condições de luz e escuro (MANN et al., 2012). De acordo com
os resultados, na presença de luz visível ao inseto, não se observou preferência entre plantas
sadias e infectadas, porém, na ausência de luz visível ocorreu maior atratividade para plantas
infectadas, sugerindo que o inseto foi guiado pela pista olfativa.
46
6
CONCLUSÕES
- Plantas de ‘Ágata’ e Bach-4 infectadas por ToCV são mais atrativas para adultos de B.
tabaci biótipo B entre 4 e 6 horas da infestação;
- A infecção por ToCV em plantas de ‘Ágata’ e Bach-4 não afeta a oviposição de B. tabaci
biótipo B;
- Fêmeas adultas de B. tabaci biótipo B fazem mais picadas de prova (pd) e apresentam maior
duração de atividade na fase floemática, em plantas de ‘Ágata’ infectadas por ToCV;
- Há correlação positiva na movimentação dos adultos de B. tabaci biótipo B de plantas
infectadas por ToCV para plantas sadias em ‘Ágata’;
- Plantas de ‘Ágata’ e Bach-4 infectadas por ToCV induziram os menores tempos de duração
para o ciclo ovo-adulto de B. tabaci biótipo B;
- O tipo de volátil e sua quantidade diferem entre clones (‘Ágata’ e Bach-4) e entre plantas
sadias e infectadas por ToCV;
- A atratividade de adultos de B. tabaci biótipo B para plantas de ‘Ágata’ infectadas por
ToCV, é maior quando comparadas com plantas sadias, na ausência de luz visível ao inseto.
47
7 REFERÊNCIAS BIBLIOGRÁFICAS
ACCOTTO, G.P.; VAIRA, A.M.; VECCHIATI, M.; FINETTI SIALER, M.M.;
GALLITELLI, D.; DAVINO, M. First report of Tomato chlorosis virus in Italy. Plant
Diseases. 85:1208,2001
ALVAREZ-RUIZ, P.; GAMEZ JIMENEZ, C.; LEYVA – LOPEZ, N.E.; MENDEZ –
LOZANO, J. First report of Tomato chlorosis infecting tomato crops in Sinaloa, Mexico.
New Disease Report. 2007
ARIMURA, G.; KOST, C.; BOLAND, W. Herbivore-induced, indirect plant defences.
Biochimica Biophysica Acta 1734 91–111 10.1016/j.bbalip. 2005.03.00, 2005.
BARBOSA, J.C.; TEIXEIRA, A.P.M.; MOREIRA, A.G.; CAMARGO, L.E.A.; BERGAMIN
FILHO, A.; KITAJIMA E.W.; REZENDE, J.A.M. First report of Tomato chlorosis vírus
infecting tomato crops in Brazil. Plant Disease 92: 1709. 2008.
BARBOSA, J.C.; COSTA,H.; GIORIA, R.; REZENDE, J.A.M. Occurrence of Tomato
chlorosis virus in tomato crops in five Brazilian States. Tropical Plant Pathology, 36(4),
2011.
BARBOSA, L.F.; YUKI,V.A.; MARUBAYASHI, J.M.; DE MARCHI, B.R.; PERINI,
F.L.; PAVAN, M.A.; DE BARROS, D.R.; GHANIM, M.; MORIONES, E.; NAVASCASTILLO, J.; KRAUSE-SAKATE, R. First report of Bemisia tabaci Mediterranean (Q
biotype) species in Brazil. Pest Management Sciences. 71:501-04, 2015.
BASS, C.; PUINEAN, M.; ZIMMER, C.T., DENHOLM, I.; FIELD, L.M.; FOSTER, S.P.
The evolution of insecticide resistance in the peach potato aphid Myzus persicae. Insect
Biochem Molecular Biology 51:41–51, 2014.
BERDIALES, B.; BERNAL, J.J.; SAEZ, E.; WOUDT, B.; BEITIA, F.; RODRIGUES–
CEREZO, E.; Occurrence of cucurbit yellow stunting disorder virus (CYSDV) and beet
48
pseudo-yellows virus in cucurbit crops in Spain and transmission of CYDV by two biotypes
of Bemisia tabaci. European. Journal. Plant Pathology. 105, 211–215, 1999.
BERLINGER, M.J.; Host plant resistance to Bemisia tabaci. Agriculture Ecosystems and
Environment. 17(1/2):69-82,1986.
BERNAYS, E.A.; CHAPMAN, R.F. Host-plant selection by phytophagous insects. Chapman
& Hall, New York, 1994.
BERRY, S. D.; FONDONG, V.N.; REY, C. ROGAN, D.; FAUQUET, C. M.; BROWN, J.K.
Molecular evidence for five distinct Bemisia tabaci (Homoptera: Aleyrodidae) geographic
haplotypes associated with cassava plants in Sub Saharan Africa. Annals of the
Entomological Society of America, 97(4):852-859, 2004.
BESE, G.; BÓKA, K.; KRIZBAI, L.; TAKÁCS, A. First report of Tomato chlorosis virus in
tomato from Hungary. Plant Disease, Saint Paul. 95(3):367, 2011.
BETHKE,J.A.; PAINE,T.D.; NUESSLY,G.S. Comparative biology, morphometrics and
development of two populations of Bemisia tabaci (Homopera: Aleyrodidae) on cotton and
poinsettia. Annals of the Entomological Society of America, 84:407-411, 1991.
BLUA, M.J. & PERRING, M.T. Alate Production and Population Increase of Aphid Vectors
on Virus-Infected Host Plants. Oecologia, 92:65-70, 1992.
BONDAR, G. Aleyrodídeos do Brasil (2ª. Contribuição). Boletim do laboratório de
Pathologia Vegetal, 5:37, 1928.
BOSQUE-PÉREZ, N.A.; EIGENBRODE, S.D. The influence of virus-induced changes in
plants on aphid vectors: insights from luteovirus pathosystems. Virus Research, 159:201205, 2011.
BROWN, J.K.; BIRD, J. Whitefly-transmitted geminiviruses and associeted disorders in the
Americas and the Caribbean Basin. Plant Disease, 76(3):220-225, 1992.
49
BROWN, J. K.; FROHLICH, D. R.; ROSELL, R. C. The sweet potato or silver leaf
whiteflies: biotypes of Bemisia tabaci or a species complex. Annual Review of Entomology,
40:511-534, 1995b.
BUCKNER, J.S.; FREEMAN, T.P.; RUUD, R.L.; CHU, C.C.; HENNEBERRY, T.J.
Characterization and functions of the whitefly egg pedicel. Archive Insect Biochemistry
Physiology, 49:22-33, 2002.
BYRNE, D.N. & BELLOWS JUNIOR, T.S. Whitefly biology. Annual review of
Entomology, 36:431-47, 1991.
CAMERON, R.; LANG, E.B.; ANNAN, I.B.; PORTILLO, H.E.; ALVAREZ, J.M. Use of
fluorescence, a novel technique to determine reduction in Bemisia tabaci (Hemiptera:
Aleyrodidae) nymph feeding when exposed to benevia and other insecticides. Journal of
Economic Entomology. 106:597-603, 2013.
CARMO-SOUZA, M.; MORENO, A.; GARZO,E.; FERERES,A. A non-persistently
transmitted-virus induces a pull-push strategy in its aphid vector to optimize transmission and
spread. Virus Research, 186: 38-46, 2014.
CARVALHO DIAS, C.A. Cultura da batata. Campinas: Secretaria de Agricultura e
Abastecimento. Documento Técnico da CATI, 33: 65, 1993.
CASTRO, R.M.; HERNANDEZ, E.; MORA, F.; RAMIREZ, P.; HAMMOND, R.W. First
report of Tomato chlorosis virus in tomato in Costa Rica. Plant Disease, 93:970, 2009.
CHAPMAN, R.F.; BERNAYS, E.A.; SIMPSON, S.J. Attraction and Repulsion of the Aphid,
Cavariella aegopodii, by plant odors. Journal of Chemical Ecology.7:881 -888, 1981.
CHERMENSKAYA, T. D.; PETROVA, M. O.; SAVELIEVA, E. I. Laboratory and field
evaluation of biological active substances of plant origin against greenhouse whitefly,
Trialeurodes vaporariorum Westw (Homoptera: Aleyrodidae). Archives of Phytopathology
Plant Protection, 42(9):864-873, 2009.
50
CHU, C.C.; HENNEBERRY, T.J.; COHEN, A.C. Bemisia argentifolli (Homoptera:
Aleyrodidae): host preference and factors affecting oviposition and feeding sites preference.
Environmental Entomology, 24(2):354-360, 1995.
CHU, C.C.; FREEMAN, T.P.; NATWICK, E.T.; BUCKER, J.S.; NELSON, D.R.;
HENNEBERRY, T.J. Bemisia argentifolii adult, nymph and egg densities and egg
distribution on selected upland cottons. Journal of Entomology, 35:39-47, 2000ab.
COHEN, S.; DUFFUS, J.E.; LIU, H.Y.; A new Bemisia tabaci biotype in the south western
united states and its role in silver leaf of squash and transmission of lettuce infectious yellows
virus. Phytopathology, 82:86–90,1992
COHEN, A.C.; HENNEBERRY, T.J.; CHU, C.C. Geometric relationships between whitefly
feeding behavior and vascular bundle arrangements. Entomologia Experimentalis et
Applicata, 78:135-142, 1996.
COSTA, A.S.; COSTA, C.L.; SAUER, H.F.G. Surto de mosca-branca em culturas do Paraná
e São Paulo. Anais da Sociedade Entomologia do Brasil. Itabuna. 2(1):20-30, 1973.
COSTA, A.S.; RUSSELL, L.M. Failure of Bemisia tabaci to breed on cassava plants in Brasil
(Homoptera: Aleyrodidae). Ciência Cultivar.27:388-90,1975.
COSTA, H.S.; BROWN, J.K. Variability in biological characteristics, isozyme patterns and
virus transmission among populations of Bemisia tabaci Genn. in Arizona. Phytopathology.
80(10):888, 1990.
DE BARRO, P. J.; LIU, S.; BOYKIN, L.M.; DINSDALE, A. B. Bemisia tabaci: A statement
of species status. Annual Review of Entomology, 56:1-19, 2011.
DEMPSEY, D.A.; SHAH, J.; KLESSIG, D.F. Salicylic acid and disease resistance in plants.
Critical Review in Plant Science, 18:547-575, 1999.
51
DOVAS, C.I.; KATIS, N.I.; AVGELIS, A.D. Multiplex detection of crinivirus associated
with epidemics of a yellowing disease of tomato in Greece. Plant disease, 86:1345-1349,
2002
EIGENBRODE, S.D.; TRUMBLE, J.T. Antibiosis to bett armyworn (Spodoptera exigua) in
Lycopersicon acessions. Horticultural Science, 28(9):932-934, 1993.
EIGENBRODE, S.D.; TRUMBLE, J.T.; MILLAR, J.G.; WHITE, K.K. Topical toxicity of
tomato sesquiterpenes to the beet armyworm and the role of these compounds in resistance
derived from an accession of Lycopersicon hirsutum f. typicum. Journal Agricultural and
Food Chemistry, 42(3):807-810, 1994.
EIGENBRODE, S.D.;DING, H.; SHIEL, P.; BERGER, P.H. Volatiles from potato plants
infected
with
potato
leafroll
virus
attract
and
arrest
persicae (Homoptera: Aphididae). Proceedings of the Royal
the
virus
vector, Myzus
Society of London
B:
Biological Sciences, 269:455–460, 2002.
FANG, Y.; JIAO,X. G.; XIE, W.; WANG, S. L.; WU, Q. J.; SHI, X. J.;CHEN, G.;
SU,Q.;YANG, X.; PAN, H. P.; ZHANG, Y. J. Tomato yellow leaf curl virus alters the host
preferences of its vector Bemisia tabaci. Scientific Report. 3:2876, 2013.
FAUQUET, C.M.; MAYO, M.A.; MANILOFF, J.; DESSELBERGER, U.; BALL, L.A. Virus
taxonomy: 1sth report of the International Committee on Taxonomy of Viruses. London:
Elsevier Academic Press. 2005.
FERERES, A.; PEREZ, P.; GAMENO, C.; PONZ, F. Transmission of Spanish pepper-PVY
isolates by aphid vectors: epidemiological implications. Environmental Entomology.
22:1260-1265.1993.
FERERES, A. The role of aphid salivation in the transmission of plant viruses.
Phytoparasitica, 35(1):3-7, 2007.
52
FERNANDES, F.R.; De ALBUQUERQUE, L.C.; BOITEUX,L.S.; De AVILA, A.C.;
INOUE-NAGATA,A.K. Diversity and prevalence of Brazilian bipartite begomovirus species
associated to tomatos. Virus Genes.36:251-258.2008.
FILGUEIRA,F.A.R. Novo manual de olericultura: Agrotecnologia moderna na produção e
comercialização de hortaliças. Ed. Viçosa: Editora UFV.402.2000.
FILGUEIRA,F.A.R. Novo manual de olericultura: Agrotecnologia moderna na produção e
comercialização de hortaliças. 2°Ed. Viçosa: Editora UFV.412.2003.
FIRDAUS, S.; HEUSDEN, A. W.; HIDAYATI, N.; SUPENA, E. D. J; VISSER, R. G. F.;
VOSMAN, B. Resistance to Bemisia tabaci in tomato wild relatives. Euphytica, 187:31-45,
2012.
FONSECA, M. E. N.; BOITEUX, L.S.; ABREU, H.; NOGUEIRA, I.; PEREIRACARVALHO, R. C. Physalis angulata: A New Natural Host of Tomato chlorosis virus in
Brazil. Plant Disease. 97(5):692, 2013.
FONT, M. I.; JUÁREZ, M.; MARTÍNEZ, O.; JORDÁ, C. Current status and newly
discovered natural hosts of Tomato infectious chlorosis virus and Tomato chlorosis virus in
Spain. Plant Disease, 88:82, 2004.
FONTES, F.H.M.; COLOMBO, C.A.; LOURENÇÃO, A.L. Caracterização molecular e
divergência genética de Bemisia tabaci (Genn.) (Hemiptera: Aleyrodidae) em diferentes
culturas e locais de cultivo. Neotropical Entomology, 39:221-226, 2010.
FONTES, F.H.M.; COLOMBO, C.A.; LOURENÇÃO, A.L. Structure of genetic diversity of
Bemisia tabaci (Genn.) (Hemiptera: Aleyrodidae) populations in Brazilian crops and
locations. Scientia Agricola, 69:47-53, 2012.
FORBES, A.R . The stylets of the green peach aphid, Myzus persicae (Homoptera:
Aphididae). The Canadian Entomologist, 101:31-41, 1969.
53
FORTES, I. M.; NAVAS-CASTILLO, J. Potato (Solanum tuberosum) is an experimental and
natural host of Tomato chlorosis virus. 3rd Conference of the International Working
Group on Legume and Vegetable Viruses. Ljubljana, Slovenia, 56. 2008.
FORTES, I. M.; MORIONES, E.; NAVAS-CASTILLO, J. Tomato chlorosis virus in pepper:
prevalence in commercial crops in south-eastern Spain and symptomatology under
experimental conditions. Plant Pathology. doi:10.1111/j.1365- 3059.2011.02584.x.2012
FREITAS, J.A. Resistência genética de tomateiro Lycopersicon sp. à mosca branca Bemisia
spp. mediada por zingibereno contido em tricomas glandulares. Lavras, 1999. (Doctoral
Thesis in Plant Breeding) - Universidade Federal de Lavras.
FREITAS, D. M. S. ; NARDIN, I. ; SOUZA-DIAS, J. A. C. ; Rezende, J.A.M. . Detecção do
Tomato chlorosis virus em tubérculos de batata no estado de Goiás, Brazil. In: Congresso
Nacional de Virologia, 2011, Atibaia-SP. Anais do XXII Encontro Nacional de Virologia.
Virus Rewiews & Research, v. 16, 2011.
FREITAS, D. M. S.; NARDIN, I.; SHIMOYAMA, N.; SOUZA-DIAS, J. A. C.; REZENDE,
J. A. M. First report of Tomato chlorosis virus in potato in Brazil. Plant Disease, 96,
593.2012.
GAFFNEY, T.; FRIEDRICH, L.; VERNOOIJ, B.; NEGROTTO, D.; NYE, G.; UKNES, S.;
WARD, E.; KESSMANN, H.; RYALS, J. Requirement of salicylic acid for the induction of
systemic acquired resistance. Science, 261:754-756, 1993.
GALLO, D.; NAKANO, O.; SILVEIRA NETO, S.; CARVALHO, R.P.L.; BAPTISTA, G.C.;
BERTI FILHO, E.; PARRA, J.R.P.; ZUCCHI, R.A.; ALVES, S.B.; VENDRAMIM, J.D.;
MARCHINI, L.C.; LOPES J.R.S.; OMOTO, C. Entomologia Agrícola, FEALQ. 920, 2002.
GÁRZO, E.I.G. Selección y caracterización de germoplasma de melón resistente a
Aphisgossypii (Glover) y a los virus que transmite. Tesis Doctoral presentada a la Universidad
Politécnica de Madrid, Escuela Técnica Superior de Ingenieros Agrónomos. Departamento de
Producción Vegetal: botánica y protección vegetal, 201pp., 2002.
54
GELMAN, D.B.; BLACKBURN, M.B.; HU, J.S.; GERLING, D. The nymphal-adult molt of
the silverleaf whitefly (Bemisia argentifolii): timing, regulation, and progress. Archive Insect
Biochemistry Physiology, 51:67-79, 2002.
GERLING, D. Whitflies: their bionomics pest satatus and management. Intercept Ltd,
Andover. 1990.
GERSHENZON, J.; CROTEAU, R. Terpenoids. Herbivores :Their interactions with
secondary metabolites, Vol.1: The chemical participants, 2nd ed., G.A. Rosenthal and M.R.
Berenbaum, eds., Academic press, 165-219, 1992.
GILL, R.J. The morphology of whiteflies. In: GERLING, D. (Ed.) Whiteflies: their
bionomics, pest status and management. Andover: Intercept.13-46, 1990.
HARBORNE, J. B. The flavonoids: advances in research since 1986. London: Chapman &
Hall, 676 p, 1994.
HOFFMANN-CAMPO, C. B.; MOSCARDI, F.; CORRÊA- FERREIRA, B.S.; OLIVEIRA,
L.J.; SOSA-GÓMEZ, D.R.; PANIZZI, A.R.; CORSO, I.C.; GAZZONI, D.L.; OLIVEIRA,
E.B. Pragas da soja no Brasil e seu manejo integrado. Circular Técnica Embrapa Soja,
30:1-70, 2000.
HOLBROOK, F.R. Aldicarb and thiofanox: effect on the feeding activity of green peach
aphids. Journal of Economic Entomology,70:742–744.1977.
IBGE Grupo de Coordenação de Estatísticas Agropecuárias - GCEA/IBGE, DPE, COAGRO Levantamento Sistemático da Produção Agrícola, Março 2015
INBAR, M.; GERLING, D. Plant-mediated interactions between whiteflies, herbivores, and
natural enemies. Annual Review of Entomology, 53: 431-448,2008.
INGWELL, L.L.; EIGENBRODE, S.D.; BOSQUE-PÉREZ, N.A. Plant viruses alter insect
behavior to enhance their spread. Science Report, 2:1-6, 2012.
55
JIMÉNEZ-MARTÍNEZ, E.S.; BOSQUE-PÉREZ, N.A.; BERGER, P.H.; ZEMETRA, R.S.;
DING, EIGENBRODE, S. D. Volatile cues influence the response of Rhopalosiphum
padi (Homoptera: Aphididae) to barley yellow dwarf virus infected transgenic and
untransformed wheat. Environmental Entomology. 33:1207-1216, 2004b.
JONES, D.R. Plant viruses transmitted by whiteflies. European Journal of Plant Pathology.
109:195-219, 2003.
KARBAN, R.; BALDWIN, I.T. Induced responses to herbivory. University of Chicago
Press, 1997.
KESSLER, A.; BALDWIN, I.T. Defensive function of herbivore induced plant volatile
emissions in nature. Science 291:2141-2144, 2001.
LA POINTE, S.L. & TINGEY, W.M. Feeding response of the green peach aphid
(Homoptera: Aphididae) to potato glandular trichhomes. Journal Economical Entomology,
77:386-389.1984.
LARA, F.M. Princípios de resistência de plantas a insetos. 2 ed. São Paulo: ED. Ícone.
336p, 1991.
LEONARD,S.H.; HOLBROOK,R., Minimum acquisition and transmission times for potato
leafroll virus by green peach aphid. Annals of the Entomological Society of American. 710:
493-495. 1978.
LIU, S. S.; COLVIN, J.; DE BARRO, P. J. Species concepts as applied to the whitefly
Bemisia tabaci systematics: How many species are there? Journal of Integrative
Agriculture, 11: 176-186, 2012.
LIU, B.; PREISSER, E.L.; CHU, D.; PAN, H.; XIE, W.; WAN, S.; WU, Q.; ZHOU, X.;
ZHANG, Y.. Multiple forms of vector manipulation by a plant-infecting virus: Bemisia
tabaci and Tomato yellow leaf curl virus. Journal of Virology, 87: 4929-4937, 2013.
56
LOPES, C.A. In: LOPES,C.A.;BUSO, J.A. Cultivo da Batata (Solanum tuberosum L.)
Brasilia: Embrapa/CNPH, Boletim Técnico, 8:35, 1997.
LÓPEZ, M.A. Mosca blanca: descripcion, ecologia, daños y estrategias para el manejo. INIA:
INIA (Ed.). Equador, 1995. 16 p. (Boletín Divulgativo, 253).
LOURENÇÃO, A.L.; NAGAI, H. Surtos populacionais de Bemisia tabaci no Estado de São
Paulo. Bragantia, 53(1):53-59,1994.
LOURENÇÃO, A. Histórico e danos de Bemisia argentifolii no Brasil. In: Resumos do XVI
Congresso Brasileiro de Entomologia, 8-9, 1997.
LOURENÇÃO, A.L.; FANCELLI, M.; VENDRAMIM, J.D.; DIAS, C.T.S. Atratividade e
preferência para oviposição de Bemisia tabaci (Gennadius) (Hemiptera: Aleyrodidae) biótipo
B em genótipos de tomateiro. Neotropical Entomology, 32(2), 2003.
LOURENÇÃO, A.L.; VENDRAMIN, J.D.; FUGI, C.G.Q.; HERNÁNDEZ, C.R. Resistência
de plantas de importância económica a la mosca blanca Bemisia tabaci biótipo B. In: Ortega,
A.L.D. (ed.) Temas selectos para el manejo integrado. México, Colégio de Postgraduados,
2008.
LOURO, D.; ACCOTTO, G.P.; VAIRA, A.M. Occurrence and diagnosis of Tomato chlorosis
vírus in Portugal. European Journal of Plant Pathology, 106:589-592, 2000.
LOZANO, G.; MORIONES, E.; NAVAS-CASTILLO, J. First report of sweet pepper
(Capsicum annuum) as a natural host plant for Tomato chlorosis virus. Plant Disease, 88:224,
2004.
LUAN, J. B.; WANG, Y. L.; WANG, J.; WANG, X. W.; LIU, S. S. Detoxification activity
and energy cost is attenuated in whiteflies feeding on Tomato yellow leaf curl China virusinfected tobacco plants. Insect Molecular Biology, 22: 597-607, 2013a.
57
LUAN, J. B.;YAO, D. M.; ZHANG, T.;WALLING, L. L.; YANG, M.;WANG, Y. J.;LIU, S.
S. Suppression of terpenoid synthesis in plants by a virus promotes its mutualism with
vectors. Ecology Letters 16: 390-398, 2013b.
MALUTA, N. K. P ; GARZO, E ; MORENO, A ; LOPES, J. R. S ; FERERES, A . Tomato
Yellow Leaf Curl Virus Benefits Population Growth of the Q Biotype of Bemisia tabaci
(Gennadius) (Hemiptera: Aleyrodidae). Neotropical Entomology, 43:385-392, 2014.
MANN, R.S.; ALI, J.G.; HERMANN, S.L.; TIWARI, S.; PELZ-STELINSKI, K.S.;
ALBORN, H.T. Induced Release of a Plant-Defense Volatile ‘Deceptively’ Attracts Insect
Vectors to Plants Infected with a Bacterial Pathogen. PLoS Pathogoly, 8(3), 2012.
MARKHAM, K.R. Techniques od flavonoid identification, Biological Techniques Series.
Academic Press: London, 1982.
MARTÍN, B.; COLLAR, J.L.; TJALLINGII, W.F.; FERERES, A. Intracellular ingestion and
salivation by aphids may cause the acquisition and inoculation of non-persistently transmitted
plant viruses. Journal Genetics Virology, 78:2701-2705, 1997.
MARTIN,J. H.; MOUND,L.A. An annotated check list of whiteflies (Insecta: Hemiptera:
Aleyrodidae). Zootaxa, 1492: 1-84, 2007.
MARTINEZ-ZUBIAUR, Y.; FIALLO-OLIVÉ, E.; CARRILLO-TRIPP, J.; RIVERABUSTAMANTE, R. First report of Tomato chlorosis vírus infecting tomato in single and
mixed infectious with Tomato yellow leaf curl virus in Cuba. Plant Disease, Saint
Paul..92(5):836, 2008.
MARUBAYASHI, J.M.; YUKI, V.A.; ROCHA, K.C.G.; MITUTI, T.; PELEGRINOTTI,
F.M. At least two indigenous species of the Bemisia tabaci complex are present in Brazil.
Journal Applied Entomology, 137:113–121, 2013.
MAUCK, K.E; DE MORAES, C.M; MESCHER, M.C. deceptive chemical signals by a plant
virus attract insect vectores to inferior hosts. Proceeding of National Academy of Science of
the USA, 1(1):1-6, 2010.
58
MAUCK, K.; BOSQUE-PÉREZ, N.A.; EIGENBRODE, S.D.; DE MORAES, C.;
MESCHER, M. Transmission mechanisms shape pathogen effects on host–vector
interactions:evidence from plant viruses. Functional Ecology, 26:1162-1175, 2012.
MARTELLI,
G.P.;
GHANEM-SABANADZOVIC,
N.A.;
AGRANOVSKY,
A.A.;
RWAHNH, M.A.; DOLJA, V.V.; DOVAS, C.I.; FUCHS, M.; GUGERLI, J.S.;HU, J.S.;
JELKMANN, W.; KATIS, N.I.; MALIOGKA, V. I.; MELZER, M.J.; MENZEL, W.;
MINAFRA, A,; ROTT, M.E.; ROWHANI, A.; SABANADZOVIC, S.; SALDARELLI, P.
Taxonomic revision of the family Closteroviridae with special reference to the gravepine
leaffroll-associated members of the genus Ampelovirus and the putative species unassigned to
the family. Journal of Plant Pathology, 94:7-19, 2012.
MC LEAN, D. L. & KINSEY, M. G. A technique for electronically recording aphid feeding
and salivation. Nature, 202:1358-1359, 1964.
McKENZIE,C.L. Effect of Tomato mottle virus (ToMOV) on Bemisia tabaci biotype b
(homoptera: aleyrodidae) oviposition and adult survivorship on healthy tomato. Florida
Entomological Society, 85(2):367-368, 2002.
MEDINA-ORTEGA, K.J.; BOSQUE-PÉREZ, N.A.; NGUMBI, E.; JIMÉNEZ-MARTÍNEZ,
E.S.; EIGENBRODE, S.D. Rhopalosiphum padi (Hemiptera: Aphididae) responses to volatile
cues from barley yellow dwarf virus-infected wheat. Environmental Entomology, 38:836845, 2009.
MICHEREFF-FILHO, M.; MACHINI, W. D. B.; MENDONÇA, J. L.; FONSECA, M. E.;
FERNANDES-ACIOLI, N. A. N.; BOITEUX, L. S. Resposta à mosca-branca (Bemisia
tabaci) e ao Tomato severe rugose virus de acessos de Solanum subgênero Leptostemonum.
Horticultura Brasileira, 30:440-445, 2012.
MORENO-DELAFUENTE, A.; GARZO, E.; MORENO, A.; FERERES, A. A Plant Virus
Manipulates the Behavior of Its Whitefly Vector to Enhance Its Transmission Efficiency and
Spread. PLoS ONE 8(4): e61543, 2013. doi:10.1371/journal.pone.0061543
59
MORRIS, J.; STEEL, E.; SMITH, P.; BOONHAM, N.; SPENCE, N.;BARKER, I. Host range
studies for Tomato chlorosis virus, and Cucumber vein yellowing virus transmitted by
Bemisia tabaci (Gennadius). European Journal of Plant Pathology, 114, 265–273, 2006.
MOUND, L.D.; HALSEY, S.H. Whitefly of the world: a systematic catalogue of the
Aleyrodidae (Homoptera) with host plant and natural enemy data. New York, British Mus.
National History. and John Wiley & Sons, 340, 1978.
NAVAS-CASTILLO, J.; CAMERO,R.; BUENO, M.; MORIONES, E. Severe yellowing
outbreaks in tomato in Spain associated with infections of Tomato chlorosis virus. Plant
Diseases, 84:835-837, 2000.
NAVAS-CASTILLO, J.; OLIVÉ, E.F.; CAMPOS, S.C. Emerging virus diseases transmitted
by whiteflies. Annual Review of Phytopathology, 49: 219-248, 2011.
O’DONNELL P.J.; SCHMELZ, E.A.; MOUSSATCHE, P.; LUND, S.T.; JONES, J.B.;
KLEE, H.J. Susceptible to intolerance — a range of hormonal actions in a susceptible
Arabidopsis pathogen response. Plant Journal, 33:245-257, 2003.
OLIVEIRA, C. M.; AUAD, A. M.; MENDES, S. M.; & FRIZZAS, M. R. Economic impact
of exotic insect pests in Brazilian agriculture. Journal of Applied Entomology, 137, 1-15,
2013. doi: 10.1111/jen.1 2013
ORLANDO, A. & SILBERSCHMIDT, K. Estudos sobre a transmissão da doença de vírus de
solanáceas “necrose das nervuras” por afídeos e algumas relações entre esse vírus e seu
principal vector. Arquivos Instituto Biológico.16:133–152.1945.
PAN, H. P.; LI, X. C.; GE, D. Q.; WANG, S. L.; WU, Q. J.; XIE, W.; JIAO, X. G.; CHU, D.;
LIU, B. M.; XU, B. Y.; ZHANG, Y. J. Factors affecting population dynamics of maternally
transmitted endosymbionts in Bemisia tabaci. PloS one 7(2): e30760, 2012.
PANDA , N.; KHUSH, G.S. Host plant resistance to insects. CABI, 431, 1995.
60
PEREIRA, J.E.S & FORTES, G.R.L. Organogênese de ápices meristemáticos de batata em
meios de isolamento e multiplicação in vitro. Horticultura. Brasileira, 22(2):197-201, 2004.
.
PERRING, T. M. The Bemisia tabaci species complex. Crop Protection 20: 725-737, 2001.
POLSTON, J.E.; DE BARRO, P.; BOYKIN, L. M. Transmission specificities of plant viruses
with the newly identified species of the Bemisia tabaci species complex. Pest Management
Science, 1547- 1552, 2014.
POWELL, G.; TOSH, C.R.; HARDIE, J. Host plant selection by aphids: behavioral,
evolutionary, and applied perspectives. Annual Review Entomology, 51:309-330, 2006.
PRADO, J.C.; PEÑAFLOR, M.F.G.V.; CIA, E.; VIEIRA, S.S.; SILVA, K.I.; CARLINIGARCIA, L.A.; LOURENÇÃO, A.L. Resistence of cotton genotypes with diferente leaf color
and trichome density to Bemisia tabaci biotype B. Journal of Applied Entomology (aceito
para publicação), 2015.
PRICE, J.F.; TABORSKY, D. Movement of immature Bemisia tabaci (Homoptera:
Aleyrodidae) on poinsettia leaves. Florida Entomologist, 75(1):151-153, 1992.
PROKOPY, R.J.; OWENS, E.D. Visual detection of plants by herbivorous insects. Annual
Review of Entomology, 28: 337-364, 1983.
RADCLIFFE ,E.; RAGSDALE, D. Aphid-transmitted potato viruses: the importance of
understanding vector biology. American Journal of Potato Research, 79: 353–386, 2002.
RAHIMI, F.R.; CARTER, C.D. Inheritance of zingiberene in Lycopersicon. Theoretical and
Applied Genetics, 87:593-597, 1993.
RAJABASKAR D.; BOSQUE-PÉREZ N.A.; EIGENBRODE S.D. Preference by a virus
vector for infected plants is reversed after virus acquisition. Virus Research,186: 32-37,
2014.
61
RAMAN, K.V.; TINGEY, W.M.; GREGORY, T. Potato glycoalkaloids: effect on survival
and feeding behavior of the potato lefhopper. Journal of Economic Entomology, 72:337341.1979.
ROCHA, A.B.O.; LOURENÇÃO, A.L.; MIRANDA-FILHO, H.S.; HAYASHI, P.C.R.;
RAMOS, V.J. 2012. Resistência de clones de batata a Bemisia tabaci biótipo B. Horticultura
Brasileira, 30:32-38. 2012.
RODRIGUÉZ-LOPÉZ, M.J.; E. GARZO, J.P.; BONANI, A. FERERES, R. FENÁNDEZMUÑOZ & E. MORIONES. 2011. Whitefly resistance traits derived from the wild Tomato
Solanum pimpinellifolium affect the spread of Tomato yellow leaf curl virus.
Phytopathology, 101 1191-1201.2011
RUBINSTEIN, G.; CZOSNEK, H. Long-term association of tomato yellow leaf curl virus
(TYLCV) with its whitefly vector Bemisia tabaci: Effect on the insect transmission capacity,
longevity and fecundity. Journal General Virology, 78, 2683–2689, 1997.
SARMENTO, R. A. A herbivorous mite down-regulates plant defence and produces web to
exclude competitors. PLoS One 6, e23757, 2011.
SARRIA, E.; CID, M.; GARZO, E.; FERERES, A. Workbook for automatic paramenter
calculation of EPG data. Computers and Electronics in Agriculture, 67:35-42, 2009.
SEVEG, L.; WINTERMANTEL, W.M.; POLSTON, J.E.; LAPIDOT, M. First report of
Tomato chlorosis virus in Israel. Plant Disease, 88:1160. 2004
SHAH, J.; KLESSIG, D.F: Salicylic acid: signal perception and transduction. In:
Biochemistry and Molecular Biology of Plant Hormones, 33:513-541, 1999.
SILVA, M.S.; LOURENÇÃO, A.L.; SOUZA-DIAS, J.A.C.; MIRANDA FILHO, H.S.;
RAMOS, V.J.; SCHAMMASS, E.A. Resistance of potato genotypes (Solanum spp.) to
Bemisia tabaci biotype B. Horticultura Brasileira 26:221-226.2008.
62
SKINNER, R. H.; COHEN, A. C. Phosphorous nutrition and leaf age effects on sweetpotato
whitefly (Homoptera: Aleyrodidae) host selection. Environmental Entomology, 23:693-698,
1994.
SOLÓRZANO-MORALES, A.; BARBOZA, N.; HERNÁNDEZ, E.; MORA-UMAÑA, F.;
RAMÍREZ, P.; HAMMOND, R.W. Newly discovered natural hosts of Tomato chlorosis virus
in CostaRica. Plant Disease, 95:497, 2011.
SOTTORIVA, L. D. M.; LOURENÇÃO, A. L.; COLOMBO, C. A. Performance of Bemisia
tabaci (Genn.) Biotype B (Hemiptera: Aleyrodidae) on weeds. Neotropical Entomology,
43:574-581, 2014.
SOUZA, A.P.; VENDRAMIN,J.D. Efeitos de estratos aquosos de meliáceas sobre Bemisia
tabaci biótipo B em tomateiros. Bragantia, 59(1):173-179, 2000.
SOUZA-DIAS, J.A.C. Viroses de batata e suas implicações na produção de batata semente no
estado de São Paulo. Summa Phytopathology, 21: 264-266, 1996.
SOUZA-DIAS, J.AC.; IAMAUTI, M.T. Doenças da Batateira (Solanum tuberosum). Manual
de Fitopatologia. Cap.16. 4. Ed. São Paulo: Agronômica Ceres, 2005.
SOUZA-DIAS,J.AC.; SAWASAKI,H.E.; ELIAS,L.M.; MALUF,H. Tomato severe rugose
virus: Another Begomovirus causing Leaf Deformation and Mosaic Symptoms on Potato in
Brazil. Plant Disease, 92:487-487, 2008.
SPSS Inc., 2010. IBM Statistics SPSS 19.0 Package for Windows. SPSS, Chicago, USA.
STÃDLER, E. Oviposition and feeding stimuli in leaf surface waxes. In Insects and the plant
surface. B. Juniper and R. Southwood (eds); Edward Arnold Publisher, 105-121, 1986.
STOUT, M. J.; THALER, J. S.; THOMMA, B. P. H. J. Plant-mediated interactions between
pathogenic microorganisms and herbivorous arthropods. Annual Review Entomology,
51:663–689, 2006.
63
SU, Q.; PREISSER, E.L.;XIE, W.; WANG, S.L.;WU, Q.J.;ZHANG, Y.J. "Manipulation of
host quality and defense by a plant virus improves performance of whitefly vectors." Journal
of Economic Entomology, 108(1):11-19, 2015.
SUMMERS, C.G.; NEWTON, A.S.; ESTRADA, D. Intraplant and interplant movement of
Bemisia argentifolii (Homoptera: Aleyrodidae) crawlers. Environment of Entomology,
25:1360-1364, 1996.
TAIZ, L.; ZEIGER, E. Metabólitos secundários e defesa vegetal. Fisiologia Vegetal. 3ed–
Porto Alegre: Artmed, 13:309-332, 2004.
TJALLINGII, W.F. Continuos recording of stylet penetration activites by aphids, p.89-99. In
Campbell, R.K.; Eikenbary, R.D. (eds) Aphid-plant genotype interaction. Elsevier, 386,
1990.
TOLOY, S.R. Período mínimo para a aquisição do Tomato severe rugose virus (ToSRV) por
Bemisia tabaci biótipo B em tomateiros e identificação de sítios de aquisição do vírus.
Dissertação de Mestrado apresentada a Universidade de São Paulo, Escola Superior de
Agricultura Luiz de Queiroz, 2015.
TSAI, W.S.; SHIH, S.L.; GREEN, S.K.; HANSON, P.; LIU, H.Y. First report of the
occurrence of Tomato chlorosis virus and Tomato infectious chlorosis virus in Taiwan. Plant
Disease, 83:311, 2004.
TURLINGS, T.C.J.; TUMLINSON, J.H.; LEWIS, W.J. Exploitation of herbivore induced
plant odors by host –seeking parasitic wasps. Science, 250: 1251-1253, 1990.
TURLINGS, T.C.J.; LOUGHRIN, J.H.; McCALL, P.J.; ROSE, U.S.R.; LEWIS, W.J.;
TUMLINSON, J.H. How caterpillar-damaged plants protect themselves by attracting parasitic
wasps. Proceeding of the National Academy of Sciences, 92: 4169-4174, 1995.
VALLE, G.E.; LOURENÇÃO, A.L.; ZUCCHI, M.I.; PINHEIRO, J.B.; DE ABREU, A.G.
Population variability of Bemisia tabaci (Genn.) in different hosts. Genetics Molecular
Research, 12(4):4615-4624, 2013.
64
VAN LENTEREN, J. C. & NOLDUS, L. P. J. J. Whitefly–plant relationships: Behavioural
and ecological aspects. In ‘‘Whiteflies: Their Bionomics, Pest Status and Management’’
(D. Gerling, Ed.), 47–89, 1990.
VILLAS BÔAS, G.L.; FRANÇA, F.H.; MACEDO, N. Potencial biótico da mosca-branca
Bemisia argentifoliia diferentes plantas hospedeiras. Horticultura Brasileira, 20(1):7179.2002.
WALKER, G.P.; PERRING, T.M. Feeding and oviposition behavior of whiteflies
(Homoptera: Aleyrodidae) interpreted from AC electronic feeding monitor waveforms.
Annals of the Entomological Society of America, 87:363-374, 1994.
WALKER, G.P.; PERRING, T.M.; FREEMAN, T.P. Life history, functional anatomy,
feeding and mating behavior. Bemisia: bionomics and management of Global Pest, 4:109161, 2010.
WANG, J.; BING, X.L.; LI, M.; YE, G.Y.; LIU, S.S. Infection of tobacco plants by a
begomovirus improves nutritional assimilation by a whitefly. Entomology Experimentalis et
Applicata, 144: 191-201, 2012.
WESTON, P.A.; JOHNSON, D. A.; BURTON, H.T.; SNYDER, J.C. Trichome secretion
composition, trichome densities, and spider mite resistance of tem accessions of Lycopersicon
hirsutum. Journal American Society Horticultural Science, 114(3):492-498, 1989.
WISLER, G.C.; LI, R.H.; LIU, H.Y.; LOWRY, D.S.; DFFUS, J.E. Tomato chlorosis virus: a
new whitefly transmitted phloem-limited, bipartite closterovirus of tomato. Phytopathology,
88:402-409, 1998.
WINTERMANTEL, W.M.; POLSTON, J.E.; ESCUDERO,J.; PAOLI, E.R. First report of
Tomato chlorosis vírus in Puerto Rico. Plant Diseases, 85:228, 2001.
WINTERMANTEL, W.M.; WISLER, G.C.; ANCHIETA, A.G.; LIU, H.Y.; KARASEV,
A.V.; TZANETAKIS, I.E. The complete nucleotide sequence and genome organization of
Tomato chlorosis virus. Archive Virology, 150:2287-2298, 2005.
65
WINTERMANTEL, W.M.; WISLER, G.C. Vector specificity, hoste range, and genetic
diversity of Tomato chlorosis virus. Plant Diseases, 90:814-819, 2006.
WU, Y.; DAVIS, T.S.; EIGENBRODE, S.D. Aphid behavioral responses to virus-infected
plants are similar despite divergent fitness effects. Entomologia Experimentalis et
Applicata, 3:246-255, 2014.
XU, C. X.; WANG, X. M.; STANSLY, P. A.; REN, S. X. Behavioral interactions between
Bemisia
tabaci (Homoptera: Aleyrodidae) and Tetranychus truncatus (Acarina:
Tetranychidae). Florida Entomolgy, 94:800-808, 2011.
ZARATE, S. I.; KEMPEMA, L. A.; WALLING, L. L. Silverleaf whitefly induces salicylic
acid defenses and suppresses effectual jasmonic acid defenses. Plant Physiology, 143:866875, 2007.
ZEIDAN, M.; GREEN, S.K.; MAXWELL, D.P.; NAKHALA, M.K.; CZOSNEK, H.
Molecular analysis of whitefly-transmitted tomato geminiviruses from Southeast and East
Asia. Tropical Agricultural Research and Extension, 1:107-115, 1998.
ZHANG, T.; LUAN, J. B.; QI, J. F.; HUANG, C. J.; LI, M.; ZHOU, X. P.; LIU, S. S.
Begomovirus-whitefly mutualism is achieved through repression of plant defences by a virus
pathogenicity factor. Molecular Ecology, 21:1294-1304, 2012.
66