RIDA®QUICK Malaria
Código do produto: N7006
Código do produto: N7007
R-Biopharm AG, An der neuen Bergstrasse 17, D-64297 Darmstadt, Alemanha
Tel.: +49 (0) 61 51 81 02-0, Fax: +49 (0) 61 51 81 02-20
C
1. Uso previsto
Para diagnósticos in vitro. O RIDA®QUICK Malaria é um teste rápido imunocromatográfico para
a detecção qualitativa de antígenos Plasmodium falciparum (P.f.), Plasmodium vivax (P.v.),
Plasmodium ovale (P.o.) e Plasmodium malariae (P.m.) em sangue total. É destinado ao rápido
diagnóstico da malária assim que os primeiros sintomas clínicos aparecem.
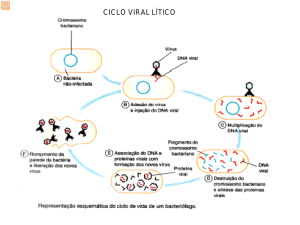
2. Sumário e explicação do teste
Em diversos países tropicais, a malária ainda é um grave problema e, em algumas regiões, é
um problema que continua a crescer. Há uma diferenciação entre os três diferentes tipos de
malária. O mais perigoso é uma forma causada pelo patógeno Plasmodium falciparum.
Conhecida como malária tropical, esta forma é quase que exclusivamente responsável por
mortes e causa da maioria das doenças de malária importadas para os países industriais. Os
patógenos dos outros tipos de malária são Plasmodium vivax e Plasmodium ovale (malária
terciária) bem como Plasmodium malariae (malária quaternária). Nos anos recentes, o
Plasmodium knowlesi foi incluído como o quinto patógeno da malária. Ele possui um potencial
similar para a doença como P. falciparum e não pode ser diferenciado de P. malariae
microscopicamente e, geralmente, é confundido com ele.
Todos os patógenos da malária são transmitidos através da mordida de um mosquito fêmea
anófelo. O período de incubação pode variar entre alguns dias (malária tropica) e muitos anos
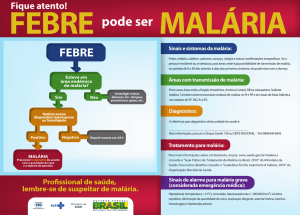
(malária quaternária). Os sintomas da malária são relativamente atípicos. Eles geralmente
incluem sintomas similares aos da gripe, sem os sinais de um resfriado comum. Estes, por sua
vez, frequentemente incluem surtos de febre com calafrios, dores de cabeça, dores nas costas
e dores no membro. Nos casos de evolução atípica, os sintomas podem ser, na maioria,
sintomas gastrointestinais. Pode ocorrer pouca ou a ausência de febre. No caso da malária
tropical, podem ocorrer complicações fatais após o sexto dia da doença, e elas podem ser
evitadas através de terapia eficaz e precoce. Este é o motivo pelo qual um diagnóstico precoce
é indispensável.
A profilaxia para a malária é composta pela prevenção contra as mordidas do mosquito e, se
necessário, a administração de medicamento para malária em dosagens preventivas ou
terapêuticas. Contudo, já foram desenvolvidas resistências contra todos os medicamentos para
malária, particularmente no caso de Plasmodium flaciparum. No entanto, a quimioprofilaxia
pode reduzir significativamente o risco de malária em regiões com muitas resistências a
medicamento. Tomar o medicamento para a malária para autotratamento, conforme seja
necessário (terapia em espera), só é considerada para curtas estadias em regiões propensas à
malária ou em viagens em regiões com um risco muito baixo de malária, bem como nos casos
de intolerâncias conhecidos contra medicação profilática. Nestes casos, recomenda-se utilizar
um teste de malária rápido e fácil de usar que seja adequado para a viagem. Particularmente,
em regiões onde existam médicos especializados em doenças tropicais, um teste rápido de
malária é muito útil para diagnósticos precoces, que podem prevenir atrasos fatais. Assim, se
um teste rápido for positivo, o medicamento utilizado nas viagens pode ser usado de forma
RIDA®QUICK Malaria
2016-01-07
2
direcionada.
Um método padrão comum para o diagnóstico mínimo de malária em um laboratório é a
detecção de plasmódio no sangue periférico com a ajuda de uma "gota espessa de sangue"
após a coloração Giemsa. O teste rápido RIDA®QUICK Malaria é uma alternativa rápida que
também pode ser realizado por pessoas sem treinamento especial. O teste também pode ser
usado como método de varredura para diversos exames em bancos de sangue. No caso de
morfologia parasita indefinida microscopicamente ou morfologia parasita que possa ser difícil
avaliar, o teste também pode ser usado como um teste confirmatório para malária. O teste
rápido RIDA®QUICK Malaria é também muito adequado para o monitoramento do tratamento,
porque pode detectar a redução de antígenos do plasmódio ainda circulando no sangue,
mesmo se a morfologia do plasmódio de diferentes estágios do sangue no esfregaço do
sangue não for mais reconhecível sob o microscópio. No entanto, o diagnóstico definitivo da
malária baseia-se no exame microscópico do sangue, auxiliado por parâmetros laboratoriais
adicionais em conjunção com o diagnóstico clínico do paciente.
3. Princípio do teste
O teste RIDA®QUICK Malaria é um teste rápido imunocromatográfico de estágio único para a
detecção combinada de proteína enriquecida com histidina (PfHRP-2) específico para
Plasmodium falciparum, bem como desidrogenase de lactato específica para plasmódio, que
ocorre em todos os patógenos de malária. Os anticorpos de captura contra o antígeno HRP-2
do Plasmodium falciparum e contra LDH específico de plasmódio são imobilizados em duas
linhas cruzadas na membrana de nitrocelulose localizada no compartimento da bandeja. Além
disso, há uma terceira linha, a linha de controle, em que os outros anticorpos de captura
específicos são conectados. Além disso, anticorpos fixos ao ouro coloidal em especificidade
adequada são localizados na área para a aplicação da amostra de sangue. A lise de eritrócitos
e a liberação de antígenos presentes no espécime acontece após a amostra de sangue ser
transferida para o funil fornecido na bandeja de teste e a adição subsequente de reagentes no
segundo funil fornecido para este propósito. Neste processo, o antígeno existente (PfHRP-2
e/ou pLDH) se liga aos anticorpos marcados em dourado, flui através da membrana de
celulose e atravessa as três linhas cruzadas com anticorpos imobilizados no processo. No caso
de espécimes positivos, o antígeno e complexo do anticorpo marcado em dourado ligam-se a
estes anticorpos imobilizados e, depois, condensam em uma ou duas linhas do teste de cor
rosa (T1 e/ou T2) e também à linha de controle rosa (C), que aparece em todos os casos.
Apenas a linha de controle rosa é visível em amostras de sangue negativa para o plasmódio.
4. Conteúdo da embalagem
Os reagentes em um kit são suficientes para testes 25 (N7006) ou 5 (N7007)
Cassette
25 (5) teste
Reagent
3 (1) mL
Micro Pipet
25 (5) unidades
RIDA®QUICK Malaria
25 (5) bandejas de teste embaladas individualmente
Ampolas com reagente de extração
MICROSAFE®Tubes 5 µl
2016-01-07
3
5. Reagentes e seu armazenamento
O kit pode ser armazenado em temperaturas entre 2 e 40 °C e pode ser utilizado até a data de
validade impressa. Ele deve ser protegido contra umidade e congelamento e armazenado em
local seco. Nenhuma garantia de qualidade poderá ser assegurada após o término do prazo de
validade. Similarmente, a possibilidade de uso das bandejas não pode ser garantida se a
embalagem das bandejas estiver danificada.
6. Materiais necessários, mas não fornecidos
- Temporizador
- Recipiente de descarte com solução de hipoclorito de sódio de 0,5%
7. Precauções
Apenas para diagnóstico in vitro.
Todas as bandejas de teste são destinadas para apenas uma utilização e não devem ser
reutilizadas.
Os reagentes e bandejas de diferentes lotes não devem ser misturados.
Esse teste deve ser realizado apenas por pessoal de laboratório treinado. As diretrizes para
trabalho em laboratórios médicos devem ser seguidas. Sempre cumpra estritamente as
instruções para uso deste teste.
Os reagentes contêm azida de sódio como conservante. Não deve-se permitir que essa
substância entre em contato com a pele ou com membranas mucosas.
Não pipete amostras ou reagentes com a boca. Evite o contato com membranas mucosas ou
pele ferida. Ao manusear os espécimes, utilize luvas descartáveis e, ao finalizar o teste, lave as
mãos. Não fume, coma ou beba em áreas onde as amostras estiverem sendo processadas.
Todos os reagentes e materiais que entrarem em contato com espécimes potencialmente
infecciosas devem ser tratados com os desinfetantes adequados (por exemplo, hipoclorito de
sódio) ou submetidos à autoclavagem a uma temperatura de 121 °C por pelo menos (1) hora.
8. Coleta e armazenamento de amostras
Os espécimes de sangue devem ser coletados em tubos padrão limpos e podem ser
armazenados por até (3) dias em temperatura ambiente ou entre 2 a 8 °C antes do uso. Para
longos armazenamentos, as amostras de sangue podem ser armazenadas a -20 °C. Para
evitar a coagulação, os tubos de coleta para amostras de sangue podem conter EDTA, citrato e
heparina.
9. Procedimento do teste
9.1. Informação geral
O espécime, os reagentes e a bandeja de teste devem estar em temperatura ambiente (entre
20 e 25 °C) antes do uso. As bandejas de teste devem ser retiradas da embalagem adicional
RIDA®QUICK Malaria
2016-07-01
4
um pouco antes do uso. Uma vez utilizadas, as bandejas de teste não devem ser reutilizadas.
O teste não deve ser realizado sob luz solar direta.
9.2. Preparo da amostra
Os espécimes coletados e armazenados de acordo com o pt. 8, depois de estarem em
temperatura ambiente (20 a 25 ºC), podem ser usados não diluídos no teste.
Similarmente, sangue fresco após puncionar a ponta do dedo, anteriormente desinfetado com
álcool, pode ser coletado diretamente usando a Micro Pipet fornecida com o kit de tubo de 5 µl
MICROSAFE® e usado de acordo com o procedimento de teste descrito abaixo. Para o uso
adequado do MICROSAFE®Tubes, observe estritamente as seguintes instruções.
9.3. Teste da amostra
Remova a bandeja de teste Cassette do alumínio e coloque em uma superfície plana.
Transfira 5 µl de sangue tocando cuidadosamente a membrana de teste na base do funil de
espécime (Sangue) com a ponta da pipeta de uma pipeta descartável, Micro Pipet, contida no
kit MICROSAFE® Tubes ou, alternativamente, uma pipeta de laboratório que possa ser
ajustada para 5 µl.
Importante:
Ao utilizar uma Micro Pipet MICROSAFE®Tubes, não pressione a ampola ao coletar o sangue.
O enchimento acontece automaticamente até a marcação de 5 µl uma vez que a ponta da
pipeta seja imersa na amostra de sangue. Se a ampola for pressionada, uma vez que a ponta
da pipeta entre em contato com a membrana de teste na base do funil de espécime da
bandeja, 5 µl do sangue será transferido para a membrana de teste. Para este propósito, por
favor, observe as instruções contidas nas micro pipetas.
Volumes inexatos de espécime podem resultar em resultados incorretos que não podem ser
analisados.
Subsequentemente, seguindo o mesmo processo, pipete quatro (4) gotas do reagente Reagent
usando o frasco de gota no funil marcado "Reagente". Por gentileza, certifique-se de que o
reagente seja completamente absorvido pela membrana. Esta é a única forma de garantir que
reagentes suficientes combinem com as gotas de sangue aplicadas e fluam através da
membrana juntas, com o objetivo de detectar possíveis patógenos de malária. Através da
janela de observação da bandeja com as marcações laterais T1, T2 e C, é possível observar
como a mistura flui através da membrana.
A marcação C deve aparecer após, no máximo, cinco (5) minutos e uma faixa rosa deve
aparecer na membrana. Isto significa: o teste foi realizado corretamente e funcionou. Com o
passar do tempo, a membrana, que começa branca, fica vermelha apenas por causa do
sangue.
O resultado final poderá ser lido após 30 minutos. As faixas que aparecem depois não têm
influência na avaliação do teste.
Os padrões da faixa são avaliados e interpretados de acordo com as instruções contidas no kit.
RIDA®QUICK Malaria
2016-07-01
5
10. Controle de qualidade, sinais de deterioração do reagente
O teste deve ser avaliado apenas se a bandeja de teste estiver intacta antes de pipetar a
suspensão de espécime e não forem vistas mudanças na cor ou nas faixas da membrana de
teste. Além disso, após o período de incubação de cinco (5) minutos, pelo menos as faixas de
controle vermelho-violeta devem estar visíveis. Se não aparecerem, verifique os seguintes itens
antes de repetir o teste:
- A vida útil das bandejas de teste e dos reagentes utilizados
- A execução correta do teste
- Contaminação dos reagentes
Se, após a repetição do teste, com uma nova bandeja de teste, as faixas de controle ainda não
aparecerem, por favor, entre em contato com o fabricante ou seu agente R-Biopharm local.
11. Avaliação e interpretação
Devem aparecer no máximo três faixas, vistas a partir do campo de aplicação do sangue, na
seguinte sequência: Uma faixa de reação de cor rosa na linha de teste T2 e outra na linha de
teste T1 e também a faixa de controle rosa na linha de controle C.
Se a faixa de controle C estiver ausente, o teste não poderá ser avaliado e é inválido!
São possíveis as seguintes interpretações:
-
Positivo para Malária: todas as três faixas (T2, T1 e C) ou apenas uma das duas faixas
T são visíveis ao longo da faixa C.
Negativo para Malária: apenas a faixa de controle C é visível.
Inválido: não existem faixas visíveis ou outra constatação além das mencionadas
acima. As descolorações das faixas que aparecem depois dos 30 minutos não têm valor
de diagnóstico e não devem ser avaliadas. Uma visão geral de todas as possibilidades
de constatação das três faixas específicas T2, T1 e C podem ser encontradas nas
instruções de aplicação contidas no kit de teste.
12. Limitações do método
O teste RIDA®QUICK Malaria é um teste essencialmente qualitativo para detecção de
antígenos solúveis específicos de plasmódio em amostras de sangue. Não é possível associar
entre a intensidade das faixas específicas visíveis e a ocorrência ou severidade dos sintomas
clínicos.
Os resultados obtidos sempre devem ser interpretados em combinação com os sinais
clínicos e com os sintomas e outros parâmetros laboratoriais.
Um resultado positivo não descarta a presença de outros patógenos ou causa infecciosos.
Um resultado negativo não descarta uma possível infecção com patógenos de malária. Pode
ser causado por uma distribuição insuficiente de plasmódio no sangue no momento da coleta
de sangue. Se houver motivos anamnésticos substanciais para a suspeita de malária, um
segundo teste com uma amostra de sangue novo e fresco deve ser realizado cerca de 12
RIDA®QUICK Malaria
2016-07-01
6
horas depois. Um diagnóstico final deve sempre ser verificado ou confirmado por métodos
laboratoriais adicionais, como exame microscópico do esfregaço de sangue.
13. Características de desempenho
13.1. Sensibilidade clínica e especificidade
Em um estudo prospectivo de janeiro a dezembro de 2013, um total de 93 amostras de sangue
foram examinadas no Swiss Tropical e Public Health Institute (Swiss TPH) em Basel com o
teste rápido RIDA®QUICK Malaria comparado a um padrão dourado (microscopia de uma
camada espessa de sangue e esfregaço de sangue). Os espécimes vieram de pacientes com
suspeita de malária que apresentaram TPH ou foram enviados de hospitais, laboratórios e
médicos estabelecidos de todo a Suíça. Todos os espécimes foram testados em paralelo com
outro teste rápido disponível comercialmente. Os dois testes rápidos detectaram a proteína
enriquecida com histidina (HRP2) específico para P. falciparum e outra proteínas específica
pan-malária diferente em uma segunda faixa para a detecção de outras espécies de plasmódio.
No teste rápido RIDA®QUICK Malaria, é a desidrogenase de lactato específica para plasmódio
e, no NOW ® Malaria, aldolase específico para plasmódio. Os resultados são resumidos na
tabela 1. Os resultados de ambas faixas são resumidos em um resultado geral. Por meio da
microscopia, não foi possível determinar as espécies de um de 93 espécimes originais. Este
espécime não foi incluído na avaliação.
Tabela 1: Os resultados de 93 amostras de sangue com suspeita de malária em comparação
com dois testes rápidos para malária comerciais com os métodos de padrão ouro do
Instituto Swiss TPH em Basel
RIDA®QUICK Malaria
Microscopia
de um esfregaço/gota
espessa de sangue
NOW® Malaria
+
-
+
-
+
43
1*
40
4§
-
6#
43
5†
44
*
P. ovale, parasitemia < 0.1%
§
P. falciparum (1x) , P. ovale (1x) parasitemia < 0.1%, P. vivax (1x), P. malariae (1x)
#
5 x controle de terapia de espécime anterior positiva microscopicamente; 1 de 6 positivo de PCR
confirmado
#
4 x controle de terapia de espécime anterior positiva microscopicamente; 1 de 5 positivo de PCR
confirmado
Deste modo, as seguintes especificações de teste são calculadas para os dois procedimentos
de teste rápido:
Sensibilidade:
97,7%
90,9%
Especificidade:
87,8%
89,8%
RIDA®QUICK Malaria
2016-07-01
7
13.2. Sensibilidade analítica
O limite de detecção para o teste rápido RIDA®QUICK Malaria também foi determinado no
Instituto Swiss TPH através da diluição em série de duas amostras de sangue P. falciparumpositivo e uma para amostra de sangue P. vivax positivo. A diluição, onde uma faixa fraca era
visível na linha T1 ou T2, foi considerada o limite de detecção. Os limites de detecção
determinados desta forma foram determinados apenas para as duas espécies de plasmódio
que foram detectadas com mais frequência. Totalizaram:
P. falciparum: 45 plasmódio/µl de sangue
P. vivax: 100 plasmódio/µl de sangue
13.3. Especificidade analítica
A fim de testar possíveis reações cruzadas com componentes potencialmente perigosos (fator
reumatoide (RF), anticorpos anti-nucleares (ANA) e anticorpos humanos anti-rato (HAMA)) bem
como vários patógenos, diferentes espécimes positivos para tais componentes e patógenos
foram testados no RIDA®QUICK Malaria. Apenas um dos patógenos testados (HCV, HIV, HBV,
vírus da dengue, vírus Chikungunya, Esquistossoma) mostrou uma reação cruzada fraca.
Todos os espécimes com ANA e HAMA, bem como concentrações do fator reumatoide até
300 IU/mL foram negativos. A 400 IU/mL RF, houve uma fraca descoloração na faixa de teste
T2. A Tabela 2 mostra os resultados em uma visão geral. Não podem ser descartadas, no geral,
outras possíveis reações cruzadas. Resultados positivos devem sempre ser verificados antes
de introduzir um tratamento específico anti-malária através de outro método padrão de
laboratório (veja pt. 12 Limites do Método).
Tabela 2: Resultados dos testes sobre especificidade analítica
Patógenos/fatores inconvenientes
Vírus Chikungunya
Vírus da dengue
Vírus da Hepatite B
Vírus da Hepatite C
Vírus da imunodeficiência humana
Esquistossoma
Fator reumatoide
HAMA
ANA
Número de espécimes
testados
10
10
11
21
14
3
6 (200–400 IU/mL)
2 (400–600 ng/mL)
5 (titra 160–1280)
Resultados
Negativo
Negativo
Negativo
Negativo *
Negativo
Negativo
Negativo #
Negativo
Negativo
* 3 dos 21 espécimes testados resultaram em um sinal na faixa de teste T2
#
A 400 IU/mL, o resultado na faixa de teste T2 foi fraco positivo.
RIDA®QUICK Malaria
2016-07-01
8
Apêndice
Símbolos específicos do teste:
Cassette
Bandeja de teste
Reagent
Ampolas com reagentes de extração
Micro Pipet
MICROSAFE®Tubes 5 µl
RIDA®QUICK Malaria
2016-07-01
9
Referências
1.
Gatton M.L. et al.: Pan-Plasmodium band sensitivity for Plasmodium falciparum detection
in combination malaria rapid diagnostic tests and implications for clinical management
Malaria Journal (2015) 14:115
2.
Wilson, M.: Malaria Rapid Diagnostic Tests. Clin Infect Dis (2012) 54 (11): 1637-1641
3.
Fogg C. et al.: Assessment of three new parasite lactate dehydrogenase (pan-pLDH) tests
for diagnosis of uncomplicated malaria. Trans Roy Soc Trop Med Hyg (2008) 102:25-31
4.
Moody, A.: Rapid Diagnostic Tests For Malaria Parasites. Clin Microbiol Rev. (2002) Jan.
15(1): 66–78
5.
Arai M. et.al.: Laboratory evaluation of the Rapid malaria P.f./PAN (pLDH)
immunochromatographic test for detecting the panmalarial antigen using a rodent
malaria model. Am J Trop Med Hyg ( 2004) Feb.70(2):139-43
6.
Laferi H. et al.: False Positive Dipstick Test for Malaria. Lancet (1998) 337: p 1635
7.
Garcia M. et al.: Immunochromatographic test for malaria diagnosis. Lancet (1996) 347: p
1549
8.
Kilian A.H.D. et al.: Comparison of two rapid, HRP2-based diagnostic tests for
Plasmodium falciparum. Trans Roy Soc Trop Med Hyg (1997) 91: p 666-667
9.
Singh N. et al.: Malaria diagnosis by field workers using an immunochromatographic test.
Trans Roy Soc Trop Med Hyg (1997) 91:p 396-397
RIDA®QUICK Malaria
2016-07-01
10