Tensão superficial: um conceito físico muito importante que pode ser
trabalhado em Biologia, Matemática e Química
Prezados alunos e alunas:
O presente tutorial foi elaborado visando à facilitação na aquisição de novos
conhecimentos relacionados à “tensão superficial”, ao seu aprofundamento e esclarecimento
de dúvidas. Também serve para indicação de bibliografia e de endereços de “sites”
relacionados aos assuntos abordados.
Observe-se que outras fontes de pesquisa poderão ser utilizadas (em especial da
“internet”) e que a ajuda dos(as) professores(as) poderá ser requerida. Todavia, saliente-se
que os(as) professores(as) só irão auxiliar em situação extrema. Isso significa, portanto, que
é desejável autonomia dos alunos na busca de respostas aos questionamentos surgidos.
Quando, por outro lado, os conceitos em estudo forem eminentemente físicos e
ainda existirem dúvidas, os alunos poderão buscar auxílio diretamente com professor de
Física.
Por último, é conveniente destacar que os próprios colegas de grupo poderão
ajudar. Às vezes, as dúvidas são comuns e o compartilhamento de idéias facilita a
elucidação das mesmas.
Bom trabalho!
Professores Adalberto, Cristiane, Josiane, Luiz Antônio e Valdir.
Sugestões de “sites” para pesquisas
https://periodicos.ufsc.br/index.php/fisica/article/view/6420/5936
http://www.iq.ufrgs.br/aeq/html/publicacoes/matdid/livros/pdf/sabao.pdf
http://www.clubedaquimica.com/index.php?option=com_content&view=article&id=50&Itemid=
11
http://www.feiradeciencias.com.br/sala07/07_T01_05.asp
http://www.if.ufrgs.br/tex/fis01101/exemplounidade2.htm
http://qnesc.sbq.org.br/online/qnesc16/v16_A02.pdf
http://www.old.diariodepernambuco.com.br/mundo/nota.asp?materia=20100922084518&ass
unto=31&onde=Brasil
http://www.portalpositivo.com.br/cadastro2014/entra_chave.asp
http://www.agracadaquimica.com.br/index.php
http://web.ist.utl.pt/ist12219/data/90.pdf
O nosso cotidiano e a tensão superficial
Ao lavar louças, preferimos água
quente. Por quê? A principal razão é que a
tensão superficial da água sofre uma
diminuição com o aquecimento, fazendo
com que ela molhe mais facilmente o
tecido. Também, sabão ou detergente
também auxiliam na lavagem, pois
diminuem a tensão superficial da água,
fazendo com que a água penetre mais
facilmente onde há sujeira. Isso,
naturalmente, vale para lavagem de
roupas.
A icterícia pode ser detectada em
laboratório através de um teste muito
simples que tem a ver com a T.S.
Considere que a urina normal possui uma
tensão superficial de 0,066 N/m, mas se a
urina contiver bile (o que ocorre em caso
de icterícia), a tensão superficial da urina
diminui para +/- 0,055 N/m. Que teste é
feito? Espalha-se enxofre em pó sobre a
superfície da urina; o pó flutua na urina
normal, no entanto, ele afunda se a tensão
superficial da urina é diminuída pela
presença da bile, indicando a icterícia.
Nossos pulmões possuem uma
substância parecida com o detergente, a
qual apresenta propriedade de ser
tensoativa. Trata-se de um surfactante
pulmonar, pois é capaz de romper a
tensão superficial entre o líquido dos
alvéolos pulmonares e o ar dos pulmões
facilitando a inspiração.
O corpo humano só produz os
surfactantes nos estágios finais da
gestação. As crianças prematuras (que
nasceram antes de completar os 9 meses
de gestação) não conseguem respirar
direito e precisam ser tratadas surfactantes
artificiais até que passem a produzir o seu
próprio.
A tensão superficial também é
importante para os insetos aquáticos. Eles
podem caminhar na superfície da água!
Também é a tensão superficial que
permite a formação de bolhas.
As ondas em lagos e mares são
importantes para manter a oxigenação da
água. A tensão superficial é essencial para
a formação de ondas. Essas ondas são
formadas quando o vento sopra na
superfície da água.
A tensão superficial é também
responsável pelo efeito de capilaridade
que ocorre no sistema circulatório de
plantas. Com isso, a água pode ir da raiz
até as folhas através desses capilares.
A tensão superficial é também
denominada
coesão
específica
ou
constante de capilaridade. Ela depende da
natureza do líquido e diminui à medida que
a temperatura se eleva. À temperatura
crítica, é nula.
o
Tensão superficial de alguns líquidos, a 20 C
Água
0,0722 N/m
Mercúrio
0,4650 N/m
Etanol
0,0223 N/m
Acetona
0,0237 N/m
Pequenos insetos, por serem leves e
somando-se a isso a alta tensão
superficial da água, podem caminhar na
sua superfície. Isso facilita a postura de
ovos e conseqüente sucesso na sua
proliferação.
A T.S. impede que o inseto afunde.
O tecido de um guarda-chuva detém a
água porque a tensão superficial se opõe
a entrada da água nos poros do tecido.
2
Texto n.o 1
Tensão superficial: estudo químico submicroscópico.
Mesmo uma gota de água é formada por uma quantidade muito grande de
moléculas, as quais estão unidas umas às outras através de atrações muito fortes
denominadas ligações de hidrogênio. Atribuem-se a essas ligações muitas das propriedades
interessantes (às vezes estranhas) da água. Assim, por exemplo, o alto ponto de ebulição
da água (100oC, se Patm=760mmHg) é explicado pela forte atração intermolecular. As ditas
ligações de hidrogênio são, na verdade, interações (atrações) que ocorrem entre átomos de
hidrogênio (daí o nome) e átomos de flúor, oxigênio e nitrogênio.
Para compreender o que são ligações de hidrogênio, é necessário antes considerar
que a água é uma substância polar, ou seja, suas moléculas apresentam polos. São ditos
polos porque constituem regiões com comportamentos opostos em termos de carga elétrica,
isto é, polo positivo e pólo negativo. Como numa mesma molécula podem existir vários
dipolos, a soma de todos eles (momento dipolar resultante) deverá ser diferente de zero
para que a mesma seja considerada polar. É a geometria molecular (orientação espacial)
que determina, por soma vetorial, a polaridade ou não das moléculas com dipolos.
Um modelo bastante usado para explicar a polaridade da água é a seguir
representado. É geometria angular da água que, por soma vetorial diferente de zero, torna-a
“polar”.
Fig. 1: modelo molécula de água e polaridade.
Voltando às ligações de hidrogênio, podemos dizer que são ligações
intermoleculares especiais, as quais ocorrem entre moléculas vizinhas e surgem por que o
hidrogênio apresenta eletronegatividade baixa se comparado à eletronegatividade dos
outros elementos citados anteriormente (F, O, N), levando ao surgimento de um ou mais
dipolos (positivo e negativo) na molécula. No caso particular da água, os hidrogênios da
molécula representam polos positivos devido à baixa eletronegatividade (2,2 na escala de
Pauling). O oxigênio representa o polo negativo, pois sua eletronegatividade é maior (3,4 na
escala de Pauling). Como vimos, por causa da geometria molecular, isso torna a molécula
de água polar. Ocorrendo aproximação de molécula de água vizinha, com orientação
favorável (hidrogênio voltado para oxigênio) surge, então, atração intermolecular forte devido
à polarização contrária.
Figura 2: modelo de ligação de hidrogênio na água,
3
Entretanto, entre as moléculas da superfície da água isso não ocorre, pois não há
moléculas em todas as suas direções. Isso origina a chamada tensão superficial da água. É
isso, por exemplo, que ocorre com as moléculas que estão na superfície de uma bolha de
sabão: elas realizam ligações de hidrogênio apenas com as moléculas que estão ao seu
lado.
.
Figura 3: modelo para tensão superficial.
Por que a bolha de sabão é redonda?
A Lei de Laplace afirma que a pressão manométrica no interior de uma membrana
elástica (diferença de pressão entre o interior e o exterior da membrana) é diretamente
proporcional à tensão superficial da membrana (nesse caso a tensão superficial é uma
propriedade da membrana de água e sabão) e inversamente proporcional ao raio de
curvatura da membrana.
- ∆P é a variação de pressão entre superfícies (sempre maior no lado côncavo);
- T é a tensão superficial (água e sabão);
- R raio da esfera (bolhas, gotas).
Como o gás no interior da bolha está em equilíbrio, a pressão é a mesma em todos
os pontos internos à bolha e, além disso, a pressão externa também é constante (pressão
atmosférica), a pressão manométrica é constante em todos os pontos da bolha. Assim, se a
pressão manométrica é constante e a tensão superficial também é constante (por ser uma
propriedade da membrana de água e sabão), pela Lei de Laplace, o raio da curvatura da
bolha deve ser o mesmo em qualquer ponto. A única superfície fechada que possui o
mesmo raio de curvatura em todos os pontos é a superfície esférica e, portanto, a bolha
deve ser esférica.
4
Texto n.o 2
Tensão superficial: unidades de medida
Utilizaremos a ilustração a seguir para entender a unidade de medida da tensão
superficial. Perceba que a força de coesão é normal (perpendicular) ao segmento
considerado.
Fig.1: representação da T.S. em uma superfície plana de um líquido.
Considere-se:
- Um segmento de reta AB (∆ℓ) na superfície livre de um líquido;
-Em cada ponto desse segmento, uma força (∆F) sendo exercida pela “película”
superficial na própria superfície e normal ao segmento.
Chama-se tensão superficial (T), a força de coesão superficial por unidade de
comprimento da linha na qual ela se aplica.
Sendo assim:
Isso significa que a tensão superficial obedece à expressão:
Ou ainda:
Por isso podemos adotar as unidades, entre outras:
- Newton/centímetro (N.m-1);
- dina/centímetro (d.cm-1, C.G.S);
- newton/metro (N.m-1, S.I);
Propomos um desafio
Um aluno, lendo um texto sobre a natureza das bolhas de sabão, encontrou em
uma tabela valores para a tensão superficial.
Tabela 1–Tensão superficial de alguns líquidos.
SUBSTÂNCIA
TENSÃO SUPERFICIAL (d.cm-1)
Álcool etílico (etanol)
23,06
Água destilada
72,72
Lauril sulfato de sódio (detergente)
25,28
Percebeu que os valores não se encontram no SI? Faça, então, a conversão.
http://www.plnciencia.com.br/roteiros/1330.PDF
5
Texto n.o 4
Capilaridade depende da tensão superficial?
Já
vimos
várias
situações
cotidianas em que o fenômeno chamado
tensão superficial está presente. Outro
fenômeno muito interessante é a
capilaridade e, como poderemos observar,
está relacionado ao primeiro.
Considerando que esse tubo é de
vidro podemos explicar esse fenômeno
pela interação das moléculas de água (ou
de mercúrio) com o vidro, a qual varia de
acordo com o diâmetro do tubo, o tipo de
líquido e sua viscosidade e a temperatura.
A chamada capilaridade pode ser
evidenciada através de um experimento
muito simples, o qual consiste em colocar
um tubo fino (como o cabelo, daí capilar)
de vidro em um recipiente contendo água
ou ainda através do sistema representado
na figura 1. No primeiro caso, observa-se,
após algum tempo, que a água sobe no
tubo e entra em repouso a uma
determinada altura acima da superfície da
água. Um fato interessante é que, se em
vez da água, utilizamos mercúrio (um
metal líquido), o nível deste no interior do
tubo capilar se estabiliza abaixo do nível
do líquido.
Para que o líquido suba – exemplo da
água – as moléculas do tubo que estão
acima da superfície da água o atraem as
moléculas desta. Assim, o líquido começa
a subir e se alinha a essas moléculas que
provocaram a atração.
Fig.2: modelo explicando a capilaridade.
A tensão superficial do líquido que
penetra no tubo e a curvatura do menisco
formado exercem um papel importante no
fenômeno
da
capilaridade,
pois
determinam a pressão de Laplace. É esta
pressão, na verdade, que faz a água
ascender.
Recorde-se que a pressão de Laplace
é dada por:
Fig.1: experimento sobre capilaridade.
O fenômeno capilaridade engloba
tanto a subida ou descida de um líquido
por meio de um tubo fino (capilar). Através
da observação cuidadosa do experimento
ilustrado na figura 1, percebe-se uma
curvatura (de raio Ro) que pode ser
côncava ou convexa, dependendo do
líquido. Essa curvatura é denominada
menisco. No caso do mercúrio, por
exemplo, a curvatura é convexa.
- P é a pressão de Laplace;
- T é a tensão superficial do líquido;
- Ro é o raio da curvatura.
Fig. 3: detalhe da superfície côncava no capilar.
6
Levando-se em conta a equação de
Laplace, sendo alta a tensão superficial e
pequena a curvatura do tubo, espera-se
uma pressão significativa e suficiente para
que o líquido suba.
Uma consequência importante da
tensão superficial dos líquidos para o
entendimento dos fenômenos capilares é o
fato de que, se a superfície de um líquido
deixar de ser plana, surge uma nova
pressão P (figura 3) que pode atuar no
mesmo sentido das forças que tendem a
puxar as moléculas para o interior do
líquido (gera superfície convexa) ou
opostamente (gera superfície côncava).
Ainda
sobre
a
capilaridade,
salientamos as inúmeras situações
cotidianas em que está presente. Na
Biologia, quando se estuda a função do
xilema, a capilaridade precisa ser
considerada. Xilema é um sistema de
tubos capilares, presentes no interior das
plantas, os quais transportam água com
sais minerais desde a raiz até as folhas. O
diâmetro interno desses tubos é da ordem
de 10−5m e é graças a isso que os
nutrientes conseguem atingir regiões mais
altas da planta.
A seguir, propomos um experimento
simples envolvendo capilaridade e que
poderá ser realizado em casa (individual
ou em grupo). Fotografe o experimento em
etapas e mostre aos professores e
professoras.
Cromatografia em papel: separando cores
de canetinhas hidrográficas
A denominação cromatografia (vem do
grego khroma, cor) em papel tem origem
no fato de que, inicialmente, esta técnica
era empregada apenas na separação dos
componentes de materiais coloridos.
1. Materiais necessários
- Água
- Copos de vidro lisos
- Tiras de papel-filtro (1,5 cm x 15 cm)
- Canetas hidrográficas de cores diferentes
2. Montar o sistema a seguir representado.
Fig.5: montagem do experimento.
3. Utilizando a caneta esferográfica de cor
azul escuro, marcar, a 3 cm da
extremidade inferior, uma bolinha do
tamanho de uma cabeça de alfinete.
Cuidar para a “bolinha” não tocar a
superfície da água.
4. Observar o que acontece durante
alguns minutos. Repetir para outras cores.
5. Não esquecer! É importante fotografar
cada etapa para mostrar em aula.
Fig.4: representação artística, em corte transversal,
de um caule.
Outro exemplo de cotidiano é o que
permite o funcionamento das lamparinas a
álcool ou querosene. O combustível sobre
através do pavio e consegue atingir a
chama por capilaridade.
6. Explicar o que ocorrido, pesquisando
ainda maneiras alternativas de realizar
esse experimento.
http://www.leb.esalq.usp.br/aulas/lce200/C
ap7.pdf
http://www.feiradeciencias.com.br/sala21/P
QE_09.asp
7
Comentando alguns experimentos realizados
Bolhas gigantes e tensão superficial
Um dos experimentos realizados consistiu na
brincadeira de fazer bolhas gigantes. Por que foi possível fazer
bolhas gigantes? A variedade de ingredientes necessária pode
ser conferida a seguir. Entretanto, achamos oportuno também
comentar as suas funções na mistura, relacionando-as,
preferencialmente, a conceitos físico-químicos.
Saliente-se, que, a fim de diminuir essa superfície ao
mínimo e ficar mais estável, a película adquire o formato
esférico, com menor área de superfície em relação ao volume.
Qual a função do detergente?
O detergente é um agente “tensoativo” ou “surfactante”, pois ele diminui essa
tensão superficial da água. A bolha se mantém sem estourar em virtude das interações entre
as moléculas de água que restaram depois de se adicionar o detergente.
Para que serve o xarope de milho?
Sendo formado por 80% de glicose e 20% de frutose, isto é, monossacarídeos ou
oses, as quais possuem em sua estrutura vários grupos hidroxila (–OH).
Essas várias hidroxilas aumentam a quantidade de ligações de hidrogênio, pois
haverá esse tipo de ligação entre suas moléculas e também com as moléculas de água.
Como resultado, a evaporação da água na superfície da bolha será dificultada e as bolhas
demorarão mais tempo para estourar; além de se tornarem mais resistentes, aumentando a
probabilidade de se fazer bolhas maiores.
Essa função do xarope de milho mostra que é possível usar no lugar dele qualquer
substância que apresente vários grupos hidroxilas em sua estrutura, como a sacarose, por
exemplo, que é o açúcar comum, e também a glicerina.
http://www.manualdomundo.com.br/2013/02/receita-de-bolha-de-sabao/
http://protj.wordpress.com/2007/04/30/p14466/
8
Afundando alfinetes, mas sem derramar
O que impede a água de se derramar pelas bordas enquanto são introduzidos os
alfinetes? É a tensão superficial. A água comporta-se como se fosse uma “pele elástica”,
“esticando-se” sem se romper, à medida que o volume total (água+agulhas) vai aumentando.
Fig.1: ilustração do experimento realizado com alfinetes.
Repare que se forma uma “barriga” (para os matemáticos é um segmento de
esfera), a qual terá um limite de resistência, dependendo do número de alfinetes colocados.
Supondo que um alfinete típico tenha volume da ordem de 5 mm3 e que na “barriga”
a base possua raio da secção medindo 3cm (30mm) e a altura aproximada de 1mm, quantos
alfinetes foram colocados? Peça ajuda à professora ou ao professor de Matemática.
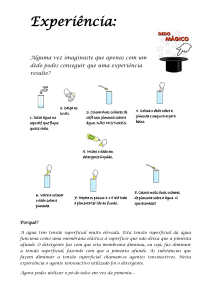
Rompendo a tensão superficial
Quando colocamos talco na água, vimos que ele não afundou. Isso foi possível
porque as moléculas de água sofrem uma grande atração entre elas (ligações de
hidrogênio). No interior do líquido, todas as moléculas de água sofrem essas forças de
atração em todas as direções. Mas, as moléculas de água que estão na superfície sofrem a
atração apenas das moléculas na horizontal e das outras que estão abaixo, no líquido, já
que em cima tem apenas ar.
Como o número de moléculas se atraindo é menor, existe uma compensação e uma
força maior de atração acontece na superfície que acaba formando quase uma "pele" de
água. Essa "pele" é chamada de tensão superficial da água, conforme já havíamos
estudado. É essa tensão superficial que impede o afundamento das partículas do talco.
Entretanto, o detergente é capaz de romper a tensão superficial e, com isso, afundam. Uma
reportagem de jornal (“link” abaixo) ilustra o que foi dito, relatando a possibilidade de
combate ao mosquito transmissor do vírus da dengue colocando na água determinado
composto químico (supostamente inofensivo ao meio ambiente)
http://www.old.diariodepernambuco.com.br/mundo/nota.asp?materia=20100922084518&ass
unto=31&onde=Brasil
9
Atividade de (auto)avaliação
Orientações
A presente atividade está relacionada ao assunto tensão superficial e deverá ser
realizada em grupo, sendo que as respostas (arquivos) serão enviadas aos professores
[email protected] e [email protected] até a data combinada em aula.
Para resolver as questões propostas, utilize como referência bibliográfica os textos
deste arquivo, comentários e anotações das aulas experimentais ou ainda “sites” confiáveis.
Na digitação das respostas, utilize fontes Arial ou Times New Roman, tamanho12, cor
azul, visando à facilitação da correção por parte do professor ou da professora.
Fique atento aos erros de ortografia, pois serão observados.
Professora Josiane e professor Luiz Antônio.
De acordo com nosso experimento de eletrólise, a água não pode mais ser
considerada elemento, conforme pensava Aristóteles. Sabemos hoje que é formada por dois
átomos de hidrogênio e um de oxigênio, daí aceitarmos a fórmula H2O. Quanto à sua
geometria, admite-se que uma molécula de água é angular e, por diferença de
eletronegatividade seus elementos, apresenta uma zona positiva e outra negativa.
Também em nossas aulas experimentais, vimos que a água apresenta propriedades
muito interessantes que a tornam única na natureza. Dentre as várias propriedades,
destacamos a tensão superficial.
- Do ponto de vista submicroscópico (em nível atômico/molecular) o que é tensão
superficial?
- Tensão superficial é propriedade exclusiva da água? Qual a influência da
temperatura sobre a mesma?
- Medir a tensão superficial é, muitas vezes, necessário para caracterizá-la. Por que,
no SI sua unidade é N/m?
- Por que, acrescentando detergente ou sabão, a tensão superficial diminui? Qual a
importância disso na limpeza de roupas ou de louças?
- Bolhas de sabão tendem a adquirir a forma esférica. Por que isso acontece,
considerando-se também do ponto de vista energético?
- Mosquitos podem ter a sua reprodução facilitada graças ao fenômeno tensão
superficial. Por quê? Qual seria, com base nisso, uma boa solução para o combate ao
mosquito Aedes egypti e conseqüente diminuição da dengue?
- A respiração de bebês prematuros pode ser dificultada por deficiência do efeito
“surfactante” nos alvéolos pulmonares. Qual relação dessa dificuldade com a propriedade
tensão superficial?
- A tensão superficial influencia ainda no fenômeno capilaridade. Qual a relação
disso com a equação de Laplace? Que importância deve ser dada à capilaridade na nutrição
vegetal?
10