Moderna plus
1
química
química na abordagem
do cotidiano
Parte II
Unidade F
Capítulo 18 Forças intermoleculares
tito
canto
1
informe-se sobre a química
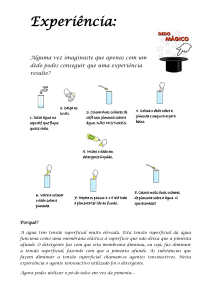
Tensão superficial
Pequena agulha
Água
pura
Adicionando
uma gota de
detergente
Se colocarmos, com muito cuidado e muito delicadamente, uma pequena agulha sobre a superfície da água pura, ela permanecerá aí, apesar de ser
feita de um material quase oito vezes mais denso que a água. Se, no entanto,
adicionarmos uma gota de detergente à água, imediatamente ela afundará.
Água
+
detergente
A água possui uma alta tensão superficial ou, em outras palavras, sua
superfície possui uma resistência relativamente alta a ser deformada e, consequentemente, a ser atravessada por pequenos objetos. Isso é explicado pelas
ligações de hidrogênio que mantêm as moléculas fortemente unidas.
A presença de sabões e detergentes diminui a tensão superficial, porque
essas substâncias tendem a se acumular na superfície, diminuindo a força
atrativa entre as moléculas. Dizemos que são agentes tensoativos ou surfactantes, pois atuam sobre a tensão superficial.
Molécula “típica”
presente no líquido
Molécula da
superfície
luiz iglesias nuñez/cid
nasa/
spl/latinstock
Uma molécula “típica” presente em um
líquido é atraída por todas as suas vizinhas.
Já uma molécula da superfície só é atraída
pelas moléculas laterais e inferiores. Há uma
“compactação” maior entre as moléculas da
superfície, o que dá origem à tensão superficial
do líquido, que será tanto mais forte quanto mais
intensas forem as interações intermoleculares.
fabio colombini
www.modernaplus.com.br
Astronauta em órbita observa uma
gota de água. Nesse ambiente de
imponderabilidade, a tensão superficial
tende a fazer a amostra de água
assumir a forma esférica.
Alguns insetos andam sobre a água graças à elevada tensão superficial
desse líquido.
A elevada tensão
superficial da água
se explica pelas
fortes atrações
(ligações de
hidrogênio) entre
uma molécula da
superfície e suas
vizinhas.
química
Moderna plus
química na abordagem
do cotidiano
Parte II
Unidade F
Capítulo 18 Forças intermoleculares
Você entendeu a leitura?
1 (UFPA) Os insetos mostrados na figura não afundam na água devido
ao (à)
markus gayda/vestibular ufpa-2007
a)presença de pontes de hidrogênio, em função da elevada polaridade da molécula de água.
b)fato de os insetos apresentarem uma densidade menor que a da
água.
c) elevada intensidade das forças de dispersão de London, em consequência da polaridade das moléculas de água.
d)interação íon-dipolo permanente, originada pela presença de
substâncias iônicas dissolvidas na água.
e) imiscibilidade entre a substância orgânica que recobre as patas
dos insetos e a água.
2 (F. M. Pouso Alegre-MG) Pontes de hidrogênio são interações que, em
líquidos, provocam aumento da tensão superficial. Qual das substâncias líquidas abaixo terá maior tensão superficial?
a)benzeno
b)ciclo-hexano
c) tetracloreto de carbono
d)éter etílico
e) água
Comentário dos autores:
www.modernaplus.com.br
O benzeno (C6H6) e o ciclo-hexano (C6H12) são derivados do petróleo. O tetracloreto de carbono tem fórmula CC,4 e o éter etílico tem fórmula molecular C4H10O e
fórmula estrutural:
H
H
H
H
H
H
C
C
O
C
C
H
H
H
H
H
H
1
tito
canto
2