UNIVERSIDADE DO ESTADO DO AMAZONAS - UEA
FUNDAÇÃO DE MEDICINA TROPICAL DO AMAZONAS – FMT-AM
MESTRADO EM DOENÇAS TROPICAIS E INFECCIOSAS
ESTUDO CLÍNICO E EPIDEMIOLÓGICO COM GESTANTES
PORTADORAS DO AGHBS – EVIDÊNCIAS DA POSSIBILIDADE DE
TRANSMISSÃO VERTICAL
IRAN GRIJÓ PRAIA
Manaus – AM
2005
IRAN GRIJÓ PRAIA
ESTUDO CLÍNICO E EPIDEMIOLÓGICO COM GESTANTES
PORTADORAS DO AGHBS – EVIDÊNCIAS DA POSSIBILIDADE DE
TRANSMISSÃO VERTICAL
Dissertação apresentada ao Programa de
Pós Graduação em Medicina Tropical da
Universidade do Estado do Amazonas em
convênio com a Fundação de Medicina
Tropical do Amazonas, como requisito para
obtenção do título de Mestre em Doenças
Tropicais e Infecciosas.
Orientador: Professor Doutor Wornei Silva Miranda Braga
MANAUS
2005
FICHA CATALOGRÁFICA
PRAIA, Iran Grijó;
Estudo clínico e epidemiológico com gestantes portadoras do AgHBs –
evidências da possibilidade de transmissão vertical / Iran Grijó Praia. Manaus – AM: UEA;
FMTAM, 2005.
48 p.
Dissertação (Mestrado em Doenças Tropicais e Infecciosas).
1. Hepatite viral B 2. AgHBs 3. AgHBe 4. PCR 5. Transmissão vertical 6.
gravidez
FOLHA DE JULGAMENTO
ESTUDO CLÍNICO E EPIDEMIOLÓGICO COM GESTANTES
PORTADORAS DO AGHBS – EVIDÊNCIAS DA POSSIBILIDADE DE
TRANSMISSÃO VERTICAL
IRAN GRIJÓ PRAIA
“Esta Dissertação foi julgada adequada para obtenção do Título de Mestre em
Doenças Tropicais e Infecciosas, aprovada em sua forma final pelo Programa de
Pós-Graduação em Medicina Tropical da Universidade do Estado do Amazonas em
convênio com a Fundação de Medicina Tropical do Amazonas”.
______________________________________
Prof. Wornei Silva Miranda Braga, Dr.
Orientador
________________________________________
Profª. Maria das Graças Vale Barbosa, Dra.
Coordenadora do Programa de Pós-Graduação
Banca Julgadora:
______________________________________
Prof. Wornei Silva Miranda Braga, Dr.
Presidente
______________________________________
Profª. Ione Rodrigues Brum, Dra.
______________________________________
Prof. Luiz Ferreira, Dr.
DEDICATÓRIA
À memória de meus sogros, Armando e Lília Centeio dos Santos. Aos meus
amores e afetos Lília Célia, Geíze e Igor Praia, e às minhas queridas famílias Grijó e
Praia.
AGRADECIMENTOS
Minha gratidão a todos os que se alegraram comigo nesta empreitada, e
também aos que choraram comigo.
Ao meu irmão Jair Grijó Praia que aposta em mim sem motivo algum.
Muito grato ao Doutor Professor Wornei de Miranda Braga, meu orientador pela
sua ajuda sábia e sinérgica; à Doutora. Maria das Graças Vale Barbosa, exemplo
para mim de determinação, pelo incentivo e confiança.
Grato à ajuda e amizade inestimáveis da Sta. Cristiane da Costa Souza.
Não posso deixar de agradecer aos funcionários do ambulatório e do Serviço
de Arquivo Médico – SAME da FMT-AM.
Agradeço aos funcionários do Centro de Referência de Imunizações Especiais CRIE. Às bibliotecárias da FMT-AM: Arthemísa Seabra da Silva, Melquizete de
Souza Almeida e Gisella Paula G. Gonzáles, que trabalharam silenciosa e
proficuamente para que este estudo acontecesse.
Especial reconhecimento às Acadêmicas de Medicina, Júlia Beatriz Coelho e
Kelly Simone Castro dos Santos pela inestimável ajuda e tolerância.
Meu agradecimento pelo o apoio recebido dos funcionários do laboratório de
análises clínicas e da Gerência de Virologia da FMT-AM.
Obrigado à minha madrinha e tia Dolores Praia, ela sabe o por quê.
Agradeço também ao apoio da SUFRAMA e Fundação MURAKI.
Também sou grato a muitos pensadores pela inspiração e influência ao estudar
assunto tão relevante.
Aos nobríssimos colegas do mestrado que me desejaram sucesso, ou não.
Quero ser grato a quem não foi lembrado(a) aqui nestas linhas, porém torceu,
apostou e me ajudou nesta empreitada.
Eterno reconhecimento às pacientes, em cujos olhares eu identificava a cada
consulta toda perplexidade sobre o que lhe sucedia associada à centelha de
esperança da cura para si e de proteção do ente querido ainda no útero; Eu tentei.
Finalmente, não obstante, o dever de agradecer logo no princípio desta página,
toda minha ação de graça a Quem, por seu intermédio, Dele, todas as coisas se
fizeram, e, sem Ele, nada do que foi feito se fez: Jesus Cristo, Filho de DEUS.
Epígrafe
“Certamente ele tomou sobre si as nossas
enfermidades, e as nossas dores levou sobre si; e nós o
reputávamos por aflito, ferido de Deus, e oprimido.
Mas ele foi traspassado pelas nossas transgressões, e
moído pelas nossas iniqüidades; o castigo que nos traz a paz
estava sobre ele, e pelas suas pisaduras fomos sarados”.
Isaias 53: 4-5
RESUMO
A hepatite B é uma doença que pode levar a severas conseqüências se transmitida
verticalmente, porém a identificação das grávidas com risco de transmitirem o vírus da
hepatite B (VHB) para seus filhos trás a esperança de poder prevenir esses efeitos através
da imunização passiva e ativa dos bebês logo após o nascimento. A infecção pelo VHB
representa um importante problema de saúde pública na Amazônia ocidental. Há poucos
estudos sobre a prevalência do VHB em grávidas no norte do Brasil. O objetivo do estudo foi
analisar a clínica e a epidemiologia de grávidas portadoras do AgHBs e identificar
evidências da possibilidade da transmissão vertical. Foi realizado um estudo descritivo
retrospectivo com base na busca de dados de mulheres grávidas submetidas ao
rastreamento do VHB na gerência de virologia da Fundação de Medicina Tropical do
Amazonas (FMTAM) e outro prospectivo com grávidas acompanhadas no ambulatório
específico de gravidez e doenças infecciosas e parasitárias da FMTAM. Foi encontrada uma
prevalência de 2,5% (IC 95% 1,9 - 3,1%) de portadoras do AgHBs. Foram encontradas
mães reativas para o AgHBe e positivas para o teste da PCR, bem como quatro recémnascidos apresentaram PCR reativa para o VHB-DNA em amostras do cordão umbilical, e
um bebê das grávidas do estudo retrospectivo apresentou reatividade para o AgHBs,
demonstrando a possibilidade da transmissão vertical. Embora algumas mães tenham
apresentado alterações no exame físico e laboratorial não é possível inferir que as mesmas
fossem decorrentes da infecção viral, pois tais alterações são encontradas no estado
fisiológico da gravidez. Em 53,6% dos recém-nascidos de mães portadoras do VHB foram
realizados os procedimentos de imunoprofilaxia recomendados, 10,7% dos recém-nascidos
não receberam a intervenção e em 35,7% não foi possível ter sua situação definida. Este
estudo foi capaz de demonstrar a possibilidade de transmissão vertical do VHB na
população estudada, bem como identifica problemas na saúde pública em face à
necessidade de se cobrir 100% dos partos de portadoras do VHB com medidas de
profilaxia. Recomenda que o rastreamento do VHB em grávidas deva ser prioridade básica
na região.
Palavras chaves: Hepatite viral B, AgHBs, AgHBe, PCR, Transmissão vertical,
gravidez
ABSTRACT
Hepatitis B may leads to severe consequences if transmitted vertically. Nevertheless,
the identification of pregnant women at risk of transmission brings great hope due to the
possibility of prophylactic measures just after the delivery. Hepatitis B infection is a serious
public health problem at the western Amazon. There is little literature about the prevalence of
HBV infection within pregnant women in the north region of Brazil. The main objective of this
study was to describe the most important epidemiological and clinical features of pregnant
women HBsAg carriers and to identify the possibility of vertical transmission of HBV within
the study population. We did a descriptive study with a retrospective analysis of data of
pregnant women serologically screened at the Fundação de Medicina Tropical do Amazonas
(FMTAM) and a prospective study with pregnant women HBsAg carriers assisted at the
outpatient’s clinic for pregnancy and infectious diseases of the FMTAM. We found a
prevalence of HBsAg carriers of 2.5% (95% CI 1.9 – 3.1%). We also found the presence of
women carries of HBeAg and PCR for the HBV-DNA reactive in samples of mother and
umbilical cord, and one baby of the retrospective study was reative for HBsAg,
demonstrating the possibility of vertical transmission of HBV within study population. We
could not demonstrate association with clinical finds and HBV infection, as those
abnormalities found are also common during pregnancy. 53.6% of the mothers were assisted
at the delivery, 10.7% of the newborns did not get the immunoglobulin and the vaccine and
of 35.7% we could not define their real situation. We were able to demonstrate with this study
the possibility of vertical transmission of HBV infection within the study population, it also
identifies problems with the public health care, in face of the need of covering 100% of births
of mothers HBsAg carries with prophylactic measures, and highlight the importance of the
screening of HBV infection among pregnant women in this specific region.
Key words: Hepatitis B, HBsAg, HBeAg, PCR, vertical transmission, pregnancy
LISTA DE TABELAS
TABELA 1 Perfil sorológico dos filhos das pacientes grávidas portadoras do
AgHBs....................................................................................................................... 40
TABELA 2 Demonstrativo do status sorológico de infecção pelo VHB entre mães
que retornaram ao ambulatório de doenças infecciosas e parasitárias para grávidas
.................................................................................................................................. 40
TABELA 3 Demonstrativo do status sorológico de infecção pelo VHB entre parentes
que retornaram ao ambulatório ................................................................................ 40
TABELA 4 Perfil clínico e sorológico das pacientes grávidas acompanhadas no
ambulatório especializado da FMT-AM .................................................................... 43
TABELA 5 Perfil sorológico de mães PCR reativas ................................................ 44
TABELA 6 Perfil sorológico de mães de recém-nascidos PCR reativos ................. 44
TABELA 7 Profissão exercida pelas grávidas no primeiro atendimento ................. 47
LISTA DE FIGURAS
FIGURA 1 Prevalência do AgHBs em grávidas ..................................................... 36
FIGURA 2 Faixa etária das grávidas ...................................................................... 37
FIGURA 3 Prevalência do AgHBe em grávidas testadas ...................................... 37
FIGURA 4 Área de moradia das grávidas .............................................................. 38
FIGURA 5 Naturalidade das grávidas .................................................................... 39
FIGURA 6 Idade das grávidas acompanhadas ...................................................... 41
FIGURA 7 Exame físico das grávidas .................................................................... 45
FIGURA 8 Local de moradia das pacientes grávidas atendidas ............................ 46
FIGURA 9 Número de grávidas naturais do Estado do Amazonas ....................... 46
FIGURA 10 Naturalidade das grávidas acompanhadas na FMT-AM ...................... 47
FIGURA 11 Análise do Tempo de Atividade de Protrombina (TAP) ........................ 48
FIGURA 12Níveis de hemoglobina em grávidas AgHBs reativas atendidas na
FMTAM ..................................................................................................................... 49
FIGURA 13 Amostragem por número de gestação das pacientes atendidas .......... 50
LISTA DE ABREVIATURAS
AgHBc
Antígeno core do vírus da hepatite B
AgHBe
Antígeno originado do core viral, indicativo de replicação do vírus da
hepatite B.
AgHBs
Antígeno de superfície do vírus da hepatite B
ANTI-HBc
Anticorpo anticore
ANTI-HBcT
Anticorpo anticore total
ANTI-HBe
Anticorpo que indica resposta imune parcial com diminuição da replicação
ANTI-HBsAg
Anticorpo que indica resposta imune com cura da infecção ou resposta
vacinal
ANTI-HDT
Anticorpo anti-hepatite D
CRIE
Centro de Referência de Imunobiológicos Especias
FMTAM
Fundação de Medicina Tropical do Amazonas
HVD
Vírus da hepatite D
PCR
Reação em cadeia da Polimerase
UEA
Universidade Estadual do Amazonas
UFAM
Universidade Federal do Amazonas
VHB
Vírus da hepatite B
VHB-DNA
Ácido desoxidoribonucleico do vírus da hepatite B
SUMÁRIO
1. INTRODUÇÃO
1.1
Hepatite B
2. OBJETIVOS
1
1
10
2.1
Objetivo Geral
10
2.2
Objetivos Específicos
10
3. METODOLOGIA
11
3.1
Modelo de Estudo
11
3.2
Universo de Estudo
11
3.2.1. População de Estudo
11
3.2.2. Participantes
12
Coleta das Amostras
13
3.3.1. Análise Sorológica das Amostras
13
3.4
Fonte de Erros
14
3.5
Análise dos Dados
15
3.3
4. RESULTADOS
16
4.1
Estudo Retrospectivo
16
4.2
Estudo Prospectivo
20
5. DISCUSSÃO
29
6. CONCLUSÃO
34
7. REFERÊNCIAS BIBLIOGRÁFICAS
35
8. ANEXOS
41
Anexo 1 - Perfil sorológico das pacientes no estudo retrospectivo
42
Anexo 2 - Perfil Clínico e Laboratorial das Pacientes Grávidas Acompanhadas
no Ambulatório Especializado da FMT-AM
43
Anexo 3 – Folder Informativo
44
Anexo 4 – Questionário
45
Anexo 5 – Termo de Consentimento Livre e Esclarecido
49
Anexo 6 – Carta de Apresentação
51
1
1 INTRODUÇÃO
A afirmação de que a hepatite viral constitui-se em uma das principais causas de
doença aguda e crônica e de mortalidade em todo o mundo (HADLER et al, 1987),
constitui-se ainda no início do século 21, uma assertiva atual e pertinente aos
desafios a serem enfrentados pela ciência. Neste momento, vários são os vírus
identificados como causadores de hepatites: o vírus da hepatite A (VHA), o vírus da
hepatite B (VHB), o Vírus da hepatite Delta (VHD), vírus defectível associado sempre
ao VHB, e já uma série de outros estão sendo reconhecidos, como os vírus da
hepatite C (VHC), e da hepatite E, (VHE), que repercute seriamente sobre a
gestação com a mortalidade em gestante atingindo cerca de 15-20%, e o vírus da
hepatite G (VHG).
1.1 Hepatite B
A hepatite viral tipo B é um importante problema de saúde pública em todo o
mundo, sendo endêmica em algumas regiões do planeta, especialmente no sudeste
da
Ásia,
África
Equatorial
e
localidades
da
Amazônia
(BRAGA,
2001;
CUNNINGHAM, 1993; FERREIRA, 2000). É uma infecção universalmente
prevalente, embora seja com distribuição espacial heterogênea. Ela é responsável
por expressivo número casos de cirrose hepática e carcinoma primário do fígado, em
conseqüência de infecção crônica que parte de suas vítimas desenvolve – estado de
portador sintomático ou não (SOUTO et al, 2004).
A Organização Mundial de Saúde (OMS) estima a existência de cerca de 325
milhões de portadores crônicos e que aproximadamente dois bilhões de pessoas já
tiveram contato com o VHB (BRASIL, 2003). Aproximadamente 40% desses
portadores adquirem a infecção por transmissão perinatal, enquanto 35 a 40 % se
infectam durante a idade pré-escolar e apenas 10 a 15% na vida adulta (OLIVEIRA
et al, 1993). Os países mais afetados são aqueles com baixo desenvolvimento
socioeconômico. Então, extensas regiões tropicais apresentam-se entre as porções
da superfície terrestre de mais alta prevalência da infecção (SOUTO et al, 2004).
2
Critérios estabelecidos pela Organização Mundial de Saúde classificam as
regiões do planeta em três áreas distintas de acordo com as taxas de prevalência do
VHB: alta endemicidade em que as taxas de prevalência excedem a 8% e onde 75%
da população se infectam precocemente na infância; média endemicidade, nas quais
2 a 7% da população são portadores do vírus e mais de 50% tiveram uma infecção
pelo vírus no passado; e as de baixa endemicidade nas quais menos de 2% da
população são portadores do VHB (BRASIL, 2003).
No Brasil a prevalência de hepatite B apresenta padrão heterogêneo sendo
descritas taxas de prevalência de anti HBC em crianças no primeiro ano de vida, de
mais de 3%, indicando a importância da rota vertical de transmissão (SILVEIRA,
1999). A República Federativa do Brasil é um país que apresenta uma diversidade
étnica, econômica e regional, em cujo território a infecção pelo VHB também tem
distribuição muito heterogênea, com tendência a aumentar no sentido sul-norte
(SOUTO et al, 2004).
A região sul do país é considerada de baixa endemicidade; as regiões oeste,
nordeste e sudeste são áreas de endemicidade intermediária (FUNASA, 2003);
certas localidades da bacia Amazônia, onde se tem identificado as hepatites como
uma causa importante de morbiletalidade (BENSABATH, 1987; FUNASA, 2003) e
ainda o estado do Espírito Santo e a região oeste do estado de Santa Catarina são
considerados de alta endemicidade onde a prevalência do AgHBs é superior a 7%
(FUNASA, 2003).
O VHB foi o primeiro vírus causador de hepatites em humanos a ter seu genoma
identificado e caracterizado. Em 1963 Blumberg et al descobriram uma seqüência de
antígeno, que denominam antígeno Austrália, no sangue de arborígenos
australianos (JIA-HORNG, DING-SHINN, 2002). Posteriormente, em 1970 Dane et al
usando microscopia imune-eletron descreveu as partículas de 42 nm que são os
virions da hepatite B; o termo antígeno Austrália é hoje identificado como a antígeno
de superfície do VHB, denominado AgHBs e relacionado com o envelope viral (JIAHONRG, DING-SHINN, 2002).
3
O VHB compreende um pequeno número de vírus que compartilham uma série
de características, como o tropismo pelos hepatócitos e um genoma constituído de
uma molécula de DNA de fita parcialmente dupla. No gênero Orthohepadnavirus
estão
classificados
os
vírus
que
infectam
os
mamíferos
e
no
gênero
Avihepadnavirus, os vírus que infectam as aves. Embora os hepadnavírus
apresentem uma série de características em comum com os anteriores, existem
diferenças com os genomas dos vírus das aves que são menores que os dos vírus
de mamíferos (GOMES, 2003).
O estudo da biologia molecular do VHB está dificultado com a incapacidade
deste vírus de infectar e se propagar em linhagens celulares convencionais; o cultivo
do VHB só ocorre em células primárias de origem humana, porém a disponibilidade
de sistemas como linhagem de hepatomas que suportam a replicação do VHB
quando transfectadas com genoma viral clonado podem produzir formas virais
replicativas intermediárias e estruturas semelhantes às partículas infecciosas
(GOMES, 2003).
A infecção pelo vírus da hepatite B pode causar doença hepática aguda ou
crônica, incluindo cirrose e carcinoma hepatocelular (JIA-HORNG, DING-SHINN,
2002). As injúrias às células hepáticas são imunologicamente moduladas, e a
história natural da infecção crônica pode ser dividida em três fases baseadas na
relação vírus-hospedeiro: tolerância imunológica, limpeza imunológica e integração
do genoma viral. Quatro sorotipos (adw, ayw, adr e ayr) e sete genótipos (A/G) do
VHB foram identificados e demonstrado suas distintas distribuições geográficas (JIAHORNG, DING-SHINN, 2002; RUIZI; QUIJANO, 2003).
O VHB é um vírus formado por DNA, hepatotrópico, pertencente à família
Hepadnaviridae (ARRAES, 2003; CUNNINGHAM, 1993) que tem uma estrutura
complexa
com
duplo
envoltório;
o
externo
contém
proteínas
antigênicas
denominadas de antígenos de superfície do VHB (AgHBs); o interno constitui
juntamente com o DNA e uma enzima (DNA- polimerase), o core, que apresenta
proteína antígena de centro estrutural (AgHBc) e um antígeno solúvel chamado
AgHBe. Os antígenos dão origem a peptídeos que uma vez expressos nos
4
hepatócitos, estimulam a resposta imune celular buscando a supressão da infecção
viral ( SILVA, 2003; TORRES, 1993).
A transmissão do VHB se faz fundamentalmente através das vias parenteral e
sexual, sendo considerada uma doença sexualmente transmissível. A transmissão
vertical também é causa freqüente de disseminação do VHB e representa a principal
via de dispersão do VHB nas regiões de altas prevalências (ARRAES, 2003;
BRASIL, 2003; CDC, 1988; FERREIRA, 2000;). São também importantes na
epidemiologia do VHB, os contatos intradomiciliares e a exposição precoce, durante
a infância em áreas endêmicas (BRASIL, 2003; KIESSLICH, 2003).
De modo geral, a taxa de letalidade da infecção pelo VHB em pacientes
hospitalares é de 0,8 a 2%, podendo ser maior em indivíduos acima dos 40 anos de
idade e naqueles em que há associação com o VHD. No Brasil, a taxa de
mortalidade relaciona à infecção pelo VHB é de 0,6 por 100.000 habitantes
(FONSECA, 2002; FUNASA, 2003).
Em recém-nascidos de mães portadoras do VHB, a cronicidade é a regra e
ocorre
em
85
a
90%
dos
infectados
(ARRAES,
2003;
BRASIL,
2003;
CUNNINGHAM, 1993; FERREIRA, 2000). A transmissão perinatal do VHB é a mais
importante causa de infecção crônica da hepatite B, apesar de existir a imunização
passiva e ativa no nascimento (VAN NUNEN, 2000). O risco de transmissão mãefilho pode ser previsto pelos níveis de VHB-DNA, bem como a evolução crônica em
recém-natos infectados (KIESSLICH, 2003; VAN NUNEN, 2000).
As técnicas utilizadas no diagnóstico laboratorial incluem ensaio imunoenzimático
e radioimunoenzimático que procuram identificar no soro os antígenos AgHBs e
AgHbe e os anticorpos AntiHBc, AntiHBe, AntiHBs. Estas revelam-se estratégicas
não apenas para o diagnóstico, mas são úteis no seguimento da infecção viral,
assim como na avaliação do estado clínico do paciente e na monitorização
terapêutica (FERREIRA, 2000).
A fase aguda da infecção caracteriza-se pela presença do antígeno de superfície
do VHB, AgHBs, anticorpos IGM Anti-HBc e AgHBe. Na convalescença os antígenos
5
desaparecem e surgem anticorpos do tipo Anti-HBs, Anti-HBc e Anti-Hbe.
O
anticorpo Anti-HBs é protetor e indicativo de recuperação ou cura, além de
imunidade para reinfecções, ele também é detectado em pessoas que tenham
recebido a vacina para hepatite B (FERREIRA, 2000; MAHONEY ,1999).
Em
indivíduos
com
hepatite
crônica
a
AgHBs
permanece
detectável
persistentemente. A hepatite crônica é definida sorologicamente como a persistência
do antígeno de superfície do VHB por mais de seis meses (FERREIRA, 2000). Na
sua longa duração observa-se duas fases distintas e de duração variável; na
primeira, que em geral corresponde ao período mais precoce da doença, há intensa
replicação viral com a presença no soro do AgHBs, do AgHBe e do próprio DNAVHB. Este período persiste por vários anos e ao longo do tempo estes pacientes
tendem a permanecer positivos para o anti-HBe, indicando que o grau de replicação
reduziu (FERREIRA, 2000 MINISTÉRIO SAÚDE, 2003).
Enfim, através da biópsia hepática se pode avaliar os pacientes cronicamente
infectados pelo VHB, mediante a graduação da magnitude do processo inflamatório
e da fibrose e ainda através de técnicas de imunohistoquímica, documentar a
presença de antígenos S e Core do VHB no tecido (FERREIRA, 2000).
A transmissão vertical, aquela de mãe para filho, pode acontecer desde a
concepção até o final da gravidez, também no período perinatal que termina no
primeiro mês de vida e ao longo dos primeiros anos de vida, particularmente no
primeiro ano de vida (RUIZ-MOREÑO, LEAL, MILLÁN, 2003).
Fatores como a alta carga viral, altos títulos de antígenos de superfície (AgHBs),
bem como do marcador de replicação viral, o AgHBe, tornam o risco da transmissão
vertical aumentado. A descoberta do antígeno ‘e’ do VHB e a sua relação com o
número de partículas virais circulantes, também estabelecem a íntima relação que
existe entre transmissão vertical e o status materno deste marcador viral. Mulheres
VHB com AgHBs e AgHBe positivas são capazes de transmitir a doença para seus
conceptos, enquanto que se forem negativas para o AgHBe e positivas para AntiHBe não são capazes de transmitir a infecção (CUNNINGHAM, 1993; DAVIES,
2003; XU, 2003).
6
A infecção aguda complica 0,1% das gestações, sendo o risco de contaminação
fetal mínimo no primeiro trimestre, podendo chegar a 70% no segundo e terceiro
trimestre.
A infecção intra-uterina ocorre em 5% dos casos, a grande maioria acontece
durante o trabalho de parto e nascimento pela ingestão de sangue e de secreções
maternas (ARRAES, 2003; CUNNINGHAM, 1993; RUOCCO, 2003).
Na infecção perinatal, a história natural da infecção crônica do VHB pode ser
dividida em três fases baseadas na interação hospedeiro-vírus; na primeira fase há
uma replicação intensa viral ou tolerância imune, onde os pacientes são AgHbe
positivos
e
têm níveis
elevados
do
DNA-VHB,
o
paciente
apresenta-se
assintomático, concentração sérica normal da aminotransferase e mínima lesão
histológica
hepática (JIA-HORNG,
DING-SHINN,
2002); na
segunda fase,
caracterizada pelo baixo nível de replicação viral, alguns portadores crônicos do
VHB assintomáticos passam a apresentar sinais e sintomas sugestivos de hepatite
aguda ou períodos de agudizacão, a lesão histológica já se acentua pela eliminação
dos hepatócitos onde ocorrera alta replicação viral; a terceira fase há persistência
sérica do AgHBs, mas o AgHBe torna-se indetectável; é a fase não replicadora e os
portadores crônicos geralmente estão assintomáticos e a doença hepática torna-se
inativa.
O célere surgimento do Anti-HBe no curso natural da infecção crônica do VHB
geralmente indica evolução favorável, pois costuma estar associada com a parada
de replicação do vírus e a não progressão da doença hepática (JIA-HORNG, DINGSHINN, 2002).
Assim, os riscos de transmissão vertical estão aumentados quando a mãe
apresenta alta carga viral, altos títulos de marcadores como o AgHBs e a presença
do marcador de replicação viral, AgHBe;
além do que o risco de infecção do
concepto após hepatite aguda tipo B, autolimitada, ocorrida na gravidez depende do
período em que
a infecção ocorreu, sendo maior se ela ocorreu no terceiro
trimestre, neste caso 80 a 90% dos neonatos serão AgHBs positivos em contraste
7
com 10% de positivos se a doença ocorrer no primeiro trimestre (ARRAES et al,
2003).
Quando a mãe tem AgHBe e não é administrada imunoprofilaxia ao recémnascido, o risco de transmissão oscila entre 70-90%; uma vez infectado, tem 85-90%
de probabilidade de evoluir para portador crônico da doença e, deles mais que 25%
evoluem com cirrose ou hepatocarcinoma (RUIZ-MOREÑO, 2003).
A elevada tendência do recém-nascido, que adquire o VHB através da
transmissão vertical, de desenvolver a infecção crônica poderia ser explicada pela
dificuldade do neonato em desenvolver adequadamente uma resposta imunológica
decorrente da elevada exposição do feto ao vírus durante a gestação, isto é, a
passagem precoce de AgHBe através da placenta poderia induzir progressiva
tolerância das células T fetais aos antígenos alvos, AgHBc e AgHBe, expressados
nas membranas dos hepatócitos, levando à cronicidade da infecção viral em
infectados perinatalmente (RUIZ-MOREÑO, 2003; SILVEIRA, 2004).
A transmissão perinatal do VHB decorre da exposição das mucosas fetais ao
sangue ou fluidos maternos infectados, isto pode acontecer via placentária por
hemorragias, mas geralmente ocorre durante o parto ou ocasionalmente pósnascimento, embora raramente na amamentação (JOSHI, HEATHCOTE, 2004). Há
uma marcante associação entre a transmissão intra-uterina do VHB e a infecção
pelo vírus nas células capilares endoteliais placentárias (XU, 2003), porém a
infecção do neonato pela ingestão de material infectado durante o trabalho de parto
e pós-parto imediato é mais comum (CUNNINGHAM, 1993).
O risco permanece alto da transmissão ocorrer nos primeiros anos de vida da
criança (JOSHI; HEATHCOTE, 2004).
Os procedimentos invasivos durante o pré-natal, como a aminiocentese, parecem
ter pouca repercussão na transmissão vertical do VHB (CUNNINGHAN, 1993;
DAVIES, 2003). Porém, alguns autores defendem que a transmissão pode resultar
de procedimentos intra-uterinos, como a aminiocentese, devendo, portanto, ser
evitados (JOSHI; HEATHCOTE, 2004). Ainda que índices reduzidos de transmissão
8
perinatal sejam observados com o parto cirúrgico cesariano, comparado com o parto
natural, vaginal, cesariana de rotina não está recomendada (JOSHI, HEATHCOTE,
2004).
A hepatite B é a principal causa de icterícia na gravidez, porém, muitas vezes
seus sinais e sintomas podem ser confundidos com outras patologias que acometem
a gestante como a hiperemêse gravídica ou as infecções urinárias, por exemplo
(ARRAES, 2003; RUOCCO, 2003). A evolução da infecção pelo vírus B em
mulheres não parece ser alterada pela gestação, pelo menos em países
desenvolvidos; e a hepatite fulminante que ocasionalmente complica, não parece ter
maior prevalência durante a gravidez; a gestação também pode ter seu curso
alterado por esta doença levando a partos prematuros e crescimento intra-uterino
restrito (CUNNINGHAM, 1993; RUOCCO, 2003).
O VHB está presente no leite materno, havendo contra-indicação formal da
amamentação (RUOCCO, 2003), embora a transmissão perinatal não seja
incrementada pela a amamentação, particularmente se a imunoprofilaxia tiver sido
administrada (JOSHI, HEATHCOTE, 2004).
A transmissão vertical do VHB pode ser evitada com a administração precoce da
imunoglobulina B, seguida da vacinação específica em neonatos, filhos de mulheres
com hepatite B previamente identificadas, durante o pré-natal, pela triagem
sorológica a que mulheres grávidas são submetidas (CUNNINGHAM, 1993; BRASIL,
2003), rotina já adotada no Brasil.
No estado do Amazonas a hepatite B representa um importante problema de
saúde pública, pois que uma grande parte de sua população é jovem e cresce às
custas de imigrações e de alta taxa de natalidade com gravidezes nem sempre
planejadas e assistidas pelo sistema de saúde.
Assim, faz-se de grande necessidade o conhecimento da prevalência da infecção
pelo VHB nas mulheres grávidas no Amazonas. Bem como, estabelecer o risco de
transmissão vertical de modo a oferecer, às autoridades de saúde, números e dados
que ajudem a criar estratégias que contribuam para o bem-estar populacional,
9
sobretudo para as mulheres e crianças, que vivam com indivíduos portadores do
AgHB.
10
2 OBJETIVOS
2.1 Geral
Determinar a prevalência de VHB nas grávidas que procuraram a gerência de
virologia da FMT-AM para realizar testes sorológicos da rotina do pré-natal e
naquelas acompanhadas no ambulatório de doenças Infecciosas e parasitárias e
gravidez, bem como em seus conviventes e recém-nascidos, e identificar a
ocorrência da transmissão vertical do vírus.
2.2 Específicos
1. Determinar a porcentagem de marcadores sorológicos do VHB em grávidas
que procuraram a FMTAM para testes de rotina do pré-natal.
2. Verificar o risco de transmissão vertical na população estudada: através da
detecção do DNA no soro da grávida AgHBs positiva e do sangue do cordão
umbilical.
3. Identificar possíveis fatores determinantes de transmissão do VHB na
população estudada.
4. Avaliar impacto clínico da presença do VHB na gravidez na população
estudada.
5. Verificar a porcentagem da intervenção.
11
3 METODOLOGIA
3.1 Modelo de estudo
Este é um estudo descritivo de caráter retrospectivo e prospectivo onde se
mediu a prevalência de infecção pelo VHB em gestantes atendidas no ambulatório
de doenças infecciosas e gravidez da FMT-AM e naquelas que procuraram a
gerência de virologia da Fundação de Medicina Tropical do Amazonas no período do
mês de julho de 1996 a julho do ano de 2005, avaliou-se os aspectos clínicos mais
importantes da infecção do VHB na gravidez, buscando identificar indicativos da
possibilidade de transmissão vertical em ambas abordagens.
3.2 Universo de estudo
3.2.1 População de estudo
O estudo teve como alvo a população feminina grávida da demanda
espontânea submetida a testes sorológicos do VHB da rotina do pré-natal ou que
foram encaminhadas à FMT-AM ou procuraram o serviço de virologia do mesmo
para submeterem-se por solicitação do pré-natalista para sorologia para o AgHBs.
O número de mulheres investigadas foi definido de acordo com o número de
grávidas que procuraram a FMT-AM para realização de testes sorológicos para o
VHB, durante o período do estudo. Compomos a amostra nas duas abordagens com
89 portadoras do AgHbs.
O estudo avaliou duas populações distintas de mulheres grávidas, de acordo
com a natureza do estudo:
1. População do estudo retrospectivo – esta população foi composta por
indivíduos que realizaram testes sorológicos de screening durante a gravidez, no
período de julho de 1996 até setembro de 2003.
2. População do estudo prospectivo – esta população foi composta por
mulheres grávidas, residentes em Manaus, apresentando AgHBs positivo, que foram
12
acompanhadas no ambulatório especificamente criado para este fim, no período de
setembro de 2003 a julho do ano de 2005.
3.2.2 Participantes
As grávidas com AgHBs positivo que foram selecionadas para participarem do
estudo retrospectivo e prospectivo foram incluídas a partir do banco de dados da
Gerência de Virologia e convidadas a participar após caracterização do perfil
sorológico de infecção pelo VHB.
•
Estudo retrospectivo: as mulheres grávidas identificadas no banco de
Dados do laboratório de Virologia da FMT-AM como portadoras do AgHBs foram
visitadas e convidadas a participar deste estudo. Depois de assinado o termo de
consentimento informado, as mulheres, que aceitaram, foram submetidas à
entrevista e preenchimento do questionário a fim de identificar possíveis fatores
determinantes de transmissão do VHB. Também foi coletado sangue da criança
nascida na ocasião do diagnóstico sorológico e dos conviventes da casa dela.
Foram incluídos os contatos intradomiciliares que habitam com os casos índices, os
que tiveram contato íntimo com as gestantes
AgHBs positivas,
quais sejam:
companheiro, parceiro, esposo, filho(s) e outros. Foram excluídos aqueles a quem
não tivemos acesso.
A partir da identificação das reativas para o AgHBs criou-se um banco de dados
em planilha do Microsoft Excel e foi iniciado um programa de visita aos domicílios
das mulheres, em cujo prontuário ou requisição de exames
encontramos o
endereço da mesma, quando então as convidamos para comparecer ao ambulatório
de gravidez de doenças infecciosas e parasitárias da FMT-AM, além do que era
também deixado folder informativo sobre hepatite B e gravidez, elaborado para o
presente projeto. Anexo 3.
Após concordarem formalmente em participar da pesquisa assinando o
consentimento livre e esclarecido foi preenchido questionário e coletada amostra de
13
sangue para a realização de testes sorológicos para toda a família, sendo oferecidas
também informações sobre a hepatite B.
•
Estudo prospectivo: As gestantes com resultado positivo que
conceberam no período de desenvolvimento do estudo, outubro de 2003 a julho de
2005, também foram convidadas a participar do estudo. Depois de assinado o termo
de consentimento informado, foi realizado inquérito sorológico familiar e a gestante
foi acompanhada durante o período da gravidez e orientada sobre a importância da
coleta do sangue do cordão umbilical do recém-nascido pela equipe da maternidade
que assistiu ao parto. Bem como foi informada do programa de prevenção da
transmissão vertical do VHB através da administração da vacina e imunoglobulina
específica disponibilizada pelo Ministério da Saúde do Brasil à FMT-AM. Foram
incluídos os contatos intradomiciliares que habitam com os casos índices, os que
tiveram contato íntimo com as gestantes AgHBs positivas, quais sejam companheiro,
parceiro, esposo, filho(s) e outros. Foram excluídos aqueles a quem não tivemos
acesso.
3.3 Coleta das amostras
Foram coletados 10 ml de sangue, de cada indivíduo selecionado, por punção
venosa com sistema vascutainer em dois tubos distintos, sendo um (5 ml) sem
conservantes e outro com EDTA (K 3 ).
Foram coletados 2 ml do sangue do cordão umbilical do recém-nascido, no
momento do parto, após laqueadura tubária ou dequitação placentária, mediante
seringa descartável, acondicionando-se 1 ml em tubo sem conservante e 1 ml em
outro com EDTA.
3.3.1 Análise sorológica das amostras
Foi realizada pelo método imunoenzimático (ELISA), utilizando-se kits
comerciais, obedecendo aos seguintes critérios: 1 – Todas as amostras foram
testadas para o AgHBs e Anti-HBc total; 2 – As amostras reativas para o AgHBs
foram testadas para o AgHBe e o Anti-AgHBe; 3 – Todas as amostras foram
14
testadas para VHD e VHC; 4 – No estudo prospectivo o sangue do cordão do bebê
foi analisado através da reação de polimerização em cadeia para o DNA do vírus da
hepatite B.
Todo o pessoal da FMT-AM envolvido no programa, tais como investigadores,
bioquímicos, técnicos e estudantes foram adequadamente vacinados contra hepatite
B, com títulos de Anti-HBs superiores a 10 UI/l. Medidas gerais de biossegurança,
visando proteção dos indivíduos incluídos no estudo e técnicos, por barreiras, com o
uso de luvas, máscaras e óculos de proteção, descarte seguro de agulhas e
seringas foram adotados durante a obtenção, o manuseio e processamento das
amostras.
3.4 Fontes de erros
Os
possíveis
erros
potenciais
que
talvez
tenham
sido
introduzidos
inadvertidamente pelo desenho do estudo, particularmente os relacionados à
seleção dos indivíduos a serem incluídos, são os seguintes:
Viés de seleção: como a FMT-AM é referência no diagnóstico das hepatites
virais e a gerência de virologia atende grande parte da demanda do pré-natal da
cidade de Manaus e se constitui em referência para alguns municípios do Estado,
acreditamos ter avaliado uma amostra bastante representativa.
Viés de perda: nos casos de mudança de endereço, óbito, recusa espontânea
em não participar da pesquisa ou procedência de alguma cidade do interior do
Amazonas. Para buscar amenizar esse erro, foram feitas visitas aos domicílios das
mulheres que fizeram parte da população de estudo.
Viés de classificação: problemas na classificação sorológica dos indivíduos
estudados podem ter decorrido devido à qualidade dos kits utilizados. Utilizamos os
melhores kits reconhecidamente de melhor recomendação existente no mercado
para procurar minimizar problemas com a sensibilidade desses produtos.
15
3.5 Análise dos dados
Os dados foram registrados em um banco de dados. Análises estatísticas foram
conduzidas utilizando-se pacotes de software, incluindo o Epi-Info e SPSS.
16
4 RESULTADOS
O estudo foi realizado de outubro de 2003 a julho de 2005 e a análise
compreende duas abordagens: um estudo retrospectivo e outro prospectivo, ambos
de caráter descritivo, onde se avaliou pacientes gestantes da demanda espontânea
da Fundação de Medicina Tropical do Amazonas (FMT-AM). Serão comentados
separadamente e os pontos comuns e inconsistências nas conclusões da
dissertação.
4.1 Estudo retrospectivo
Foi conduzido um estudo retrospectivo com base na busca de dados de
mulheres grávidas submetidas ao rastreamento do VHB na Gerência de Virologia da
FMTAM, no período de julho de 1996 a outubro de 2003.
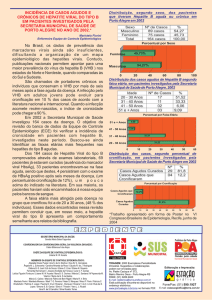
Das 2.470 mulheres grávidas que realizaram sorologia para o VHB, no período,
61 apresentaram reatividade para o AgHBs representando uma prevalência de 2,5%
(IC 95% 1,9-3,1%) (Figura 1).
AgHBs; 2,5%
Não reativas;
97,5%
Figura 1 – Prevalência do AgHBs em grávidas atendidas na FMTAM no período
entre Julho/96 a Out/2003.
17
As pacientes apresentavam idade que variava de doze a quarenta e sete anos,
média de 29 anos. A maior prevalência do AgHBs foi encontrada na faixa etária dos
20 aos 30 anos (Figura 2).
18
Número de pacientes
16
14
12
10
8
6
4
2
0
12 a 15
16 a 20
I21 a 25 I26 a 36 31 a 35
> 35
Sem
registro
Faixa Etária
Figura 2 – Distribuição da faixa etária das grávidas incluídas no estudo.
Apenas 11 das 61 foram testadas para antígeno "e” (AgHBe) com uma
prevalência de 27% (3/11) (Figura 3).
AgHBe
27%
Não reagentes
73%
Figura 3 – Prevalência do AgHBe em grávidas testadas.
18
Vinte e duas pacientes tinham registro de uma segunda amostra testada para o
AgHBs, desta, duas (9%) apresentaram-se não reagentes para o antígeno, trinta e
nove não realizaram um segundo teste. Dezessete apresentavam AntiHBcT
reagentes, duas negativas. Em quinze pacientes encontramos 3 (20%) reagentes
para o anti-VHD. Nenhuma das trinta e três pacientes testadas foi reagente para o
anti-HCV (Anexo 1).
As informações obtidas não eram coletadas uniformemente e algumas eram
praticamente impossíveis de serem resgatadas. Em 90% das fichas, por exemplo,
constava a idade da gestante, no entanto, somente em 38% foi possível conhecer o
local de moradia. Destas, 20% moravam na zona oeste de Manaus, 18% na zona
norte, 11% na zona centro-oeste, 5% na zona leste, 3% na zona centro-sul e 3% na
zona sul da cidade (Figura 4).
Oeste
20%
Sem registro
38%
Norte
18%
Sul
5%
Centro-Sul
3%
Leste
5%
Centro-Oeste
11%
Figura 4 – Área de Moradia das grávidas.
Em 51% dos registros das pacientes, havia referência à naturalidade, com 28%
nascidas em Manaus, 15% no interior do Estado e 8% de outros Estados. Em 49%
não há registro da naturalidade (Figura 5).
19
Capital / AM
28%
Sem registro
49%
Outras
naturalidades
8%
Interior / AM
15%
Figura 5 – Naturalidade das grávidas
Foram realizadas 14 visitas domiciliares. Das quatorze pacientes visitadas, sete
retornaram para nova avaliação. Identificamos duas com sinais sorológicos de
replicação viral, potenciais transmissoras e um dos bebês testados se revelou
reativo para o AgHBs. Entre os parentes das pacientes que retornaram, 26 eram
filhos (as), todavia, apenas oito fizeram testes sorológicos, sete foram não reagentes
para o AgHBs e um foi reagente e três deles tinham Anti-HBct reagente; 4 irmã(os),
5 esposos, sendo que apenas 3 realizaram e eram AgHBs não reagentes e uma
avó, esta AgHbs reagente (Tabelas 1, 2 e 3).
Tabela 1
Perfil sorológico dos filhos das pacientes
Identificação
1º HBSAG
ANTIHBCT
ANTIHCV
Filho 1
N
P
N
Filho 2
N
P
-
Filho 3
N
N
-
Filho 4
N
P
-
Filho 5
N
N
-
Filho 6
P
-
N
Filho 7
N
N
-
Filho 8
N
N
-
(N) Negativo
(P) Positivo
(-) Sem registro
20
O perfil sorológicos da mãe cujo(a) filho(a) foi AgHBs reagente pode ser
apreciada na Tabela 2.
Tabela 2
Demonstrativo do status sorológico de infecção pelo VHB entre mães que
retornaram ao ambulatório.
Mãe 1ºAgHBs
2ºAgHBs
A
B
P
P
C
P
D
P
P
E
P
P
F
P
G
P
(P) Positivo
AgHBe
AntiHBc T
HBeag
ANTIHE
ANTIHDT
ANTIHCV
N
PCR
-
Filho AgHBs
N
N
N
N
N
-
-
-
N
P
N
P
-
N
-
N
-
-
-
-
P
-
P
-
-
-
N
-
-
-
-
-
N
N
N
N
P
P
-
-
-
-
-
P
P
P
P
-
P
N
-
N
N
(N) Negativo
P
-
(-) Sem registro
Tabela 3
Demonstrativo do status sorológico de infecção pelo VHB entre parentes que
retornaram ao ambulatório.
Mãe
1ºAgHBs
2ºAgHBs
AgHBe
Filho AgHBs +
Parente
AgHBs +
AntiHBc T
Parente
A
P
P
P
-
-
P
AntiHBc T +
-
B
P
N
-
N
P
N
P
C
P
P
N
N
N
P
P
D
P
P
P
-
-
P
-
E
P
-
-
N
-
P
-
F*
P
-
N
N
-
P
-
G
P
P
N
-
-
P
-
(P) Positivo
(N) Negativo
(-) Sem registro
* Mãe de bebê AgHBs
4.2 Estudo prospectivo
O estudo prospectivo se propôs a acompanhar a grávida portadora de AgHBs
do diagnóstico ao parto, avaliando aspectos clínicos e virológicos.
Foram identificadas 37 grávidas reativas para o AgHBs, destas, sete não
retornaram para continuidade das observações após a primeira avaliação, embora
tenham concordado em participar do estudo, e duas, tiveram a segunda amostra não
reativa para o AgHBs sendo afastadas do estudo, ficando a amostragem final em 28
21
pacientes, 18 recém-nascidos e 55 pessoas que conviviam na mesma casa da
paciente: 16 maridos, 11 filhos(as), 11 irmãos(ãs), 7 sobrinhos(as), 5 avós, 1
enteado e uma empregada doméstica.
A idade das grávidas atendidas variou de dezenove a quarenta e quatro anos
com uma média de idade de vinte e sete anos. A maioria das gestantes tinha entre
20 a 25 anos (43%) (Figura 6). A idade dos parentes da grávida variou entre dois e
cinqüenta anos, com média de vinte e dois anos.
Número de pacientes
14
12
10
8
6
4
2
0
15 a 19
20 a 25
26 a 30
31 a 35
> 35
Idade
Figura 6 – Idade das grávidas acompanhadas no estudo prospectivo.
Das 37 grávidas inicialmente cadastradas, 30 repetiram a sorologia, sendo
acompanhado o estado de portadora em 28 delas, pois duas das pacientes tiveram
a segunda amostra negativa.
Os outros marcadores do VHB não foram testados de forma uniforme, por
motivos operacionais, em todas as pacientes acompanhadas. Oito pacientes
(28,57%) tiveram suas amostras testadas para o AgHBe, destas, nenhuma
apresentou reatividade sendo todas reagentes para o anti-HBe.
22
Em nove (32,14%) das 28 pacientes foram realizados exames para o VHD,
onde três (37,14%) apresentaram-se reativas; dez grávidas (35,71%) tiveram suas
amostras testadas para o VHC, todas com resultado não reagente. 11 grávidas
(39,28%) realizaram teste da PCR, sendo três positivas (27,27%) (Tabelas 4).
Tabela 4
Perfil Clínico e Sorológico das Pacientes Grávidas Acompanhadas no ambulatório
Especializado da FMT-AM
AgHBs
Confirmatór
Paciente
Idade
Exa Fis
Aghbs 1
io
ANTI-HBcT
AgHBe
ANTI-HBe
ANTI-HDT
PCR
1
23
normal
P
P
P
N
P
-
N
2
18
normal
P
P
P
-
P
-
P
9
29
normal
P
P
-
-
-
-
-
13
21
normal
P
P
P
-
-
-
-
26
22
normal
P
P
-
-
-
N
N
27
33
-
P
P
P
N
P
N
-
31
26
normal
P
P
P
-
-
-
N
42
23
normal
P
P
P
-
-
-
-
48
29
-
N
P
P
-
-
P
-
49
41
-
P
P
P
-
-
N
-
50
29
-
P
P
-
-
-
-
P
53
44
normal
P
P
-
-
-
-
-
54
19
-
P
P
P
-
-
-
N
58
26
-
P
P
P
N
P
-
-
59
21
normal
P
P
P
-
-
-
N
67
25
normal
P
P
P
-
P
N
-
70
30
eritema pal
P
P
-
-
-
-
P
73
23
-
P
P
P
-
-
-
-
74
35
Normal
P
P
P
N
P
-
-
77
31
Normal
P
P
P
N
P
N
-
79
29
-
P
P
P
N
P
-
-
80
24
-
P
P
P
-
-
-
-
81
23
Normal
P
P
P
-
-
-
-
82
26
Normal
P
P
P
N
P
N
-
83
21
Normal
P
P
P
N
P
P
-
84
27
Normal
P
P
P
-
-
-
-
88
25
Normal
P
P
-
-
-
-
-
90
24
esplen+e.P
P
P
P
-
P
P
-
Em três dos 18 recém-nascidos foi realizado teste para o AgHBs, sendo todos
não reativos; enquanto que no teste da PCR, do sangue do cordão umbilical,
realizado em nove deles, em quatro (44,44%) das amostras foram isolados DNA viral
(Tabela 5).
23
Tabela 5
Perfil sorológico de mães de recém-nascidos PCR reativos
Identificação AgHBs
Materno
Anti-HBcT
AgHBe
Anti-
Anti -
Anti-HCV PCR
Materno
Materno
AgHBe
Delta
Materno
Materno
Materno
RN α
P
P
N
P
N
-
-
RN β
P
P
-
-
P
-
N
RN γ
P
P
-
-
-
-
N
RN δ
P
P
-
P
-
N
-
(P) Positivo
(N) Negativo
(-) Sem registro
Quanto à aplicação de vacina e imunoglobulina hiperimune contra o VHB após
o nascimento, em 15 (83,33%) dos recém-nascidos acompanhados a intervenção foi
feita em tempo hábil.
Todas as mães que tinham o teste da PCR reativa, indicativa de replicação
viral, apresentavam exame físico normal, sendo que uma delas apresentava eritema
palmar.
Uma das 28 grávidas apresentava esplenomegalia, além do eritema palmar,
porém a mesma não teve suas amostras sangüíneas testadas para o AgHBe ou
PCR indicativos de replicação viral.
O exame físico das pacientes foi normal em dezessete (61%) delas, em duas
(7%) estava alterado com a presença de esplenomegalia e eritema palmar. De nove
(32%) não temos o registro do ato (Figura 7).
24
SEM REGISTRO
32%
NORMAL
61%
ALTERADO
7%
Figura 7 – Percentual dos achados referente ao exame físico das grávidas.
Das 28 grávidas, 12 (43%) moravam na zona norte da cidade de Manaus, seis
(21%) na zona oeste, duas (7%) na zona leste, três na zona centro-oeste (11%),
outras três na zona sul (11%) e duas (7%) na zona centro-sul (Figura 8).
SUL
11%
CENTRO-OESTE
11%
CENTRO-SUL
7%
OESTE
21%
LESTE
7%
NORTE
43%
Figura 8 – Local de moradia das pacientes grávidas atendidas.
Das 28 pacientes, doze (42,86%) eram naturais de Manaus, dez (35,71%) eram
naturais da parte ocidental do Amazonas onde estão localizados municípios tidos
como área endêmica do VHB, duas das grávidas nasceram em municípios do
25
Estado do Pará, de uma não havia registro; uma era nascida em Manacapuru, uma
em Nova Olinda do Norte e uma em Manaquiri (Figura 9).
Nova Olinda do Norte
Manaquiri
Codajás
Manacapuru
Carauari
Lábrea
Manaus
0
2
4
6
8
10
12
14
Figura 9 – Número de grávidas naturais do Estado do Amazonas.
Outros
Sem
registro; 1 Estados; 2
Outros
municípios
do
Amazonas;
4
Amazonas área
ocidental ; 9
Capital do
Amazonas;
12
Figura 10 – Naturalidade das grávidas acompanhadas na FMT-AM.
11 das grávidas acompanhadas eram donas de casa, de quatro não há registro
sobre profissão, enquanto que as restantes em número de 13 exerciam profissões
como a de funcionário público, babá, cabeleireiro, auxiliar de cabeleireiro, militar,
estudante, industriária, vendedora e uma estava desempregada (Tabela 6).
26
Tabela 6
Profissão exercida pelas grávidas no primeiro atendimento
Profissão das grávidas
Quantidade
Autônoma
1
Aux. Cabeleireiro
1
Aux. De tesouraria
1
Auxiliar produção
1
Cabeleireira
1
Babá
1
Desempregada
1
Dona de casa
11
Estudante
1
Funcionária pública
1
Industriária
1
Militar
1
Serviços gerais
1
Sem registro
4
Vendedora
1
Total
28
O tempo de protrombina, prova de escolha para a investigação do sistema
extrínseco da coagulação sangüínea e do fibrinogênio, foi analisado em 15
pacientes, cujos resultados podem ser visualizados na Figura 11.
10 a 11
11,01 a 12
12,01 a 13
acima de 13
Sem registro
0
2
4
6
8
10
12
14
Núm ero de pacientes
Figura 11 – Análise do tempo de atividade de Protrombina em segundos (TAP)
27
Duas das grávidas que tiveram seu soro analisado para o tempo de atividade
da protrombina apresentaram um tempo prolongado.
O perfil laboratorial hemático das grávidas neste estudo, demonstrou que
nenhuma das pacientes tinha níveis de hemoglobina abaixo ou igual a 10,0 g/dl. Dez
(36%) apresentavam níveis de hemoglobina também baixa entre 10,0 a 11 g/dl; dez
(36%) delas tinham a hemoglobina sangüínea de 11,1 a 12 g/dl; duas (7%) delas
tinham a hemoglobina sangüínea entre 12,1 e 13 g/dl; e em seis (21%) delas o
exame não foi realizado (Figura 12).
Níveis de Hemoglobina - g/dl
SR
12,1 a 13
11,1 a 12
10,1 a 11
8 a 10
0
5
10
15
número de pacientes
Figura 12 – Níveis de hemoglobina em grávidas AgHBs reativas atendidas na FMTAM.
Três das 28 grávidas estudadas (10,71%) apresentavam elevação da
Transaminase glutâmico-oxalacética ou aspartato-aminotransferase.
Na análise das proteínas séricas de 21 pacientes, 12 tinham albumina menor
que 3,4g/dl e dezessete de dezenove pacientes tinham globulina maior que 3,1g/dl.
28
Das pacientes atendidas, nove (31%) eram primigestas; sete (24%) eram
secundigestas; cinco (19%) encontravam-se na terceira gestação; quatro (15%)
encontravam-se na quarta gestação; uma (4%) na sexta; e duas (7%) sem registro.
A exceção de uma paciente que em torno da segunda metade da gravidez, pariu
prematuramente com óbito fetal por prematuridade. 18 pacientes acompanhadas
pariram a termo; sobre as outras dez não tivemos informação (Figura 13).
G1 P0 A0
G2 P1 A0
G4 P2 A1
G3 P2 A0
sr
G2 P0 A1
G6 P3 A2
G4 P3 A0
G3 P1 A1
G3 P0 A2
0
2
4
6
8
10
Número de pacientes
Figura 13 – Amostragem por número de gestação das pacientes atendidas.
29
5 DISCUSSÃO
A análise dos dados dos estudos retrospectivo e prospectivo demonstram
uma prevalência do AgHBs que situa a população de grávidas em Manaus no
padrão de moderada intensidade conforme classificação da OMS.
A prevalência geral encontrada em nosso estudo foi de 2,5%, maior do que as
encontradas em outros estudos brasileiros. SABINO et al.; 1992, encontrou em São
Paulo, 0,4% de pacientes grávidas reativas para o AgHBs. Em um estudo conduzido
por Oliveira, 1993, no Distrito Federal, a prevalência de AgHBs em grávidas foi 0,6%;
já Silva, 1983, na Bahia, encontrou a prevalência de AgHBs de 1,7%.
Alguns autores referem taxas entre 3% e 9% para o AgHBs entre grávidas de
regiões endêmicas do estado do Amazonas, principalmente das calhas dos rios
Juruá e Purus, consideradas hiperendêmicas (KIESSLICH et al, 2003), sugerindo
que Manaus seja área de pouca circulação do VHB, pois no mesmo estudo a
prevalência de AgHBs em grávidas encontrada na sub-região do Rio Negro foi de
1,3%. As diferenças das prevalências encontradas devem-se ao fato do estudo ter
sido realizado na Amazônia Ocidental, área classificada como de média
endemicidade.
Como a FMT-AM é considerada instituição de referência, para onde são
encaminhadas grande parte das grávidas para serem submetidas ao rastreamento
sorológico durante o pré-natal, tendo sido atendidas gestantes de todas as zonas da
cidade, independente da distância da Instituição, a amostra avaliada tem grande
probabilidade de ser representativa. Inclusive, tanto no estudo retrospectivo como no
prospectivo, as maiores prevalências de portadoras do AgHBs foram encontradas
entre moradoras das zonas de maior densidade populacional, áreas de antigas
invasões, para onde vão os migrantes.
A média de idade de 29 anos das portadoras no estudo retrospectivo e de 27
no prospectivo sustenta a necessidade de implementação de programa de
rastreamento para o VHB entre mulheres em idade reprodutiva e intensificação do
30
programa de imunização para o VHB em recém-nascidos e adolescentes, pois em
áreas endêmicas, a infecção ocorre precocemente durante a infância através de
mães portadoras ou contato interpessoal (BRASIL, 2002; FONSECA, 1998).
A prevalência do AgHBs entre as grávidas foi maior no grupo etário entre 20 a
30 anos (60%); Silva, na Bahia, encontrou uma prevalência igual a 78% entre 15 a
30 anos. Esse achado mostra a possibilidade de transmissão vertical, já que essas
mulheres encontram-se em idade reprodutiva, mas não foram imunizadas
precocemente, provavelmente por falha no sistema.
No estudo retrospectivo, embora o número de mulheres testadas para o
AgHBe e reação da PCR tenha sido pequeno, três foram reagentes ao antígeno e
três
à
PCR,
indicando
replicação
viral
com
potencial
de
transmissão
(CUNNINGHAM, 1993; KIESSLICH, 2003).
Entre as sete pacientes que retornaram ao ambulatório e incluídas no estudo
retrospectivo, identificamos a presença do AgHBs entre familiares, avó e filho com
sinais sorológicos marcadores de infectividade em potencial (AgHBe), indicando a
possibilidade de transmissão vertical do VHB. Enquanto que no estudo prospectivo
quatro recém-nascidos tinham a reação da PCR no cordão umbilical positiva.
Demonstrando a possibilidade, embora rara, da transmissão vertical, à semelhança
do encontrado por Brasil et al. em 2003.
Este achado, embora em número pequeno reforça a necessidade de se
estabelecer mecanismos de estímulos à imunização ativa de recém-nascidos e
adolescentes, de forma a reduzir o status de portador crônico com doença ativa ou
não, para desta maneira cercear a transmissão vertical e todas suas mazelas.
A idade dos parentes das grávidas variou entre dois e 50 anos, com média de
22 anos; a transmissão horizontal no Estado do Amazonas parece ser via importante
de transmissão do VHB (BRASIL et al, 2003) devendo-se enfatizar a necessária
imunoprevenção precoce. O baixo padrão de vida da família brasileira da região
norte, onde em sua maioria, mais de três pessoas co-habitam no mesmo domicílio,
constituem-se um foco de transmissão através de contato pessoal.
31
A associação do VHB e do VHD nos estudos foi encontrada em seis
pacientes. Sendo três pacientes no estudo retrospectivo e três no prospectivo, no
total 6,7% das participantes, prevalência inferior à encontrada por BRAGA et al.
(2001) entre indígenas do Estado do Amazonas. Tal diferença talvez se deva a
diferenças populacional e regional.
Não foi encontrada associação entre o VHB e o VHC na população de estudo.
Apenas 43 pacientes do total geral do estudo, foram testadas para o VHC. Não
tendo sido encontrada associação entre o VHB e o VHC.
A Amazônia Ocidental é considerada uma área brasileira de endemicidade
importante de infecção do VHB (BRASIL et al., 2003), sobretudo na região mais
ocidental onde estão localizados municípios onde nasceram 35,71% (Figura 12), das
grávidas acompanhadas e onde a grande maioria da população contrai o VHB ainda
na idade pré-escolar (KIESSLICH et al., 2003); com taxas de prevalência do AgHBs,
entre grávidas, que variam entre 0,8% a 8,7% (KIESSLICH et al., 2003). Assim
podemos conjecturar que as pacientes naturais daquela área, acompanhadas em
nosso estudo podem ter sido expostas precocemente ao vírus o que favorece a
evolução para a cronicidade da infecção (SABINO et al., 1992; BRASIL et al., 2003;
EDMUNDS et al, 1996) embora não tenhamos encontrado sinais clínicos definidores
de cronicidade na amostra avaliada.
Na transmissão do VHB são reconhecidos como fator de risco, entre outros, a
atividade profissional na área de saúde (SABINO et al., 1992) em nosso estudo
54,2% das grávidas laborava com o público, contudo nenhuma se inseria no perfil de
risco profissional, a semelhança do referido na literatura em que cerca de 50% dos
casos de portadores de AgHBs não se identifica nenhum fator de risco admitido
(SABINO et al., 1992).
Acompanhamos duas pacientes cujos companheiros ou cônjuges eram
portadores do vírus da imunodeficiência adquirida (HIV). Em relação à co-infecção
com outras enfermidades dez das pacientes referiam corrimento vaginal, duas
referiam passado de sífilis e outra de verrugas genitais.
32
Embora sem valor estatístico no referido trabalho, há que valorizar a história
de outras doenças sexualmente transmissíveis, também reconhecida como fator de
risco na transmissão do VHB (MINISTÉRIO DA SAÚDE 2003; SABINO 1992) bem
como é conhecido que doenças do fígado freqüentemente complicam a infecção
pelo HIV, podendo preparar o terreno para a progressão para a AIDS.
A concentração normal de hemoglobina no sangue varia em torno de 15g por
100 ml. Os limites normais são de 13,5 a 18 no homem e de 11,5 a 16,4 na mulher.
Na gravidez os valores da contagem de eritrócitos, da hemoglobina e do hematócrito
são nitidamente menores do que aqueles não gravídicos. Sabe-se que os valores de
hemoglobina começam a diminuir no terceiro e quinto mês de gestação atingindo
seus níveis mais baixos do quinto ao oitavo mês. Consideram-se anêmicas as
grávidas com taxa de hemoglobina inferior a 10g/dl. Nenhuma das pacientes
possuía hemoglobina abaixo de 10g/dl.
A elevação das transaminases ocorre nos processos com necrose e
destruição celular, como por exemplo, nas hepatopatias, não havendo alteração da
mesma no decorrer da gravidez, tornando-se elevadas quando há complicações
infecciosas ou hipertensivas. As pacientes estudadas e que apresentaram alteração
destas enzimas hepáticas não apresentaram alterações clínica que as justificassem.
Com relação às proteínas totais do soro, estas diminuem aproximadamente
20% no segundo trimestre gestacional por substancial diminuição da albumina.
Existe ainda discreto aumento das globulinas.
A
albumina
é
a
proteína
mais
abundante
do
plasma,
sintetizada
exclusivamente pelo fígado e possui papel muito importante em diversas funções do
organismo, como transporte diferentes substâncias e a manutenção da pressão
oncótica. A fração albumina das proteínas plasmáticas constitui-se em indicador da
cronicidade e da intensidade das afecções hepáticas já que a síntese da mesma se
dá exclusivamente nos hepatócitos. Em condições normais, o fígado é um órgão
pouco importante para a síntese da globulina, mas nas hepatopatias crônicas, há um
aumento da capacidade da síntese dessa proteína por esse órgão (Anexo 2). As
33
alterações encontradas nas proteínas séricas das pacientes estudas não podem ser
imputadas a hepatopatia, pois o próprio estado fisiológico da gravidez, gera tais
alterações(CUNNINGHAM, 1993).
Quanto à expressão clínica, observamos que as pacientes apresentavam-se
assintomáticas, o que está de acordo com os achados em outros estudos (BRASIL,
2003). Algumas alterações encontradas não podem ser associadas à doença
crônica do VHB, já que o estado de hiperestrogenia fisiológica da gravidez pode
acarretá-las (ARRAES et al, 2003).
34
6 CONCLUSÃO
1. A porcentagem dos portadores de AgHBs em grávidas em nosso estado
possivelmente é uma das mais elevadas, revelando-se um sério problema de saúde
pública. A prevalência encontrada em nosso estudo foi de 2,5% de grávidas AgHBs
reativas, bem maior que as relatadas em outras regiões do país.
2. Tanto o estudo prospectivo como o retrospectivo, indicam a possibilidade de
transmissão vertical do VHB na população estudada, visto terem sido encontradas
mães e recém-nascidos com a presença de DNA viral pela reação de PCR.
3. Identificamos a falha no sistema de vigilância, pois que 3/15 (10,7%) dos
recém-nascidos não receberam a imunoglobulina, por fatores relacionados à falha
na comunicação, transporte e informação.
4. Dadas às limitações do método de coleta dos dados aqui apresentados, não
consideramos o presente trabalho como um levantamento epidemiológico, havendo
necessidade do presente trabalho ser continuado, particularmente pela escassez de
publicações semelhantes na região norte do país.
35
7 REFERÊNCIAS BIBLIOGRÁFICAS
ARRAES, Luiz Cláudio; et al. Prevalência de hepatite B em parturientes e perfil
sorológico perinatal. Revista da Federação Brasileira das Sociedades de
Ginecologia e Obstetrícia/FEBRASGO. São Paulo: Ponto, v.25, n.8, p 571-576,
set. 2003.
BENSABATH, Gilberta et al. Caracteristicas serologicas y epidemiologicas de la
hepatitis virica aguda en la cuenca amazonica del Brasil. Boletin de la Oficina
Sanitaria Panamericana. V.103(4), p. 351-362. 1987.
BRAGA, Wornei Silva Miranda; et al. Ocorrência de infecção pelo vírus da hepatite B
(VHB) e delta (VHD) em sete grupos indígenas no Estado do Amazonas. Revista da
Sociedade Brasileira de Medicina Tropical, Uberaba, v. 34, n. 4, p. 349, jul-ago.
2001.
BRASIL, Leila Melo; et al. Prevalência de marcadores para o vírus da hepatite B em
contatos domiciliares no estado do Amazonas. Revista da Sociedade Brasileira de
Medicina Tropical, Uberaba, vol. 36, n. 5, p. 565-570, set-out. 2003.
CDC – CENTER FOR DISEASE CONTROL.
Report. V. 37, n.22, p. 341-351. 1988.
Morbidity and Mortality Weekly
CONTI, M. I. Bonanno et al; Madri HBsAG positive e immunizzazione dei neonati:
esperienza del’USP n. 1 di trapani. Minerva Pediatric, Trapani; v.42; p. 233-235;
jun. 1990.
CUNNINGHAM, F. Gary. et al. Williams Obstetrics. 19. ed. EUA: Prentice-Hall
Internactional Inc, p. 1157-60. 1993.
DAVIES, G., et. al. Amniocentesis and women with hepatitis B, hepatitis C, of human
immunodeficiency vírus. Journal of Obstetrics and Gynaecology, Canadá, v. 25,
n.2, p. 145-52, fev. 2003.
EDMUNDS, W.J.; et al. Epidemiological patterns of hepatitis B virus (HBV) in highly
endemic areas. Epidemiol Infect. Cambridge University Press; p.313-325; 1996.
FERRAZ, Maria Lúcia Gomes; Hepatites virais; in: MONTELEONE, Pedro Paulo
Roque; VALENTE, Carlos Alberto (cord.); Infectologia em Ginecologia e
Obstetrícia. São Paulo: Editora Atheneu; p.194; 1998.
FERREIRA, Cristina Targa; SILVEIRA, Themis Reverbel da. Hepatites virais:
aspectos da epidemiologia e da prevenção. Revista Brasileira de Epidemiologia.
São Paulo. V.7; n. 4; p. 473-487; dez. 2004. Disponível em:
<http://www.scielo.br/scielo.php?script.> Acesso em 04 mar. 2005.
FERREIRA, João Leandro de Paula; PINHO, João Renato Rebello. Hepatite G. . in:
FOCACCIA, Roberto (ed. Científico); Tratado das hepatites virais. São Paulo:
Editora Atheneu, 2003. p. 365-369.
36
FERREIRA, Marcelo Simão. Diagnóstico e tratamento da hepatite B. Revista da
Sociedade Brasileira de Medicina Tropical, Uberaba. v.3, n. 4, p. 389-400, jul-ago.
2000.
FOCACCIA, Roberto; SOUZA, Fernando Vieira de;. Hepatite C. in: VERONESI,
Ricardo; FOCACCIA, Roberto (ed.). Tratado de Infectologia. São Paulo: Editora
Atheneu, 1996. p. 314-322.
FONSECA, José Carlos Ferraz da. Hepatite D. Revista da Sociedade Brasileira de
Medicina Tropical, Uberaba. v. 35, n. 2, p. 184-190, mar-abr. 2002.
FONSECA, José Carlos Ferraz da. In: Veronesi R, Focaccia A (eds) Tratado de
Infectologia – Hepatites Virais, São Paulo, p. 67-79, 1998.
FUNASA, Hepatites virais. Disponível em: <http://www.funasa.gov.br> Acesso em:
20 jul. 2003.
GOMES, Selma de Andrade; Genoma Viral do VHB; FOCACCIA, Roberto (ed.
Científico); Tratado das hepatites virais. São Paulo: Editora Athenu, 2003. p. 119125.
GONÇALES, Neiva Sellan Lopes. Virologia Molecular. Hepatite E. in: FOCACCIA,
Roberto (ed. Científico); Tratado das hepatites virais. São Paulo: Editora Athenu,
2003. p.351-358.
HADLER C. Stephen, et al. La Hepatitis em las Américas: Informe del grupo
colaborador de la OPS. Boletin de la oficina sanitária panamericana. V.103(3),
p.185-209. 1987.
JAISWAL, SP et al. Hepatitis during pregnancy. Int. Journal Gynaecology
Obstetric.
V.72(2),
p.103-108,
2001.
Disponível
em:
<http:www.ncbi.nlm.nih.gov/entrez/query.fcgi?CMD=text&DB=pubmed>
JIA-HORNG, Kao; DING-SHINN, Chen. Global control of hepatitis B virus infection.
The Lancet Infectious Diseases, v. 2, p. 395-403, jul. 2002.
JOSHI, Supriya, HEATHCOTE, E. Jenny; Preventing Transmission of Hepatitis B.
Disponível em: <http://clinicaloptions.com/hep/ev/2004-6.asp> Acesso em: 13 ago.
2005.
KIESSLICH, Dagmar, et al. Prevalência de marcadores sorológicos e moleculares do
vírus da hepatite B em gestantes do Estado do Amazonas, Brasil . Epidemiologia e
Serviço de Saúde Revista do Sistema Único de Saúde do Brasil, Brasília:
Ministério da Saúde. V 12, n.3, p. 155-164, jul-set 2003.
LIMA, Maria Patelli Juliani Souza; Hepatite C e Gravidez. . in: FOCACCIA, Roberto
(ed. Científico); Tratado das hepatites virais. São Paulo: Editora Athenu, 2003.
p.253-258.
37
MAHONEY, Francis J.; Update on Diagnosis, Management, and Prevention of
Hepatitis B Vírus Infection. Clinical Microbiology Reviews . v.12; p. 351-366;
abr.1999.
MINISTÉRIO DA SAÚDE DO BRASIL. Hepatites virais: O Brasil está atento.
Brasília: Editora MS, p. 1-7. 2003.
MOURA, Miguel Carneiro de; Marinho, Rui Tato. Epidemiologia da hepatite A; in:
Tratado das hepatites virais. São Paulo: Editora Atheneu, 2003. p. 84-86.
NETO, Edmundo P. A. Lopes; JÚNIOR, Hoel Sette. In: : VERONESI, Ricardo;
FOCACCIA, Roberto(ed.). Tratado de Infectologia. São Paulo: Editora Atheneu,
1996. p.330-334.
PERIM, Eduardo Brás; PASSOS, Afonso Dinis Costa; Hepatite B em gestantes
atendidas pelo Programa do Pré-Natal da Secretaria Municipal de Saúde de Ribeirão
preto, Brasil: prevalência da infecção e cuidados prestados ao recém-nascidos.
Revista Brás. Epidemiol.; São Paulo; v. 8; n. 3; set. 2005.
RUIZ-MOREÑO, Mercedes; LEAL,A; MILLÁN,A. HBV e Gravidez. in: FOCACCIA,
Roberto (ed. Científico); Tratado das hepatites virais. São Paulo: Editora Athenu,
2003. p.155-165.
RUIZZI, Octavio Lorenzo Alfonso; QUIJANO, Massiel de Rosário. Hepatitis B. Uma
problemática mundial. Revista Cubana de Medicina , Ciudad de la Habana, v.42, n.
4; jul-ago. 2003.
RUOCCO, Rosa Maria de Souza Aveiro. Hepatites virais. In: ZUGAIB, Marcelo;
BITTAR, Roberto Eduardo (ed.) Protocolos assistenciais : Clínica Obstétrica da
Faculdade de Medicina da USP. 2.ed. São Paulo: Editora Atheneu, p. 199 – 206.
2003.
SABINO, et. Al; Freqüência de marcadores de hepatite B em gestantes de primeira
consulta em centros de saúde de área metropolitana, São Paulo, Brazil. Revista do
Instituto Medicina Tropical de São Paulo, São Paulo; v. 34; n. 6; p. 535-541; novdez. 1992.
SILVA, Luciana Rodrigues. Transmissão vertical do vírus B da hepatite em
Salvador. Salvador: UFBA, 1984. Dissertação (mestrado), Faculdade de Medicina,
Universidade
Federal
da
Bahia,
1984.
Disponível
em:
<http//www.bases.bireme.br/cgi-bin/wxislind exe/iah/online/> Acesso em 05 jun.2004.
SILVA, Ricardo José de Oliveira e; et al . Vacinação anti-hepatite B em profissionais
de saúde. Jornal Brasileiro de Doenças Transmissíveis, Niterói.v. 15, n. 3, p.5155. 2003.
SILVEIRA, Thêmis R; et al. Hepatitis B seroprevelence in Latin América. Rev Panam
Salud Publica, v.6, n.6, p.378-383. 1999.
38
SMEDILE, Antonina; PAGANIN, S.; RIZZETTO, Mario. História Natural.
Transmissão. Imunodiagnóstico do VHD. . in: FOCACCIA, Roberto (ed. Científico);
Tratado das hepatites virais. São Paulo: Editora Athenu, 2003. p.331-343
SOUTO, Francisco José Dutra. Distribuição da hepatite B no Brasil: atualização do
mapa epidemiológico e preposições para seu controle. Gastroenterologia e
Endoscopia Digestiva. V. 18(4), p. 143-150. 1999.
TORRES, Paulo R.; MENDES, Cláudio G. de. Marcadores Virais no Diagnóstico
da Hepatite. Rio de Janeiro: Byk Química e Farmacêutica, p. 9-11, 1993.
VAN NUNEN, Andeltje B. et. al. Lamuvidine in the last 4 weeks of pregnancy to
prevent perinatal transmission in higly viremic chronic b patients. Letters to editor.
Journal of Hepatology, v. 32, p. 1040-42. 2000.
VELASCO, Maria Cristina Cañero, Profilaxia vacinal da hepatite A; in: FOCACCIA,
Roberto (ed. Científico); Tratado das hepatites virais. São Paulo: Editora Athenu,
2003. p.101-116.
XU, D., et al. Risk factors and machanism of transplacental transmission of hepatitis
B vírus: a case-control study. Journal of Medical Virology, EUA, v. 67, n.1, p. 2026, maio. 2002.
39
8 ANEXOS
Anexo 1. Perfil sorológico das pacientes no estudo retrospectivo
PACIENTE
3
4
5
6
7
8
11
12
14
16
18
19
20
21
22
23
24
25
29
32
33
34
35
36
37
38
39
40
41
44
45
46
47
51
52
55
56
57
60
61
62
63
64
65
66
68
69
71
72
78
82
86
87
88
89
90
91
92
93
94
95
(P) Reagente
1º AgHBs
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
2ºAgHBs
P
N
P
P
P
P
P
P
P
P
P
N
P
P
P
P
P
P
P
P
P
P
ANTI-HBcT
P
P
P
P
P
P
N
N
P
P
P
P
P
P
P
P
P
P
P
P
P
P
N
P
P
P
P
P
P
P
P
P
P
P
P
P
P
(N) Não reagente
AgHBe
N
N
N
N
N
N
N
N
P
P
P
-
ANTI-AgHBe
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
P
N
P
P
P
P
P
N
N
N
P
-
(-) Sem registro
ANTI-HDT
N
N
N
P
N
N
N
N
N
N
P
P
N
N
N
ANTI-HCV
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
40
Anexo 2 – Perfil Clínico e Laboratorial das Pacientes Grávidas Acompanhadas no
Ambulatório Especializado da FMT-AM
HEMOGLOBINA
PACIENTE IDADE EXAME FÍSICO
-
TAP(s)
(g/dl)
TGO
TGP
BT
BD
ALBUMINA GLOBULINA
1
23 Normal
-
10,10
-
-
-
-
-
-
2
18 Normal
12,10
11,30
17,00
30,00
0,65
0,12
3,10
3,20
9
29 Normal
12,80
12,00
15,00
29,00
-
-
2,80
4,00
13
21 Normal
-
12,00
21,00
26,00
0,42
0,08
2,00
-
26
22 Normal
12,60
12,30
25,00
34,00
0,42
0,10
4,10
4,30
27
33 -
-
-
-
-
-
-
-
-
31
26 Normal
11,90
10,60
27,00
45,00
0,64
0,14
4,80
3,50
42
23 Normal
10,40
11,70
21,00
19,00
0,39
0,11
3,20
4,60
48
29 -
15,10
12,80
42,00
85,00
0,92
0,23
3,60
-
49
41 -
-
-
-
-
-
-
-
-
50
29 -
-
-
-
-
-
-
-
-
53
44 Normal
12,60
10,50
37,00
37,00
0,71
0,14
3,40
3,30
54
19 -
-
10,30
19,00
32,00
0,30
0,14
2,00
3,40
58
26 -
-
-
22,00
27,00
0,78
0,54
-
-
59
21 Normal
11,96
10,30
-
-
0,61
0,19
3,30
3,40
67
25 Normal
13,40
11,50
19,00
31,00
0,43
0,15
2,90
3,50
70
30 Eritema pal
-
10,40
33,00
58,00
0,40
0,28
6,04
2,05
73
23 -
-
-
18,00
22,00
,
,
2,50
3,40
74
35 Normal
11,00
11,60
26,00
30,00
0,43
0,13
3,30
4,00
77
31 Normal
-
10,50
20,00
34,00
1,19
0,17
3,40
3,10
79
29 -
-
11,90
-
-
-
-
-
-
80
24 -
-
-
-
-
-
-
-
-
81
23 Normal
-
11,80
26,00
33,00
-
-
3,10
3,90
82
26 Normal
10,90
11,30
20,00
25,00
0,40
0,04
2,80
3,80
83
21 Normal
11,10
11,80 123,00 148,00
0,32
0,16
3,20
4,50
84
27 Normal
12,20
10,30
16,00
25,00
0,32
0,04
2,60
4,30
88
25 Normal
11,20
10,80
18,00
29,00
0,42
0,26
2,60
3,70
90
24 esplenomegalia+
eritema palmar
12,80
11,00
63,00
81,00
0,52
0,23
2,70
3,80
SEM REGISTRO
41
Anexo 3 – Folder Informativo
O que essas vacinas que os bebês
tomam fazem ?
Essas vacinas ajudam o corpo dos
bebês a criar antivírus que protegem
contra Hepatite B
Quando o adulto ou a criança tem os
anticorpos de Hepatite B ele se torna
resistente ao vírus.
Após alguns meses que seu bebê
tomou as 3 doses e mais a
Imunoglobulina do Vírus da Hepatite B,
o médico fará um simples teste de
sangue.
Esse teste irá dizer se seu bebê está
produzindo os anticorpos.
Pergunte ao seu médico sobre o teste
de sangue
exame a fim de ver se possuem o vírus
em seu corpo.
Se eles não têm o vírus da Hepatite B,
devem então se vacinar para se
proteger.
Hepatite B pode ser prevenida ?
Se você nunca teve Hepatite B, você
deve tomar 3 doses da vacina ...
... e ficar protegido para sempre !
Para
mulheres
grávidas e
novas
mamães
E se meu bebê não tomar as vacinas ?
9 entre 10 bebês que nascem de mãe
infectada irão ser portadores do vírus
pro resto de suas vidas. Bebês que se
tornam portadores tem chance de 1
em 4 de morrer de problemas no
fígado. 19 de 20 bebês que tomam a
vacina fiam protegidos por toda vida.
Estou preocupada de dar vacina contra
Hepatite B pra meu filho.
A vacina de Hepatite B é segura pro
bebê.
Ela não vai afetar o crescimento do seu
bebê.
Se seu bebê pega o vírus ao invés da
vacina, ele se torna passível de ter
problemas no fígado.
Porquê meu parceiro e as pessoas que
vivem comigo precisam fazer o teste ?
Como o vírus da Hepatite B pode ser
passado pra eles, eles devem fazer
O que é Hepatite B ?
Hepatite B é um germe (vírus) que
invade o seu corpo e ataca o seu
fígado. O seu fígado ajuda o seu corpo
a fazer a digestão da comida que
você come e armazena
energia.Também ajuda o seu corpo a
eliminar toxinas.
Hepatite B mata ?
A maioria das pessoas não morrem
disso. Há casos nos quais a Hepatite B
pode causar danos permanentes no
fígado (cirrose [Sis-O-sis]). A Hepatite B
pode causar também câncer do
fígado, o qual pode causar a morte.
Um bom tratamento pode diminuir esse
risco.
Como se pega Hepatite B ?
O contágio ocorre pelo sangue ou por
outros fluídos corporais de alguém que
contém o vírus.
Principais meios de contágio de
Hepatite B:
1.
Manter relação sexual, sem
proteção, com alguém que tem
hepatite;
2.
Bebês nascidos de mães que tem
Hepatite B;
3.
Compartilhar agulhas e seringas;
4. Você pode transmitir Hepatite B se
você é um portador do vírus ou se
você acabou de adquirir.
A
Hepatite
B
e você
Adaptado de Hepatitis and You. CDC
Existe a possibilidade de me livrar do
vírus da Hepatite B ?
O vírus da Hepatite B leva cerca de 2
meses para aparecer no sangue.
Ele pode ficar no seu sangue por meses
ou anos.
Hepatite Tipo B Aguda
9 entre 10 adultos se livram do vírus
após alguns meses.
Diz-se que é Hepatite tipo B Aguda.
Hepatite B Crônica
1 entre 10 adultos nunca se livrará do
vírus dizemos que possuem Hepatite B
Crônica. São chamados portadores.
Tratamento contra Hepatite B Crônica
Informe-se com o seu médico sobre
tratamentos contra a doença.
Muitos permanecem como portadores
se não receberem tratamento.
Melhores atitudes que portadores
podem tomar:
Ter certeza de que seus filhos se
vacinaram contra Hepatite B;
Tenha certeza de que eles não
transmitirão a outros;
Receba um bom tratamento
médico.
Como transmito Hepatite B para o meu
filho ?
Quando uma pequena parte do seu
sangue entra no bebê ao nascer.
Posso amamentar meu bebê se sou
portadora de Hepatite B?
Sim.
Se o seu bebê for vacinado com
Imunoglobulina do Vírus da Hepatite B e
com vacina contra Hepatite B até 12
horas após o nascimento, ele pode ser
amamentado.
Cuide bem da região do mamilo para
prevenir rachaduras e sangramento.
Meu bebê pode morrer de Hepatite B ?
A maior parte dos bebês não morrem
de Hepatite B.
9 entre 10 bebês nascidos de mães
infectadas acabam se tornando
portadores do vírus, se não receberem
vacina.
Se seu bebê tomar todas as 3 doses da
vacina e mais a Imunoglobulina do
Vírus da Hepatite B, ele tem 95% de
chance de estar protegido da Hepatite
B pro resto da sua vida.
Vacinas de Hepatite B para bebês, se a
mãe tem Hepatite B:
ao nascer = vacina de Hepatite B +
Imunoglobulina do Vírus da Hepatite B
1 – 2 meses de vida = vacina de
Hepatite B
6 meses de vida
= vacina de
Hepatite B
42
Anexo 4 – Questionário
FUNDAÇÃO DE MEDICINA TROPICAL DO AMAZONAS
GERÊNCIA DE VIROLOGIA
Ambulatório de Gestação e Doenças Infecto-Contagiosas
QUESTIONÁRIO
Projeto: Transmissão Vertical da Hepatite B: Estudo retrospectivo e prospectivo com mulheres
gestantes diagnosticadas na FMT-AM.
IDENTIFICAÇÃO
1 – Nº Prontuário: ____________________________
2 – Nome: _________________________________________________________________
3 – Endereço: ______________________________________________________________
4 – Telefone: _______________________ Telefone 2 (amigo ou parente): ______________
5 – Idade: ________
Data de nascimento: ___/___/___
Sexo: [ ] M
[ ] F
6 – Local de nascimento: ________________________________________ UF: _______
7 – Procedência: ____________________________________________________________
8 – Tempo em que vive neste local: _____________________________________________
9 – Fonte de encaminhamento: ________________________________________________
HISTÓRIA FISIOLÓGICA E OBSTÉTRICA
1 – Menarca: _________ anos
2 – Gestações, Partos e Abortos: G__ P __ A __
3 – Parto: Cesária ( ) Normal ( ) Domiciliar ( ) Maternidade ( )
4 – Tempo de nascimento: a termo ( ) pré-termo ( ) pós-termo ( )
5 – Nº de filhos: ___ vivos Desenvolvimento: ___________________________________
___ mortos Causa do óbito: ___________________________________
6 – Imunização do recém-nascido: [ ] vacina
[ ] Imunoglobulina
[ ] Não sabe informar
ASPECTOS SÓCIO-ECONÔMICOS
1 – Grau de instrução:
[ ] Analfabeto [ ] Semi-analfabeto [ ] 1º Grau [ ] 2º Grau [ ] 3º Grau
2 – Ocupação Principal: ______________________________________________________
Ocupação Secundária: ____________________________________________________
3 – Horas de trabalho por dia: ____ (_____________________________________) h
4 – Situação atual:
[ ] Trabalhando [ ] Desempregada [ ] Aposentada [ ] Aposentada por invalidez
5 – Estado civil:
[ ] Casada [ ] Relação estável [ ] Separada / divorciada [ ] Viúva [ ] Solteira
6 – Composição familiar (membros da família ou outros)
Nº
Nome
Idade Sexo Consangüinidade
Ocupação
43
7 – Características do domicílio:
7.1 – Quantos cômodos tem a sua casa ?
_____ (_____________________________) cômodos.
7.2 – Quantas pessoas vivem na casa ?
_____ (_____________________________) pessoas.
7.3 – Qual o número de pessoas por quarto ? _____ (_____________________________) pessoas.
FATORES DE RISCO
1 – Fez cirurgia? SIM [ ] NÃO [ ]
1.1 – Se sim, que tipo ? _____________________________________________________________
1.2 – Onde ? _____________________________________________________________________
1.3 – Por quê ? ___________________________________________________________________
1.4 – Quando ? ___________________________________________________________________
2 – Recebeu transfusão de sangue ou hemoderivados ? SIM [ ] NÃO [ ]
2.1 - 1.1 – Se sim, Onde ? ___________________________________________________________
2.2 – Porquê ? ____________________________________________________________________
2.3 – Quando ? ___________________________________________________________________
3 – Compartilha escova de dentes com outras pessoas ? SIM [ ] NÃO [ ]
4 – Compartilha lâmina de barbear ? SIM [ ] NÃO [ ]
5 – Tem tatuagem ? SIM [ ] NÃO [ ]
5.1 – Se sim, há quanto tempo ? _____ (__________________________________) anos.
6 – Tem orelha furada ? SIM [ ] NÃO [ ]
6.1 – Se sim, há quanto tempo ? _____ (__________________________________) anos.
7 – Quantos anos você tinha quando manteve a sua primeira relação sexual ?
_______ (_____________________________) anos
[ ] Não quis responder
[ ] Criança
8 – Quantos anos você tinha quando começou a ter relações sexuais pelo menos uma vez por mês ?
_______ (_____________________________) anos
[ ] Não quis responder
[ ] Criança
9 – Quantos parceiros regulares você teve na sua vida ? _____ (______________________)
parceiros
[ ] Não quis responder
[ ] Criança
10 – Fora o seu parceiro regular, você mantém relações sexuais com outras pessoas ?
_______ (_____________________________) anos
SIM [ ] NÃO [ ]
[ ] Não quis responder
11 – Se sim, durante a sua vida sexual ativa, qual o número de parceiros casuais que você teve ?
_____ (______________________) parceiros
NÃO [ ] quis responder
12 – Você sabe se algum de seus parceiros teve alguma doença venérea ?
SIM [ ] NÃO [ ]
Se sim, especificar: _______________________________________________
[ ] Não quis responder
13 – Você já teve alguma doença abaixo:
[ ] Gonorréia [ ] Sífilis [ ] Verrugas genitais [ ] Corrimento genital [ ] Bolhas genitais [ ] Cancro
[ ] Outras, especificar: _______________________________________________________________
14 – Você tem hábito de usar camisinha (preservativo) ?
SIM [ ] NÃO [ ]
[ ] Não quis responder
15 – Você trabalha em serviço de saúde ? SIM [ ] NÃO [ ]
15. 1 – Houve algum acidente ocupacional ? SIM [ ] NÃO [ ]
16 – Uso de drogas injetáveis ? SIM [ ] NÃO [ ]
17 – Alguém na sua casa teve:
Hepatite ? SIM [ ] NÃO [ ]
Icterícia ? SIM [ ] NÃO [ ]
Colúria ? SIM [ ] NÃO [ ]
Se sim, quem ? Mãe [ ] Pai [ ] Irmão/ã [ ] Companheiro/a [ ] Filho/a
[ ] Outros : ________________________________________________________________________
18 – Você já teve icterícia ? SIM [ ] NÃO [ ]
19 – Você já teve colúria ? SIM [ ] NÃO [ ]
44
ASPECTOS CLÍNICOS
Sintomas
[
[
[
[
] Astenia
] Febre
] Cefaléia
] Prurido
[
[
[
[
] Anorexia
[ ] Náuseas
] Dor articular [ ] Dores musculares
] Diarréia
[ ] Acolia fecal
] Hematêmese
[ ] Melena
[ ] Vômitos
[ ] Dor abdominal
[ ] Colúria
[ ] Perda ponderal
Somatoscopia
Peso: ______________ kg
Estado Geral: [ ] Bom
A _______ x _________ mmHg
[ ] Regular
[ ] Mal
Sinais
[ ] Edema
[ ] Icterícia
[ ] Circulação colateral
[ ] Ginecomastia
[
[
[
[
] Ascite
] Aranhas vasculares
] Atrofia muscular
] Atrofia testicular
Temperatura: ___________ºC
[ ] Anemia
[ ] Eritema palmar
[ ] Alopecia
Exame Físico
1. Lesões de pele ? SIM [ ] NÃO [ ] – Se sim, descrever tipo e local.
_________________________________________________________________________________
_________________________________________________________________________________
2 – Fígado palpável ? SIM [ ] NÃO [ ] Se sim, doloroso ? SIM [ ] NÃO [ ]
Tamanho: _____________________ cm do RCD
Consistência: Normal [ ] Mole [ ] Endurecido [ ] Muito duro [ ]
Superfície: Lisa [ ] Irregular [ ]
3 – Baço palpável ? SIM [ ] NÃO [ ] Se sim, doloroso ? SIM [ ] NÃO [ ]
Consistência: Normal [ ] Mole [ ] Endurecido [ ] Muito duro [ ]
RESULTADOS DOS TESTES DE LABORATÓRIO
TESTE
HBSAG
ANTI-HBS
AHBCIGM
AHBCT
HBEAG
ANTIHBE
HBV-DNA
ANTIHCV
HCV-RNA
HDAG
AHDIGM
AHDT
1ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
2ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
3ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
4ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
5ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
6ª
[AMOSTRA
]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
[ ]P [ ]N
45
TESTE
ALT
DATA 1
DATA 2
DATA 3
DATA 4
DATA 5
DATA 6
AST
GGT
FOSF
BT
BD
ALBU.
GLOB.
PLAQ.
TAP
HEM
LEUC
URE
CREA
GLIC
QUANTIFICAÇÃO DA CARGA VIRAL DO VHB
Resultado
Método
Data
Método
Data
GENOTIPAGAM
Resultado
DATA: _____/_____/_____
__________________________________________________
ENTREVISTADOR
46
Anexo 5 – Termo de Consentimento Livre e Esclarecido
GOVERNO DO ESTADO DO AMAZONAS
FUNDAÇÃO DE MEDICINA TROPICAL DO AMAZONAS
GERÊNCIA DE VIROLOGIA
TERMO DE CONSENTIMENTO LIVRE E ESCLARECIDO
I – DADOS DE IDENTIFICAÇÃO DA PACIENTE:
Nome: ____________________________________________________________________
Prontuário: _________________________________________ R.G. ___________________
Sexo: ( ) M ( ) F
Profissão: _______________________ Escolaridade: ____________
Endereço: _________________________________________________________________
__________________________________________________________________________
Cidade: ________________________________ UF: _____ CEP: _____________________
Telefone 1: _____________________________ Telefone 2: _________________________
II – DADOS DE IDENTIFICAÇÃO DA CRIANÇA:
Nome: ____________________________________________________________________
Prontuário: ________________________________________________________________
Sexo: ( ) M ( ) F
Idade: _______________________
Endereço: _________________________________________________________________
__________________________________________________________________________
Cidade: ________________________________ UF: _____ CEP: _____________________
Telefone 1: _____________________________ Telefone 2: _________________________
III – DADOS SOBRE A PESQUISA CIENTÍFICA:
Título: Estudo Clínico e Epidemiológico com Gestantes Portadoras do AgHBs – Evidências da
Possibilidade de Transmissão Vertical
Pesquisador Responsável: Iran Grijó Praia
Gerência de Virologia / Fundação de Medicina Tropical do Amazonas
Aprovação do Estudo pela Comissão de Ética em Pesquisa da FMT-AM em ___ / ___ / ___
IV – EXPLICAÇÃO À PACIENTE:
A Gerência de Virologia da FMT-AM, está desenvolvendo projeto de pesquisa em mulheres
infectadas pelo Vírus da Hepatite B (VHB), cujos os objetivos principais são:
1 – Geral
Determinar a prevalência do vírus da hepatite B (VHB), em grávidas que procuram a Gerência de
Virologia da FMT-AM para realizar testes sorológicos da rotina do pré-natal.
2 – Específicos
• Descrever a ocorrência de marcadores sorológicos de infecção pelo VHB, em relação aos
aspectos demográficos, sócio-econômicos e obstétricos;
• Identificar possíveis fatores determinantes de transmissão do VHB;
• Verificar o risco de transmissão vertical, detecção do DNA e quantificação da carga viral do VHB
O conhecimento desses dados permitirá conhecer os prejuízos causados pela hepatite B nas
mulheres grávidas e em seus filhos; além de fornecerem informações sobre o grau de transmissão
vertical. De modo a oferecer, às autoridades de saúde, números e dados que ajudem a estabelecer
estratégias que contribuam para o bem-estar populacional, sobretudo para as mulheres e crianças.
Este projeto será conduzido sob a responsabilidade do médico, Dr. Iran Grijó Praia.
V – Participação no Estudo:
Sua participação neste estudo será através de entrevista; consulta no ambulatório de gestação e
doenças infecto-contagiosas; coleta de sangue e; para as mulheres que durante o período de
desenvolvimento deste estudo estiverem gestantes, será realizado acompanhamento até o momento
do parto.
47
Entrevista: Tem por finalidade levantar dados sobre você, dos seus filhos e dos familiares que moram
no seu domicílio, como: 1. sócio-demográficos (local de moradia,l tempo em que vive neste local,
local de nascimento, idade, anos de escolaridade, cidade onde morou); 2. Sobre as doenças que já
teve (alguns dados serão coletados do seu prontuário); 3. Sobre suas práticas sexuais; 4. Risco de
infecção pelo VHB; 5. Sobre o número de filhos; 6. O tipo de parto a que foi submetida em cada
gestação. O seu prontuário médico será revisto no período de 1 (um) ano, para obtenção de
informações referentes ao pré-natal, ao tratamento e exames sorológicos para o VHB. As entrevistas
serão realizadas nas dependências da FMT-AM, propriamente no ambulatório de gestação e doenças
infecto-contagiosas, durante a consulta médica. A entrevista só ocorrerá após: 1. O devido
esclarecimento de suas dúvidas; 2. A leitura deste termo de consentimento livre e esclarecido e 3) A
assinatura do mesmo.
Coleta de Sangue: A coleta será realizada em você, em cada filho respectivo ao período gestacional
dos exames sorológicos positivos para o VHB. Dos recém-nascidos, logo após o parto, será feita a
coleta de sangue do cordão umbilical. Serão coletados 10 ml de sangue (o equivalente a duas
colheres de sobremesa). Neste material serão realizados exames laboratoriais para a determinação
sorológica do Vírus da hepatite B (VHB). A coleta será feita com agulhas descartáveis e por
profissional capacitado, de modo a minimizar os risco inerentes a este procedimento tais como: dor
pela punção, hematomas e flebites (inflamação no local onde foi feita a picada para a coleta do
sangue).
Acompanhamento: As mulheres estiverem gestantes no período de setembro de 2003 a julho de
2005, serão acompanhadas pelos pesquisadores deste projeto até o momento do parto. Os recémnascidos receberam ainda na Maternidade todos os cuidados de imunização necessários: 1. vacina
conta o VHB e imunoglobulina.
O estudo não implica em riscos do ponto de vista clínico, e sua participação é voluntária, podendo
seu consentimento ser retirado a qualquer momento, sem que isto traga prejuízos ao seu atendimento
ou à continuação de seu tratamento.
VI – RESULTADOS E SIGILO DOS DADOS:
O Coordenador e os pesquisadores deste estudo se comprometem a enviar os laudos dos resultados
de exames para o serviço de saúde onde você está sendo atendido, tão logo estes estejam prontos.
O estudo garante a confidencialidade dos dados obtidos. Em nenhum momento serão tornados
públicos os dados relacionados à sua identidade.
VII – FORMAS DE RESSARCIMENTO E INDENIZAÇÃO
Para eventuais ressarcimentos e danos decorrentes da pesquisa a Fundação de Medicina Tropical
FMT-AM se propõe a atender os participantes.
VIII – CONSENTIMENTO PÓS-ESCLARECIDO
Declaro que, após a leitura do texto acima e após ter sido convenientemente esclarecido, consinto em
participar, na qualidade de paciente, deste projeto de pesquisa e, direito a uma cópia deste
Termo.
Local e data ____________________________________, ___ / ___ / ___
Assinatura da paciente ou responsável: ___________________________
Pesquisador que obteve o consentimento:
Nome: _____________________________________________________
Assinatura: _________________________________________________
MARCA DACTICLOSCÓPIA
Qualquer dúvida, favor entrar em contato com o Dr. Iran Grijó Praia, pelo telefone (92) 9983-6884
Dr. Iran Grijó Praia
CRM-AM 1540
48
Anexo 6 – Carta de Apresentação
Caro Colega:
Esta é a senhora __________________________________________________________________,
gestante que participa de um programa de prevenção da transmissão vertical da hepatite B e que
autorizou sua inclusão no estudo que estamos fazendo como dissertação de mestrado da UEA/FMTAM sobre a prevalência da hepatite B em grávidas e a transmissão vertical do vírus da hepatite B(
VHB). Este pode ser transmitido por sangue e seus derivados, compartilhamento de seringas,
sexualmente e durante o período gestacional, particularmente durante o parto. A transmissão
materno-infantil reponde pela maior parte da disseminação viral em países como o Brasil. As
gestantes AgHBs são infectantes e a possibilidade da criança tornar-se infectada é de 70 a 90%;
caso não ocorra a imunização do RN pela imunoglobulina e a vacina cerca de 90% dos infectados
serão carregadores crônicos do VHB e poderão desenvolver infecção crônica e suas complicações
como a cirrose hepática e o hepatocarcinoma. Portanto solicito sua colaboração nesta ação colhendo
sangue do cordão umbilical 2,5 ml em frasco com anticoagulante e 2,5 ml em frasco sem o
anticoagulante, entregando-os aos familiares de modo que os mesmos os transportem ao laboratório
de virologia da FMT-AM acompanhados da requisição anexa.
A parte da prevenção deverá ser feita pela equipe do CRIE da FMT-AM que deve ser acionada até 12
horas pós parto através dos telefones: 238-1711 e 238-1767 quando então a mesma se dirigirá ao
hospital / maternidade e aplicará a imunoglobulina e vacina anti hepatite B no recém nascido.
Certos de contar com sua sensibilidade e atenção, colocamo-nos a sua inteira disposição.
Iran Grijó Praia – 9983-6884