Colégio Anglo – São Carlos
Lista de Exercícios: Modelos Atômicos – 9º E.F.
Profª Beatriz – 13/09/2015
01) "O espaço entre as moléculas atômicas está ocupado por partículas de carga negativa". Esta
é uma afirmação feita por:
a) Dalton;
d) Richter;
b) Thomson;
e) Proust.
c) Rutherford;
02) Há exatos 100 anos, J.J. Thomson determinou, pela primeira vez, a relação entre a massa e a
carga do elétron, o que pode ser considerado como a descoberta do elétron. É reconhecida como
uma contribuição de Thomson ao modelo atômico,
a) o átomo ser indivisível.
b) a existência de partículas subatômicas
c) os elétrons ocuparem níveis discretos de energia.
d) os elétrons girarem em órbitas circulares ao redor do núcleo.
e) o átomo possuir um núcleo com carga positiva e uma eletrosfera.
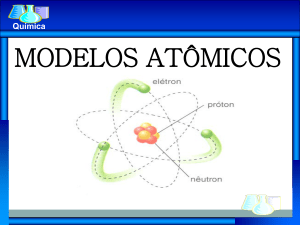
03) Compare os modelos atômicos de Dalton, Thomson, Rutherford Rutherford-Bohr.
04) Ao resumir as características de cada um dos sucessivos modelos do átomo de hidrogênio,
um estudante elaborou o seguinte resumo:
MODELO ATÔMICO: Dalton
CARACTERÍSTICAS: átomos maciços e indivisíveis.
MODELO ATÔMICO: Thomson
CARACTERÍSTICAS: elétron, de carga negativa, incrustado em uma esfera de carga positiva.
A carga positiva está distribuída, homogeneamente, por toda a esfera.
MODELO ATÔMICO: Rutherford
CARACTERÍSTICAS: elétron, de carga negativa, em órbita em torno de um núcleo central, de
carga positiva. Não há restrição quanto aos valores dos raios das órbitas e das energias do
elétron.
MODELO ATÔMICO: Bohr
CARACTERÍSTICAS: elétron, de carga negativa, em órbita em torno de um núcleo central, de
carga positiva. Apenas certos valores dos raios das órbitas e das energias do elétron são
possíveis.
O número de ERROS cometidos pelo estudante é:
a) 0
b) 1
c) 2
d) 3
05) Na produção de fogos de artifício, diferentes metais são misturados à pólvora para que os
fogos, quando detonados, produzam cores variadas. Por exemplo, o sódio, o estrôncio e o cobre
produzem, respectivamente, as cores amarela, vermelha e azul.
Se a localização dos elétrons num determinado nível depende da sua quantidade de energia, é
INCORRETO afirmar que:
a) quando a pólvora explode, a energia produzida excita os elétrons dos átomos desses metais,
fazendo-os passar de níveis de menor energia para níveis de maior energia.
b) os níveis de menor energia são aqueles mais próximos do núcleo, e os níveis de maior
energia são aqueles mais distantes do núcleo.
c) quando o elétron retorna para o estado fundamental, ele cede energia anteriormente recebida
sob a forma de luz.
d) a luminosidade colorida nos fogos de artifício não depende do salto de elétrons de um nível
para outro.
e) no laboratório, o estrôncio poderia ser identificado pela coloração vermelha quando este
recebe o calor de uma chama.
06) Historicamente, a teoria atômica recebeu várias contribuições de cientistas.
Assinale a opção que apresenta, na ordem cronológica CORRETA, os nomes de cientistas que
são apontados como autores de modelos atômicos.
a) Dalton, Thomson, Rutherford e Bohr.
b) Thomson, Millikan, Dalton e Rutherford.
c) Avogadro, Thomson, Bohr e Rutherford.
d) Lavoisier, Proust, Gay-Lussac e Thomson.
e) Rutherford, Dalton, Bohr e Avogadro.
07) O inglês John Dalton, baseado nos resultados de medidas das massas dos participantes de
reações químicas, propôs o primeiro modelo atômico científico. Como era esse modelo? Como
seu modelo ficou conhecido?
08) Qual é a grande descoberta de Thomson com os seus experimentos? Os seus resultados
experimentais levaram a elaboração de um novo modelo atômico, que leva por terra o modelo
atômico de Dalton. Como podemos diferenciar os modelos de Dalton e Thomson? Como o
modelo atômico de Thomson ficou conhecido?
09) Ernest Rutherford realizou em 1911 uma experiência que envolveu a interação de partículas
alfa com a matéria. Uma amostra de polônio radioativo emite partículas alfa (portadoras de
carga elétrica positiva) que incidem sobre uma lâmina muito fina de ouro. Um anteparo indica a
trajetória das partículas alfa após terem atingido a lâmina de ouro.
As interpretações dadas por Rutherford para os resultados dessa experiência permitiram
a criação de um modelo para o átomo.
a) Quais os principais resultados experimentais que levaram Rutherford a criar esse modelo para
o átomo?
b) Como é esse modelo?
10) O sódio e seus compostos, em determinadas condições, emitem luz amarelo-alaranjada
característica. Explique este fenômeno em termos de elétrons e níveis de energia, segundo o
Modelo Atômico de Bohr.