Aula 19
Temática: Métodos de obtenção dos Alcanos (Parte II)
Na aula de hoje, concluiremos o assunto dos métodos de
obtenção dos alcanos. Pirólise, reações de substituição, halogenação, nitração,
sulfonação são tópicos abordados na aula de hoje.
Pirólise é a decomposição de um composto pelo calor. Os alcanos de peso
molecular elevado não resistem a temperaturas superiores a 300 °C sem sofrer
decomposição. Quando se faz passar um alcano através de um tubo metálico
aquecido a 500 ° - 700° C, ele se fragmenta (pirólise) em uma mistura de
alcanos de peso molecular menor, como ilustrado abaixo:
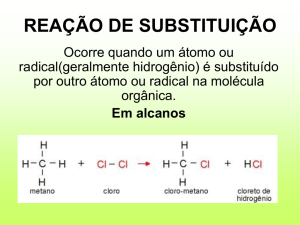
Reações de substituição estas são as reações típicas dos alcanos que é a
substituição por radicais livres, pois por serem os alcanos compostos
saturados, não dão reações de adição. As principais reações de substituição
são: halogenação, Nitração, Sulfonação.
Halogenação é reação com halogênio (grupo 7A da tabela periódica).
Com excesso de cloro a reação prossegue
Os compostos clorados são importantes como solventes orgânicos nãoinflamáveis, usados tanto em laboratório como na indústria.
Nitração é a substituição de hidrogênio pelo grupo nitrito, NO2.
CH3 – H + HO – NO2
Ácido nítrico
CH3 – NO2 + H2O
nitrometano
Sulfonação é a reação de um alcano com o acido sulfúrico concentrado a altas
temperaturas.
Mecanismo da substituição por radical livre:
Vimos na aula de hoje mais alguns métodos para a obtenção
dos alcanos. Na próxima aula passaremos a estudar os alcenos. Até lá!