Produção de gás de síntese a partir da reforma seca com O2 (oxy-dry
reforming) do metano utilizando catalisadores LaNi1-xAlxO3
André Conceiçãoa, Ana Paula Lisboaa, Iana Santosa, Mariana Rochaa, Soraia Brandãoa
a
Grupo de Catálise e Polímeros (GCP) / IQ / UFBA / Rua Barão de Geremoabo, 147, Campus Universitário de Ondina,
Salvador/BA,Brasil
*[email protected]; [email protected].
RESUMEN
Catalisadores tipo perovskita contendo La-Ni-Al substituídos (LaNi1-xAlxO3) foram utilizados e avaliados na
reação combinada entre a reforma seca e oxidação parcial do metano (oxy-dry). Os resultados demonstram
que o material preparado possui boa resistência a altas temperaturas, à medida que mais alumínio é
adicionado à estrutura. Os materiais preparados foram caracterizados por DRX, HSD e TPR e os resultados
dos testes catalíticos foram bastante promissores. LaNi0,2Al0,8O3 obteve o melhor resultado de seletividade
ao H2 e CO (acima de 80%), já os melhores resultados, em termos de rendimento do H 2 e conversão do CH4
foi obtido por LaNi0,8Al0,2O3, com 80% e 70%, respectivamente. A razão H2/CO variou entre 1,51 - 1,68.
Palabras clave: Reforma Catalítica; Perovskitas, Níquel, Alumínio, Lantânio.
ABSTRACT
Perovskite type catalysts La-Ni-Al substituted (LaNi1-xAlxO3) were used and evaluated in the combined
reaction between the dry reforming and partial oxidation of methane (Oxy-Dry). The results show that the
material prepared has good resistance to high temperatures, as more aluminum is added to the structure.
The synthesized materials were characterized by XRD, HSD, and TPR and results of the catalytic tests were
very promising. LaNi0,2Al0,8O3 had the best result of selectivity to H2 and CO (above 80%), while the best results
in terms of yield H2 and CH4 conversion was obtained for LaNi0,8Al0,2O3, with 80 % and 70%, respectively. The
H2 / CO ratio ranged from 1.51 to 1.68.
Keywords (Calibri, 11pt, negrita, justificado): Catalytic reforming; Perovskite, Nickel, Aluminium,
Lanthanum.
1
1. Introducción
O gás de síntese (H2/CO) é utilizado como
matéria prima para diversas aplicações industriais,
dentre elas, a reação de Fischer-Tropsch. A reação
de reforma a vapor é o método mais comum
utilizado na produção desse gás [1-3], entretanto,
esta razão H2/CO, em torno de 3, é deveras alta
para a reação de Fischer-Tropsch. A reforma a
vapor tem como principal desvantagem o gasto de
energia e capital necessários para mantê-la em
operação.
Trabalhos recentes têm focado na reforma
seca do metano como alternativa [4-6] à reforma
a vapor, principalmente em lugares onde há maior
escassez de água para uso industrial, além da
utilização de gases causadores do efeito estufa.
No entanto, assim como na reforma a vapor, esta
reação é altamente endotérmica e necessita de
grande quantidade de energia [5]. Já a oxidação
parcial do metano é moderadamente exotérmica
mas, mesmo gerando mínimas quantidades de
CO2 no decorrer da reação, faz com que gere
grande quantidade de pontos quentes (hot spots)
no reator de leito fixo [7].
A combinação entre a reforma do metano
com CO2 na presença de oxigênio tem sido
realizada com êxito nos últimos anos e [7-8] vem
sendo um processo de reação promissora e
eficiente na produção de gás de síntese por várias
razões, como a melhora no superaquecimento do
leito do catalisador, a redução da deposição de
coque na superfície do catalisador, pois o oxigênio
contido no meio reacional oxida o carbono
depositado, o controle de um nível satisfatório da
razão H2/CO além da redução dos gases de efeito
estufa. [8]
Vários metais como Ni, Co, Fe [9] [10] ou
metais nobres (Pt, Rh, Pd, Ir) [11] [12] têm sido
estudados como ativos para a reação de reforma.
No entanto, o principal problema é a rápida
desativação do catalisador devido a deposição de
coque. Alguns trabalhos têm estudado a
desativação [12] [13] e vêm mostrando que os
metais nobres são menos sensíveis à deposição de
coque, em comparação com o níquel. Algumas
melhorias para o uso do níquel, como sistemas
bimetálicos (Ni-Mn; Ni-Fe) [14] [15] e a adição de
metais alcalinos e/ou de terras raras [16-18] têm
ajudado [20] a reduzir deposição de carbono.
Compostos com uma estrutura definida ou
solução sólida contendo Al ou Mg também têm
despertado interesse [17][19][21]. No presente
trabalho, perovskitas lantânio-alumínio-níquel
preparadas a partir dos precursores nitratos foram
XXV Congreso Iberoamericano de Catálisis
examinadas na reação de reforma seca com
oxigênio (oxy-dry).
2. Experimental
2.1. Preparo dos Catalisadores
Os óxidos mistos LaNixAl1-xO3 foram
preparados a partir do método do citrato. Os
nitratos de níquel, alumínio e lantânio foram
dissolvidos em solução aquosa contendo ácido
cítrico. A proporção metal ácido cítrico é de 1/1,5.
A solução de ácido cítrico foi aquecida
previamente à 40°C, com agitação, até a completa
dissolução do sólido. Após isso, os nitratos de
níquel e alumínio (x = 0 à x = 1) foram adicionados,
nesta mesma ordem, aumentando a temperatura
para valores entre 70-80°C mantida, sobre
agitação, por 1 hora, cada. Por fim, o nitrato de
lantânio foi adicionado ao sistema a temperaturas
entre 80-90°C. A solução resultante foi evaporada
sob refluxo até a formação de uma resina. Em
seguida, todas as resinas foram pré-calcinadas a
300°C por 3 h sob uma taxa de 10°C min -1 a partir
de 25°C. O material obtido foi macerado e
calcinado a 900°C, por 4 h, sob fluxo de ar sintético
de 50 mL min-1 para a formação da fase perovskita.
Os materiais preparados foram codificados
conforme Tabela 1, em que a substituição
estequiométrica do níquel pelo alumínio, com as
letras ”N” representando o níquel e “A”
representando o alumínio e a fração decimal
(exceto pelos LaNiO3 e LaAlO3) das quantidades
desses metais presentes, ou não, em cada
composto preparado logo após cada letra.
Também foi acrescentada a temperatura de
calcinação e a duração da mesma, ao fim do
código.
Tabla 1. Codificação dos materiais sintetizados.
Composto (LaNi1-xAlxO3)
LaNiO3
LaNi0,8Al0,2O3
LaNi0,6Al0,4O3
LaNi0,5Al0,5O3
LaNi0,4Al0,6O3
LaNi0,2Al0,8O3
LaAlO3
Codificação
N1A09004
N8A29004
N6A49004
N5A59004
N4A69004
N2A89004
N0A19004
2.2. Caracterização dos materiais LaNi1-xAlxO3
Os materiais obtidos foram caracterizados
através da Difração de Raios X sem e com variação
de temperatura (DRX e HSD), da Redução com
Hidrogênio à Temperatura programada (TPR-H2).
3
Os óxidos preparados foram caracterizados
por DRX utilizando um difratômetro de raios X
Shimadzu, modelo XRD-6000 com radiação CuKα
para determinação das fases cristalinas (λ= 1,5418
Å). A Redução do hidrogênio à temperatura
programada (TPR) foi realizada utilizando 20mg da
amostra através de um reator tubular em “U” de
quartzo (DI = 1,3 cm) numa unidade
multipropósito acoplada ao espectrômetro de
massas com detector quadrupolar da Balzers,
modelo QMS 200. As análises foram realizadas sob
fluxo de 30 mL min-1 da mistura H2/He (5% H2 em
mol) a uma taxa de aquecimento de 10°C.min-1 de
30°C à 1000°C, onde o sinal do gás H2 (m/z = 2) foi
acompanhado.
2.3. Caracterização dos materiais LaNi1-xAlxO3
As condições reacionais foram as seguintes:
um reator de leito fixo metálico (DI = 9.0mm);
temperatura reacional: 800°C; temperatura de
redução: 600°C; taxa de fluxo na redução: 30
mL.min-1 H2; taxas de fluxo de alimentação: 40
mL.min-1 CH4, 20 mL.min-1 CO2 e 10 mL.min-1 O2;
massa do catalisador: 20 mg. Os gases foram
analisados, na saída, por um cromatógrafo
Shimadzu GC 2014 acoplado a um TCD, que
analisaram os gases remanescentes (CH4, O2 e
CO2) e a produção dos gases CO e H2. Foi utilizada
uma unidade MICROACTIVITY-Reference da PID
Eng & tech. Todos os testes foram realizados por
24h. Também foi realizado um teste reacional sem
o uso de catalisador para avaliar se a temperatura
reacional oferece por si só, ou não, energia
suficiente para que a reação ocorra.
As amostras foram previamente reduzidas
sob atmosfera de H2, com uma taxa de 10°C min-1
e aquecimento das linhas de transferência até
600°C. A atmosfera redutora foi mantida por 30
min. A conversão do metano, a seletividade e o
rendimento do H2 foram calculados da seguinte
forma, conforme equações 1-3:
Conversão CH4:
% = (𝐶𝐻4(𝑒𝑛𝑡) − 𝐶𝐻4(𝑠𝑎𝑖) ) ∗ 100 ⁄𝐶𝐻4(𝑒𝑛𝑡)
(1)
Seletividade H2:
% = (𝐻2 ) ∗ 100⁄2 ∗ (𝐶𝐻4(𝑒𝑛𝑡) − 𝐶𝐻4(𝑠𝑎𝑖)
(2)
Rendimento H2:
% = (𝐻2 ) ∗ 100⁄𝐶𝐻4(𝑒𝑛𝑡)
XXV Congreso Iberoamericano de Catálisis
(3)
3. Resultados y discusión
Caracterização dos materiais LaNi1-xAlxO3
Os diagramas de DRX da série LaNi1-xAlxO3
foram comparados conforme os diagramas de
referência da base de dado do ICSD. As análises
de difração de raios X foram realizadas para
determinação das fases constituintes dos
compostos tipo perovskita com composição
variando de x = 0,0 à x = 1,0 mostradas abaixo na
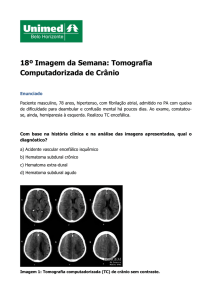
Figura 1. Os perfis de difração de raios X mostram
que as condições de síntese e calcinação
utilizadas foram adequadas para formação das
estruturas perovskitas, tendo como referência os
picos característicos do material LaNiO3 marcado
por ( ) .
A confirmação da fase perovskita, com
simetria romboédrica e sem a presença de outras
fases segregadas, foi confirmada para todos os
compostos sintetizados, além disso pôde-se
verificar um aumento na intensidade dos picos à
medida em que o alumínio é adicionado à
estrutura do material, sugerindo um aumento na
cristalinidade do mesmo.
Figura 1. Difratogramas da estrutura LaNi1-xAlxO3.
Foram feitos estudos TPR para avaliar a
redutibilidade das amostras, em especial do níquel,
sítio ativo metálico do catalisador nas reações de
reforma. O LaNiO3 não é muito estável sob atmosfera
redutora. Com base nessas propriedades, foram
estudadas as curvas de redução à temperatura
programada dos catalisadores conforme Figura 2.
Através da interpretação da mesma, é
evidente que o LaAlO3 é irredutível dentro da faixa de
temperatura estudada. Pelo contrário, LaNiO3 é
reduzida em duas zonas: a primeira em La2NiO5 (290 410°C) e, em seguida, a segunda em Ni/La2O3 (~520°C).
O primeiro pico de redução é semelhante para
todas as amostras e a sua temperatura se situa entre
245 e 335°C. O segundo pico varia de 520°C para
N1A09004 e 350°C para N2A89004. À medida em que
o elemento alumínio é inserido na estrutura do
composto, ou seja, maior o valor de x em LaNi1-xAlxO3,
menor o consumo de hidrogénio.
4
intensidades muito baixas, em relação à intensidade
dos picos do percussor N1A09004. Devido a isso, os
esses materiais ganham maior estabilidade a variações
de temperatura sob atmosfera redutora. Nas duas
figuras pode ser observada a diminuição no tamanho
dos picos de maior intensidade com o aumento da
temperatura.
Figura 2. Redução do hidrogênio à
Temperatura programada de alguns dos compostos
LaNi1-xAlxO3.
As análises de HSD foram realizadas conforme
a maior temperatura de redução obtida na análise de
TPR, para os catalisadores. As temperaturas estudadas
foram de 350°C, 450°C, 600°C, 700°C e 800°C, sendo
que esta última foi avaliada por ser a mesma
temperatura de reação dos testes catalíticos. As
Figuras 3, 4 e 5 mostram os difratogramas
comparativos das amostras de N1A09004, N2A89004 e
N5A59004 para as diferentes temperaturas de
redução. Analisando o primeiro gráfico, podemos
observar a redução das espécies N3+ a N2+ (reação 1) à
350°C, além da redução das espécies N2+ a N0 (reação
2) à 600°C.
2LaNiO3 + H2 → La2Ni2O5 +H2O
(reação 1)
La2Ni2O5 + 2H2 → La2O3 + 2Ni0 + 2H2O
(reação 2)
Figura 4. Difratograma HSD da estrutura LaNi0,5Al0,5O3.
Figura 5. Difratograma HSD da estrutura LaNi0,2Al0,8O3.
Figura 3. Difratograma HSD da estrutura LaNiO3.
Nas figuras 4 e 5 não é perceptível a redução
do material, visto que não há mudanças no perfil dos
difratogramas estudados, ou seja, a fase perovskita
permanece imutável com o aumento da temperatura.
Isso também pode ser comprovado através do gráfico
de TPR para os compostos contendo alumínio em sua
estrutura, em que há picos de redução com
XXV Congreso Iberoamericano de Catálisis
Conforme já descrito, os testes catalíticos
foram realizados à 800°C com pré-tratamento das
amostras (redução) à 600°C.
A média dos valores da razão H2/CO
encontrados, para N2A89004, N5A59004 e N8A29004
de 1,60, 1,51 e 1,68 respectivamente, conforme figura
6. As seletividades ao hidrogênio e ao carbono, com o
passar do tempo podem ser observadas através da
figura 7, variando em média de 80 a 85% para o H2 e
de 71 a 80% para o CO. Os melhores resultados foram
encontrados para o composto N2A89004.
Na saída dos gases do cromatógrafo foi
observada a formação de quantidade considerável de
água, fato que faz levar em conta a reação oposta à de
deslocamento gás-água, ou reação reversa de “shift”,
conforme reações 3 e 4.
CO + 3H2 → CH4 + H2O
(reação 3)
CO2 + H2 → CO + H2O
(reação 4)
5
A figura 8 apresenta a conversão do metano
para os mesmos materiais. O composto N8A29004
apresentou os melhores resultados com valores
crescentes de conversão e sua curva teve um
comportamento crescente ao longo do tempo até se
estabilizar, assim como N5A59004. Já o material
N2A89004 chegou a seu máximo na primeira aquisição
de dados e se manteve constante ao longo do tempo.
Figura 6. Razão H2/CO dos compostos LaNi0,2Al0,8O3,
LaNi0,5Al0,5O3 e LaNi0,8Al0,2O3 conforme tempo de
reação.
Conforme figura 9, N8A29004 apresentou o
melhor resultado em relação ao rendimento para o H2.
Os gráficos apresentaram mesmo comportamento
crescente para N5A59004 e N8A29004, além do
mesmo comportamento de estabilidade nos
resultados desde o primeiro ponto de aquisição de
dados para N8A29004.
Figura 9. Rendimento (H2) para LaNi0,2Al0,8O3,
LaNi0,5Al0,5O3 e LaNi0,8Al0,2O3, em porcentagem.
Os resultados da reação de 8h para o teste em
branco se encontram na figura 10. Pode-se notar que
os valores de Rendimento e conversão do metano não
foram significativos, apresentando valores menores
que 2%.
Figura 7. Seletividade ao H2 e ao CO para (1) =
LaNi0,2Al0,8O3, (2) = LaNi0,5Al0,5O3 e (3) = LaNi0,8Al0,2O3,
em porcentagem.
Figura 10. Oxy-dry: conversão (CH4), rendimento (H2) e
rendimento (CO) sem uso de catalisador.
4. Conclusiones (Calibri, 12pt, negrita)
Figura 8. Conversão do CH4 para LaNi0,2Al0,8O3,
LaNi0,5Al0,5O3 e LaNi0,8Al0,2O3, em porcentagem.
XXV Congreso Iberoamericano de Catálisis
Todos os compostos tipo perovskita
LaNixAl1-xO3, conforme análise por DRX, foram
produzidos com êxito, demonstrando que o
método de preparação (citrato) foi apropriado.
Com a substituição gradativa do níquel pelo
alumínio, foi observado que os compostos sofrem
redução mínima, mantendo-se sobre a forma de
perovskita nas condições reacionais, fato
comprovado através das análises de HSD e TPR. O
6
LaNi0,8Al0,2O3 apresentou melhor resultado frente
aos outros materiais testados, dentro dos
parâmetros reacionais estudados, exceto pela
seletividade, em que o material LaNi0,2Al0,8O3
obteve valores equiparáveis para H2 e foram
melhores para o CO. Os catalisadores foram
ativos e seletivos para a reação de reforma seca
com O2, com razão H2/CO dentro da faixa
estequiométrica esperada [8].
5. Agradecimientos (Calibri, 12pt, negrita)
Os Autores agradecem à Fapesb, Capes e
CNPq pelo financiamento.
6. Referencias (Calibri, 12pt, negrita)
15. H. Provendier, C. Petit, C. Estournes, S. Libs, A.
Kiennemann. Applied Catalysis A 180 (1999) 163173.
16. Z. Chang, Q. Wu, J. Li, Q. Zhu. Catalysis Today,
30 (1996) 147-155.
17. A. Slagtern, U. Olsbye, R. Bloom, I. M. Dahl, H.
Fjelluay. Applied Catalysis A 145 (1996) 375-388.
18. R. Blom, I. M. Dahl, A. Slagtern, B. Sortland, A.
Spjelkavik, E. Tangstad. Catalysis Today. 21 (1994)
535-543
19. E. Ruckenstein, Y. H. Hu. Applied Catalysis A
133 (1995) 149-161.
20. Y. Kathiraser, W. Thitsartarn, K. Sutthiumporn,
S. Kawi. Journal of Physical Chemistry C 117 (2013)
8120–8130.
21. X. Zheng, S. Tan, L. Dong, S. Li, H. Chen, S. Wei.
Fuel Processing Technology 137 (2015) 250–258.
1. H..S Roh, I.H. Eum, D.W. Jeong. Renewable
Energy 42 (2012) 212-216.
2. B. Bej, N.C. Pradhan, S. Neogi. Catalysis Today
207 (2013) 28-35.
3. D. Mei, V. A. Glezakou, V. Lebarbier, L. Kovarik,
H. Wan, K. O. Albrecht, M. Gerber, R. Rousseau, R.
A. Dagle. Journal of Catalysis, 316 (2014) 11-23.
4. A Serrano-Lotina, L Daza. International Journal
of Hydrogen Energy 39 (2014) 4089-4094.
5. E. Ruckenstein, Y.H. Hu. Industrial and
Engineering Chemistry Research 37 (1998) 17441747.
6. I. Luisetto, S. Tuti, E. Di Bartolomeo.
International journal of hydrogen energy 37
(2012) 15992-15999.
7. B. Nematollahi, M. Rezaei, M. Khajenoori
International journal of hydrogen energy 36
(2011) 2969-2978.
8. K. Tomishige, M. Nurunnabi, K. Maruyama, K.
Kunimori. Fuel Processing Technology 85 (2004)
1103–1120.
9. A. Jahangiri, H. Aghabozorg, H. Pahlavanzadeh,
J. Towfighi. International Journal of Chemical
Reactor Engineering 12 (2014) 25-34.
10. E. Yang, Y. Noha, S. Ramesha, S. S. Lima, D. J.
Moon. Fuel Processing Technology 134 (2015)
404-413.
11. S. Palma, L. F. Bobadilla, A. Corrales, S.
Ivanova, F. Romero-Sarria, M. A. Centeno, J. A.
Odriozola. Applyed Catalysis B: Environmental 144
(2014) 846-854.
12. H. Arandiyan, Y. Peng, C. Liu, H. Chang, J. Li.
Journal Chem. Technol. Biotechnol., 2014, 89:
372–381.
13. M. C. J. Bradford, M. A. Vannice. Journal of
Catalysis 173 (1998) 157-171.
14. J. S. Choi, K. I. Moon, Y. G. Kim, J. S. Lee, C. H.
Kim, D. Trimm. Catalysis Letters 52 (1998) 43-47.
XXV Congreso Iberoamericano de Catálisis
7