Nogueira e cols
Mixoma atrial esquerdo como causa de síncope
Arq Bras
Relato
de Cardiol
Caso
2003; 81: 202-5.
Mixoma Atrial Esquerdo como Causa de Síncope
em uma Adolescente
Danilo Castellani Nogueira, Delio Bontempo, Antonio Carlos Menardi, Walter Vilella de A. Vicente,
Paulo José de Freitas Ribeiro, Paulo Roberto Barbosa Evora
Ribeirão Preto, SP
Relato de um caso de mixoma em átrio esquerdo, acometido em paciente de 14 anos com episódios recorrentes
de síncope, encaminhada à cardiologia após investigação neurológica inconclusiva. Os autores discutem as
manifestações clínicas da doença chamando a atenção
para as dificuldades diagnósticas, mediante as apresentações inespecíficas dos sintomas.
De acordo com a clássica casuística do Instituto da
Patologia das Forças Armadas (Washington, D.C.), os
tumores primários do coração, benignos ou malignos, são
encontrados em 0,001% - 0,28% de todas as autópsias, e os
mixomas representam 50% dos tumores benignos do coração 1. Experiências clínicas de duas das maiores instituições
brasileiras (InCor-USP e Instituto Dante Pazzanese de Cardiologia), demonstram a ampla prevalência dos mixomas
cardíacos como tumores cardíacos primários. No InCorUSP, em uma casuística de 50 pacientes coletados em um período de 18 anos, 84% eram do tipo histológico do mixoma 2.
No Instituto Dante Pazzanese de Cardiologia, a experiência
é semelhante: em um período de 28 anos, com uma casuística de 52 portadores de tumores cardíacos, sendo que 82,7%
eram mixomas 3.
No Hospital do Coração de Ribeirão Preto, em um período de 23 anos, cirurgiões do CECORP - Centro especializado do Coração e Pulmão de Ribeirão Preto, operaram 7 pacientes para remoção de tumores cardíacos, sendo 6 portadores de mixomas e um leiomiossarcoma metastático. Entre
os 6 portadores de mixomas cardíacos, a idade variava de 14
a 78 anos e 4 eram do sexo feminino, sendo todos localizados em átrio esquerdo.
Hospital do Coração de Ribeirão Preto/Fundação Waldemar B. Pessoa, CECORP
Centro Especializado do Coração e Pulmão de Ribeirão Preto e Faculdade de Medicina da UNAERP.
Correspondência: Paulo Roberto B. Evora - Rua Rui Barbosa, 367/15 - 14015-120
Ribeirão Preto, SP - E-mail: [email protected]
Recebido para publicação em 10/01/02
Aceito em 9/8/02
Em um período superior a 50 anos (1949 a 2001), foram
publicados 20 artigos nos Arquivos Brasileiros de Cardiologia referentes aos tumores cardíacos primários (fonte: Medline e Index Medicus). O levantamento bibliográfico revelou, ainda, 5 artigos na Revista Brasileira de Cirurgia Cardiovascular (fonte: Scielo) e 13 em outras revistas brasileiras
(fonte: Bireme). Em uma estimativa baseada nessas três
fontes de referências foram relatados em torno de 270 casos
na literatura brasileira.
Embora a síncope seja um sintoma amplamente descrito, como conseqüência da obstrução do trato de entrada do
ventrículo esquerdo, a sua incidência na adolescência é rara,
dificultando a avaliação clínica de síncope nessa faixa
etária. Em um único caso descrito de síncope em adolescente, a causa foi a obstrução do trato de saída do ventrículo
esquerdo por um mixoma localizado nessa câmara cardíaca 4.
Um relato na literatura brasileira apresentou um caso de acidente vascular isquêmico em criança do sexo feminino com
oito anos de idade 5 .
Esses dados justificam o relato deste caso de síncope
em uma adolescente, causada pela presença de um mixoma
cardíaco do átrio esquerdo, que obstruía valva mitral de forma intermitente.
Relato do Caso
Paciente do sexo feminino, 14 anos, moradora da cidade de São Simão, SP, procurou consultório de cardiologia
clínica no mês de abril/00 com queixa de três episódios de
síncope nos últimos três meses. Durante esse intervalo de
tempo esteve em avaliação com um neurologista, sem conclusão diagnóstica em relação às síncopes, sendo então
encaminhada ao cardiologista devido à presença de uma
taquicardia em repouso.
Na primeira consulta com o cardiologista, estabeleceuse diagnóstico de síncope a esclarecer, porém ao exame físico chamou a atenção a presença de taquicardia com uma
freqüência cardíaca de 130bpm, e do baixo peso corporal
com acentuada perda de peso nos últimos três meses. A
Arq Bras Cardiol, volume 81 (nº 1), 202-5, 2003
202
Arq Bras Cardiol
2003; 81: 202-5.
ausculta cardíaca, nessa ocasião, não evidenciou nenhum
sopro cardíaco. Com a hipótese clínica de hipertireoidismo
foram solicitadas as dosagens de hormônios tireoidianos e
a realização de um eletrocardiograma. A função hormonal
estava normal e no eletrocardiograma identificou-se uma
taquicardia sinusal, acompanhada de uma possível sobrecarga de átrio esquerdo. Levantou-se, então, a hipótese
diagnóstica de uma cardiopatia com sobrecarga atrial
esquerda, sendo solicitado radiografia de tórax e ecocardiograma transtorácico. A radiografia mostrou hilos aumentados, aumento da densidade na topografia do átrio esquerdo
e abaulamento do tronco da artéria pulmonar. O ecodopplercardiograma evidenciou átrio esquerdo com dilatação moderada, apresentando no seu interior imagem sugestiva de
tumor intracardíaco do tipo mixoma e valva mitral com discreta insuficiência, causada pelo deslocamento do tumor
para dentro do ventrículo esquerdo (fig. 1-B). A paciente foi
então encaminhada para o serviço de cirurgia cardíaca.
Na consulta pré-operatória, uma semiologia dirigida
para o diagnóstico, revelou uma história de síncope há quatro meses, com palidez extrema e recuperação cerca de 1min
após. Teve novo quadro semelhante durante colheita de
amostra de sangue. Apresentou novo pródromo do sintoma, que passou ao sentar-se. Com acentuação de anemia
começou a apresentar cansaço aos grandes esforços e perdeu 9kg em 4 meses. Surgiu tosse constante ao deitar-se, e a
criança referia que em determinadas posições não apresentava dispnéia, conseguindo dormir muito bem em decúbito
Nogueira e cols
Mixoma atrial esquerdo como causa de síncope
ventral. Não apresentava antecedente familiar de neoplasia
cardíaca. À ausculta cardíaca apresentava sopro sistólico
em foco mitral, que mudava de características conforme a
mudança de decúbito. A pressão arterial era de 90/60mmHg,
a freqüência cardíaca de 100bpm, e não apresentava sinais
congestivos. Os exames pré-operatórios mostraram hemoglobina de 9,1g/dl, hematócrito de 32%, 7400 leucócitos/dl,
548000 plaquetas/mm3, creatinina 0,6 g/dl, uréia 18 g/dl e urina rotina sem anormalidades.
Realizou-se o procedimento cirúrgico com auxílio de
circulação extracorpórea, em maio/00, através de uma esternotomia mediana. A cardiotomia consistiu de uma incisão
transversa dos átrios direito e esquerdo, ampliando-se a
incisão por cerca de 2cm rumo ao septo interatrial. Observaram-se cavidades direitas tensas e levemente aumentadas,
um tumor grande em átrio esquerdo preenchendo quase
toda a câmara cardíaca, com pedículo na parede atrial entre a
veia do lobo inferior e teto da origem da veia cava inferior.
Realizou-se a exérese do tumor com retirada de sua base de
implantação e sutura direta da parede atrial no local da retirada do tumor. O diagnóstico anatomopatológico foi conclusivo com o diagnóstico de mixoma cardíaco (fig. 2).
Em um ano recuperou 11 quilos, não mais apresentando síncopes e palpitações com o desaparecimento do quadro de anemia. Encontra-se absolutamente assintomática
em um seguimento de 20 meses.
Discussão
Os tumores cardíacos são situações não muito comuns
na prática clínica, sendo mais freqüentes os tumores secundários, numa razão que pode chegar a 40:1. Os tumores cardíacos primários são raros e geralmente apresentam um
caráter benigno, sendo o mixoma o tumor primário responsável por 50% dos casos. O mixoma cardíaco tem uma prevalência maior em mulheres, e raro em crianças, e localiza-se,
principalmente, no átrio esquerdo, com uma incidência superior a 70% nesta câmara, sendo 94% tumores solitários.
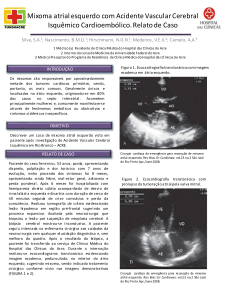
Fig. 1 - Estudo ecocardiográfico. A) Modo M: o asterisco assinala imagens ecodensas do tumor; B) janela ecocardiográfica bidimensional “quatro câmaras”: a seta
mostra claramente o tumor prolapsando através da valva mitral; C) janela ecocardiográfica bidimensional “quatro câmaras” (abaixo) mostrando o resultado pós-operatório sem a imagem tumoral.
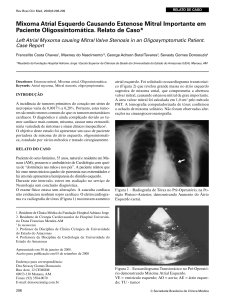
Fig. 2 - Mixoma extirpado cirurgicamente com auxílio de circulação extracorpórea. A
seta realça a impressão do anel valvar mitral em sua posição mediana transversa e o
asterisco assinala o pedículo do tumor.
203
Nogueira e cols
Mixoma atrial esquerdo como causa de síncope
Acomete principalmente os indivíduos entre a 3ª e 6ª década de vida e não apresenta nenhum padrão de herança característico, exceto o mixoma familiar que apresenta herança
autossômica dominante. Os mixomas são redondos ou
ovais, compactos, sésseis ou pedunculados. Os mixomas
pedunculados são os mais freqüentes, chegando a representar 83% dos casos. Surgem do endocárdio a partir de uma
célula mesenquimal ou célula multipotente do subendocárdio, formando uma massa branca, amarelada ou amarronzada, freqüentemente recoberta por trombos. Apresenta tamanho médio de 5cm de diâmetro e peso de 50 a 60g.
Apesar do tumor ter características benignas a sintomatologia irá depender do tamanho, forma, mobilidade e
localização do tumor, sendo as manifestações mais comuns
a dispnéia em até 80% dos pacientes em alguns estudos e
insuficiência cardíaca congestiva em 56%.Os pacientes podem apresentar-se com dor torácica atípica, síncope, letargia, mal estar, perda de peso, palpitação, edema periférico,
edema agudo de pulmão, embolia pulmonar, isquemia cerebral e ataque isquêmico transitório, fibrilação atrial, flutter
atrial e outras taquiarritimias, hemoptise, embolização periférica e infecção com quadro clínico de endocardite bacteriana. Os pacientes podem apresentar ausculta similar a estenose mitral associado ao ruído tumoral (plop tumoral). O
exame mais útil no diagnóstico é o ecocardiograma, que apresenta grande sensibilidade e pode diagnosticar até 100%
dos casos. Alguns dados inespecíficos podem ser observados como aumento da velocidade de hemossedimentação,
anemia, leucocitose, trombocitopenia, trombocitose, hipogamaglobulinemia e proteína C reativa aumentada.
Em uma metanálise da literatura, utilizando referências
da Medline, selecionamos 295 pacientes com mixoma, sendo
68% (202) do sexo feminino e 32% (93) do sexo masculino. A
prevalência de mixomas em átrio esquerdo atingiu 81% (239
pacientes), 16% (47) em átrio direito e 3% (9) em outra localização. A idade média dos pacientes ficou em torno de 48
anos e 92,7% deles eram sintomáticos. As manifestações
clínicas apresentaram variações nos diversos estudos, sendo predominante o sintoma de dispnéia por insuficiência
cardíaca congestiva. Outros fenômenos bastante citados na
literatura são: a embolização que varia de 17% a 50%, taquiarritmia de 24% a 25,7%, sintomas constitucionais de 9,3% a
45% que estão presentes apenas em mixoma atrial esquerdo, dor no peito de 12,9% a 25% e síncope de 6% a 18,9%.
Os mixomas devem estar incluídos no diagnóstico diferencial de doença valvular cardíaca, insuficiência cardíaca, cardiomegalia, endocardite bacteriana, distúrbios do ritmo supraventricular e ventricular, síncope, embolias pulmonar e sistêmica. A investigação laboratorial inclui a pesquisa de proteínas inflamatórias, o aumento da velocidade de
hemossedimentação, a presença de anemia, eletroforese
anormal, hipoproteinemia e elevação de fosfatase alcalina.
Na avaliação do paciente com síncope cardíaca é fundamental a realização de eletrocardiograma e ecocardiograma, para o diagnóstico de arritmias cardíacas e doenças valvares. Os tumores cardíacos são geralmente diagnosticados pelas imagens ecográficas devido a estas investiga204
Arq Bras Cardiol
2003; 81: 202-5.
ções. Outros métodos podem auxiliar no diagnóstico do mixoma, como a tomografia computadorizada e a ressonância
nuclear magnética, e podem ser importantes para orientar a
abordagem cirúrgica. A cineangiocoronariografia pode ser
um exame de grande valia na detecção dos tumores, tendo
evidenciado 84% dos casos em alguns estudos. A avaliação cardíaca pré-operatória completa é importante para
conduzir o cirurgião à correção de outros problemas cardíacos como reconstrução valvar, implantação valvar artificial
e reconstrução de parede atrial.
A intervenção cirúrgica com ressecção completa do
tumor é essencial para a cura da doença e evita a recidiva do
tumor com subseqüentes reoperações que expõe o paciente
a outras complicações como sangramentos e necessidade de
hemoderivados 6-8. A taxa de recidiva do tumor é muito baixa,
sendo a sobrevida após a cirurgia elevada, com uma taxa de
mortalidade hospitalar em torno de 4 %. Um dos casos, operado pelo CECORP, tratava-se de uma recidiva do tumor. Interessante relato de caso da literatura nacional revela a recorrência de mixoma com localização multicavitária, existindo algumas evidências de que a recidiva possa relacionar-se com
a produção de fatores de crescimento. Alem dessa possibilidade outros possíveis mecanismos de recidiva incluem:
excisão incompleta do tumor, implantação intracardíaca,
embolização periférica e crescimento a partir de outro foco.
Mas, de um modo geral, o resultado cirúrgico em longo prazo
é muito bom, permanecendo poucos pacientes sintomáticos
em classe funcional I da New York Heart Association
(NYHA) e uma minoria em classe funcional II.
Nossa paciente apresentava quadro de síncope cardíaca, um sintoma responsável por 2 a 3% das síncopes que
levam a uma avaliação médica. Estas síncopes ocorrem devido à diminuição do débito cardíaco pela obstrução tumoral.
Este tipo de sintoma é mais comum após período de curta
atividade física e reversível tão logo ocorra a desobstrução.
A obstrução, principalmente por tumores pedunculados
grandes, pode levar a uma diminuição no fluxo cerebral e
ocasionar morte súbita.
Os portadores de mixoma cardíaco apresentam-se com
uma tríade clássica de sintomas: manifestações constitucionais, embólicas ou obstrutivas. No caso relatado, a adolescente não apresentou fenômenos embólicos. As manifestações constitucionais, muitas vezes lembram doença autoimune. Quando se buscam explicações para a anemia e a
acentuada perda de peso, desaparecidas com a retirada do
tumor, não é possível concluir-se por algum mecanismo específico. Não se sabe se o tumor secreta alguma substância
ou se ele se relaciona com algum mecanismo imunológico
semelhante ao que ocorre na fisiopatologia das doenças
auto-imunes. Outro detalhe a ser destacado é a pouca idade
da paciente. Este dado poderia sugerir uma característica
congênita, porém um cuidadoso interrogatório sobre os
antecedentes familiares não revelou nenhum caso semelhante em sua família. De qualquer forma fica o alerta para a
possibilidade de um mixoma de cavidades cardíacas esquerdas como causa de síncope, ressaltando-se a sua raridade em crianças e adolescentes.
Arq Bras Cardiol
2003; 81: 202-5.
Nogueira e cols
Mixoma atrial esquerdo como causa de síncope
Referências
1.
2.
3.
4.
Mc Allister HA Jr, Fenoglio JJ Jr. Tumors of the cardiovascular system. Fascicle
15, Second Series. Atlas of Tumor Pathology. Washington DC: Armed Forces
Institute of Pathology, 1978.
Fernandes F, Soufen HN, Ianni BM, Arteaga E, Ramires FJ, Mady C. Primary
neoplasms of the heart: clinical and histological presentation of 50 cases. Arq
Bras Cardiol 2001; 76: 231-7.
Abdulmassih CN, Salerno PR, Dinkhuysen JJ, et al. Correção cirúrgica dos
tumores primários do coração. Rev Bras Cir Cardiovasc 1992; 7: 145-52.
Delgado LJ, Montiel J, Guindo J, et al. Myxoma of the left ventricle: a cause of
syncope in an adolescent. Rev Esp Cardiol 1998; 51: 674-6.
5.
6.
7.
8.
Takakura IT, Godoy MF, Soares MJ, Moscardini AC, Braile DM. Mixoma atrial
esquerdo com acidente vascular cerebral isquêmico em criança. Arq Bras Cardiol
1998; 71: 135-7.
Reynen K. Cardiac myxomas. N Engl J Med 1995; 333: 1610-7.
Husar J, Ivancan V, Korda Z, et al. Cardiac myxoma: diagnostic approach, surgical
treatment and follow up: a twenty years experience. J Cardiovasc Surg 1996; 37:
113-7.
Lijoi A, Scoti P, Faveto C, et al. Surgical management of intracardiac myxomas: a
16-year experience. Tex Heart Inst J 1993; 20: 231-4.
Bula resumida – MICARDIS® Telmisartam - Uso adulto - Forma farmacêutica e apresentações: Comprimidos de 40 mg: embalagens com 14 e 28 comprimidos. Comprimidos de 80 mg: embalagens com 14 e 28
comprimidos. Composição: Cada comprimido contém 40 mg ou 80 mg de telmisartam. Excipientes q.s.p. 1 comprimido. Indicações: Tratamento da hipertensão arterial, como monoterapia ou em associação com
outros agentes anti-hipertensivos. Contra-indicações: Hipersensibilidade ao ingrediente ativo ou aos excipientes. Gravidez e lactação. Obstrução biliar. Disfunção hepática ou renal grave. Intolerância hereditária
à frutose. Precauções: Hipertensão renovascular: pacientes com estenose arterial renal bilateral ou estenose da artéria com um único rim funcionando: risco aumentado de hipotensão grave e insuficiência renal.
Disfunção renal ou transplante hepático: monitoração periódica dos níveis séricos de potássio e creatinina. Não há experiência em pacientes com transplante renal recente. Desidratação: hipotensão
sintomática, especialmente após a primeira dose, pode ocorrer em pacientes que têm volemia e/ou sódio depletado, o que deve ser corrigido antes do início da terapêutica com MICARDIS. Outras condições de
estimulação do SRAA e condições dependentes da atividade SRAA (insuficiência cardíaca congestiva grave): hipotensão aguda, hiperazotemia, oligúria ou, raramente, insuficiência renal aguda.
Hiperaldosteronismo primário: não se recomenda o uso de MICARDIS. Estenose valvar aórtica e mitral e cardiomiopatia hipertrófica obstrutiva: Recomenda-se precaução especial. Hipercalemia: recomendase monitoração adequada dos níveis séricos de potássio em pacientes de risco. Diuréticos poupadores de potássio, suplementos de potássio, sais de potássio ou outros medicamentos que podem aumentar
os níveis de potássio, como a heparina: podem levar a um aumento da potassemia. Portanto, nestas situações MICARDIS deve ser administrado com cautela. Distúrbios hepatobiliares: pode-se esperar redução
da depuração em pacientes com disfunções obstrutivas do sistema biliar ou insuficiência hepática, pois a eliminação da droga é principalmente biliar. Intolerância à frutose: os comprimidos de MICARDIS contém
sorbitol; portanto, é inadequado para pacientes com intolerância hereditária à frutose. Outros: menor eficácia na redução da pressão arterial na população negra do que na população não-negra. Cardiopatia
isquêmica ou doença cardiovascular isquêmica pode resultar em infarto do miocárdio. Interações medicamentosas: MICARDIS pode aumentar o efeito hipotensor de outros agentes anti-hipertensivos. Observouse um aumento de 20% da concentração plasmática média de digoxina. Relataram-se aumentos reversíveis das concentrações séricas de lítio e de toxicidade; portanto, recomenda-se cuidadosa monitoração
do uso concomitante com lítio. Gravidez e lactação: Contra-indicado. Reações adversas: As reações adversas à droga obtidas a partir de todos os estudos clínicos com telmisartam foram: Infecções do trato
urinário, infecções do trato respiratório superior, ansiedade, visão anormal, vertigem, dor abdominal, diarréia, boca seca, dispepsia, flatulência, dor de estômago, eczema, aumento de suor, artralgia, dor nas
costas, cãibras nas pernas ou dores nas pernas, mialgia, sintomas de tendinite, dor no peito, sintomas de gripe. Além disso, desde a introdução de telmisartam no mercado, relataram-se casos raros de eritema,
prurido, desmaio, insônia, depressão, vômito, hipotensão, bradicardia, taquicardia, dispnéia, eosinofilia, trombocitopenia, fraqueza e perda de eficácia. Relataram-se casos isolados de angioedema, urticária
e outros eventos relacionados. Investigações: Raramente, observaram-se diminuição na hemoglobina ou aumento no ácido úrico. Observaram-se aumentos na creatinina ou nas enzimas hepáticas. Efeitos
na habilidade de dirigir e utilizar máquinas: Ainda não se realizaram estudos específicos. Contudo, ao dirigir ou operar máquinas, pode ocasionalmente ocorrer tontura ou sonolência. Posologia: A dose
recomendada é de 40 mg uma vez ao dia. Alguns pacientes podem apresentar benefício com dose diária de 20 mg. Em casos em que a pressão arterial pretendida não seja atingida, a dose de MICARDIS pode
ser aumentada para no máximo 80 mg uma vez ao dia. Alternativamente, MICARDIS pode ser usado em combinação com diuréticos tiazídicos, como a hidroclorotiazida, para se obter uma redução maior da
pressão arterial. Quando se considerar um aumento da dose, deve-se levar em conta que o máximo efeito anti-hipertensivo é geralmente atingido quatro a oito semanas após o início do tratamento. MICARDIS
pode ser administrado com ou sem alimento. Insuficiência renal: Não há necessidade de ajustes de dose em pacientes com insuficiência renal leve a moderada. Telmisartam não é removido do sangue por
hemofiltração. Insuficiência hepática: Nos pacientes portadores de insuficiência hepática leve a moderada, não se deve exceder a dose diária de 40 mg. Pacientes idosos: Não são necessários ajustes de doses.
Crianças e adolescentes: Não há dados de segurança e eficácia de MICARDIS em crianças e adolescentes. VENDA SOB PRESCRIÇÃO MÉDICA - MS - 1.0367.0110 - Boehringer Ingelheim do Brasil Química
e Farmacêutica Ltda.
Bula resumida – MICARDIS® HCT – Telmisartam/Hidroclorotiazida - Uso adulto - Composição: Cada comprimido de MICARDIS HCT contém 40 mg/12,5 mg ou 80 mg/12,5 mg de telmisartam/hidroclorotiazida.
Embalagens com 14 e 28 comprimidos. Excipientes q.s.p. 1 comprimido. Indicações: Tratamento da hipertensão arterial. MICARDIS HCT, como associação de dose fixa, é indicado em pacientes cuja pressão
arterial não é adequadamente controlada com telmisartam ou hidroclorotiazida isoladamente. Posologia: MICARDIS HCT deve ser administrado uma vez ao dia. A dose de MICARDIS pode ser aumentada
gradativamente antes de substituí-lo pelo MICARDIS HCT. A substituição direta da monoterapia pelas combinações fixas pode ser considerada. MICARDIS HCT 40/12,5 mg pode ser administrado em pacientes
cujas pressões sangüíneas não sejam adequadamente controladas por MICARDIS 40 mg ou hidroclorotiazida. MICARDIS HCT 80/12,5 mg pode ser administrado em pacientes cujas pressões arteriais não sejam
adequadamente controladas por MICARDIS 80 mg ou por MICARDIS HCT 40/12,5 mg. O máximo efeito anti-hipertensivo é obtido após 4 a 8 semanas de tratamento. Quando necessário, MICARDIS HCT pode ser
administrado com outros anti-hipertensivos. MICARDIS HCT pode ser administrado com ou sem alimento. Devido ao componente hidroclorotiazida, MICARDIS HCT não deve ser usado em pacientes com
disfunção renal grave. Nos casos leves a moderados, não se observaram efeitos adversos renais e não é necessário ajuste de dose. Recomenda-se monitoração periódica da função renal. Nos casos de
insuficiência hepática leve a moderada, não se deve exceder a dose de 40/12,5 mg uma vez ao dia. MICARDIS HCT não é indicado em pacientes com insuficiência hepática grave. Não são necessários ajustes
de dose conforme a idade. Ainda não se estabeleceram a segurança e a eficácia de MICARDIS HCT em pacientes menores de 18 anos. Contra-indicações: Hipersensibilidade aos componentes ativos,
excipientes ou substâncias derivadas de sulfonamidas (como HCT). Gravidez e lactação. Colestase e distúrbios obstrutivos biliares. Insuficiência hepática ou renal grave (depuração de creatinina <30 ml/min).
Hipopotassemia refratária e hipercalcemia. Precauções: Não utilizar nos casos de colestase, distúrbios biliares obstrutivos ou insuficiência hepática grave. Usar com cautela nos casos de função hepática
alterada ou doença hepática progressiva, pois pode ocorrer coma hepático. Há maior risco em pacientes com estenose arterial renal bilateral ou estenose com um único rim funcionando. Micardis HCT não deve
ser administrado em pacientes portadores de disfunção renal grave. Não há experiência quanto à administração de MICARDIS HCT em pacientes com grave insuficiência renal ou com um rim transplantado
recentemente. Recomenda-se a monitoração periódica dos níveis séricos de potássio, creatinina e ácido úrico. A azotemia associada a diuréticos tiazídicos pode ocorrer em pacientes com função renal alterada.
Pode ocorrer hipotensão sintomática em pacientes que têm volemia e/ou sódio depletado. Insuficiência cardíaca congestiva grave ou doença renal, estenose da artéria renal tratada concomitantemente com
drogas que afetem o sistema renina-angiotensina-aldosterona foram associados com hipotensão aguda, hiperazotemia, oligúria ou, raramente, insuficiência renal aguda. Aldosteronismo primário: não se
recomenda o uso de telmisartam, precaução especial em estenose valvar aórtica ou mitral e cardiomiopatia hipertrófica obstrutiva. Como tiazidas podem prejudicar a tolerância à glicose, pode ser necessário
ajuste no tratamento em diabéticos e pode ocorrer manifestação de diabetes latente. A hidroclorotiazida aumenta os níveis de colesterol e triglicérides; contudo, nenhum ou poucos efeitos adversos foram
relatados na dose de 12,5 mg contida em MICARDIS HCT. Pode ocorrer hiperuricemia ou precipitação de gota devido a hidroclorotiazida. Pode ser necessária monitoração periódica dos níveis séricos de
eletrólitos, uma vez que a hidroclorotiazida pode causar desequilíbrio eletrolítico ou de fluidos (hipopotassemia, hiponatremia e alcalose hipoclorêmica). O tratamento concomitante com telmisartam pode
reduzir a hipopotassemia induzida por diuréticos, devido aos efeitos antagônicos. Diuréticos poupadores de potássio, suplementos de potássio ou substitutos do sal contendo potássio devem ser utilizados
concomitantemente com cautela. Não há evidências de que MICARDIS HCT reduza ou previna hiponatremia induzida por diuréticos. A deficiência de cloreto é geralmente leve. Tiazidas podem causar elevação
dos níveis séricos de cálcio e magnésio. Interromper o uso antes dos testes de função da paratireóide. Não utilizar em intolerância hereditária à frutose. A redução excessiva da pressão arterial no caso de doença
cardiovascular isquêmica pode ser prejudicial. Relatou-se exacerbação ou ativação do lupus eritematoso sistêmico com o uso de hidroclorotiazida. Recomenda-se cautela no uso de anti-hipertensivos ao dirigir
e operar máquinas. Interações medicamentosas: Relataram-se aumentos reversíveis das concentrações séricas de lítio durante administração concomitante com inibidores da enzima conversora de
angiotensina. Relataram-se casos de interação com antagonistas dos receptores da angiotensina II. O risco de toxicidade por lítio pode ser aumentado com o uso de MICARDIS HCT. Recomenda-se a monitoração
dos níveis séricos de lítio durante o uso concomitante. O efeito de depleção de potássio da hidroclorotiazida é atenuado pelo efeito poupador de potássio do telmisartam, mas é potencializado por outros diuréticos
caliuréticos, laxantes, corticosteróides, ACTH, anfotericina, carbenoxolona, penicilina G sódica, ácido salicílico e derivados. Por outro lado, o uso concomitante de diuréticos poupadores de potássio,
suplementos/sais de potássio ou outras drogas podem aumentar os níveis séricos de potássio. Nesses casos, recomenda-se a monitoração dos níveis plasmáticos de potássio. Recomenda-se monitoração
periódica de potássio na administração de MICARDIS HCT com digitálicos, antiarrítmicos e drogas que são conhecidamente indutoras de torsades de pointes. Telmisartam pode aumentar o efeito hipotensor de
outros agentes anti-hipertensivos. Observou-se um aumento de 20% da concentração plasmática média de digoxina. Não se identificaram outras interações de importância clínica. Interações com a
hidroclorotiazida: álcool, barbitúricos ou narcóticos (potencialização da hipotensão ortostática); drogas antidiabéticas (ajustes de dose podem ser necessários); metformina (risco de acidose láctica);
colestiramina e resina colestipol (absorção de hidroclorotiazida é prejudicada); corticosteróides, ACTH (depleção eletrolítica, principalmente aumento de hipopotassemia); glicosídeos digitálicos
(hipopotassemia ou hipomagnesemia induzida por tiazídicos favorece o aparecimento de arritmias cardíacas induzidas por digitálicos); drogas antiinflamatórias não-esteroidais (a administração de droga
antiinflamatória não-esteroidal pode reduzir o efeito diurético, natriurético e anti-hipertensivo dos diuréticos tiazídicos em alguns pacientes). Os efeitos das aminas hipertensoras podem ser levemente
diminuídos. Os relaxantes musculares esqueléticos não-despolarizantes são potencializados pela hidroclorotiazida. Medicamentos uricosúricos podem requerer ajustes. Verificou-se aumento da incidência
de reações de hipersensibilidade ao alopurinol. Os efeitos hiperglicêmicos dos beta-bloqueadores e diazóxido podem ser aumentados pelas tiazidas. Os agentes anticolinérgicos (por exemplo, atropina,
biperideno) podem aumentar a biodisponibilidade das tiazidas. As tiazidas podem aumentar os eventos adversos da amantadina. As tiazidas podem reduzir a excreção renal de drogas citotóxicas (por exemplo,
ciclofosfamida, metotrexato). Gravidez e lactação: É contra-indicado. Se ocorrer gravidez, telmisartam deve ser descontinuado o mais breve possível. As tiazidas atravessam a barreira placentária e podem
causar distúrbios eletrolíticos no feto e é possível que ocorram outras reações. Relataram-se casos de trombocitopenia ou icterícia neonatal com o tratamento tiazídico materno. Tiazidas são excretadas no leite
humano e podem inibir a lactação. Reações adversas: Foram relatadas as seguintes reações adversas: Bronquite, faringite, sinusite, infecções do trato respiratório superior, infecções do trato urinário,
sialadenite, eosinofilia, anemia aplástica, anemia hemolítica, depressão da medula óssea, leucopenia, neutropenia/agranulocitose, trombocitopenia, alergia, reações anafiláticas, perda do controle da diabete,
hipercolesterolemia, hiperuricemia, hipopotassemia, causa ou aumento da depleção de volume, desequilíbrio eletrolítico, hiponatremia, anorexia, perda de apetite, hiperglicemia, ansiedade, depressão,
inquietação, tontura, desmaio, insônia, escotomas, parestesia, distúrbios do sono, visão alterada, visão borrada temporariamente, xantopsia, vertigem, bradicardia, taquicardia, arritmias cardíacas, hipotensão,
hipotensão postural, angiite necrotizante (vasculite), dispnéia, sofrimento respiratório (incluindo pneumonite e edema pulmonar), dor abdominal, diarréia, dispepsia, gastrite, dor de estômago, boca seca,
flatulência, vômito, constipação, pancreatite, icterícia (icterícia hepatocelular ou colestática), eczema, aumento do suor, eritema, prurido, reações cutâneas do tipo lupus eritematoso, vasculite cutânea, reações
de fotossensibilidade, erupções cutâneas, reativação do lupus eritematoso cutâneo, necrólise epidérmica tóxica, atralgia, artrose, dor nas costas, dor nas pernas, mialgia, cãibras nas pernas, sintomas de
tendinite, fraqueza, espasmo muscular, nefrite intersticial, disfunção renal, glicosúria, impotência, sintomas de gripe, dor, dor no peito, perda da eficácia, febre. Investigações: Diminuição da hemoglobina, aumento
do ácido úrico, aumento na creatinina, aumento das enzimas hepáticas, aumento dos triglicérides. Assim como ocorre com outros antagonistas da angiotensina II, relataram-se casos isolados de angioedema,
urticária e outras reações relacionadas. VENDA SOB PRESCRIÇÃO MÉDICA. - MS 1.0367.0134 Boehringer Ingelheim do Brasil Química e Farmacêutica Ltda.
205