UNIVERSIDADE ESTADUAL PAULISTA “JÚLIO DE MESQUITA FILHO”
FACULDADE DE CIÊNCIAS AGRONÔMICAS
CAMPUS DE BOTUCATU
OCORRÊNCIA DE BEGOMOVÍRUS EM PLANTAS DE PIMENTÃO NO
ESTADO DE SÃO PAULO E COMPORTAMENTO DE GENÓTIPOS DE Capsicum
spp. AO Tomato severe rugose virus E A Bemisia tabaci MEAM1
KÉSSIA DE FÁTIMA DA CUNHA PANTOJA
Dissertação apresentada à Faculdade de
Ciências Agronômicas da UNESP Campus de Botucatu, para obtenção do
título de Mestre em Agronomia
(Proteção de Plantas).
BOTUCATU – SP
Fevereiro/2014
UNIVERSIDADE ESTADUAL PAULISTA “JÚLIO DE MESQUITA FILHO”
FACULDADE DE CIÊNCIAS AGRONÔMICAS
CAMPUS DE BOTUCATU
OCORRÊNCIA DE BEGOMOVÍRUS DE PLANTAS DE PIMENTÃO NO
ESTADO DE SÃO PAULO E COMPORTAMENTO DE GENÓTIPOS DE Capsicum
spp. AO Tomato severe rugose virus E A Bemisia tabaci MEAM1
KÉSSIA DE FÁTIMA DA CUNHA PANTOJA
Orientadora: Profa. Dra. Renate Krause Sakate
Co-Orientadora: Profa. Dra. Kelly Cristina Gonçales Rocha
Dissertação apresentada à Faculdade de
Ciências Agronômicas da UNESP Campus de Botucatu, para obtenção do
título de Mestre em Agronomia
(Proteção de Plantas).
BOTUCATU – SP
Fevereiro/2014
UNIVERSIDADE ESTADUAL PAULISTA “JULIO DE MESQUITA FILHO”
FACULDADE DE CIÊNCIAS AGRONÔMICAS
CAMPUS DE BOTUCATU
CERTIFICADO DE APROVAÇÃO
TÍTULO: “OCORRÊNCIA DE BEGOMOVÍRUS DE PLANTAS DE PIMENTÃO
NO ESTADO DE SÃO PAULO E COMPORTAMENTO DE GENÓTIPOS DE
Capsicum spp. AO Tomato severe rugose virus E A Bemisia tabaci MEAM1”
ALUNA: KÉSSIA DE FÁTIMA DA CUNHA PANTOJA
ORIENTADORA: PROFA. DRA. RENATE KRAUSE SAKATE
CO-ORIENTADORA: PROFA. DRA. KELLY CRISTINA GONÇALES ROCHA
Aprovado pela Comissão Examinadora
Data da realização: 25 de fevereiro de 2014.
“Sonhe com aquilo que você quer ser,
porque você possui apenas uma vida
e nela só se tem uma chance
de fazer aquilo que quer.
Tenha felicidade bastante para fazê-la doce.
Dificuldades para fazê-la forte.
Tristeza para fazê-la humana.
E esperança suficiente para fazê-la feliz.
As pessoas mais felizes não tem as melhores coisas.
Elas sabem fazer o melhor das oportunidades
que aparecem em seus caminhos.
A felicidade aparece para aqueles que choram.
Para aqueles que se machucam
Para aqueles que buscam e tentam sempre.
E para aqueles que reconhecem
a importância das pessoas que passaram por suas vidas.
Aprendi que hoje é reflexo de ontem, que dor fortalece, que vencer engrandece.
Aprendi que sonhar não é fantasiar, que o valor está na força da conquista,
que fazer é melhor que falar, que o olhar não mente, que viver é aprender com
os erros…
E umas das coisas que aprendi é que se deve viver apesar de.”
(Clarice Lispector)
“O que vale na vida não é o ponto de partida e sim a caminhada. Caminhando
e semeando, no fim terás o que colher.”
(Cora Coralina)
I
Agradeço a Deus, pela vida e por todas as graças concedidas.
DEDICO
Aos meus pais, Maria de Fátima Cunha Pantoja e Isac Nepomuceno Pantoja,
por terem me concedido a vida, por todo ensinamento, educação e compreensão.
Pelos momentos bons e ruins que estiveram ao meu lado, pelo incentivo de cada
dia. Agradeço pelas inúmeras vezes que me enxergaram melhor do que sou, pela
capacidade de me olharem devagar. Pelo apoio que sempre me deram e por
acreditarem nos meus sonhos. Agradeço a vocês, meus pais por natureza, e por
amor.
Ao meu querido irmão Jorge Luíz Cunha Pantoja, pelo amor, amizade e
companheirismo de sempre. Por ser você, meu querido e amado irmão.
Amo Vocês!
“Percebe e entende que os melhores amigos. São aqueles que estão em casa
esperando por ti. Acreditam nos momentos mais difíceis da vida, eles sempre
estarão por perto, pois só sabem te amar. E se por acaso a dor chegar, ao teu
lado vão estar. Pra te acolher e te amparar, pois não há nada como um lar. Tua
família volta pra ela. Tua família te ama e te espera. Para ao teu lado sempre
estar...( Tua Família- Anjos de Resgate).
II
AGRADEÇO
A minha amiga,
Cristiane Melo de Sousa, pela amizade, apoio e companheirismo de sempre.
Pelos momentos alegres e de descontração. Pelos momentos tristes que
dividimos. Pelos momentos em que perdi a paciência, e você veio com palavras
amenas e me acalmou. Pelos momentos de esperança, em que pensamos no
futuro juntas. Por estar sempre ao meu lado nessa jornada e pela ajuda nessa
vitória.
Aos meus queridos amigos de Belém,
Kleber Sousa, pela amizade, apoio e companheirismo de sempre, pelas horas
concedidas de conversas, conselhos e aprendizado. Por estar sempre ao meu
lado em todos os momentos. Por me compreender.
Luana Oliveira, pela amizade, apoio e companheirismo. Por acreditar sempre
nos meus sonhos e em mim. Por nossas conversas e nossos momentos de
descontração.
A Fernando Dias,
Pelo apoio, companheirismo e dedicação, por me ensinar a ver a vida de outra
forma. Por seus conselhos, sua companhia. Por nossos momentos. Por ser quem
é.
Aos amigos do laboratório de Virologia em especial, Daiana Bampi, Evelynne
Ûrzedo, Leysimar Pitzr e Leonardo Barbosa, pelo companheirismo e
principalmente pela amizade.
(“Amigos, pra sempre. Bons amigos que nasceram pela fé. Amigos, pra sempre.
Para sempre amigos sim, se Deus quiser” )
Obrigada a todos por contribuírem para meu sucesso e para meu crescimento
como pessoa. Sou o resultado da confiança e da força de cada um de vocês.
III
AGRADECIMENTOS
À CAPES, pela concessão da bolsa de estudos .
À Universidade Estadual Paulista “Júlio de Mesquita Filho”, Faculdade de Ciências
Agronômicas – Campus de Botucatu, assim como ao Departamento de Proteção de Plantas,
pela oportunidade da realização do curso de mestrado.
À minha Orientadora e prof ª Renate Krause Sakate pela orientação, conselhos e apoio
ao longo deste trabalho, sendo estes requisitos essenciais para minha formação
profissional.
À minha Co-Orientadora Kelly Cristina Gonçales Rocha, pelo apoio, orientação,
ensinamento, amizade e companheirismo. Por acreditar sempre e auxiliar para o
desenvolvimento deste trabalho. Pelo apoio em minha formação profissional e pessoal.
À Drª Alessandra de Jesus Boari, minha primeira orientadora na vida acadêmica, pela
orientação e apoio. Pelos ensinamentos primordiais na fitopatologia e virologia e pela
grande contribuição no meu desenvolvimento profissional.
Ao Prof. Marcelo Agenor Pavan, pela ajuda e contribuições neste trabalho.
Ao Prof. Drº Edson Luiz Lopes Baldin, pelo apoio e ensinamentos transmitidos. E ao
Laboratório de Resistência de Plantas à Insetos e Plantas Inseticidas (LARESPI) .
À Drª. Arlete M. T. Melo, pelo fornecimento de sementes.
Á Sakata Seed Sudamerica pelo apoio prestado.
À minha amiga de curso Amanda Gretter Frias, pela amizade e apoio.
Aos colegas, Bruno De Marchi, David Spadotti, Gerson Suzuki, Júlio Marubayashi, Letícia
Moraes, Milena Leite, Mônica Fecury e Taty Mituti.
E ao funcionário do Departamento de Proteção Vegetal, Paulinho.
A todos que contribuíram para realização deste trabalho, muito obrigada!
IV
SUMÁRIO
1.
RESUMO ...................................................................................................................1
2.
SUMMARY ...............................................................................................................3
3.
INTRODUÇÃO ..........................................................................................................5
4.
REVISÃO DE LITERATURA ...................................................................................8
4.1.
Importância econômica de pimentas e pimentões .................................................8
4.2.
Família Geminiviridae – Gênero Begomovirus ................................................... 10
4.3.
A importância dos begomovírus para o gênero Capsicum. .................................. 13
4.4. Bemisia tabaci: características biológicas, taxonômicas e transmissão de
begomovírus ................................................................................................................. 14
4.5.
5.
Efeito da resistência de Capsicum na dispersão de Begomovírus ........................ 18
MATERIAL E MÉTODOS....................................................................................... 20
5.1.
Coleta de amostras, detecção e variabilidade de begomovírus em Capsicum ......20
5.2.
Comportamentode
genótipos
de
Capsicum
spp.
ao
ToSRV...........................................................................................................................22
5.2.1. Obtenção do Inóculo de ToSRV e genótipos de Capsicum spp. .............................. 22
5.2.2 Inoculação, avaliação dos sintomas e da presença do ToSRV nos genótipos ............ 24
5.3. Avaliação de atratividade e preferência para oviposição de B. tabaci MEAM1 em
genótipos de Capsicum spp. .......................................................................................... 24
5.3.1. Teste com chance de escolha ................................................................................. 25
5.3.2. Teste sem chance de escolha.................................................................................. 25
5.4. Avaliação dos aspectos biológicos de Bemisa tabaci MEAM1 em genótipos de
Capsicum spp.................... ............................................................................................ 27
5.5. Dispersão primária e secundária do ToSRV em genótipos de Capsicum spp.
assintomáticos ao vírus ................................................................................................. 29
5.5.1. Dispersão Primária ............................................................................................. 30
5.5.2. Dispersão Secundária ......................................................................................... 31
6.
RESULTADOS E DISCUSSÃO ............................................................................... 32
V
6.1. Detecção e variabilidade de begomovírus em Capsicum ....................................... 32
6.2.
Comportamento de genótipos de Capsicum spp ao ToSRV ................................ 35
6.3. Atratividade e preferência para oviposição de B. tabaci MEAM1 em genótipos de
Capsicum spp. .............................................................................................................. 39
6.3.1.
Experimento com chance de escolha ........................................................... 39
6.3.2.
Experimento sem chance de escolha ........................................................... 43
6.4. Avaliação dos aspectos biológicos de B. tabaci MEAM1 em genótipos de
Capsicum spp................................................................................................................. 44
6.5. Dispersão primária e secundária do ToSRV em genótipos de Capsicum spp.
assintomáticos ao vírus ................................................................................................. 47
7.
CONCLUSÕES ........................................................................................................ 50
8.
REFERÊNCIAS BIBLIOGRÁFICAS ....................................................................... 51
VI
LISTA DE FIGURAS
Figura 1. Representação esquemática do genoma do Bean golden yellow mosaic virus
(BGYMV), espécie-tipo do gênero Begomovirus . Extraído de (GUTIERREZ, et al.(2004).
........................................................................................................................................ 11
Figura 2. Ensaios de atratividade e preferência de oviposição de Bemisia tabaci MEAM1
em genótipos de Capsicum spp. em gaiolas de vidro. ....................................................... 26
Figura 3. Genótipos de Capsicum sob iluminação tipo fluorescente “plant light” (Grolux F
20 W T12). ...................................................................................................................... 28
Figura 4. Representação esquemática do ciclo de vida de Bemisia tabaci (MEAM1), Aovo; B- 1ºínstar; C- 2º ínstar; D- 3º ínstar; E- 4º ínstar e F- adulto. ................................... 28
Figura 5. Detalhe do ensaio de dispersão primária ........................................................... 30
Figura 6. Detalhe do ensaio de dispersão secundária ....................................................... 31
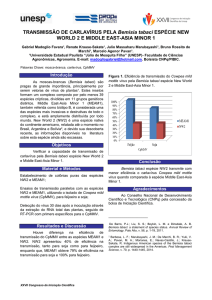
Figura 7. Análise filogenética de begomovírus provenientes de pimentão do Estado de
São Paulo e outros begomovírus do GenBank, baseado no alinhamento de nucleotídeos
referente à parte da região codificadora para a proteína capsidial. Valor de Bootstrap 2000,
Programa Mega Versão 5.2. Seqüências de begomovírus utilizadas: ToSRV (JX 415196) e
ToYVSV (EF459696). ..................................................................................................... 34
Figura 8. Expressão dos sintomas observados em genótipos de Capsicum spp. infectados
com Tomato severe rugose vírus, com base na escala diagramática descrita por Rocha et
al., 2012a . ....................................................................................................................... 36
VII
LISTA DE TABELAS
Tabela 1. Período, localidade e número de plantas de pimentão sintomáticas coletadas
nos Períodos de agosto de 2012 a janeiro de 2013. ........................................................... 21
Tabela 2. Relação de acessos de espécies de Capsicum spp pertencente ao Banco de
Germoplasma do Instituto Biológico de Campinas, IAC. .................................................. 23
Tabela 3. Levantamento dos vírus em plantas de pimentão coletadas em diferentes
municípios do Estado de São Paulo durante 2012/2013. ................................................... 33
Tabela 4. Resposta de acessos de Capsicum spp. inoculados por Bemisia tabaci com
Tomato severe rugose virus (ToSRV). ............................................................................. 37
Tabela 5. Média do número de adultos de Bemisia tabaci (MEAM1) presentes em
genótipos de Capsicum spp. em 24, 48 e 72h após liberação e média de oviposição em teste
com escolha. .................................................................................................................... 41
Tabela 6. Médias de adultos de Bemisia tabaci (MEAM 1) em diferentes genótipos de
Capsicum spp., 24 e 48h após liberação e média de ovos após 48h, em teste sem chance de
escolha ............................................................................................................................. 43
Tabela 7. Duração média (±EP) de período de incubação, instares ninfais e período ninfal
total de Bemisia tabaci (MEAM 1) em diferentes genótipos de Capsicum spp. ................. 44
Tabela 8. Médias de mortalidade ninfal (%) de Bemisia tabaci (MEAM 1) mantidos em
sete genótipos de Capsicum spp. ...................................................................................... 45
Tabela 9. Médias de período de desenvolvimento (ovo a adulto), viabilidade ninfal (%) e
número total de adultos emergidos de Bemisia tabaci (MEAM 1) em sete genótipos de
Capsicum spp. .................................................................................................................. 46
Tabela 10. Dispersão primária e secundária de ToSRV nos genótipos de Capsicum spp.
inoculados por B. tabaci MEAM1. ................................................................................... 48
1
1. RESUMO
A mosca branca Bemisia tabaci MEAM1, (Hem: Aleyrodidae) é
considerada uma das pragas mais ameaçadoras em todo o mundo, principalmente por sua
capacidade de transmitir vírus, em especial os begomovírus. Diante da importância desse
vírus e de seu vetor, o presente trabalho avaliou a ocorrência de begomovírus em áreas de
produção de pimentão. Do total de 83 amostras de pimentão analisadas somente 13
(15,66%) foram positivas para begomovírus, sendo encontradas as espécies já relatadas
para o estado de São Paulo: Tomato severe rugose virus (ToSRV) e Tomato yellow vein
streak virus (ToYVSV). Verificou-se também a presença de Cucumber mosaic virus
(CMV) e tospovírus nas plantas analisadas. O trabalho também teve como objetivo avaliar
a resposta de 36 genótipos de Capsicum à infecção pelo ToSRV, à atratividade e à
preferência para oviposição por moscas brancas em testes de livre escolha. Após esta
análise preliminar, foram selecionados os genótipos C. annuum (IAC-1551; IAC-1566;
IAC-1579), C. chinense (IAC-1545; IAC-1549) e C. frutescens (IAC-1544) (assintomático
ao vírus e não atrativo ao vetor) e C. baccatum (IAC-1357) (sintomático ao ToSRV e
atrativo ao vetor), para as etapas subsequentes. Os genótipos IAC-1566, IAC-1544 e IAC1357 também foram avaliados quanto à dispersão primária e secundária do ToSRV pela
mosca-branca. C. annuum (IAC-1551; IAC-1566; IAC-1579), C. chinense (IAC-1545;
IAC-1549) e C. frutescens (IAC-1544) mostraram-se assintomáticos ao isolado de ToSRV
avaliado durante 80 dias após inoculação e as médias de oviposição e atratividade variaram
de 0,33 a 2,66 ovos/genótipo e 0,25 a 3,50 adultos/genótipo respectivamente, em teste com
chance de escolha. No teste sem chance de escolha foi observada baixa atratividade e
oviposição
de adultos de
mosca-branca
nos genótipos
IAC-1544;
IAC-1551;
2
IAC-1579; IAC-1545 e IAC-1549 que diferiram estatisticamente da IAC-1357 cujo
período de desenvolvimento ninfal foi de 30,25 dias e a porcentagem de adultos de mosca
branca foi de 27,78%. O desenvolvimento completo de ovo a adulto também foi observado
em C. chinense (IAC-1545), porém com porcentagem de emergência de insetos de 4,45%.
Os demais genótipos não permitiram o desenvolvimento de adultos da mosca branca. Nos
ensaios de dispersão primaria e secundária não foi observada diferença no número de
plantas infectadas dos genótipos IAC 1357 e IAC-1566. Os resultados indicam que os
genótipos IAC-1544; IAC- 1551; IAC- 1579 e IAC- 1549 são promissores para programas
de melhoramento genético de Capsicum no Brasil, pois mostraram baixa atratividade e
oviposição, além de inibirem o desenvolvimento ninfal, podendo ser indicados em
programas de manejo contra begomovírus e mosca branca.
____________________________
Palavras-chave: mosca-branca, begomovírus, pimentas, dispersão.
3
2. SUMMARY
BEGOMOVIRUS OCCURRENCE IN PEPPER PLANTS IN SÃO PAULO
STATE AND BEHAVIOR TO Tomato severe rugose virus AND Bemisia tabaci
MEAM1 IN Capsicum spp. GENOTYPES. Botucatu, 2014.
p. Dissertação
(Mestrado em Agronomia/Proteção de Plantas) – Faculdade de Ciências
Agronômicas. Universidade Estadual Paulista.
Autor: Késsia De Fátima Cunha Pantoja
Orientador: Renate Krause-Sakate
Co-Orientador: Kelly Cristina Gonçales Rocha
The Whitefly Bemisia tabaci MEAM1 (Hem: Aleyrodidade) is
considered one of the most threatening pests worldwide, mainly because of its ability to
transmit viruses, especially begomoviruses. Given the importance of this virus and its
vector, the present study evaluated the of occurrence of begomoviruses in production areas
of peppers. Of the total of 83 samples analyzed only 13 (15,66%) were positive for
begomovirus, and the two species already reported for state of São Paulo Tomato severe
rugose virus (ToSRV) and Tomato yellow vein streak virus (ToYVSV) were detected on
the plants. Cucumber mosaic virus (CMV) and tospovirus were also detected on the plants
analyzed. We also evaluate 36 genotypes of Capsicum for ToSRV infection, for
attractiveness and oviposition preference by whiteflies released in choice experiments.
4
After this preliminary analysis, the genotypes C. annuum (IAC-1551, IAC-1566, IAC1579), C. chinense (IAC-1545, IAC-1549) and C. frutescens (IAC-1544) (assymptomatic
for ToSRV and less attractive for the whitefly) and C. baccatum (IAC-1357) (symptomatic
for ToSRV and more attractive for the vector) were selected for the subsequent. The
genotypes IAC-1566, IAC-1544 and IAC-1357 were also evaluated for the primary and
secondary dispersion of ToSRV by the whiteflies. C. annuum (IAC-1551, IAC-1566, IAC1579), C. chinense (IAC-1545, IAC-1549) and C. frutescens (IAC-1544) were
asymptomatic for ToSRV at 80 days after inoculation and the averages of attractiveness
and oviposition ranged from 0.33 to 2.66 eggs / genotype and 0.25 to 3.50 adults /
genotype, respectively, with whiteflies released in free choice test. In the no choice test,
low attractiveness and oviposition of adult whiteflies were observed for genotypes IAC1544, IAC-1551, IAC-1579, IAC-1545 and IAC-1549 which were statistically different
from IAC -1357. The nymphal development for genotype IAC-1357 was 30.25 days and
the percentage of whitefly adults was 27.78%. The complete development from egg to
adult was also observed in C. chinense (IAC-1545), but with insect emergence percentage
of 4.45%. For the other genotypes no adult emergence could be observed. The low
attractiveness and oviposition by whiteflies and also inhibit of adults observed in
genotypes IAC- 1544; IAC-1551; IAC- 1579 and IAC- 1549 made them interesting for
breeding programs of Capsicum in Brazil.
______________________
Keywords: whitefly, begomoviruses, peppers, dispersion.
5
3. INTRODUÇÃO
O gênero Capsicum, da família Solanaceae, apresenta importância
agrícola mundial e é largamente cultivada nas regiões temperadas e tropicais, não só
devido sua importância econômica como especiaria, mas também por seu valor nutricional,
ornamental e medicinal (POZZOBON et al., 2006). Este gênero é composto por 31
espécies, sendo cinco classificadas como domesticadas, que são: C. annuum L. (pimentão,
pimenta doce), C. chinense Jaqc. (pimenta-de-cheiro, pimenta-de-bode, murici), C.
frutescens L. (pimenta malagueta) e C. baccatum L. (dedo-de-moça, chapéu-de-frade),
grandemente consumidas e produzidas no Brasil, e a Capsicum pubescens L., não cultivada
neste país (LANNES et al., 2007). Destacam-se por terem boa adaptação às condições de
clima tropical e grande diversidade genética que é evidenciada, por exemplo, em seus
frutos e flores que apresentam variedades de tamanhos, formas e colorações
(HAVERROTH; NEGREIROS, 2011; ZENI ; BOSIO, 2011).
6
Atualmente o pimentão é produzido em todo o território brasileiro,
mas os maiores produtores são os estados de São Paulo e Minas Gerais, responsáveis por
uma área de aproximadamente 5.000 hectares e produção e 120.000 toneladas (RIBEIRO;
CRUZ, 2003). No mundo, segundo dados da FAO - Organização das Nações Unidas para a
agricultura, em 2011 a produção mundial foi de 29,6 milhões de toneladas e no Brasil a
produção é de 197 mil toneladas (CONAB, 2010). Seus frutos são comercializados
principalmente na coloração verde e vermelha, apesar de serem também produzidos frutos
de cor amarela, marfim, laranja e arroxeada (FILGUEIRA, 2003). A produção destina-se
para o consumo in natura e processamento de molhos, conservas e outras formas de
preparo de pimenta (CARVALHO et al., 2003).
Apesar dos avanços tecnológicos incorporados na produção,
doenças de origens bióticas e abióticas podem interferir na produção, com destaque para
àquelas causadas por vírus. As doenças de etiologia viral limitam consideravelmente a
produção de pimentas e pimentões. No Brasil já foram relatados vários gêneros de vírus
que infectam pimentões: Begomovirus, Tomato severe rugose virus (ToSRV) e a espécie
tentativa Tomato yellow vein streak virus (ToYVSV) (NOZAKI et al., 2006; NOZAKI et
al., 2010); Cucumovirus , Cucumber mosaic virus (CMV) (FRANGIONE et al., 2002);
Potyvirus, Potato virus Y(PVY) (COSTA; ALVES, 1950) Pepper yellow mosaic virus
(PepYMV) (INOUE-NAGATA et al,. 2002); Tobamovirus, Tobacco mosaic virus (TMV),
Pepper mild mottle virus (PMMoV) e Tomato mosaic virus (ToMV) LIMA et al., 2000);
Tospovirus Tomato spotted wilt virus (TSWV), Groundnut ringspot virus - GRSV) e
Tomato chlorotic spot virus (TCSV) (ÁVILA, et al., 2004).
Em pimentão, o primeiro relato de begomovírus ocorreu no
Submédio do Vale São Francisco, que compreende os estados da Bahia e Pernambuco
(LIMA et al., 1999; LIMA et al., 2001), e no Estado de São Paulo em 2005 (NOZAKI, et
7
al., 2006, NOZAKI, 2007). Neste último, o vírus foi caracterizado como Tomato severe
rugose virus (ToSRV). No Estado de Goiás o primeiro relato do ToSRV ocorreu em uma
cultivar de pimenta dedo-de-moça (Capsicum bacatum) (BEZERRA-AGASIE et al.,
2006). A transmissão e dispersão de begomovírus no campo ocorre pela ação das moscasbrancas, Bemisia tabaci, (Hemiptera: Aleyrodidae) (STANLEY et al., 2005).
Nos últimos anos, os problemas fitossanitários associados a insetos
do gênero Bemisia tornaram-se cada vez mais frequentes em tomateiros e pimentões
cultivados em todo o mundo. A mosca - branca B. tabaci é atualmente considerada uma
das principais pragas destrutivas do século 20 (JONES et al., 2008). As condições
climáticas da maior parte do território do Brasil permitem o cultivo de várias espécies de
plantas hospedeiras durante o ano todo, o que favorece à multiplicação e dispersão
contínua da mosca branca (FARIA et al., 2000). Uma das principais consequências do
aumento populacional desse inseto tem sido o aumento na incidência de vírus pertencentes
ao gênero Begomovirus e também Crinivirus (NAVAS-CASTILLO et al., 2011).
A utilização de cultivares resistente pode ser considerada a opção
mais eficaz, durável e estável dentro da estratégia de manejo integrado (ROCHA et al.,
2012b). Porém, no Brasil não há variedades comerciais de pimentão indicadas como
resistentes a begomovírus. Portanto, os objetivos do trabalho foram: avaliar reação de 36
genótipos de Capsicum spp. ToSRV, quanto a atratividade, oviposição e aspectos
biológicos de B. tabaci (MEAM1), a dispersão primária e secundária do ToSRV pela B.
tabaci espécie MEAM1, também conhecida como biótipo B, prevalente no Brasil.
8
4. REVISÃO DE LITERATURA
4.1.
Importância econômica de pimentas e pimentões
O pimentão pertence ao gênero Capsicum (Grego Kato – picar ou
arder), família Solanaceae, neste gênero encontram-se os pimentões, as pimentas doces e
pimentas picantes. A classificação do gênero é realizada com base nos níveis de
domesticação, podendo as espécies ser consideradas silvestres semi domesticadas e
domesticadas (BIANCHETTI; CARVALHO, 2005). Há grande variação na forma,
tamanho e coloração dos frutos em plantas pertencentes ao gênero Capsicum (BOSLAND;
VOTAVA, 1999).
As solanáceas apresentam distribuição mundial, exceto na
Antártida, sendo que a maior diversidade de espécies ocorre nas Américas do Sul e
Central. Capsicum é um gênero tipicamente americano, com a existência de apenas uma
espécie fora das Américas (BIANCHETTI et al., 1999).
O cultivo de pimentão ocorre praticamente em todas as regiões do
Brasil, sendo cultivados aproximadamente 13 mil ha, com produção de 290 mil toneladas
de frutos (MAROUELLI; SILVA, 2012). O Estado de São Paulo cultiva cerca de 23,70 %
dessa área, seguido pelos estados do RJ, MG, SC, PR, GO e CE. Apenas 4,70% de toda a
9
área produtora de pimentão no é feita sob cultivo protegido, localizando-se no estado de
São Paulo e no Distrito Federal (KOBORI et al., 2008).
Segundo Cruz e Banci (2008), as pimenteiras do gênero Capsicum
possuem um cultivo relativamente fácil, quando comparadas a outras solanáceas, como a
batata, tomate e mesmo o pimentão. Estes autores afirmam que é possível distinguir as
pimentas dos pimentões através de características morfológicas e pela pungência do fruto,
isto é, pelo sabor picante conferido por alcaloides denominados capsaicinóides. As plantas
de pimentão não possuem frutos pungentes e normalmente são grandes e largos, de
formato retangular, quadrado ou triangular. Diferentemente do pimentão, as pimentas
apresentam certa rusticidade no campo e um ciclo mais longo, com um período de colheita
que pode ser realizado por mais de um ano (CNPH, 2001). Mesmo cultivadas de maneira
rústica, dezenas de variedades de pimentas são produzidas no Brasil, ocasionando
movimentações financeiras de milhões ao ano, considerando-se o mercado interno e as
exportações (MATTOS et al., 2008).
Durante o desenvolvimento e produção, as culturas de pimentas e
pimentões são afetadas por doenças de origens bióticas e abióticas. O sucesso na produção
depende, em grande parte, de cuidados dispensados ao controle de doenças, insetos e
nematóides. O nível de produtividade e qualidade dos frutos será tanto melhor quanto
menor for à incidência desses problemas (PEIXOTO et al., 1999). Os problemas
fitossanitários associados a insetos do gênero Bemisia (Hemíptera: Aleyrodidae) tornaramse cada vez mais frequentes na cultura de pimentas e pimentões cultivados em todo o
mundo (NARANJO; ELLSWORTH, 2001), exigindo atenção dos produtores.
10
4.2.
Família Geminiviridae – Gênero Begomovirus
A família Geminiviridae é constituída por espécies de vírus
caracterizados estruturalmente pela morfologia geminada da partícula viral, com 18-30 nm
e geneticamente por possuir uma (monopartidos) ou duas (bipartidos) moléculas de DNA
circular de fita simples (ssDNA) encapsidado em partículas icosaédricas geminadas
(STANLEY et al., 2005). Cada uma das moléculas apresenta 2500-3000 nucleotídeos (nt)
encapsidada por uma única proteína estrutural (proteína capsidial) que se arranja na forma
de 22 capsômeros formando dois icosaedros incompletos que confere o aspecto geminado
das partículas virais, característico desta família de vírus deplantas (BROWN et al., 2011).
Segundo a classificação do Internacional Committee on Taxonomy
of Viruses (ICTV, 2012) a família Geminiviridae, é composta por 7 gêneros: Begomovirus,
Becurtovirus, Curtovirus, Eragrovirus, Mastrevirus, Topocuvirus e Turncurtovirus. Estes
gêneros são subdivididos com base no número de componentes do genoma, tipo de inseto
vetor, gama de hospedeiros e relacionamento filogenético. O gênero Begomovirus é
considerado o mais importante dentro da família, devido ao elevado número de espécies
que causam infecção em plantas. Estes vírus podem ser divididos em dois grandes grupos,
os que possuem genoma monopartido (DNA-A) e os que possuem genoma bipartido
(DNA-A e DNA-B). Neste gênero, encontram-se os vírus transmitidos por mosca branca
para dicotiledôneas, sendo o membro tipo o Bean golden yellow mosaic virus-BGYMV
(Figura 1) (GUTIERREZ, et al 2004; STANLEY et al., 2005).
11
Figura 1. Representação esquemática do genoma do Bean golden yellow mosaic virus (BGYMV), espécietipo do gênero Begomovirus. Extraído de (GUTIERREZ, et al.(2004).
A
maioria
das
espécies
de
begomovírus
apresenta
dois
componentes genômicos e ambos os componentes são essenciais para a infecção sistêmica
eficiente do vírus na planta (STANLEY et al., 2005). O DNA-A codifica todas as proteínas
necessárias para a transcrição, replicação e encapsidação de ambos os DNAs, enquanto o
DNA-B contribui com as funções necessárias para o movimento do vírus na planta e
desenvolvimento de sintomas (ROJAS et al., 2005). Assim, o componente DNA-A
codifica a CP (capa proteica ou AV1) no sentido viral e quatro proteínas no sentido
complementar: Rep (“replication associated protein” ou AC1), responsável pela replicação
de ambos os componentes (DNA A e DNA B); TrAP (“transcriptional activator protein”
ou AC2), REn (“replication enhancer protein” ou AC3) e AC4, proteína ainda com função
desconhecida. O DNA-B codifica duas proteínas responsáveis pelo movimento e pela
expressão de sintomas: a proteína NSP (“nuclear shuttle protein” ou BV1), no sentido
viral, e outra no sentido complementar, a MP (proteína de movimento ou BC1). Ambos os
componentes genômicos possuem tamanho parecido não compartilhando identidade de
sequência, exceto por uma região altamente conservada (>90% de identidade nucleotídica)
com aproximadamente 200 nucleotídeos, denominada de região comum (RC) (FONTES et
12
al., 1994; GUTIERREZ, 2000). A transcrição dos genes virais tanto no DNA-A com em
DNA-B, ocorre tanto no sentido viral (5‟ 3‟) como no sentido complementar (3‟ 5‟).
A replicação ocorre através de uma forma replicativa de DNA fita
dupla (dsDNA) utilizando o mecanismo ciclo rolante. A síntese de ssDNA viral é iniciada
quando a proteína Rep (“replication-associatedprotein”) cliva o DNA (A e B) na sequência
TAATATT↓AC (nonanucleotídeo conservado entre os membros da família) localizada em
uma estrutura em forma de “hairpin” dentro da região intergênica e auxilia na etapa de
síntese de sequencia. Os geminivírus não codificam uma DNA polimerase e,
consequentemente, são dependentes de fatores do hospedeiro para sua replicação (ROJAS
et al., 2005).
Espécies de begomovírus com genoma monopartido possuem os
genes necessários para desempenhar todas as funções essenciais do vírus, sejam aquelas
relacionadas à replicação ou ao movimento viral célula-a-célula e à longa distância e
diferem em número de ORFs em relação ao DNA-A dos bipartidos. Estes vírus, por
exemplo, ToLCV e ToYLCV, possuem duas ORFs (CP e AV2) no sentido viral, enquanto
os bipartidos apresentam apenas a CP ( PADIDAM et al., 1996). Em essência, o genoma
dos begomovírus monopartidos é homólogo ao DNA-A de bipartidos. Os genes nos
sentido complementar C1, C2 e C3 são homólogos dos AC1, AC2 e AC3, respectivamente
(STANLEY et al., 2005). De acordo com NAVAS-CASTILLO et al. (2011), um grande
número de begomovírus monopartidos demonstraram estar associados com os ssDNA
satélites conhecidos como beta-satelites. Estas moléculas são determinantes na
patogenicidade e são completamente dependentes de um vírus para a sua replicação,
encapsidação e transmissão.
Os Begomovirus, tradicionalmente eram divididos em dois grandes
grupos, os originados do Novo Mundo (Américas - Hemisfério Ocidental) que
13
correspondiam aos begomovírus bipartidos e os do Velho Mundo (Europa, Ásia e África –
Hemisfério Oriental), monopartidos. No Velho Mundo, predomina o complexo viral
denominado „Tomato yellow leaf curl disease‟ (TYLCD) (NAVAS-CASTILLO et al.,
2011). No entanto, esse panorama mudou com a introdução de espécies monopartidas no
continente americano em diversos países, infectando diferentes culturas em especial
plantas de tomateiro e pimentão (GLICK et al., 2009).
4.3.
A importância dos begomovírus para o gênero Capsicum.
O gênero Begomovirus há tempo vem sendo relatados em
pimentões e pimentas em diversas regiões do mundo. Até o momento, 15 espécies de
begomovírus foram encontradas em plantas do gênero Capsicum (FAUQUET et al., 2008)
e mais duas exclusivamente verificadas no Brasil, o ToSRV e o ToYVSV ( ROCHA et al.,
2010). No Brasil, relatos de infecção de plantas de pimentão por begomovírus ocorreram a
partir de 1999, no estado de Pernambuco (LIMA et al., 2001). Em 2003, a espécie Tomato
severe rugose virus (ToSRV) foi relatada em pimenta “dedo-de-moça” (Capsicum
baccatum var. pendulum), em Petrolina de Goiás (BEZERRA-AGASIE et al., 2006). Em
2005, além do ToSRV, foi verificada a espécie tentativa Tomato yellow vein streak virus
(ToYVSV) no Estado de São Paulo e em 2010, ToSRV foi relatado em Minas Gerais
(NOZAKI et al., 2006; NOZAKI et al., 2010). Outros trabalhos mostraram a
predominância da espécie ToSRV nos cultivos de pimentão e tomateiro no estado de São
Paulo (ROCHA et al., 2010).
Em outras regiões do mundo, várias espécies foram relatadas
infectando Capsicum spp. O Serrano golden mosaic virus (SGMV) é geminivírus
14
associado ao pimentão, encontrado no sul dos Estados Unidos e México (BROWN e
POULOS, 1990). No México destacam-se principalmente as espécies Pepper huasteco
virus, PHV, Pepper golden mosaic virus (PepGMV) e Pepper huasteco yellow vein virus
(PHYVV) (GARCÍA-NERIA; BUSTAMANTE, 2011). Roye et al. (1999) observaram, desde
1992, enrolamento e enfezamento com ou sem margens amarelas nas folhas de tomate e
pimentão do sul e parte central da Jamaica, e identificaram uma nova espécie de
begomovírus denominada Tomato dwarf leaf curl virus (TDLCV). Pepper leaf curl virus
(PepLCV), outra espécie em plantas de pimentão, foi encontrada e caracterizada em
Taiwan (SHIH et al., 2001). Infecção pelo TYLCV em C. annuum e C. chilense foi
relatada em diferentes partes do mundo, como no Sul da Espanha (REINA et al., 1999) e
Cuba (QUIÑONES et al., 2002). Fauquet et al. (2008) registraram a ocorrência de várias
espécies e espécies tentativas de begomovírus em Capsicum spp. em diversas regiões do
mundo.
4.4.
Bemisia tabaci: características biológicas, taxonômicas e transmissão de
begomovírus
As moscas brancas da espécie Bemisia tabaci estão classificadas na ordem
Hemiptera (Família: Aleyrodidae), são insetos que se alimentam da seiva do floema das
plantas, tanto na fase ninfal como na fase adulta ( LAZAROWITZ et al., 1992; VILLAS
BÔAS et al., 1997). São insetos diminutos, medindo de 1 a 2 mm, sendo as fêmeas maiores
que os machos (NATESHAN et al., 1996). Os adultos de mosca-branca têm o dorso de
coloração amarelo pálido e as asas brancas. Como suas asas cobrem quase todo o corpo, a
cor predominante é o branco, daí ser erroneamente denominada de mosca branca
15
(TOSCANO et al., 2002). Seu ciclo de vida compreende quatro fases (ovo, ninfa e adulto)
e sofre influência das condições climáticas e ambientais, principalmente temperatura,
umidade relativa do ar e planta hospedeira (GILL, 1990). As fêmeas podem ovipositar
de 130 a 300 ovos durante o ciclo, dependendo da planta hospedeira e da temperatura
(TOSCANO et al., 2002). A reprodução é sexuada ou por partenogênese arrenótoca, na
qual fêmeas não fecundadas resultam em ovos que darão machos estéreis e dependendo
das condições climáticas, há 11 a 15 gerações por ano (GILL, 1990).
A mosca-branca é encontrada principalmente nos trópicos e
subtrópicos, porém sua presença já foi descrita em todos continentes (BROWN, 2000). O
sucesso de dispersão está estritamente relacionado à expansão da monocultura da maioria
das espécies cultivadas, às condições dos sistemas agrícolas modernos, ao aumento da
utilização de agrotóxicos, selecionando populações resistentes e, principalmente, à grande
facilidade em se adaptar aos diversos hospedeiros ( BROWN et al., 1992).
Bemisia tabaci começou a ter destaque internacional como séria
praga em campo aberto e também em cultivo protegido a partir dos anos 70, devido às
infestações ocorridas no Sudão e, a seguir, na década de 80, nos EUA (DE BARRO et al.,
2011). Seus danos às plantas compreendem alterações nos processos fisiológicos,
reduzindo a transpiração e a fotossíntese. Também pode ocorrer perda de vigor com
consequente redução no desenvolvimento, em decorrência da alimentação de adultos e
ninfas (INBAR; GERLING, 2008; MCAUSLANE et al., 2004). Outros danos típicos são
desordens fisiológicas m função da alimentação do inseto, como o prateamento das folhas
em aboboreiras e o amadurecimento irregular dos frutos do tomateiro (BROWN et al.,
1995).
No entanto, a maior importância da moscas brancas se deve ao fato
de ser capaz de transmitir mais de 200 espécies de vírus, grande parte deles com
16
significativo impacto econômico na produção de hortaliças (NAVAS-CASTILLO et al.,
2011). Esses vírus são pertencentes a diferentes gêneros como os Begomovirus (família
Geminiviridae), Crinivirus (Closteroviridae), Carlavirus (Betaflexiviridae) e Ipomovirus
(Potyviridae). Os begomovírus e os crinivirus são considerados atualmente os mais
importantes limitadores da produção de tomate, além de sua incidência ter sido verificada
também em culturas como o pimentão e a batata (BARBOSA et al., 2008, FREITAS et al.,
2012).
As populações de B. tabaci apresentam alta variabilidade biológica
intra-específica e genética, porém são morfologicamente idênticas, incapazes de serem
distinguidas tanto no estágio juvenil como no adulto (ROSELL et al., 1997; BROWN et
al., 2000; CALVERT et al., 2001).
Existiam aproximadamente 41 biótipos, sendo que apenas dois
destes (biótipo A e B) eram encontrados no Brasil (RABELLO et al., 2008). Estudos mais
recentes com B. tabaci demostraram que ela não é composta de biótipos. Em vez disso,
DINSDALE et al. (2010) e DE BARRO et al. (2011) baseados na análise do gene da
mitocôndria cytochroma oxidase I (mtCOI) propuseram que B. tabaci é constituída por um
complexo de diferentes espécies. Esta nova classificação leva em consideração os estudos
entre cruzamentos de indivíduos classificados em diferentes biótipos (XU et al., 2010;
ELBAZ et al., 2010; WANG et al., 2010; SUN et al., 2011) revelaram um isolamento
reprodutivo completo ou incompleto de acasalamento entre estas diferentes populações, o
último reduzindo a aptidão dos descendentes. Esta abordagem sugeriu que B. tabaci é um
complexo de espécies composto por pelo menos 24 espécies distintas. Recentemente, doze
novas espécies foram identificadas, quatro na China (HU et al. 2011) uma na Argentina,
denominada New World 2 (ALEMANDRI et al., 2012), uma na China, denominada Asia
IV; duas no Japão, Japan 1e 2; uma na Indonésia, Asia II 12; uma na Índia, Asia II 11; uma
17
em Uganda, SubSah Af 5 e uma em Camarões, denominada Africa, totalizando 36 espécies
distintas (FIRDAUS et al., 2013).
Um dos membros do complexo de espécies, a Middle East-Asia
Minor One (MEAM1) ou comumente referida na literatura como biótipo B é a mais
conhecida e de maior distribuição mundial. B. tabaci MEAM1 foi detectada no Brasil no
começo de 1990, provavelmente pelo comércio internacional de plantas ornamentais
(LOURENÇÃO; NAGAI, 1994). A partir do início da década de 1990, a incidência de
begomovírus em diversas culturas, principalmente tomateiro, aumentou vertiginosamente
(RIBEIRO et al., 2003) e esse aumento esteve diretamente relacionado à introdução desta
nova espécie de B. tabaci. Outro membro do complexo de espécies de B. tabaci, New
World 1, também referida como biótipo A, foi coletado pela primeira vez nos EUA em
batata-doce. O biótipo A tornou-se um problema sério em algodão e cucurbitáceas no
sudoeste dos EUA e no México por volta de 1981 (BROWN, 2000). Recentemente, uma
amostragem ampla de espécimes de B. tabaci foi realizada no Estado de São Paulo e
verificou-se a predominância da espécie MEAM1 em plantas cultivadas (ROCHA et al.,
2011; MARUBAYASHI et al., 2012). A modalidade de transmissão de begomovírus por
moscas brancas é do tipo circulativa não propagativa (BROWN, 1997; MORIN et
al.,1999). O vírus circula na hemolinfa, mas não replica no vetor, envolvendo a passagem
de partículas virais do intestino para a hemolinfa do inseto, da hemolinfa para as
glândulas salivares e destas para outras plantas (HULL, 2004). O período latente dos
begomovírus está em torno de 6 a 16 horas até o início da transmissão (SANTOS et al.,
2003).
18
4.5.
Efeito da resistência de Capsicum na dispersão de Begomovírus
A transmissão e dispersão de begomovírus em cultivos de pimentas
e pimentões ocorre pela ação da mosca branca alimentando-se em fontes de vírus de áreas
próximas, podendo ser de cultivos antigos como também de plantas alternativas no campo.
A utilização de cultivares resistente pode ser considerada a opção mais eficaz, durável e
estável dentro da estratégia de manejo integrado de viroses em hortaliças. Trabalhos têm
sido realizados na busca para encontrar genes de resistência em plantas silvestres do
gênero Capsicum (ANAYA-LÓPEZ et al 2003; GODÍNEZ-HERNÁNDEZ et al 2001;
HERNÁNDEZ-VERDUGO et al. 2001; GARCÍA-NERIA; BUSTAMANTE, 2011;
ROCHA et al., 2012b).
No México, foi identificado um acesso de C. chinense como
resistente aos begomovírus PepGMV e PHYVV (ANAYA-LÓPEZ et al. 2003, GARCÍANERIA e BUSTAMANTE, 2011) e plantas selvagens de C. annuum resistentes ao PHV
(HERNÁNDEZ-VERDUGO et al., 2001). C. annuum Catarino Cascabel utilizado
comercialmente no México (RODRIGUES et al., 2011) e C. annuum Silver utilizado como
porta-enxerto no Brasil são resistentes a Phytophthora capsici e nematóides (Meloidogyne
javanica, M. incognita races 1, 2, 3 e 4) (OLIVEIRA et al., 2009) e mostraram-se
assintomáticos ao ToSRV (ROCHA et al., 2012b).
Outra estratégia se baseia na resistência natural de plantas à insetos
vetores de vírus, podendo ser esta resistência proporcionada por barreiras físicas e/ou
químicas presentes em caules e folhas de plantas (SMITH, 2005). De acordo com
Rodríguez-López et al. (2011), a presença de barreiras físicas como os tricomas
glandulares que secretam substâncias químicas como acylaçucares mostraram efeito
negativo para a infestação de B. tabaci e redução na incidência do begomovírus
19
monopartido Tomato yellow leaf curl virus na Espanha. No Brasil, Matos et al. 2009,
mostraram redução na população de ácaro branco em pimentas e pimentões, atribuídos a
presença de tricomas, os quais impediram a ação desta praga.
20
5. MATERIAL E MÉTODOS
5.1.
Coleta de amostras, detecção e variabilidade de begomovírus em Capsicum
Plantas de pimentão com sintomas de vírus foram coletadas nas
regiões de Lins, Reginópolis, Pirajuí, Piedade, Vitoriana, e Elias Fausto, estado de São
Paulo (Tabela 1). As folhas foram acondicionadas em sacos plásticos, dentro de caixas de
isopor e levadas ao laboratório de virologia da FCA/ UNESP, Botucatu para análise
molecular. No total foram coletas 83 amostras de tecidos foliares de pimentão durante o
período de 2012/2103. O critério para a escolha e coleta das plantas nas áreas de cultivos
foi a presença de sintomas de amarelecimento, distorção foliar e mosaico e histórico de
infestação de mosca branca.
21
Tabela 1. Período, localidade e número de plantas de pimentão sintomáticas coletadas
nos Períodos de agosto de 2012 a janeiro de 2013.
Coletas
1
2
3
4
5
6
7
8
9
10
11
Períodos de coletas
Agosto/2012
Agosto/2012
Agosto/2012
Agosto/2012
Agosto/2012
Agosto/2012
Outubro/2012
Outubro/2012
Janeiro/2013
Janeiro/2013
Janeiro/2013
Localidade
Nº de plantas coletadas
Lins /Aberto
Lins /Aberto
Lins /Aberto
Lins /Aberto
Pirajuí / Estufa
Pirajuí / Estufa
Pirajuí / Estufa
Reginópolis / Estufa
Piedade / Aberto
Vitoriana / Estufa
Elias Fausto
7
3
3
16
14
2
4
10
11
10
3
83
Total
A extração de DNA genômico total das folhas de pimentão foi
realizada segundo o método descrito por Dellaporta et al. (1983). O DNA total extraído de
cada amostra foi submetido à reação de amplificação por círculo rolante (RCA) (INOUENAGATA et al, 2004) utilizando-se do kit Templi Phi (Amersham Biosciences) seguindo
as instruções do fabricante. O produto final do RCA foi submetido à reação “Polymerase
Chain Reaction” (PCR) utilizando-se os oligonucleotídeos iniciadores “universais”
PALIv1978/PAR1c496, que amplificam um fragmento com aproximadamente 1100bp do
DNA-A dos begomovírus correspondente à parte da ORF (Open Reading Frame) AC1
(Rep), à região comum e parte da ORF AV1 (CP) (ROJAS et al, 1993).
Treze amostras de DNA total positivas para begomovírus foram reamplificadas por PCR com os pares de oligonucleotídeos V324/C889 (BROWN
et
al,2001) e enviadas para sequenciamento. As sequências obtidas foram comparadas entre si
e com outras sequências de begomovírus depositadas no GenBank, utilizando-se os
programas Blast n (http://www.ncbi.nlm.nih.gov/blast) e Clustal W (TOMPSON et al.,
1994). A análise filogenética foi realizada com o programa MEGA versão 5.2 (TAMURA
et al., 2011), utilizando o método de “Neighbor-Joining”, com valor de “bootstrap” 2000.
Todas as amostras foram analisadas para a presença de Cucumber
mosaic virus, potyvírus e tospovírus. O RNA total das plantas foi extraído pelo método de
Bertheau et al. (1998), e o produto submetido à reação RT-PCR com oligonucleotídeos
22
universais para CMV, potyvírus e tospovírus (035-3/038-8, BOARI et al, 2000 ,
WCIEN/PV1 MOTA et al., 2004 e BR60/BR65, EIRAS et al., 2001), respectivamente. O
produto foi analisado em gel de agarose 1%.
5.2. Comportamento de genótipos de Capsicum spp. ao ToSRV
5.2.1. Obtenção do Inóculo de ToSRV e genótipos de Capsicum spp.
O isolado de ToSRV, proveniente de plantas de tomateiro
infectadas, foi cedido pela Empresa Sakata Seed Sudamerica. Trinta e seis genótipos de
Capsicum spp. foram fornecidos pelo Instituto Agronômico de Campinas/IAC, e são
provenientes do banco de germoplasma do centro de pesquisa (Tabela 2). A semeadura dos
genótipos foi realizada em bandejas de poliestireno expandido com 220 células contendo
substrato comercial.
23
Tabela 2. Relação de acessos de espécies de Capsicum spp pertencente ao Banco de
Germoplasma do Instituto Biológico de Campinas, IAC.
No de
ordem
Acesso
Nome comum
Nome científico
Observações
1
IAC-1259 Pimenta 1259
Capsicum baccatum
cruzamento natural
2
IAC-1280 Tipo Habañero
C. chinense
cruzamento natural
3
4
IAC-1309 Serra do Japi
IAC-1349 Dedo-de-moça
? (provável espécie silvestre) cruzamento natural
C. baccatum
cruzamento natural
5
IAC-1351 Coração de galinha
C. chinense ?
cruzamento natural
6
7
IAC-1352 Dedo-de-moça
IAC-1353 Amarela doce
C. baccatum
C. annuum
cruzamento natural
cruzamento natural
8
9
IAC-1357 Gigante segregante
IAC-1360 Murupi segregante
C. baccatum
C. chinense
cruzamento natural
cruzamento natural
10
IAC-1366 Aji amarelo
C. baccatum
cruzamento natural
11
12
13
14
IAC-1367
IAC-1526
IAC-1532
IAC-1544
C. frutescens
C. chinense
C. chinense ?
C. frutescens
cruzamento natural
autofecundada
autofecundada
autofecundada
15
16
IAC-1550 Jalapeño
IAC-1551 Guajillo
C. annuum
C. annuum
autofecundada
autofecundada
17
18
19
20
IAC-1566
IAC-1579
IAC-1588
IAC-1589
Vermelha doce
Pimenta doce
Pimenta doce
PI 159236
C. annuum (a confirmar)
C. annuum (a confirmar)
C. annuum (a confirmar)
C. chinense
autofecundada
autofecundada
autofecundada
autofecundada
21
22
23
24
IAC-1590
IAC-1643
IAC-1644
IAC-1646
Panca
Biquinho doce
Fidalga (tipo habañero)
Scoth Bonnet (tipo habañero)
C. chinense
C. chinense
C. chinense
C. chinense
autofecundada
cruzamento natural
cruzamento natural
cruzamento natural
25
IAC-1647 Pimenta-de-cheiro
C. chinense
cruzamento natural
26
27
IAC-1533 Peruana
IAC-1535 Malagueta
C. pubescens
C. frutescens
autofecundada
autofecundada
28
IAC-1545 Murici
C. chinense
autofecundada
29
30
IAC-1547 Hortivale-1
IAC-1549 Fidalga (tipo habañero)
?
C. chinense
autofecundada
autofecundada
31
IAC-1552 Murupi original
C. chinense
autofecundada
32
33
34
35
IAC-1573
IAC-1580
IAC-1587
IAC-1592
C. chinense
?
?
?
autofecundada
autofecundada
autofecundada
autofecundada
36
IAC-1594 Cocota
?
autofecundada
Tabasco
PI 152225
Ornamental
Piripiri
Cumari-do-pará
Olho de peixe
Laranja doce
Hortivale doce
24
5.2.2 Inoculação, avaliação dos sintomas e da presença do ToSRV nos
genótipos
Todas as etapas do experimento de análise de resistência a ToSRV
em diferentes genótipos de Capsicum foram realizadas no campo experimental Sakata
Seed Sudamérica, em Bragança Paulista, SP.
A inoculação das plantas foi realizada aos 30 dias após a
semeadura. As bandejas contendo as mudas foram dispostas em uma sala de criação de
moscas-brancas virulíferas, mantidas diretamente na fonte de inóculo com o ToSRV,
utilizando-se em média 50 insetos por planta sadia.
O período de acesso de inoculação (PAI) foi de sete dias. Após este
período, as mudas foram pulverizadas com inseticidas (IMIDACLOPRID 600 FS +
BUPROFEZIN 150g após o PAI) para eliminar todos os adultos, ninfas e ovos da mosca branca. Dez mudas de cada genótipo foram transplantadas em vasos plásticos de 5 litros, e
mantidas em estufa com sistema de fertirrigação por gotejamento, por 80 dias.
A presença e a expressão de sintomas foram avaliados
semanalmente. A análise da infecção pelo vírus foi realizada aos 30 e 60 dias após
inoculação pelas técnicas RCA-PCR. O DNA total de cada planta por genótipo foi extraído
utilizando-se o método de Doyle e Doyle (1987) seguido de RCA-PCR utilizando-se os
oligonucleotídeos descritos por Rojas et al.(1993). O produto final da reação foi verificado
em gel de agarose 1%, corado com SYBR® Safe DNA (Invitrogen).
5.3. Avaliação de atratividade e preferência para oviposição de B. tabaci MEAM1
em genótipos de Capsicum spp.
Adultos de B. tabaci previamente identificados como pertencentes
ao biótipo B, ou espécie MEAM1, (Marubayashi et al., 2012) foram mantidos em estufa
contendo plantas de couve (Brassica oleracea L. var. acephala) e soja (Glycine max).
25
5.3.1.
Teste com chance de escolha
No experimento com chance de escolha, 36 genótipos de Capsicum
(5.2.1.) foram semeados em bandejas de poliestireno expandido com 220 células contendo
substrato comercial (Plantmax®). Após 30 dias da emergência, quatro plantas de cada
genótipo foram transferidas para vasos plásticos de 1L com solo esterilizado e adubado.
Quarenta dias após a emergência (DAE), estas plantas (uma de cada genótipo) foram
acondicionadas no interior de gaiolas metálicas de 2,5 x 3,0 x 2,5 m, com teto revestido
por plástico e sombrite (30%) e as laterais revestidas por telado anti-afídeo e distribuídas
aleatoriamente em um círculo no chão. Os vasos contendo as plantas ficaram espaçados em
cerca de 25 cm, a fim de evitar o contato entre as mesmas. Cada gaiola foi considerada um
bloco, seguindo um delineamento de blocos casualizados (DBC) e efetuando-se quatro
repetições para cada grupo. As gaiolas foram infestadas com cerca de 3600 adultos da
mosca-branca (aproximadamente 100 casais por genótipo).
A atratividade foi avaliada com 24, 48 e 72 horas após a liberação
dos insetos, contando-se, com o auxílio de um espelho, o número de adultos presentes na
parte
abaxial dos folíolos. Cada avaliação foi composta pela média de três folhas
marcadas. Após a última avaliação, o trifólio de cada planta foi retirado e levado ao
laboratório, onde com o auxílio de um microscópio estereoscópico (aumento de 40
x), foi contado o número de ovos presentes na face abaxial.
5.3.2. Teste sem chance de escolha
Os genótipos Capsicum frutescens (IAC-1544); C. annuum (IAC1551, IAC-1566 e 1579) e C. chinense (IAC-1545 e IAC-1549) apresentaram menor
atratividade à mosca branca no teste com chance de escolha, e também foram
assintomáticos ao ToSRV, sendo portanto selecionados para o teste sem chance de escolha.
Foi utilizado o genótipo C. baccatum (IAC-1357) como padrão de susceptibilidade, pois
este foi altamente atrativo à mosca branca, e suscetível ao ToSRV .
O experimento sem chance de escolha foi realizado em arenas de
vidro (25cm x 25cm x 7cm) (Figura 2). Seis folíolos totalmente desenvolvidos e de cada
genótipo foram destacados e dispostos em círculo no interior das arenas. Através de um
26
orifício superior central da arena foram liberados 15 casais de mosca branca sem distinção
do sexo. Cada arena representou uma repetição em delineamento inteiramente casualizado,
efetuando-se 10 por genótipo. As gaiolas foram mantidas em casa-de-vegetação sob
condições controladas (T= 25±2º C, U.R.= 60±10% ). O número de moscas-brancas
presentes em cada folíolo foi contado 12, 24 e 48 h após a liberação. Após 48 h os ovos
presentes na parte abaxial foram contados sob microscópio estereoscópico (aumento de 40
x), segundo o método descrito em Rodriguez-Lopes et al. (2011).
Foi calculada a média de mosca branca e do número de ovos por folíolo
através da análise de variância (ANOVA), quando significativa as médias foram
comparadas pelo teste de Tukey, a 5% para ambos os experimentos com e sem chance de
escolha.
Figura 2. Ensaios de atratividade e preferência de oviposição de Bemisia tabaci MEAM1
em genótipos de Capsicum spp. em gaiolas de vidro.
27
5.4. Avaliação dos aspectos biológicos de Bemisa tabaci MEAM1 em genótipos de
Capsicum spp.
O ensaio foi realizado no Laboratório de Resistência de
Plantas a Insetos e Plantas Inseticidas (LARESPI) do Departamento de Proteção Vegetal,
FCA/ UNESP, Botucatu, SP. Neste foi avaliado o desenvolvimento de ovo a adulto B.
tabaci MEAM1, nos mesmos genótipos testados em (5.3.2.).
A semeadura foi feita em bandejas e 30 dias após emergência
(DAE), as mudas foram transplantadas para copos plásticos (500 ml) contendo substrato
comercial (Plantmax®). Quando as plantas apresentavam-se com quatro folhas
verdadeiras, estas foram infestadas com adultos do inseto no interior de sala de criação de
moscas-brancas sob condições controladas ( T= 25±2º C, U.R.= 60±10% ) por 24 horas.
Após esse período, os insetos adultos foram removidos e as plantas conduzidas a uma sala
climatizada (T= 26±2º C, U.R.= 60±10% e fotofase de 12 horas), onde sob o auxílio de um
microscópio estereoscópico (aumento de 40 x), foram deixados 30 ovos (com coloração e
formato normais) na face abaxial de cada folíolo. Os ovos excedentes foram retirados com
auxílio de hastes flexíveis de algodão. Foram utilizados três folíolos por genótipo, sendo
que cada folíolo continha 30 ovos e representou uma repetição, totalizando 3 por genótipo
(90 indivíduos), em delineamento inteiramente casualizado (BALDIN; BENEDUZZI,
2010).
As plantas permaneceram sob a iluminação de lâmpadas dos tipos
fluorescente “super luz do dia” (20 w) e fluorescente “plant light” (Grolux F 20 W T12)
(Figura 3), visando melhorar o desenvolvimento das mesmas em laboratório e evitar
possível estiolamento.
28
Figura 3. Genótipos de Capsicum sob iluminação tipo fluorescente “plant light” (Grolux F
20 W T12).
As avaliações em cada genótipo foram realizadas diariamente e
sempre no mesmo horário, até o final do ciclo do inseto (Figura 4) em cada genótipo.
Foram avaliados os seguintes parâmetros biológicos do inseto: média de período de
incubação dos ovos, duração e viabilidade dos estágios ninfais, duração total da fase
jovem, mortalidade por ínstar e total da fase jovem (BALDIN; BENEDUZZI, 2010).
A
B
C
D
E
Figura 4. Representação esquemática do ciclo de vida de Bemisia tabaci
(MEAM1), A- ovo; B- 1ºínstar; C- 2º ínstar; D- 3º ínstar; E- 4º ínstar e F- adulto.
F
29
5.5. Dispersão primária e secundária do ToSRV em genótipos de Capsicum spp.
assintomáticos ao vírus
Três genótipos com diferenças quanto à suscetibilidade ao ToSRV
e atratividade para B. tabaci foram selecionados para o teste de dispersão dispersão: IAC1357 (sintomático e atrativo à mosca branca); IAC-1544 e IAC-1566 (assintomáticos e
pouco atrativos).
Para os ensaios, tanto de dispersão primária (dispersão de vírus
após a introdução de moscas virulíferas) quanto de dispersão secundária (dispersão de
vírus a partir de plantas infectadas para plantas sadias), foram utilizadas 20 plantas de cada
genótipo, cultivadas em vasos plásticos contendo substrato comercial. As plantas foram
dispostas em círculo e avaliadas em gaiolas metálicas individualizadas (revestidas com tela
anti-afídica, gaiolas com armação de ferro, cobertas com tecido “voil” com dimensões de
3x3x2 m). Para a transmissão do ToSRV foram utilizados adultos de B. tabaci. Para o
desenvolvimento do experimento da dispersão primária e secundária, utilizou-se o método
de Rodriguéz-Lópes et al. (2011) com algumas modificações. Foram realizados
experimentos de dispersão primária e secundária independentes entre os genótipos (IAC1357 com IAC1566) e (IAC-1357 com IAC-1544).
30
5.5.1.
Dispersão Primária
Para analisar o efeito dos genótipos sintomáticos e assintomáticos
de Capcium spp. na dispersão primária foram utilizadas adultos de moscas-brancas
previamentes submetidos a um período de acesso de aquisição (PAA) de 24 horas em
ramos de plantas de tomate (cultivar „Santa Clara) infectada por ToSRV (confirmada por
RCA-PCR). Após este período, em média 30 adultos/planta foram sugados com auxílio de
um aspirador bucal e posteriormente liberados ao centro das 20 plantas de cada genótipo
no interior da gaiola (Figura 5). A dispersão primária de ToSRV foi estudada após a
permanência por 48h (período de acesso de inoculação PAI) das moscas brancas junto aos
genótipos. Após o período de transmissão, todas as plantas foram tratadas com inseticida e
transferidas para outra casa-de-vegetação livre de mosca branca e analisadas para a
presença de sintomas e do vírus aos 30 e 60 dias após inoculação pelas técnicas RCA-PCR.
Figura 5. Detalhe do ensaio de dispersão primária
31
5.5.2. Dispersão Secundária
O experimento de dispersão secundária foi realizado nas mesmas
gaiolas anti-afídicas. Visando à desinfestação das possíveis moscas- brancas presentes, foi
pulverizado, as quais permaneceram sem plantas por 24 horas. No experimento foram
utilizadas plantas sadias e infectadas (20 dias antes de sua utilização; e confirmadas por
RCA-PCR) para cada genótipo.
Para a análise da dispersão secundária do ToSRV, 20 plantas de
cada genótipo novamente foram dispostas em círculo e ao centro foram colocadas três
plantas infectadas de cada um dos genótipos dispostas em forma de triângulo. Ao centro do
triangulo foram liberados 30 insetos de B. tabaci MEAM1 avirulíferas/planta (Figura 6).
Após 48 horas todas as plantas foram pulverizadas com inseticida específico para B. tabaci
MEAM1 e as plantas transferidas para gaiolas com tela anti-afídica, à prova de insetos. A
presença do vírus foi analisada por RCA-PCR aos 30 e 60 dias após inoculação .
Figura 6. Detalhe do ensaio de dispersão secundária
32
6. RESULTADOS E DISCUSSÃO
6.1. Detecção e variabilidade de begomovírus em Capsicum
Do total de 83 amostras de pimentão analisadas, 13 foram positivas
para a infecção por begomovírus (Tabela 3), o que representou apenas 15,66%. Estes dados
mostraram que a ocorrência da doença foi menor do que constatado nos levantamentos
realizados por Lima et al. (2001) no Nordeste brasileiro onde foi observada incidência de
43,8 % de infecções por begomovírus em pimentão e Rocha et al., (2010) que durante o
período de 2007 a 2009 verificou incidência de 46,90% de plantas de pimentão infectadas
por begomovírus no Estado de São Paulo.
Além da infecção por begomovírus verificou-se nas amostras a
presença de plantas de pimentão infectadas com CMV e tospovirus no município de Lins
tanto em campo aberto quanto em estufa. Nos municípios de Pirajuí, Reginópolis e Elias
Fausto foram verificados a presença de plantas infectadas por begomovírus e tospovírus,
porém não em infecção mista. Não foi verificada infecção por potyvírus nas amostras das
regiões analisadas (Tabela 3).
33
Tabela 3. Levantamento dos vírus em plantas de pimentão coletadas em diferentes municípios do Estado de São Paulo durante 2012/2013.
Propriedades/Cultivo
1 Lins /Aberto
2 Lins / Aberto
3 Lins / Aberto
4 Lins / Estufa
5 Pirajuí / Estufa
6 Pirajuí / Estufa
7 Pirajuí / Estufa
8 Reginópolis / Estufa
9 Piedade / Aberto
10 Vitoriana / Estufa
11 Elias Fausto
Total
Begomovirus
Total de
amostras
analisadas
Nº de amostras
positivas para
begomovírus
ToSRV
ToYVSV
7
3
3
16
14
2
4
10
11
10
3
83
2
0
2
2
0
0
2
3
0
0
2
13 (15,66%)
1
0
2
1
0
0
2
3
0
0
1
10
1
0
0
1
0
0
0
0
0
0
1
3
CMV
Potyvirus
Tospovirus
1
1
1
3
0
0
0
0
0
0
0
6 (7,23%)
0
0
0
0
0
0
0
0
0
0
0
0
1
1
2
1
1
0
0
1
0
0
1
8 (9,64%)
34
A análise da variabilidade foi realizada para 13 amostras positivas
para presença de begomovírus. Entre os isolados de ToSRV, a identidade de nucleotídeos
para o fragmento de 1100 nucleotídeos dos isolados de ToSRV mostrou variação de 97% a
99% com sequências de ToSRV (JX 415196.1) e entre os isolados de ToYVSV, 97% a
99% com o isolado ToYVSV (EF 459696.1). Os resultados mostraram predominância do
isolado ToSRV, pois este foi encontrado em 10 amostras, enquanto que o isolado ToYVSV
em apenas 3 amostras. A árvore filogenética (Figura 7) ilustra a separação dos dois ramos
filogenéticos para as duas espécies.
50P- Pirajuí
52P- Pirajuí
53P- Reginópolis
19P-Lins
ToSRV-JX415196
54P - Reginópolis
60P-Reginópolis
445P Elias Fausto
12P- Lins
7P- Lins
13P- Lins
500P- Elias Fausto
ToYVSV - EF459696
6P- Lins
17P- Lins
0.02
Figura 7. Análise filogenética de begomovírus provenientes de pimentão do Estado de
São Paulo e outros begomovírus do GenBank, baseado no alinhamento de nucleotídeos
referente à parte da região codificadora para a proteína capsidial. Valor de Bootstrap 2000,
Programa Mega Versão 5.2. Seqüências de begomovírus utilizadas: ToSRV (JX 415196) e
ToYVSV (EF459696).
35
6.2. Comportamento de genótipos de Capsicum spp ao ToSRV
Dos 36 genótipos avaliados, 23 desenvolveram sintomas de
infecção causadas pelo vírus ToSRV. A análise da presença do vírus mostrou que todas as
plantas inoculadas foram positivas para presença do mesmo. A expressão dos sintomas
variou desde suaves até mais severos. A intensidade dos sintomas nas plantas inoculadas
foi realizada com avaliação da severidade da doença, por meio de escala de notas (ROCHA
et al., 2012a). Foi empregada uma escala variando de 1 a 5, em que 1=ausência de
sintomas, 2=ligeira descoloração dos folíolos, 3=descoloração com início de enrugamento
dos folíolos, 4=descoloração e enrugamento dos folíolos e 5=clorose severa e enrugamento
acentuado dos folíolos no terço superior da planta (Figura 8).
Seis
genótipos
avaliados,
IAC-1309
(espécie
selvagem
desconhecida), IAC-1349 e IAC-1366 (Capsicum baccatum), IAC-1351 e IAC-1532
(Capsicum chinense) e IAC-1547 (Capsicum sp. espécie desconhecida) desenvolveram
sintomas mais severos comparados aos demais, com nota média de 4,00 na escala
diagramática atribuída para plantas de pimentão, Catarina Cascabel e Silver foram
previamente identificados como assintomáticos para infecção por ToSRV (Rocha et al.,
2012).
Os genótipos IAC-1589 (C. chinense) e IAC-1533 (C. pubescens)
apresentaram inicialmente níveis moderados a fortes de sintomas aos 20 dias após a
inoculação.
No
entanto,
folhas
jovens
subsequentes
tornaram-se
praticamente
assintomáticas. Segundo Chellappan et al. (2004), a recuperação do hospedeiro contra
infecção viral tem sido relatada em alguns sistemas de interação planta e vírus, incluindo a
interação com geminivírus. Carrillo-Tripp et al. (2007) demonstraram remissão de
sintomas em plantas de pimentão infectadas por PepGMV com 15 dias após inoculação.
36
1
2
3
4
5
Figura 8. Expressão dos sintomas observados em genótipos de Capsicum spp. infectados
com Tomato severe rugose vírus, com base na escala diagramática descrita por Rocha et
al., 2012a .
Para treze genótipos das espécies C. chinense (IAC-1280, IAC1644, IAC-1646, IAC-1545, IAC-1549), C. frutescens (IAC-1367, IAC-1544), C. annuum
(IAC-1551, IAC-1566, IAC-1579, IAC-1588) e Capsicum sp. (IAC-1587), as plantas
permaneceram assintomáticas em todo o período avaliado (81 d.a.i.) apesar do DNA viral
ter sido detectado aos 30 e 60 d.a.i (Tabela 4). Provavelmente as plantas assintomáticas
mostram algum tipo de resistência ao isolado ToSRV não avaliado, como por exemplo
resistência na movimentação do vírus na planta. Ou algum mecanismo de silenciamento
dos genótipos contra o vírus.
Morilla et al. (2005) encontraram plantas assintomáticas de C. annuum
infectadas por dois isolados de TYLCV (TYLCV-Mld and TYLCV-Alm). Plantas de C.
chinense também foram assintomáticas para a presença de Pepper golden mosaic virus
(PepGMV) e Pepper huasteco yellow vein virus (PHYVV) (ANAYA-LÓPEZ et al. 2003,
GARCÍA-NERIA; BUSTAMANTE, 2011).
37
Tabela 4. Resposta de acessos de Capsicum spp. inoculados por Bemisia tabaci com Tomato severe rugose virus (ToSRV).
N°
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
Acesso
IAC-1259
IAC-1280
IAC-1309
IAC-1349
IAC-1351
IAC-1352
IAC-1353
IAC-1357
IAC-1360
IAC-1366
IAC-1367
IAC-1526
IAC-1532
IAC-1533
IAC-1535
IAC-1544
IAC-1545
IAC-1547
IAC-1549
IAC-1550
IAC-1551
IAC-1552
IAC-1566
IAC-1573
IAC-1579
IAC-1580
IAC-1587
Espécie
Capsicum baccatum
Capsicum chinense
Wild species
Capsicum baccatum
Capsicum chinense
Capsicum baccatum
Capsicum annuum
Capsicum baccatum
Capsicum chinense
Capsicum baccatum
Capsicum frutescens
Capsicum chinense
Capsicum chinense
Capsicum pubescens
Capsicum frutescens
Capsicum frutescens
Capsicum chinense
Capsicum sp.
Capsicum chinense
Capsicum annuum
Capsicum annuum
Capsicum chinense
Capsicum annuum
Capsicum chinense
Capsicum annuum
Capsicum sp.
Capsicum sp.
RCA/PCR
30D. A.I.
9/10
9/10
4/10
7/10
9/10
9/10
10/10
10/10
10/10
10/10
8/10
6/10
9/10
1/10
6/10
8/10
4/10
6/10
2/10
9/10
8/10
2/10
8/10
2/10
6/10
5/10
2/10
60D. A.I.
8/10
8/10
10/10
5/10
10/10
9/10
4/10
4/10
8/10
10/10
9/10
6/10
8/10
7/10
7/10
5/10
5/10
7/10
2/10
3/10
3/10
2/10
5/10
2/10
4/9
5/10
2/10
Plantas sintomáticas
30 D.A.I.
60 D.A60 D.AI.
3/10
3/10
0/10
0/10
9/10
9/10
6/10
6/10
6/10
6/10
5/10
5/10
3/10
3/10
7/10
7/10
3/10
3/10
9/10
9/10
1/10
0/10 (1 Remissão)
2/10
2/10
7/10
7/10
2/10
1/10 (1 Remissão)
7/10
7/10
0/10
0/10
0/10
0/10
7/10
7/10
0/10
0/10
3/10
3/10
0/10
0/10
2/10
2/10
0/10
0/10
2/10
2/10
0/10
0/9
1/10
1/10
0/10
0/10
Escala
diagramatica
2,0
1,0
4,0
4,0
4,0
2,6
2,7
2,6
2,0
4,0
1,0
3,3
4,0
3,0
2,0
1,0
1,0
3,9
1,0
3,3
1,0
2,5
1,0
3,0
1,0
4,0
1,0
38
Tabela 4. (Continuação)
28
29
30
31
32
33
34
35
36
IAC-1588
IAC-1589
IAC-1590
IAC-1592
IAC-1594
IAC-1643
IAC-1644
IAC-1646
IAC-1647
Capsicum annuum
Capsicum chinense
Capsicum chinense
Capsicum sp.
Capsicum sp.
Capsicum chinense
Capsicum chinense
Capsicum chinense
Capsicum chinense
2/10
2/10
2/10
2/10
7/10
1/10
0/10
0/10
0/10
4/10
5/9
2/10
2/10
7/10
2/10
6/10
4/10
4/10
0/10
5/9
5/10
2/10
1/10
2/10
0/10
0/10
2/10
Legenda: RCA/PCR: Amplificação de círculo rolante/ Reação em cadeia polymerase.
D.A.I: dias após inoculação
0/10
1/9 (4 Remissões)
5/10
2/10
1/10
2/10
0/10
0/10
2/10
1,0
2,0
2,8
3,0
4,0
3,5
1,0
1,0
1,0
39
6.3. Atratividade e preferência para oviposição de B. tabaci MEAM1 em genótipos
de Capsicum spp.
6.3.1.
Experimento com chance de escolha
Os resultados dos ensaios de atratividade e preferência para
oviposição mostraram diferença significativa entre os acessos de Capsicum spp. avaliados às
48h e 72h após a liberação de adultos nas gaiolas. A menor média de adultos foi encontrada
com 72h após infestação, nos genótipos IAC-1526, IAC-1535 e IAC-1544, com 0,17; 0,33 e
0,33 adultos por genótipo, respectivamente (Tabela 5). A escolha da mosca branca por um
hospedeiro mais favorável para oviposição não ocorre somente para sua alimentação, mas
também pela capacidade da sobrevivência dos descendentes (NOMIKOU et al., 2003). A
variação do número de insetos por planta entre o menos e o mais atrativo foi de 0,33 e 12,58
indivíduos, para os genótipos IAC-1544 e IAC-1357, respectivamente (Tabela 5). A diferença
de atratividade para moscas brancas em plantas hospedeiras pode indicar mecanismos de
resistência
relacionados
a
fatores
de
natureza
morfológica
e/ou
químicas
(CHERMENSKAYA et al. 2009).
A análise de preferência para oviposição de mosca branca mostrou
diferença significativa entre os genótipos. O número médio de ovos de B. tabaci variou de
0,33 a 152,83 ovos/genótipo. As menores médias de adultos e ovos depositados nas folhas
após 72h foram observados em 9 genótipos: C. chinense (IAC-1526, IAC-1545 e IAC1549), C. pubescens (IAC-1533), C. frutescens (IAC-1535 e IAC-1544) e C. annuum
(IAC-1551, IAC-1566 e IAC-1579) (Tabela 5). De acordo com Firdaus et al. (2012), a
oviposição é um elemento do ciclo de vida da mosca branca que é muito difícil de
controlar, com controle biológico e/ou inseticida, assim, reduzir a oviposição pode se
tornar uma estratégia de manejo de moscas brancas. A baixa preferência para oviposição
de B. tabaci MEAM1, pode ser considerada um mecanismo de resistência do tipo
antixenose, que envolve a morfologia e componentes voláteis produzidos pela planta
(BALLINA-GOMEZ et al., 2013).
Diferentes níveis de atratividade e não-preferência para oviposição
foram verificados nos genótipos analisados neste trabalho. Alguns materiais apresentaram
textura diferente nas folhas, assim como a presença de tricomas. Portanto, barreiras físicas,
arquitetura ou mesmo a intensidade de cor podem afetar a escolha do hospedeiro
40
(SIPPELL et al., 1987), assim como pubescência da folha (MCAUSLANE 1996),
espessura da cutícula (CHANNARAYAPPA et al., 1992) e metabólitos que atuam como
repelentes ou atrativos (CHERMENSKAYA et al., 2009).
41
Tabela 5. Média do número de adultos de Bemisia tabaci (MEAM1) presentes em genótipos de Capsicum spp. em 24, 48 e 72h após liberação
e média de oviposição em teste com escolha.
N°
Acesso
Média de adultos (n°)
Espécie
(24h)
(48h)
Média de ovos (72h)
(72h)
1
IAC-1259
Capsicum baccatum
7,87±3,94
8,25±2,84 abcd
5,00±2,20 ab
39,25±16,55 ab
2
IAC-1280
Capsicum chinense
7,41±3,68
5,41±2,68 abcd
3,50±0,48 ab
13,50±7,85 ab
3
IAC-1309
Wild species
9,08±3,88
13,50±7,51 abc
12,83±8,75 a
43,42±23,47 a
4
IAC-1349
Capsicum baccatum
5,83±3,58
6,75±4,15 abcd
7,16±4,21 ab
57,50±50,30 ab
5
IAC-1351
Capsicum chinense
4,08±0,98
3,66±±, 81 abcd
2,16±1,08 ab
26,08±23,77 ab
6
IAC-1352
Capsicum baccatum
2,75±0,88
1,75±0,37 abcd
1,00±0,49 ab
6,16±4,75 b
7
IAC-1353
Capsicum annuum
3,58±1,26
4,67±1,13 abcd
3,75±0,79 ab
4,58±2,70 b
8
IAC-1357
Capsicum baccatum
11,83±6,77
12,58±7,18 abcd
12,58±8,24 a
152,83±117,89 a
9
IAC-1360
Capsicum chinense
6,83±2,53
4,50±1,68 abcd
5,17±1,77 ab
14,91±4,33 ab
-
-
-
(*)
10
IAC-1366
Capsicum baccatum
-
11
IAC-1367
Capsicum frutescens
4,08±1,08
3,50±1,27 abcd
5,00±1,26 ab
18,42±8,37 ab
12
IAC-1526
Capsicum chinense
0,50±0,32
0,42±0,25 d
0,50±0,29 ab
0,17±0,10 b
13
IAC-1532
Capsicum chinense
2,91±1,16
1,58±0,48 abcd
0,92±0,08 ab
5,83±3,69 b
14
IAC-1533
Capsicum pubescens
1,91±1,19
0,67±0,56 cd
0,33±0,24 ab
1,16±0,62 b
15
IAC-1535
Capsicum frútices
0,58±0,39
0,17±0,10 d
0,25±0,16 b
0,33±2,34 b
16
IAC-1544
Capsicum frutescens
1,25±1,04
1,66±1,06 abcd
0,33±0,19 ab
0,33±0,19 b
17
IAC-1545
Capsicum chinense
5,00±1,57
2,50±0,29 abcd
1,50±0,44 ab
2,00±3,50 b
18
IAC-1547
Capsicum SP.
-
-
-
-
42
Tabela 5. (Continuação)
19
IAC-1549
Capsicum chinense
7,33±1,89
4,75±1,38 abcd
3,50±0,80 ab
2,00±3,83 b
20
IAC-1550
Capsicum annuum
3,50±1,44
2,00±0,41 abcd
1,58±0,34 ab
5,41±1,59 b
21
IAC-1551
Capsicum annuum
1,47±0,69
0,75±0,48 bcd
0,25±0,08 b
1,77±0,88 b
22
IAC-1552
Capsicum chinense
2,33±0,79
2,00±0,47 abcd
0,83±0,52 ab
4,00±6,61 b
23
IAC-1566
Capsicum annuum
2,16±0,91
1,08±0,34 abcd
1,00±0,24 ab
2,66±0,78 b
24
IAC-1573
Capsicum chinense
2,75±1,03
1,17±0,29 abcd
1,83±0,85 ab
3,33±2,23 b
25
IAC-1579
Capsicum annuum
2,58±0,46
2,83±1,07 abcd
2,67±1,05 ab
2,66±1,08 b
26
IAC-1580
Capsicum sp.
2,58±0,93
1,66±0,68 abcd
1,42±0,21 ab
6,33±7,86 b
27
IAC-1587
Capsicum sp.
13,00±8,56
15,08±8,59 ab
11,83±8,68 ab
41,33±9,10 ab
28
IAC-1588
Capsicum annuum
2,08±1,76
1,92±1,15 abcd
1,50±0,62 ab
22,0±16,17 ab
29
IAC-1589
Capsicum chinense
6,08±1,05
7,25±2,10 abcd
5,50±1,26 ab
16,00±9,65 ab
30
IAC-1590
Capsicum chinense
8,92±4,07
7,25±2,50 abcd
6,00±2,12 ab
10,00±4,23 ab
31
IAC-1592
Capsicum sp.
11,08±2,83
13,50±4,94 a
7,66±2,93 ab
15,66±10,97 ab
32
IAC-1594
Capsicum sp.
-
-
-
-
33
IAC-1643
Capsicum chinense
1,42±0,31
2,25±1,23 abcd
1,16±0,52 ab
2,33±1,19 b
34
IAC-1644
Capsicum chinense
2,75±0,94
2,41±1,12 abcd
3,00±1,47 ab
8,83±4,80 ab
35
IAC-1646
Capsicum chinense
-
-
-
-
36
IAC-1647
Capsicum chinense
5,25±2,63
3,25±1,44 abcd
1,50±0,29 AB
12,25±5,19 ab
(*)
Não avaliado. Média seguida de mesma letra na coluna não difere entre si pelo Teste de Tukey (P ≥ 0.05).
43
6.3.2.
Experimento sem chance de escolha
Com 12 h após liberação dos insetos adultos nas gaiolas não foi
observada diferença significativa entre os genótipos. Verificou-se baixa atratividade de
adultos de mosca branca nos genótipos IAC-1544; IAC-1545; IAC-1549; IAC-1579 nas
avaliações de 24 e 48h após liberação dos insetos e estes diferiram estatisticamente do
genótipo IAC-1566 (Tabela 6).
As maiores médias de ovos depositados nas folhas após o período de
48h foram observadas nos genótipos IAC-1357 e IAC-1566 (4,22 e 5,08 ovos/genótipo,
respectivamente), diferindo estatisticamente de IAC-1544 (0,62 ovos/genótipo), e de IAC
1545(1,30) menos ovipositados (Tabela 6). Ballina-Gómez et al. (2013) compararam
diferentes genótipos de C. annuum e encontraram menor oviposição de B. tabaci na cultivar
Maax (0.3 ovos/cm2) em comparação com Parado (2.0 ovos/cm2).
Tabela 6. Médias de adultos de Bemisia tabaci (MEAM 1) em diferentes genótipos de
Capsicum spp., 24 e 48h após liberação e média de ovos após 48h, em teste sem chance de
escolha
Nº de adultos (± EP)
Genótipos
IAC-1357
IAC-1544
IAC-1545
IAC-1549
IAC-1551
IAC-1566
IAC-1579
12h
0,48 ± 0,09 a
0,28 ± 0,17 a
0,47 ± 0,12 a
0,75 ± 0,03 a
0,67 ± 0,10 a
0,88 ± 0,11 a
0,85 ± 0,19 a
24h
0,70 ± 0,12 abc
0,45 ± 0,05 bc
0,44 ± 0,06 c
0,49 ± 0,08 bc
0,75 ± 0,19 ab
0,94 ± 0,07 a
0,60 ± 0,07 bc
48h
0,57 ± 0,13 ab
0,33 ± 0,07 b
0,25 ± 0,11 b
0,45 ± 0,09 b
0,80 ± 0,19 a
0,80 ± 0,10 a
0,37 ± 0,05 b
Nº de ovos( ±
EP)
48h
4,22 ± 0,97 ab
0,62 ± 0,13 d
1,30 ± 0,28 dc
2,82 ± 0,51 bc
2,77 ± 0,59 bc
5,08 ± 0,51 a
1,42 ± 0,30 dc
44
6.4. Avaliação dos aspectos biológicos de B. tabaci MEAM1 em genótipos de
Capsicum spp.
O período médio de incubação dos ovos de B. tabaci nos diferentes
genótipos de Capsicum spp. variou de 7 a 7,7 dias (Tabela 7). A viabilidade desses ovos
foi de 100%, e não houve diferença entre os genótipos avaliados. Uma vez que os adultos
de B. tabaci MEAM1 utilizados na oviposição foram criados em plantas de couve e
transferidos para as plantas dos diferentes genótipos de Capsicum spp, este resultado
evidencia que o período de incubação e a viabilidade dos ovos de B. tabaci, não
dependeram do genótipo utilizado, e sim da planta hospedeira de criação. Ballina-Gómez
et al. (2013) mostrou diferença significativa na viabilidade dos ovos de B. tabaci, porém o
período de incubação não diferiu para os diferentes genótipos de Capsicum testados. O
período de incubação de ovos de B. tabaci sobre folhas de diferentes variedades de
abobrinhas variou entre 6,2 e 7,7 dias (BALDIN; BENEDUZZI, 2010).
A duração média dos estádios ninfais de B. tabaci MEAM1 variou
para cada genótipo estudado. No primeiro ínstar a duração média foi de 5,97 dias a 7,49 dias,
para os genótipos IAC-1551 e IAC-1549; respectivamente. No segundo e terceiro instares, o
período de desenvolvimento foi menor e variou de 3,13 a 2,09 dias e 7,13 a 6,69 dias, nos
genótipos IAC-1545 e IAC-1357, respectivamente (Tabela 7).
Tabela 7. Duração média (±EP) de período de incubação, instares ninfais e período ninfal
total de Bemisia tabaci (MEAM 1) em diferentes genótipos de Capsicum spp.
Incubação
1o instar
2o ínstar
3o instar
4o ínstar
IAC-1357
7,00±0,00
7,22±0,01
7,13±0,12
6,69±0,23
2,21±0,04
Período
ninfal
(dias)
23,25±0,04
IAC-1544
7,00±0,00
6,00±0,00
4,33±0,05
-
-
-
IAC-1545
7,00±0,00
7,11±0,01
3,13±0,05
2,09±0,27
0,67±0,00
14,33±0,10
IAC-1549
7,02±0,00
7,49±0,04
4,84±0,09
4,50±0,34
-
-
IAC-1551
7,70±0,01
5,97±0,03
5,24±0,49
3,00±0,00
-
-
IAC-1566
7,12±0,01
6,70±0,01
6,10±0,11
2,18±0,07
1,11±0,15
-
IAC-1579
7,00±0,00
6,32±0,02
5,16±0,13
3,87±0,11
1,11±0,47
-
Média (dias)
Genótipos
45
As ninfas que se desenvolveram sobre o hospedeiro IAC-1544
chegaram até o estágio N2 e morreram antes de completar o estágio N3. Nos genótipos
IAC-1549; IAC-1551; IAC-1566 as ninfas morreram na fase N4. Desta forma, pôde-se
concluir que os genótipos IAC-1544; IAC-1549; IAC-1551; IAC-1566 apresentaram efeito
negativo no desenvolvimento ninfal de B. tabaci, pois não possibilitou o desenvolvimento
completo de ovo a adulto dos insetos que estavam nestes genótipos. A emergência de
adultos de mosca branca foi observada somente nos genótipos sintomático e IAC-1545.
Ballina-Gómez et al. (2013) demonstrou que a porcentagem de sobrevivência ninfal foi
drasticamente afetada e variou em alguns genótipos testados (36,2 a 95,1%). Resultados
semelhantes foram obtidos para diferença na sobrevivência ninfal de B. tabaci em
diferentes acessos de tomateiros, L. pennelliie L. hirsutum (MUIGAI et al., 2003;
FANCELLI et al., 2003).
A mortalidade ocorreu com mais evidência durante o 4o ínstar de
desenvolvimento ninfal nas hospedeiras IAC-1549; IAC-1551; IAC-1566 e IAC-1579
(Tabela 8). Em apenas dois genótipos foi possível verificar o ciclo completo de B. tabaci
MEAM1 com emergências de 25 e 4 adultos de mosca - branca dos genótipos IAC-1357 e
IAC-1545, e representou viabilidade ninfal de 27,78% e 4,45%, respectivamente (Tabela
9).
Tabela 8. Médias de mortalidade ninfal (%) de Bemisia tabaci (MEAM 1) mantidos em
sete genótipos de Capsicum spp.
Genótipos
IAC-1357
IAC-1544
IAC-1545
IAC-1549
IAC-1551
IAC-1566
IAC-1579
Incubação
0,00
0,00
0,00
0,00
0,00
0,00
0,00
Mortalidade %
1o ínstar 2o ínstar 3o ínstar
4,44
11,77
55,81
0,00
0,00
100,00
0,00
0,00
87,78
2,22
21,75
90,00
16,67
82,22
87,50
4,44
2,26
57,03
0,00
23,33
81,84
4o ínstar
22,73
63,64
100,00
100,00
100,00
100,00
Viabilidade
ninfal (%)
27,78
4,45
-
46
Tabela 9. Médias de período de desenvolvimento (ovo a adulto), viabilidade ninfal (%) e
número total de adultos emergidos de Bemisia tabaci (MEAM 1) em sete genótipos de
Capsicum spp.
Fases de desenvolvimento
Genótipos
IAC-1357
IAC-1544
IAC-1545
IAC-1549
IAC-1551
IAC-1566
IAC-1579
Ovo – adulto
Ovo – 2º instar
Ovo – adulto
Ovo – 3º instar
Ovo – 3º instar
Ovo – 4º instar
Ovo – 4º instar
Período de
duração
(ovo-adulto)
30,25
17,33
21,33
23,85
21,91
23,85
25,86
Viabilidade
Ninfal (%)
Nº de
adultos/genótipo
27,78
4,45
-
25
4
-
A repelência de uma determinada planta a um inseto pode ocorrer
devido à volatilização de substâncias químicas provenientes das folhas, que afetam
negativamente a preferência
do inseto, afastando-o, e também
por fatores físicos,
relacionados às cores das folhas, que também podem afetar a seleção hospedeira, tanto
para alimentação quanto para oviposição (LARA, 1991; VENDRAMIM; GUZZO,
2009). Em pimentão esse fatores ainda são investigados, porém como base nas observações
feitas neste trabalho é possível que substâncias químicas estejam envolvidas na expressão
de não-preferência de alguns genótipos contra a mosca-branca. A repelência de um
material sobre um inseto é de importância fundamental, visto que ao impedir que o inseto
chegue até a planta, evita que o mesmo se alimente do genótipo e oviposite
(MARTINEZ, 2002).
As características físicas das superfícies foliares, como pilosidade,
presença de tricomas, cerosidade, espessura, dureza e textura da epiderme são fatores que
podem afetar a preferência do inseto em relação a uma planta, tanto para alimentação
quanto para oviposição. A importância dos tricomas como fonte de resistência contra a
mosca-branca B. tabaci já foi relatada por diversos autores (LAMBERT et al., 1995;
FANCELLI et al., 2005; BALDIN et al., 2005).
47
Os resultados indicam que os genótipos acima citados são
promissores para programas de melhoramento genético de Capsicum no Brasil, pois
mostraram baixa atratividade e oviposição, além de não possibilitar o desenvolvimento
ninfal, podendo ser indicados em programas de manejo contra begomovírus e moscabranca.
6.5. Dispersão primária e secundária do ToSRV em genótipos de Capsicum spp.
assintomáticos ao vírus
No experimento de dispersão primária de ToSRV, detectou-se uma
porcentagem maior (45 %) de plantas infectadas no genótipo assintomático IAC-1566, do
que no IAC-1357 (30%) com 30 dias (D.A.I.). Já no experimento de dispersão primária de
ToSRV para IAC-1357 e IAC-1544, o genótipo IAC-1357, mostrou maior número de
plantas infectadas que o genótipo assintomático IAC-1544, correspondendo a 12 (60%) e 6
(30%) plantas infectadas por genótipo, respectivamente. Na análise de 60 (D.A.I.) foram
detectadas menos plantas infectadas para todos os genótipos avaliados. Na dispersão
secundária, foi observada uma redução na frequência de plantas infectadas para os
genótipos assintomáticos aos 30 (D.A.I.) e aos 60 D.A.I., não houve diferença entre o
genótipo IAC-1357 e os assintomáticos IAC-1566 e IAC-1544 (Tabela 10). Resultados
semelhantes, de menor eficiência na transmissão após aquisição viral em fontes resistentes
de tomateiro, foi observado por Lapidot et al. (2001). Rodriguéz-Lopez et al. (2011)
também observaram redução na dispersão primária e secundária em plantas com
resistência a TYLCV.
Em síntese, comparando os resultados de dispersão primária e
secundária, pode-se inferir que a maior eficiência de transmissão e incidência de
begomovírus ocorre principalmente com a migração constante de vetores virulíferos de
fora para dentro da área plantada. Desta forma, o uso de genótipos com baixa atratividade e
preferência da mosca-branca pode resultar em menor dispersão do ToSRV por B. tabaci
MEAM1 dentro de um cultivo.
48
Tabela 10. Dispersão primária e secundária de ToSRV nos genótipos de Capsicum spp. inoculados por B. tabaci MEAM1.
Dispersão Primária
Indivíduos
IAC-1357
30
60
IAC-1566
IAC-1357
IAC-1566
30
30
30
IAC-1357
IAC-1544
30
60
30
60
30
30
1
+
+
2
+
+
+
+
+
3
+
+
+
+
+
4
+
+
+
5
+
+
+
6
+
+
7
+
+
8
+
9
+
60
2
+
+
5
+
6
+
+
7
8
+
60
+
+
+
+
+
+
9
Indivíduos
IAC-1544
+
4
+
60
10
10
11
11
+
12
13
+
14
+
15
+
Dispersão Secundária
Dispersão Primária
IAC-1357
1
3
Dispersão Secundária
12
15
+
+
+
+
+
+
13
+
60
+
+
+
+
60
+
+
49
Tabela 10. (Continuação)
16
16
17
+
18
17
+
19
20
N. pl infec/
+
6/20
1/20
+
+
9/20
6/20
+
18
+
19
20
3/20
0/20
3/20
0/20
N. pl aval
Porcentagem
de plantas
infectadas
N. pl infec/
+
+
+
+
12/20
9/20
4/20
1/20
3/20
0/20
3/20
60%
45% 30% 20%
5%
15%
0%
15%
6/20
N. pl aval
30%
5%
45%
30% 15%
0%
15%
0%
Porcentagem
de plantas
infectadas
50
7. CONCLUSÕES
ToSRV é a espécie de begomovírus predominante em
pimentão nas regiões produtoras do Estado de São Paulo;
O genótipo IAC-1357 - Capsicum baccatum (pimenta dedo
de moça) é altamente suscetível ao ToSRV e à mosca branca;
Desenvolvimento completo de ovo a adulto somente nos
genótipos IAC 1357 e IAC 1545;
Os genótipos Capsicum frutescens (IAC-1544); C. annuum
(IAC-1551, IAC-1566 e AC-1579) e C. chinense (IAC-1549) são assintomáticos ao
ToSRV, e expressam antixenose e antibiose sobre B. tabaci MEAM1;
dispersão primária.
Foi verificada maior eficiência de transmissão do ToSRV na
51
8. REFERÊNCIAS BIBLIOGRÁFICAS
ALEMANDRI, V. et al. Species within the Bemisia tabaci (Hemiptera: Aleyrodidae)
complex in soybean and bean crops in Argentina. Journal of Economic Entomology,
Lanham, v. 105, n.6, p. 48-53, 2003.
ANAYA-LÓPEZ, J. L. et al. Resistance to geminivirus mixed infections in Mexican wild
peppers. HortScience, Alexandria, v. 38, n. 2, p. 251-255, 2003
ÁVILA, A. C. et al. Ocorrência de viroses em tomate e pimentão na região serrana do
estado do Espírito Santo. Horticultura Brasileira, Brasília, DF, v. 22, n. 3, p. 655-658,
jul-set 2004.
BALDIN, E. L. L.; BENEDUZZI, R. A. Characterization of antibiosis and antixenosis
to the whitefly silverleaf Bemisia tabaci B biotype (Hemiptera: Aleyrodidae) in several
squash varieties. Journal of Pest Science, Heidelberg ,v. 83, n.3 , p. 223-229, 2010.
BALDIN, E. L. L.; VENDRAMIM, J. D.; LOURENÇÃO, A. L. Resistência de genótipos
de tomateiro à mosca-branca Bemisia tabaci (Gennadius) Biótipo B (Hemiptera:
Aleyrodidae). Neotropical Entomology, Londrina, v. 34, n. 3, p. 435-441, 2005
BALLINA-GOMEZ, H. et al. Resposta de Bemisia tabaci Genn. (Hemiptera: leyrodidae)
biótipo B de genótipos de pimenta Capsicum annuum (Solanales: Solanaceae).
Neotropical Entomology, Dordrecht, v. 42, n. 2, p. 205-210, 2013.
52
BARBOSA , L. R. et al. Eficiência de Chrysoperla externa (Hagen, 1861)(Neuroptera:
Chrysopidae) no controle de Myzus persicae (Sulzer, 1776) (Hemiptera: Aphididae) em
pimentão (Capsicum annum L.) Ciência. agrotecnologia., Lavras, v. 32, n. 4, p. 11131119, 2008.
BERTHEAU ,Y. et al. DNA amplification by polymerase chain reaction (PCR) In:
PEROMBELON, M. C. M.; WOLF J. M. van der. (Ed.). Methods for the Detection and
Quantification of Erwinia carotovora subsp. atroseptica on Potatoes. Scotland, Scottish
Crop Research Institute, 1998. p. 39-59. (Occasional Publication, 10).
BIANCHETTI, L. B.; CARVALHO, S. I. C. Subsídios à coleta de germoplasma de
espécies de pimentas e pimentões do gênero Capsicum (Solanáceas). In: WALTER, B. M.
T; CAVALCANTE, T. B. Fundamentos para coleta de germoplasma vegetal: teoria e
Prática. Brasília , DF: Embrapa Recursos Genéticos e Biotecnologia, 2005. p. 355-385.
BIANCHETTI, L. B. et al. Coleta de germoplasma de espécies silvestres de Capsicum no
sudeste brasileiro. In: II SIMPÓSIO DE RECURSOS GENÉTICOS PARA A AMÉRICA
LATINA E CARIBE, 2., Brasília. Anais... Brasília, DF: Embrapa-Cenargen, 1999. (CDROM).
BOARI, A. J. et al. Caracterização Biológica e Molecular de Isolados do “Cucumber
mosaic virus” Provenientes de Oito Espécies Vegetais. Fitopatologia Brasileira, Brasília,
v. 25, n. 1, p. 49-58, 2000.
BROWN, J.K.; POULOS, B.T. Serrano golden mosaic virus - a newly identified whitefly
transmitted geminivirus of pepper and tomato in the United States and Mexico. Plant
Disease, St. Paul ,v. 74, p. 720, 1990.
BROWN, J. K. et al. Family Geminiviridae. In: ANDREW, M. Q. K. et al (Ed.). Virus
Taxonomy: ninth report of the International Committee on Taxonomy of Viruses.
Elsevier, San Diego, p. 351-373, 2011.
BROWN, J. K. Molecular markers for the identification and global tracking of
whitefly vector-begomovirus complexes. Virus Research, Amsterdam , v. 71, n.1-2, p.
233-260, 2000.
53
BROWN, J. K.; FROHLICH, D. R.; ROSELL, R. C. The sweetpotato or silverleaf
whiteflies: biotypes of Bemisia tabaci or a species complex. Annual Review of
Entomology, Palo Alto, v. 40, p. 511-534, 1995.
BROWN, J. K.; BIRD, J. Whitefly-transmitted geminiviruses and associated disorders in
the Americas and the Caribbean Basin. Plant Disease, St. Paul ,v. 76, n. 3, p. 220-225,
1992.
CALVERT, L. A. et al. Analisa marcador DNA mitocondrial morfológica e de mosca
branca (Homoptera: Aleyrodidae) colonizadoras mandioca e feijão na Colômbia. Anais da
Sociedade Entomológica da América, v. 94, p. 512-519, 2001.
CARRILLO-TRIPP, J.; LOZOYA-GLORIA, E.; RIVERA-BUSTAMANTE, R. F.
Symptom remission and specific resistance of pepper plants after infection by Pepper
golden mosaic virus. Phytopathology, St. Paul, v. 97, n. 1, p. 51-59, 2007.
CARVALHO, S. I. C.; BIANCHETTI, L. B; HENZ, G. P. Germoplasm collection of
Capsicum spp. Maintained by Emprapa Hortaliças (CNPH). Capsicum and Eggplant
Newsletter, Turin, v. 22, p. 17-20, 2003.
CHELLAPPAN, P. et al. Short interfering RNA accumulation correlates with host
recovery in DNA virus-infected hosts, and gene silencing targets specific viral sequences.
Journal Virology, Washington, v. 78, p. 7465-7477, 2004.
CHERMENSKAYA, T. D.; PETROVA, M. O.; SAVELIEVA, E. I. Laboratory and field
evaluation of biological active substances of plant origin against greenhouse whitefly,
Trialeurodes vaporariorum Westw (Homoptera: Aleyrodidae). Archives Of
Phytopathology Plant Protection, Abingdon, v. 42, n. 9, p. 864-873, 2009.
CNPH. Projeto Capsicum. Brasília: Embrapa Hortaliças, 2001. Disponível em:
<http://www.cnph.embrapa.br/projetos/capsicum/index.html>. Acesso: 27 de nov. de 2013.
CONAB. Companhia Nacional do Abastecimento. Acompanhamento da safra brasileira
de grãos. Brasília: CONAB, 2010.
54
COSTA, A. S.; ALVES, S. Mosaico do pimentão. Bragantia, Campinas, v. 10, n. , p.9596, 1950.
CRUZ, D. M. R.; BANCI, C. A. Produção de mudas e plantio. In: RIBEIRO, C. S. C.
Pimentas – Capsicum. Brasíia, DF: Embrapa Hortaliças, 2008. p.73-79.
DE BARRO, P. J. et al. Bemisia tabaci: a statement of species status. Annual Review of
Entomology,
Palo
Alto
,v.
56,
,
p.
1-19,
2011.Disponível
em:
<http://www.annualreviews.org/doi/full/10.1146/annurev-ento-112408-085504>. Acesso
em: 14 nov. 2013.
DELLAPORTA, S. L.; WOOD, J.; HICKS, J. B. A plant DNA minipreparation: version
II. Plant Molecular Biology, Dordrecht, v. 1, n.4 , p. 19-21, 1983.
DINSDALE, A. et al. Refined global analysis of Bemisia tabaci (Hemiptera:
Sternorrhyncha: Aleyrodoidea: Aleyrodidae) Mitochondrial cytochrome oxidase 1 to
identify species level genetic boundaries. Annals of the Entomological Society of
America, Lanham , v. 103, p. 196-208, ANO.
DOYLE, J. J.; DOYLE J.L. A rapid DNA isolation procedure for small quantities of fresh
leaf tissue. Phytochemical Bulletin, St. Louis ,v. 19, p. 11-15, 1987.
EIRAS, M. et al. Caracterização molecular do Tomato chlorotic spot virus isolado de jiló
no Estado de São Paulo. Fitopatologia Brasileira 26:515. 2002 .
ELBAZ, M.; LAHAV, N.; MORIN, S. Evidence for pre-zygotic reproductive barrier
between the B and Q biotypes of Bemisia tabaci (Hemiptera: Aleyrodidae). Bulletin Of
Entomological Research , Cambridge, v. 100, n.5 , p. 581-590, 2010.
FANCELLI, M. et al. Exsudato glandular de genótipos de tomateiro e desenvolvimento de
Bemisia tabaci (Genn.) (Sternorrhyncha: Aleyrodidae) biótipo B. Neotropical
Entomology, Londrina, v. 34, p. 659-665, 2005.
FANCELLI, M. et al . Atratividade e preferência para oviposição de Bemisia
tabaci (Gennadius) (Hemiptera: Aleyrodidae) biótipo B em genótipos de tomateiro.
Neotropical Entomology, Londrina, 32: 319-328, 2003.
FAO. Global food losses and food waste. Disponível em PDF. Internacional Comgress
Save Food. Rome, 2011.
55
FARIA, J. C. et al . Situação atual das geminiviroses no Brasil. Fitopatologia Brasileira,
Brasilia, v. 25, n. 2, p. 125-137, 2000.
FAUQUET, C. M. et al. Geminivirus strain demarcation and nomenclature. Archives of
Virology, Vienna, v. 153, n. 4, p. 783-821, 2008.
FILGUEIRA, F. A. R. Novo manual de olericultura: agrotecnologia moderna na
produção e comercialização de hortaliças. Viçosa: UFV, 2003. 412 p.
FIRDAUS, S. et al. The Bemisia tabaci species complex: Additions from different parts of
the world. Insect Science, Richmond, v.20 , n. 6, p. 723-733, 2013
FONTES, E. P. B. et al. Geminivirus replication origins have a modular organization.
Plant Cell, Heidelberg, v. 6, n.3 , p. 405-416, 1994.
FRANGIONI, D. S. S.; PAVAN, M. A.; COLARICCIO, A. Triagem de genotipos de
pimentão para resistência ao Cucumber mosaic vírus (CMV) subgrupo I. Fitopatologia
Brasileira, Brasília, DF, v. 27, p 204, 2002.
FREITAS, D. M. S. Tomato severe rugose virus (ToSRV) e Tomato chlorosis virus
(ToCV): relações com a Bemisia tabaci biótipo B e eficiência de um inseticida no
controle da transmissão do ToSRV. 2012. 74 f. Tese (Doutorado em Fitopatologia)-Escola
Superior de Agricultura “Luiz de Queiroz”, Universidade de São Paulo, Piracicaba, 2012.
GARCÍA-NERIA, M. A.; BUSTAMANTE, R. F. R. Characterization of geminivirus
resistance in an accession of Capsicum chinense Jacq. Molecular Plant-Microbe
Interactions, St. Paul, v. 24, n. 2, p. 172-182, 2011.
GILL, R. J. The morphology of whiteflies. In: GERLING. D. (Ed.). Whiteflies: their
bionomicas pest status and management. Andaver: Intercept, p. 13-46, 1990.
GLICK, E.; LEVY, Y.; GAFNI, Y. The viral etiology of tomato yellow leaf curl disease –
a review. Plant Protection Science, Prague, v. 45, n. 3, p. 81-97, 2009.
GODÍNEZ-HERNÁNDEZ, Y. Characterization of resistance to Pepper huasteco
geminivirus in chili peppers from Yucatan, Mexico. Hort Science, Alexandria, v. 36, n.1 ,
139-142, 2001.
56
GUTIERREZ, C. et al. Geminivirus DNA replication and cell cycle interactions.
Veterinary Microbiology, Amsterdam, v. 98, n.2 , p. 111-119, 2004.
GUTIERREZ, C. Geminiviruses and the plant cell cycle. Plant Molecular Biology,
Dordrecht, v. 43, n. , p. 763-772, 2000.
HAVERROTH, M.; NEGREIROS, P. R. M. Calendário agrícola, agrobiodiversidade e
distribuição espacial de roçados Kulina (Madeja), Alto Rio Envira, Acre, Brasil.
Sitientibus série Ciências Biológicas,Brasil, v.11, n.2, p.299-308, 2011.
HERNÁNDEZ-VERDUGO, S. et al. Screening wild plants of Capsicum annuum for
resistance to Pepper huasteco virus (PHV): Presence of viral DNA and differentiation
among populations. Euphytica, Dordrecht, v. 122, n. 5-6, p. 31-36, 2001.
HU, J. et al. An extensive field survey combined with a phylogenetic analysis reveals rapid
and widespread invasion of two alien whiteflies in China. PLoS ONE, San Francisco , v.
6, n.1, 2011.
HULL, R. Matthews’ Plant Virology. California: Elsevier Academic Press, 1001 p.
2004.
INTERNATIONAL COMMITTEE ON TAXONOMY OF VIRUSES. Descriptions of
Bovine Leukemia Virus. Amsterdam, 2012 . Disponível em: <http://www.ictvdb.org>
Acesso em: 26 nov. 2013.
INBAR, M.; GERLING, D. Interações mediadas por plantas entre as moscas-brancas,
herbívoros e inimigos naturais. Annual Review Entomology, Palo Alto, v. 53, n. , p. 43148, 2008.
INOUE-NAGATA, A. K. et al. Pepper yellow mosaic virus, a new potyvirus in sweet
pepper, Capsicum annuum. Archives of Virology, Vienna, v. 147, n. , p. 849-855, 2002.
JONES, C. M. et al. High-throughput allelic discrimination of B and Q biotypes of the
whitefly, Bemisia tabaci, using TaqMan allele-selective PCR. Pest Management Science,
Chichester, v. 64, n. , p. 12-15, 2008.
KOBORI, R. F.; GIORIA, R.; BRUNELLI, K.R. Impacto potencial das mudanças
climáticas sobre as doenças do pimentão no Brasil. In: GHINI, R.; HAMADA, E.
57
Mudanças climáticas impactos sobre doenças de plantas no Brasil. Brasília: Embrapa
Informação Tecnológica, 2008. 331 p.
LAMBERT, A. L.; MCPHERSON, R. M.; ESPELIE, K. E. Soybean host plant resistance
mechanisms that alter abundance of whiteflies. (Homoptera: Aleyrodidae).
Environmental. Entomology, Laham, v. 24, p. 1381-1386, 1995.
LANNES, S.D. et al. Growth and quality of Brazilian accessions of Capsicum chinense
fruits. Scientia Horticulturae, Amsterdam, v. 112, p.266-270, 2007.
LAPIDOT, M. et al. Effect of host plant resistance to tomato yellow leaf curl virus
(TYLCV) on virus acquisition and transmission by its whitefly vector. Phytopathology,
St. Paul, v. 91, p. 1209-1213, 2001.
LARA, F. M. Princípios de resistência de plantas a insetos. 2. ed. São Paulo: Ícone,336
p. 1991
LAZAROWITZ, S. G. Geminiviruses: Genome structure and gene function. Critical
Reviews in Plant Sciences, Philadelphia, v. 11, n. 4, p. 327-349, 1992.
LIMA, M. F. et al. Distribuição de geminivírus nas culturas do tomate e pimentão em doze
municípios do Submédio do Vale São Francisco. Fitopatologia brasileira, Fortaleza, v.
26, n. 1, p. 81-85, 2001.
LIMA, M. F. et al. Levantamento e identificação das espécies de Tospovirus em tomateiro
e pimentão no Submédio do Vale do São Francisco e no Distrito Federal. Summa
Phytopathologica, Jaboticabal, v. 26, n. 2, p. 205-210, 2000.
LIMA, M. F. et al. Detection of sweet pepper whitefly-transmited geminivírus in the
“Submédio” of San Francisco Valley. In: Anais do 22º CONGRESSO PAULISTA DE
FITOPATOLOGIA, 1999. Jaboticabal: Editora, 1999. p. 106.
LOURENÇÃO, A. L.; NAGAI, H. Surtos populacionais de Bemisia tabaci no Estado de
São Paulo. Bragantia, Campinas, v. 53, n.1 , p. 53-59, 1994.
MARUBAYASHI, J. M. et al. At least two indigenous species of the Bemisia tabaci
complex are present in Brazil. Journal of Applied Entomology, Berlin, v. 137, n.1-2 , p.
113-121 , 2012.
58
MARTINEZ, S. S. O nim Azadirachta indica: natureza, usos múltiplos, produção.
Londrina: IAPAR, 2002. 142 p.
MATOS, C. H. C. et al. Os tricomas deCapsicum spp. interferem nos aspectos biológicos
do ácaro-branco Polyphagotarsonemus latus Banks (Acari: Tarsonemidae). Neotropical
Entomology, Dordrecht, v. 38, n. 5, p. 589-594, 2009.
MATTOS, L. M. et al Caracterização pós-colheita de espécies de Capsicumspp. Revista
em Agronegócios e Meio Ambiente, Maringa, v. 1, n. 2, p. 179-186, 2008.
MCAUSLANE, H. J. Influência da folha pubescência na preferência para oviposição
de Bemisia argentifolii (Homoptera: Aleyrodidae) em soja . Environmental Entomology,,
v. 25, p. 834-841, 1996.
MORILLA, G. et al. Pepper (Capsicum annuum) is a dead-end host for Tomato yellow
leaf curl virus. Phytopathology, St. Paul, v. 95, n. 9, p. 1089-1097, 2005.
MORIN, S. et al. Groel homologue from endosymbiotic bacteria of the whitefly
Bemisiatabaci is implicated in the circulative transmission of tomato yellow leaf
curl. Virology, Maryland Heights, v. 256, p. 75-84, 1999.
MOTA, L. D. C. et al. Pfaffia mosaic virus: a new potyvirus found infecting Pfaffia
glomerata in Brazil. Plant Pathology, Malden, v. 53, p. 368-373, 2004.
MUIGAI, S. G. et al. Greenhouse and field screening of wild Lycopersicon germplasm for
resistance to the whitefly Bemisia argentifolii. Phytoparasitica, Dordrecht, v. 31, n.1 , p.
27-38, 2003.
NARANJO, S. E.; ELLSWORTH, P. C. Desafios e oportunidades para manejo de pragas de
Bemisia tabaci no novo século. Protculturas, v. 20, n. Edição Especial, p. 707-869, 2001.
NATESHAN, H. M. et al. Host range, vector and serological relationships of cotton leaf
curl virus from southern India. Annual Applied Biology, Chichester, v. 128, n. , p. 233244, 1996.
NAVAS-CASTILLO, J.; FIALLO-OLIVE, E.; SANCHEZ-CAMPOS, S. Emerging virus
diseases transmitted by whiteflies. Annual Review of Phytopathology, Palo Alto p. 219248, 2011.
59
NOMIKOU, M., et al. Phytoseiid predators of whiteflies feed and reproduce on non-prey
food sources. Experimental e Applied Acarology, Dordrecht, v. 31, p. 15-26, 2003.
NOZAKI, D.N.; KRAUSE-SAKATE, R. ; PAVAN, M.A. Begomovírus infectando a
cultura de pimentão no Estado de São Paulo. Summa Phytopathologica, São Paulo, v.36,
n.3, p.244-247, 2010.
NOZAKI, D.N. et al. Occurrence of Begomovirus infecting pepper crops (Capsicum
annum) in Minas Gerais. In: ENCONTRO NATIONAL DE VIROLOGIA, 21., 2010,
Gramado. Anais... (ou Resumos...) Gramado: Virus Reviews & Research, Brasil,.p. 114114, 2010.
NOZAKI, D. N. Estudos biológicos e moleculares de begomovírus infectando
pimentão (Capsicum annuum) no estado de São Paulo. 2007. 94 f. Tese (Doutorado em
Agronomia/Proteção de Plantas)-Faculdade de Ciências Agronômicas, Universidade
Estadual Paulista, Botucatu, 2007.
NOZAKI, D. N. et al. First report of Tomato severe rugose virus infecting pepper plants in
Brazil. Fitopatologia Brasileira, Brasília, v. 31, p. 321, 2006.
OLIVEIRA, C. D. et al. Resistência de pimentas a nematóides de galha e compatibilidade
enxerto/porta-enxerto entre híbridos de pimentão e pimentas. Horticultura Brasileira,
Brasília, v. 27, p. 520-526, 2009.
PADIDAM, M.; BEACHY, R. N.; FAUQUET, C. M. The role of AV2 („precoat‟) and coat
protein in viral replication and movement in tomato leaf curl geminivirus. Virology,
Maryland Heights, v. 224, p. 390-404, 1996.
PEIXOTO, J. R. et al. Avaliação de genótipos de pimentão no período de inverno, em
Araguari, MG. Pesquisa Agropecuária Brasileira, Brasília, v. 34, n. 10, p. 1865-1869,
1999.
POZZOBON, M. T.; WITTMANN, M. T. A meiotic study of the wild and
semidomesticated Brazilian species of genus Capsicum L. (Solanaceae). Cytologia, Japão,
v.71, n. 3, p. 275-287, 2006.
QUIÑONES, M. et al. First report of Tomato yellow leaf curl virus infecting pepper plants
in Cuba. Plant Disease, St. Paul, v.86, p.73, 2002.
60
RABELLO, A. R. et al. Diversity analysis of Bemisia tabaci biotypes: RAPD, PCRRFLP and sequencing of the ITS1 rDNA region. Genetics and Molecular Biology,
Ribeirao Preto, v. 31, p. 585-590, 2008.
REINA, J. et al. First report of Capsicum annuum plants infected by tomato yellow leaf
curl virus. Plant Disease. St. Paul v.83, p.1176, 1999.
RIBEIRO, C. S. C.; CRUZ, D. M. R. Comércio de sementes de pimentão está em
expansão: apenas o mercado nacional movimenta US$ 1, 5 milhão. Revista Cultivar
Hortaliças e Frutas, Pelotas, n. 21, set. 2003.
ROCHA, K. C. G. et al. Avaliação de danos causados pelo Tomato severe rugose
virus (ToSRV) em cultivares de pimentão. Summa Phytopathologica, Botucatu, v. 38, ,
87-89. 2012a.
ROCHA, K. C. G. et al. Evaluation of resistance to Tomato severe rugose virus (ToSRV)
in Capsicum spp. genotypes. Tropical Plant Patholog, Brasília, v. 37, n. 5, p. 314-318,
2012b.
ROCHA, K. C. G. et al. Only the B biotype of Bemisia tabaci is present on vegetables in
São Paulo State, Brazil. Scientia Agricola, Piracicaba, v. 68, p. 120-123, jan. 2011.
ROCHA, K. C. G. et al.Ocorrência e variabilidade genética do Tomato severe rugose virus
em tomateiro e pimentão no Estado de São Paulo. Summa Phytopathologica, Botucatu,
v. 36, p. 222-227, 2010.
RODRÍGUEZ, H. B. The role of chili in human nutrition. In: TORRES, H. H. P. (Ed.).
Chili: a key feature of independence and the Revolution. Cidade do México D.F: Herdez
Foundation, 2011. p. 29-40.
RODRÍGUEZ-LÓPEZ, M. J. et al. Whitefly resistance traits derived from the wild tomato
Solanum pimpinelli folium affect the preference and feeding behavior of Bemisia tabaci
and reduce the spread of Tomato yellow leaf curl virus. Phytopathology, St. Paul, v. 101,
p. 1191-1201, 2011.
ROJAS, M. R. et al. Exploiting chinks in the plant's armor: Evolution and emergence of
geminiviruses. Annual Review of Phytopathology, Palo Alto, v. 43, p. 361-394, 2005.
61
ROJAS, M. R. et al. Use of degenerate oligonucleotídeos in the polymerase chain
reaction to detect whitefly-transmitted geminiviruses. Plant Disease, St. Paul, v. 77, n. ,
p. 340-347, 1993.
ROSELL, R. C. et al. Análise da variação morfológica em populações distintas de Bemisia
tabaci (Homoptera: Aleyrodidae). Anais da Sociedade Entomológica da América, v. 90,
p. 575-589, 1997.
ROYE, M.E. et al. Tomato dwarf leaf curl virus, a new bipartite geminivirus associated
with tomatoes and peppers in Jamaica and mixed infection with Tomato yellowf leaf curl
virus. Plant Pathology, Viçosa, v. 48, p. 370-378, 1999.
SANTOS, C. D. G.; ÁVILA, A.C.; RESENDE, R. O. Estudo da interação de um
begomovírus isolado de tomateiro com a mosca branca. Fitopatologia brasileira, Brasília,
v. 28, p. 664-673, 2003.
SIPPELL, D. W.; BINDRA, O. S.; KHALIFA, H. Resistance to whitefly (Bemisia tabaci)
in cotton (Gossypium hirsutum) in the Sudan. Crop Protection., Amsterdam, v. 6, p. 171178, 1987.
SHIH, S.L.; ROFF, M.M.N.; GREEN, S.K. Virology Unit, Asian Vegetable Research and
Development Center, P.O. Box 42, Shanhua, Tainan, Taiwan, Republic of China.(2001).
SMITH, C.M. Plant resistence to arthropods molecular and conventionae approaches.
Springer, The Netherlands, 2005.423p.
STANLEY, J. et al. Geminiviridae. In: FAUQUET, C. M. Virus taxonomy: eighth
Report of the International Committee on Taxonomy of Viruses. London: Elsevier, 2005.
p. 301-326.
SUN, D. B. et al. Incompatibilidade reprodutiva entre as B e Q biótipos de mosca
branca Bemisia tabaci: evidências genéticas e comportamentais. Entomological Research,
Chichester, v. 101, p. 211-220, 2011.
THOMPSON, J. D. et al. CLUSTAL W: improving the sensitivity of progressive multiple
sequence alignment through sequence weighting, position-specific gap penalties and
weight matrix choice. Nucleic Acids Research, Oxford, v. 22, , p. 4673-4680, 1994.
62
TOSCANO, L. C.; BOIÇA JÚNIOR, A. L.; MARUYAMA, W. I. Fatores que afetam a
oviposição de Bemisia tabaci (Genn.) Biótipo B (Hemiptera: Aleyrodidae) em tomateiro.
Neotropical Entomology, Dordrecht, v. 31, p. 631-634, 2002.
WANG, Z. Y. et al. Biótipo e estado de resistência a inseticidas da mosca branca Bemisia
tabaci da China. Pest Management Science. Chichester v. 66, p. 1360-1366, 2010.
VILLAS BÔAS, G. L. et al. Manejo integrado da mosca-branca Bemisia argentifolii.
Brasília, DF: EMBRAPA-CNPH, 1997. 11 p. (Circular Técnica da Embrapa Hortaliças, 9).
VENDRAMIM, J. D.; GUZZO, E. C. Resistência de plantas e a bioecologia e nutrição dos
insetos. In: PANIZZI, A. R.; PARRA, J. R. P. (Ed.). Bioecologia e nutrição dos insetos:
bases para o manejo integrado de pragas. Brasília, DF: Embrapa Informação Tecnológica,
p. 1055-1105, 2009.
XU, J.; BARRO, P. J.; LIU, S. S. Incompatibilidade reprodutiva entre os grupos genéticos
de Bemisia tabaci suporta a proposição de que a mosca branca é um complexo de espécies
crípticas. Entomological Research, Chichester, v. 100, p. 359-366, 2010.
ZENI, A. L.; BOSIO, F. O uso de plantas medicinais em uma comunidade rural de Mata
Atlântica – Nova Rússia, SC. Neotropical Biology and Conservation, Espanha, v. 6,
n.
1,
p.
55-63,
2011.
Disponível
em:
http://www.unisinos.br/index.php/neotropical/article/view/997.pdf.Doi:
10.4013/nbc.2011.61.07.