Arq Bras Cardiol
volume 72, (nº 5), 1999
Chalela
e cols.
Artigo
Original
Cintilografia na detecção do miocárdio viável
Detecção do Miocárdio Viável. Estudo de Perfusão, Antes e
Após a Cirurgia de Revascularização em Portadores de
Infarto do Miocárdio
Willliam A. Chalela, Paulo J. Moffa, José A. F. Ramires, Aguinaldo P. Moraes,
José Soares Jr, José C. Meneghetti
São Paulo, SP
Objetivo – Comparar as imagens dos SPECT com 201Tl
e o 99mTc-MIBI na identificação de miocárdio viável, em regiões comprometidas por infarto.
Métodos – Foram estudados 32 pacientes (59,3±9,8
anos e 87,6% masculino) portadores de infarto do
miocárdio, com ondas Q ao ECG e fração de ejeção do
ventrículo esquerdo <50%. Submeteram-se a cinecoronarioventriculografia esquerda e ao SPECT antes (inclusive
a reinjeção de 201Tl) e após a cirurgia de revascularização.
O reconhecimento de viabilidade miocárdica foi considerado a melhora da perfusão verificada após a cirurgia.
Resultados - Das 102 regiões analisadas, 40 (39,2%)
foram reversíveis ao protocolo convencional com 201Tl e 52
(51,0%) ao da reinjeção. Portanto, 12/62 (19,4%) regiões
reversíveis a mais foram verificadas pela reinjeção. Com o
99m
Tc-MIBI, foram demonstradas apenas 14 (13,7%) regiões
com reversibilidade e todas também verificadas aos protocolos com 201Tl. Após a cirurgia, das 93 regiões analisadas,
49 (52,7%) foram viáveis. A sensibilidade, especificidade,
acurácia, valores preditivos positivo e negativo foram na
seqüência: SPECT com 201Tl - 65,3%, 90,9%, 77,4%, 88,9%
e 70,2%, da reinjeção com 201Tl - 81,6%, 81,8%, 81,7%,
83,3% e 80,0%; com 99mTc-MIBI - 20,4%, 90,9%, 53,8%,
71,4% e 50,6%. A regressão logística mostrou que a reinjeção com 201Tl foi melhor preditor de viabilidade (P<0,001).
Conclusão – Nossos dados justificam eleger o 201Tl
para a pesquisa de viabilidade, sendo esta, melhor comprovada pelo protocolo da reinjeção.
Palavras-chave:
viabilidade miocárdica, doença arterial
coronariana, cintilografia de perfusão
miocárdica
Instituto do Coração do Hospital das Clinicas - FMUSP
Correspondência: William Azem Chalela - Incor - Serviço de Radioisótopos Av. Dr. Enéas C. Aguiar, 44–AB - 05403-000 - São Paulo, SP
Recebido para publicação em 20/8/98
Aceito em 24/3/99
Nos pacientes com doença arterial coronariana (DAC),
a cardiomiopatia isquêmica resulta em freqüentes hospitalizações ou mesmo morte. Além disso, os pacientes com cardiomiopatia isquêmica grave têm alta mortalidade, quando
tratados clinicamente, com sobrevida 1 em dois anos, ao redor de 31%, e tendo o transplante cardíaco 2,3 como uma das
indicações.
A cardiomiopatia isquêmica pode decorrer da falência
miocárdica por extensas áreas de infarto, ou por regiões de
miocárdio hipocontrátil devido à hipoperfusão crônica sem
necrose. A presença de miocárdio viável poderá favorecer a
indicação para revascularização miocárdica, impedindo
evolução para aumento da área necrótica e conseqüente
piora da função ventricular, havendo assim, necessidade de
transplante cardíaco 4.
A identificação correta da condição de viabilidade
miocárdica constitui elemento de importância quanto ao
tipo de terapêutica a ser adotada: revascularização miocárdica, ressecção de áreas aneurismáticas fibróticas, ou transplante cardíaco.
Sabe-se que, freqüentemente, os dados clínicos, o eletrocardiograma (ECG), a coronariografia e a avaliação da
motilidade regional em repouso, não nos auxiliam na distinção entre fibrose e miocárdio viável.
Inicialmente, utilizaram-se o potencial pós-extrassistólico e a injeção de agentes inotrópicos positivos para identificar o miocárdio viável com base na restauração da contração segmentar analisada através de sensores colocados diretamente sobre o epicárdio em condições experimentais, ou
pela análise da motilidade da parede ventricular na cineventriculografia convencional. Recentemente, a ecocardiografia e a ventriculografia radioisotópica, com estresse farmacológico (baixas doses de dobutamina), vêm sendo utilizadas com o mesmo propósito.
A tomografia por emissão de pósitrons é considerada
a técnica não invasiva mais sensível na identificação de
viabilidade. Permite avaliar o fluxo regional (amônia marcada
Arq Bras Cardiol, volume 72 (nº 5), 523-534, 1999
523
Chalela e cols.
Cintilografia na detecção do miocárdio viável
com o nitrogênio-13) e o metabolismo miocárdico de carboidratos (glicose marcada com o flúor-18) e lipídeos (palmitato
marcado com o carbono-11). No entanto, seu uso é limitado,
devido ao elevado custo do equipamento, necessidade de
uma equipe multiprofissional, além da meia vida ultra-rápida
dos traçadores.
A técnica de imagem cardíaca, a cintilografia de perfusão miocárdica (CPM), baseada no estudo da perfusão miocárdica e da integridade da membrana celular, tem gerado
substancial sucesso clínico para a pesquisa de viabilidade
miocárdica 5.
Assim, o presente trabalho objetivou a investigação
de músculo viável em regiões comprometidas pelo infarto do
miocárdio (IM), através da CPM com imagens tomográficas
[SPECT (single photon emission computed tomography)].
Para tal finalidade, usaram-se, como radiofármacos, tanto o
cloreto de tálio - 201 (201Tl) como o 2-metoxi-isobutil-isonitrila marcado com tecnécio-99m (99mTc-MIBI). A melhora da
perfusão observada após a revascularização destas áreas
serviu de modelo para efeito dos cálculos estatísticos.
O 201TI é o radiofármaco mais usado como marcador de
perfusão miocárdica para o estudo de viabilidade miocárdica. O 99mTc-MIBI é muito utilizado para o diagnóstico de
insuficiência coronariana obstrutiva, porém existe falta de
informações adequadas sobre seu uso para a detecção do
miocárdio viável.
Métodos
Dos 113 pacientes encaminhados para o estudo de viabilidade pela CPM, foram selecionados 32 com história clínica de IM e que preencheram os seguintes critérios de inclusão: tempo de evolução do IM entre 3 e 12 meses; presença
de onda Q ou complexo QS com duração >40ms ao ECG;
classe funcional 6 até III, tanto para angina do peito (AP)
como para a insuficiência cardíaca congestiva (ICC); fração
de ejeção global do ventrículo esquerdo (FEVE) <50%; sem
contra-indicação absoluta e em condições adequadas para
realização do teste ergométrico (TE). Foram excluídos: quadro clínico instável; uso de agentes trombolíticos e/ou revascularização miocárdica na fase aguda do IM; presença
de bloqueio de ramo do feixe de His ao ECG; hipertensão arterial sistêmica não controlada; valvopatias, pericardiopatias ou outras cardiomiopatias associadas.
Antes da cirurgia de revascularização do miocárdio
(RM), todos os pacientes foram submetidos a estudo hemodinâmico e da CPM com 201Tl e 99mTc-MIBI, associados ao
TE, até seis meses antes do procedimento. Após a RM, confirmada de forma completa 7, os pacientes que puderam ser
reavaliados nessa fase, realizaram a CPM com os mesmos
radiofármacos na situação de repouso e ao redor de três
meses, e o estudo hemodinâmico até seis meses após o procedimento. O tempo mínimo da realização entre os estudos
da CPM foi entre três dias e, no máximo sete dias. Os pacientes foram analisados em vigência de medicação com as
mesmas dosagens durante todo o seguimento.
524
Arq Bras Cardiol
volume 72, (nº 5), 1999
Esta pesquisa científica foi aprovada pela comissão
científica do INCOR e também pelo comitê de ética do Hospital das clínicas da FMUSP. Todos os pacientes concordaram em participar do estudo, após os esclarecimentos pertinentes.
Os traçados de ECG foram realizados de forma convencional e concomitante aos dias das realizações dos exames
cintilográficos. Desta forma, dividiram-se os segmentos
miocárdicos acometidos por IM em regiões septal, anterior,
inferior, dorsal e lateral, conforme padrão estabelecido na
literatura 8.
Quanto ao grau de estreitamento, as lesões coronárias
foram classificadas segundo o percentual de obstrução: lesões severas ocluídas (100% da luz), subocluída (>90% e
<100%); lesão crítica de 70 a 90%; lesão não crítica <70%.
Foi verificada ainda a presença de circulação colateral (Cc),
quanto a sua origem, e a intensidade avaliada semiquantitativamente 9. Convencionou-se como responsável pela ocorrência do infarto a artéria ocluída, ou subocluída ou com
lesão crítica, e que correspondesse anatomicamente à região comprometida, isto é: o ramo interventricular anterior
(IA) para regiões septal, anterior e apical; artéria coronária
direita (CD) para a região inferior e o ramo circunflexo (Cx)
para as regiões lateral e dorsal. Nos casos em que a CD e a Cx
apresentavam-se com lesões semelhantes, admitiu-se como
artéria responsável aquela que fosse dominante, a CD quando para região inferior, e o ramo Cx, quando analisada a região dorsal.
A análise da movimentação das paredes ventriculares
foi realizada através da cineventriculografia esquerda, na
projeção oblíqua anterior direita (OAD). As alterações da
motilidade foram classificadas em: hipocinesia – diminuição
discreta, moderada ou acentuada da motilidade parietal do
VE; acinesia – perda total da movimentação; discinesia –
expansão sistólica paradoxal de um determinado segmento
do VE. Criou-se uma graduação arbitrária variando de zero
até cinco, de acordo com a cinética do VE (0 = normal, 1 a 3 –
hipocinesia discreta a acentuada; 4 = acinesia e 5 = discinesia). Considerou-se, como melhora das anormalidades cinéticas, a diminuição em pelo menos um ponto na graduação,
quando comparada às fases pré e pós procedimento.
A FEVE global foi calculada pelo método uniplanar de
Dodge 10 modificada por Kennedy 11.
Os TEs foram realizados da forma convencional 12. Foram utilizados a esteira rolante de rampa móvel e o protocolo de Ellestad 13, com o registro de 12 derivações clássicas
simultâneas.
O protocolo de estudo da CPM com 201Tl compreendeu três fases: 1ª, as imagens foram adquiridas imediatamente após a injeção do radionuclídeo realizada no pico do
exercício; a dose injetada foi de 111 MBq (3mCi) e as imagens
tomográficas obtidas com o paciente em decúbito dorsal; 2ª,
após 4h e da mesma forma, foram adquiridas as imagens de
redistribuição; 3ª, realizada após 24h, com nova dose administrada em repouso e com a aquisição das imagens tomográficas realizadas após 4h denominadas de reinjeção.
Arq Bras Cardiol
volume 72, (nº 5), 1999
Para o estudo da perfusão com o 99mTc-MIBI, todo o
procedimento foi realizado no mesmo dia. Inicialmente, obtiveram-se as imagens em repouso, com a infusão endovenosa de 296 a 370 MBq (8 a 10mCi), realizando, em seguida o
estresse físico (EF), injetando-se no esforço máximo três vezes
a dose de repouso, ou seja, 888 a 1110 MBq (24 a 30mCi) e
obtendo-se novas imagens. Após a RM, realizou-se a CPM
em repouso com ambos os radiofármacos. Para o 201Tl, as
imagens foram adquiridas 4h após a injeção. Para a aquisição das imagens tomográficas foi utilizada câmara de cintilação Siemens, modelo Orbiter ZLC-Digitrac 750, acoplada a
um computador Maxdelta (Microvax - 3300). As imagens
analógicas foram convertidas em digitais numa matriz 64x64,
64 projeções com duração de 20s cada, sobre um arco de
180º, iniciando-se da OAD de 45º até a oblíqua posterior
esquerda (OPE) de 45º (modo de aquisição step/shoot). O filtro utilizado foi o Butterworth, com número de ordem cinco,
e freqüência de corte (Cutoff) de 0,4 Ny (Ny- freqüência de
Nyquist) para o 201Tl e 0,5 Ny para o 99mTc-MIBI.
Após a reconstrução, foram obtidos os cortes transversais a cada 6,09mm, reorientados para o eixo do coração,
permitindo assim, a determinação dos cortes correspondentes aos três planos mutuamente perpendiculares ao sistema
de coordenadas fixado para o coração: corte coronal ou eixo
longo horizontal (no sentido inferior-anterior); corte oblíquo ou eixo curto (no sentido ápice- base); corte sagital ou
eixo longo vertical (no sentido septo-lateral). Dividiu-se o
coração em cinco regiões: septal, anterior, inferior, apical e
lateral (látero-dorsal) e, a cada uma delas, foi atribuído um
valor através de um sistema de graduação arbitrária de quatro pontos, conforme a captação do radiofármaco (0 = captação normal; 1 = hipocaptação discreta; 2 = hipocaptação
moderada; 3 = hipocaptação acentuada ou ausência de
captação). A diminuição em pelo menos um ponto desta
graduação, na região analisada, quando se compararam as
imagens de EF com as outras fases, foi interpretada como a
hipocaptação transitória, e considerada parcial quando não
se observou valor zero nas imagens de redistribuição e/ou
reinjeção e/ou repouso. Por outro lado, a manutenção desta
pontuação determinou a hipocaptação persistente (fibrose). Convencionou-se a denominação: hipocaptação ou defeito reversível, quando presente a transitoriedade na comparação das imagens na fase pré RM, e de viáveis após a cirurgia; na mesma seqüência, para os defeitos persistentes,
de irreversíveis e não viáveis.
Para este estudo, foram analisadas apenas as regiões
do VE comprometidas pelo IM, verificadas ao ECG. A região
apical foi considerada como extensão do comprometimento
das regiões anterior e/ou inferior, desde que mostrasse valor de pontuação superior a zero na graduação. A melhora
da captação regional miocárdica, ou seja, a melhora da
perfusão dos cardiócitos, observada pelo protocolo de repouso, por um ou por outro radiotraçador, constituiu o padrão para determinar os verdadeiros viáveis.
Para cumprir os objetivos deste trabalho, foram montadas tabelas descritivas. As variáveis contínuas foram apresentadas descritivamente por meio de médias e desvios-
Chalela e cols.
Cintilografia na detecção do miocárdio viável
padrão. Realizaram-se comparações antes e após a cirurgia
de RM com os testes 14 dos sinais de Wilcoxon (teste não
paramétrico) ou t-Student (pareado). A concordância entre
os resultados de reversibilidade e/ou viabilidade miocárdica
foi verificada com a estatística Kappa 15 (K). Os valores
>0,75 representam uma concordância excelente, entre 0,40 e
0,75, uma boa concordância e <0,40, uma concordância limítrofe. Foram calculadas as variáveis operacionais de sensibilidade (S), especificidade (E), acurácia (A), valores preditivos positivo (VPP) e negativo (VPN), tendo como modelo
de comparação, os resultados da CPM após a cirurgia. A
resposta de viabilidade, confirmada após a cirurgia de RM,
foi ajustada modelo de regressão logística, com processo
stepwise de seleção de variáveis, em que consideraram-se
os demais protocolos como fatores preditores.
O nível de significância utilizado foi de 0,05. Os cálculos foram processados no sistema SAS 16. Também foi
verificada a análise da variabilidade intra e inter-observador,
e assim, reavaliada uma amostragem de 10 casos com intervalo de pelo menos 30 dias.
Resultados
Os dados da população estudada encontram-se na tabela I. A média da idade foi de 59,3±9,8 anos (variação de 42
a 75 anos), sendo 28 (87,6%) do sexo masculino e 4 (12,4%)
do feminino. O tempo médio de evolução do IM, foi de
8,14+3,29 meses.
Constituíram-se 78 regiões miocárdicas comprometidas por fibrose, assim distribuídas: 23 (29,5%) septais, 23
(29,5%) anteriores, 21 (26,9%) inferiores, 10 (12,8%) laterais
e 1 (1,3%) em região dorsal.
Os dados gerais da cinecoronarioventriculografia esquerda, encontram-se na tabela II. Foi realizada em média
2,79+2,73 meses antes da cirurgia de RM. Quanto ao número
de artérias comprometidas com lesões significativas em IA,
CD e Cx o estudo mostrou uma artéria em um (3,1%) paciente; 2 artérias em 7 (21,9%), sendo a combinação de IA e CD a
mais freqüente (71,4%); 3 artérias em 24 (75,0%). A Cc foi
evidenciada em 24 (75,0%) pacientes. A motilidade regional
pôde ser verificada nas paredes anterior, inferior e apical do
VE, totalizando 96 regiões da casuísta global. As alterações
encontradas foram: 61 (63,4%) regiões com hipocinesia de
graus variados - 13 (13,5%) discretas, 26 (27,0%) moderadas
e 22 (22,9%) acentuadas - 23 (24%) com acinesia e 11
(11,6%) com discinesia. A FEVE global observada em todos
os pacientes foi em média de 34,9±10,2%, com a seguinte
distribuição: 10 (31,2%) pacientes com FEVE >40% e <48%
e 19 (59,4%) com FE >20% e <40%, e 3 (9,4%) com FE <20%.
Os pacientes que foram a óbito no pós-operatório (PO) imediato, mostraram FEVE de 20%, 30% e 43%.
Os principais parâmetros clínicos, eletrocardiográficos,
hemodinâmicos e metabólicos obtidos ao TE associado à
CPM com 201Tl e 99mTc-MIBI, não mostraram diferenças significativas. As médias respectivas ao esforço máximo foram:
freqüência cardíaca 132±20,6bpm e 130,5±18,6bpm, pressão
525
Chalela e cols.
Cintilografia na detecção do miocárdio viável
Arq Bras Cardiol
volume 72, (nº 5), 1999
Tabela I - Características gerais da população
No
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
Nome
GAL
RM
MIS
OVA
ACGD
SS
TJ
AOA
PSS
PL
CP
MTM
OF
BM
DCA
PAAG
JMP
NCP
JBS
JMB
FP
NGS
JB
GMS
SAC
JMC
SAA
GDS
AM
JCNN
GTB
MFL
Idade
(anos)
Sexo
61
42
61
47
49
65
55
74
72
65
48
67
63
72
63
65
54
65
56
74
56
42
61
63
67
52
44
75
65
45
62
49
M
M
M
M
M
M
M
M
M
M
M
M
M
M
M
M
F
F
M
M
M
F
M
M
M
M
M
M
M
M
M
F
Peso
(kg)
Alt.
(Cm)
IMC
(kg/m2)
HAS
88
79
102
92
63
67
68
63
86
60
86
81
70
65
68
79
51
66
73
75
66
52
70
70
72
85
71
81
82
78
56
90
1,75
1,70
1,78
1,79
1,62
1,65
1,70
1,72
1,72
1,60
1,74
1,66
1,70
1,80
1,73
1,77
1,58
1,56
1,54
1,60
1,55
1,46
1,70
1,70
1,72
1,73
1,58
1,72
1,71
1,80
1,63
1,60
28,7
27,3
31,9
28,7
24,0
24,6
23,5
21,3
29,1
23,4
28,4
29,4
24,2
20,1
22,7
25,2
20,4
27,1
30,8
29,3
27,5
24,4
24,2
24,2
24,3
28,4
28,4
27,4
28,0
24,1
21,1
35,2
sim
sim
não
sim
sim
sim
sim
não
sim
não
não
não
não
não
não
sim
sim
sim
sim
sim
sim
não
sim
não
não
sim
não
não
sim
sim
não
sim
DM
HC
HT
TAB
AF
S
Não
Não
Sim
Não
Sim
Sim
Não
Não
Sim
Não
Não
Sim
Não
Sim
Sim
Sim
Não
Sim
Não
Não
Sim
Sim
Não
Não
Não
Sim
Não
Não
Sim
Sim
Não
Não
não
não
sim
não
sim
não
sim
não
não
não
não
não
sim
não
não
não
sim
sim
não
não
sim
sim
não
não
não
não
sim
não
sim
não
não
sim
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
não
sim
sim
não
sim
não
não
sim
sim
sim
sim
sim
sim
sim
sim
não
sim
sim
não
sim
não
não
não
sim
sim
sim
sim
sim
sim
não
sim
não
não
não
sim
sim
sim
não
não
não
não
sim
não
sim
não
sim
não
não
não
não
sim
não
sim
não
não
sim
não
sim
sim
não
não
não
não
não
sim
ECG - Regiões
A I L D
S
S
A
A
S
S
A
A
S
S
S
A
A
A
I
L
I
I
I
I
I
I
I
S
A
S
S
S
S
S
S
S
A
A
A
A
A
A
A
L
L
L
L
I
S
A
S
A
S
S
A
A
S
S
S
S
A
A
A
A
I
I
I
I
I
I
I
I
I
I
I
I
I
L
L
L
L
L
D
Tempo EVL.
(meses)
CF
AP
CF
ICC
3,8
10,3
12,0
3,8
6,8
12,0
4,3
6,9
11,7
11,7
4,6
3,1
12,0
3,3
11,6
11,1
12,0
4,2
8,7
11,7
11,8
5,5
11,6
12,0
11,1
12,0
3,4
5,7
3,3
3,3
11,9
3,7
I
III
III
III
II
II
III
III
III
I
I
II
III
II
I
I
III
III
I
I
III
III
III
I
III
I
I
II
III
III
III
III
III
III
III
II
III
II
III
III
III
III
II
II
II
III
III
III
II
II
II
III
I
III
III
III
III
III
III
III
III
III
III
III
Alt. Altura; IMC- índice de massa corporal em kg/m2; HAS- hipertensão arterial sistêmica; DM- diabetes melito; HC- hipercolesterolemia; HT- hipertrigliceridemia;
TAB- tabagismo; AF- antecedentes familiares para doença arterial coronária; ECG- eletrocardiograma com ondas Q ou complexos QS patológicos; EVL- evolução
do último infarto em meses até a cirurgia; RM- revascularização do miocárdio; CF- classe funcional (New York Heart Association); AP- angina do peito; ICCinsuficiência cardíaca; S- septal; A- anterior; L- lateral; I- inferior; D- dorsal.
arterial sistólica de 159,5±30,5mmHg e 153,7±23,2mmHg e
duplo produto de 21159,2±5676,1 e 20063,0±4125,9, não mostrando diferenças significativas. A incidência de AP, o gasto
energético e as alterações do segmento ST tiveram comportamento semelhantes em ambos os estudos, demonstrando
que os isótopos radioativos foram injetados em condições
semelhantes, e assim, não demonstrando fatores externos
que pudessem alterar a acurácia de ambos os estudos da
CPM.
Na cirurgia de RM, todas as artérias com lesões >50%
foram revascularizadas, portanto, em todos os casos esta se
fez de forma completa. O período de seguimento após a cirurgia de RM foi de 15,16+10,17 meses. Três (9,4%) pacientes
foram a óbito no PO imediato por choque cardiogênico e um
outro após quatro meses e de forma súbita. Vinte e nove
(90,6%) pacientes foram avaliados pela classe funcional, antes e após a RM, em relação aos sintomas da AP e da ICC (fig.
1), e a análise estatística mostrou-se significativa (p<0,001)
quanto à melhora dos dois parâmetros analisados.
O estudo cinecoronariográfico após a RM, pôde ser
realizado em 23 pacientes (4,98±1,09 meses após o procedimento cirúrgico) e todos os enxertos mostraram-se pérvios.
526
A melhora das alterações cinéticas ocorreu em 48 (69,6%)
regiões e a permanência ou não em 21 (30,4%) regiões miocárdicas, comparativamente à fase anterior à revascularização. Esta distribuição mostrou-se significativa, com
p<0,001. A média da FEVE global nesta fase foi maior
(46,4+13,5%), e com significado estatístico (p<0,001), quando comparada à fase anterior à cirurgia (fig. 2).
Para a detecção do miocárdio viável através da CPM,
foram analisadas antes da cirurgia de RM, as 78 regiões miocárdicas verificadas pelo ECG, e incluídas 24 regiões apicais
verificadas como extensão do comprometimento das paredes anterior e/ou inferior. Portanto, à CPM foram analisadas
102 regiões miocárdicas, consideradas comprometidas pelo
IM. Para a CPM com 201Tl, a análise do protocolo convencional (comparando as imagens de estresse e as da redistribuição de 4h), mostrou 40 (39,2%) regiões reversíveis e 62
(60,8%) irreversíveis (defeito fixo); o da reinjeção (imagens de
estresse e as da reinjeção de 24h) mostrou 52 (51,0%) e 50
(49%) regiões miocárdicas reversíveis e irreversíveis, respectivamente. Portanto, o protocolo da reinjeção identificou 12
regiões reversíveis (19,4%) que foram classificadas como
irreversíveis pelo estudo convencional. Com o protocolo
convencional (imagens de estresse e de repouso) utilizando
1,87
5,23
0,23
2,23
5,53
3,40
5,67
5,37
4,70
4,80
5,70
2,50
5,70
2,10
0,43
3,47
4,37
1,50
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
CD
CD
CD
CD
CD
CD
CD
CD
Bal.
CD
CD
CD
CD
CD
CD
CD
CD
CD
Cx
CD
CD
CD
CD
CD
CD
CD
CD
CD
CD
CD
CD
CD
Dom.
80
100
100
30
100
70
100
100
90
100
100
100
100
100
100
100
100
100
90
100
100
80
100
100
100
100
90
100
100
80
-
95
-
-
-
IA
-
-
-
-
-
CD
-
-
-
-
-
-
IA
-
CD
-
CD
-
-
-
IA
-
-
IA
-
-
-
Lesão Orig.
%
CD
IA
Cx
-
Cx
-
-
-
-
-
IA
-
IA
CD
CD
-
Cx
Cx
-
Cx
CD
Cx
Cx
CD
CD
Cx
-
-
Cx
-
-
-
Cc
++
+++
-
++
-
-
-
-
-
+
-
+++
+
+
-
++
++
-
+++
+++
+++
+++
+++
+
++
-
-
++
-
-
-
100
95
95
95
80
95
100
80
99
90
100
100
95
100
100
100
100
100
90
100
100
95
100
80
100
100
80
100
99
100
100
99
CD
-
-
-
CD
-
-
-
-
-
-
-
-
-
-
CD
-
CD
-
-
CD
-
-
-
-
-
-
-
-
-
-
-
Grau Lesão Orig.
%
IA
IA
-
-
-
Cx
-
IA
-
-
-
IA
-
-
IA
-
Cx
Cx
IA
-
IA
IA
CD
CD
-
IA
CD
-
-
-
-
-
-
Cc
++
-
-
-
+++
-
++
-
-
-
++
-
-
+
-
++
++
+++
-
+++
+++
++
+++
-
+
+++
-
-
-
-
-
-
80
40
-
90
-
-
-
-
90
-
-
90
90
-
-
-
-
-
-
70
-
80
-
70
30
-
-
70
-
-
80
80
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Grau Lesão Orig.
%
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
IA
-
Cc
Coronariografia
DI
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
+++
-
70
-
-
30
100
-
90
100
-
95
-
-
100
75
75
-
-
100
40
40
80
100
-
40
70
40
-
30
100
-
100
70
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Grau Lesão Orig.
%
Cx
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Cc
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
70
70
30
-
-
80
-
100
90
-
100
-
-
-
80
-
-
-
80
80
40
100
-
-
80
100
100
-
100
-
-
-
-
-
-
-
CD
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Grau Lesão Orig.
%
ME
-
-
-
-
-
Cx
-
-
-
-
3
-
-
-
-
-
-
-
-
-
-
Cx
-
-
-
Cx
Cx
-
-
-
-
Cc
-
-
-
-
-
+++
-
-
-
-
+
-
-
-
-
-
-
-
-
-
-
+++
-
-
-
+++
+++
-
-
-
-
-
-
30
40
-
-
-
-
-
-
40
-
-
-
-
-
-
-
-
-
40
-
-
-
-
-
40
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Grau Lesão Orig.
%
CE
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Cc
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Grau
A
HD
HA
HA
HM
A
HA
HM
A
HM
HD
HA
HM
D
D
HA
A
HM
HM
D
A
A
A
HM
A
HA
N
A
HM
D
HM
A
Ant.
Cine E.
HM
HM
HD
HM
HM
HD
HD
HÁ
HM
HM
HM
HA
HA
HA
HA
HÁ
HD
HA
HM
HM
HA
HM
HA
HD
HM
HA
HD
HA
HM
HM
HD
HA
Inf.
Mot. Reg.
A
HD
HD
HA
HA
D
D
A
A
A
A
HA
HD
D
D
A
A
A
HA
D
D
A
A
HM
A
HA
HD
A
D
HM
HM
A
Ap
27
30
26
35
35
38
42
40
30
47
33
43
30
35
35
39
20
36
40
28
17
46
12
39
21
48
48
20
45
18
47
35
FE
D - intervalo de tempo; RM- revascularização miocárdica; CINE E- cineventriculogragia esquerda; Dom- dominância; CD- artéria coronária direita; IA- ramo interventricular anterior; DI- ramos diagonais; Cx- ramo circunflexo; MEramo marginal esquerdo; CE- artéria coronária esquerda; Mot. Reg- motilidade regional; FE- fração de ejeção global; Cc- circulação colateral; Orig- origem; Ant- anterior; inf. inferior; Ap- apical; Bal- balanceada; N- normal; HDhipocinesia discreta; HM- moderada; HA- acentuada; A- acinesia; D- discinésia;
- Artéria responsável pelo infarto do miocárdio
4,17
0,87
4,00
9
0,50
2,33
8
31
32
1,07
7
30
3,13
6
6,0
3,57
5
0,23
0,70
4
29
1,53
3
28
0,63
5,70
2
Meses
D RM
1
No
Tabela II - Dados gerais do estudo cinecoronarioventriculográfico realizado antes da cirurgia de revascularização
Arq Bras Cardiol
volume 72, (nº 5), 1999
Chalela e cols.
Cintilografia na detecção do miocárdio viável
527
Chalela e cols.
Cintilografia na detecção do miocárdio viável
ANGINA DO PEITO
p < 0,001
Arq Bras Cardiol
volume 72, (nº 5), 1999
ICC
p < 0,001
Fig. 1 - Comportamento da classe funcional segundo a New York Heart Association, antes e após a cirurgia de revascularização do miocárdio. N= 29 pacientes; ICC- insuficiência
cardíaca congestiva; RM- revascularização do miocárdio.
Fig. 2 - Distribuição e médias com desvios padrão da fração de ejeção do ventrículo
esquerdo, obtidas antes e após a cirurgia de revascularização.
99m
Tc-MIBI, verificaram-se 14 (13,7%) regiões reversíveis e as
restantes 88 (86,3%) mostraram defeito fixo (tab. III).
Após a cirurgia de RM, 29 dos 32 pacientes puderam
realizar a CPM, com exceção dos três casos que foram a óbito em fase precoce. Portanto, 93/102 (91,2%) regiões foram
analisadas: 21 (22,6%) septais, 21 (22,6%) anteriores, 22
(23,7%) apicais, 19 (20,4%) inferiores e 10 (10,7%) láterodorsais. Foram classificadas como verdadeiras viáveis 49
(52,7%) regiões, sendo 41 (44,1%) concordantes entre as
CPM e as 8 restantes, 4 (4,3%) verificadas com o 201TI e 4
(4,3%) com o 99mTc-MIBI; as outras 44 (47,3%) regiões,
como verdadeiras não viáveis (tab. III). A concordância dos
resultados em 85 (91,4%) regiões mostrou-se significativa
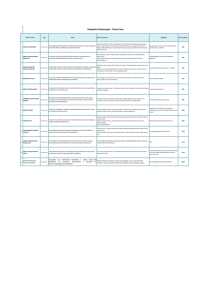
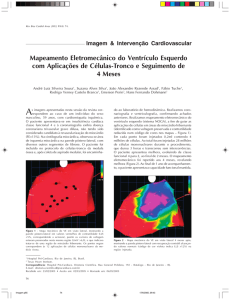
(p<0,001) com reprodutibilidade excelente (k= 0,828).
As figuras 3 e 4 mostram um exemplo da CPM com os
cortes tomográficos do eixo oblíquo, de um paciente com
IM e músculo viável.
528
Os cálculos das variáveis operacionais S, E, A, VPP e
VPN em toda casuística, foram respectivamente: 65,3%,
90,9%, 77,4%, 88,9% e 70,2% para o protocolo convencional
com 201Tl; e de 81,6%, 81,8%, 81,7%, 83,3% e 80,0% para o
da reinjeção; de 20,4%, 90,9%, 53,8%, 71,4% e 50,6% para o
protocolo convencional com 99mTc-MIBI. Depreende-se, em
função desses resultados que houve subestimação do
miocárdio viável pelo protocolo convencional com 99mTcMIBI. A maior captação, observada após a revascularização
das regiões miocárdicas com IM - áreas de fibrose porém ainda viáveis - foi melhor demonstrada pela CPM com 201Tl e,
principalmente, com o protocolo da reinjeção. Pôde-se confirmar, através da regressão logística, que o protocolo da
reinjeção foi o melhor preditor de viabilidade (p<0,001).
Verificou-se, através das lesões severas (obstrução
>90% da luz), que a coronária e a Cc no mesmo território foram
responsáveis pela perfusão de 24/49 (49,0%) das regiões viáveis e 26/44 (59,0%) das não viáveis. Mostraram freqüências
semelhantes, portanto, sem significado estatístico. Porém, a
intensidade semiquantificada da Cc de +++/++++ foi mais freqüente nas regiões viáveis (60%), e de +/++ nas não viáveis
(78,6%), diferenças estas significantes e p= 0,004 (tab. IV).
Das 69 regiões miocárdicas avaliadas pela cineventriculografia após a RM, 49 delas foram responsáveis pelo IM.
Observou-se melhora da motilidade em 3 6/49 (73,5%) após
a RM (p<0,001) (fig. 5).
A relação entre a recuperação da perfusão e da função
sistólica, pôde ser verificada em 49 regiões miocárdicas, ou
seja, foi concordante em 34 (69,4%) regiões, das quais 25
(51,0%) melhoraram a perfusão e a motilidade regional após
a RM e 9 (18,4%) regiões não melhoraram. Esta relação foi
discordante em 15 (30,6%) regiões analisadas - 11 (22,4%)
melhoraram a motilidade e 4 (8,2%) a captação dos radiofármacos. Entretanto, a melhora da captação (perfusão) regional do VE relacionou-se significativamente (p=0,011) com a
melhora da motilidade.
1,6
5,2
1,4
2,4
3,9
1,3
0,8
1,7
3,5
0,7
0,8
0,3
0,1
3,8
0,4
4,7
0,6
0,8
0,4
3,4
1,7
2,4
1,4
4,5
3,4
0,3
0,4
2,2
0,1
0,1
4,6
0,4
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
R
R
-
I
-
R
I
I
-
R
R
-
I
I
S
Tl
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
R
R
-
I
-
R
I
I
-
R
R
-
I
I
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
R
R
-
I
-
R
I
I
I
R
R
-
I
I
R
R
-
I
-
I
I
I
I
R
I
I
-
I
-
-
I
-
-
R
-
I
-
I
I
I
R
R
I
-
I
-
-
-
I
-
-
I
I
-
-
I
I
-
-
-
-
-
-
-
-
I
I
R
-
-
I
-
-
-
I
-
Regiões miocárdicas
A
AP
In
L
201
-
-
-
-
-
-
-
-
-
-
-
I
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
D
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
R
R
R
-
I
-
R
I
I
-
R
R
-
R
R
S
201
Tl
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
R
R
R
-
I
-
R
I
I
I
R
R
-
R
R
R
R
R
R
-
I
I
-
I
-
R
-
-
R
I
I
I
R
R
R
-
I
-
R
I
I
-
R
R
-
R
R
R
R
-
I
-
I
I
I
I
R
I
I
-
I
-
-
R
-
-
R
-
I
-
I
I
I
R
R
I
-
R
-
-
-
I
-
—
I
I
-
-
I
I
-
-
-
-
-
-
-
-
I
I
R
-
-
I
-
-
-
R
-
Regiões miocárdicas
A
AP
In
L
Reinjeção
-
-
-
-
-
-
-
-
-
-
-
I
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
D
4,4
0,2
0,2
0,2
1,9
0,2
0,2
3,6
4,7
1,5
2,2
1,5
3,2
0,2
0,6
0,8
4,5
0,3
3,9
0,2
0,4
0,7
0,7
3,6
1,5
0,6
1,4
3,7
2,2
1,3
5,1
1,4
D RM
Meses
I
I
I
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
I
R
-
I
-
I
I
I
-
I
I
-
I
I
S
I
I
I
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
I
R
-
I
-
I
I
I
-
I
I
-
I
I
I
I
I
R
-
I
I
-
I
-
R
-
-
R
I
I
I
I
I
R
-
I
-
I
I
I
I
I
I
-
I
I
-
-
-
I
-
-
I
I
-
-
I
I
-
-
-
-
-
-
-
-
I
I
I
-
-
I
-
-
-
I
-
I
I
-
I
-
I
I
I
I
R
I
I
-
I
-
-
I
-
-
R
-
I
-
I
I
I
I
I
I
-
I
Regiões miocárdicas
A
AP
L
In
Convencional 99mTc - MIBI
-
-
-
-
-
-
-
-
-
-
-
I
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
D
2,8
-
3,1
3,0
3,1
3,1
2,9
2,6
2,8
2,7
2,9
3,0
2,8
3,2
2,8
3,1
3,0
3,3
3,1
3,3
3,0
3,1
3,0
3,0
3,0
3,0
3,2
3,0
3,0
2,7
3,1
D RM
Meses
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
NV
V
V
-
NV
-
V
NV
V
-
V
V
-
V
NV
S
201
Tl
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
NV
V
V
-
NV
-
V
NV
V
-
V
V
-
V
NV
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
NV
V
V
-
NV
/
V
NV
V
NV
V
V
-
V
NV
-
V
-
NV
-
NV
NV
V
NV
V
-
NV
-
NV
-
-
NV
-
-
NV
-
NV
-
NV
V
NV
V
V
NV
-
NV
-
-
-
NV
-
-
NV
V
-
-
-
NV
-
-
-
-
-
-
-
-
NV
-
NV
NV
V
NV
-
-
V
-
Regiões Miocárdicas
A
AP
In
L
Repouso -
-
-
-
-
-
-
-
-
-
-
-
NV
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
2,9
-
3,2
3,1
3,2
3,0
3,0
2,7
3,1
2,9
2,7
-
3,0
3,1
2,9
3,3
-
3,0
2,9
3,1
3,2
3,1
3,2
3,1
3,0
3,1
3,1
3,3
3,2
3,1
2,8
3,2
D RM
D Meses
Após a cirurgia de revascularização do miocárdio
D - intervalo de tempo; RM- revascularização do miocárdio; S- septal; A- anterior; Ap- apical; In- inferior; L- lateral; D- dorsal; I- irreversível; R- reversível; V- viável; NV- não viável.
D RM
Meses
No
Convencional
Antes da cirurgia de revascularização do miocárdio
Tabela III - Dados gerais dos resultados obtidos através das cintilografias de perfusão miocárdica.
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
V
V
V
-
NV
-
V
NV
NV
-
V
V
-
V
NV
S
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
V
V
V
-
NV
-
V
NV
NV
NV
V
V
-
V
NV
V
-
V
V
-
NV
NV
-
V
-
V
-
-
NV
NV
NV
-
V
V
V
-
NV
-
V
NV
NV
-
V
V
-
V
NV
-
-
-
NV
-
-
NV
V
-
-
-
NV
-
-
-
-
-
-
-
-
NV
NV
V
-
-
NV
-
-
-
V
-
-
V
-
NV
-
NV
NV
V
NV
V
-
NV
-
NV
-
-
V
-
-
NV
-
NV
-
NV
NV
NV
V
-
V
-
-
Regiões Miocárdicas
A
AP
L
In
Repouso - 99mTc - MIBI
-
-
-
-
-
-
-
-
-
-
-
NV
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
D
Arq Bras Cardiol
volume 72, (nº 5), 1999
Chalela e cols.
Cintilografia na detecção do miocárdio viável
529
Chalela e cols.
Cintilografia na detecção do miocárdio viável
Arq Bras Cardiol
volume 72, (nº 5), 1999
Fig. 3 - Cintilografia de perfusão miocárdica com 201Tl e os cortes tomográficos no plano oblíquo. RM - revascularização do miocárdio. As imagens da redistribuição sugerem viabilidade nas regiões anterior e lateral; as da reinjeção também na parede inferior. Após a RM, as imagens confirmam viabilidade das regiões anterior, inferior e lateral.
Discussão
Nos pacientes com DAC e função do VE diminuída, a
cirurgia de RM tem mostrado um impacto positivo na sobrevida ao longo do tempo. No presente estudo, a sobrevida
no período médio evolutivo de 15,2±10,2 meses foi de
96,6%. Dos 29 pacientes que receberam alta hospitalar, apenas um (3,4%) morreu subitamente.
A presença do miocárdio viável não é o único dado suficiente para indicar a revascularização, mas também a extensão da área que, uma vez recuperada, irá levar mudanças, tanto no quadro clínico como na evolução da história
530
natural após a revascularização. Neste sentido, os benefícios da cirurgia puderam ser confirmados pelo estado funcional da AP e da ICC.
O estudo mostrou ainda, sobrevida hospitalar de
90,6%, sendo que nenhum paciente com FE <20% foi a óbito
nesta fase. Observaram-se 19 pacientes com FE >20% e
<40% dos quais dois foram a óbito no PO imediato, portanto, a sobrevida hospitalar nestes limites da FE foi de 17/19
(89,5%) pacientes, semelhante aos observados na literatura.
Hochberg e cols. 17 estudaram 466 pacientes com DAC e
FEVE <40% submetidos à cirurgia de RM e acompanhados
por um período de 36 meses. A sobrevida hospitalar (até 30
Arq Bras Cardiol
volume 72, (nº 5), 1999
Chalela e cols.
Cintilografia na detecção do miocárdio viável
Fig. 4 - Cintilografia de perfusão miocárdica com 99mTc-MIBI e os cortes tomográficos no plano oblíquo. RM - revascularização do miocárdio. As imagens do protocolo convencional
mostram defeitos persistentes nas regiões anterior, inferior e lateral. Após a RM, as imagens confirmam que estes defeitos persistentes continham músculo viável.
dias após a cirurgia) para os pacientes com FEVE >20% e
<39% foi de 89%. O estudo CASS 18 encontrou benefícios
significantes da cirurgia, em um subgrupo de pacientes com
DAC nos três vasos principais e FEVE entre 35% a 50%. Verificaram, ainda, sobrevida prolongada após a cirurgia de
RM nos pacientes com diminuição da função do VE, particularmente naqueles com FEVE <25%, definindo que a presença de severa falência cardíaca não constitui contra-indicação específica para a cirurgia de RM.
Estes dados, aliados à melhora clínica da adequada sobrevida hospitalar após a alta, são animadores para a realização da cirurgia de RM em pacientes com diferentes graus
de disfunção ventricular esquerda e DAC. No entanto, a
melhora observada após a RM representa uma complexa in-
teração entre mecanismos compensatórios, anatomia coronária, resultados cirúrgicos e seleção dos pacientes.
Quanto mais tardia for a avaliação - dois a três meses
após a cirurgia - tanto mais correta será a interação entre a
recuperação da perfusão e função do VE, injúria peri-operatória e as condições dos enxertos.
O estudo da CPM com 201Tl, mostrou, ao protocolo
convencional, 40/102 (39,2%) regiões, e o da reinjeção 52/
102 (51,0%) regiões com reversibilidade. Portanto, das 62/
102 regiões irreversíveis pelo protocolo convencional, 12/
62 (19,4%) regiões foram reversíveis à reinjeção. Esse achado foi inferior aos da literatura. Vários estudos mostram,
que o protocolo da reinjeção, comparativamente ao convencional com 201Tl, supera em cerca de 31 a 49% os defei531
Chalela e cols.
Cintilografia na detecção do miocárdio viável
Arq Bras Cardiol
volume 72, (nº 5), 1999
Tabela IV - Relação entre a presença e a intensidade da circulação
colateral com as regiões miocárdicas consideradas viáveis pela
cintilografia de perfusão miocárdica
Regiões
Miocárdicas
+/++
N
Viáveis
10
Circulação colateral
+++/++++
%
N
%
40,0
15
P
60,0
Total
25
0,004
Não viáveis
22
78,6
6
21,4
28
Total
32
60,4
21
39,6
53
Fig. 5 - Comportamento da motilidade regional observada, antes e após a revascularização das regiões acometidas pelo infarto do miocárdio. D - discinesia; A - acinesia;
HA - hipocinesia acentuada; HM - hipocinesia moderada; HD - hipocinesia discreta; N - normal.
tos considerados irreversíveis 19-21. No estudo, a menor superestimação da fibrose poderia ser justificada pela metodologia utilizada, uma vez que as imagens da redistribuição
do protocolo convencional foram realizadas em período
mais tardio aos citados.
A superestimação da fibrose (hipocaptação irreversível) ao protocolo convencional comparado ao da reinjeção
com 201Tl, encontra-se na dependência do fenômeno da redistribuição. Logo após a captação inicial de 201Tl pelo miocárdio, há uma contínua troca deste cátion monovalente
com a corrente sangüínea determinando sua redistribuição.
O 201Tl é continuadamente liberado do miocárdio normal e
substituído pelo 201Tl recirculante, a partir da atividade residual da corrente sangüínea. Embora, sua biodistribuição
inicial apresente semelhança com o K+, a redistribuição
compartimental apresenta diferentes velocidades de troca
entre os meios intra e extra-celular. A entrada do 201Tl para o
interior da célula é dependente da oferta regional, como
também da integridade da membrana e da bomba de Na+/K+.
Porém, as alterações metabólicas das células isquêmicas
alteram a taxa de extração e a troca com o meio extracelular.
532
Diferente das células fibróticas, o miocárdio viável guarda
um metabolismo lento que mantém a estrutura celular básica, possibilitando a recuperação de suas funções originais.
Este complexo mecanismo de defesa pode ser detectado
pela metodologia radioisotópica e permite a observação,
por imagem da biodistribuição dinâmica, destes radiofármacos, no músculo cardíaco. O menor acúmulo e washout lento do 201Tl nas áreas isquêmicas, comparados com a maior
velocidade de saída das áreas com perfusão normal, resultam nos defeitos perfusionais. Este processo, baseado na
redistribuição, só pode ocorrer se o miocárdio encontra-se
viável, com a membrana celular intacta 22-24.
No entanto, o fenômeno da redistribuição é altamente
influenciado pela concentração sérica deste traçador e do
washout celular. A redistribuição pode ocorrer mais tardiamente em situações em que exista hipoperfusão em repouso
devida à estenose coronária severa, ausência de hiperemia
após o estresse em conseqüência da isquemia induzida,
anormalidades metabólicas de longa duração e baixa concentração sérica deste radiofármaco 22,25. A lentidão da redistribuição, observada nas áreas de músculo isquêmico
(viável), faz com que as imagens de 3 a 4h apresentem limitações na diferenciação do miocárdio viável e fibrótico.
Com o protocolo convencional usando o 99mTc-MIBI,
o estudo mostrou apenas 14/102 (13,7%) regiões reversíveis, sendo que o com 201Tl identificou 26 (25,5%) regiões reversíveis a mais, e o da reinjeção 38 (37,3%) regiões, quando
comparadas ao protocolo convencional com 99mTc-MIBI.
Portanto, os protocolos com 201Tl foram superiores na
detecção de defeitos reversíveis em áreas acometidas por
IM. Estes dados foram semelhantes aos encontrados na literatura.
Cuocolo e cols. 26 estudaram 20 portadores de DAC e
disfunção VE (FE de 30% + 8%), através da CPM com 201Tl e
99m
Tc-MIBI comparando os protocolos convencionais com
os da reinjeção. Em 122 regiões, que mostraram defeitos
irreversíveis ao protocolo convencional com 201Tl, 57 (47%)
delas foram reversíveis ao protocolo da reinjeção. Em relação ao protocolo convencional com 99mTc-MIBI, observou-se reversibilidade em 22 (18%) regiões. Portanto, o
99m
Tc-MIBI não identificou 35 (29,0%) regiões quando comparado o protocolo da reinjeção. Dilsizian e cols. 27, usando
metodologia similar, encontraram subestimação do protocolo com 99mTc-MIBI em 36% quando comparado ao da
reinjeção. Assim, observa-se que as imagens da reinjeção
com 201Tl identificam maior número de regiões miocárdicas
com viabilidade em relação ao 99mTc-MIBI.
Trabalhos clínicos e experimentais já demonstraram
que, no tecido normal, logo após a extração inicial, o 99mTcMIBI se fixa na célula miocárdica, apresentando mínima
redistribuição mais tardiamente. Quando ocorre despolarização das membranas celulares e mitocondrias, tal como
ocorre no fenômeno isquêmico, há dificuldade na captação
e no armazenamento deste traçador 28,29. Possivelmente,
graus mais importantes de alterações metabólicas diminuem
a capacidade da extração (transporte passivo) do 99mTcMIBI. Por outro lado, a manutenção da bomba de Na+/K+
Arq Bras Cardiol
volume 72, (nº 5), 1999
Chalela e cols.
Cintilografia na detecção do miocárdio viável
ATPase, importante fator para a sobrevivência celular, pouco interferiria na extração do 201Tl (transporte ativo).
Pôde-se verificar pelo estudo estatístico, que o protocolo da reinjeção foi a melhor abordagem para a detecção do
miocárdio viável e que houve importante depreciação do
99m
Tc-MIBI em comparação ao 201Tl para identificação de
viabilidade miocárdica.
A tomografia por emissão de pósitrons 30 (PET) é considerada a técnica não invasiva mais sensível na identificação do miocárdio viável e tem sido utilizada para comparação com outros métodos. Vários estudos 20,31 demonstraram
que a captação de 201TI, após a reinjeção é tão sensível
quanto as imagens do PET com 18-F- deoxiglicose (FDG) na
detecção de viabilidade. A concordância entre os resultados foram de 88% para o 1º estudo e de 85% no 2º. Outros
estudos 19,20,32-34 mostraram valores preditivos semelhantes,
tendo como padrão, a recuperação funcional observada
após a revascularização: VPP de 78% a 85% para o PET, e de
73% a 87% para o protocolo da reinjeção; o VPN de 80% a
92% para o PET, e de 75% a 100% para o protocolo da reinjeção. No presente estudo, encontraram-se, ao protocolo da
reinjeção, valores preditivos semelhantes: positivo de
83,3% e negativo de 80,0%, usando-se como modelo a restauração da perfusão verificada pela maior captação dos
cardiócitos, após a revascularização cirúrgica.
Foi encontrada relação significativa entre a recuperação da perfusão dos cardiócitos e a da função sistólica regional (p = 0,011) após a revascularização das áreas comprometidas pelo IM.
Este dado foi relevante para se verificar que as anormalidades metabólicas em conseqüência direta da inadequada perfusão foram recuperadas após a restauração do
fluxo coronário. Miocárdio com disfunção contrátil crônica
não é suficiente para indicar a revascularização. A presença e a extensão da área potencialmente recuperável - miocárdio viável - aliada à adequada anatomia coronária, poderão
levar a mudanças no quadro clínico após revascularização.
A cinecoronarioventriculografia, apesar de suas limitações, tem sido utilizada para a avaliação da precisão diagnóstica dos métodos que estudam a isquemia miocárdica
devido, provavelmente, à carência de outra metodologia,
mais objetiva e precisa, na identificação de DAC. Ela também
oferece inúmeros problemas relativos à possibilidade de
subestimação ou superestimação de lesões coronárias 35. A
angiografia quantitativa computadorizada 36 parece ser mais
objetiva que a estimativa visual, mas também apresenta divergências entre as várias metodologias utilizadas (método
densitométrico e método geométrico), especialmente,
quando se analisam placas instáveis e excêntricas. Existe a
possibilidade de o grau de estenose anatômica não significar o estado do fluxo coronário em situações particulares
como durante o estresse cardíaco 37,38.
As avaliações da perfusão e da função sistólica do VE
apresentam algumas limitações, especialmente no que se
refere à inexistência de metodologia quantitativa precisa e
de uso prático. A melhor forma de quantificação disponível
para a prática, atualmente, é o método semiquantitativo de
graduação. Portanto, o método é observador dependente,
acarretando variações intra e inter-observadores comuns
para a maioria dos métodos diagnósticos.
Neste estudo, a variabilidade intra e inter-observador
foi na seqüência de 4,6% e de 7% para a coronariografia; de
3% e 4% para a cineventriculografia esquerda; de 2% e 4%
para o TE; de 4% e 5,1% para a CPM.
Apesar destas limitações, as variabilidades intra e
inter-observadores foram aceitáveis. A CPM e a cinecoronarioventriculografia com quantificação visual são práticas
aceitas e realizadas na imensa maioria dos centros médicos.
Agradecimentos
Aos Profs. Drs. José A. Marin-Neto e Giovanni
Bellotti, às equipes cirúrgicas dos Profs. Drs. Adib D.
Jatene e Sergio A. Oliveira e do serviço de radioisótopos do
Incor-HCFMUSP, pela colaboração recebida.
Referências
1.
2.
3.
4.
5.
6.
7.
Franciosa JA, Wilen M, Ziesche S, Cohn JN. Survival in men with severe chronic
left ventricular failure due to either coronary heart disease or idiopathic dilated
cardiomyopathy. Am J Cardiol 1983; 51: 831-6.
Primo G, Le Clerc JL, Goldstein JP, De Smet JM, Joris MP. Cardiac transplantation
for the treatment of end-stage ischemic cardiomyopathy. Adv Cardiol 1988; 36:
293-7.
Kriett JM, Kaye MP. The registry of the international society for heart transplantation: seventh official report - 1990. J Heart Transplant 1990; 9: 323-30.
Iskandrian AS, Shelbert HR. Myocardial viability assessment. J Nucl Med
1994a; 35(suppl): 1S-3S.
Lucas JR, Botvinick EH, Dae MW. Myocardial viability: evidence provided by the
analysis of left ventricular systolic function. Coron Artery Dis 1993; 4: 485-94.
New York Heart Association: the criteria committee. Inc: Diseases of the heart
and blood vessels. nomenclature and criteria for diagnosis 6th ed. Boston: Little
Brown, 1964.
Braunwald E. Heart Disease. A Textbook of Cardiovascular Medicine. 5th ed.
Philadelphia: WR Saunders Co, 1996.
8.
9.
10.
11.
12.
13.
14.
15.
Tranchesi J. Eletrocardiograma Normal e Patológica. Noções de Vectorcardiografia. 6ª ed. São Paulo: Editora Athenas, 1983: 724.
Arie S. Circulação colateral com fator de proteção do miocárdio em portadores de
insuficiência coronária crônica (Tese mestrado). São Paulo: Faculdade de Medicina da Universidade de São Paulo, 1977: 53.
Dodge HT, Sandler H, Bellew BW, Lord Jr JD, Seatle W. The use of biplane angiography for the measurement of left ventricular volume in man. Am Heart J 1960; 60: 762.
Kennedy JW, Baxley WA, Figley MN. Quantitative angiography. The normal left
ventricle in man. Circulation 1966, 34: 272.
Consenso Nacional de Ergometria. Florianópolis, SC. Arq Bras Cardiol 1995;
65: 189-211.
Ellestad MA. Stress Testing. Principles and Practice. 3rd ed. Philadelphia: Daves
Company, 1986: 526.
Rosner B. Fundamentals of Biostatistics - 2nd ed. Boston: PWS Publishers,
1986: 584.
Fleiss JL. Statistical Methods for Rates and Proportions. New York: John Wiley
& Sons, 1981: 325.
533
Chalela e cols.
Cintilografia na detecção do miocárdio viável
16. SAS Institute Inc., SAS/STAT User’s Guide, Version 6, 4th ed, vol. 2, Cary, NC:
SAS Institute Inc., 1989: 1686.
17. Hochberg MS, Parsonnet V, Gielchinsky I, Hussain SM, Newark NJ. Coronary
artery bypass grafting in patients with ejection fractions below forty percent. J
Thorac Cardiovasc Surg 1983; 86: 519-27.
18. Coronary Artery Surgery Study (CASS): a randomized trial of coronary artery
bypass surgery: survival data. Circulation 1983; 68: 939-50.
19. Dilsizian V, Rocco T, Freedman N, Martins BL, Bonow RO. Enhanced detection
of ischemic but viable myocardium by the reinjection of tlhallium after stressredistribution imaging. N Engl J Med 1990; 323: 141-6.
20. Tamaki N, Ohtani H, Yamashita K, et al. Metabolic activity in the areas of new fillin after thallium-201 reinjection: comparison with positron emission tomography using fluorine-18-deoxyglucose. J Nucl Med 1991; 32: 673-8.
21. Hendel RC. Single-photon perfusion imaging for the assessment of myocardial
viability. J Nucl Med 1994; 35: 235-315.
22. Strauss HW, Harrison K, Langan JK, Lebowitz E, Pitt B - Thallium-201 for
myocardial imaging: relation to thallium-201 to regional myocardial perfusion.
Circulation 1975; 51: 641-5.
23. Weich HF, Strauss W, Pitt B. The extraction of thallium-201 by the myocardium.
Circulation 1977; 56: 188-97.
24. Pohost GM, Alpert NM, Ingwall JS, Strauss W. Thallium-201 redistribution:
mechanism and clinical utility. Semin Nucl Med 1980; 10: 70-93.
25. Camici P, Araujo LI, Spinks T, et al. Increase uptake of 18F-fluorodeoxyglucose in
post-ischemic myocardium in patients with exercise induced angina. Circulation
1986; 74: 81-6.
26. Cuocolo A, Pace L, Ricciardelli B, Chiariello M, Trimarco B, Salvatore M. Identification of viable myocardium in patients with chronic coronary artery disease:
comparison of thallium-201 scintigraphy with reinjection and technetium-99m
methoxyisobutyl isonitrile. J Nucl Med 1992; 33: 505-11.
27. Dilsizian V, Arrighi JA, Diodati JG, et al. Myocardial viability in patients with
chronic coronary artery disease: comparison of Tc-99m MIBI with Thallium
reinjection and F-18 fluorodeoxyglucose. Circulation 1994; 89: 578-87.
534
Arq Bras Cardiol
volume 72, (nº 5), 1999
28. Okada RD, Glover D, Gaffney T, Williams S. Myocardial kinetics of technetium99m hexakis-2-methoxy-2-methypropyl-isonitrile. Circulation 1988; 77:
491-8.
29. Sinusas AJ, Watson DD, Cannon JM, Jr ME, Beller GA. Effect of ischemia and
postischemic dysfunction on myocardial uptake of technetium-99m labeled
methoxyisobutyl isonitrile and thallium-201. J Am Coll Cardiol 1989; 14:
1785-93.
30. Gropler RJ, Bergmann SR - Myocardial viability- what is the definition? J Nucl
Med 1991; 32: 10-2.
31. Bonow RO, Dilsizian V, Cuocolo A, Bacharach SL. Identification of viable myocardium in patients with coronary artery disease and left ventricular dysfunction: comparison of thallium scintigraphy with reinjection and PET imaging
with 18F-fluorodeoxyglucose. Circulation 1991; 83: 26-37.
32. Tillisch J, Brunken R, Marshall R, et al. Reversibility of cardiac wall-motion abnormalities predicted by position tomography. N Engl J Med 1986; 314: 884-8.
33. Tamaki N, Yonekura Y, Yamashita K, Saji H, Magata Y, Senda M. Position
emission tomography using fluorine-18-deoxglucose in evaluation of coronary
artery bypan grafting. Am J Cardiol 1989; 64: 860-5.
34. Ohtani H, Tamaki N, Yonekura Y, et al. Value of thallium-201 reinjection after
delayed SPECT imaging for predicting reversible ischemia after coronary artery
bypass grafting. Am J Cardiol 1990; 66: 394-9.
35. Fleming RM, Kiekeeide RL, Gould KL. Patterns in visual interpretation of
coronary arteriograms as detected by quantitative coronary angiography. J Am
Coll Cardiol 1991; 18: 945-51.
36. Rodrigues AS, Santaera O, Fernandez M, et al. - Digital coronaryangiography: a new
approach in the analysis of atherosclerotic plaque. Medicine 1991; 51: 209-16.
37. Meyer SL, Dousk GCM, Twieg DB - Influence of dobutamine on hemodynamias
and coronary blood flow in patients with and withont coronary artery disease.
Am J Cardiol 1976; 38: 103-8.
38. White CW, Wright CB, Doty DB, et al. Does visual interpretation of the coronary
arteriogram predict the physiologic importance of a coronary stenosis? N Engl
J Med 1984; 310: 819-24.