Mecanismo de ação das incretinas e o potencial terapêutico de
moléculas relacionadas no tratamento do diabetes mellitus tipo 2
Cristiana Ferreira de Brito*
Elainy Rodrigues de Oliveira Lima*
Juliane Aparecida de Oliveira*
Linara Cristhinni Scotta Merlo*
Nayara Temponi Campos*
Flávia Lúcia Abreu Rabelo**
RESUMO
As incretinas GLP-1 e GIP são hormônios produzidos pelo trato gastrointestinal e
liberados no intestino em resposta à ingestão de alimentos. Desempenham importante
papel na modulação da atividade das células β-pancreáticas, com isso potencializam a
secreção de insulina, além de aumentar a sensibilidade dos seus tecidos-alvo. Como
estratégia para favorecer o prolongamento dos efeitos das incretinas, tem sido
desenvolvidas substâncias análogas ao GLP-1 que mimetizam sua ação (exenatida e
liraglutida) e inibidores da enzima que degrada as incretinas (sitagliptina e
vildagliptina). Estudos clínicos mostram que a administração desses fármacos, em
monoterapia ou associados a outros medicamentos antihiperglicêmicos, é eficaz no
controle glicêmico e na redução de peso em pacientes com DM2. Esta revisão tem foco
no mecanismo de ação das incretinas sobre as células pancreáticas e possíveis ações
terapêuticas para o tratamento do diabetes mellitus tipo 2.
PALAVRAS-CHAVE: Incretinas; Vias de sinalização; Diabetes mellitus tipo 2;
Análogos de GLP-1; Inibidores da DPP-4
ABSTRACT
Incretins GLP-1 and GIP are hormones produced by the gastrointestinal tract and
liberated in the intestine, in response to the ingestion of food. They fulfill important role
in the modulation of the response of cells of the pancreatic islets to the ingestion of
food, thus they potentialize the insulin secretion by the pancreatic β-cells, beyond
increasing the sensibility of the target tissues to the insulin. As strategy to favour the
prolongation of incretins effects have been developed GLP-1 analogs mimetics
(exenatide and liraglutide) and enzyme inhibitors of the incretins degradation
(sitagliptin and vildagliptin). Clinical trials have shown incretins based drugs
administration, on monoterapy or in association with other anti-hyperglicemic drugs, to
be efficacious in glycemic control and weight loss in patients with type 2 diabetes. This
review focuses in the action mechanism of incretin on pancreatic cells and possible
therapeutic target for the treatment of diabetes mellitus type 2.
KEYWORDS: Incretins; Signalling pathways; Diabetes mellitus type 2; GLP-1 analogs;
DPP-4 inhibitors.
INTRODUÇÃO
* Farmacêuticas egressas da Universidade Vale do Rio Doce - UNIVALE, Governador Valadares, Minas
Gerais, Brasil; ** Professora Doutora em Bioquímica pela Universidade Federal de Minas Gerais UFMG, Belo Horizonte, Minas Gerais, Brasil; Docente dos cursos de Enfermagem e Farmácia da Nova
Faculdade, Contagem, Minas Gerais, Brasil; [email protected]
O diabetes mellitus tipo 2 (DM2) é causado por redução da sensibilidade dos
tecidos-alvo aos efeitos metabólicos da insulina, condição descrita como resistência à
insulina. Em contraste com o diabetes mellitus tipo 1 (DM1), o DM2 está associado ao
aumento da concentração plasmática de insulina, que ocorre como resposta
compensatória das células do pâncreas, devido à diminuição da utilização e
armazenamento dos carboidratos. Entretanto, mesmo os níveis aumentados de insulina
não são suficientes para manter a regulação normal da glicose, devido à acentuada
redução da sensibilidade dos tecidos periféricos à insulina. (GUYTON & HALL, 2006,
p. 831-832).
O processo de digestão e absorção dos alimentos nos mamíferos ocorre
principalmente no intestino, que funciona também como um órgão de liberação de
hormônios denominados incretinas, que desempenham importante papel na modulação
da resposta das células das ilhotas pancreáticas, capazes de potencializar a secreção de
insulina, e consequentemente, levar à diminuição de glucagon. Elas ajudam a baixar as
taxas de glicose no sangue, sobretudo depois das refeições, quando esses níveis tendem
a aumentar. (DOYLE & EGAN, 2007, p. 14; NELSON & COX, 2006, p. 895-896).
Os dois principais hormônios incretinas são polipeptídeo inibitório gástrico
(GIP) e peptídeo 1 tipo glucagon (GLP-1), que pertencem a uma super-família do
peptídeo glucagon, e como tal, existe alguma homologia da sequência de aminoácidos
entre esses peptídeos e o glucagon. O hormônio predominante é o GLP-1 que, além de
estimular a secreção de insulina, suprime a liberação de glucagon, desacelera o
esvaziamento gástrico, diminui a ingestão de alimentos e a resistência à insulina.
(CHACRA, 2006, p. S613-S614, GUPTA, 2012, p. S47-S48).
Em estudos realizados nos anos 60, por Nauck e colaboradores, a administração
de glicose por via oral mostrou ser capaz de causar resposta de insulina maior do que a
observada com a infusão de glicose por via endovenosa (EV), apesar dos níveis
sanguíneos mais altos de glicose consequentes da administração EV. Esse fato é
conhecido como efeito incretina, que significa que a ingestão de glicose estimula a
liberação de incretinas pelo intestino, esses hormônios aumentam a secreção de insulina,
além da secreção induzida apenas pela glicose absorvida. Do mesmo modo, o grau de
secreção de incretinas depende da quantidade de glicose ingerida e as incretinas são
responsáveis por aproximadamente 75% da resposta da insulina depois da ingestão de
50g de glicose. (CHACRA, 2006, p. S615; NAUCK et al., 1986 apud DOYLE &
EGAN, 2007, p. 1).
Há inúmeros interesses nos mecanismos responsáveis pela rápida melhora do
diabetes mellitus (DM) que é conseguida principalmente após o tratamento cirúrgico,
onde são aproximadas partes do íleo ao estômago de modo a intensificar a secreção de
incretinas, que consequentemente levará a uma maior secreção de insulina, captando
maior quantidade de glicose da corrente sanguínea e controlando a glicemia. Apesar de
sua eficácia, esse é um método invasivo e de alto custo, o que leva ao investimento na
terapêutica medicamentosa com substâncias que favoreçam a ação das incretinas. Para o
desenvolvimento desses fármacos faz-se necessário o conhecimento do mecanismo de
ação e das vias de sinalização das incretinas e suas relações com secreção de insulina e
com consequente normalização da glicemia em indivíduos portadores de DM2.
(MARTINS & SOUZA, 2007, p. 344).
1 INCRETINAS
O intestino, além de promover a digestão e a absorção dos alimentos, produz
hormônios, denominados incretinas, capazes de potencializar a secreção de insulina e
consequentemente levar à diminuição de glucagon. Elas ajudam a baixar as taxas de
glicose no sangue, sobretudo após as refeições, quando esses níveis tendem a aumentar.
(DOYLE & EGAN, 2007, p. 1-2; 14; GALLWITZ, 2005, p. 61-62).
A hipótese da existência de incretinas foi postulada na década de 30, mas
somente na década de 60 foram reconhecidas como hormônios insulinotrópicos. Em
1986, Nauck e colaboradores postularam que essas substâncias eram originadas no
intestino, liberadas devido à ingestão de grande quantidade de nutrientes, pois
aumentavam a secreção de insulina. Nesse estudo, também foi possível verificar que,
após a ingestão oral de glicose, 75% da sua absorção era devido à secreção de incretinas
(NAUCK et al., 1986, apud DOYLE & EGAN, 2007, p.1).
Os dois principais hormônios incretinas são: o GIP e GLP-1 (BOSI, 2008, p.
102; DOYLE & EGAN, 2007, p. 1-2; GUPTA, 2012, p. S47).
O GIP é um peptídeo de 42 aminoácidos, clivado de seu precursor Pro-GIP
secretado a partir do trato gastrointestinal no duodeno e jejuno pelas células K após a
ingestão de nutrientes. GIP age rapidamente sobre células β-pancreáticas para estimular
a liberação de insulina, e assim, garantir a rápida absorção de glicose pelos tecidos.
Além disso, GIP promove a remoção de triglicerídeos da circulação, processo
parcialmente mediado pela sua capacidade de estimular a atividade da lipase
lipoprotéica, que é uma enzima que converte triglicerídeos em ácidos graxos,
permitindo sua captação pelos tecidos periféricos. (FULURIJA, 2008, p.1,; GUPTA,
2012, p. S51).
O GLP-1 é um peptídeo de 36 aminoácidos, secretado na corrente sanguínea
pelas células L enteroendócrinas, encontradas principalmente no íleo e no cólon do
intestino (FULURIJA, 2008, p. 6). GLP-1 inibe a secreção de glucagon e o
esvaziamento gástrico, conducentes à redução da glicemia e aumenta a concentração das
células β mesmo em indivíduos com diabetes tipo 1. GLP-1 é reconhecido como um
potenciador da secreção induzida de insulina que contribui substancialmente para seu
efeito. (CHIA & EGAN, 2008, p. 3703-3704; GALLWITZ, 2005, p. 62; HANSOTIA,
2007, p.143).
2 MECANISMO de ação das incretinas
Quando
a
glicose
sanguínea
aumenta,
no
período
pós-prandial,
os
transportadores GLUT1 e GLUT2 presentes na membrana das células β-pancreáticas
captam este carboidrato para equilibrar suas concentrações do lado externo e interno da
membrana. No interior da célula, a glicose é rapidamente fosforilada a glicose-6-fosfato
pela glicoquinase, que determina a velocidade da glicólise, ou seja, ativa a geração de
piruvato e sua entrada no ciclo do ácido cítrico. Subsequente, o metabolismo oxidativo
fornece a ligação entre os produtos do metabolismo da glicose e a secreção da insulina.
O aumento da relação citoplasmática adenosina trifosfato (ATP)/adenosina difosfato
(ADP) decorrente da glicólise aeróbica causa despolarização da membrana plasmática
através do fechamento dos canais de K+ sensíveis ao ATP (KATP). Isso permite a
abertura dos canais de Ca2+ voltagem-dependentes levando à liberação dos estoques
intracelulares de Ca2+. Esse aumento na concentração citosólica de Ca2+ desencadeia a
fusão das vesículas secretoras que contêm insulina à membrana plasmática com rápida
exocitose desse peptídeo. (DOYLE & EGAN, 2007, p. 14).
Então, o processo de exocitose aguda de insulina pode ser dividido em duas vias:
1) a via inicialmente desencadeada, onde ocorre o fechamento dos canais de KATP,
despolarização e aumento nas concentrações intracelulares de Ca2+; e 2) a via
amplificadora, onde há um aumento na exocitose das vesículas secretoras de insulina
induzida por Ca2+. As incretinas são capazes de ativar essas vias, por meio de sua
ligação a receptores específicos e a consequente ativação de moléculas citoplasmáticas
sinalizadoras. Além disso, a contínua ativação do receptor de GLP-1 (GLP-1R) também
aumenta a síntese de insulina e a proliferação de células β (DOYLE & EGAN, 2007, p.
14-19).
2.1 RECEPTORES de incretinas nas células β-pancreáticas
Os receptores para GLP-1 e GIP são da classe dos receptores acoplados à
proteína G (GPCRs). Assim como outros receptores desse tipo, possuem sete domínios
α-helicoidais transmembrana (TM1-TM7), três alças extracelulares (EC1, EC2, EC3),
três alças intracelulares (IC1, IC2, IC3), um grupo amino terminal extracelular e um
domínio carboxilo terminal intracelular. (DOYLE & EGAN, 2007, p. 2-3).
As proteínas G contêm três subunidades, uma das quais se encontra ligada à
guanosina difosfato (GDP). Quando uma proteína G se liga a um receptor ativo, a sua
subunidade α sofre uma mudança conformacional e troca o seu GDP por um guanosina
trifosfato (GTP). A subunidade α, quando ligada ao GTP, separa-se das outras
subunidades, torna-se capaz de ativar diferentes mecanismos de transdução de sinal.
(DOYLE & EGAN, 2007, p. 4; HOLST & GROMADA, 2004, p. E200).
GPCRs estão agrupados em cinco famílias principais baseadas na similaridade
estrutural e sequencial: família A (rodopsina), B (secretina), C (glutamato), adesão e
"frizzled/taste". (ROSENBAUM, RASMUSSEN & KOBILKA, 2009, p. 356)
O GLP-1R é um membro da classe B e consiste em uma proteína de 64 kDa.
Dentro da classe B, os receptores para os hormônios peptídicos formam uma subclasse
de receptores da família glucagon, que também incluem receptores de glucagon, GLP-2,
GIP, liberador do hormônio do crescimento (GHRH) e secretina. No entanto, a ligação
das incretinas aos seus receptores é muito específica sem qualquer reatividade cruzada
relevante a receptores para outros peptídeos, com exceção do glucagon, que se liga a
GLP-1R, mas com 100-1000 vezes menos afinidade do que a GLP-1. (DOYLE &
EGAN, 2007, p. 2).
2.2 VIAS de sinalização ativadas pelas incretinas
Muitos estudos têm sido feitos com objetivo de elucidar as vias de sinalização
ativadas pelas incretinas nas células β-pancreáticas após sua interação com os
receptores. Entretanto, as investigações estão mais concentradas no GLP-1. Apesar
disso, alguns autores consideram que GLP-1 e GIP compartilham de mecanismos de
ação muito semelhantes. (DOYLE & EGAN, 2007, p. 1; 14; HOLST & GROMADA,
2004, p. E202-E203).
O GLP-1R é acoplado à subunidade Gαs e, portanto, envolvimento com o
ligante agonista resulta em ativação de adenilato ciclase (AC), com formação de AMP
cíclico (cAMP), que ativa proteína quinase A (PKA) que é um componente chave na
regulação da secreção de insulina, uma vez que essa enzima é responsável por várias
reações de fosforilação necessárias para a atividade secretora das células β. A cascata de
sinalização induzida pelas incretinas também envolve uma via independente de PKA,
mas induzida por cAMP, que é a ativação de moléculas conhecidas como proteínas de
troca diretamente associadas à cAMP (EPAC), também denominadas cAMP-GEFs
(“cAMP-regulated guanine nucleotide exchange factors”). Essas moléculas são
proteínas quinase efetoras que fosforilam polipeptídeos da família Ras. A ativação das
vias PKA e EPAC induzida por GLP-1 leva a uma multiplicidade de acontecimentos,
incluindo alteração da atividade dos canais iônicos, movimentação de cálcio
intracelular, e reforça a exocitose, contendo grânulos de insulina (DOYLE & EGAN,
2007, p. 10-11; HOLST & GROMADA, 2004, p. E200).
GLP-1, ao se ligar no receptor GLP-1R, provoca um aumento do cAMP, isso
leva à ativação de ambos PKA e EPAC. Moderadas concentrações de cAMP levam
preferencialmente à ativação de PKA, enquanto maiores concentrações favorecem a via
EPAC. Níveis aumentados de cAMP incrementam os níveis de ATP como
consequência da ativação da glicólise provocada pela ação de PKA sobre as enzimas
glicolíticas. Mantidos os aumentos de cAMP pela ativação de GLP-1R, haverá a
translocação de PKA ao núcleo onde promova a modulação de PDX-1 (“pancreatic and
duodenal homebox 1”) e a ativação de CREB (“cAMP response element binding”) com
consequente transcrição de insulina. Além disso, na secreção aguda de insulina, PKA e
EPAC atuam sobre os canais KATP e canais de K+ voltagem-dependentes (Kv), as
vesículas secretoras de insulina e canais IP3/Ca2+ no retículo endoplasmático (DOYLE
& EGAN, 2007, p. 10-11). Alguns dos eventos que se seguem à ligação das incretinas a
seus receptores e que dependem de cAMP estão representados na figura 1.
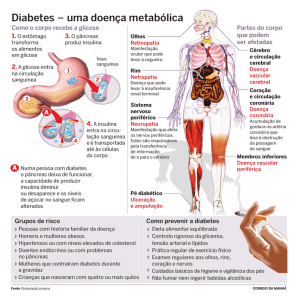
Fig. 1 - Representação esquemática das principais vias de sinalização ativadas pela
ligação das incretinas a seus receptores nas células β-pancreáticas. (AC: adenilato
ciclase; ADP: adenosina difosfato; ATP: adenosina trifosfato; cAMP: adenosina
monofosfato cíclica; CREB: proteína
elemento-ligante responsiva a cAMP;
EPAC: proteína de troca ativada por cAMP; G: proteína G; GIP: polipeptídeo
inibitório gástrico; GLP: peptídeo tipo glucagon; I: insulina; IP: fosfatidil inositol;
IRS: substrato do receptor de insulina; PDX: fator promotor de insulina; PKA:
proteína quinase dependente de cAMP; RE: retículo endoplasmático.) Fonte:
Adaptado de HOLST & GROMADA, 2004, p. E200; DOYLE& EGAN, 2008, p.
73.
A ligação de GLP-1 a seu receptor também ativa as vias Ca2+/Calmodulina,
proteínas quinases ativadas por mitógenos (MAPquinases) e fosfatidil inositol-3
quinases (PI3 quinases) que também podem ter relação com a estimulação da secreção
de insulina mediada pelas incretinas. Finalmente, a produção de ATP reforçada pelo
aumento da mobilização de Ca2+, que por sua vez atua sobre desidrogenases
mitocondriais, leva ao aumento da atividade de mTOR (“mammalian target of
rapamycin”) e seus efetores S6K1 (“p70 ribosomal protein S6 kinase 1”). mTOR está
implicado em aumento da mitose de células β. A ativação de GLP-1R também leva à
estabilização da transcrição de insulina, estimulando a translocação núcleocitoplasmática de proteína de ligação à polipirimidina (PTB) que se liga a regiões ricas
em uracila do RNA mensageiros (mRNAs), que codificam a insulina e proteínas das
vesículas secretoras de insulina, estabilizando estes mRNAs (DOYLE & EGAN, 2007,
p. 14).
2.3 INATIVAÇÃO das incretinas
GIP e GLP-1 têm sua atividade suprimida após clivagem catalisada pelo
dipeptidil peptidase-4 (DPP-4). DPP-4, originalmente conhecida como marcador CD26
da superfície celular de linfócitos ou proteínas de ligação à adenosina desaminase
(ADA), é uma complexa enzima, acoplada na superfície da membrana celular que
transmite sinais intracelulares através de uma pequena cauda intracelular e apresenta-se
também como uma forma menor e solúvel presente na circulação. (CHIA & EGAN,
2008, p. 3710; DRUCKER, 2007, p. 1335-1336; HERMAN et al., 2006, p. 4617).
DPP-4 é uma serina protease constituída de 766 aminoácidos que cliva
preferencialmente hormônios peptídeos contendo dois resíduos de alanina ou prolina
subsequentes. GIP e GLP-1 são substratos endógenos fisiológicos para DPP-4, e esta
tem sua ação mediada pelo aumento dos níveis dos hormônios, sendo uma enzima
amplamente expressa, que circula livremente ou se liga à membrana celular na maioria
dos tecidos, incluindo o trato gastrointestinal, o fígado, os rins, os linfócitos e as células
endoteliais. A DPP-4 inativa o GLP-1 e o GIP ao clivar os peptídeos na região amino
terminal e induzir a formação de dois metabólitos, GLP-1 (aminoácidos 9-36) e GIP
(aminoácidos 3-42). É essa rápida degradação pela DPP-4 que limita os efeitos do GLP1 e do GIP na homeostase da glicose. (CHIA & EGAN, 2008, p. 3710-3711;
DRUCKER, 2007, p. 1335-1336).
Tem sido demonstrado que níveis circulantes de DPP-4 são maiores em
indivíduos com hiperglicemia crônica e diabetes tipo 2, no entanto, se a atividade de
DPP-4 circulante está correlacionada aos níveis plasmáticos de GLP-1 ativo em
humanos não é conhecido. (DRUCKER, 2007, p. 1335).
3 TRATAMENTO do diabetes baseado nas ações dos hormônios incretinas
Ainda que não exista uma cura definitiva para o DM, os pacientes podem ter
uma vida longa e saudável se seguirem com atenção e cuidado o tratamento. O diabético
tipo 2, muitas vezes, consegue compensar sua doença apenas com dieta. Muitos
pacientes obesos mantêm-se totalmente compensados apenas chegando a seu peso ideal.
Outros, porém, necessitam de medicamentos para estabilizar os níveis de açúcar no
sangue. (HERMAN et al., 2006, p. 4612-4613; INZUCCHI et al., 2008, p. 576).
Uma nova categoria de antihiperglicêmicos, baseada na terapia da modulação do
sistema incretinas tem surgido recentemente. Estratégias terapêuticas para o DM2
relacionadas às incretinas incidem sobre a utilização de análogos do GLP-1 (liraglutida
e exenatida) e dos inibidores de DPP-4 (vidalgliptina e sitagliptina) (HERMAN, 2006,
p. 4612; INZUCCHI et al., 2008, p. 580-581).
A eficácia e segurança desses fármacos têm sido claramente demonstradas por
um grande número de ensaios clínicos como a redução da hemoglobina glicosilada
(HbA1c) no jejum e pós-glicose e, em alguns casos, os fármacos apresentam ainda um
efeito favorável sobre a redução do peso. Além disso, a baixa taxa de eventos
hipoglicêmicos vista em estudos com esses fármacos fortalece as evidências de sua
aplicabilidade. (CHIA & EGAN, 2008, p. 3708-3710; INZUCCHI et al., 2008, p. 577578). Alguns estudos mostram ainda que a estimulação dos receptores GLP-1R possui
efeitos cardioprotetores, promove a diminuição da pressão arterial, inibe o acúmulo de
monócitos/macrófagos na parede arterial e aumenta os níveis séricos de HDL. (GUPTA,
2012, p. S51).
3.1 ANÁLOGOS do GLP-1
As primeiras experiências com o GLP-1, administrado EV, foram animadoras e
confirmaram o potencial para terapias com incretinas no tratamento de diabetes. No
entanto, ficou claro desde o início que o GLP-1 em si foi impróprio para uso
terapêutico, devido à sua meia vida muito curta, secundária à rápida inativação pela
enzima DPP-4. (BOSI et al., 2008, p. 103-104).
Os análogos do GLP-1 são uma nova classe de agentes farmacológicos, com
ações antihiperglicêmicos, que mimetizam os efeitos de incretinas endógenos, inclusive
o aumento da secreção de insulina dependente de glicose. Vários análogos de GLP-1,
que foram desenvolvidos a partir das incretinas, se mostraram resistentes à degradação.
por DPP-4 (HINNEN et al., 2006, p. 614-615, GUPTA, 2013, p. 415).
A figura 2 ilustra as estruturas dos principais análogos de GLP-1 desenvolvidos
para o tratamento do diabetes, exenatida e liraglutida.
Fig. 2 - Estrutura da GLP-1 nativa, exenatida e liraglutida. O
dipeptídeo N-terminal “HA” da GLP-1 é clivado pela DPP-4.
(Fonte: Adaptado de CHIA & EGAN, 2008, p. 3704)
A exenatida é a versão sintética da exendina-4 que é um peptídeo de 39
aminoácidos, isolado a partir da secreção da glândula salivar do lagarto Gila Monster
(Heloderma suspectum). A exenatida tem 53% de sequência homóloga ao GLP-1
humano e possui uma alta afinidade pelo receptor análogo de GLP-1. Esse peptídeo não
possui um aminoácido alanina na posição 2, que direciona a clivagem do DPP-4,
tornando-o mais estável proteoliticamente que o GLP-1. Sendo assim, a sua ação é
devido à sua semelhança estrutural com GLP-1, mas esta forma sintética tem uma maior
duração de ação. (BOSI et al., 2008, p. 103; CHIA & EGAN, 2008, p. 3704; GUPTA,
2013, p. 415-416).
A semelhança estrutural entre exenatida e GLP-1 confere ao fármaco seus
efeitos insulinotrópicos através de sua ligação ao GLP-1R, nas células β-pancreáticas.
(SCHNABEL, WINTLE & KOLTERNAN, 2006, p. 70).
A exenatida foi aprovada em abril de 2005 pelo FDA (Food and Drug
Administration), como adjuvante no controle glicêmico de pacientes com DM2 em uso
de metformina, sulfoniluréia, ou uma combinação de metformina e sulfoniluréia.
Ensaios randomizados têm mostrado que a exenatida foi eficaz na melhoria do controle
glicêmico em combinação com a metformina ou sulfoniluréia. Raramente foi observado
hipoglicemia em pacientes tratados com essas combinações. (BOND, 2006, p. 281;
EDWARDS, 2004, p. 271; SCHNABEL, WINTLE & KOLTERNAN, 2006, p. 71).
Inicialmente, a dose de exenatida utilizada é 5 mcg por via subcutânea duas
vezes por dia, 60 minutos antes do café da manhã e jantar, podendo ser ajustada a 10
mcg por via subcutânea, duas vezes por dia, para alcançar um melhor resultado após 1
mês de tratamento. (BOND, 2006, p. 283; EDWARDS, 2004, p. 272; GREEN &
FLATT, 2007, p. 500; SCHNABEL, WINTLE & KOLTERNAN, 2006, p. 72).
A absorção da exenatida atinge a concentração plasmática média 2,1 horas
após a injeção subcutânea e esta droga é primariamente eliminada por filtração
glomerular seguida da degradação proteolítica, com uma meia-vida de eliminação de
2,4 horas. Em pacientes com insuficiência renal leve a moderada, a eliminação não é
consideravelmente reduzida, não sendo necessário o ajuste de dose. Já em pacientes
com insuficiência renal grave, a utilização da exenatida é contraindicada, pois sua meia
vida é significativamente reduzida. (BOND, 2006, p. 281).
Há crescente evidência de que a perda de peso pode ser benéfica tanto na
prevenção como no tratamento do DM2, melhorando a sensibilidade insulínica e
retardando a progressão do diabetes, mas também é reconhecido que esta é difícil de
conseguir na maioria dos pacientes. Estudos com exenatida demonstram que a melhora
no controle glicêmico obtida com sua administração está acompanhada por redução
significativa no peso corporal. Esse atributo oferece uma vantagem significativa à
exenatida
sobre
muitos
outros
medicamentos
antihiperglicêmicos,
como
as
sulfoniluréias ou tiazolidinodionas, que tendem a promover ganho de peso. (GREEN &
FLATT, 2007, p. 501; PINKNEY, FOX & RANGANATH, 2010, p. 402-403).
Além da perda de peso e melhorias no controle glicêmico, promovidas pela
utilização clínica de exenatida, também são observadas a diminuição da produção de
glucagon, estimulações da sensação de saciedade, inibição do esvaziamento gástrico
atrasando a digestão e absorção dos carboidratos e possivelmente aumento no gasto
energético. Em particular, o potencial de redução no peso corporal em pacientes com
diabetes tipo 2 pode ter um impacto positivo sobre o desenvolvimento de complicações
vasculares e resultados a longo prazo no paciente. (BOND, 2006, p. 283-284; GREEN
& FLATT, 2007, p. 502; SCHNABEL, WINTLE & KOLTERNAN, 2006, p. 74).
A exenatida melhora o controle glicêmico em pacientes com diabetes tipo 2,
reduzindo significativamente a HbA1c, em jejum e hiperglicemia pós-prandial.
Considerando que a hiperglicemia pós-prandial parece ser fator de risco de doenças
cardiovasculares mais importante que os níveis plasmáticos de glicose no jejum em
pacientes com DM2, o controle farmacológico da glicemia após as refeições com
exenatida tem um potencial para a redução da incidência dessas complicações a longo
prazo. (SCHNABEL, WINTLE & KOLTERNAN, 2006, p. 71-72, PINKNEY, FOX &
RANGANATH, 2010, p. 403).
Seu uso é comumente associado a efeitos adversos gastrointestinais, incluindo
náuseas, vômitos e diarréia. Como terapia continuada, as náuseas parecem declinar em
termos de gravidade e apresentam-se como efeito dose-dependente. Um número
relativamente baixo de episódios de hipoglicemia foram notificados quando em
associação com sulfoniluréias. Nos estudos, foram comparados exenatida com
sulfoniluréia utilizados isoladamente. Não existem estudos adequados em mulheres
grávidas, no entanto, em camundongos, foi demonstrado que exenatida reduz o
crescimento fetal e tem efeitos esqueléticos na dose máxima recomendada de 20 mcg /
dia. (BOND, 2006, p. 283).
Outro fármaco desenvolvido para o tratamento de diabetes é a liraglutida. Sua
estrutura é baseada nas modificações de GLP-1 por meio de substituição de Lisina-34
por Arginina-34 e a fixação de uma cadeia de ácido graxo de 16 carbonos no resíduo de
Lisina 26 (ligação feita por meio de uma molécula de ácido glutâmico), que
presumivelmente dificulta a clivagem pela DPP-4. Essa modificação, por si só, parece
ser suficiente para conferir certa resistência ao liraglutida, como também é observado
com alterações semelhantes à GIP. As substituições efetuadas no GLP-1 promovem a
lenta absorção e degradação do liraglutida em comparação com o GLP-1 fisiológico,
possivelmente através da interação com albumina e uma capacidade de formar
agregados no tecido subcutâneo, resultando em um tempo para concentração máxima de
9-14 horas, e meia-vida de até 13 horas após administração subcutânea, onde se percebe
melhor adesão do paciente sem efeitos adversos com doses adequadas. (CHIA &
EGAN, 2008, p. 3705; GALLWITZ, 2005, p. 63-64; MCGILL, 2009, p. 50; PRATLEY
& GILBERT, 2008, p. 81-82).
São características importantes da terapia medicamentosa com liraglutida: 1)
oferece baixo risco de hipoglicemia; 2) melhora o funcionamento das células β; 3) não
está associada ao ganho de peso; 4) está associada com pequenos ou moderados efeitos
adversos gastrointestinais; 5) o fármaco é indicado para administração de uma única
dose diária. Efeitos adversos mais frequentemente relatados foram náuseas e vômitos,
especialmente nas doses mais elevadas. Também não há desenvolvimento de anticorpos,
observado em ensaios de até 14 semanas. (CHIA & EGAN, 2008, p. 3705, GUPTA,
2013, p. 416).
A administração de liraglutida leva à redução da glicemia de jejum, aumento da
primeira fase da secreção de insulina após refeições e supressão da produção pósprandial de glucagon. O medicamento age de forma dependente da glicose, o que
significa que estimula a secreção de insulina e inibe a secreção de glucagon, somente
quando os níveis de glicose estão mais altos que o normal. (COSTA & FORTI, 2006, p.
S621). Vários estudos clínicos mostram que a liraglutida tem efeitos benéficos na
função das células β-pancreáticas. Em pacientes com DM2, este fármaco foi capaz de
aumentar marcadamente a função das células β em 24 horas, fato demonstrado pelo
significante aumento na secreção de insulina induzida por glicose. (MCGILL, 2009, p.
51).
Em um estudo com pacientes diabéticos tipo 2, foi relatado que uma única dose
de liraglutida foi capaz de restaurar a sensibilidade das células β à glicose. Além disso,
foi demonstrado por meio de um estudo duplo-cego de 12 semanas que a liraglutida
melhora a função da célula β e é eficiente no controle da glicemia em pacientes com
DM2. Em doses de 0,225 a 0,75 mg por dia, a liraglutida diminui os níveis de HbA1c
em pacientes com DM2 em até 0,75% comparando a um placebo. Outro dado
experimental mostra que a liraglutida em doses diárias de 0,45 a 0,75 mg melhorou o
controle glicêmico e o peso corporal tanto quanto à metformina (COSTA e FORTI,
2006, p. S621).
A associação entre a liraglutida e outros fármacos usualmente prescritos para
pacientes com diabetes também tem sido investigada. Foi demonstrado que a
administração de liraglutida associado à metformina durante 5 semanas reduziu em
média 0,8% a HbA1c quando comparado ao tratamento apenas com a metformina.
Quando administrados juntos, esses fármacos foram mais eficientes na redução da
glicemia no jejum e do peso corporal quando comparados à associação
metformina/glimepirida. (CHIA & EGAN, 2008, p. 3705).
Sullivan e colaboradores utilizaram um modelo de simulação computadorizada
para avaliar o efeito das intervenções farmacológicas com liraglutida em monoterapia
ou associada à glimepirida na saúde de pacientes com DM2, utilizando parâmetros
clínicos, tais como HbA1c, pressão arterial sistólica, lipídios séricos e índice de massa
corporal. De modo geral, os resultados mostraram que pacientes em uso da associação
liraglutida/glimepirida podem ter maior sobrevida e redução das complicações
decorrentes do DM2 em um período de 10 a 30 anos, quando comparado com pacientes
utilizando a associação rosiglitazona/glimepirida. (SULLIVAN et al., 2009, n.p.).
3.2 INIBIDORES da DPP-4
Os inibidores do sistema enzimático DPP-4 são novos medicamentos
promissores para o tratamento do diabetes tipo 2. A lógica do uso de inibidores da DPP4 baseia-se na hipótese de reforço endógeno do GIP e GLP-1, através da inibição da sua
atividade enzimática. Considerando a ampla expressão de enzimas da família DPP, uma
condição essencial de um agente antihiperglicêmico é a sua seletividade para a DPP-4,
com relação às outras isoformas, denominadas DPP-8 e DPP-9, a fim de minimizar o
risco de efeitos adversos. (ROSENSTOCK et al., 2008, p. 32-33; VELLA et al., 2007,
p. 1478).
Sitagliptina e vildagliptina (figura 3) são altamente seletivos para a DPP-4 e
capazes de aumentar a concentração de GLP-1 endógeno, sendo esses fármacos
atualmente os únicos inibidores da DPP-4 aprovados para uso clínico. Seguindo a
mesma linha, uma série de outras moléculas, incluindo saxagliptina e alogliptina, estão
atualmente sob investigação em fase 2 e fase 3 dos ensaios clínicos. A grande vantagem
que esses fármacos apresentam é a via de administração, que é oral. (ROSENSTOCK et
al., 2008, p. 34-35; VELLA et al., 2007, p 1478, 1480).
Fig. 3 - Estrutura da sitagliptina e vildagliptina. (Fonte: Adaptado de CHIA &
EGAN, 2008, p. 3704)
Inibidores da DPP-4 melhoram o controle glicêmico, a secreção de insulina, e a
função de células ß-pancreáticas (DICEMBRINI, PALA & ROTELLA, 2011, n.p.). Em
pacientes com diabetes tipo 2, tratamento crônico com inibidores da DPP-4 diminui
glicose pós-prandial, glicemia de jejum e HbA1c e é bem tolerada com efeitos neutros
no peso e uma baixa incidência de eventos adversos gastrointestinais e hipoglicemia
(HERMAN et al., 2006, p. 4616; INZUCCHI et al., 2008, p. 578).
O inibidor do DPP-4 sitagliptina já teve seu uso aprovado como segundo agente
de escolha para o tratamento do DM2, em indivíduos que não responderam ao primeiro
agente, como metformina, sulfoniluréia e tiazolidinodiona ou então, como terceiro
agente de escolha, quando a terapia combinada de dois agentes não alcançou a meta
glicêmica. A dose de sitagliptina é de 100 mg por dia, no entanto esta deve ser corrigida
em pacientes com insuficiência renal. Além disso, mostrou-se efetiva quando utilizada
em associação com a metformina, a sulfoniluréia ou a tiazolidinodiona. (HERMAN, et
al., 2006, p. 4617-4618; INZUCCHI et al., 2008, p.577).
Sitagliptina não interage com outras proteases intimamente relacionadas à DPP4. Esse fármaco é rapidamente absorvido, atingindo pico de níveis plasmáticos 1-6 h
após a administração. Sua meia-vida é 8-14 h, com biodisponibilidade de 87%, com ou
sem alimentos. Cerca de 80% da dose é excretada inalterada pelo rim, com 15% da
droga metabolizada pela citocromo P3A4 e citocromo P2C8 no fígado. Com a
administração de 100 mg por dia, a atividade de DPP-4 é inibida em mais de 80% por
um período de 24 horas. (BERGMAN et al., 2006, p. 56-57; BOSI, et al, 2008, p. 104).
Como resultado, a concentração de GLP-1 intacta e biologicamente ativa é aumentada
de 2 a 3 vezes no período pós-prandial. (GALLWITZ, 2007, p. 204).
Além dos efeitos da sitagliptina sobre o metabolismo da glicose, estudos em
camundongos mostraram que o tratamento com esse fármaco por 2 a 3 meses levou à
melhora de parâmetros lipídicos como concentrações plasmáticas de triacilgliceróis e
ácidos graxos livres. (GALLWITZ, 2007, p. 205).
A vildagliptina, outro fármaco da classe, é um inibidor seletivo e competitivo da
DPP-4 e possui baixo peso molecular. Após a administração oral, vildagliptina é
rapidamente absorvida e atinge níveis plasmáticos em 1-2 horas. Sua meia-vida de 2
horas é menor que a da sitagliptina. Sua biodisponibilidade é de 85%, e sua
farmacocinética não é afetada pelos alimentos. A administração de 100mg, diariamente,
inibe a 98% da atividade da DPP-4, em 45 minutos após a administração e 60%, após
24 horas. Aproximadamente 85% do vildagliptina é metabolizado no fígado e os 15%
restantes são eliminados inalterados pelos rins. (BOSI et al., 2008, p. 104;
ROSENSTOCK et al., 2008, p. 32).
Ensaios clínicos avaliaram a vildagliptina como monoterapia inicial em
comparação ao placebo e metformina, rosiglitazona, ou acarbose, e também como
primeira combinação terapêutica com pioglitazona em comparação com a droga em
monoterapia. Pacientes com dificuldade no controle glicêmico tiveram redução maior
da HbA1c, após 24 semanas de uso do fármaco. Dados do estudo sobre a ampliação do
grupo com melhor controle glicêmico mostraram que a redução máxima de HbA1c
ocorreu em torno de 24-30 semanas. Como monoterapia, vildagliptina 50mg,
administrada duas vezes por dia, foi tão eficaz quanto a rosiglitazona 8 mg, uma vez ao
dia, acarbose 100mg três vezes ao dia, em relação à diminuição das concentrações de
HbA1c, mas não tão eficaz como metformina 1000mg duas vezes ao dia. A terapia
combinada com vildagliptina e pioglitazona mostrou-se melhor no controle glicêmico
do que vildagliptina ou pioglitazona em monoterapia. (CHIA & EGAN, 2008, p. 3711).
Vildagliptina é eficaz quando administrado como terapia adjuvante aos pacientes
inadequadamente controlados com sulfoniluréia, metformina, tiazolidinodiona, ou
terapia com insulina. Além disso, vildagliptina e pioglitazona também foram eficazes
como terapia adjuvante para os pacientes que eram inadequadamente controlados com
metformina. (CHIA & EGAN, 2008, p. 3711).
Os efeitos adversos da vildagliptina são comparáveis ao do sitagliptina.
vildagliptina não tem risco de eventos adversos gastrointestinais, porém há um aumento
de risco para infecção urinária e cefaleia. (CHIA & EGAN, 2008, p. 3712,
DICEMBRINI, PALA & ROTELLA, 2011, n.p.).
CONCLUSÃO
A ligação entre as incretinas GLP-1 e GIP e seus receptores nas células βpancreáticas leva à ativação das cascatas de sinalização celular que envolvem PKA e
EPAC, de modo dependente da concentração de cAMP. O resultado dos eventos
decorrentes da ativação dessas vias é o aumento das concentrações intracelulares de
Ca2+ necessário ao processo de exocitose da insulina.
Nos últimos anos, foram desenvolvidos fármacos baseados na ação das
incretinas para o tratamento de pacientes com DM2. Esses fármacos atuam basicamente
de duas formas distintas: mimetizando a ação das incretinas (exenatida e liraglutida) ou
inibindo a ação da enzima responsável pela degradação das incretinas, dipeptidil
peptidase-4 (sitagliptina e vildagliptina).
A terapia com “medicamentos incretinas” tem se mostrado eficaz na utilização
como monoterapia ou associados a outros antihiperglicêmicos, assim é possível reduzir
as doses dos medicamentos e, consequentemente, os efeitos adversos. A terapia, apesar
de custo elevado, possui grandes benefícios para o paciente como diminuição das
complicações cardiovasculares.
REFERÊNCIAS
BERGMAN, Arthur J. et al. Pharmacokinetic and pharmacodynamic properties of
multiple oral doses of sitagliptin, a dipeptidyl peptidase-IV inhibitor: a double-blind,
randomized, placebo-controlled study in healthy male volunteers. Clin Ther., v. 28, n.1,
p. 55-72, Jan., 2006.
BOND, Aaron. Exenatida (Byetta) as a novel treatment option for type 2 diabetes
mellitus. Proc (Bayl Univ Med Cent), Texas, v. 19, n. 3, p. 281–284, Jul., 2006.
BOSI, Emanuele et al. Incretin-based therapies in type 2 diabetes: A review of clinical
results. Diabetes Res Clin Pract, v. 82, p. 102-107. Nov., 2008.
CHACRA, Antônio R. Efeito fisiológico das incretinas. Adv Stud Med, São Paulo, v. 6
(7 B), p. S613 – S617, Jul., 2006.
CHIA, Chee W.; EGAN, Josephine M. Incretin-based therapies in type 2 diabetes
mellitus. Clin Endocrinol Metab, v. 93, n. 10, p. 3703-3716, Oct., 2008.
COSTA e FORTI, Adriana. Estratégias terapêuticas baseadas nas vias do GLP-1. Adv
Stud Med, v. 6 (7B), p. S618-S626, Jul., 2006.
DICEMBRINI, Ilaria; PALA, Laura; ROTELLA, Carlo M. From theory to clinical
practice in the use of GLP-1 receptor agonists and DPP-4 inhibitors therapy. Exp
Diabetes Res, v. 2011, art. ID 898913, 2011.
DOYLE, Máire E.; EGAN Josephine M. Mechanisms of action of GLP-1 in the
pancreas. Pharmacol Ther, v. 3, p. 1-83, Mar., 2007.
DRUCKER, Daniel J. Dipeptidyl peptidase-4 inhibition and the treatment of type 2
diabetes. Diabetes Care, v. 30, n. 6, p. 1335-1343, Jun., 2007.
EDWARDS, C Mark B. GLP-1: target for a new class of antidiabetic agents? J R Soc
Med, v. 97, p. 270–274, Jun., 2004.
FULURIJA, Alma, et al.. Vaccination against GIP for the treatment of obesity. PLoS
One, v. 3, n. 9, p. 1-11, Sep., 2008.
GALLWITZ, Baptist. New therapeutic strategies for the treatment of type 2 diabetes
mellitus based on incretins. Rev Diabetic Stud, v. 2, n. 2, p. 61-69, 2005.
GALLWITZ, Baptist. Review of sitagliptin phosphate: a novel treatment for type 2
diabetes. Vasc Health Risk Manag, v. 3, n. 2, p. 203-210, 2007.
GREEN, Brian D.; FLATT, Peter R. Incretin hormone mimetics and analogues in
diabetes therapeutics. Best Pract Res Clin Endocrinol Metab, v. 21, n. 4, p. 497–516,
2007.
GUPTA, Vishal. Pleiotropic effects of incretins. Indian J Endocrinol Metab, v.
16(Suppl 1), p. S47-S56, Mar., 2012.
GUPTA, Vishal. Glucagon-like peptide-1 analogues: an overview. Indian J Endocrinol
Metab, v. 17, n.3, p. 413-421. May-Jun., 2013.
GUYTON, Arthur C.; HALL, John E. Insulina, glucagon e diabete melito. In: ______.
Tratado de fisiologia médica. 10 ed. Rio de Janeiro: Guanabara Koogan, 2006. p. 827840.
HANSOTIA, Tania et al. Extrapancreatic incretin receptors modulate glucose
homeostasis, bodyweight, and energy expenditure. J Clin Invest, v. 117, p. 143-152,
2007.
HERMAN, Gary A., et al. Effect of single oral doses of sitagliptin, a dipeptidyl
peptidase-4 inhibitor, on incretin and plasma glucose levels after an oral glucose
tolerance test in patients with type 2 diabetes. J Clin Endocrinol Metab, v. 91, n. 11, p.
4612–4619, Nov., 2006.
HINNEN, Deborah, et al. Incretin mimetics and DPP-IV inhibitors: new paradigms for
the treatment of type 2 diabetes. J Am Board Fam Med, v. 19, n. 6, p. 612 – 620, 2006.
HOLST, Jens Juul; GROMADA, Jesper. Role of incretin hormones in the regulation of
insulin secretion in diabetic and nondiabetic humans. Am J Physiol Endocrinol Metab,
v. 287, p. E199-E206, 2004.
INZUCCHI, Silvio E., et al. New drugs for the treatment of diabetes - Part II: incretinbased therapy and beyond. Circulation, v. 117, p. 574-584, 2008.
MARTINS, Marcus V.D.C.; SOUZA, Antônio A. P. Mecanismos cirúrgicos de controle
do diabetes mellitus tipo 2 após cirurgia bariátrica. Rev Col Bras Cir, v. 34, n. 5, p. 343346, 2007.
MCGILL, Janet B. Impact of incretin therapy on islet dysfunction: an underlying defect
in the pathophysiology of type 2 diabetes. Postgrad Med, v. 121, n.1, p. 46-58, Mar.,
2009.
NAUCK, M. A. et al. Incretin effects of increasing glucose loads in man calculated
from venous insulin and C-peptide responses. J Clin Endocrinol Metab. v. 63, p. 492–
498, 1986.
NELSON, David L.; COX, Michael M. Integração e regulação hormonal do
metabolismo dos mamíferos. In: ______. Princípios de bioquímica. 4 ed. São Paulo:
Sarvier, 2006, p. 872-914.
PINKNEY, Jonathan; FOX, Thomas; RANGANATH, Lakshminarayan. Selecting GLP1 agonists in the management of type 2 diabetes: differential pharmacology and
therapeutic benefits of liraglutide and exenatide. Ther Clin Risk Manag, v. 6, p. 401411, 2010.
PRATLEY, Richard E.; GILBERT, Matthew. Targeting incretins in type 2 diabetes:
role of GLP-1 receptor agonists and DPP-4 inhibitors. Rev Diabet Stud, v. 5, n. 2, p. 7394, 2008.
ROSENBAUM, Daniel, M; RASMUSSEN, Soren, G.F.; KOBILKA, Brian K. The
structure and function of G-protein-coupled receptors. Nature, v. 459, p. 356-363, May,
2009.
ROSENSTOCK et al. Effects of the dipeptidyl peptidase-IV inhibitor vildagliptin on
incretin hormones, islet function, and postprandial glycemia in subjects with impaired
glucose tolerance. Diabetes Care, v. 31, p. 30–35, 2008.
SCHNABEL, Catherine A; WINTLE, Matthew; KOLTERMAN, Orville. Metabolic
effects of the incretin mimetic exenatida in the treatment of type 2 diabetes. Vasc Health
Risk Manag, v. 2, n. 1, p. 69–77, 2006.
SULLIVAN, Sean D. et al. Long-term outcomes in patients with type 2 diabetes
receiving glimepiride combined with liraglutida or rosiglitazone. Cardiovasc Diabetol,
v.8, art. ID 12, Feb., 2009.
VELLA, Adrian. et al. Effects of dipeptidyl peptidase-4 inhibition on gastrointestinal
function, meal appearance, and glucose metabolism in type 2 diabetes. Diabetes, v. 56,
n. 5, p. 1475-1480, May, 2007.