INSUFICIÊNCIA RENAL AGUDA
Paulo R. Margotto/Márcia Pimentel de Castro
Capítulo do Livro Assistência ao Recém-Nascido de Risco, editado por
Paulo R. Margotto2a Edição/ 2004
INTRODUÇÃO
A Insuficiência Renal Aguda (IRA) pode ser definida como deficiência súbita da
função glomérulo -tubular levando a distúrbios da homeostase do organismo.
Caracteriza-se por alterações no equilíbrio hidroeletrolítico e ácido básico,
descontrole hormonal, elevação da creatinina e uréia sangüíneas, oligúria, embora em
alguns casos possa haver poliúria desde o início do quadro.
Vale lembrar que 97% dos recém-nascidos (RN) urinam nas primeiras 24 horas de
vida, e que 4% a 22% dos RN apresentam a 1a. micção na sala de parto.
FUNÇÃO RENAL DO RECÉM-NASCIDO
Na vida intra-uterina, a placenta é o principal regulador da composição de líquidos;
a contribuição do rim na manutenção da homeostase é mínima, sendo apenas responsável
pela manutenção de um volume adequado de líquido amniótico.
Com o nascimento, o rim passa a atender às necessidades normais do recémnascido, sendo que suas funções se aperfeiçoam à medida que se processa o crescimento.
Frente às situações em que ocorre desequilíbrio da homeostase, conseqüente a
fatores patogênicos ou iatrogênicos, o rim pode não responder de forma adequada, como
acontece em crianças maiores e em adultos. Essas limitações refletem uma "imaturidade"
ainda observada nesse período. São elas:
- Taxa de filtração glomerular (TFG) baixa, secundária a uma resistência vascular
aumentada ao nível das artérias glomerulares. Enquanto 2% a 3% do débito cardíaco vai
para os rins na vida intra-uterina (esses órgãos não têm a função de controlar o meio
interno, função esta desempenhada pela placenta),ao nascimento este percentual do débito
cardíaco como fluxo sanguíneo renal deve ser sextuplicado em poucos dias, atingindo 12%
a 18% no RN a termo, aproximando-se de 25% que é o nível de adultos. A taxa de filtração
glomerular é de aproximadamente 26ml/min/1.73 m² com:34 semanas de idade
gestacional.Com 25 semanas, a TFG é de 2 ml/min/1.73 m², alcançando níveis de
maturação na idade de 9-12 meses (aproximadamente 125 ml/min/1.73 m²). Podemos
calcular a TFG pela fórmula: K x comprimento do RN creatinina sérica (fórmula de
Schwartz), sendo K uma constante, cujo valor é 0.33 para RN de baixo peso e 0.45 para RN
a termo (K representa a creatinina urinária por unidade de peso corporal). Existe, então,
limite da capacidade do RN para resistir ao stress de uma sobrecarga de água.
- Desenvolvimento glomerular mais avançado que o tubular, resultando em
desequilíbrio glomérulo-tubular. Esta assertiva induz a um julgamento injusto: embora a
taxa de reabsorção tubular seja ainda pior do que a TFG, a função tubular de reabsorção ou
excreção por superfície quadrada de túbulos é melhor do que a função glomerular
propriamente dita. Existem poucos túbulos e estes são pequenos; a nefrogênese que se dá de
modo centrífugo (da pelve para o córtex) só se completa na 34ª semana. Os primeiros
néfrons a surgir são os justa-medulares, que têm o glomérulo no córtex ou próximo à
medula, cuja alça de Henle é profunda (atinge a medula) e representam 15% da população
total de néfrons na vida adulta. Estes são os mais eficientes para a manutenção do meio
interno. Os outros 85% dos néfrons são corticais, menos eficazes (têm a alça de Henle mais
curta) e surgem por volta da 34ª semana de gestação. Assim sendo, não é justo afirmar que
os RN têm uma imaturidade tubular tão exagerada quando comparada com a função
glomerular; a superfície dos túbulos é pequena, de modo que a função final fica diminuída.
- Deficiente concentração: incapacidade de alcançar níveis de osmolaridade
urinária acima de 700 mOsm/1. Os túbulos têm uma capacidade limitada de concentrar e
de diluir urina, e esta capacidade freqüentemente é agredida por situações relacionadas a
outras enfermidades que o RN apresenta, especialmente a hipóxia, quando a reabsorção de
Na+ do ultrafiltrado, que consome energia, fica extremamente prejudicada, em decorrência
do processo oxidativo comprometido.Há imaturidade morfológica da alça de Henle e
disponibilidade limitada de uréia nesta faixa etária.
- Limitada habilidade de diluir face a uma sobrecarga de água.
Limitação da taxa de excreção de água resulta de uma limitada taxa de filtração
glomerular (TFG). Condições em que o líquido do espaço extra celular está aumentado,
como nas situações de excesso de hormônio anti-diurético ou situações que associam-se à
secreção inapropriada de hormônio anti-diurético (meningite, asfixia e hemorragia intra
ventricular, entre outras), provocam aumento de peso, diminuição da diurese e aumento da
densidade urinária (no caso de Síndrome de secreção inapropriada do hormônio antidiurético: consulte o capítulo de Hidratação Venosa).
- Baixa capacidade de tampão do rim: concentrações baixas de bicarbonato
sanguíneo.
HOMEOSTASE DO SÓDIO
Recém-nascidos de termo tendem a manter um balanço positivo de sódio, devido a
uma forte tendência de reabsorver o sódio filtrado. Frente a uma sobrecarga de sódio,
apresentam taxa de excreção limitada do soluto, com risco de hipernatremia. A habilidade
máxima do RN a termo excretar sódio está em torno de 12 mEq/kg/dia de Na+
Em recém-nascidos pré-termo, no período de 2 - 5 semanas de vida, observa-se
uma inadequada reabsorção tubular de sódio, provocando uma resposta natriurética (a
hiponatremia é mais severa na 2ª - 3ª semana de vida). A hipernatremia pode ser observada
em duas situações especiais: perdas renais aumentadas de água (diurese osmótica – vale
lembrar os efeitos da hiperglicemia) ou perdas insensíveis aumentadas. Neste último caso, a
hipernatremia ocorre com o espaço extracelular normal ou levemente diminuído. Sinais /
sintomas: perda de peso acentuada, tendência à hipotensão, com densidade urinária
aumentada, aumento da frequência cardíaca, diurese diminuída e algum grau de acidose
metabólica. Esta é a situação mais comum nas Unidades de Cuidados Intensivos Neonatais,
em virtude da pouca valorização que se costuma dar às perdas insensíveis através da pele
(imaturidade dos extratos córneos). É preciso lembrar que um RN pré-termo tem
aproximadamente 85% a 90% de seu peso corporal representado por água, enquanto que no
RN a termo esta proporção cai para 75% e no lactente de 3 meses é de aproximadamente
60%.
HOMEOSTASE DO POTÁSSIO
Recém-nascidos muito baixo peso: apresentam balanço positivo de K+ durante
todo o período neonatal. O risco de hipercalemia é grande, mesmo na ausência de oligúria,
devendo a calemia ser monitorizada precocemente. Hipercalemia não oligúrica tem sido
relatada em 50% nestes RN na primeira semana de vida, sendo atribuído a deficiência da
+
Na-K-ATPase e ao grande desvio de K para o extracelular. Mais recentemente tem sido
atribuída ao baixo fluxo na veia cava superior (reflexo da redução do fluxo sanguíneo
sistêmico e subsequentemente, da taxa de filtração glomerular)
-
Papel da Aldosterona
Níveis elevados de aldosterona são insuficientes para promover a absorção
adequada do excesso de sódio que chega ao túbulo distal, incapaz de manter, então, o
balanço do íon. Altas concentrações plasmáticas de aldosterona podem refletir uma
compensação para menor resposta dos túbulos renais (a partir da 3ª semana de vida, os
túbulos renais respondem bem a aldosterona).
FISIOPATOLOGIA:
Várias teorias apontam uma combinação de mecanismos atuando na gênese da IRA:
1- vasoconstrição renal:
Um fluxo sanguíneo renal menor acarretaria lesões às células epiteliais tubulares,
resultando em um aumento na concentração do sódio no fluído que chega à mácula densa.
Uma quantidade maior de soluto no túbulo distal estimularia a liberação de componentes
vasoativos do aparelho justaglomerular (ativação do sistema renina-angiotensina).
A angiotensina II, ativada pela renina, provocaria vasoconstricção da arteríola
pré-glomerular, com aumento da resistência vascular cortical e diminuição da TFG .
Esse "feed-back" túbulo glomerular conservador de água e eletrólitos tem a
desvantagem de ser indiscriminado, retendo também, catabólitos nitrogenados e outras
substâncias. À medida que acontece a recuperação gradual tubular, melhora a absorção de
sódio, desestimulando progressivamente o mecanismo compensador.
Estudos recentes têm investigado o papel da adenosina como potente
vasoconstrictor renal, razão pela qual a teofilina, um antagonista da adenosina, pode
prevenir a IRA induzida pela hipoxemia.
2- Fatores relacionados ao Néfron:
a) células epiteliais necrosadas eliminadas para dentro da luz tubular poderiam
ficar impactadas causando obstrução da luz, principalmente na curva da alça de Henle. A
obstrução, pelo aumento da pressão no espaço de Bowman, aboliria completamente a
formação do filtrado.
b) Segundo fator relacionado ao néfron seria a perda retrógrada do filtrado
glomerular (tubular "backleak"). A perda da integridade estrutural tubular tornaria-o
permeável às substâncias que normalmente não penetrariam na membrana basal, como
insulina e creatinina, e, ainda, mais sensível à absorção de líquidos e outros solutos.
CAUSAS DA INSUFICIÊNCIA RENAL AGUDA
- Insuficiência pré-renal: ocorre quando se instala fluxo sangüíneo renal
insuficiente. Não havendo lesão renal, a reversibilidade do processo dependerá da correção
hemodinâmica, pois a persistência da condição anormal poderá significar causa importante
da IRA intrínseca.
- Insuficiência renal: implica em lesão do parênquima renal. Causas congênitas e
adquiridas.
- Insuficiência pós-renal: são incomuns. Ocorrem por obstrução do fluxo urinário
depois de formada a urina. Resultam de malformações congênitas ou pressões extrínsecas,
como tumores, hidronefrose e válvula de uretra posterior.
Quadro 1 Principais causas de Insuficiência Renal no Neonato*
Pré- renais
Obstrução pós-renal
Insuficiência renal intrínseca
Hipotensão causada por:
Obstrução ureteral
Anomalias congênitas
-Choque séptico
-válvula de uretra
-displasia cística
-Hemorragia materna
posterior
-hipoplasia
anteparto
-imperfuração
-agenesia
-Hemorragia gêmeo a
prepucial
-rins policísticos
gêmeo
-estreitamento
Inflamatórias
-Hemorragia neonatal
uretral
-sífilis ou toxoplasmose
-Cirurgia cardíaca
-divertículo uretral
-congênitas
-Insuficiência
cardíaca
-megauretra
-pielonefrite
congestiva
-ureterocele
Vasculares
-Asfixia perinatal
-obstrução
-trombose venosa
-Desidratação
ureteropélvica ou
-necrose cortical
ureterovesical
-trombose arterial
Tumores
extrínsecos
-CID
comprimindo a saída da Necrose Tubular Aguda
bexiga
-asfixia perinatal
Bexiga neurogênica
-desidratação
-choque
-nefrotoxinas
* Segundo Rahman, N. , Boinear, F. G. e Lewy, J. E.: Renal failure in the perinatal period.
Clin Perinatol 8: 241, 1981.
A asfixia perinatal é a causa mais comum de IRA intrínseca no RN, podendo também ser
pré-renal, uma vez que a asfixia contribui com a hipoperfusão renal, além de ocorrer um
desvio de sangue dos rins para melhorar a circulação ao nível de coração e cérebro. Estudos
recentes demonstraram que falência renal, definida por aumento de nível de creatinina
sérica, tem uma prevalência de 61% em associação com severa asfixia em RN a termo, e é
predominantemente não oligúrica. Uma vez que RN a termo sadios apresentam valores de
creatinina sérica de 0,89mg%, (+- 0,02 mg%) no primeiro dia de vida e 0,50 mg% (+- 0,02
mg%) a partir do 5o. dia, insuficiência renal aguda (IRA) pode ser definida como níveis de
creatinina sérica superiores a 1,5mg% associado com uma função renal materna
normal.(deve-se determinar o nível de creatinina sérica materna na hora do parto)
Insuficiência renal não oligúria pode ser definida como débito urinário menor que 1ml/kg/h
depois do primeiro dia de vida. Em casos de asfixia, os autores observaram a presença de
IRA não oligúrica em 61% dos RN a termo que sofreram asfixia grave; IRA oligúrica, em
25% e anúrica em menos de 15%. Foi proposto um escore de morbidade, capaz de
determinar, com uma hora de vida, a probabilidade do RN desenvolver falência renal com
100% de sensibilidade e 72% de especificidade. Este escore baseia-se na escala de Apgar
no 5o. minuto (menor que 6) e valor do déficit de base (aferido através da gasometria
arterial) na 1a. hora de vida (menor que 10).Taxas de filtração glomerular persistentemente
baixas e disfunção tubular têm sido relatadas em 40% dos sobreviventes de insuficiência
renal aguda no período neonatal, na ausência de malformações do trato genitourinário.
Quanto a nefrotoxicidade dos antibióticos, estima-se que 10 a 30% dos pacientes em
uso de aminoglicosídeos apresentam IRA transitória, geralmente de natureza não oligúrica.
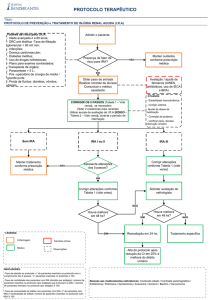
DIAGNÓSTICO:
-História clínica: dados colhidos devem dar enfoque a condições clínicas que
potencialmente puderam desenvolver dano renal. Suspeitar de oligúria nos RN com
ausência de diurese nas primeiras 24 horas (93% urinam dentro deste período, débito
urinário < 15 a 20 ml/kg/24h).
- Exame Físico: investigar estado de hidratação, jato urinário, sinais de choque ou
hipovolemia, pressão arterial eem
mm
meem
mbbrrooss ssuuppeerriioorreess ee iinnffeerriioorreess, pulso, pressão venosa
central, freqüência cardíaca.
Massas tumorais na região do flanco e hipogástrio, malformações da parede
abdominal. Anormalidade do trato urinário inferior.
- Exames laboratoriais:
a) sangue:
Sódio e Potássio: pode ocorrer hiponatremia dilucional ou por disfunção tubular
e/ou hipercalemia;
Uréia e creatinina: ao nascimento refletem valores maternos, até por volta de 48
horas de vida.. Na IRA a uréia está em níveis superiores a 28 mg%, e a creatinina acima de
1 mg% (níveis normais de creatinina: 0.8-1 mg% e a partir dos 7 dias de vida: 0.3-0.4
mg%). Sabe-se que 30% da uréia filtrada a nível glomerular é reabsorvida a nível tubular.
Outros fatores podem determinar um aumento de uréia: dieta rica em proteínas, oferta
aumentada de proteínas na Nutrição Parenteral Total (NPT), hemorragia gastrintestinal e
desidratação, por exemplo. Portanto, não é o melhor indicador para avaliar a função renal.
A creatinina expressa a função tubular, uma vez que é secretada pelo túbulo e não mais
reabsorvida. O aumento de creatinina da ordem de 0,5mg/dl/dia indica uma redução severa
da TFG. Quando a creatinina sérica dobra, a TFG cai 50%.Quando a relação
uréia/creatinina é maior que 20, deve-se suspeitar de um aumento da produção de uréia ou
aumento de sua reabsorção a nível tubular. Condições que resultam em diminuição do
volume intravascular acarretam um aumento da reabsorção tubular de água e de uréia, sem
alteração significativa da função glomerular.
Hemocultura: etiologia de infecção;
Gasometria: acidose metabólica;
Hipocalcemia, Hiperfosfatemia e hipomagnesemia.
b) Urina:
Densidade urinária (normal 1005 - 1010). Se, acima destes valores: há
anormalidade (multiplicando os dois últimos números da densidade urinária por 30, você
tem a osmolaridade urinária: ex: DU = 1010-;Osmolaridade urinária = 300). Osmolaridade
urinária máxima: RN pré-termo = 600 mOsm/l; RN a termo = 800 mOsm/l; adulto = 1.200
mOsm/l.
Sedimento urinário: presença de hematúria, cilindros, leucocitúria: indicam
lesão renal;
Uréia, creatinina, sódio e potássio urinários.
c) ECG: Alterações observadas na hiperpotassemia.
d) Ultra-sonografia: Avaliação de massas renais e alterações morfológicas na
estrutura do parênquima renal.
e) Urografia excretora: Pouco utilizado, risco de maior toxicidade do
contraste.
f) Biópsia renal
DIAGNÓSTICO DIFERENCIAL:
Diante de um paciente com oligúria e azotemia, torna-se importante a distinção
entre IRA pré-renal e renal propriamente dita, pois a abordagem terapêutica será diferente.
Testes diagnósticos para a diferenciação:
- suspeita clínica de depleção de volume: administrar solução fisiológica ou plasma, num
volume de 20ml/Kg durante 60 a 20 min; ppooddeennddoo--ssee cchheeggaarr aattéé 4400 m
mll//kkgg.. Se persistir
oligúria :- furosemide 2mg/Kg/dose; se não houver diurese (> 2 ml/Kg/hora), após 60-120
min = IRA intrínseca).Atualmente dá-se preferência à solução de cristalóide.
Teste da excreção de fração sódio (ENaF):Na+urina/Na+sangueX 100
Cr urina/Cr sangue
IRA pré-renal = ENaF < 2,5%
IRA renal = ENaF > 2,5%
Para os RN com menos de 31-32 semanas, valores maiores da ENaF, tem sido proposto
(5%), tornando difícil a interpretação do ENaF nestes RN com IRA.
- Relação uréia plasmática/creatinina plasmática
IRA pré-renal (aproximadamente 70% dos casos): aumento desproporcional da
uréia em relação a creatinina . Proporção > 10:1.
IRA renal intrínseca (aproximadamente 25% dos caos): aumento proporcional de
uréia e creatinina. Proporção <10:1
IRA pós-renal: menos de 5% dos casos.
Osmolaridade urinária (mOsml/l): IRA pré-renal > 400 e IRA intrínseca: < 400
TRATAMENTO
Uma vez diagnosticada a IRA, torna-se necessário uma monitorização cuidadosa
para prevenir ou tratar precocemente as complicações.
Tratamento Geral:
1- Administração de líquidos e eletrólitos:
A reposição de volume deverá se limitar às perdas insensíveis e às perdas de
fluído externo (urina, SOG, drenos). Deverá ser subtraída a água endógena diária produzida
pelo metabolismo (9ml/Kg/peso). As perdas insensíveis nos 3 primeiros dias são:
As perdas insensíveis no RN em 24h variam com o peso de nascimento
700-1000g: 82ml/kg
1001-1250g: 56ml/kg
1251-1500g: 46ml/kg
> 1500g: 26ml/kg
Em uso de fototerapia ou calor irradiante, acrescentar 20 ml/Kg/dia.
A criança deverá perder 0,5 a 1% de peso.
Na fase de oligúria a administração de eletrólitos limitar-se á a perdas extra-renais.
Na fase de poliúria será baseada no balanço diário.
2- manutenção da temperatura:
manter zona de temperatura neutra.
3- Dietético:
Ingesta calórica: aproximadamente 100 cal/Kg /dia;
Administração: Leite Materno;
Nutrição parenteral total
4. Manutenção da pressão arterial:
Expansão volumétrica (já descrita anteriormente)
Uso de droga vasoativas: quando se tem certeza de que não há depleção de volume
circulante, e o paciente mantém-se hipotenso. Deve-se procurar manter uma PA adequada, a
fim de garantir uma pressão de perfusão adequada em nível de artérias renais,
possibilitando e favorecendo a filtração glomerular.
Dopamina: em baixas dose (2 – 5 microgramas/kg/min) produz pequena ação sobre
o coração e aumenta o fluxo sanguíneo renal, esplâncnico, coronário e cerebral. Com uma
taxa de infusão de 10 a 20 microgramas/kg/min a vasoconstricção aumenta e
consequentemente também a pressão sanguínea. No entanto a taquicardia pode ser
significante e problemática, uma vez que diminui o tempo diastólico e, conseqüentemente,
o enchimento coronário.
Dobutamina: catecolamina sintética que possui ação relativamente seletiva sobre os
receptores beta adrenérgicos. Seus efeitos incluem aumento da contratilidade cardíaca e
freqüência cardíaca, usualmente acompanhada por uma leve dilatação do leito vascular
periférico.Em pacientes com choque cardiogênico, ela aumenta o débito cardíaco, diminui a
pressão capilar pulmonar e a resistência vascular sistêmica. Deve ser avaliado o seu uso
após identificação da causa da IRA (baixa perfusão renal secundária a falência de bomba
cardíaca). Dose: 5 a 10 micrograma/kg/minuto.
Adrenalina (consulte o capítulo de Choque Séptico): é uma catecolamina potente
que age mais diretamente nos receptores adrenérgicos do que através da liberação de
norepinefrina armazenada. Tem ação relacionada à dose. A infusão de doses baixas (menos
que 0,3 microgramas/kg/minuto) está primariamente associada com efeitos beta
adrenérgicos, incluindo: aumento da contratilidade cardíaca, freqüência cardíaca, pressão de
pulso e pressão sanguínea sistólica. Em doses maiores que 0,3 microgramas/kg/minuto, os
efeitos alfa adrenérgicos predominam, produzindo aumento da pressão sistólica e diastólica
e diminuição da pressão de pulso. Está indicada em presença de sinais de perfusão ruim
em pacientes com volume intravascular adequado e ritmo estável, e na bradicardia
com repercussão hemodinâmica. Deve ser administrada em cateter venoso central, para
garantir uma via segura de administração e minimizar o risco de extravasamento. Como a
adrenalina tem uma meia vida curta (2 minutos), a infusão deve ser ajustada a cada 5
minutos, até ser alcançado o efeito clínico desejado. Dose: 0,1 a 1 micrograma/kg/minuto.
Apresentação: frascos 1 mg/ml (1:1000).
Choque séptico:é uma das causas mais freqüentes de choque no RN, o que pode, entre
outros fatores, levar a um quadro de IRA. Além do tratamento preconizado do choque
(consulte o capítulo de Choque Séptico), considerar o uso de corticóide neste caso
específico, quando a etiologia estiver bem determinada, para tratamento da hipotensão do
RN de muito baixo peso. Hidrocortisona: dose de 1 mg/kg/dose, de 12/12 horas ou 20 a 40
mg/m2/dia em 2 ou 3 doses em infusão venosa. Área corporal (m2) = (0,05 x kg) + 0,05
. Estudos recentes referem evidências de correção da hipotensão em RN que
receberam dose de corticóide, após ter se tentado estabilizar os níveis pressóricos com
infusão de dopamina (até 15 microgramas/kg/minuto) e epinefrina, sem sucesso.
TRATAMENTO DAS COMPLICAÇÕES
1- Hiponatremia
- Origem iatrogênica (sobrecarga fluida)
- Se Na plasmático < 120 ou sem sintomas - Restrição Hídrica.
- Se Na < 120 ou se houver problema no SNC, administrar NaCl - 3%
(0,5 mEq = 1 ml, diluir NaCl 20% 11x) Correção Sódio para = 125 mEq Na = (Na desejado
- Na inicial) x 0,7 x Peso (2 horas).(consulte o capítulo de Hidratação Venosa)
2- Hipercalemia:
a) K+ 5.5 a 7.0 com ECG normal
Diminui aporte VO ou EV, correção da acidose.
b) K+ > 7, com alterações no ECG (ondas T elevadas, Fibrilação)
Gluconato de cálcio 10% - 0,5 a 1 ml/Kg/ (2-4 min) monitorização
Glicose + insulina regular (solução polarizante): 1 U insulina/4g glicose
Ex: RN c/ 1.2 kg- 7 mEq/l de potássio: 19.2ml SG 25% + 4.8 U de insulina
regular
4g glicose x 1.2 kg = 4.8g glicose e 1ml SG 25% = 0.25g de glicose. Então, 4.8g de glicose
equivale a (4.8 0.25) 19.2 ml SG 25% ( consulte o capítulo de Hidratação Venosa)
Se não houver resposta: salbutamol – 5 mcg/kg em 15 min (o K+ sérico cai
significantemente em 15 minutos; o salbutamol, que é um estimulador beta2, induz a
entrada do K+ para a célula. Alguns centros utilizam o salbutamol como a primeira linha de
tratamento da hipercalemia; 1 ml de salbutamol = 0.5mg = 500mcg). Manutenção:
0,2mcg/Kg/min
Correção da acidose metabólica com bicarbonato de sódio: O metabolismo celular produz
cerca de 2 mEq/kg/dia de ácido fosfórico, sulfúrico e ácidos não voláteis. Estes ácidos são
tamponados pelo bicarbonato extracelular, gerando CO2, água e sais de ânion ácido. A
homeostasia é preservada pelos rins, que excretam ácidos e regeneram o bicarbonato,
consumido na reação de tamponamento. A correção da acidose metabólica na IRA deve ser
cuidadosa, pelo risco de desenvolver hipocalcemia e sobrecarga hídrica.Na verdade, esta
correção deve ser secundária à correção da causa base; quando não for possível, através s de
meios dialíticos.
Diálise peritoneal
3- Hipertensão arterial
Restrição hídrica ou diálise peritoneal
Elevações agudas = administração de drogas como:
Hidralazida 0.1-0.5 mg/kg/dose, 6/6 horas EV e por VO ÷ 0.25 - 1mg/kg/dose
cada 6-12h
(Apresolina R) 1 amp.= 20 mg/ml.
1 comp = 25 mg e 50 mg
Efeito adverso: taquicardia. Iniciar propanolol na dose de 0.1 mg/kg/dose de 6/6/ ou 8/8 h,
em 10 min. EV. se VO: 0,25 mg/kg/dose de 6/6/ ou 8/8h (Inderal R; 1 ampola = 1 ml = 1
mg e comp. = 10 mg)
Metildopa : 2.5-10. mg/Kg/dose 12/12h - VO Inconveniente: nem sempre é possível utilizar
a via oral.
Aldomet R; 1 comp= 250mg e 500 mg
Captopril : 0,1-0,4 mg/Kg/dose (1 a 4 vezes/dia). Iniciar com 0,1 e aumentar
semanalmente - Capoten R : 1 comp. = 12, 5, 25 e 50 mg.
4- Anemia
Quando severa: papa de hemácias 10 ml/Kg (2 horas)
5- Hipocalcemia
Suplementação de cálcio ou derivados da vitamina D
6- Convulsões:
Correção dos distúrbios metabólicos
Anticonvulsivantes (Consultar capítulo de Convulsões Neonatais)
7- Acidose metabólica
RN <= 1500 gr: manter pH > 7.20
RN > 1500 gr: manter pH > 7.25
Risco de tetania, convulsões, pela diminuição do cálcio ionizado, após correção
da acidose.
8- Infecções:
Uso do antibiótico dependendo da sensibilidade da bactéria, tendo a dose ajustada
ao grau de distúrbio renal. (ver tabela)
Intervalos para Administração de Antibióticos na Insuficiência Renal
IR moderada+
IR grave Ampicilina
6 horas
6 horas (evitar dose alta)
Carbenecilina
6-12 horas
12-16 horas
Cefalotina
6 horas
8-12 horas
Cloranfenicol
6 horas
8-12 horas
Gentamicina
12-24 horas
48 horas
Kanamicina
24-72 horas
72-96 horas
Penicilina
OBS.: Digoxina
8 horas
36 horas
12-16 horas
36-72 horas
+IRA moderada : creatinina de 3-5 mg%
- IRA grave
: creatinina acima de 5 mg%
Considerar a substituição de aminoglicosídeos por aztreonam, e de vancomicina por
teicoplanina.
9- Diálise
Diálise peritoneal é preferível em relação à hemodiálise (dificuldades técnicas).
Indicações:
Acidose intratável
Hipercalemia intratável;
Hipernatremia
Expansão anormal do fluído extracelular com hipertensão e insuficiência cardíaca
congestiva. Rápida deterioração na condição clínica geral (convulsão, coma)
Solução de Diálise a ser usada deve conter bicarbonato, pois solução com lactato aumenta
o risco de acidose lática). Usar:
volume: de 25-50 ml/kg por ciclo, com tempo de permanência entre 30-60 minutos.
Contra-indicações:
Peritonite , enterocolite necrosante
Coagulopatia
Derivação ventrículo-peritoneal
Íleo paralítico
Insuficiência respiratória (vigiar expansibilidade pulmonar).
Na presença de contra-indicação da diálise peritoneal, indicase a Hemofiltração Artério-venosa contínua (tem o inconveniente da necessidade
de heparinização contínua e reposição de fluidos). A hemodiálise é dificilmente
empregada no período neonatal.
MÉTODO:
Realizar a omentectomia e usar o catéter neonatal Tenkoff:
1. Realizar dois ou três banhos de prova, com tempo de permanência zero (banhos
contínuos).
2. Iniciar os banhos com solução a 1,5%
3. Volume de troca: 10-20 ml/kg
4. Tempo do ciclo: primeiras horas ( Infusão: 5 minutos, tempo de permanência: 45
minutos, drenagem: 10 minutos). Tempos de permanência menores melhoram a
troca de solutos de baixo peso molecular.
5. Heparina: usar 250 UI por litro de dialisado
6. Temperatura 38ºC
7. Banhos: Isotônicos: 1,5%, Hipertônicos: 4,25%. Depende da quantidade de
volume a ser retirada (banhos hipertônicos causam maior irritação peritoneal).
8. Potássio: acrescentar nos banhos na concentração de 4mEq/l, quando o potássio
sérico cair abaixo de 4mEq/L
9. Infecção: em caso de suspeita, colher líquido peritoneal e enviar para análise e
cultura. Peritonite 100 leucóciots/mm3
10. Acidose: o dialisado contém lactato como tampão. Bebês e pacientes com
insuficiência hepática não conseguem converter lactato em bicarbonato. Não se
deve acrescentar bicarbonato à bolsa, porque ela contém cloreto de
Cálcio que formará cristais com o bicarbonato. Fazer correção com bicarbonato
Endovenoso, se necessário.
11.Realizar a diálise de forma contínua.
1
3
2
4
5
6
1. Bolsa com solução iso ou hipertônica.
2. Med-med
3. Bolsa pequena com solução aquecida para o paciente.
4. Bolsa pequena para drenagem.
5. Med-med
6. Bolsa grande
DIÁLISE PERITONEAL
1 * Transferir da bolsa número 1 (solução isotônica) ou da bolsa número 2 (solução hipertônica) para o
microfix a quantidade de solução conforme prescrição.
2 * Clampear a pinça após transferência.
3 * Transferir a solução do microfix para bolsa intermediária (bolsa n. 03 )fechar clamp.
4 * Após aquecimento da solução, abrir o clamp e infundir a solução na cavidade abdominal do recém
nascido. Fechar o clamp.
5 * Anotar o início e o término da infusão.
6 * Deixar a solução na cavidade o tempo determinado na prescrição (tempo de perfusão).
7 * Abrir o clamp na extremidade de saída do circuito e deixar drenar para bolsa pequena (número 3), que
está na parte inferior do carrinho. Fechar o clamp após a drenagem.
8 * Anotar o início e o término da drenagem.
9 * Transferir a solução drenada (bolsa número 4) para o microfix . 2, fechar o clamp anotar o volume e
transferi-lo para a bolsa número 4 ( final ) . No ítem observações registrar o aspecto da solução drenado
e/ou intercorrências.
Obs : Ao terminar a infusão da solução para o recém nascido e fechar o clamp , voltar a preencher a bolsa
intermediária ( número 2) com a solução prescrita e deixá-la na placa em aquecimento.
10 * Anotar no ítem balanço, a diferença entre o volume infundido(solução ) e o volume
drenado(total).Registrar o balanço como negativo quando a drenagem for maior que a infusão e positivo
quando a infusão for maior que a drenagem.
PROGNÓSTICO:
- Mortalidade 33 - 78%:
Depende da natureza e severidade da lesão renal
inicial e habilidade com que os distúrbios bioquímicos são manuseados
- Critérios de mau prognóstico:
Anúria de 4 dias ou mais
Falta de visualização renal pela cintilografia.
Bibliografia
1.Marques A. Insuficiência Renal Aguda. In: Marba STM, Filho Mezzacappa F. Manual de
Neonatologia. UNICAMP- Revinter, Rio de Janeiro, pg 147, 1998.
2.Kemper MJ, Harps E, Muller - Wiefel DE. Hyperkalemia: therapeutic options in acute
and chronic renal failure. Clin Nephrol 46: 67, 1996
3.Lorenz JM, Kleinman LI, Markarian K. Potassium metabolism in extremely low birth
weight infants in the first week of life. J Pediatr 131: 81, 1997
4.Margotto PR. Insuficiência renal aguda. Boletim Informativo Pediátrico- BIP (Brasília),
N º 42, 1985.
5.Atiyeh BA, Dabbagh SS, Gruskin AB. Evaluation of renal function during childhood.
Pediatr Rev 17:175, 1996.
6.Stewart CL, Barnett R. Acute renal failure in infants, children, and adults. Crit Care Clin
13:575, 1997.
7.Sherbotie JR. Insuficiência renal no recém-nascido. In: Polin RA, Yoder MC, Burg FD.
Neonatologia Prática, 2ª Edição, Artes Médicas, Porto Alegre, pg 315, 1996.
8.Huet F, Semama D, Grimaldi M, Guignard JP, Gouyon JB. Effects of theophylline on
renal insufficiency in neonates with respiratory distress syndrome. Intensive Care Med
21:511, 1995.
9.Rahman N et al. Renal failure in the perinatal period. Clin Perinatol 8: 241, 1981.
10.Procianoy SR. Choque no recém-nascido. In. Margotto PR. Boletim Informativo
Pediátrico (BIP), Brasília, N° 64, pg 179, 2001
11- Gaissmaier RE, Pohlandt F. Single-dose Dexamethasone Treatment of Hypotension in
Premature Infants. J Pediatr 134:70, 1999
12- Bourchier D. Randomised trial of dopamine compared with hydrocortisone for
treatment of hypotensive very low birthweight infants. – Arch Dis Child Fetal Neonatal Ed
76: F174, 1997
12.Karlowicz MG, Aldeman RD. Nonoliguric and oliguric acute renal failure in
asphyxiated term neonates. Pediatr Nefhrol 9: 718, 1995
13.Miranda LEV. Distúrbios do metabolismo do sódio no período neonatal. In. Margotto
PR. Boletim Informativo Pediátrico (BIP), Brasília, N° 64, pg 153, 2001
14.Suporte avançado de vida em pediatria. American Academy of Pediatrics. American
Heart Association, American Heart association Capítulo 6, pag 13, 1977.
15.Chameides L, Hazinski M.Fluidoterapia e Medicação. American Academy of
Pediatrics/Amwerican Heart Association, pg 6-1, 1997
16-Kluckow M. Avaliação do fluxo sanguíneo sistêmico no recém-nascido pré-termo,
Complicações do baixo fluxo sistêmico e Tratamento da hipotensão arterial ou fluxo
sanguíneo baixo no recém-nascido prematuro. In. Margotto PR. Suporte cardiovascular no
recém-nascido pré-termo extremo. Boletim Informativo Pediátrico (BIP), N° 66, pg 140,
2003