1) O NOCl gasoso se decompõe, em determinadas condições, em NO e Cl2 também
gasosos. No estudo da cinética da decomposição do NOCl foram obtidos os
seguintes dados:
[NOCl] (mol.L-1)
0,20
0,40
0,60
-1 -1
-9
-9
Velocidade (mol.L .s )
1,60 x 10
6,40 x 10
1,44 x 10-8
Indicar a alternativa que contém a expressão correta da velocidade e a constante de
velocidade (k) para a reação de decomposição do NOCl.
a) K.[NOCl]; k = 8 x 10-9 s-1
b) K.[NOCl].[NO].[Cl2]; k = 8 x 10-9 L. mol-1. s-1
c) K.[NOCl]2.[NO]; k = 4 x 10-8 .s-1
d) K.[NOCl]2. k = 4 x 10-8 L. mol-1. s-1
e) K.[NOCl]3. k = 4 L. mol-1. s-1
2) A velocidade da reação
(CH3CO)2O + 2 C2H5OH 2 CH3COOC2H5 + H2O
é igual a k . [(CH3CO)2º] . [C2H5OH]2 sob certas condições. A reação é de:
a) Ordem zero
b) 1ª ordem
c) 2ª ordem
d) 3ª ordem
e) 4ª ordem
3) Dados experimentais sobre a reação do brometo de t-butila com hidroxila, a 55oC
(CH3)3CBr + OH- (CH3)3COH + BrConcentrações iniciais (mol/L)
Velocidade
(mol.L-1.s-1)
(CH3)3CBr
OH1
0,10
0,10
0,0010
2
0,20
0,10
0,0020
3
0,30
0,10
0,0030
4
0,10
0,20
0,0010
5
0,10
0,30
0,0010
Assinale a opção que contém a expressão da velocidade dessa reação.
a) V = k.[ (CH3)3CBr]
b) V = [OH-]
c) V = k.[ (CH3)3CBr]2. [OH-]
d) V = k.[ (CH3)3CBr]3. [OH-]2
e) V = k.[ (CH3)3CBr]. [OH-]
4) A reação de decomposição do NaClO realiza-se em duas etapas:
I.
2 NaClO Na Cl + NaClO2 (lenta)
II.
NaClO2 + NaClO NaCl +NaClO3 (rápida)
A equação da velocidade desta composição é:
a) V = k.[ NaClO2]
b) V = k.[ NaClO2].[ NaClO]
c) V = k.[ NaClO3]
d) V = k.[NaCl].[ NaClO2]
e) V = k.[ NaClO]2
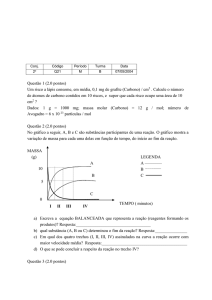
5) Numa reação que ocorre em solução (reação I), há o desprendimento de oxigênio e a
sua velocidade pode ser medida pelo volume do O2(g) desprendido. Uma outra
reação (reação II) ocorre nas mesmas condições, porém consumindo O2(g) e este
consumo mede a velocidade desta reação. O gráfico representa os resultados
referentes às duas reações:
Considerando as duas horas iniciais, qual das reações tem velocidade maior?
Justifique a sua resposta.
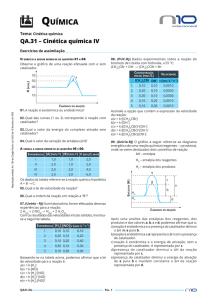
6) Soluções de água oxigenada, H2O2, decompõem-sedando água e gás oxigênio. A
figura a seguir representa a decomposição de três soluções de água oxigenada em
função do tempo, sendo que uma delas foi catalisada por óxido de ferro (III), Fe2O3.
a) Qual das curvas representa a reação mais lenta? Justifique em função do gráfico.
b) Qual das curvas representa a reação catalisada? Justifique em função do gráfico.