CAPÍTULO
e51
Doença das Altitudes
udes
Buddha Basnyat
Geoffrey Tabin
Doença das Altitudes
■ DOENÇA AGUDA DAS MONTANHAS E EDEMA CEREBRAL DAS
GRANDES ALTITUDES
A DAM é uma síndrome neurológica causada por sintomas inespecíficos (cefaleia, náuseas, fadiga e tontura) com poucos achados físicos
que se desenvolvem 6-12 horas após a subida para uma grande altitude. A DAM deve ser diferenciado de exaustão, desidratação, hipotermia, ressaca por álcool e hiponatremia. Acredita-se que a DAM e
o ECGA representem extremidades opostas de um contínuo de distúrbios neurológicos relacionados com a altitude. O ECGA (mas não
A DAM) é uma encefalopatia cujos achados principais são ataxia e
alteração de consciência com envolvimento cerebral difuso, mas geralmente sem déficits neurológicos focais. A progressão dessas manifestações pode ser rápida. Também pode ser visto papiledema e, com
maior frequência, hemorragias retinianas. As hemorragias retinianas
ocorrem com frequência acima de 5.000 metros, mesmo em pessoas
sem sintomas clínicos de DAM ou ECGA. Não está claro se as hemorragias retinianas e as hemorragias cerebrais em grandes altitudes
são causadas pelo mesmo mecanismo; porém, um relato revelou uma
correlação entre ECGA e retinopatia.
Fisiopatologia
O mecanismo exato que causa essa síndrome é desconhecido. As
evidências apontam para um processo no sistema nervoso central.
Estudos com RM sugeriram que edema cerebral vasogênico (intersticial) é um componente da fisiopatologia do ECGA. No contexto do
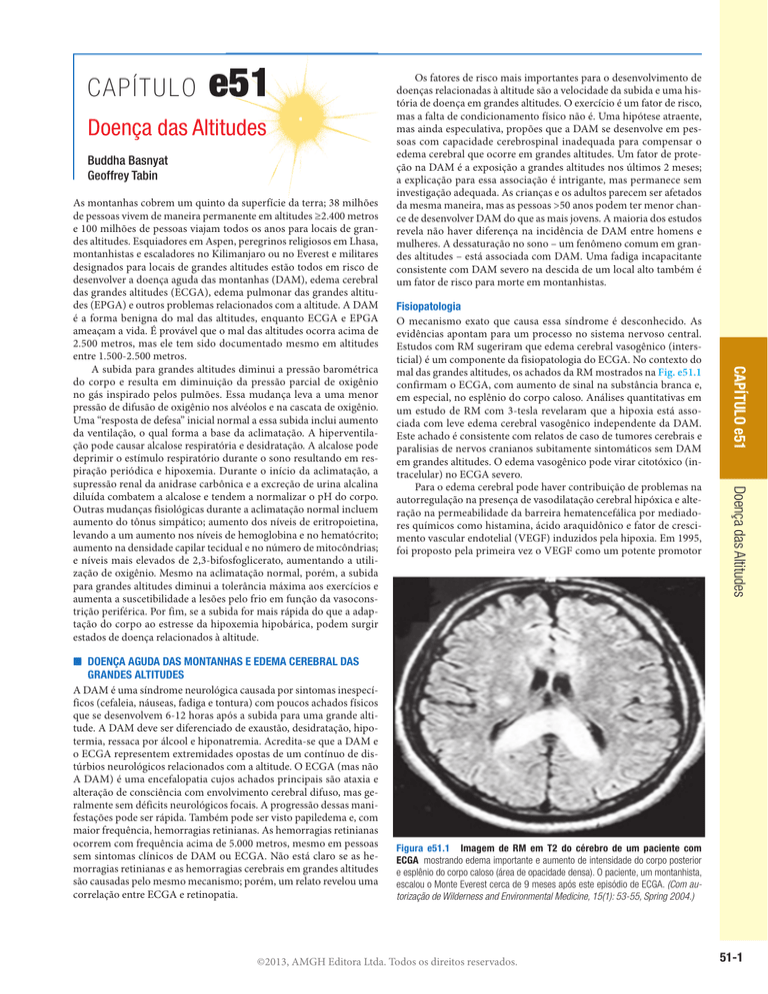
mal das grandes altitudes, os achados da RM mostrados na Fig. e51.1
confirmam o ECGA, com aumento de sinal na substância branca e,
em especial, no esplênio do corpo caloso. Análises quantitativas em
um estudo de RM com 3-tesla revelaram que a hipoxia está associada com leve edema cerebral vasogênico independente da DAM.
Este achado é consistente com relatos de caso de tumores cerebrais e
paralisias de nervos cranianos subitamente sintomáticos sem DAM
em grandes altitudes. O edema vasogênico pode virar citotóxico (intracelular) no ECGA severo.
Para o edema cerebral pode haver contribuição de problemas na
autorregulação na presença de vasodilatação cerebral hipóxica e alteração na permeabilidade da barreira hematencefálica por mediadores químicos como histamina, ácido araquidônico e fator de crescimento vascular endotelial (VEGF) induzidos pela hipoxia. Em 1995,
foi proposto pela primeira vez o VEGF como um potente promotor
CAPÍTULO e51
As montanhas cobrem um quinto da superfície da terra; 38 milhões
de pessoas vivem de maneira permanente em altitudes ≥2.400 metros
e 100 milhões de pessoas viajam todos os anos para locais de grandes altitudes. Esquiadores em Aspen, peregrinos religiosos em Lhasa,
montanhistas e escaladores no Kilimanjaro ou no Everest e militares
designados para locais de grandes altitudes estão todos em risco de
desenvolver a doença aguda das montanhas (DAM), edema cerebral
das grandes altitudes (ECGA), edema pulmonar das grandes altitudes (EPGA) e outros problemas relacionados com a altitude. A DAM
é a forma benigna do mal das altitudes, enquanto ECGA e EPGA
ameaçam a vida. É provável que o mal das altitudes ocorra acima de
2.500 metros, mas ele tem sido documentado mesmo em altitudes
entre 1.500-2.500 metros.
A subida para grandes altitudes diminui a pressão barométrica
do corpo e resulta em diminuição da pressão parcial de oxigênio
no gás inspirado pelos pulmões. Essa mudança leva a uma menor
pressão de difusão de oxigênio nos alvéolos e na cascata de oxigênio.
Uma “resposta de defesa” inicial normal a essa subida inclui aumento
da ventilação, o qual forma a base da aclimatação. A hiperventilação pode causar alcalose respiratória e desidratação. A alcalose pode
deprimir o estímulo respiratório durante o sono resultando em respiração periódica e hipoxemia. Durante o início da aclimatação, a
supressão renal da anidrase carbônica e a excreção de urina alcalina
diluída combatem a alcalose e tendem a normalizar o pH do corpo.
Outras mudanças fisiológicas durante a aclimatação normal incluem
aumento do tônus simpático; aumento dos níveis de eritropoietina,
levando a um aumento nos níveis de hemoglobina e no hematócrito;
aumento na densidade capilar tecidual e no número de mitocôndrias;
e níveis mais elevados de 2,3-bifosfoglicerato, aumentando a utilização de oxigênio. Mesmo na aclimatação normal, porém, a subida
para grandes altitudes diminui a tolerância máxima aos exercícios e
aumenta a suscetibilidade a lesões pelo frio em função da vasoconstrição periférica. Por fim, se a subida for mais rápida do que a adaptação do corpo ao estresse da hipoxemia hipobárica, podem surgir
estados de doença relacionados à altitude.
Os fatores de risco mais importantes para o desenvolvimento de
doenças relacionadas à altitude são a velocidade da subida e uma história de doença em grandes altitudes. O exercício é um fator de risco,
mas a falta de condicionamento físico não é. Uma hipótese atraente,
mas ainda especulativa, propões que a DAM se desenvolve em pessoas com capacidade cerebrospinal inadequada para compensar o
edema cerebral que ocorre em grandes altitudes. Um fator de proteção na DAM é a exposição a grandes altitudes nos últimos 2 meses;
a explicação para essa associação é intrigante, mas permanece sem
investigação adequada. As crianças e os adultos parecem ser afetados
da mesma maneira, mas as pessoas >50 anos podem ter menor chance de desenvolver DAM do que as mais jovens. A maioria dos estudos
revela não haver diferença na incidência de DAM entre homens e
mulheres. A dessaturação no sono – um fenômeno comum em grandes altitudes – está associada com DAM. Uma fadiga incapacitante
consistente com DAM severo na descida de um local alto também é
um fator de risco para morte em montanhistas.
Figura e51.1 Imagem de RM em T2 do cérebro de um paciente com
ECGA mostrando edema importante e aumento de intensidade do corpo posterior
e esplênio do corpo caloso (área de opacidade densa). O paciente, um montanhista,
escalou o Monte Everest cerca de 9 meses após este episódio de ECGA. (Com autorização de Wilderness and Environmental Medicine, 15(1): 53-55, Spring 2004.)
©2013, AMGH Editora Ltda. Todos os direitos reservados.
51-1
PARTE XIX
de vazamento capilar no cérebro em grandes altitudes e estudos em
ratos sustentaram este papel. Embora os estudos preliminares com o
VEGF em montanhistas tenham alcançado resultados inconsistentes
e não tenham revelado associação com o mal das altitudes, evidências indiretas deste papel para esse fator de crescimento na DAM e
no ECGA surgiram da observação de que a dexametasona, quando
usada na prevenção e tratamento de DAM e ECGA, bloqueia a suprarregulação hipóxica do VEGF. Outros fatores no desenvolvimento
do edema cerebral podem ser a liberação de óxido nítrico mediada
pelo cálcio e de adenosina mediada por neurônios promovendo a vasodilatação cerebral.
O aumento da atividade simpática desencadeado pela hipoxia
também pode contribuir para quebra da barreira hematencefálica.
Tem sido notado aumento no diâmetro da bainha do nervo óptico
conforme o aumento na gravidade do MAM, sugerindo um papel
importante para o aumento das pressões intracranianas na fisiopatologia da DAM. Por fim, o efeito da hipoxia em espécies reativas
oxidantes e o papel dessas espécies na DAM clínico não estão claros.
A fisiopatologia do sintoma mais comum e proeminente da
DAM – cefaleia – permanece incerta, pois o cérebro é um órgão insensível; apenas as meninges contêm fibras nervosas sensitivas do
trigêmeo. A causa da cefaleia das grandes altitudes é multifatorial;
vários fatores químicos e mecânicos ativam uma via final comum:
o sistema trigeminovascular. Na gênese da cefaleia das grandes altitudes a resposta aos anti-inflamatórios não esteroides (AINEs) e aos
glicocorticoides fornece evidências indiretas para o envolvimento de
inflamação e das vias do ácido araquidônico. Embora a International
Headache Society reconheça que as grandes altitudes possam desencadear a enxaqueca, não está claro se a cefaleia das grandes altitudes e
a enxaqueca têm a mesma fisiopatologia. Porém, o sumatriptano (50
mg por via oral dentro de 1 hora da subida) evita a DAM.
Doenças das Altas Altitudes e Doença Descompressiva
Prevenção e tratamento (Quadro e51.1)
A subida gradual, com tempo adequado para a aclimatação, é o melhor método para a prevenção do mal das altitudes. Acima de 3.000
QUADRO e51.1
metros, costuma ser recomendada uma subida gradual de ≤300 metros a partir da altitude em que a pessoa dormiu no dia anterior, sendo útil usar cada terceiro dia de ganho em altitude do sono como dia
extra para a aclimatação. Passar uma noite em uma altitude intermediária antes de subir mais pode aumentar a aclimatação e atenuar o
risco de DAM. Com certeza um itinerário flexível que permita dias
de repouso adicionais será útil. Viajantes em regiões de grandes altitudes devem estar alertados sobre os sintomas do mal das altitudes e
devem ser encorajados a não subir mais se surgirem esses sintomas.
Qualquer suspeita de EPGA (veja adiante) ou ECGA obriga a descer.
A profilaxia farmacológica no momento da viagem a grandes altitudes é necessária para pessoas com história de DAM ou quando
não é possível uma subida gradual e uma aclimatação – p. ex., quando há necessidade de subir rapidamente para propósitos de resgate
ou quando o voo para uma grande altitude é necessário. A acetazolamida (125-250 mg 2 x/dia) administrada por 1 dia antes da subida
e continuada por 2-3 dias é efetiva. Parestesias e sensação de formigamento são parefeitos comuns da acetazolamida. A dexametasona
(8 mg/dia em doses divididas) também é efetiva. Um grande ensaio
randomizado duplo-cego e controlado com placebo em montanhistas com aclimatação parcial mostrou claramente que o Ginkgo biloba
não é efetivo na prevenção de DAM. Até o momento não foi relatado
nenhum ensaio com AINEs na prevenção de DAM.
Para o tratamento de DAM leve pode ser adequado o uso apenas
de repouso e analgésicos. A descida e o uso de acetazolamida e (se
disponível) oxigênio são suficientes para tratar a maioria dos casos
de DAM moderada. Mesmo uma descida pequena (400-500 metros)
pode ser adequada para alívio dos sintomas. Para DAM moderada
ou ECGA inicial a dexametasona (8 mg por via oral ou parenteral)
é altamente efetiva. Para o ECGA, a descida imediata é mandatória.
Quando a descida não é possível em função de condições climáticas
ruins ou escuridão, uma simulação de descida em uma câmara hiperbárica portátil é efetiva e, como a administração de dexametasona,
ela “poupa tempo”. Como a nifedipina, os inibidores da fosfodiesterase-5 não têm lugar no tratamento de DAM ou ECGA.
Manejo do mal das altitudes
Condição
Manejo
a
Doença aguda das montanhas (DAM) leve
Interrupção da subida
Tratamento com acetazolamida (250 mg a cada 12 horas)
b
Descida
a
DAM moderada
Descida imediata para sintomas crescentes
Uso de oxigênio em baixo fluxo quando disponível
c
Tratamento com acetazolamida (250 mg a cada 12 horas) e/ou dexametasona (4 mg a cada 6 horas)
d
Terapia hiperbárica
Edema cerebral de grandes altitudes (ECGA)
Evacuação ou descida imediata
Administração de oxigênio (2-4 L/min)
Tratamento com dexametasona (8 mg VO/IM/IV; depois, 4 mg a cada 6 horas)
Terapia hiperbárica se a descida não for possível
Edema pulmonar de grandes altitudes (EPGA)
Evacuação ou descida imediata
Minimização de exercícios mantendo-se o paciente aquecido
Administração de oxigênio (4-6 L/min) para obter saturação de O2 >90%
e
Terapia adjunta com nifedipina (30 mg de liberação lenta a cada 12 horas)
Terapia hiperbárica se a descida não for possível
a
A classificação dos casos como leves ou moderados é sujeita ao julgamento baseado na gravidade da cefaleia e na presença e intensidade de outras manifestações (náuseas, fadiga, tontura, insônia).
Não há altitude fixa especificada; o paciente deve descer para um ponto abaixo daquele em que os sintomas surgiram.
c
A acetazolamida trata e a dexametasona mascara os sintomas. Para a prevenção (ao contrário do tratamento), pode-se usar 125-250 mg de acetazolamida a cada 12 horas ou (quando a acetazolamida está contraindicada – p. ex., em pessoas com alergia à sulfa) 4 mg de dexametasona a cada 12 horas.
d
Na terapia hiperbárica o paciente é colocado em um saco ou câmara portátil de altitude para simular a descida.
e
A nifedipina (30 mg de liberação lenta a cada 12 horas) também é efetiva para a prevenção do EPGA da mesma maneira que salmeterol (125 g inalados 2 x/dia), taladafil (10 mg 2 x/dia) ou
dexametasona (8 mg 2 x/dia).
b
51-2
©2013, AMGH Editora Ltda. Todos os direitos reservados.
Doença das Altitudes
Fisiopatologia
O EPGA é um edema pulmonar não cardiogênico que se caracteriza
por vasoconstrição pulmonar focal que causa perfusão excessiva em
algumas regiões. Essa anormalidade leva, por sua vez, a um aumento na pressão capilar pulmonar (>18 mm Hg) e a uma falha capilar
de “estresse”. O mecanismo exato para a vasoconstrição não é conhecido. A disfunção endotelial por hipoxia pode ter um papel por
prejudicar a liberação de óxido nítrico, um vasodilatador derivado
do endotélio. Em grandes altitudes as pessoas propensas ao EPGA
têm níveis reduzidos de óxido nítrico exalado. A efetividade dos
inibidores da fosfodiesterase-5 no alívio da hipertensão pulmonar
induzida pela altitude, na diminuição da tolerância aos esforços e
na hipoxemia sustenta o papel do óxido nítrico na patogênese do
EPGA. Um estudo demonstrou que o uso profilático de taladafil,
um inibidor da fosfodiesterase-5, diminui em 65% o risco de EPGA.
Por outro lado, o endotélio também sintetiza a endotelina-1, um potente vasoconstritor cujas concentrações são mais elevadas do que
a média em montanhistas propensos ao EPGA. A bosentana, um
antagonista do receptor de endotelina, atenua a hipertensão pulmonar induzida pela hipoxia, mas há necessidade de mais estudos de
campo com esse fármaco.
O exercício e o frio levam ao aumento da pressão intravascular
pulmonar e podem predispor ao EPGA. Além disso, elevações no tônus simpático desencadeadas pela hipoxia podem causar venoconstrição pulmonar e extravasamento desde os capilares pulmonares até
os alvéolos. Consistente com esse conceito, a fentolamina, a qual faz
bloqueio alfa-adrenérgico, melhora a hemodinâmica e a oxigenação
no EPGA mais do que outros vasodilatadores. Os estudos com taladafil citados anteriormente também investigaram a dexametasona
na prevenção do EPGA. De maneira surpreendente, a dexametasona
reduziu em 78% a incidência de EPGA – uma diminuição maior do
que com o taladafil. Além da possibilidade de aumentar a disponibilidade de óxido nítrico endotelial, a dexametasona pode ter alterado
a atividade simpática excessiva associada com o EPGA: a frequência
cardíaca dos participantes no braço do estudo com dexametasona diminuiu de maneira significativa. Por fim, as pessoas suscetíveis ao
EPGA também mostram atividade simpática aumentada durante respiração hipóxica por curto prazo em pequenas altitudes.
Como muitos pacientes com EPGA têm febre, leucocitose periférica e aumento na velocidade de sedimentação globular, a inflamação
tem sido considerada como fator etiológico no EPGA. Porém, evidências fortes sugerem que a inflamação no EPGA seja um epifenômeno em vez de causa primária. Todavia, processos inflamatórios (p.
ex., aqueles desencadeados por infecções virais do trato respiratório)
predispõem as pessoas ao EPGA – mesmo aquelas que são constitucionalmente resistentes a essa complicação.
Outro mecanismo proposto para o EPGA é um problema na
eliminação transepitelial de sódio e água a partir dos alvéolos. Os
agonistas beta-adrenérgicos fazem suprarregulação da eliminação
do fluido alveolar em modelos animais. Em um estudo randomizado
duplo-cego e controlado com placebo de montanhistas suscetíveis ao
EPGA, a inalação profilática do agonista beta-adrenérgico salmeterol
reduziu em 50% a incidência de EPGA. Outros efeitos dos beta-agonistas também podem contribuir para a prevenção do EPGA, mas
esses achados também sugerem que a eliminação do líquido alveolar
pode desempenhar um papel patogênico nessa doença.
CAPÍTULO e51
■ EDEMA PULMONAR DE GRANDES ALTITUDES
Diferente do ECGA (um problema neurológico), o EPGA é primariamente um problema pulmonar e, dessa forma, não precisa ser precedido por DAM. O EPGA se desenvolve dentro de 2-4 dias após a
chegada em uma grande altitude; ele raras vezes ocorre após mais
do que 4 ou 5 dias na mesma altitude, provavelmente em função do
remodelamento e adaptação que deixam a vasculatura pulmonar
menos suscetível aos efeitos da hipoxia. Uma rápida velocidade de
subida, história de EPGA, infecções do trato respiratório e temperaturas geladas são fatores de risco. Os homens são mais suscetíveis do
que as mulheres. As pessoas com anormalidades da circulação cardiopulmonar que levam à hipertensão pulmonar – p. ex., forame oval
patente, estenose mitral, hipertensão pulmonar primária e ausência
unilateral da artéria pulmonar – têm risco aumentado de EPGA,
mesmo em altitudes moderadas. Por exemplo, o forame oval patente
é quatro vezes mais comum entre pessoas suscetíveis a EPGA em relação à população geral. A ecocardiografia está recomendada quando
houver desenvolvimento de EPGA em altitudes relativamente pequenas (<3.000 metros) e sempre que houver suspeita de anormalidades
cardiopulmonares que predisponham a EPGA.
A manifestação inicial de EPGA pode ser uma redução na tolerância aos esforços maior do que a esperada naquela altitude. Embora uma tosse seca e persistente possa anunciar o EPGA e possa ser
seguida pela produção de escarro hemático, a tosse nas montanhas é
quase universal e o mecanismo não é bem compreendido. Taquipneia
e taquicardia, mesmo em repouso, são marcadores importantes à medida que a doença progride. Podem ser ouvidos estertores na ausculta, mas eles não são diagnósticos. O EPGA pode estar acompanhado
por ECGA. Opacidades focais ou localizadas (Fig. e51.2) ou edema
intersticial linear podem ser notados na radiografia de tórax. No passado, o EPGA era confundido com pneumonia causada pelo frio ou
com insuficiência cardíaca devido à hipoxia e ao exercício. Não são
vistas as linhas B de Kerley nem o padrão de asas de morcego na
radiografia. O eletrocardiograma pode revelar sobrecarga ou mesmo
hipertrofia de ventrículo direito. A hipoxemia e a alcalose respiratória estão presentes de maneira consistente a menos que o paciente
esteja usando acetazolamida, quando então pode haver acidose metabólica. A gasometria arterial não é necessária na avaliação do EPGA;
uma leitura da saturação de oxigênio com oxímetro de pulso costuma
ser suficiente. A existência de uma forma subclínica de EPGA provavelmente tenha sido sugerida por um aumento no gradiente alvéolo-arterial de oxigênio em montanhistas no Everest próximos do pico,
mas não há evidências concretas que correlacionem essa anormalidade com o desenvolvimento de EPGA clinicamente relevante.
GENÉTICA
Figura e51.2 Radiografia de tórax de um paciente com EPGA mostrando
opacidade nos campos médio e inferior à direita simulando uma consolidação pneumônica. A opacidade melhorou de forma quase completa em 2 dias com descida e
oxigênio.
O fator induzido pela hipoxia, o qual é importante na
adaptação a grandes altitudes, controla as respostas transcricionais à hipoxia por todo o corpo, estando envolvido
na liberação de VEGF no cérebro, eritropoiese e outras
funções pulmonares e cardíacas em grandes altitudes. O
fator induzido pela hipoxia é regulado por meio de degradação proteassomal dependente de oxigênio e, assim, responde a variações na
©2013, AMGH Editora Ltda. Todos os direitos reservados.
51-3
disponibilidade de oxigênio. Embora o polimorfismo genético possa
influenciar a suscetibilidade ao EPGA, os dados até o momento não
estão claros. O polimorfismo genético na sintase de óxido nítrico endotelial tem sido associado com suscetibilidade ao EPGA no Japão,
mas não na Europa. Embora o polimorfismo do gene da enzima conversora da angiotensina pareça conferir uma vantagem de desempenho em grandes altitudes, não há associação com a suscetibilidade
ao EPGA.
PARTE XIX
Doenças das Altas Altitudes e Doença Descompressiva
51-4
Prevenção e tratamento (Tabela e51.1)
Permitir tempo suficiente para a aclimatação subindo de maneira
gradual (como discutido anteriormente para DAM e ECGA) é a melhor maneira de evitar o EPGA. A nifedipina de liberação lenta (30
mg) administrada uma ou duas vezes ao dia, previne o EPGA em
pessoas que devem subir rapidamente ou que têm história de EPGA.
Outros fármacos para a prevenção de EPGA estão listados na Tabela
e51.1 (nota de rodapé e). Embora a dexametasona esteja listada para
a prevenção, o seu perfil de efeitos adversos requer monitoramento
cuidadoso. Tem sido demonstrado que a acetazolamida atenua a vasoconstrição pulmonar hipóxica e essa observação merece estudos
adicionais na prevenção de EPGA. Porém, um estudo não conseguiu
demonstrar diminuição na vasoconstrição pulmonar em pessoas
parcialmente aclimatadas que receberam acetazolamida.
O reconhecimento precoce é fundamental no tratamento do
EPGA, em especial quando ele não é precedido por sintomas de
MAM como cefaleia e náuseas. Fadiga e dispneia em repouso podem
ser as únicas manifestações iniciais. A descida e o uso de oxigênio
suplementar (visando deixar a saturação >90%) são as intervenções
terapêuticas mais efetivas. O esforço físico deve ser mínimo e o paciente deve ser mantido aquecido. A terapia hiperbárica em câmara
portátil de altitude pode ser usada se a descida não for possível e se
não houver disponibilidade de oxigênio. A nifedipina oral de liberação lenta (30 mg 1-2 x/dia) pode ser usada como terapia adjunta. Os
beta-agonistas inalatórios, que são seguros e fáceis de carregar, são
úteis na prevenção do EPGA e podem ser efetivos no seu tratamento, embora nenhum ensaio tenha sido realizado ainda. A inalação
de óxido nítrico e a pressão positiva na expiração também podem
ser medidas terapêuticas úteis, mas podem não estar disponíveis nas
grandes altitudes. Nenhum estudo investigou os inibidores da fosfodiesterase-5 no tratamento do EPGA, mas relatos têm descrito o seu
uso na prática clínica. Os pontos principais do tratamento permanecem sendo a descida e (quando disponível) o oxigênio.
No caso de DAM, se os sintomas melhorarem (com ou sem acetazolamida), o paciente pode voltar a subir de maneira gradual para
maiores altitudes. Diferente da síndrome do desconforto respiratório
agudo (outra forma de edema pulmonar não cardiogênico), a arquitetura pulmonar no EPGA costuma estar bem preservada, havendo rápida reversão das anormalidades (Figura e51.2). Este fato tem
permitido que algumas pessoas com EPGA voltem a subir de forma
gradual após alguns dias de descida e repouso. No ECGA não é aconselhável voltar a subir após alguns dias.
■ OUTROS PROBLEMAS DE GRANDES ALTITUDES
Problemas do sono
Os mecanismos subjacentes aos problemas do sono, os quais estão
entre as reações adversas mais comuns em grandes altitudes, incluem
aumento da respiração periódica, mudanças na arquitetura do sono
com aumento do tempo em estágios de sono mais leve e mudanças no sono REM. Os viajantes devem ser tranquilizados de que a
qualidade do sono melhora com a aclimatação. Nos casos em que
há necessidade de usar fármacos, a acetazolamida (125 mg antes de
deitar) é especialmente útil, pois diminui os episódios de hipoxemia
e alivia as interrupções do sono causadas por excesso de respiração
periódica. Não se sabe se a combinação de acetazolamida com temazepam ou zolpidem é mais efetiva do que a administração isolada de
acetazolamida. Usadas em combinação, as doses de temazepam e zolpidem não devem ser aumentadas em >10 mg nas grandes altitudes.
Evidências limitadas sugerem que o diazepam causa hipoventilação
em grandes altitudes e, dessa forma, está contraindicado. Para montanhistas com apneia obstrutiva do sono que fazem uso de máquinas
de pressão positiva contínua nas vias respiratórias (CPAP) que não
fazem compensação de pressão, pode haver necessidade de ajuste nos
parâmetros de pressão.
Problemas gastrintestinais
Em função da pressão atmosférica diminuída e da consequente expansão dos gases intestinais em grandes altitudes, muitos viajantes
experimentam distensão abdominal e flatulência excessiva. Na ausência de diarreia esses fenômenos são normais e, algumas vezes,
desconfortáveis. Porém, a diarreia concomitante pode indicar o envolvimento de bactérias ou do parasita Giardia, que são comuns em
muitos locais de grandes altitudes nos países em desenvolvimento.
Pode haver necessidade de tratamento imediato com líquidos e antibióticos empíricos para combater a desidratação nas montanhas. Por
fim, as hemorroidas são comuns em viagens a grandes altitudes; o
tratamento inclui compressas quentes, aplicação de pomada de hidrocortisona e medidas para evitar a constipação.
Tosse em grandes altitudes
A tosse nas grandes altitudes pode ser muito debilitante e é, algumas
vezes, suficientemente severa para causar fraturas costais, em especial acima de 5.000 metros. É provável que a etiologia seja multifatorial. Embora a tosse em grandes altitudes tenha sido atribuída à
inspiração de ar frio e seco, essa explicação parece não ser suficiente
por si só; em estudos de longa duração em câmaras hipobáricas, a
tosse ocorreu apesar de temperatura e umidade controladas. A implicação é de que a hipoxia também desempenha um papel. O exercício
pode precipitar tosse em grandes altitudes, possivelmente em função
da perda de água no trato respiratório. Os beta-agonistas de longa
duração e os glicocorticoides evitam a broncoconstrição que de outra
forma ocorreria pelo frio e pelo exercício. Em geral, infecções não
costumam ser uma etiologia comum. Relatos isolados têm descrito a
eficácia da inalação de uma combinação de fluticasona e salmeterol
no tratamento da tosse em grandes altitudes. Sabe-se que tanto o salmeterol quanto os glicocorticoides evitam o EPGA, o qual pode ser
uma causa não reconhecida de tosse.
Eventos neurológicos de grandes altitudes não relacionados com
“doença da altitude”
Ataques isquêmicos transitórios (AITs) e AVEs têm sido bem descritos em viajantes de grandes altitudes fora do contexto de doença da
altitude. Porém, essas descrições não se baseiam em causa (hipoxia)
e efeito. A população que sofre AVE e AIT ao nível do mar costuma
ser de uma faixa etária mais elevada com outros fatores de risco, enquanto aqueles acometidos em grandes altitudes são mais jovens e,
provavelmente, têm menos fatores de risco para doença vascular aterosclerótica. Outros mecanismos (p. ex., vasoespasmo, edema focal,
vasoconstrição por hipocapnia, hipoxia em zonas limítrofes de fluxo
sanguíneo cerebral mínimo ou shunts cardíacos da direita para a esquerda) podem agir nos AITs e AVEs de grandes altitudes.
Também têm sido bem descrito a ocorrência de hemorragia subaracnóidea, amnésia global transitória, delirium e paralisias de nervos cranianos (p. ex., paralisia de reto lateral) em grandes altitudes
e fora do contexto de doença das altitudes. A síncope é comum em
altitudes moderadamente grandes, costuma ocorrer logo após a subida e parece ser um evento vasovagal relacionado com a hipoxemia.
Raras vezes ocorrem convulsões com ECGA, mas hipoxemia e hipocapnia, as quais são prevalentes em grandes altitudes, são desencadeantes bem conhecidos que podem contribuir para convulsões
novas ou para a sua recorrência em pessoas predispostas. Contudo, o
consenso entre especialistas é de que os viajantes com epilepsia bem
controlada podem subir em grandes altitudes. Problemas oftalmológicos, como cegueira cortical, amaurose fugaz e hemorragias retinianas com envolvimento macular e comprometimento da visão, são
©2013, AMGH Editora Ltda. Todos os direitos reservados.
bem reconhecidos. Problemas visuais por cirurgia refrativa prévia e
visão monocular borrada – pelo uso de um adesivo de escopolamina
(tocando o olho após ter tocado no adesivo) ou pela síndrome do
olho seco – também podem ocorrer em grandes altitudes e podem
ser confundidos com problemas neurológicos. Por fim, as pessoas
com condições de hipercoagulabilidade (p. ex., síndrome antifosfolipídeos, deficiência de proteína C) que são assintomáticas ao nível do
mar podem experimentar trombose venosa cerebral (possivelmente
por aumento da viscosidade sanguínea desencadeado por policitemia
e desidratação) em grandes altitudes. Uma história clínica adequada,
exame físico e investigações laboratoriais sempre que possível ajudarão a definir esses problemas como entidades separadas da doença
das altitudes. A administração de oxigênio (quando disponível) e a
descida imediata formam a base do tratamento da maioria desses
problemas neurológicos.
Obesidade
Embora a residência em grandes altitudes tenha sido sugerida como
forma de controlar a obesidade, também tem sido relatada a obesidade como fator de risco para DAM, provavelmente porque a hipoxemia noturna é mais pronunciada em pessoas obesas. A hipoxemia
também pode causar maior hipertensão pulmonar, dessa forma possivelmente predispondo o montanhista ao EPGA.
Anemia falciforme
A altitude elevada é uma das raras exposições ambientais que algumas vezes provoca uma crise em pessoas com traço falciforme. Mesmo ao atravessar montanhas de apenas 2.500 metros, sabe-se que
as pessoas com anemia falciforme podem ter crises vasoclusivas. A
anemia falciforme deve ser considerada quando viajantes em grandes
altitudes se sentem mal e desenvolvem dor no quadrante superior esquerdo. Os pacientes com anemia falciforme conhecida que precisam
viajar a grandes altitudes devem usar oxigênio suplementar e viajar
com cautela.
Diabetes melito
Subir montanhas em grandes altitudes pode aumentar a captação de
açúcar. Assim, a viagem a grandes altitudes pode não ter problemas
para pessoas com diabetes que estejam bem controladas com hipoglicemiantes orais. Pode ser útil realizar um exame ocular antes da
viagem. Os pacientes que usam insulina podem necessitar de doses
menores nos dias de trilhas/escaladas em relação aos dias de repouso.
Por causa dessas variações, os pacientes diabéticos devem carregar
um medidor de glicose confiável e usar insulinas de ação rápida. O
rápido acesso a doces é também fundamental. É importante que os
acompanhantes de viajantes diabéticos estejam bem esclarecidos de
problemas potenciais como a hipoglicemia.
Doença arterial coronariana
A demanda miocárdica de oxigênio e a frequência cardíaca máxima
são reduzidos em grandes altitudes porque a VO2 máxima diminui
conforme o aumento da altitude. Esse efeito pode explicar o porquê
de não serem vistos sinais de isquemia ou disfunção cardíaca não
serem vistos em pessoas saudáveis em grandes altitudes. As pessoas
assintomáticas e com bom condicionamento físico e sem fatores de
risco não precisam de nenhum teste antes da subida. Para as pessoas
com cardiopatia isquêmica, infarto do miocárdio prévio, angioplastia
e/ou cirurgia de revascularização miocárdica está indicado um teste
de esforço. Um teste de esforço fortemente positivo é uma contraindicação para viagens a grandes altitudes; um teste de esforço negativo
em uma pessoa com estilo de vida ativo ao nível do mar não autoriza
que se contraindique as grandes altitudes. Os pacientes com arritmias
mal controladas devem evitar as viagens a grandes altitudes, mas os
pacientes com arritmias que estão bem controlados com medicação
antiarrítmica não parecem ter risco aumentado.
Doença pulmonar crônica
Dependendo da gravidade da doença e do acesso aos cuidados médicos, a doença pulmonar preexistente pode nem sempre contraindicar
a viagem a grandes altitudes. Deve ser feita uma avaliação adequada
antes da viagem. Pode haver necessidade de oxigênio suplementar
se a PaO2 prevista para a altitude for <50-55 mm Hg. A hipertensão
pulmonar preexistente pode deve ser avaliada nesses pacientes. Se
o resultado for positivo, os pacientes devem ser aconselhados a não
subir a grandes altitudes; se a viagem for necessária, deve ser considerado o tratamento com nifedipina de liberação lenta (20 mg 2 x/dia).
Estudos pequenos têm revelado que quando os pacientes com doença
bolhosa atingem ~5.000 metros observa-se a expansão das bolhas e
o pneumotórax. Um oxímetro de pulso manual pode ser útil para a
verificação da saturação de oxigênio.
Asma
Embora o ar frio e os exercícios possam provocar broncoconstrição
aguda, os pacientes asmáticos costumam ter menos problemas em
Doença renal crônica
Os pacientes com doença renal crônica podem tolerar estadias curtas
em grandes altitudes, mas existe a preocupação teórica sobre a pro-
©2013, AMGH Editora Ltda. Todos os direitos reservados.
Doença das Altitudes
Hipertensão
Em grandes altitudes, o aumento da atividade simpática pode levar a
uma elevação transitória na pressão arterial que raras vezes alcança
níveis perigosamente altos. Os viajantes devem continuar a tomar sua
medicação anti-hipertensiva em grandes altitudes. Os pacientes hipertensos não têm mais chances do que os outros para o desenvolvimento de doença da altitude. Como o provável mecanismo da hipertensão em grandes altitudes é a atividade alfa-adrenérgica, fármacos
que fazem bloqueio alfa-adrenérgico como o prazosin têm sido sugeridos para pacientes sintomáticos e para aqueles com hipertensão
lábil. É melhor começar a tomar o fármaco várias semanas antes da
viagem e carregar um esfigmomanômetro. A nifedipina de liberação
lenta também pode ser útil.
Gestação
Em geral, as gestantes de baixo risco que sobem até 3.000 metros não
têm risco especial exceto pela relativa indisponibilidade de cuidados
médicos em muitas regiões de grandes altitudes, em especial nos países em desenvolvimento. Apesar da falta de dados consistentes sobre
isso, aventurar-se acima de 3.000 metros de altitude, onde a saturação de oxigênio diminui muito rapidamente, não parece aconselhável
para gestantes.
CAPÍTULO e51
■ PROBLEMAS CLÍNICOS PREEXISTENTES
Como a viagem para grandes altitudes é cada vez mais popular, condições comuns como hipertensão, doença arterial coronariana e diabetes são encontradas com frequência cada vez maior entre os viajantes de grandes altitudes. Essa situação é particularmente preocupante
para os milhares de peregrinos idosos com problemas clínicos que visitam áreas sagradas em grandes altitudes (p. ex., no Himalaia) todos
os anos. Embora a maioria desses problemas clínicos não pareça influenciar a suscetibilidade à doença das altitudes, eles podem ser exacerbados pela subida na altitude, pelos exercícios em ambiente frio e
por hipoxemia. O aconselhamento sobre a conveniência da viagem
para grandes altitudes e o impacto da hipoxia resultante nas doenças
preexistentes é cada vez mais relevante, mas não existem diretrizes
baseadas em evidências. Os riscos e benefícios pessoais devem ser
discutidos de maneira clara antes da subida.
altitudes altas em comparação com as baixas, possivelmente em função da diminuição do nível de alergênios e do aumento do nível de
catecolaminas circulantes. Apesar disso, os indivíduos asmáticos devem carregar toda a sua medicação, incluindo glicocorticoides orais,
com instruções adequadas para o uso em caso de uma exacerbação.
As pessoas com asma grave devem ser alertadas para não subirem a
altitudes elevadas.
51-5
gressão para a doença renal terminal. A acetazolamida, o fármaco
prescrito com maior frequência para a doença das altitudes, deve ser
evitado por qualquer pessoa com acidose metabólica preexistente, a
qual pode ser exacerbada pelo medicamento. Além disso, a dose de
acetazolamida deve ser ajustada quando a taxa de filtração glomerular cair abaixo de 50 mL/min e o fármaco não deve ser usado de
forma alguma se esse valor for menor do que 10 mL/min.
PARTE XIX
■ DOENÇA CRÔNICA DAS MONTANHAS E HIPERTENSÃO
PULMONAR DE GRANDES ALTITUDES
A doença crônica das montanhas (também conhecida como doença
de Monge) é uma doença de pessoas que residem por muito tempo
em altitudes acima de 2.500 metros e se caracteriza por eritrocitose
excessiva com hipertensão pulmonar moderada a severa levando a
cor pulmonale. Essa condição foi originalmente descrita na América
do Sul e também tem sido documentada no Colorado e na população
chinesa Han no Tibete. A migração para uma altitude menor resulta
na resolução da doença crônica das montanhas. Venissecção e acetazolamida são úteis.
A hipertensão pulmonar de grandes altitudes também é uma
doença subaguda de pessoas que residem por longo prazo em altitudes elevadas. Diferente da doença de Monge, essa síndrome se caracteriza primariamente por hipertensão pulmonar (sem eritrocitose) levando à insuficiência cardíaca. Soldados indianos vivendo em
extremas altitudes por períodos prolongados e bebês chineses Han
nascidos no Tibete apresentaram respectivamente as formas adulta
e infantil da doença. A hipertensão pulmonar de grandes altitudes é,
sob o ponto de vista patofisiológico, muito semelhante à “doença do
peito inchado” em bovinos. A descida para altitudes menores cura a
doença.
LEITURAS ADICIONAIS
Basnyat B, Murdoch D: High altitude illness. Lancet 361:1967, 2003
——— et al: Neurological conditions of altitude that fall outside the usual defi
nition of altitude sickness. High Alt Med Biol 5:171, 2004
Beall CM et al: Natural selection on EPAS1 (HIF2alpha) associated with low
hemoglobin concentration in Tibetan highlanders. Proc Natl Acad Sci
USA 107:11459, 2010
Gertsch JH et al: Randomised, double blind, placebo controlled comparison
of ginkgo biloba and acetazolamide for prevention of acute mountain sickness among Himalayan trekkers: Th e Prevention of High Altitude Illness
Trial (PHAIT). BMJ 328:797, 2004
Grocott MP et al: Arterial blood gases and oxygen content in climbers on
Mount Everest. N Engl J Med 360:140, 2009
Hackett PH, Roach RC: High altitude and common medical conditions,
in High Altitude: An Exploration of Human Adaptation, TF Hornbein, RB
Schoene (eds). New York, Marcel Dekker, 2001, pp 839–885
MacInnis MJ et al: Evidence for a genetic basis for altitude illness: 2010 update. High Alt Med Biol 11:349, 2010
Maggiorini M et al: Both tadalafi l and dexamethasone may reduce the incidence of high-altitude pulmonary edema: A randomized trial. Ann Intern
Med 145:497, 2006
Schoonman GG et al: Hypoxia-induced acute mountain sickness is associated with intracellular cerebral edema: A 3 T magnetic resonance imaging
study. J Cereb Blood Flow Metab 28:198, 2008
Smith TG et al: Eff ect of iron supplementation and depletion on hypoxic pulmonary hypertension: Two randomized controlled trials. JAMA 302:1444,
2009
Stream JO, Grissom CK: Update on high-altitude pulmonary edema: Pathogenesis, prevention, and treatment. Wilderness Environ Med 19:293, 2008
Wilson MH et al: Th e cerebral eff ects of ascent to high altitudes. Lancet
Neurol 8:175, 2009
Doenças das Altas Altitudes e Doença Descompressiva
51-6
©2013, AMGH Editora Ltda. Todos os direitos reservados.












